聚丙烯(polypropylene, PP)被广泛应用于食品、药品包装领域,其产量仅次于聚乙烯,是一种价格低廉、机械性能优良、可塑性强的热塑性聚合物[1-3]。尽管工业领域PP回收再生技术已经相对成熟[4],但同级回收再生为食品接触材料仍存在技术瓶颈,如使用、回收过程中PP的降解[5]、加工助剂的重复添加以及化合物污染残留等[6]的去除。目前,对于食品接触用再生聚丙烯(recycled polypropylen, rPP)的安全性研究有限,与原生聚丙烯(virgin polypropylen, vPP)在安全问题上的差异尚不清晰,许可添加的rPP比例研究数据严重不足。为了规范rPP在食品接触材料中的应用,欧盟委员会(European Commission,EU)和美国食品药物管理局已经制定了相关评估和许可制度。目前,中国在这一领域暂无明确规定,近几年正在加速推进。
在已有研究中,学者们利用各种分析技术对PP中加工助剂及挥发性物质残留和迁移进行了研究。ZENG等[7]利用电子鼻等多种方法对再生高密度聚乙烯加工过程中D-柠檬烯与α-松油醇等清洗剂残留进行了分析;佳乐麝香 (galaxolide, HHCB)等人工合成多环麝香物质在生物体内的富集和潜在的致癌和致畸风险备受关注[8],AIKINS等[9]采用气相色谱-电子电离-质谱联用对HHCB于生物的急慢性影响进行了分析研究。此外,已有研究者使用气相色谱-质谱、高效液相色谱-电喷雾质谱等多种仪器设备对PP包装材料中挥发性有机物、抗氧剂168及氧化降解产物、邻苯类增塑剂、山梨醇类成核剂及非离子抗静电剂等化合物的定性和定量分析进行了研究[10-17]。目前,将主成分分析(principal component analysis, PCA)应用于媒体、金融及塑料成分分析等多个领域[18-21],LEMON等[22]也利用分类与回归树(classification and regression tree, CART)在公共卫生领域取得了显著成果,有效实现了对复杂数据的降维、分类处理。这些研究方法和成果为本研究提供了重要的科学依据和思路及方法支持。
本研究旨在进一步研究化合物在rPP中的迁移行为,推动rPP在食品接触材料领域的安全应用。制备了向vPP中添加不同量rPP的食品级rPP薄膜,利用GC-MS和HPLC-MS建立了rPP中4种加工助剂及1种降解产物、3种挥发性物质残留量及其在70 ℃、2 h条件下向4种食品模拟物中迁移的检测方法。此外,借鉴了PCA-CART等统计方法,以期对食品级rPP薄膜进行更加有效地分析与分类。
1 材料与方法
1.1 试剂与材料
正己烷、二氯甲烷、甲醇、乙醇、异辛烷、乙腈(HPLC级)、冰乙酸、N,N-二甲基甲酰胺(AR级)、亚磷酸三(2,4-二叔丁苯基)酯(98%)、佳乐麝香标准溶液(100 μg/mL in methanol),上海麦克林生化科技有限公司;α-松油醇(98.9%),北京坛墨质检科技有限公司;硬脂酸二乙醇胺、成核剂3988、2,4-二叔丁基苯酚(97%),上海吉至生化科技有限公司;邻苯二甲酸双(2-乙基己基)酯(98%)、D-柠檬烯(95%),上海迈瑞尔生化科技有限公司;2种食品接触用vPP粒子、6种食品接触用rPP粒子、1种rPP冰激凌杯,购自国内外不同公司。
7种rPP薄膜,以PPC2和PPV2按不同质量比自制。详见表1。
表1 样品信息
Table 1 Information of sample
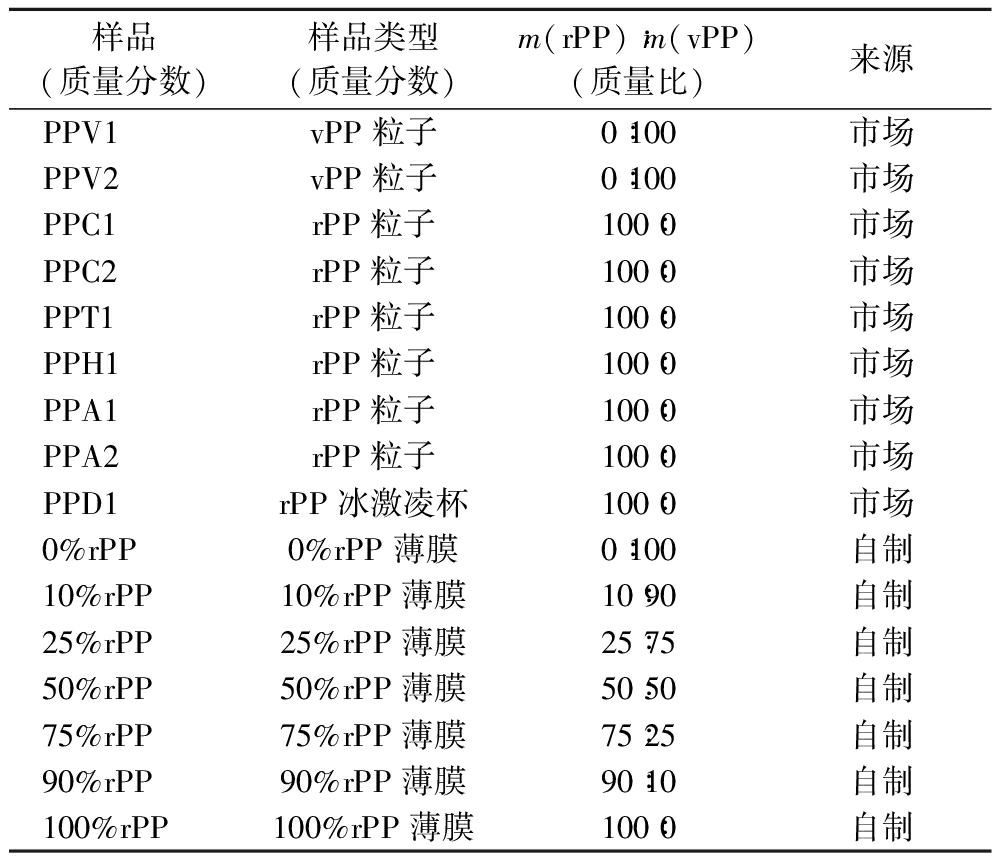
样品(质量分数)样品类型(质量分数)m(rPP)∶m(vPP)(质量比)来源PPV1vPP粒子0∶100市场PPV2vPP粒子0∶100市场PPC1rPP粒子100∶0市场PPC2rPP粒子100∶0市场PPT1rPP粒子100∶0市场PPH1rPP粒子100∶0市场PPA1rPP粒子100∶0市场PPA2rPP粒子100∶0市场PPD1rPP冰激凌杯100∶0市场0%rPP0%rPP薄膜0∶100自制10%rPP10%rPP薄膜10∶90自制25%rPP25%rPP薄膜25∶75自制50%rPP50%rPP薄膜50∶50自制75%rPP75%rPP薄膜75∶25自制90%rPP90%rPP薄膜90∶10自制100%rPP100%rPP薄膜100∶0自制
1.2 仪器与设备
DRK203B薄膜测厚仪,济南德瑞克仪器有限公司;同向双螺杆挤出造粒实验线、切粒机,广州市普同实验分析仪器有限公司;JYC-40型小型实验流延机,佛山市金中河机械有限公司;Agilent 7890A-5975C气相色谱-质谱仪、Agilent 1260-G6125B高效液相色谱-质谱仪,安捷伦科技有限公司。
1.3 仪器条件
气相色谱条件:色谱柱:Agilent DB-5MS毛细管柱(30 mm×0.25 mm×0.25 mm);升温程序:初始柱温50 ℃,保留2 min,以20 ℃/min升到300 ℃,保持8 min;不分流,进样1 μL;进样口温度250 ℃;传输线温度280 ℃;载气为高纯氦气(>99.999%),流速20 mL/min;溶剂延迟3 min。采用电离方式为电子轰击源(EI源),选择离子监测模式。
HPLC-MS色谱条件:色谱柱 Agilent Zorbax Eclipse Plus-C8 (100 mm×3.0 mm, 1.8 μm)。柱温35 ℃,流速0.4 mL/min。进样量10 μL。流动相A:水+5 mmol/L甲酸铵;B:甲醇+5 mmol/L甲酸铵。梯度洗脱程序如下:0~2.5 min:4% A~0% A和96%B~100%B;2.5~11 min:100%B。采用电喷雾离子源正离子模式(ESI+)。
8种物质在质谱中定量及定性离子见表2,SIM图谱见图1。

a-GC-MS图谱;b-HPLC-MS图谱
图1 rPP中8种物质质谱图
Fig.1 Mass spectrum of eight compounds in rPP
表2 rPP中8种物质检测参数
Table 2 Detection parameters of eight compounds in rPP
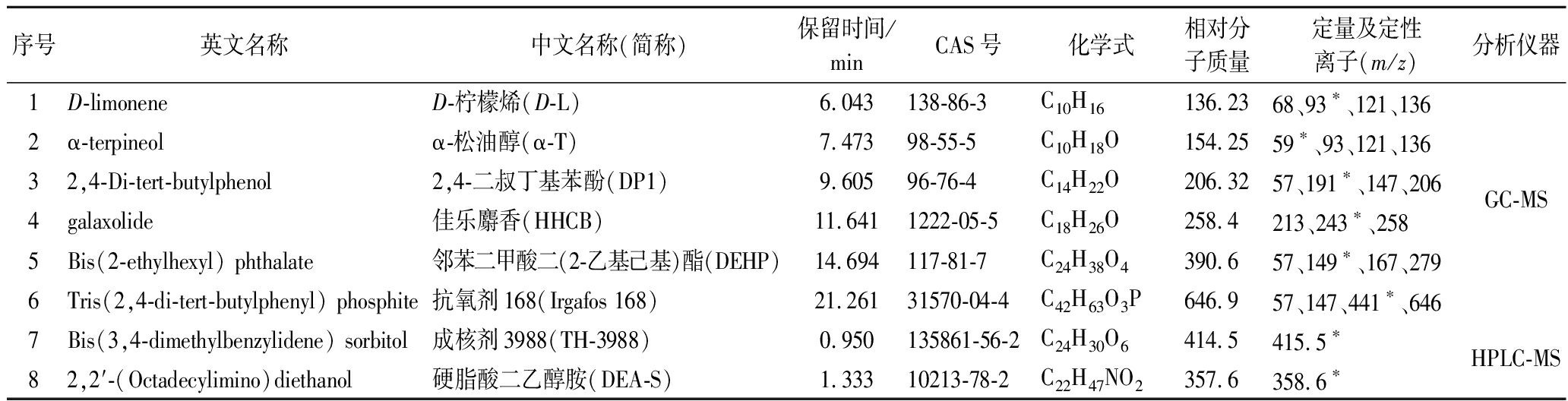
序号英文名称中文名称(简称)保留时间/minCAS号化学式相对分子质量定量及定性离子(m/z)分析仪器1D-limoneneD-柠檬烯(D-L)6.043138-86-3C10H16136.2368、93∗、121、1362α-terpineolα-松油醇(α-T)7.47398-55-5C10H18O154.2559∗、93、121、13632,4-Di-tert-butylphenol2,4-二叔丁基苯酚(DP1)9.60596-76-4C14H22O206.3257、191∗、147、206GC-MS4galaxolide佳乐麝香(HHCB)11.6411222-05-5C18H26O258.4213、243∗、2585Bis(2-ethylhexyl) phthalate邻苯二甲酸二(2-乙基己基)酯(DEHP)14.694117-81-7C24H38O4390.657、149∗、167、2796Tris(2,4-di-tert-butylphenyl) phosphite抗氧剂168(Irgafos 168)21.26131570-04-4C42H63O3P646.957、147、441∗、6467Bis(3,4-dimethylbenzylidene) sorbitol成核剂3988(TH-3988)0.950135861-56-2C24H30O6414.5415.5∗HPLC-MS82,2′-(Octadecylimino)diethanol硬脂酸二乙醇胺(DEA-S)1.33310213-78-2C22H47NO2357.6358.6∗
注:“*”定量离子;DP1,2,4-二叔丁基苯酚,为抗氧剂168降解产物,为方便和统一起见,延续本课题组简称。
1.4 实验方法
1.4.1 样品制备
将PPC2与PPV2按照表1比例混合,使用同向双螺杆挤出造粒实验线制备混合PP粒子,40 ℃烘干6 h后用小型实验流延机制备rPP薄膜,设备参数参照文献[21]并作适当调整。按照五点法用DRK203B薄膜测厚仪测量薄膜厚度。
1.4.2 方法验证
加标回收实验的回收率作为实验可行性的验证及评价。
1.4.3 残留量实验
准确称量1.000 g样品(薄膜剪碎)于30 mL具塞试管中,注入20 mL正己烷,封闭后充分振荡,超声波提取60 min,取1 mL提取液过0.22 μm滤膜于进样小瓶,上GC-MS检测;取5 mL提取液于氮吹管中,40 ℃挥干、乙腈复溶后移取1 mL过0.22 μm滤膜于进样小瓶,上HPLC-MS检测。设置3组平行及一组空白对照(下同)。物质残留量计算方法如公式(1)所示:
(1)
式中:X,化合物在样品中残留量,mg/kg;c,仪器测定浓度,ng/mL;V,提取试剂体积,mL;m,样品质量,g。
1.4.4 迁移实验
参考GB 5009.156—2016 《食品安全国家标准 食品接触材料及制品迁移试验预处理方法通则》,将薄膜裁剪成15 mm×80 mm(粒子按表面积为12 cm2计)于30 mL具塞试管中,根据GB 31604.1—2023 《食品安全国家标准 食品接触材料及制品 迁移试验通则》,分别注入20 mL 4%乙酸(体积分数,下同)、50%乙醇、95%乙醇、异辛烷4种食品模拟物(S/N=6 dm2/L),进行70 ℃、2 h迁移。
4%乙酸、50%乙醇迁移液参照文献[23]进行萃取后同95%乙醇、异辛烷迁移液,过0.22 μm滤膜于进样小瓶,上GC-MS检测;异辛烷迁移液参照1.4.2节处理后同4%乙酸、50%乙醇、95%乙醇迁移液,过0.22 μm滤膜于进样小瓶,上HPLC-MS检测,物质迁移量计算方法如公式(2)所示:
(2)
式中:X1,化合物从样品中迁移量,mg/kg;c,仪器测定浓度,ng/mL;V1,食品模拟物体积,mL;m1,食品模拟物质量,g。
1.5 数据处理
Agilent GC-MS MassHunter、Agilent OpenLab Control Panel工作站进行数据分析。使用SPSS进行数据统计分析,Duncan多重比较检验法进行显著性分析(P<0.05)。采用MATLAB(R2023a)进行PCA-CART计算分析。用Origin作图。结果表示为![]()
2 结果与分析
2.1 制备rPP薄膜厚度分析
为精准量化差异,采用DRK203B薄膜测厚仪测定薄膜的厚度。结果如表3所示,随着rPP含量的增加,薄膜厚度增加,可能是由于rPP的加入改变了PP的流动性和结晶行为,增大了结构间隙[24],从而影响薄膜的成型过程。
表3 rPP薄膜厚度 单位:μm Table 3 Thickness of rPP films
样品0%rPP10%rPP25%rPP50%rPP75%rPP90%rPP100%rPP厚度70.70±4.68ab68.80±4.11a71.27±4.49b72.03±3.65bc71.53±4.11b72.87±3.83bc74.03±3.94c
注:不同小写字母表示有显著性差异(P<0.05)。
2.2 加标回收率实验
在经检测无全阴性样品情况下,选择残留量最低的样品作为基底。
分别添加0.03、0.3、0.6 mg/kg的低、中、高3个水平混合标准溶液,设置6组平行和1组空白,测得的加标平均回收率及精密度如表4所示。结果表明,8种物质在5种溶剂中的加标平均回收率为80.0%~120.0%且相对标准偏差(relative standard deviation,RSD)≤10.0%,表明实验方法具有良好的准确度和精密度,符合要求。
表4 八种物质的加标平均回收率及精密度(n=6)
Table 4 Average spiked recoveries and precision of eight compounds (n=6)

化合物正己烷异辛烷95%乙醇50%乙醇4%乙酸0.03 mg/kg0.3 mg/kg0.6 mg/kg0.03 mg/kg0.3 mg/kg0.6 mg/kg0.03 mg/kg0.3 mg/kg0.6 mg/kg0.03 mg/kg0.3 mg/kg0.6 mg/kg0.03 mg/kg0.3 mg/kg0.6 mg/kgD-L98.3(6.1)91.9(3.3)102.2(1.4)111.5(7.3)114.5(2.6)118.2(1.3)108.5(9.2)93.0(5.6)108.3(6.1)93.0(9.4)113.7(9.3)98.6(9.7)103.1(2.7)102.8(6.3)94.3(3.8)α-T110.7(9.7)106.1(3.2)105.2(8.1)95.0(9.3)94.8(7.9)110.9(5.9)108.9(6.1)99.8(7.7)93.5(8.7)98.3(9.2)103.9(7.3)110.0(6.6)97.4(9.1)106.7(9.6)115.7(4.4)HHCB98.6(7.2)109.6(4.0)98.1(5.9)106.4(7.8)101.3(9.0)103.6(5.6)107.8(6.6)98.5(7.1)104.8(7.6)97.0(8.0)99.5(8.4)91.4(7.9)97.4(8.2)95.7(5.9)104.1(6.2)DP191.1(6.7)102.1(1.7)84.6(2.3)92.4(2.9)89.0(3.4)90.0(6.2)99.4(7.5)99.4(6.8)113.4(6.9)95.7(8.5)109.5(6.3)109.1(6.7)102.0(7.3)108.7(4.5)93.4(2.0)Irgafos 168105.4(9.0)115.1(2.8)84.1(2.0)107.3(9.4)88.0(3.6)114.8(1.7)108.1(4.9)111.4(5.9)98.7(6.8)95.0(8.5)110.7(3.6)101.4(5.3)109.6(4.3)101.8(6.3)114.5(1.0)DEHP97.5(3.7)108.8(8.6)110.4(1.8)85.2(3.8)104.4(4.5)115.8(2.4)100.7(6.4)94.1(3.8)99.5(8.3)109.8(5.0)101.1(3.5)103.9(4.2)108.6(8.9)90.6(5.4)115.3(3.2)TH-398893.7(2.7)107.9(2.3)103.3(9.8)92.8(3.8)96.7(5.7)89.6(3.4)94.0(2.2)96.4(0.4)96.5(1.0)97.1(1.6)97.6(0.6)97.2(1.3)86.0(3.4)87.6(1.2)95.2(3.2)DEA-S88.2(3.2)87.0(4.6)99.0(0.9)97.3(2.1)84.2(3.7)101.6(1.7)93.6(0.8)95.3(0.7)98.0(0.6)85.6(1.4)96.5(1.3)101.1(0.9)102.2(6.9)115.9(6.4)116.3(3.7)
注:括号中数据为精密度。
2.3 加工助剂及挥发性物质残留量
经预实验优化后,对9种市场食品接触用rPP样品和7种自制rPP薄膜中的4种加工助剂及1种降解产物、3种挥发性物质进行提取。如表5所示,8种物质在线性范围内的线性关系良好,相关系数R2≥0.995 0。以信噪比S/N≥3确定检出限(detection limit,LOD),信噪比S/N≥10确定定量限(quantification limit,LOQ),结果显示该方法在GC-MS、HPLC-MS的LOD分别为0.6、1.0 μg/L,LOQ分别为2.0、3.0 μg/L。
表5 正己烷提取8种物质的线性方程、相关系数、线性范围、方法LOD和LOQ Table 5 Linear equation, correlation coefficient, linear range, LODs, and LOQs of eight compounds from n-hexane
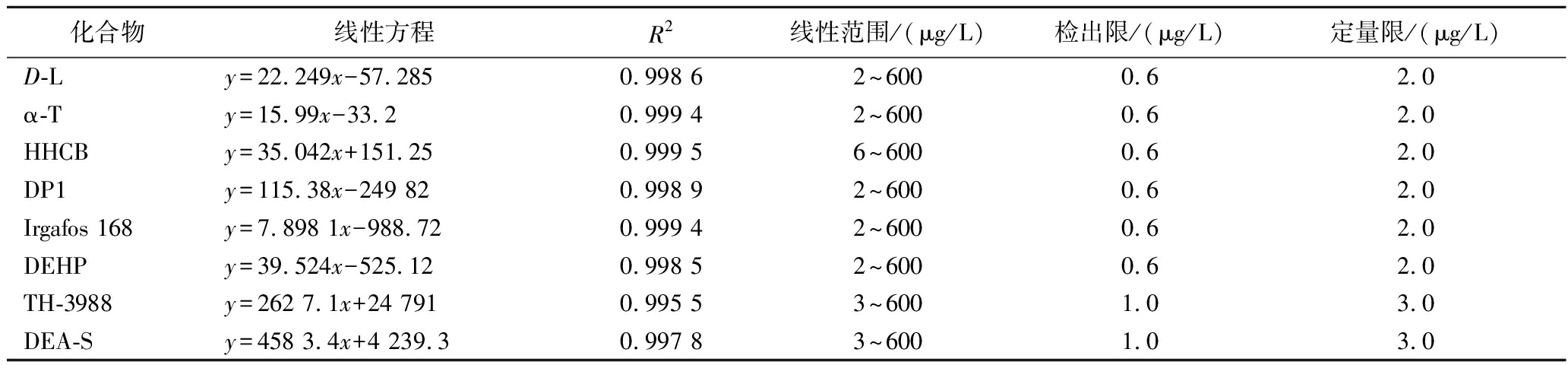
化合物线性方程R2线性范围/(μg/L)检出限/(μg/L)定量限/(μg/L)D-Ly=22.249x-57.2850.998 62~6000.62.0α-Ty=15.99x-33.20.999 42~6000.62.0HHCBy=35.042x+151.250.999 56~6000.62.0DP1y=115.38x-249 820.998 92~6000.62.0Irgafos 168y=7.898 1x-988.720.999 42~6000.62.0DEHPy=39.524x-525.120.998 52~6000.62.0TH-3988y=262 7.1x+24 7910.995 53~6001.03.0DEA-Sy=458 3.4x+4 239.30.997 83~6001.03.0
图2展示了8种物质在rPP中的残留情况。其中,挥发性物质D-L、α-T、HHCB主要源自清洗剂残留,DP1则为Irgafos 168氧化降解产物,均未被列入GB 9685—2016 《食品安全国家标准 食品接触材料及制品用添加剂使用标准》、(EU) No 10/2011清单,属于非有意添加物(non intentionally added substances,NIAS),残留量分别为0.83~12.41 mg/kg、0~34.90 mg/kg、0~16.87 mg/kg、22.46~408.11 mg/kg。

a-D-柠檬烯;b-α-松油醇;c-佳乐麝香;d-2,4-二叔丁基苯酚;e-抗氧剂168;f-邻苯二甲酸二(2-乙基己基)酯;g-成核剂3988;h-硬脂酸二乙醇胺
图2 样品中8种物质残留量
Fig.2 Residues of eight compounds in rPP
分析发现,rPP薄膜中,D-L残留量随rPP含量增高而增加,而DP1残留量则呈现相反趋势,说明rPP中DP1可能进一步发生降解[10];D-L、α-T、HHBC三种挥发性物质残留量相较粒子有所下降,是由于制备流程中加热使其挥发、分解所致[8,25]。
加工助剂Irgafos 168、DEHP、TH-3988、DEA-S的残留量分别为6.80~998.36 mg/kg、0.41~54.71 mg/kg、13.05~126.47 mg/kg、0.27~9.56 mg/kg。rPP薄膜中,rPP含量为50%时,TH-3988残留量最高;Irgafos 168、DEHP、DEA-S随着rPP含量增加呈递增趋势,DEHP不被允许添加在PP制品中,可能来自于回收过程中其他塑料制品污染。可见,rPP中上述物质残留量较高,如果用于食品包装,可能会向食品中迁移,从而存在一定安全风险。
2.4 加工助剂及挥发性物质向食品模拟物中迁移量
为研究4种加工助剂及1种降解产物、3种挥发性物质从不同rPP中向不同食品中的潜在迁移行为,实验选取了4种不同食品模拟物进行迁移实验(表6)。结果显示,8种化合物在4种食品模拟物的线性范围内线性关系良好,相关系数R2≥0.995 0,在GC-MS、HPLC-MS的LOD为0.6~3.0、1.0 μg/L,LOQ为2.0~10.0、3.0 μg/L。
表6 八种物质迁移的线性方程、相关系数、线性范围、方法LOD和LOQ Table 6 Linear equation, correlation coefficient, linear range, LODs, and LOQs for migration of eight compounds
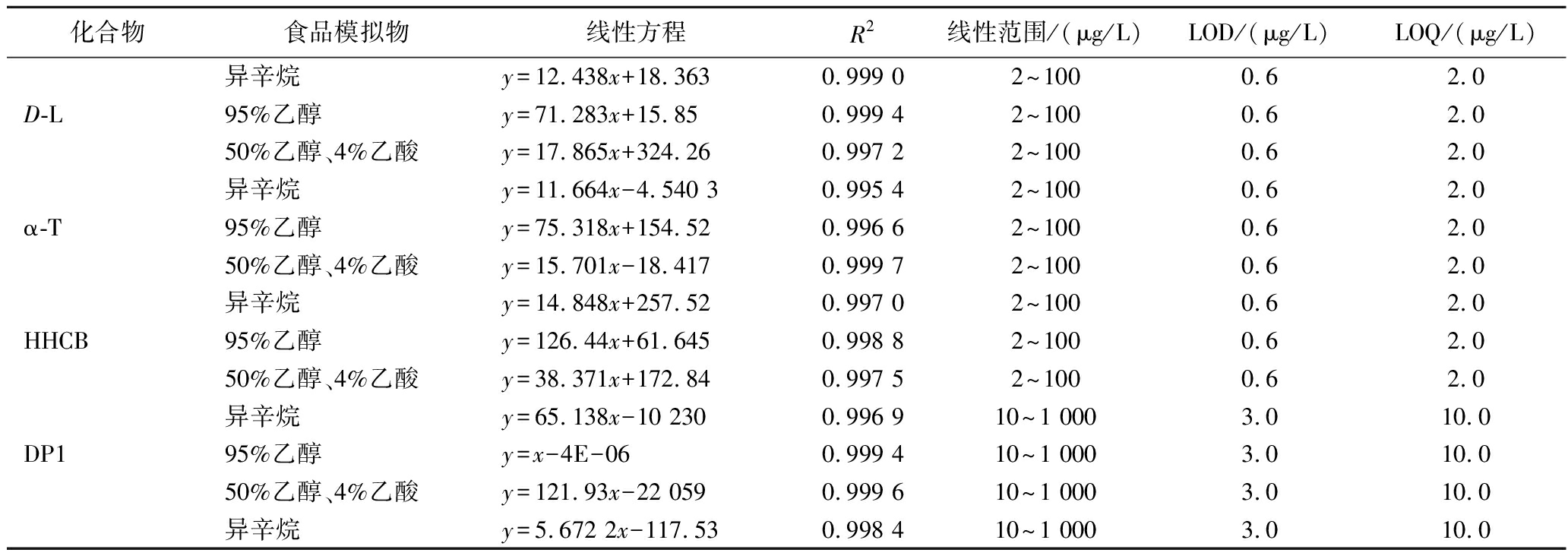
化合物食品模拟物线性方程R2线性范围/(μg/L)LOD/(μg/L)LOQ/(μg/L)异辛烷y=12.438x+18.3630.999 0 2~1000.62.0D-L95%乙醇y=71.283x+15.850.999 4 2~1000.62.0 50%乙醇、4%乙酸y=17.865x+324.260.997 2 2~1000.62.0异辛烷y=11.664x-4.540 30.995 42~1000.62.0α-T95%乙醇y=75.318x+154.520.996 62~1000.62.0 50%乙醇、4%乙酸y=15.701x-18.4170.999 72~1000.62.0异辛烷y=14.848x+257.520.997 0 2~1000.62.0HHCB95%乙醇y=126.44x+61.6450.998 82~1000.62.0 50%乙醇、4%乙酸y=38.371x+172.840.997 5 2~1000.62.0异辛烷y=65.138x-10 2300.996 9 10~1 0003.010.0DP195%乙醇y=x-4E-060.999 4 10~1 0003.010.050%乙醇、4%乙酸y=121.93x-22 0590.999 6 10~1 0003.010.0异辛烷y=5.672 2x-117.530.998 410~1 0003.010.0
续表6
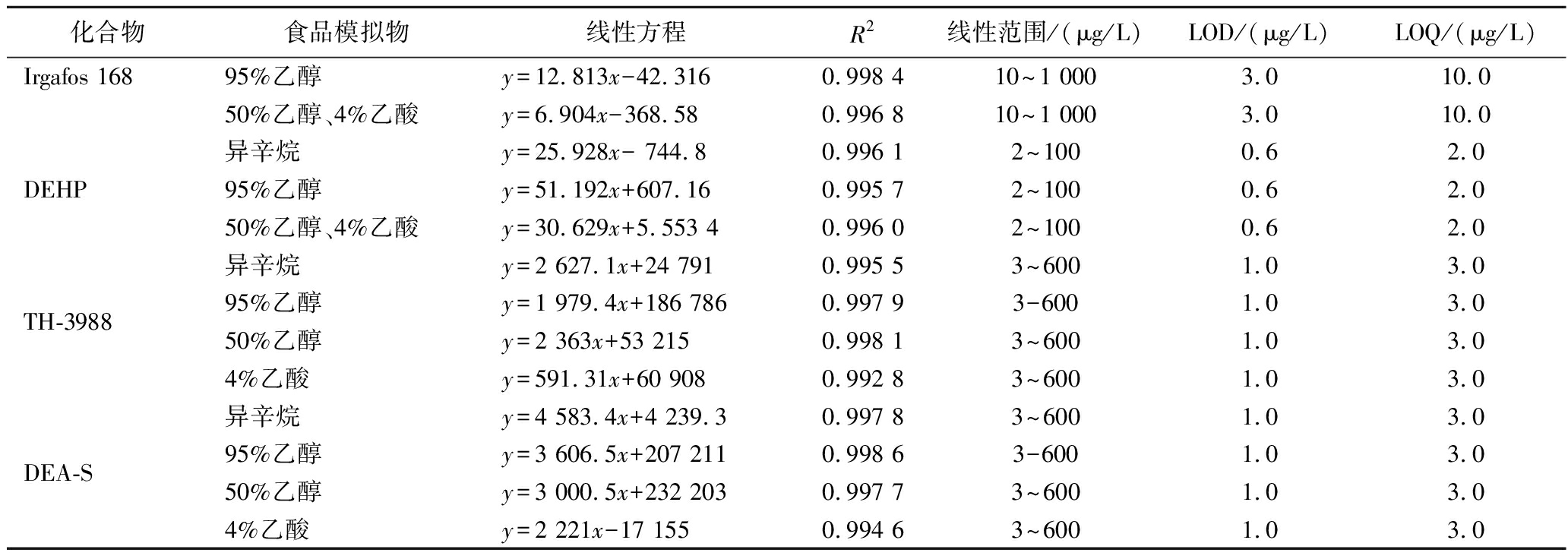
化合物食品模拟物线性方程R2线性范围/(μg/L)LOD/(μg/L)LOQ/(μg/L)Irgafos 16895%乙醇y=12.813x-42.3160.998 410~1 0003.010.050%乙醇、4%乙酸y=6.904x-368.580.996 810~1 0003.010.0异辛烷y=25.928x- 744.80.996 12~1000.62.0 DEHP95%乙醇y=51.192x+607.160.995 72~1000.62.0 50%乙醇、4%乙酸y=30.629x+5.553 40.996 0 2~1000.62.0异辛烷y=2 627.1x+24 7910.995 53~6001.03.0TH-398895%乙醇y=1 979.4x+186 7860.997 93-6001.03.050%乙醇y=2 363x+53 215 0.998 13~6001.03.04%乙酸y=591.31x+60 908 0.992 8 3~6001.03.0异辛烷y=4 583.4x+4 239.30.997 83~6001.03.0DEA-S95%乙醇y=3 606.5x+207 2110.998 63-6001.03.050%乙醇y=3 000.5x+232 2030.997 73~6001.03.04%乙酸y=2 221x-17 1550.994 6 3~6001.03.0
整体来看,8种物质向异辛烷中的迁移量和检出率最高,其次是95%乙醇和50%乙醇,在4%乙酸中迁移量极低,基本未迁出。
如表7所示,D-L、α-T、HHCB、DP1的最大迁移量超过了中国和欧盟对NIAS的迁移限量标准,即0.01 mg/kg;在异辛烷和95%乙醇中的检出率为18.75%~100%,其在rPP样品中检出率更高,为42.86%~100%,说明这4种物质在rPP存在更普遍。D-L、α-T、DP1在50%乙醇、4%乙酸中检出率最高为100%,可能是其中萜类结构能与水或酸中H+形成氢键或者其他相互作用,或是D-L在H+存在下与水加成生成α-T导致[26-28](图3)。Irgafos 168在水中会水解成疏水性更少的苯酚类降解产物,导致DP1在含水食品模拟物中存在一定迁移[29]。
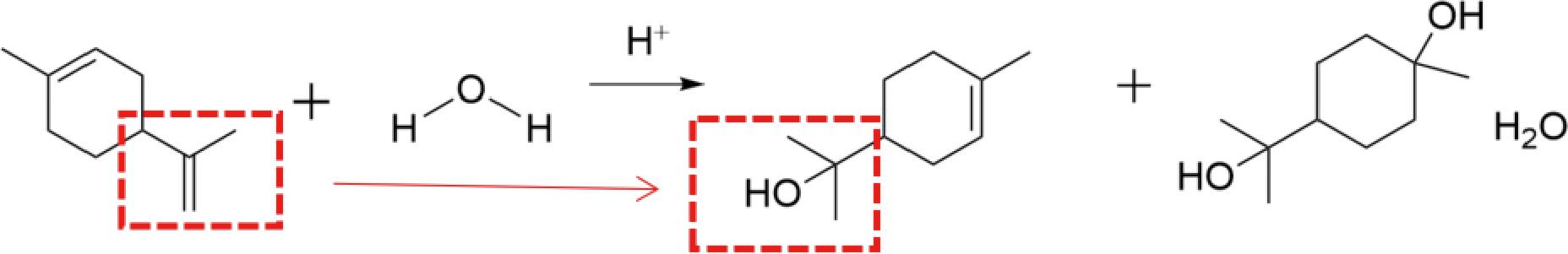
图3 酸性条件下D-L与水加成生成α-T与水合萜二醇
Fig.3 Addition of D-limonene and water to produce α-terpineol and terpine hydrate under acidic conditions
表7 PP中8种物质向不同食品模拟物中的迁移量及检出率
Table 7 Migration and detection rates of eight compounds in PP into different food simulants

化合物使用范围和最大使用量/%最大残留量/(mg/kg)SML或SML(T)/(mg/kg)异辛烷95%乙醇50%乙醇4%乙酸迁移量/(mg/kg)检出率/%迁移量/(mg/kg)检出率/%迁移量/(mg/kg)检出率/%迁移量/(mg/kg)检出率/%D-L———0~0.043T:75.00M:55.56R:71.430~0.012T:25.00M:44.44R:57.140~0.012T:37.50M:66.67R:57.140~0.002T:6.25M:11.11R:14.29α-T———0.~0.233T:81.25M:100R:1000.~0.039T:43.75M:77.78R:1000.001~0.018T:100M:100R:1000.001~0.017T:100M:100R:100HHCB———0~0.159T:25.00M:44.44R:57.140~0.019T:18.75M:33.33R:42.860~0.017T:18.75M:33.33R:42.86—T:0M:0R:0DP1———1.399~3.183T:100M:100R:1000.801~3.147T:100M:100R:1000.110~1.463T:100M:100R:1000.073~0.740T:100M:100R:100Irgafos 168PP:0.25a—60ab0.199~111.836T:100M:100R:1000.019~1.637T:100M:100R:1000~0.591T:93.75M:88.89R:85.71—T:0M:0R:0DEHPPVC:5a—1.5a0.6b60(32)ab0.6(36)b0.016~0.817T:100M:100R:1000~0.104T:87.50M:77.78R:85.710~0.059T:87.50M:77.78R:85.710~0.015T:87.50M:77.78R:85.71TH-3988PP:0.4a—60ab0.195~1.089T:100M:100R:1000.004~0.137T:100M:100R:1000~0.017T:75.00M:77.78R:100—T:0M:0R:0DEA-SPP:0.2a—60a1.2(7)b0~0.063T:87.50M:77.78R:71.430~0.010T:43.75M:33.33R:28.57—T:0M:0R:0—T:0M:0R:0
注:“a”表示参考GB 9685—2016《食品安全国家标准 食品接触材料及制品用添加剂使用标准》;“b” 表示参考(EU) No 10/2011(Commission Regulation (EU) No 10/2011 of 14 January 2011 on plastic materials and articles intended to come into contact with food);“—”表示无规定、无迁移;“T” 表示实验全部样品;“M” 表示9种市场样品;“R” 表示7种市场rPP样品。
Irgafos 168在异辛烷和95%乙醇中检出率为100%,其在2种市场rPP粒子中向异辛烷迁移量超过特定迁移限量(specific migration limit, SML) (60 mg/kg)。DEHP检出率>85.71%,可能来源于回收时聚氯乙烯或其他杂质残留,尽管迁移量低于中国现行SML (1.5 mg/kg),但其在2种市场rPP粒子中向异辛烷的迁移量超过欧盟最新修订的SML(0.6 mg/kg);其向50%乙醇和4%乙酸中也有迁移,这与DEHP分子含有的极性酯基具有一定极性有关,同时H+浓度升高,也会影响DEHP的迁移[12,30]。TH-3988为山梨醇类成核剂,被广泛用于PP制品,检出率最高为100%,但迁移量均低于SML (60 mg/kg)。DEA-S为常用非离子抗静电剂,最大迁移量低于欧盟关于C8~C18烷基胺类化合物的SML(T) (1.2 mg/kg)。
图4展示了rPP薄膜中8种物质的迁移率,其中向异辛烷的迁移率最大。D-L、DEHP、DEA-S的迁移率随着rPP含量增加呈递减趋势,DP1的迁移率则相反,这与原始PP粒子中物质残留量存在联系,亦说明rPP的加入会改变化合物的迁移行为。综合来看,在特定条件下,8种物质在rPP样品中检出率较高,可能迁移到食品中并达到一定的浓度水平,超过现行SML,应对样品进行更恶劣工况下的加速模拟实验,以探明其适宜的食品包装形式和使用条件。
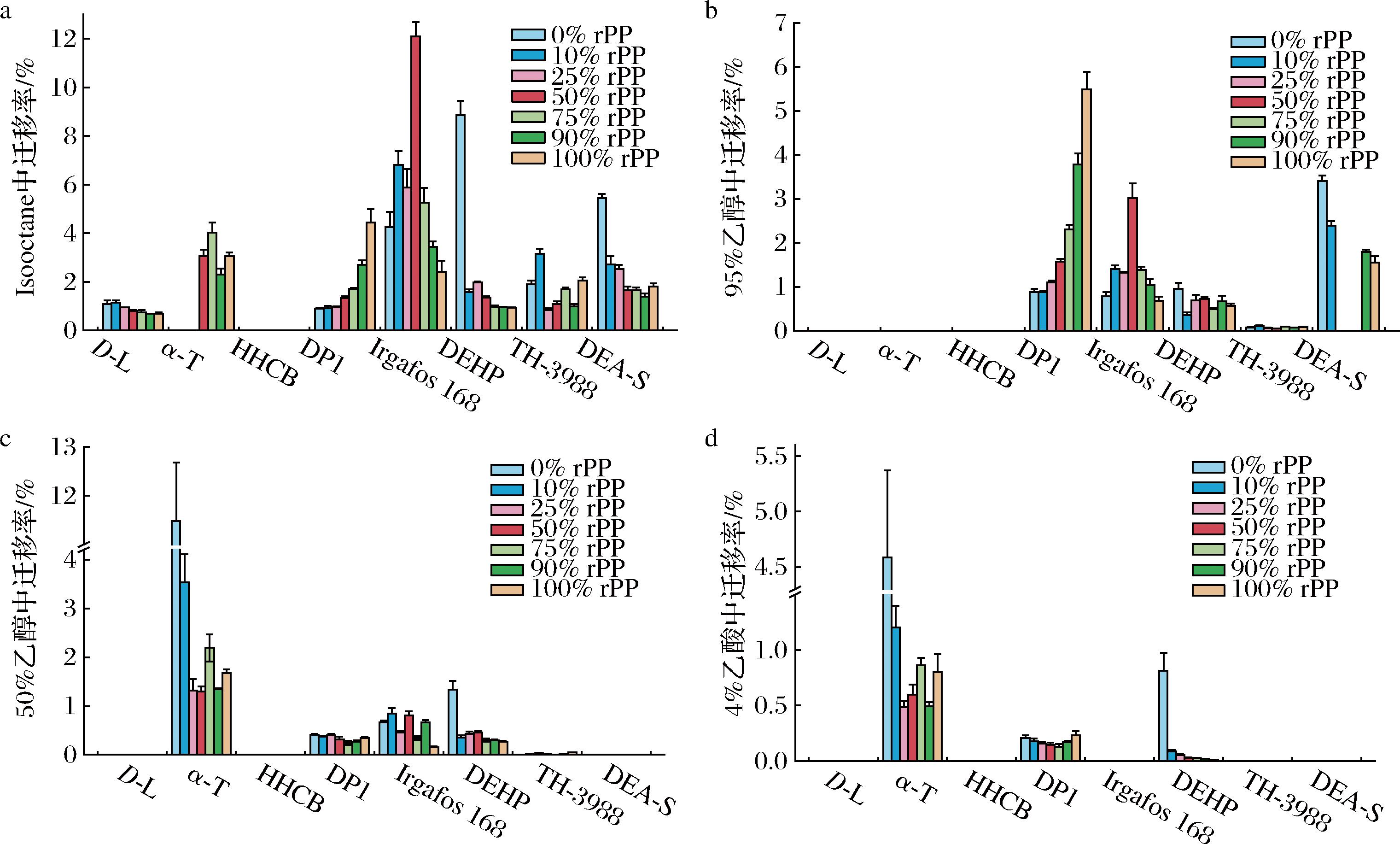
a-异辛烷;b-95%乙醇;c-50%乙醇;d-4%乙酸
图4 rPP薄膜中8中物质向不同食品模拟物的迁移率
Fig.4 Migration rate of eight compounds to different food mimics in rPP films
2.5 加工助剂及挥发性物质残留量分析
在处理和分析加工助剂及挥发性物质残留量数据时,PCA和CART算法的组合应用是一种有效的方法。PCA具有强大的数据分析功能,能够过线性变换将原始数据转换为一组线性无关的特征,进而提取数据中的主要特征分量;CART能够处理非线性关系,可以进行特征选择和重要度排序,与PCA结合可以更好地处理高维数据。PCA-CART算法具有良好的解释性,可以提高分类结果的可靠性。
2.5.1 PCA分析
将2种vPP粒子(PPV1、PPV2)与5种rPP粒子(PPC1、PPC2、PPH1、PPA1、PPA2)中的4种加工助剂及1种降解产物、2种挥发性物质(HHCB多为0,舍弃)残留量组成矩阵X,归一化到[0,1],使每种物质贡献相同,计算协方差矩阵得到特征值和特征向量,根据特征值累计贡献率>99.5%,选择前5个特征值对应的特征向量构建投影矩阵,利用PCA对矩阵X进行降三维可视化分析,得到每种物质的贡献值,如图5-a。

v1-D-柠檬烯;v2-α-松油醇;v3-抗氧剂168;v4-2,4-二叔丁基苯酚;v5-邻苯二甲酸二(2-乙基己基)酯;v6-成核剂3988;v7-硬脂酸二乙醇胺a-主成分三维图;b-主成分1与2投影;c-主成分1与3投影;d-主成分2与3投影
图5 PP粒子中7种物质残留量的PCA双标图
Fig.5 PCA biplot of residues of seven compounds in PP particles
注:“*”PP粒子在PCA双标图中的观测值。
进一步分析表明(图5-b~图5-d),主成分1与DP1成负相关;主成分2与Irgafos 168、DEA-S成正相关;主成分3与D-L、DP1、DEA-S成正相关,这揭示了物质残留量与样品之间的复杂关系,包括非线性关系,所以在PCA对数据集进行线性降维后需要借助CART进一步分类处理。
2.5.2 CART分析
为了探究物质残留量与样品之间的复杂关系并进行预测分析,将2.5.1节中PCA处理后的数据导入CART算法进行处理。图6-a展示了用于构建PCA-CART算法的7种PP粒子,0表示vPP、1表示rPP。将不同rPP含量薄膜中7种物质残留量导入PCA-CART进行预测,结果如图6-b所示,当rPP含量<25%时被归类到vPP类别。

a-构建PCA-CART的PP粒子;b-PCA-CART对rPP薄膜的分类预测
图6 基于PP中7种物质残留量的PCA-CART
Fig.6 PCA-CART based on residues of seven compounds in PP
结果表明,PCA-CART可以有效处理PP中物质残留量数据,提供了PP中物质残留量与rPP含量之间关系的相关信息,可以对数据集进行预测分析。同时表明洗涤剂残留、杂质混入以及添加Irgafos 168、TH-3988、DEA-S等助剂会使rPP中物质残留量发生较明显变化,可能对PP安全造成威胁。特别是当rPP添加量>25%时,需要对PP用于食品接触用时安全性进行重点关注。
3 结论与展望
本文基于GC-MS、HPLC-MS方法对市场上的食品级PP原生粒子、再生粒子和制品及自制rPP薄膜中4种加工助剂及1种降解产物、3种挥发性物质的残留量和向4种食品模拟物的迁移量进行了测定。8种物质在rPP中存在残留,残留量随rPP加工过程发生一定变化。添加rPP会改变化合物迁移率,可能归因于rPP形貌结构间隙与vPP相比更大,导致化合物更易迁移。8种物质向食品模拟物的迁移量和检出率从大到小依次为异辛烷、95%乙醇、50%乙醇、4%乙酸,D-L、α-T、HHCB、DP1的最大迁移量超过NIAS的SML (0.01 mg/kg),市场rPP样品中Irgafos 168、DEHP迁移量超过SML的样品数量均为2种,而TH-3988、DEA-S迁移量未超出SML(T)。利用PCA-CART处理PP粒子中物质残留量数据集,可以有效将rPP薄膜分为两类,发现rPP添加量<25%时,分类与vPP更接近。因此,rPP用于食品接触用材料时,需要根据回收地、工艺,重点对杂质、洗涤剂残留、加工助剂等进行有效安全评估,以确保食品安全。本研究为rPP用于食品接触材料安全性评估提供了数据支持,有利于推动再生塑料安全合规使用。
[1] ZHANG G H, ZHU J F, OKUWAKI A.Prospect and current status of recycling waste plastics and technology for converting them into oil in China[J].Resources, Conservation and Recycling, 2007, 50(3):231-239.
[2] BORA R R, WANG R, YOU F Q.Waste polypropylene plastic recycling toward climate change mitigation and circular economy:Energy, environmental, and technoeconomic perspectives[J].ACS Sustainable Chemistry &Engineering, 2020, 8(43):16350-16363.
[3] ALSABRI A, TAHIR F, AL-GHAMDI S G.Environmental impacts of polypropylene (PP) production and prospects of its recycling in the GCC region[J].Materials Today:Proceedings, 2022, 56:2245-2251.
[4] 向文灏, 焦永泰.聚丙烯塑料回收再生工业托盘的浅析[J].塑料包装, 2018, 28(6):15-18.XIANG W H, JIAO Y T.Analysis of polypropylene plastic recycled industrial pallet[J].Plastics Packaging, 2018, 28(6):15-18.
[5] NASIR A, YASIN T, ISLAM A.Thermo-oxidative degradation behavior of recycled polypropylene[J].Journal of Applied Polymer Science, 2011, 119(6):3315-3320.
[6] 吴东亮, 沈振, 李景菲, 等.回收塑料对聚丙烯性能影响的研究[J].新型建筑材料, 2023, 50(3):131-134.WU D L, SHEN Z, LI J F, et al.Study on the effect of recycled plastics on the properties of polypropylene[J].New Building Materials, 2023, 50(3):131-134.
[7] ZENG S F, ZENG Y, GUO P, et al.Characterization of odors and volatile organic compounds changes to recycled high-density polyethylene through mechanical recycling[J].Polymer Degradation and Stability, 2023, 208:110263.
[8] 杨顺美, 焦文涛, 刘峰, 等.电阻加热修复佳乐麝香污染土壤的工艺优化[J].环境工程学报, 2022, 16(4):1284-1293.YANG S M, JIAO W T, LIU F, et al.Optimization of response surface process for remediation of galaxolide contaminated soil by electric resistance heating[J].Chinese Journal of Environmental Engineering, 2022, 16(4):1284-1293.
[9] AIKINS D M, MEHLER W T, VEILLEUX H D, et al.The acute and chronic effects of a sediment-bound synthetic musk, galaxolide, on Hyalella azteca, Chironomus dilutus, and Lumbriculus variegatus[J].Archives of Environmental Contamination and Toxicology, 2023, 84(2):227-236.
[10] 杨岳平, 胡长鹰, 钟怀宁, 等.抗氧剂168的降解及其降解产物的测定[J].现代食品科技, 2016, 32(6):304-309.YANG Y P, HU C Y, ZHONG H N, et al.Degradation of irgafos 168 and determination of its degradation products[J].Modern Food Science and Technology, 2016, 32(6):304-309.
[11] ZHANG D, SUN G P, ZHANG X Q.Study on volatile organic compounds (VOCs) in polypropylene monomers and the effect of additives on volatile organic compounds in polypropylene composites[J].Science of Advanced Materials, 2019, 11(11):1623-1631.
[12] FANG H Q, WANG J, LYNCH R A.Migration of di (2-ethylhexyl) phthalate (DEHP) and di-n-butylphthalate (DBP) from polypropylene food containers[J].Food Control, 2017, 73:1298-1302.
[13] SALAM A.Reversed phase-HPLC method for low level quantitation of dimethyl dibenzylidene sorbitol[J].Journal of the Chemical Society of Pakistan, 2022, 44(5):436.
[14] TSOCHATZIS E D, THEODORIDIS G, GIKA H G.Development and validation of a UHPLC-qTOF MS method for the determination of sorbitol-based nuclear clarifying agents in food simulants after migration from food contact materials[J].Applied Sciences, 2021, 11(9):3789.
[15] CHOW W S, THAM W L.Effects of antistatic agent on the mechanical, morphological and antistatic properties of polypropylene/organo-montmorillonite nanocomposites[J].Express Polymer Letters, 2009, 3(2):116-125.
[16] WANG Y N, GAO X, LIU B J, et al.Identification of chemicals in a polyvinyl chloride/polyethylene multilayer film by ultra-high-performance liquid chromatography/quadrupole time-of-flight mass spectrometry and their migration into solution[J].Journal of Chromatography A, 2020, 1625:461274.
[17] GONZ LEZ-RODR
LEZ-RODR GUEZ M V, DOPICO-GARC
GUEZ M V, DOPICO-GARC A M S, NOGUEROL-CAL R, et al.Application of liquid chromatography in polymer non-ionic antistatic additives analysis[J].Journal of Separation Science, 2010, 33(22):3595-3603.
A M S, NOGUEROL-CAL R, et al.Application of liquid chromatography in polymer non-ionic antistatic additives analysis[J].Journal of Separation Science, 2010, 33(22):3595-3603.
[18] CLAUSEN C, WECHSLER H.Color image compression using PCA and backpropagation learning[J].Pattern Recognition, 2000, 33(9):1555-1560.
[19] GEORGE A.Anomaly detection based on machine learning:dimensionality reduction using PCA and classification using SVM[J].International Journal of Computer Applications, 2012, 47(21):5-8.
[20] WEN Y L, LIN P G, NIE X S.Research of stock price prediction based on PCA-LSTM model[J].IOP Conference Series:Materials Science and Engineering, 2020, 790(1):012109.
[21] 郭盼, 曾少甫, 朱蕾, 等.基于GC-MS和化学计量法探究边角料添加比例对食品接触用再生PE薄膜的影响[J].分析测试学报, 2022, 41(10):1470-1477.GUO P, ZENG S F, ZHU L, et al.Effect investigation of scrap addition ratio on recycled food contact polyethylene films based on GC-MS and chemometrics[J].Journal of Instrumental Analysis, 2022, 41(10):1470-1477.
[22] LEMON S C, ROY J, CLARK M A, et al.Classification and regression tree analysis in public health:Methodological review and comparison with logistic regression[J].Annals of Behavioral Medicine, 2003, 26(3):172-181.
[23] 葛丹阳, 刘桂华, 姜欢, 等.GC-MS/MS法测定食品接触用硅橡胶制品中6种环硅氧烷迁移量[J].分析测试学报, 2022, 41(10):1486-1493.GE D Y, LIU G H, JIANG H, et al.Determination of migration of six cyclosiloxanes in silicone rubber products for food contact by GC-MS/MS[J].Journal of Instrumental Analysis, 2022, 41(10):1486-1493.
[24] ZENG S F, ZHANG H R, LI Z K, et al.Effect of mechanical recycling on crystallization, mechanical, and rheological properties of recycled high-density polyethylene and reinforcement based on virgin high-density polyethylene[J].Journal of Applied Polymer Science, 2024, 141(11):e55097.
[25] MILLER D J, HAWTHORNE S B.Solubility of liquid organic flavor and fragrance compounds in subcritical (hot/liquid) water from 298 K to 473 K[J].Journal of Chemical and Engineering Data, 2000, 45(2):315-318.
[26] 廉长盛, 付冬梅, 张俊鹏, 等.酒花内生菌Pseudomonas oryzihabitans F0-1转化柠檬烯生成α-萜品醇的研究[J].保鲜与加工, 2021, 21(12):38-45.LIAN C S, FU D M, ZHANG J P, et al.Study on the transformation of limonene to α-terpineol by Pseudomonas oryzihabitans F0-1[J].Storage and Process, 2021, 21(12):38-45.
[27] 张璐璐, 范刚, 李晓, 等.利用RNAi技术研究基因PDIDSM_85260和PDIDSM_08010表达对柠檬烯转化生成α-松油醇的影响[J].食品科学, 2022, 43(6):141-148.ZHANG L L, FAN G, LI X, et al.Effect of the inhibition of PDIDSM 85260 and PDIDSM 08010 expression by RNA interference on the biotransformation of limonene to α-terpineol[J].Food Science, 2022, 43(6):141-148.
[28] ROM N-AGUIRRE M, DE LA TORRE-S
N-AGUIRRE M, DE LA TORRE-S ENZ L, FLORES W A, et al.Synthesis of terpineol from α-pinene by homogeneous acid catalysis[J].Catalysis Today, 2005, 107-108:310-314.
ENZ L, FLORES W A, et al.Synthesis of terpineol from α-pinene by homogeneous acid catalysis[J].Catalysis Today, 2005, 107-108:310-314.
[29] LÜTZHØFT H C H, WAUL C K, ANDERSEN H R, et al.HS-SPME-GC-MS analysis of antioxidant degradation products migrating to drinking water from PE materials and PEX pipes[J].International Journal of Environmental Analytical Chemistry, 2013, 93(6):593-612.
[30] JAYAWEERA M, PERERA H, BANDARA N, et al.Migration of phthalates from PET water bottle in events of repeated uses and associated risk assessment[J].Environmental Science and Pollution Research International, 2020, 27(31):39149-39163.