由于快节奏的现代生活方式和蓬勃发展的预制菜行业,消费者的偏好已转向更方便的食品,这种转变导致了预制菜肴的消费量增加[1]。预制菜是指是以一种或多种食用农产品及其制品为原料,使用或不使用调味料等辅料,不添加防腐剂,并经过预加工步骤,如搅拌、腌制、滚揉、成型、炒、炸、烤、煮、蒸等制成,配以或不配以调味料包,在最初的生产之后,准备好的菜肴经过后续的加工程序,如包装、灭菌和冷藏/冷冻,然后被储存、运输和最终销售[2]。
目前,预制菜常见的包装材料包括塑料、铝箔、电镀锡薄钢板等。其中,塑料包装材料具有可塑性强、价格低廉、运输便捷以及良好的防水防潮性能,在预制菜中得到了广泛的应用[3]。塑料是指以合成高分子聚合物为主要成分的可塑性材料,食品包装中最常用的有高分子聚对苯二甲酸乙二醇酯(polyethylene terephthalate, PET)、聚酰胺(polyethylene terephthalate, PA)、聚乙烯(polyethylene, PE)、聚丙烯(polypropylene, PP)等[4]。在塑料的加工过程中,为增强其性能,常会加入一些添加剂,如增塑剂、抗氧化剂、紫外吸收剂、光引发剂、润滑剂、着色剂等[5]。然而,大多数添加剂都是低分子质量的,且与聚合物基体无化学反应[6],而主要为非共价键作用如范德华力和氢键等[7],因此在特定条件下它们可能会从塑料包装中迁移出来进入食品,从而对人体造成危害。有大量研究表明,迁移物质暴露后可能对人体造成伤害,最常见的影响体现在内分泌系统、分解代谢或新陈代谢方面[8]。此外,它们还可能导致慢性疾病,如糖尿病、肥胖、乳腺癌和免疫功能障碍等[9-11]。近年来,食品塑料包装材料中添加剂迁移这一现象对人体健康造成的危害已引起社会关注,并成为研究热点。
预制菜需要根据产品本身选择适合的包装以满足特定要求,包括在灭菌、贮藏和再加热过程中承受高温、能够快速冷冻以及在煮沸过程中保持完整性[12]。尤其在油性环境中,经过热处理后,塑料包装材料中的加工助剂、油墨等有毒有害物质可能会向食品中迁移,进而引发安全问题[13]。而目前尚未有专门用于预制菜的塑料包装材料,市面上的预制菜基本都是采用普通食品所用的包装。因此需要建立一种高效、快速、高通量的定量监测预制菜塑料包装中添加剂的方法,以有效监测可能存在的风险,保证相关食品接触材料符合安全要求。目前,食品包装材料中添加剂的检测方法有液相色谱法[14-15]、液相色谱-质谱法[16-18]、气相色谱法[18-20]、气相色谱-质谱法[20-22]等。其中,液相色谱法灵敏度较低,无法满足准确定性要求;气相色谱法以及气相色谱-质谱法在分析样品时需要进行衍生化处理,操作较为繁琐;液相色谱-质谱法则无需进行衍生化处理,且在定性方面具有较高的准确性[23]。因此,本研究基于超高效液相色谱-串联质谱法(ultra-performance liquid chromatography-tandem mass spectrometry, UPLC-MS/MS)建立了同时测定预制菜塑料包装中抗氧化剂、光引发剂、荧光增白剂、紫外吸收剂等32种添加剂的残留量及迁移量的方法,旨在为预制菜塑料包装中添加剂的分析检测和安全监管提供技术参考。
1 材料与方法
1.1 材料与试剂
标准品:五类添加剂(抗氧化剂、荧光增白剂、光引发剂、紫外吸收剂、其他)的标准储备液(质量浓度为100 μg/mL),天津阿尔塔科技有限公司;聚对苯二甲酸乙二醇酯(polyethylene terephthalate, PET)、聚酰胺(polyethylene terephthalate, PA)、聚乙烯(polyethylene, PE)、聚丙烯(polypropylene, PP)材料,重庆市东银包装有限公司;甲醇、乙腈、乙酸(色谱级),ACS恩科化学公司;正己烷(色谱级),上海合勒化学科技有限公司;甲酸(质谱纯),美国Sigma公司;异辛烷(色谱级),美国TEDIA公司;无水乙醇,重庆川东化工集团有限公司;实验用水为Milli-Q超纯水。
1.2 仪器与设备
API 4000+超高效液相色谱-四极杆飞行时间质谱仪,美国AB SCIEX公司;XJ-700KT超声仪,方需科技有限公司;VORTEX 3涡旋振荡仪,IKA;MD200-2氮吹仪,杭州奥盛仪器有限公司;PR223ZH/E电子天平,常州奥豪斯仪器有限公司;FD115恒温干燥箱,德国BINDER。
1.3 实验方法
1.3.1 添加剂残留量的测定
分别将PET、PA、PE、PP剪碎至小于5 mm×5 mm的碎片。将上述4种材料分别取0.2 g试样于20 mL洁净的棕色具塞玻璃管中,加入5 mL乙腈,在40 ℃下超声提取30 min,将提取液转移至干净的玻璃管中,再加入5 mL乙腈重复提取1次,合并2次的提取液,取2 mL提取液在40 ℃下氮吹至近干,用甲醇定容至1 mL,过0.22 μm有机相微孔滤膜后使用UPLC-MS/MS分析。样品中添加剂残留量的计算如公式(1)所示:
(1)
式中:M,样品中添加剂的含量,mg/kg;c,UPLC-MS/MS测定的添加剂的质量浓度,mg/L;V,提取液稀释后的体积,mL;m,样品的质量,g。
1.3.1.1 提取溶剂的优化
本实验以回收率为指标,将32种添加剂分为抗氧化剂、光引发剂、荧光增白剂、紫外吸收剂以及其他类(包含硬脂酸、油酸酰胺、己二酸)五大类。取0.2 g 样品,加入5 mL提取溶剂,超声30 min后对甲醇、乙腈、正己烷3种溶剂进行比较,筛选出最佳提取溶剂。
1.3.1.2 提取时间的优化
取0.2 g PP、PE、PA、PET样品,加入5 mL乙腈,比较不同超声提取时间对回收率的影响。超声提取时间分别设置为10、20、30、40 min。
1.3.1.3 提取固液比的优化
取0.2 g PP、PE、PA、PET样品,分别按照1∶15、1∶20、1∶25、1∶30的固液比(g∶mL)加入不同体积(3、4、5、6 mL)的乙腈,超声提取30 min后测定4种塑料材料中五类添加剂的回收率。
1.3.1.4 提取次数的优化
取0.2 g PP、PE、PA、PET样品,加入5 mL乙腈超声提取30 min,比较不同提取次数下(1、2、3次)4种塑料材料中五类添加剂的回收率。
1.3.2 添加剂迁移量的测定
按照欧盟法规NO 10/2011及GB 31604.1—2023《食品安全国家标准 食品接触材料及制品 迁移试验通则》的要求,对样品进行迁移实验,选用4%(体积分数)乙酸、10%乙醇、异辛烷3种食品模拟物。以PP、PE、PA、PET 4种材料为基质,将其剪成3 cm×4 cm 的碎片放入干净的玻璃管中,加入20 mL食品模拟液。结合预制菜的实际应用条件,使用以下迁移条件来模拟预制菜包装经历的灭菌、贮藏以及再加热过程:a)水基模拟物(4%乙酸和10%乙醇)的迁移条件为121 ℃ 0.5 h、40 ℃ 10 d、100 ℃ 0.5 h;b)油脂类模拟物(异辛烷)的迁移条件为60 ℃ 1.5 h、20 ℃ 2 d、60 ℃ 0.5 h的迁移条件。为进行对比,选择40 ℃ 10 d的迁移条件来测定作为普通食品塑料包装的迁移量。准确移取1 mL浸泡后的食品模拟液在40 ℃下氮吹至近干,用甲醇定容至1 mL,过0.22 μm有机相微孔滤膜后使用UPLC-MS/MS分析。迁移量的计算如公式(2)所示:
(2)
式中:X,各添加剂的特定迁移量,mg/kg;c,UPLC-MS/MS测定的添加剂的质量浓度,mg/L;V,迁移实验中浸泡液的体积,L;S0,迁移实验中试样与浸泡液接触的面积,dm2。S,样品实际使用中与食品接触的面积,dm2;m,样品实际接触固态食品的质量或实际接触液态食品的体积所对应的质量,kg。对于无法估算包装袋的实际接触面积(S)与食品或食品模拟物的体积(V)的比(S/V),采用6 dm2食品接触材料接触1 kg的食品或食品模拟物。
1.3.3 标准溶液的配制
将质量浓度为100 μg/mL的5类添加剂的标准储备液以甲醇为溶剂分别稀释为10 μg/mL的中间液,准确移取各中间液1 mL至10 mL容量瓶中,加入甲醇定容制成1 μg/mL的混合标准使用液。准确移取混合标准使用液,用甲醇配制成各组分质量浓度分别为5.0、10.0、20、50、100 ng/mL的混合标准系列溶液。
1.3.4 UPLC-MS/MS仪器条件
1.3.4.1 色谱条件
色谱柱:ACQUITY UPLC BEH C18 色谱柱(100 mm×2.1 mm×1.7 μm);柱温:35 ℃;流动相A:0.1%甲酸水,B:乙腈。梯度洗脱:0.0~3.0 min,10% B;3.0~5.0 min,10%~30% B;5.0~10.0 min,30%~50% B;10.0~15.0 min,50%~56% B;15.0~32.0 min,56%~95% B;32.0~32.05 min,95%~10% B;32.05~35 min,10% B。流速:0.35 mL/min;进样量:10 μL。
1.3.4.2 质谱条件
离子源:电喷雾离子源(ESI);扫描方式:正离子扫描;检测方式:多反应监测;气帘气(N2):25 psi;雾化气(N2):55 psi;加热辅助气(N2):55 psi;离子源温度:500 ℃;去簇电压:50 V;碰撞能量:22 eV;32种添加剂的质谱参数见表1。
表1 三十二种添加剂的质谱参数
Table 1 Mass spectrometry parameters of 32 additives
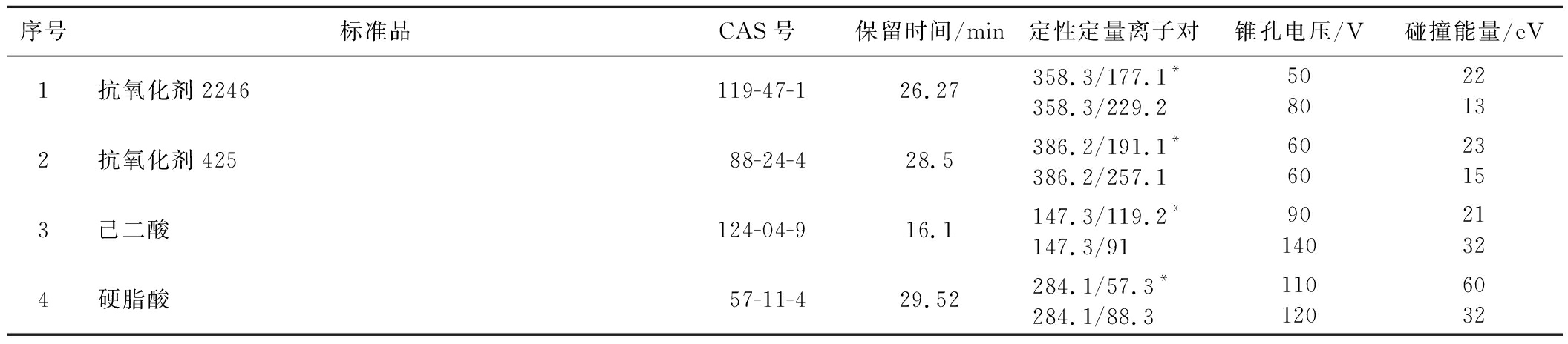
序号标准品CAS号保留时间/min定性定量离子对锥孔电压/V碰撞能量/eV1抗氧化剂2246119-47-126.27358.3/177.1*358.3/229.2508022132抗氧化剂42588-24-428.5386.2/191.1*386.2/257.1606023153己二酸124-04-916.1147.3/119.2*147.3/919014021324硬脂酸57-11-429.52284.1/57.3*284.1/88.31101206032
续表1

序号标准品CAS号保留时间/min定性定量离子对锥孔电压/V碰撞能量/eV5油酸酰胺301-02-026.33282.3/69.2*282.3/83.15050151561-(联苯基-4-基)-2-甲基-2-吗啉基丙烷-1-酮94576-68-810.32309.8/195.1*309.8/88.39090373472,4-二乙基硫杂蒽-9-酮82799-44-823.65269.2/213.2*269.2/241.47070363182-苯甲酰基苯甲酸甲酯606-28-012.09241.1/209*241.1/1528816469光引发剂369119313-12-18.17367.3/190.3*367.3/294.360602727104,4'-双(二乙基氨基)二苯甲酮90-93-717.76324.8/176.1*324.8/281.3100803937114-二甲氨基苯甲酸乙酯10287-53-312.59194.2/151*194.2/1348080314212光引发剂379119344-86-48.93381.3/190*381.3/3085050221813光引发剂90771868-10-57.7280.1/165.2*280.1/88.25050303214光引发剂EHA21245-02-325.42278.2/166.2*278.2/151.28585294215光引发剂ITX5495-84-120.97255.1/213.1*255.1/184.27070305516光引发剂TPO75980-60-816.09349.1/147.1*349.1/1195050202617米氏酮90-94-813.33269.2/148.2*269.2/120.270703030182,4-二羟基二苯甲酮131-56-611.02215.1/137*215.1/10580802535194,4'-二氟二苯甲酮345-92-613.78219.1/123.1*219.1/95.175752435202,2'-羟基-4-甲氧基二苯甲酮131-53-312.08245.2/121.1*245.2/93.250502035212-羟基-4-n-己氧基苯甲酮3293-97-826.29299/137*299/105.150503536222-羟基-4-正辛氧基二苯甲酮1843-05-629.8327/137*327/104.95050303023荧光增白剂WS91-44-112.56232.1/188.1*232.1/160.15353364024荧光增白剂PF1041-00-520.02291.1/107.1*291.1/77.115058447325荧光增白剂OB7128-64-532.74431.2/415.2*431.2/401.2130130575626荧光增白剂EBF2866-43-520.4319.1/226.1*319.1/200.17575415027荧光增白剂KCB5089-22-527.42363.1/270.1*363.1/244.1170170475128紫外吸收剂UV-9131-57-714.56229.1/150.9*229.1/77.15050164429紫外吸收剂UV-712440-22-418.53226/120*226/1075050202030紫外吸收剂UV-23470321-86-732.12448.2/370.1*448.2/915050206831紫外吸收剂UV-3263896-11-531.43316/107.1*316/2604545252032紫外吸收剂UV-3293147-75-929.83324.4/92*324.4/212.140404525
注:*表示定量离子。
1.4 数据分析
采用仪器自带的数据软件MultiQuant定性定量分析软件处理实验数据,使用Microsoft Excel 2010进行统计分析,使用Origin 2024b软件作图,使用IBM SPSS Statistics 26进行显著性分析。
2 结果与分析
2.1 色谱条件优化
液相色谱-质谱分析常用的流动相有甲醇/水和乙腈/水,其中水相中可以加入甲酸、乙酸铵来促进离子化,甲酸有助于提高正离子的信号强度[24]。本实验中32种添加剂在ESI+模式下均获得[M+H]+准分子离子峰,因此,在流动相中添加甲酸可有效提高其离子化效率。本实验考察了0.1%甲酸-甲醇和0.1%甲酸-乙腈流动相体系对目标化合物的色谱分离行为。有机相为甲醇时整体出峰较晚,仅分离出18种物质,出峰时间集中在26~34 min,各添加剂的分离度差,峰拖尾现象严重;乙腈作为有机相时分离度好,可对每种目标化合物进行精准定量测定,因此选用0.1%甲酸-乙腈作为流动相。
2.2 质谱条件优化
在ESI+离子化模式下,使用100 ng/mL混标溶液自动调谐,逐一选择适合各添加剂的准分子离子峰,确定母离子。
采用子离子扫描方式进行二级质谱分析,对子离子进行优化选择,确定定量离子和定性离子,并优化了毛细管电压、锥孔电压、碰撞能量等质谱参数,使32种添加剂的准分子离子与特征碎片离子产生的离子对强度达到最大。各添加剂的定性定量离子对、锥孔电压、碰撞能量见表1。
2.3 前处理条件优化
2.3.1 提取溶剂的选择
对于塑料添加剂的提取,多采用甲醇、乙腈、正己烷、二氯甲烷、乙酸乙酯等。本实验以提取回收率为指标,对甲醇、乙腈、正己烷溶剂进行比较,筛选出最佳提取溶剂,实验结果如图1所示。32种添加剂分为抗氧化剂、光引发剂、荧光增白剂、紫外吸收剂以及其他类(包含硬脂酸、油酸酰胺、己二酸)五大类。由图1可知,PP材料中抗氧化剂、光引发剂以及其他类在乙腈中的回收率显著(P<0.05)高于甲醇和正己烷;PE材料中除光引发剂和其他类外乙腈的回收率均显著(P<0.05)高于其余2种溶剂;PA材料中抗氧化剂和其他类中乙腈显著(P<0.05)高于其余2种溶剂,且另外3类添加剂在3种提取溶剂中的回收率相差较小;在PET材料中,乙腈相比于其余两者的回收率均具有显著性差异(P<0.05)。因此,在4种材料中,大多数添加剂在乙腈中的回收率显著(P<0.05)高于甲醇和正己烷,最终选用乙腈作为提取溶剂。

a-PP材料;b-PE材料;c-PA材料;d-PET材料
图1 四种材料在不同提取溶剂下的回收率
Fig.1 Recovery rates of four materials in different extraction solvents
注:不同字母表示差异显著(P<0.05)(下同)。
2.3.2 超声时间的选择
使用乙腈作为提取溶剂,比较了不同超声提取时间对回收率的影响。超声提取时间分别设置为10、20、30、40 min,结果见图2。结果表明,大多数添加剂的回收率随超声时间的延长而升高,且在超声提取30 min时达最大值,之后随超声时间的延长回收率基本保持不变甚至有所下降。将各类添加剂在不同时间下的回收率进行显著性分析,结果表明在PP材料中,各类添加剂在提取时间为30 min和40 min时的回收率无显著性差异,且显著(P<0.05)高于提取时间为10 min和20 min的回收率;在PE材料中,除其他类在提取时间为30 min与40 min时的回收率无显著性差异外,30 min时各类添加剂的回收率均显著(P<0.05)高于其余提取时间;在PA和PET材料中,绝大部分添加剂呈现出在30 min和40 min的回收率无显著性差异,且显著(P<0.05)高于其余提取时间的回收率。因此,确定超声提取时间为30 min。
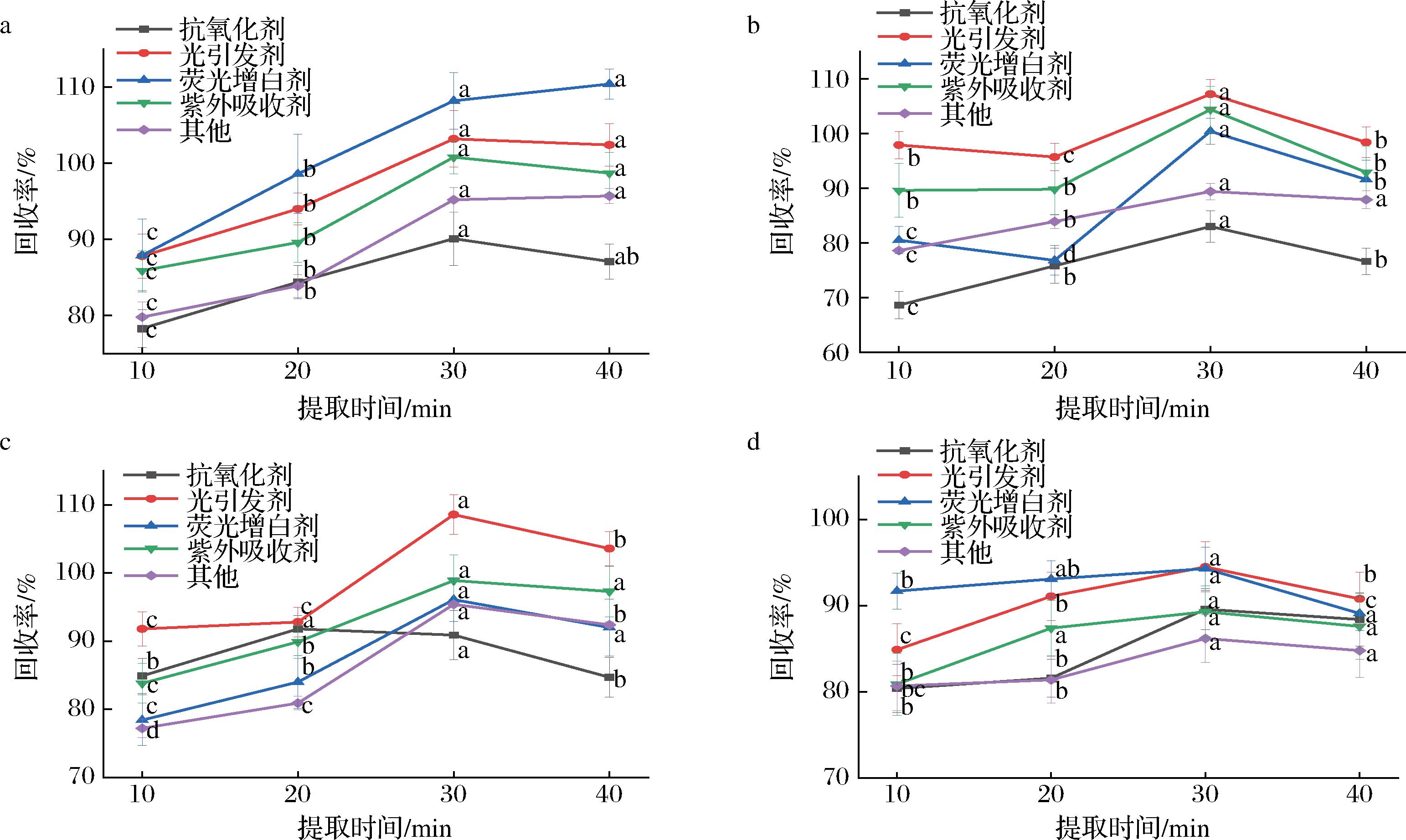
a-PP材料;b-PE材料;c-PA材料;d-PET材料
图2 四种材料在不同提取时间下的回收率
Fig.2 Recovery rates of four materials under different extraction time
2.3.3 超声固液比的选择
取0.2 g样品,分别按照1∶15、1∶20、1∶25、1∶30的固液比(g∶mL)加入不同体积(3、4、5、6 mL)的乙腈,超声提取30 min后测定4种塑料材料中五类添加剂的回收率,实验结果如图3所示。可以看出,4种塑料中各类添加剂的回收率均是在固液比为1∶25时达到最高,在1∶30时回收率基本保持不变甚至降低。这可能是由于溶剂量较小时,没有充分提取出塑料样品中的添加剂,而当溶剂量过大时,包装中添加剂已被充分提取,剩余的溶剂导致提取溶液稀释。将各类添加剂在不同提取固液比下的回收率进行显著性分析,结果表明在PP材料中,抗氧化剂和紫外吸收剂在固液比为1∶25时的回收率与1∶30无显著性差异,且显著(P<0.05)高于其余固液比下的回收率,剩余三类添加剂在1∶20时的回收率与1∶25、1∶30相比无显著性差异;在PE材料中,固液比为1∶25时的回收率显著(P<0.05)高于1∶15、1∶20,与1∶30相比除光引发剂外均无显著性差异;在PA材料和PET材料中除其他类外,固液比1∶25时的回收率相比于1∶30无显著性差异,且显著(P<0.05)高于其余两者的回收率。因此,本实验选用的超声固液比为1∶25。
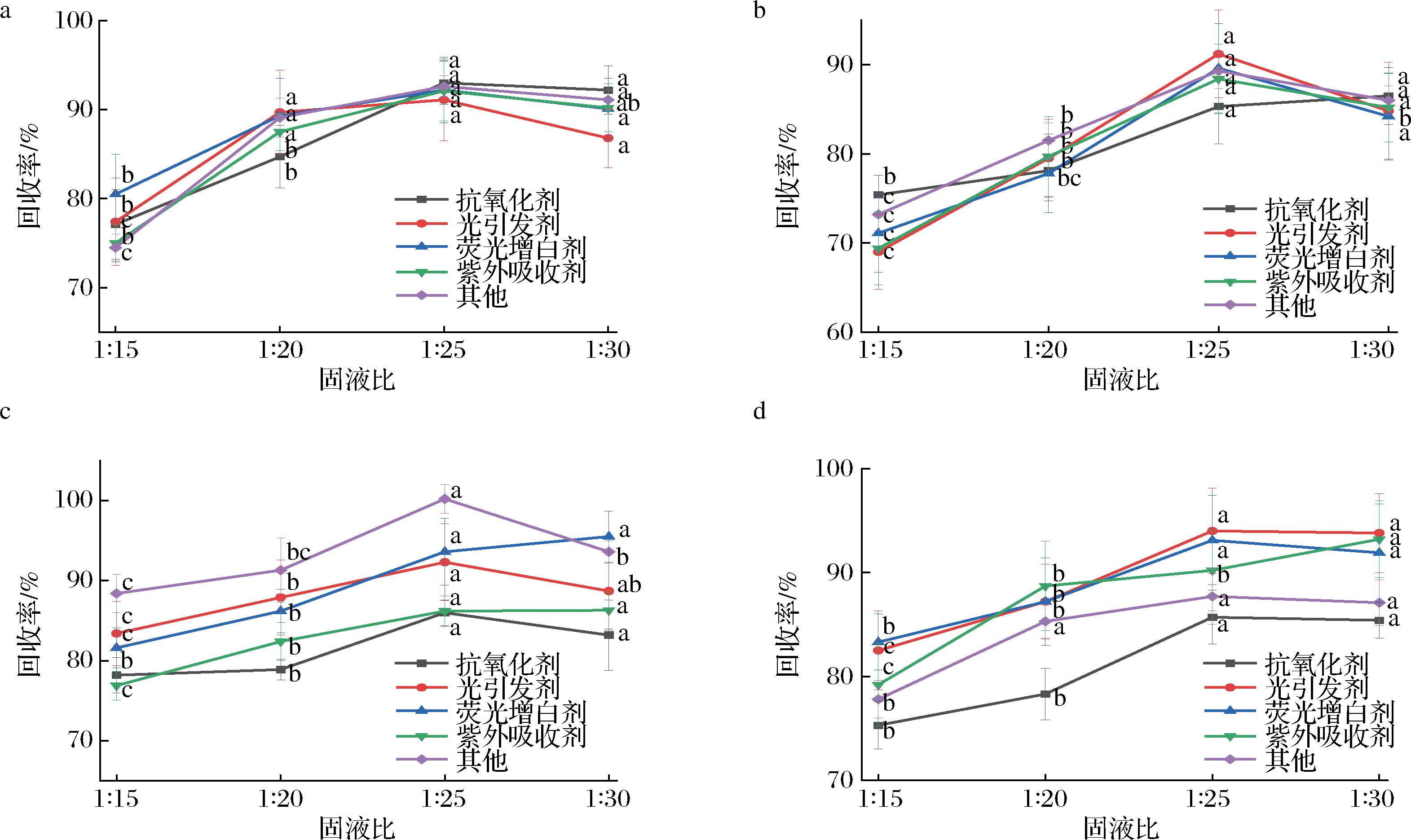
a-PP材料;b-PE材料;c-PA材料;d-PET材料
图3 四种材料在不同固液比下的回收率
Fig.3 Recovery rates of four materials under different solid-liquid ratios
2.3.4 超声提取次数的选择
取0.2 g样品,加入5 mL乙腈超声提取30 min,比较不同提取次数下(1、2、3次)4种塑料材料中五类添加剂的回收率,结果如图4所示。大多数添加剂在提取次数为2次时,回收率达到较高水平,提取2次和3次的回收率差别较小。将各类添加剂在不同提取次数下的回收率进行显著性分析,结果表明在4种材料中,除光引发剂和荧光增白剂在不同提取次数下无显著性差异外,其余添加剂在提取次数为2次时的回收率均显著(P<0.05)高于提取1次时的回收率;提取次数为2次和3次相比,除PP材料中的抗氧化剂以及PE材料中的紫外吸收剂外,其余添加剂均无显著性差异。因此,为提高提取效率,降低实验成本,缩短实验时间,本方法确定为提取2次。
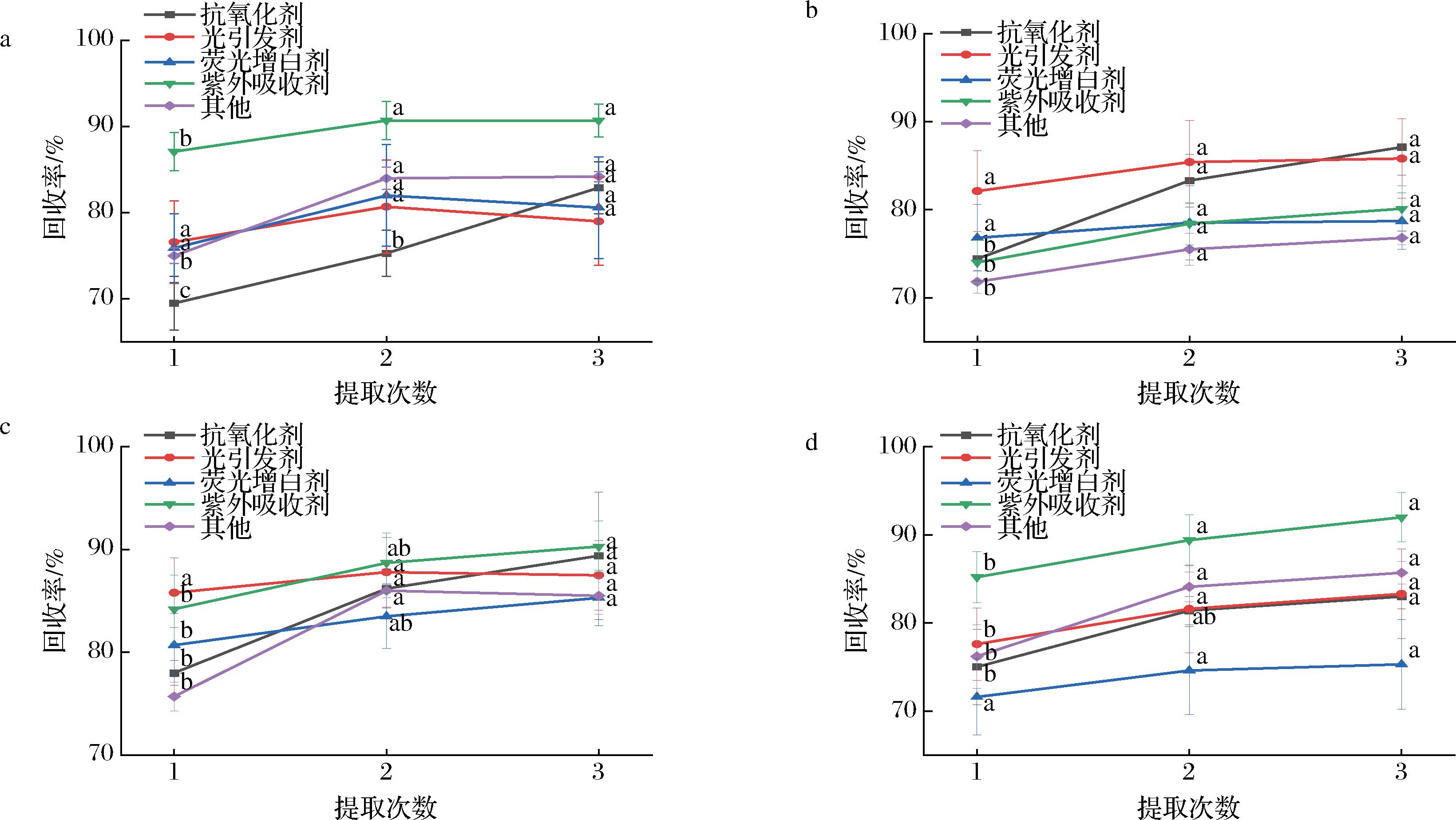
a-PP材料;b-PE材料;c-PA材料;d-PET材料
图4 四种材料在不同提取次数下的回收率
Fig.4 Recovery rates of four materials under different extraction times
2.4 线性关系、方法检出限与定量限
本文使用甲醇配制32种添加剂的系列标准溶液,质量浓度分别为5、10、20、50、100 ng/mL,在优化的色谱-质谱条件下进行分析,以各添加剂的离子峰面积为纵坐标,质量浓度为横坐标进行线性回归。32种添加剂的线性范围、线性方程、相关系数、定量限以及检出限如表2所示。实验结果表明,32种添加剂在5~100 ng/mL的线性范围内均呈良好线性关系,相关系数(r2)大于0.998,检出限(limit of detection, LOD)为1~3 ng/mL,定量限(limit of quantitation, LOQ)为5 ng/mL。
表2 三十二种添加剂的线性方程、相关系数、检出限及定量限
Table 2 Linear range, linear equation, correlation coefficient, detection limit and quantitation limit of 32 additives

序号标准品线性范围/(ng/mL)线性方程相关系数LOD/(ng/mL)LOQ/(ng/mL)1抗氧化剂22465~100y=0.338 58x+0.0188 00.999 73152抗氧化剂4255~100y=0.278 03x+0.0145 90.998 09353己二酸5~100y=1.570 16x+0.139 550.999 14354硬脂酸5~100y=1.425 77x+0.593 890.999 82155油酸酰胺5~100y=0.204 81x+0.159 430.998 502561-(联苯基-4-基)-2-甲基-2-吗啉基丙烷-1-酮5~100y=15.999 16x+0.296 780.999 571572,4-二乙基硫杂蒽-9-酮5~100y=6.765 13x+0.045 700.999 061582-苯甲酰基苯甲酸甲酯5~100y=16.418 30x+0.328 510.998 38159光引发剂3695~100y=7.488 60x+0.027 610.998 7235104,4'-双(二乙基氨基)二苯甲酮5~100y=28.104 87x+1.465 000.998 3915114-二甲氨基苯甲酸乙酯5~100y=9.019 94x+0.127 050.998 661512光引发剂3795~100y=12.138 10x+0.462 370.999 141513光引发剂9075~100y=18.010 48x+0.814 770.999 223514光引发剂EHA5~100y=41.167 55x+0.456 620.999 031515光引发剂ITX5~100y=24.251 55x+0.143 550.999 543516光引发剂TPO5~100y=3.325 84x+0.176 780.999 731517米氏酮5~100y=33.009 55x+2.648 840.998 6015182,4-二羟基二苯甲酮5~100y=3.979 99x-0.053 470.999 3235194,4'-二氟二苯甲酮5~100y=2.053 31x+0.012 520.999 6815202,2'-羟基-4-甲氧基二苯甲酮5~100y=30.505 73x+1.587 990.998 7035212-羟基-4-n-己氧基苯甲酮5~100y=4.931 61x-0.092 950.998 7725222-羟基-4-正辛氧基二苯甲酮5~100y=14.289 21x+0.137 250.999 503523荧光增白剂WS5~100y=15.230 70x+0.075 970.999 751524荧光增白剂PF5~100y=1.592 50x-0.035 420.999 953525荧光增白剂OB5~100y=1.821 44x-0.023 630.998 481526荧光增白剂EBF5~100y=3.716 01x-0.031 670.999 931527荧光增白剂KCB5~100y=2.760 50x-0.020 340.999 461528紫外吸收剂UV-95~100y=10.578 08x+0.196 640.998 272529紫外吸收剂UV-715~100y=7.155 05x-0.002 510.999 912530紫外吸收剂UV-2345~100y=9.475 67x+0.569 380.998 861531紫外吸收剂UV-3265~100y=0.146 64x+0.014 260.999 283532紫外吸收剂UV-3295~100y=1.302 69x+0.024 650.999 1725
2.5 添加剂残留量及迁移量测定实验的回收率和精密度
2.5.1 食品包装材料中添加剂残留量的测定
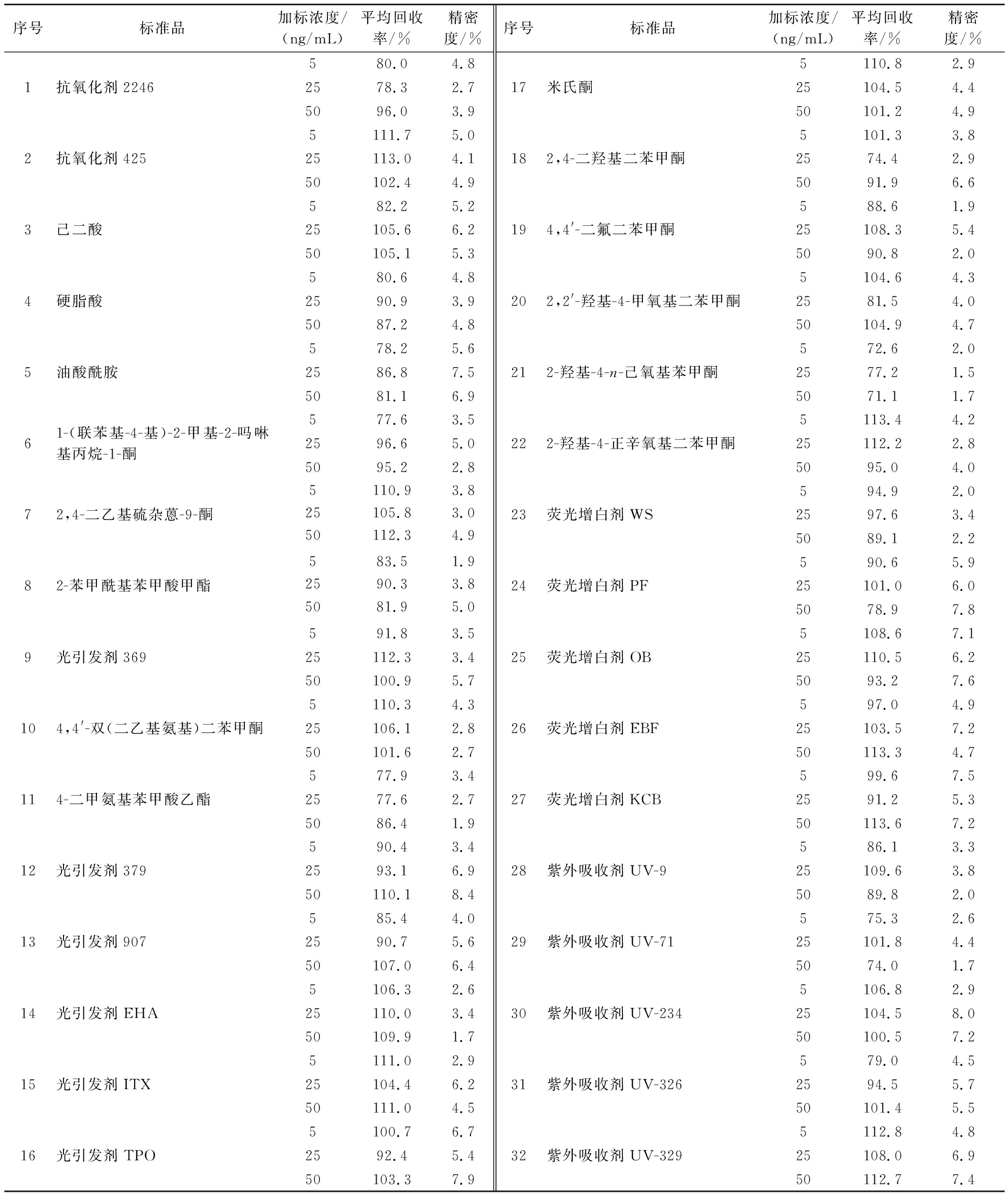
按照1.3.1节样品提取条件,分别添加定量限的1、5、10倍3个水平进行回收率实验和精密度实验,每个添加量进行6次平行实验,同时做空白实验,均扣除本底值后计算加标回收率和相对标准偏差,回收率及其精密度见表3。32种添加剂的平均回收率为71.1%~113.6%,相对标准偏差(relative standard deviation, RSD)为1.5%~8.4%,表明该方法具有较好的可靠性和重复性,满足分析要求。
表3 食品包装材料中三十二种添加剂的加标平均回收率及其精密度
Table 3 Average spiked recoveries and precision of 32 additives in food packaging materials
序号标准品加标浓度/(ng/mL)平均回收率/%精密度/%序号标准品加标浓度/(ng/mL)平均回收率/%精密度/%1抗氧化剂2246580.04.82578.32.75096.03.917米氏酮5110.82.925104.54.450101.24.92抗氧化剂4255111.75.025113.04.150102.44.9182,4-二羟基二苯甲酮5101.33.82574.42.95091.96.63己二酸582.25.225105.66.250105.15.3194,4'-二氟二苯甲酮588.61.925108.35.45090.82.04硬脂酸580.64.82590.93.95087.24.8202,2'-羟基-4-甲氧基二苯甲酮5104.64.32581.54.050104.94.75油酸酰胺578.25.62586.87.55081.16.9212-羟基-4-n-己氧基苯甲酮572.62.02577.21.55071.11.761-(联苯基-4-基)-2-甲基-2-吗啉基丙烷-1-酮577.63.52596.65.05095.22.8222-羟基-4-正辛氧基二苯甲酮5113.44.225112.22.85095.04.072,4-二乙基硫杂蒽-9-酮5110.93.825105.83.050112.34.923荧光增白剂WS594.92.02597.63.45089.12.282-苯甲酰基苯甲酸甲酯583.51.92590.33.85081.95.024荧光增白剂PF590.65.925101.06.05078.97.89光引发剂369591.83.525112.33.450100.95.725荧光增白剂OB5108.67.125110.56.25093.27.6104,4'-双(二乙基氨基)二苯甲酮5110.34.325106.12.850101.62.726荧光增白剂EBF597.04.925103.57.250113.34.7114-二甲氨基苯甲酸乙酯577.93.42577.62.75086.41.927荧光增白剂KCB599.67.52591.25.350113.67.212光引发剂379590.43.42593.16.950110.18.428紫外吸收剂UV-9586.13.325109.63.85089.82.013光引发剂907585.44.02590.75.650107.06.429紫外吸收剂UV-71575.32.625101.84.45074.01.714光引发剂EHA5106.32.625110.03.450109.91.730紫外吸收剂UV-2345106.82.925104.58.050100.57.215光引发剂ITX5111.02.925104.46.250111.04.531紫外吸收剂UV-326579.04.52594.55.750101.45.516光引发剂TPO5100.76.72592.45.450103.37.932紫外吸收剂UV-3295112.84.825108.06.950112.77.4
2.5.2 食品包装材料中添加剂迁移量的测定
按照1.3.2节处理方法,平行测定6次,32种添加剂在3种模拟物中的回收率与精密度结果见表4。在异辛烷中,32种添加剂的平均回收率为72.4%~104.9%,RSD为0.1%~8.8%;在4%乙酸中,平均回收率为73.6%~101.8%,RSD为0.3%~8.0%;在10%乙醇中,平均回收率为75.0%~107.6%,RSD为0.5%~8.3%,说明该方法准确可靠,能够实现预制菜塑料包装中添加剂迁移量的准确检测。
表4 添加剂迁移的加标平均回收率与精密度
Table 4 Average spiked recoveries and precision of additive migration

序号标准品加标浓度/(ng/mL)4%乙酸10%乙醇异辛烷平均回收率/%精密度/%平均回收率/%精密度/%平均回收率/%精密度/%1抗氧化剂2246584.50.977.92.678.60.12586.02.178.74.782.73.95088.91.482.22.585.53.52抗氧化剂425585.93.477.75.976.13.42595.12.682.78.392.73.35085.25.189.53.384.72.63己二酸588.31.578.52.886.01.72588.11.286.71.379.82.95092.72.286.54.484.72.14硬脂酸576.25.487.88.186.44.32578.52.188.52.186.21.95088.41.195.81.483.53.75油酸酰胺576.71.087.81.777.52.92579.61.783.34.085.42.55078.65.3104.37.292.51.761-(联苯基-4-基)-2-甲基-2-吗啉基丙烷-1-酮578.61.279.12.475.41.22577.33.778.43.076.63.65076.74.275.02.079.63.272,4-二乙基硫杂蒽-9-酮580.84.586.75.3104.95.42585.40.892.81.599.62.55083.33.387.03.990.51.582-苯甲酰基苯甲酸甲酯581.11.777.92.995.42.22587.52.286.82.199.94.65080.83.784.42.282.37.69光引发剂369582.41.696.53.076.43.02586.91.4101.65.176.44.05095.53.594.53.576.03.0104,4'-双(二乙基氨基)二苯甲酮586.76.198.98.178.00.62593.34.098.42.594.63.45084.42.993.66.192.24.6114-二甲氨基苯甲酸乙酯581.13.392.12.384.54.22577.41.687.63.589.86.35078.91.686.62.581.41.312光引发剂379588.53.592.28.080.42.32581.30.381.65.383.85.65084.05.693.44.794.21.013光引发剂907586.41.588.21.881.12.72578.31.778.51.779.32.45091.50.883.81.778.84.814光引发剂EHA581.23.576.44.294.48.12582.25.575.13.696.05.45079.60.480.25.488.95.615光引发剂ITX582.31.284.41.398.33.72583.12.186.13.796.66.45080.12.589.53.397.15.316光引发剂TPO584.01.484.73.096.52.42593.22.980.22.278.31.05078.91.881.51.884.22.817米氏酮575.81.776.03.680.34.22577.41.078.71.576.31.85083.42.481.82.581.82.5182,4-二羟基二苯甲酮597.57.283.74.478.62.52578.56.591.51.693.11.85083.34.791.15.590.14.3194,4'-二氟二苯甲酮580.84.777.03.396.33.42579.92.685.12.891.33.65080.32.183.93.899.12.1202,2'-羟基-4-甲氧基二苯甲酮579.77.583.65.594.56.92581.90.887.31.291.91.65085.20.589.70.591.30.7
续表4

序号标准品加标浓度/(ng/mL)4%乙酸10%乙醇异辛烷平均回收率/%精密度/%平均回收率/%精密度/%平均回收率/%精密度/%212-羟基-4-n-己氧基苯甲酮581.71.587.60.893.36.32583.91.983.91.990.92.65085.73.088.52.987.92.9222-羟基-4-正辛氧基二苯甲酮583.51.485.23.885.72.82587.22.882.22.687.72.15086.15.088.24.690.94.323荧光增白剂WS5101.86.098.15.7100.18.82594.01.898.42.499.36.95085.54.489.08.383.61.424荧光增白剂PF578.52.677.53.377.73.32576.33.178.03.484.94.05073.63.676.32.878.63.025荧光增白剂OB580.12.487.03.282.65.425101.34.3107.64.681.53.550101.08.080.43.085.01.926荧光增白剂EBF576.32.580.91.974.01.62583.91.380.31.172.41.15079.74.177.93.975.04.027荧光增白剂KCB583.91.977.64.183.33.82586.72.376.43.782.02.05084.62.984.74.878.24.228紫外吸收剂UV-9578.51.697.23.089.98.22581.45.599.92.280.71.25081.11.096.54.595.23.829紫外吸收剂UV-71580.63.178.31.483.72.02583.02.576.61.890.76.15082.22.079.84.388.21.930紫外吸收剂UV-234583.43.782.85.376.71.82582.51.378.42.388.10.95082.92.282.11.6101.84.631紫外吸收剂UV-326583.62.877.64.088.53.42577.52.385.12.989.60.75078.13.881.01.787.71.032紫外吸收剂UV-329592.71.487.73.586.63.32585.72.099.47.888.52.05091.64.596.55.098.95.3
2.6 实际样品测定
2.6.1 实际样品中添加剂残留量的测定
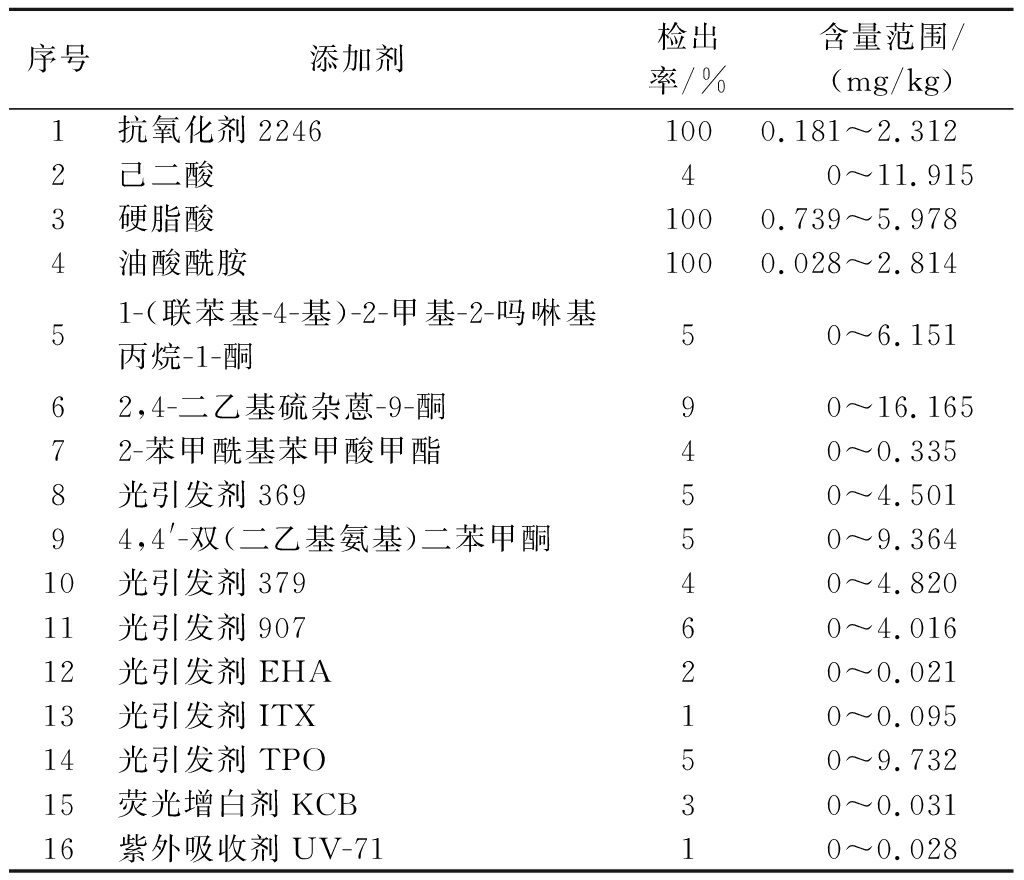
本研究对预制菜企业提供以及网购的100批次生产和流通环节的预制菜塑料包装进行检测,样品的材质主要包含PA/PE、PE/PET、PA/CPP、BOPP/PE/PET、BOPP/RCPP等。对包装中添加剂的残留量进行了测定,各添加剂的检出率及其含量范围结果如表5所示。其中抗氧化剂2246、硬脂酸、油酸酰胺的检出率为均为100%,其余物质的检出率较低。此外,荧光增白剂OB在部分样品中也被检出,但其浓度低于定量限。GB 9685—2016 《食品安全国家标准 食品接触材料及制品用添加剂使用标准》,抗氧化剂2246的残留量限制为1.5 mg/kg,荧光增白剂OB的残留量限制为0.6 mg/kg。本实验测定的样品中,16%的样品存在抗氧化剂2246超标现象,因此,相关部门应加强对预制菜塑料包装中抗氧化剂残留的关注和监管。此外,样品中有一些添加剂的残留量较高,如硬脂酸、油酸酰胺,目前国标未明确规定其限值,因此也可能存在一定的风险。
表5 实际样品中添加剂残留量的检出情况
Table 5 Detection of additive residues in actual samples
序号添加剂检出率/%含量范围/(mg/kg)1抗氧化剂2246100 0.181~2.312 2己二酸4 0~11.9153硬脂酸100 0.739~5.978 4油酸酰胺100 0.028~2.814 51-(联苯基-4-基)-2-甲基-2-吗啉基丙烷-1-酮5 0~6.15162,4-二乙基硫杂蒽-9-酮9 0~16.16572-苯甲酰基苯甲酸甲酯40~0.3358光引发剂3695 0~4.50194,4'-双(二乙基氨基)二苯甲酮5 0~9.36410光引发剂3794 0~4.82011光引发剂9076 0~4.01612光引发剂EHA2 0~0.02113光引发剂ITX1 0~0.09514光引发剂TPO5 0~9.73215荧光增白剂KCB3 0~0.03116紫外吸收剂UV-711 0~0.028
2.6.2 实际样品中添加剂迁移量的测定
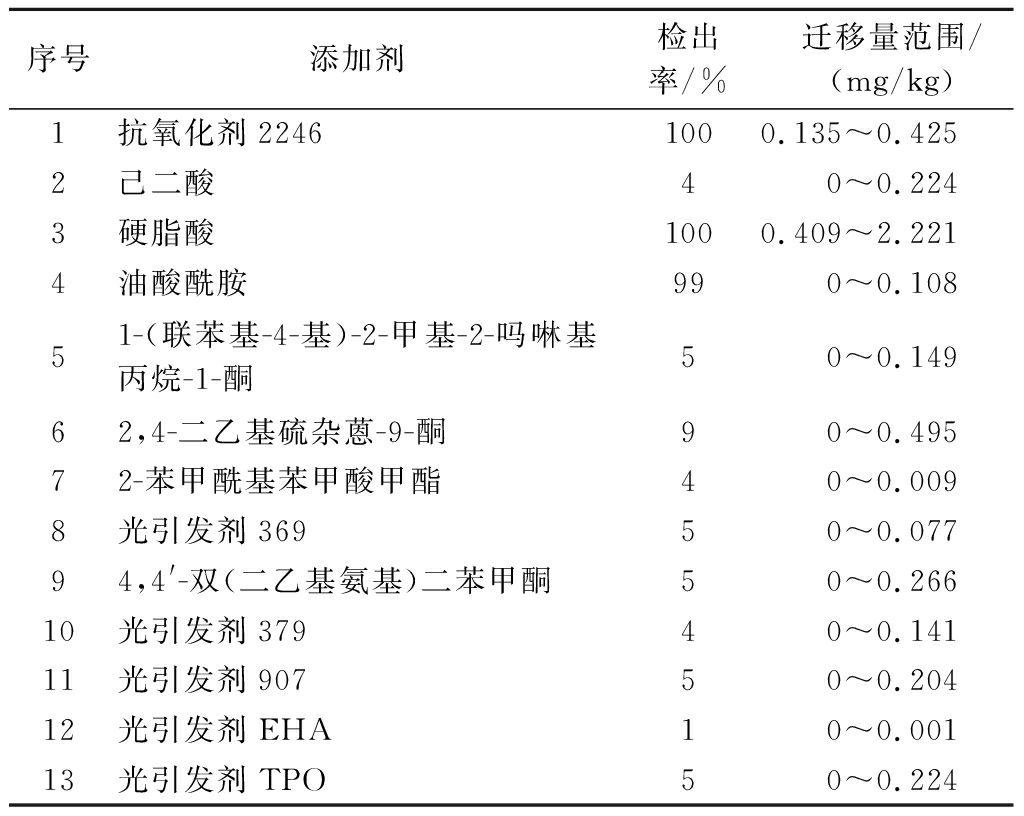
根据上述结果,选取样品添加剂残留量测定中含量较高的5个代表性样品,在4%乙酸、10%乙醇、异辛烷3种食品模拟物下进行迁移实验。结合预制菜的实际应用条件,模拟了灭菌、贮藏以及再加热过程。对于水基模拟物,选择121 ℃ 0.5 h、40 ℃ 10 d、100 ℃ 0.5 h的迁移条件;对于油脂类模拟物,选择60 ℃ 1.5 h、20 ℃ 2 d、60 ℃ 0.5 h的迁移条件。对比5个样品在3种模拟物下32种添加剂的总迁移量,结果如图5所示。样品在异辛烷中的总迁移量明显高于其余2种,表明预制菜在油脂类食品模拟物中的迁移风险更高。因此,本研究将100批次预制菜塑料包装样品在油脂类模拟物中的迁移量进行了测定,结果如表6所示。其中抗氧化剂2246、硬脂酸以及油酸酰胺的检出率高达99%以上,其余物质的检出率较低,且各添加剂的迁移量均较少。此外,荧光增白剂OB在部分样品中也被检出,但其浓度低于定量限,迁移量测定中所有样品均未超标。
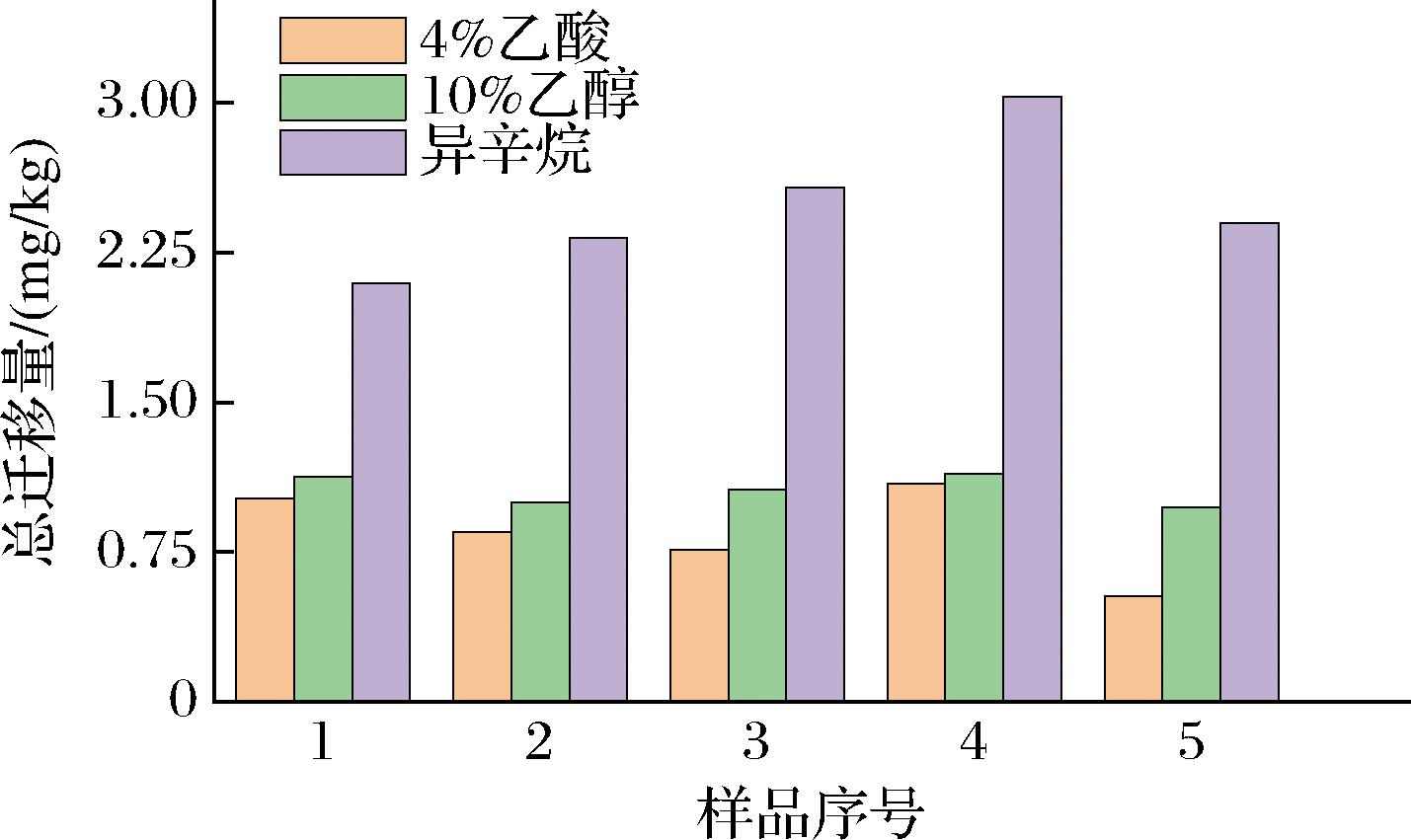
图5 样品在3种食品模拟物中的总迁移量
Fig.5 Total migration of samples in three food simulants
表6 实际样品中添加剂迁移量的检出情况
Table 6 Detection of additive migration in actual samples
序号添加剂检出率/%迁移量范围/(mg/kg)1抗氧化剂2246100 0.135~0.425 2己二酸4 0~0.2243硬脂酸100 0.409~2.221 4油酸酰胺99 0~0.10851-(联苯基-4-基)-2-甲基-2-吗啉基丙烷-1-酮5 0~0.14962,4-二乙基硫杂蒽-9-酮90~0.49572-苯甲酰基苯甲酸甲酯40~0.0098光引发剂36950~0.07794,4'-双(二乙基氨基)二苯甲酮50~0.26610光引发剂3794 0~0.14111光引发剂9075 0~0.20412光引发剂EHA1 0~0.00113光引发剂TPO5 0~0.224
此外将上述结果与100个样品在普通塑料包装迁移条件(40 ℃ 10 d)下各添加剂的平均迁移量进行了对比,结果如图6所示。由图6可知,模拟预制菜加工过程后13种添加剂的平均迁移量均显著高于普通处理。因此,这些包装在作为预制菜包装时存在的风险明显高于普通食品包装。
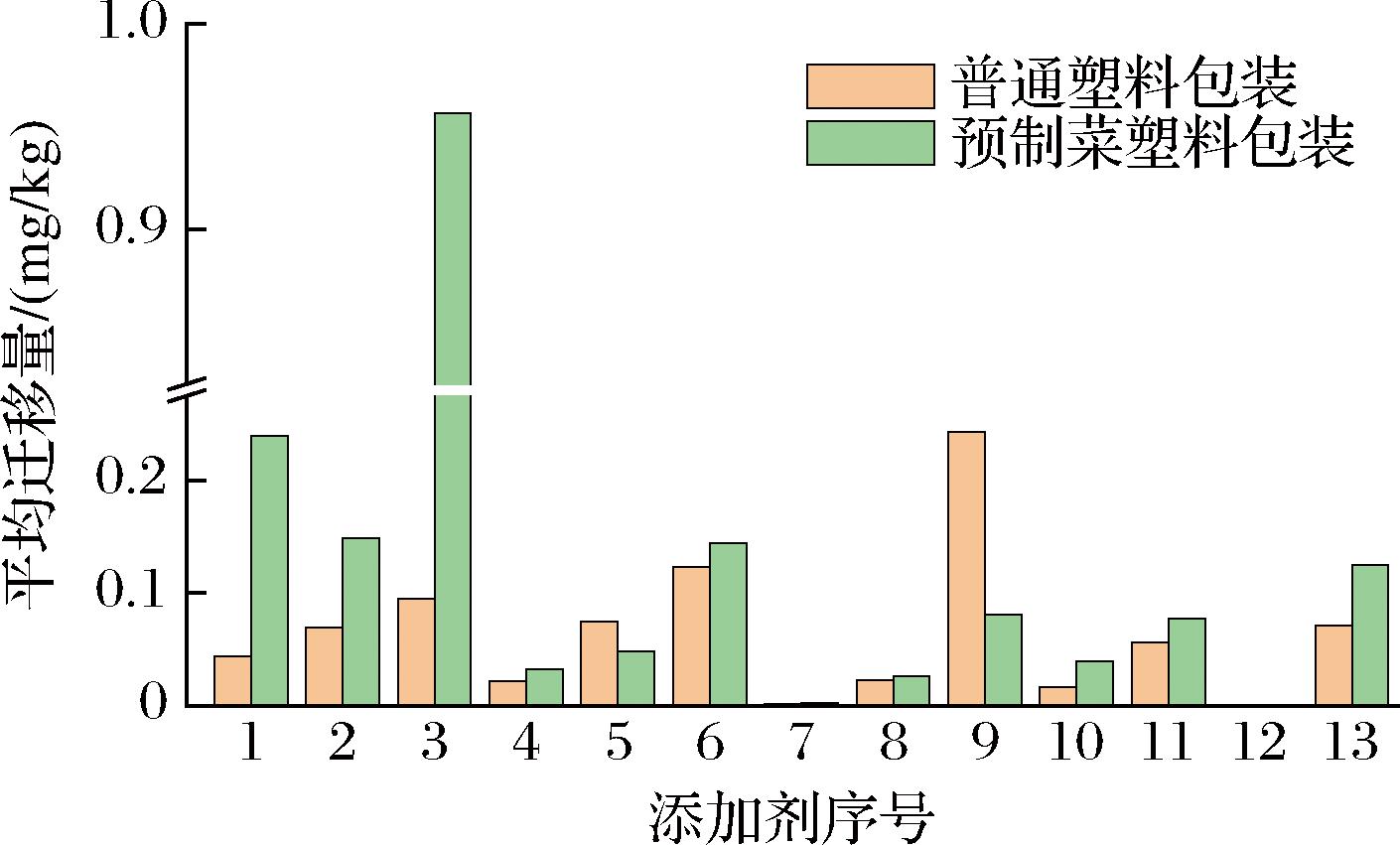
图6 样品在2种处理条件下添加剂的平均迁移量
Fig.6 Average migration of additives under two treatment conditions
3 结论
本文前期通过对流动相和前处理条件进行优化建立了UPLC-MS/MS同时测定预制菜塑料包装材料中32种添加剂残留量及迁移量的方法。32种添加剂在5~100 ng/mL内有良好的线性关系,且具有较好的回收率(71.1%~113.6%)和良好的精密度(0.1%~8.8%),满足检测要求。后期采用该方法对100批次生产和流通环节的预制菜塑料包装进行32种添加剂的残留量检测,结果发现16%的样品中抗氧化剂2246存在超标现象,同时硬脂酸、油酸酰胺的检出率也较高,因此可能存在一定的风险,相关部门应加强监管。在迁移量检测中,尽管迁移结果均符合GB 9685—2016《食品安全国家标准 食品接触材料及制品用添加剂使用标准》的要求,然而部分物质的检出率较高,且其作为预制菜包装时的迁移量明显高于普通包装。因此,为了保障消费者的饮食安全以及推动预制菜行业的健康发展,有必要加强对预制菜包装材料的关注。在后续研究中将针对筛查出的潜在高风险物质进行迁移规律分析以及复合添加剂毒理学评价,为相关监管部门评估预制菜塑料包装中迁移物质的风险提供技术支持。
本研究所建立的方法操作简单、检测化合物种类多、准确高效,可用于市售预制菜塑料包装材料中添加剂残留量及迁移量的检测。本文研究结果可用于预制菜塑料包装生产企业的内部质量控制,也可以为预制菜包装的风险监测提供技术支撑,从而给消费者带来更安全的预制菜产品。
[1] THARREY M, DROGUÉ S, PRIVET L, et al.Industrially processed v.home-prepared dishes:What economic benefit for the consumer?[J].Public Health Nutrition, 2020, 23(11):1982-1990.
[2] 刘昌乐, 刘玉茜.我国预制菜产业的发展现状、面临问题及未来展望[J].食品安全导刊, 2024(22):130-132;136.LIU C L, LIU Y Q.The development status, problems and future prospects of China’s prefabricated food industry[J].China Food Safety Magazine, 2024(22):130-132;136.
[3] 吕湘月. 食品接触塑料包装材料安全性[J].塑料助剂, 2024(1):74-77.LYU X Y.Research on the hygiene and safety analysis of plastic packaging materials in the food industry[J].Plastics Additives, 2024(1):74-77.
[4] 田陆川, 姜红.食品塑料包装材料的检验研究进展[J].安徽化工, 2021, 47(1):4-7.TIAN L C, JIANG H.Study progress on the identification of food plastic packaging materials[J].Anhui Chemical Industry, 2021, 47(1):4-7.
[5] 薛晓熠, 卫荣, 周敏, 等.浅析食品塑料包装的危害及主要检测技术[J].塑料包装, 2022, 32(4):33-36.XUE X Y, WEI R, ZHOU M, et al.Analysis on the harm of food plastic packaging and its main detection technology[J].Plastics Packaging, 2022, 32(4):33-36.
[6] ![]() T, MURAUSKAS T, NAUJALIS E.Validation and application of an LC-MS/MS method for the determination of antioxidants originating from commercial polyethylene packages and their migration into food simulants[J].Food Analytical Methods, 2024, 17(7):1087-1099.
T, MURAUSKAS T, NAUJALIS E.Validation and application of an LC-MS/MS method for the determination of antioxidants originating from commercial polyethylene packages and their migration into food simulants[J].Food Analytical Methods, 2024, 17(7):1087-1099.
[7] 华英迪, 许宜平, 赵高峰, 等.塑料添加剂的环境迁移、毒性测试与风险筛查:进展与挑战[J].生态毒理学报, 2024, 19(2):93-111.HUA Y D, XU Y P, ZHAO G F, et al.Environmental migration, toxicity testing and risk screening for plastic additives:Advances and challenges[J].Asian Journal of Ecotoxicology, 2024, 19(2):93-111.
[8] GROH K J, BACKHAUS T, CARNEY-ALMORTH B, et al.Overview of known plastic packaging-associated chemicals and their hazards[J].Science of the Total Environment, 2018, 651(2):3253-3268.
[9] SENDRA M, PEREIRO P, FIGUERAS A, et al.An integrative toxicogenomic analysis of plastic additives[J].Journal of Hazardous Materials, 2021, 409:124975.
[10] WIESINGER H, WANG Z Y, HELLWEG S.Deep dive into plastic monomers, additives, and processing aids[J].Environmental Science &Technology, 2021, 55(13):9339-9351.
[11] MUNCKE J, ANDERSSON A M, BACKHAUS T, et al.A vision for safer food contact materials:Public health concerns as drivers for improved testing[J].Environment International, 2023, 180:108161.
[12] BUMBUDSANPHAROKE N, KO S.Packaging technology for home meal replacement:Innovations and future prospective[J].Food Control, 2022, 132:108470.
[13] JIA Y Y, HU L L, LIU R F, et al.Innovations and challenges in the production of prepared dishes based on central kitchen engineering:A review and future perspectives[J].Innovative Food Science and Emerging Technologies, 2024, 91:103521.
[14] 林黛琴, 钟永红, 张涛, 等.液相色谱法分析复合膜袋中12种抗氧化剂迁移量[J].分析试验室, 2025, 44(4):494-501.LIN D Q, ZHONG Y H, ZHANG T, et al.The migration amount of 12 antioxidants in composite membrane bag analyzed by liquid chromatography[J].Chinese Journal of Analysis Laboratory, 2025, 44(4):494-501.
[15] 贺敏, 李锐, 周莹, 等.高效液相色谱法同时测定密胺制品中14种荧光增白剂残留量及迁移量[J].塑料包装, 2023, 33(6):21-25;85.HE M, LI R, ZHOU Y, et al.Simultaneous determination of 14 kinds of fluorescent whitening agents residues and migration in melamine products by high performance liquid chromatography[J].Plastics Packaging, 2023, 33(6):21-25;85.
[16] 蔡翔宇, 陈璐, 吴玉杰, 等.高效液相色谱-串联质谱法同时测定聚对苯二甲酸乙二醇酯/聚乙烯复合食品接触材料中16种抗氧化剂特定迁移量[J].食品安全质量检测学报, 2021, 12(15):5974-5982.CAI X Y, CHEN L, WU Y J, et al.Simultaneous determination of specific migration limits of 16 kinds of antioxidants in food contact polyethylene glycol terephthalate/polyethylene composite materials by high performance liquid chromatography-tandem mass spectrometry[J].Journal of Food Safety &Quality, 2021, 12(15):5974-5982.
[17] GUO R Y, LIANG X G, SU M F, et al.Occurrence, migration and health risks of fluorescent whitening agents and phthalates in bottled water[J].Journal of Hazardous Materials, 2024, 476:134631.
[18] ISCI G, DAGDEMIR E.Human health risk assessment of phthalate esters and antimony levels in beverages packaged in polyethylene terephthalate under different storage conditions[J].Journal of Food Composition and Analysis, 2024, 126:105922-.
[19] 乔海清, 王光英, 翟钰, 等.食品塑料包装材料中二元醇迁移量的测定[J].分析仪器, 2023(2):52-56.QIAO H Q, WANG G Y, ZHAI Y, et al.Determination of migration of dihydric alcohol in food plastic packaging materials[J].Analytical Instrumentation, 2023(2):52-56.
[20] 英琪, 把宁, 刘芳卫, 等.顶空-气相色谱法同时测定塑料类快递封装用品中15种有机溶剂残留量[J].塑料科技, 2024, 52(4):115-120.YING Q, BA N, LIU F W, et al.Simultaneous determination of 15 residual organic solvents in plastic express packages by headspace-gas chromatography[J].Plastics Science and Technology, 2024, 52(4):115-120.
[21] 王金鑫, 梁颖茵, 钟怀宁, 等.麦秸秆基塑料餐盒中2种合成酚类抗氧化剂及其降解产物的迁移[J].食品科学, 2024, 45(24):242-249.WANG J X, LIANG Y Y, ZHONG H N, et al.Migration studies of two synthetic phenolic antioxidants and their degradation products in wheat straw-based plastic lunch boxes[J].Food Science, 2024, 45(24):242-249.
[22] KIM H S, LEE K Y, JUNG J S, et al.Comparison of migration and cumulative risk assessment of antioxidants, antioxidant degradation products, and other non-intentionally added substances from plastic food contact materials[J].Food Packaging and Shelf Life, 2023, 35:101037.
[23] 朱霞建, 蒋力力, 尚煜豪, 等.超高效液相色谱-串联高分辨质谱法测定白酒接触材料中双酚A、双酚F和双酚S的迁移量[J].食品与发酵工业, 2024, 50(10):306-311.ZHU X J, JIANG L L, SHANG Y H, et al.Determination of the migration of bisphenol A, bisphenol F, and bisphenol S in Baijiu contacting materials by ultra performance liquid chromatography tandem high resolution mass spectrometry[J].Food and Fermentation Industries, 2024, 50(10):306-311.
[24] 蒙芳玲, 胡长鹰, 黎梓城, 等.液相色谱串联质谱法测定铝塑复合膜中芥酸酰胺和油酸酰胺[J].食品与发酵工业, 2020, 46(20):208-213.MENG F L, HU C Y, LI Z C, et al.Determination of erucamide and oleamide in aluminum-plastic compound film by liquid chromatography tandem mass spectrometry[J].Food and Fermentation Industries, 2020, 46(20):208-213.