四子王旗与西乌珠穆沁旗处于内蒙古中部地区,属于中温带干旱半干旱大陆性气候,拥有许多荒漠草原类型的天然牧场,是以蒙古族为主体民族,以畜牧业为基础经济的牧业旗县。牧区的牧民利用丰富的乳品资源,以牛乳、马乳和羊乳等为原料,通过传统发酵方式制成酸牛乳、酸马乳、酸羊乳等自然发酵乳,这些发酵乳中含有丰富的乳酸菌资源[1]。其中酸马乳更是蒙医和藏医中公认的医疗药引子[2],在蒙古族传统医学中还创立了“酸马奶疗法”[3]。酸马乳是一种以鲜马乳为原料,经自然发酵而成的酸性低酒精含量的乳饮品,现代微生物学研究表明,微生物在其中发挥着重要的作用。因此,对酸马乳中的乳酸菌进行分离鉴定具有重要的研究意义与应用价值。
乳酸菌是一类可发酵多种碳水化合物,主要终产物为乳酸的细菌总称,它们大部分是人类和动物肠道中的正常菌群,对人类有多种有益作用[4]。有研究表明,具有益生特性的乳酸菌可调节胃肠道微生物菌群,激活机体代谢反应,提高机体免疫力,预防和减轻各类疾病,如消化道疾病、流行性病毒感冒和过敏性疾病[5]。目前具有功能特性的乳酸菌已被广泛应用于制药、食品和畜牧行业[6-7]。
本研究从内蒙古四子王旗和西乌珠穆沁旗牧区采集了21份不同家畜的鲜乳及其自然发酵乳,采用纯培养技术对样品中的乳酸菌进行分离、鉴定,并分析不同样品中乳酸菌的菌群结构,以获取内蒙古牧区宝贵的乳酸菌菌种,了解不同乳源中乳酸菌的基本菌群结构。然后对酸马乳中的优势菌种马乳酒样乳杆菌进行优良菌株的筛选,以期为后续马乳酒样乳杆菌的开发利用提供优良的菌种资源。
1 材料与方法
1.1 材料与试剂
MRS肉汤培养基、M17肉汤培养基、强化梭菌培养基(reinforced clostridial medium,RCM)、营养琼脂(nutrient agar,NA),青岛海博生物技术有限公司;PCR试剂,上海派森诺生物科技有限公司;细菌基因组DNA提取试剂盒,天根生化科技有限公司;牛胆盐,德国Merck KGaA公司;胰蛋白酶、胃蛋白酶,北京康倍斯科技有限公司。
1.2 仪器与设备
SX-500型全自动高压灭菌锅,日本Tomy Digital Biology公司;ZHJH-C1214C超净工作台,上海智城仪器制造厂;CX33显微镜,日本OLYMPUS公司;5810R台式高速离心机、KDC-1044立式低速离心机,德国Eppendorf公司;PTC-200型PCR仪,美国Life Technologies公司;Bioscreen C全自动生长曲线仪,芬兰Oy Growth Curves Ab公司。
1.3 实验方法
1.3.1 样品采集
本研究的21份样品采集自内蒙古四子王旗与西乌珠穆沁旗牧区,由牧民采用传统的方法自然发酵而成,包括5份鲜牛乳、4份酸牛乳、2份鲜马乳、4份酸马乳、4份山羊乳、2份绵羊乳。样品采集时采用直接取样法。然后将采集的样品低温运输,迅速运回实验室立即进行菌株分离。
1.3.2 乳酸菌的分离鉴定
1.3.2.1 乳酸菌的分离纯化及保藏
采用10倍梯度稀释法对样品进行梯度稀释,选取稀释梯度为10-4、10-5、10-6的样品稀释液,分别移取200 μL于提前制备好的3种固体培养基(MRS、RCM、M17)上,涂匀后分别在厌氧和需氧两个条件下37 ℃恒温培养72 h。待菌落形成后,根据菌落形态特征与革兰氏染色镜检结果挑选不同的单菌落,采用平板划线法对单菌落进行分离纯化。将长好的单菌落接种到相应的液体培养基中,传代培养3代后离心收集菌体,1/3的菌体分装至1.5 mL离心管中用于后续菌株DNA的提取。剩下的菌体加入脱脂乳冻菌保护剂,分装至冻存管中,置于-80 ℃冷冻保藏[8]。
1.3.2.2 乳酸菌分子生物学鉴定
使用细菌基因组DNA提取试剂盒提取菌株的DNA,用PCR扩增仪进行16S rRNA基因扩增,PCR扩增体系及条件参考MO等[8]的方法。扩增产物送至上海美吉生物医药科技有限公司进行测序。得到完整的DNA序列后,在NCBI(https://www.ncbi.nlm.nih.gov/)中进行BLAST同源性比对,初步确定菌株的分类学地位。并在NCBI数据库下载对应菌种模式株的16S rRNA基因序列,使用MEGA 7.0软件构建系统发育树[9],进一步确定菌株分类学地位。
1.3.3 马乳酒样乳杆菌的初步筛选
将马乳酒样乳杆菌株活化后连续传代培养至第3代,按照2%的接种量分别接种于pH 3.0和6%(体积分数)乙醇的MRS液体培养基中,测定0 h的初始OD600nm值。37 ℃厌氧培养24 h后再次测定各菌株的终点OD600nm值,计算两个时间点OD600nm值的差值,每组3个平行,取平均值,差值(δOD)越大,耐受性越好。
1.3.4 乳酸菌耐受性分析
1.3.4.1 人工胃肠液耐受性
将初步筛选出的菌株接种于40 mL MRS液体培养基中,37 ℃厌氧培养,将传代培养至第3代的马乳酒样乳杆菌离心收集菌体细胞,加入5 mL PBS振荡混匀得到菌悬液。人工胃液(pH 3.0,3.0 g/L胃蛋白酶)与肠液(pH 8.0,1.0 g/L胰蛋白酶,18 g/L胆盐)的配制及试验方法采用LIU等[10]所用的方法进行。用平板计数法对菌悬液进行活菌计数,即为0 h原菌悬液的活菌数。取1 mL菌悬液于9 mL人工胃液(pH 3.0)中,37 ℃水浴3 h后测定活菌数,即为胃液3 h的活菌数。同时取1 mL胃液转接入9 mL人工肠液(pH 8.0)中,37 ℃水浴,分别测定菌株在肠液中水浴4 h与8 h(即第7 h与11 h)的活菌数。记录0、3、7、11 h的活菌数,随后计算菌株存活率[11]。
1.3.4.2 乙醇耐受性
配制乙醇体积分数为2%、4%、6%、8%、10%的MRS液体培养基。将初步筛选出的马乳酒样乳杆菌传代培养至第3代,按照2%的接种量接种于不同乙醇体积分数的MRS液体培养基中,在37 ℃培养条件下,用全自动生长曲线分析仪测定马乳酒样乳杆菌在不同乙醇体积分数下的生长曲线,每2 h测定一次OD600nm值[12]。每株菌3个平行。
1.3.5 抑菌能力
采用牛津杯法[13]测定马乳酒样乳杆菌对大肠埃希氏菌CICC 23657、肠沙门氏菌肠亚种肠炎血清型CICC 10982和金黄色葡萄球菌ATCC 12600的抑菌圈直径。马乳酒样乳杆菌用MRS液体培养基37 ℃厌氧培养12 h后,离心收集上清液。使用0.22 μm的滤膜过滤上清液获取无细胞上清液(cell-free supernatant,CFS)。使用平板计数检查调整指示菌的菌悬液浓度为106 CFU/mL左右。指示菌悬液以1%的接种量接种到NA培养基中,混合后量取20 mL倒入平板中。将牛津杯置于快要凝固的NA固体培养基平板中。待其完全凝固后,每个牛津杯中加入100 μL的CFS,CFS 4 ℃扩散10 h后37 ℃孵育18 h,测量抑菌圈的直径。每个致病菌进行3次重复实验。
1.4 数据统计分析
数据用“平均值±标准差”表示,利用Excel、SPSS、Origin等软件进行数据分析和图形绘制。
2 结果与分析
2.1 乳酸菌的分离鉴定结果
测序得到的菌株序列在NCBI网站上进行BLAST比对,初步确定411株菌株的分类学地位。使用MEGA7.0软件绘制分离株与其模式株的16S rRNA基因序列系统发育进化树,如图2所示。以此类推,将所有菌株在NCBI网站上进行BLAST序列比对分析,然后下载与分离株同源性最高的模式株构建系统发育树,分析得到所有菌株的分类学地位。
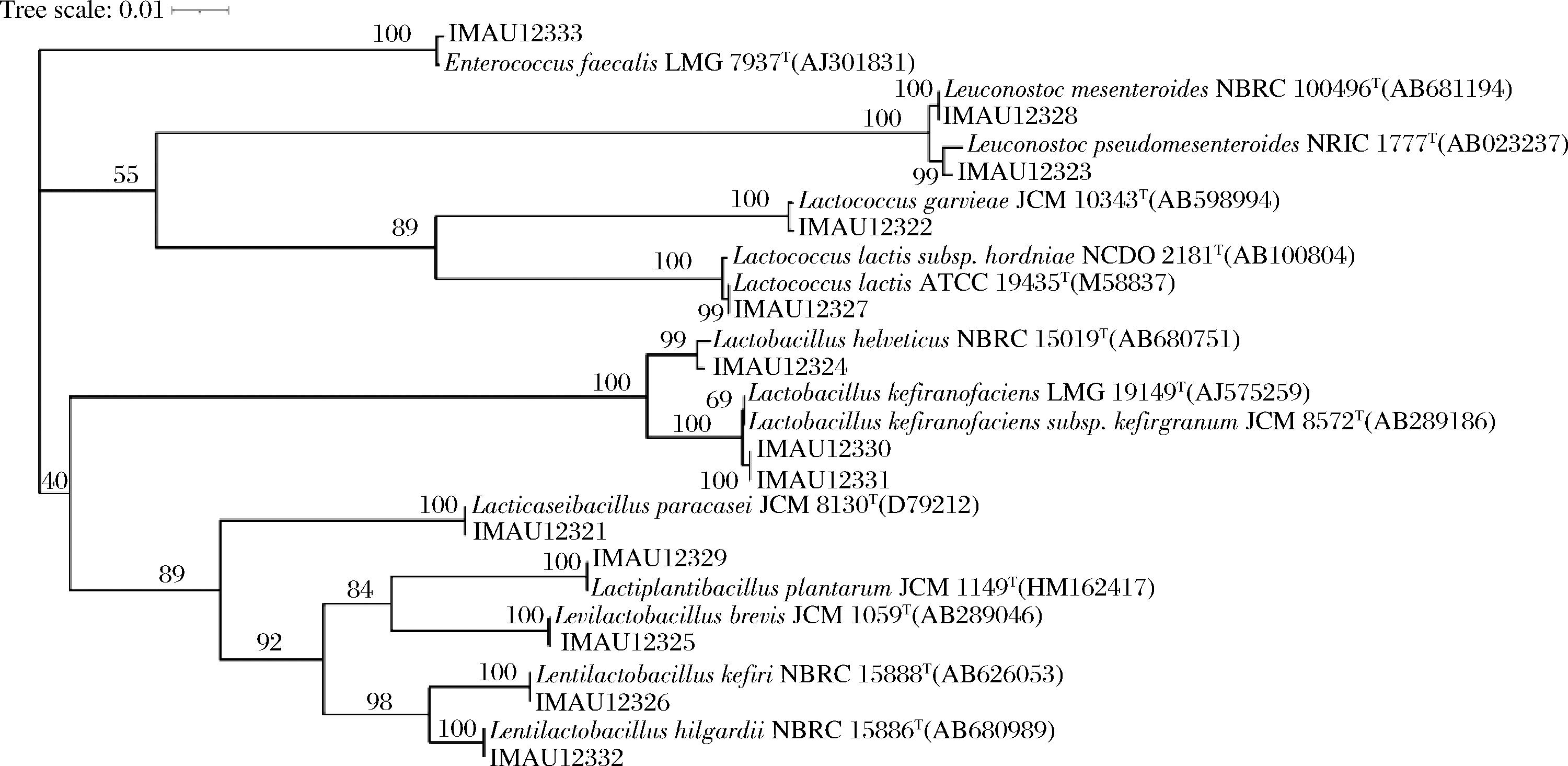
图1 部分乳酸菌分离株16S rRNA基因序列系统发育树
Fig.1 Phylogenetic tree of 16S rRNA gene sequence of partial lactic acid bacteria isolates
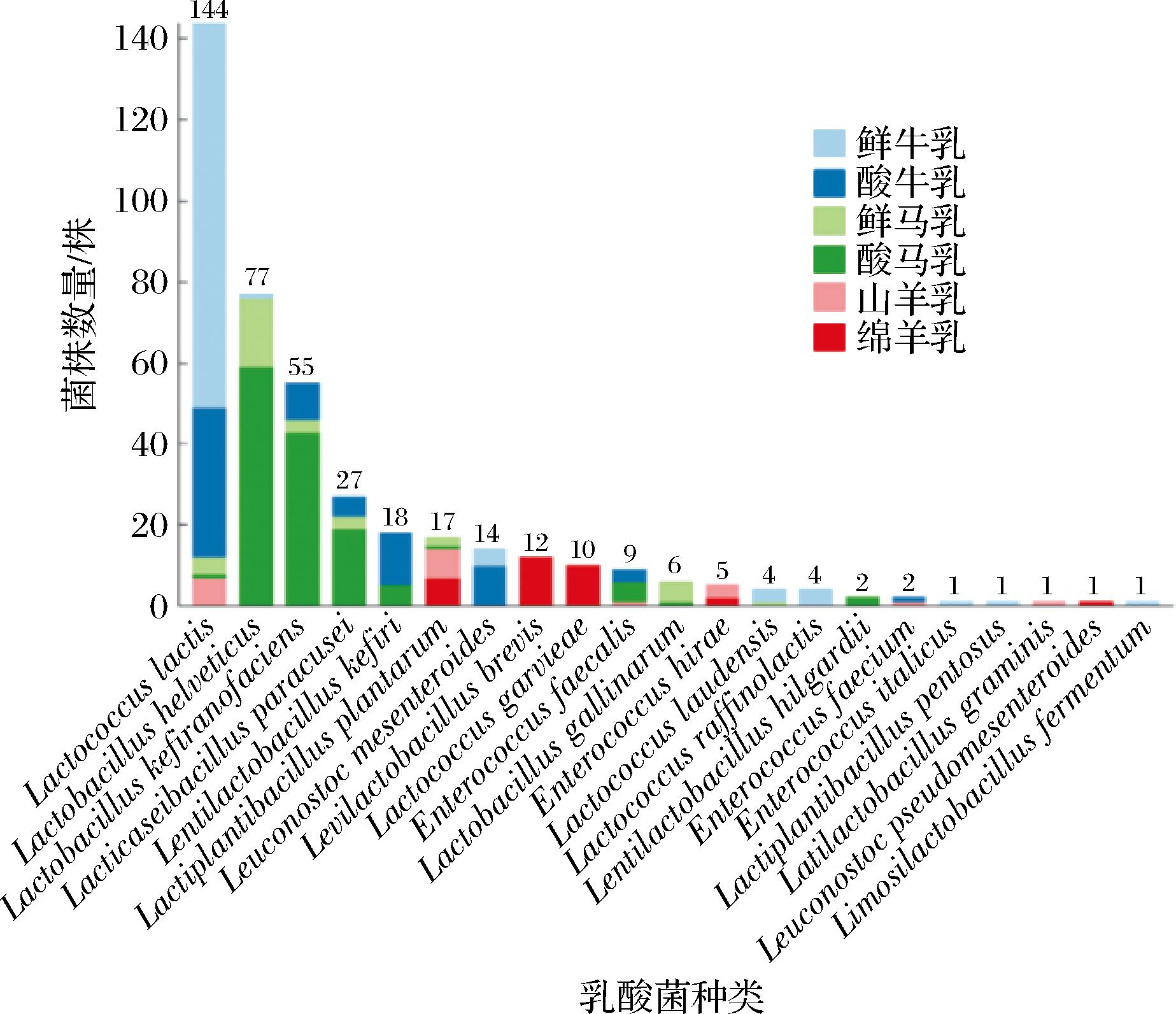
图2 乳酸菌种类与数量
Fig.2 Species and quantity of lactic acid bacteria
通过BLAST比对与系统发育树分析,得到内蒙古地区自然发酵乳中乳酸菌的分离鉴定结果。21份样品中一共分离得到411株乳酸菌,包括10个属,21个种[14]。10个属为乳球菌属(Lactococcus)、乳杆菌属(Lactobacillus)、乳植杆菌属(Lactiplantibacillus)、乳酪杆菌属(Lacticaseibacillus)、迟缓乳杆菌属(Lentilactobacillus)、促生乳杆菌属(Levilactobacillus)、广泛乳杆菌属(Latilactobacillus)、粘液乳杆菌属(Limosilactobacillus)、明串珠菌属(Leuconostoc)、肠球菌属(Enterococcus)。21个种如图2所示,其中乳酸乳球菌(Lactococcus lactis)占比最高,主要分离自牛乳,共144株,占总数的35.04%,其次为瑞士乳杆菌(Lactobacillus helveticus)和马乳酒样乳杆菌(Lactobacillus kefiranofaciens),主要分离自马乳,分别为77株与55株,各占总数的18.73%与13.38%。
2.2 不同乳源中乳酸菌优势菌群分析
统计不同样品中分离得到的乳酸菌种类及数量,分析不同菌种的相对含量,结果如图3所示。鲜牛乳共分离得到8种乳酸菌,优势乳酸菌为乳酸乳球菌(Lactococcus lactis),相对含量为86.36%;其次为棉籽糖乳球菌(Lactococcus raffinolactis)和肠膜明串珠菌(Leuconostoc mesenteroides),相对含量均为3.64%。酸牛乳共分离得到7种乳酸菌,优势乳酸菌为乳酸乳球菌,相对含量为47.44%,其次为高加索酸奶迟缓乳杆菌(Lentilactobacillus kefiri)和肠膜明串珠菌,相对含量分别为16.67%与12.82%。
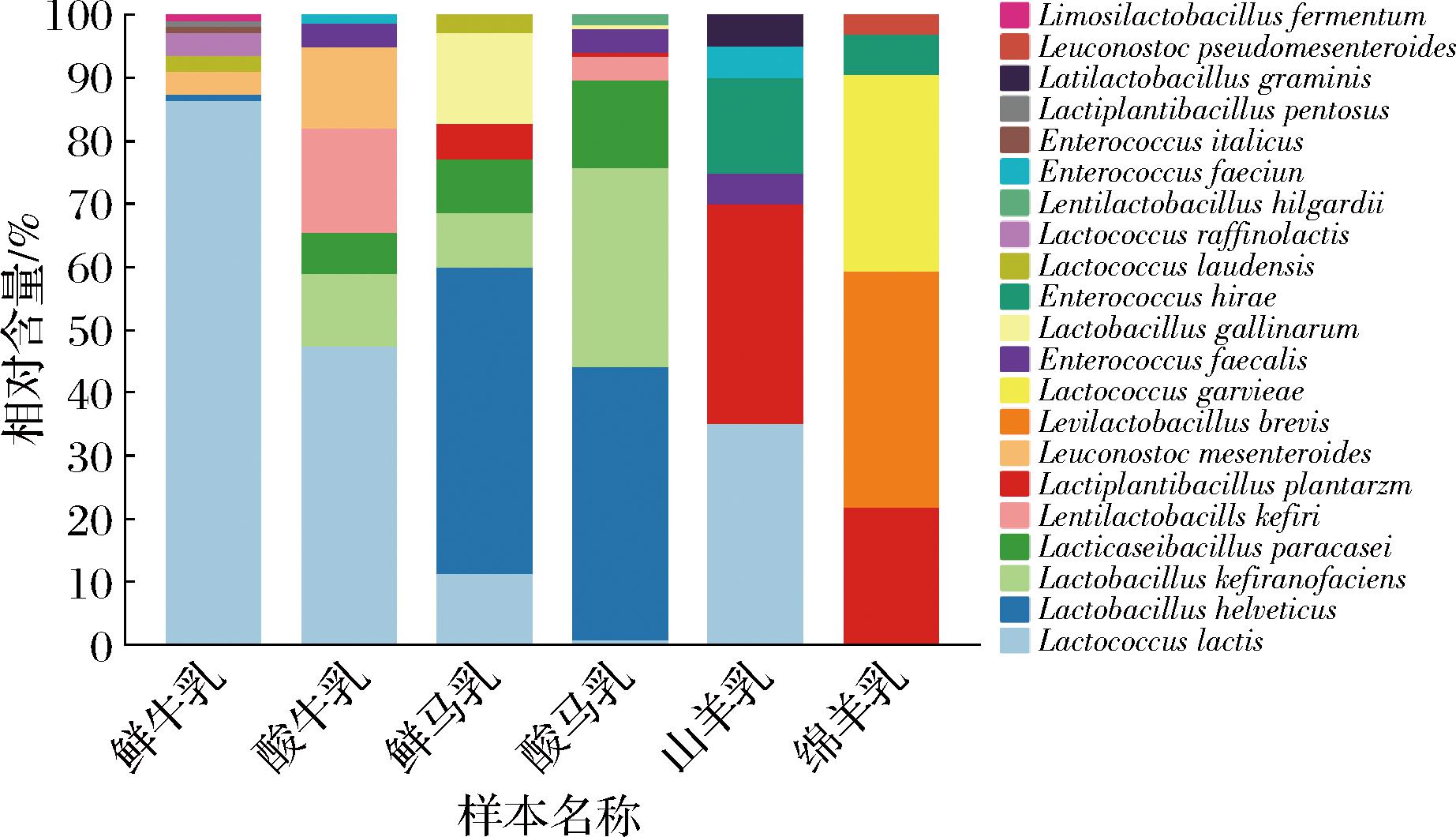
图3 不同乳源中乳酸菌分离株的相对含量
Fig.3 The relative content of lactic acid bacteria isolates in different milk sources
鲜马乳共分离得到7种乳酸菌,优势乳酸菌为瑞士乳杆菌(Lactobacillus helveticus)相对含量为48.57%,其次为鸡乳杆菌(Lactobacillus gallinarum)、乳酸乳球菌,相对含量分别为14.28%与11.42%。酸马乳共分离得到9种乳酸菌,优势乳酸菌为瑞士乳杆菌,相对含量为43.38%,其次为马乳酒样乳杆菌和类干酪乳酪杆菌,相对含量分别为31.62%与13.97%。
山羊乳共分离得到6种乳酸菌,优势乳酸菌为乳酸乳球菌与植物乳植杆菌,相对含量均为35.00%,其次为希拉肠球菌(Enterococcus hirae),相对含量为15.00%。绵羊乳共分离得到5种乳酸菌,优势菌群为短促生乳杆菌(Levilactobacillus brevis),相对含量为37.50%,其次为格氏乳球菌(Lactococcus garvieae)和植物乳植杆菌,相对含量分别为31.25%与21.88%。
菌群结构分析发现,不同乳源中乳酸菌的菌群结构存在一定的差异,山羊乳和绵羊乳的菌群结构比牛乳和马乳单一,菌群差异较大。如草广泛乳杆菌(Latilactobacillus graminis)只在山羊乳中分离得到,格氏乳球菌和短促生乳杆菌只在绵羊乳中分离得到。酸乳的乳杆菌含量高于鲜乳,而球菌在鲜乳中的含量更高,这可能是因为杆菌与球菌的细胞壁或细胞膜对酶活性的保护作用不同,导致杆菌耐酸,适合在酸奶中生长,而球菌不耐酸,在鲜奶中数量较多[15]。孙洁等[16]基于宏基因组测序分析发现苏尼特左旗和东乌珠穆沁旗的鲜牛乳中的优势菌种为乳酸乳球菌和肠膜明串珠菌。LIU等[17]研究锡林郭勒自然发酵酸牛奶中乳酸菌多样性,发现乳酸乳球菌是内蒙古中部酸牛奶中的优势菌种。夏亚男等[18]基于宏基因组分析内蒙古锡林郭勒酸马奶的微生物多样性发现瑞士乳杆菌和马乳酒样乳杆菌是酸马乳中常见的优势菌种。均与本研究结果一致。
酸马乳的菌群结构最丰富,一共分离得到了9种乳酸菌,马乳酒样乳杆菌是优势菌种之一。在2020年,中国卫生健康委员会将马乳酒样乳杆菌列入可用于食品的菌种名单,可作为一种新的食品原料添加到食品中。虽然它对生长条件的要求比较苛刻,分离纯化比较困难,但是具有许多的益生菌特性,如调节免疫代谢,调节肠道微生态,抗过敏特性和抗菌特性,这些有价值的益生特性使它成为生产有益健康的乳品(如酸马乳和开菲尔饮料)的最佳候选菌种之一[19]。于是本研究对分离得到的马乳酒样乳杆菌进行了优良菌株的筛选。
2.3 马乳酒样乳杆菌的初步筛选结果
进行初步筛选的菌株包括本次从酸马乳中分离的马乳酒样乳杆菌和内蒙古农业大学乳酸菌种质资源库中保藏的马乳酒样乳杆菌,共计93株,分离源均为酸马乳。由于酸马乳是一种酸性低酒精含量的乳饮品[3],从中分离的菌株对酸和乙醇具有一定的耐受性。从93株马乳酒样乳杆菌中初步筛选出4株分别在pH 3.0与6%(体积分数)乙醇环境下耐受性较好的菌株,如表1所示。其中马乳酒样乳杆菌IMAU12331在pH 3.0中的生长情况最好,OD600值最高。马乳酒样乳杆菌IMAU12208在6%(体积分数)乙醇环境下的生长情况最好,OD600值最高,达到了0.823。
表1 马乳酒样乳杆菌初筛结果
Table 1 The results of primary screening of
L. kefiranofaciens
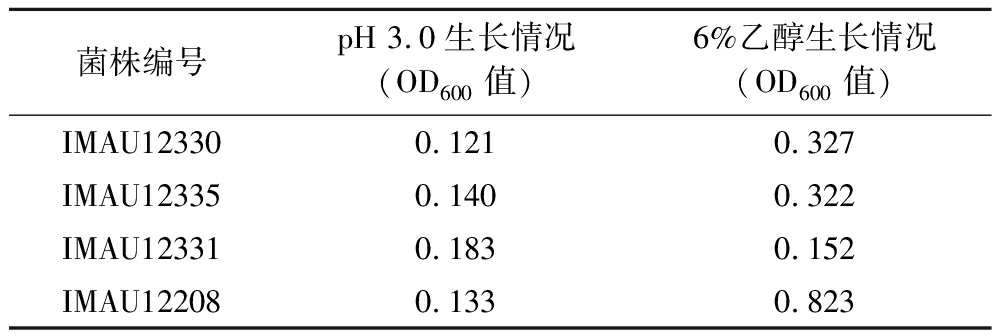
菌株编号pH 3.0生长情况(OD600值)6%乙醇生长情况(OD600值)IMAU123300.1210.327IMAU123350.1400.322IMAU123310.1830.152IMAU122080.1330.823
2.4 马乳酒样乳杆菌耐受性试验
2.4.1 人工胃肠液耐受性
胃肠液耐受性是益生菌筛选的关键环节,只有能耐受人体消化液的菌株才能到达相应部位发挥其功效成为益生菌[20]。干酪乳杆菌Zhang是从酸马乳中分离得到的一株益生菌,具有较好的胃肠液的耐受性[21]。用干酪乳杆菌Zhang作对照,初筛得到的4株马乳酒样乳杆菌对人工胃肠液的耐受性试验结果如表2所示。马乳酒样乳杆菌IMAU12331的人工胃肠液的耐受性较好,在胃液和肠液中的存活率均大于60%。马乳酒样乳杆菌IMAU12331胃液3 h的存活率为77.78%,肠液4 h和8 h的存活率分别为79.59%与64.28%。马乳酒样乳杆菌IMAU12208的人工胃肠液耐受性一般,胃液3 h的存活率为60.20%,肠液4 h与8 h的存活率分别57.20%与53.39%。马乳酒样乳杆菌IMAU12330和IMAU12335在人工肠液中的耐受性较好,但是在人工胃液中的耐受性较差,胃液3 h的存活率均小于50%。
表2 菌株对人工胃肠液的耐受性
Table 2 The tolerance of the strains to artificial gastroenteric fluid

菌株人工胃液(pH 3.0)人工肠液(pH 8.0)活菌计数/(CFU/mL)存活率/%活菌计数/(CFU/mL)存活率/%0 h3 h3 h/0 h7 h11 h7 h/3 h11 h/3 hIMAU12330(6.25±0.15)×109(1.46±0.05)×10923.36(1.29±0.05)×109(0.87±0.01)×10988.3659.59IMAU12335(8.85±0.45)×109(3.15±0.03)×10935.59(2.18±0.02)×109(2.08±0.23)×10969.2166.03IMAU12331(2.52±0.15)×109(1.96±0.41)×10977.78(1.56±0.04)×109(1.26±0.02)×10979.5964.28IMAU12208(1.96±0.02)×109(1.18±0.02)×10960.2(0.68±0.01)×109(0.63±0.01)×10957.253.39Zhang(3.60±0.05)×109(3.21±0.01)×10989.17(2.76±0.17)×109(2.58±0.12)×10985.9880.37
2.4.2 乙醇耐受性
用自动生长曲线仪测定了初筛得到的4株马乳酒样乳杆菌在不同体积分数乙醇环境(0%、2%、4%、6%、8%、10%)下的生长曲线,如图4所示。马乳酒样乳杆菌IMAU12208的乙醇耐受性最好,其次为IMAU12330与IMAU12335,IMAU12331略差。当乙醇体积分数为2%时,菌株生长状态几乎没有受到影响。马乳酒样乳杆菌IMAU12330与IMAU12208在乙醇体积分数为4%时还具有良好的生长状态,而IMAU12335与IMAU12331的生长状态略差。当乙醇体积分数为6%时,马乳酒样乳杆菌IMAU12208的生长状态略差,IMAU12330和IMAU12335较差,而IMAU12331几乎不生长。当乙醇体积分数大于6%时,除了马乳酒样乳杆菌IMAU12208,所有菌株几乎都不生长,且当乙醇体积分数达到8%时,马乳酒样乳杆菌IMAU12208仍然具有一定的生长能力。

a-IMAU12330;b-IMAU12335;c-IMAU12331;d-IMAU12208
图4 马乳酒样乳杆菌在不同体积分数乙醇环境下的生长曲线
Fig.4 The growth curves of L. kefiranofaciens in ethanol environment with different volume fractions
乙醇能够改变细胞膜通透性、造成细胞内物质流失、影响酶活性等,在菌体生长的过程中,乙醇含量过高会对菌体的生理活性、新陈代谢等方面造成不同程度的影响[22]。朱敏等[23]研究面包乳杆菌(Lactobacillus crustorum D2-5)和植物乳杆菌(Lactobacillus plantarum D5-5)发现,当乙醇体积分数达到8%时,菌株的存活率明显下降,且菌体的生长受到严重抑制。金丹等[24]发现,当乙醇体积分数为9%时,会导致部分菌株死亡,达到14%时,菌株几乎不能存活。周羽等[25]从天然果蔬发酵液中筛选出2株能耐受5%(体积分数)乙醇的副干酪乳杆菌,并以此为菌种进行果蔬发酵,发现这2株副干酪乳杆菌适用于食用酵素的发酵。陈曼曼等[26]对传统发酵蔬菜中耐受乙醇型乳酸菌的分离与筛选研究进行总结,发现乙醇耐受性优良的乳酸菌对乳酸菌发酵传统蔬菜的产业化生产具有重要意义。目前对酸马乳中乳酸菌的乙醇耐受性研究较少,本研究筛选出的马乳酒样乳杆菌IMAU12208具有较高乙醇耐受性,可为马乳酒样乳杆菌的开发利用提供参考。
2.5 抑菌能力
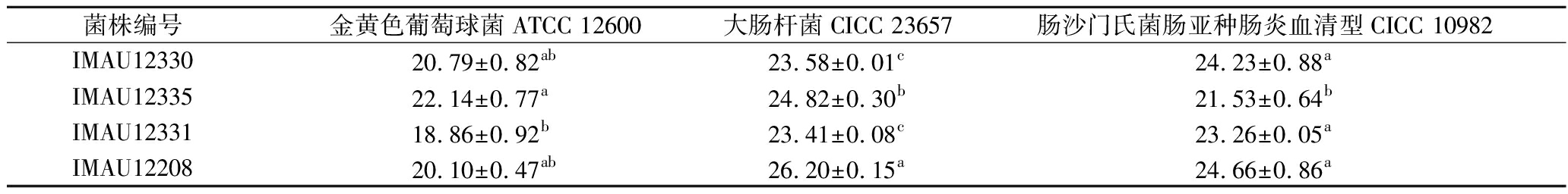
测定了马乳酒样乳杆菌对3种常见食源性致病菌(金黄色葡萄球菌ATCC 12600、大肠杆菌CICC 23657、肠沙门氏菌肠亚种肠炎血清型CICC 10982)的抑菌能力,对不同致病菌的抑菌圈直径如表3所示。马乳酒样乳杆菌IMAU12335对金黄色葡萄球菌ATCC 12600的抑菌能力最强,抑菌直径显著高于IMAU12330、IMAU12331和IMAU12208(P<0.05),直径为(22.14±0.77) mm。马乳酒样乳杆菌IMAU12208对大肠杆菌CICC 23657的抑菌能力最强,抑菌直径显著高于IMAU12330、IMAU12335和IMAU12331(P<0.05),直径为(26.20±0.15) mm。马乳酒样乳杆菌IMAU12330、IMAU12331和IMAU12208对肠沙门氏菌肠亚种肠炎血清型CICC 10982均具有良好的抑菌能力,抑菌直径显著高于IMAU12335(P<0.05),直径分别为(24.23±0.88)、(23.26±0.05)、(24.66±0.86) mm。这4株马乳酒样乳杆菌对上述3种常见致病菌均具有一定的抗菌活性。抗菌活性是乳酸菌重要的益生特性之一,具有抗菌活性的乳酸菌可以作为天然防腐剂确保食品安全,还可以预防胃肠道感染,是益生菌筛选的主要指标之一[27]。
表3 马乳酒样乳杆菌的抑菌直径
Table 3 The bacteriostatic diameter of L. kefiranofaciens
菌株编号金黄色葡萄球菌ATCC 12600大肠杆菌CICC 23657肠沙门氏菌肠亚种肠炎血清型CICC 10982IMAU1233020.79±0.82ab23.58±0.01c24.23±0.88aIMAU1233522.14±0.77a24.82±0.30b21.53±0.64bIMAU1233118.86±0.92b23.41±0.08c23.26±0.05aIMAU1220820.10±0.47ab26.20±0.15a24.66±0.86a
注:同一列不同小写字母表示显著差异(P<0.05)。
3 结论
采用纯培养技术从内蒙古牧区21份鲜乳及其发酵乳中分离得到了411株乳酸菌,包括10个属,21个种。其中乳酸乳球菌的分离率最高,其次为瑞士乳杆菌和马乳酒样乳杆菌。优势菌群分析发现不同乳源中乳酸菌的菌群结构差异较大,山羊乳和绵羊乳的菌群丰富度比牛乳和马乳单一,酸马乳的菌群结构最丰富,优势乳酸菌为瑞士乳杆菌和马乳酒样乳杆菌。从93株马乳酒样乳杆菌中筛选出了2株特性优良的菌株,分别为马乳酒样乳杆菌IMAU12331和IMAU12208。马乳酒样乳杆菌IMAU12331胃肠液的耐受性较好,在乙醇体积分数为4%时还具有良好的生长状态,具有较好的抑菌能力。马乳酒样乳杆菌IMAU12208对胃肠液的耐受一般,但乙醇耐受性较好,乙醇体积分数为8%时还具有一定的生长能力,且具有良好的抑菌能力。马乳酒样乳杆菌IMAU12331和IMAU12208具有较高的潜在应用价值,可为马乳酒样乳杆菌的开发利用提供特性优良的候选菌株。
[1] ZHANG H P, CHEN X, DAN T, et al.Traditional Chinese fermented dairy foods[M].Lactic Acid Bacteria.Dordrecht:Springer Netherlands, 2014:493-535.
[2] AFZAAL M, SAEED F, ANJUM F, et al.Nutritional and ethnomedicinal scenario of koumiss:A concurrent review[J].Food Science &Nutrition, 2021, 9(11):6421-6428.
[3] 孟和毕力格, 乌日娜, 王立平, 等.不同地区酸马奶中乳杆菌的分离及其生物学特性的研究[J].中国乳品工业, 2004, 32(11):6-11.
MENGHE B L G, WU R N, WANG L P, et al.Isolation and identification of Lactobacillus from koumiss collected in Inner Mongolia and People’s Republic of Mongolia[J].China Dairy Industry, 2004, 32(11):6-11.
[4] MASOOD M I, QADIR M I, SHIRAZI J H, et al.Beneficial effects of lactic acid bacteria on human beings[J].Critical Reviews in Microbiology, 2011, 37(1):91-98.
[5] REN C C, FAAS M M, DE VOS P.Disease managing capacities and mechanisms of host effects of lactic acid bacteria[J].Critical Reviews in Food Science and Nutrition, 2021, 61(8):1365-1393.
[6] BAO Y, ZHANG Y C, ZHANG Y, et al.Screening of potential probiotic properties of Lactobacillus fermentum isolated from traditional dairy products[J].Food Control, 2010, 21(5):695-701.
[7] SHAZADI K, ARSHAD N.Evaluation of inhibitory and probiotic properties of lactic acid bacteria isolated from vaginal microflora[J].Folia Microbiologica, 2022, 67(3):427-445.
[8] MO L X, JIN H, PAN L, et al.Biodiversity of lactic acid bacteria isolated from fermented milk products in Xinjiang, China[J].Food Biotechnology, 2019, 33(2):174-192.
[9] KUMAR S, STECHER G, TAMURA K.MEGA7:Molecular evolutionary genetics analysis version 7.0 for bigger datasets[J].Molecular Biology and Evolution, 2016, 33(7):1870-1874.
[10] LIU W J, CHEN M X, DUO L N, et al.Characterization of potentially probiotic lactic acid bacteria and bifidobacteria isolated from human colostrum[J].Journal of Dairy Science, 2020, 103(5):4013-4025.
[11] DA SILVA FERNANDES M, SANCHES LIMA F, RODRIGUES D, et al.Evaluation of the isoflavone and total phenolic contents of kefir-fermented soymilk storage and after the in vitro digestive system simulation[J].Food Chemistry, 2017, 229:373-380.
[12] WANG J L, LU C S, XU Q, et al.Comparative genomics analysis provides new insights into high ethanol tolerance of Lactiplantibacillus pentosus LTJ12, a novel strain isolated from Chinese Baijiu[J].Foods, 2022, 12(1):35.
[13] WANG X, WANG W D, LV H X, et al.Probiotic potential and wide-spectrum antimicrobial activity of lactic acid bacteria isolated from infant feces[J].Probiotics and Antimicrobial Proteins, 2021, 13(1):90-101.
[14] ZHENG J S, WITTOUCK S, SALVETTI E, et al.A taxonomic note on the genus Lactobacillus:Description of 23 novel Genera, emended description of the genus Lactobacillus beijerinck 1901, and union of Lactobacillaceae and Leuconostocaceae[J].International Journal of Systematic and Evolutionary Microbiology, 2020, 70(4):2782-2858.
[15] 张冬蕾, 任艳, 德亮亮, 等.内蒙古鄂尔多斯地区羊鲜乳与酸乳中乳酸菌的分离鉴定[J].中国乳品工业, 2015, 43(7):30-34.
ZHANG D L, REN Y, DE L L, et al.Isolation and identification of Lactic acid bacteria from ewe’s milk and yoghurt from Ordos in Inner Mongolia[J].China Dairy Industry, 2015, 43(7):30-34.
[16] 孙洁, 苏茜, 杜萍, 等.锡林郭勒鲜牛乳中乳酸菌分离鉴定及微生物多样性分析[J].食品科学, 2023, 44(18):175-182.
SUN J, SU Q, DU P, et al.Isolation and identification of lactic acid bacteria and microbial diversity in fresh cow milk from Xilin gol[J].Food Science, 2023, 44(18):175-182.
[17] LIU W J, BAO Q H, JIRIMUTU, et al.Isolation and identification of lactic acid bacteria from Tarag in Eastern Inner Mongolia of China by 16S rRNA sequences and DGGE analysis[J].Microbiological Research, 2012, 167(2):110-115.
[18] 夏亚男, 刘皓, 双全.基于宏基因组分析酸马奶的微生物多样性及功能基因[J].中国食品学报, 2022, 22(2):301-309.
XIA Y N, LIU H, SHUANG Q.Analysis on microbiological diversity and functional genes of koumiss based on metagenomic technology[J].Journal of Chinese Institute of Food Science and Technology, 2022, 22(2):301-309.
[19] GEORGALAKI M, ZOUMPOPOULOU G, ANASTASIOU R, et al.Lactobacillus kefiranofaciens:From isolation and taxonomy to probiotic properties and applications[J].Microorganisms, 2021, 9(10):2158.
[20] GU Q Z, YIN Y, YAN X J, et al.Encapsulation of multiple probiotics, synbiotics, or nutrabiotics for improved health effects:A review[J].Advances in Colloid and Interface Science, 2022, 309:102781.
[21] WU R, SUN Z, WU J, et al.Effect of bile salts stress on protein synthesis of Lactobacillus casei Zhang revealed by 2-dimensional gel electrophoresis[J].Journal of Dairy Science, 2010, 93(8):3858-3868.
[22] G-ALEGR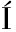 A E, L
A E, L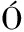 PEZ I, RUIZ J I, et al.High tolerance of wild Lactobacillus plan and Oenococcus oeni strains to lyophilisation and stress environmental conditions of acid pH and ethanol[J].FEMS Microbiology Letters, 2004, 230(1):53-61.
PEZ I, RUIZ J I, et al.High tolerance of wild Lactobacillus plan and Oenococcus oeni strains to lyophilisation and stress environmental conditions of acid pH and ethanol[J].FEMS Microbiology Letters, 2004, 230(1):53-61.
[23] 朱敏, 李宝坤, 李开雄, 等.乙醇胁迫对乳酸杆菌关键酶活力的影响[J].食品与发酵工业, 2015, 41(1):40-45.
ZHU M, LI B K, LI K X, et al.The effect of ethanol stress on the key enzymes of Lactobacillus[J].Food and Fermentation Industries, 2015, 41(1):40-45.
[24] 金丹, 蒋彩虹, 蒋艾廷, 等.塔城地区酸马奶中耐乙醇乳酸菌的筛选与鉴定[J].中国酿造, 2017, 36(3):44-48.
JIN D, JIANG C H, JIANG A T, et al.Screening and identification of ethanol tolerance lactic acid bacteria from Tacheng kumiss[J].China Brewing, 2017, 36(3):44-48.
[25] 周羽, 刘艳琼, 陈启明, 等.耐乙醇乳酸菌的分离和培养[J].食品工业, 2018, 39(12):114-119.
ZHOU Y, LIU Y Q, CHEN Q M, et al.Isolation and culture of ethanol resistant Lactobacillus[J].The Food Industry, 2018, 39(12):114-119.
[26] 陈曼曼, 吴兴壮.传统发酵蔬菜中耐乙醇型乳酸菌的研究进展[J].中国酿造, 2023, 42(1):9-14.
CHEN M M, WU X Z.Research progress of ethanol-tolerant lactic acid bacteria in traditional fermented vegetable[J].China Brewing, 2023, 42(1):9-14.
[27] CAMPANA R, VAN HEMERT S, BAFFONE W.Strain-specific probiotic properties of lactic acid bacteria and their interference with human intestinal pathogens invasion[J].Gut Pathogens, 2017, 9:12.