N-乙酰神经氨酸(N-acetyl-neuraminic acid,Neu5Ac),是一种带有N-乙酰氨基的九碳单糖。Neu5Ac通常融合在细胞膜上糖脂和糖蛋白的非还原末端,参与细胞识别事件以及各种生物过程的调节,包括病毒入侵、受精、炎症、肿瘤发生、细胞分化和细胞黏附等[1-3]。Neu5Ac被认为是开发抗流感药物扎那米韦的潜在前体,可用于治疗和预防禽流感病毒H5N1以及A型和B型流感[4-5]。此外,它被报道可用于治疗心脏病[6]和修饰纳米载体用于药物输送[7-8]。欧盟、美国和中国食品药品监督管理局已经批准Neu5Ac作为一种新的营养补充剂。Neu5Ac在营养食品和制药行业关注度越来越高,迫切需要通过经济高效的方法大规模生产。Neu5Ac的传统生产方法是从鸡蛋、牛奶、食用燕窝和酪蛋白等天然物质中提取,步骤繁多,提取收率低。后来开发的多种生产方法具有各自的局限性,如化学法分离过程复杂、酶法合成成本高、全细胞催化法操作繁琐等,不利于Neu5Ac的大规模工业化生产。利用代谢工程手段建立稳定、高效的Neu5Ac发酵生产体系,是进一步拓展Neu5Ac市场的需求。
目前,Neu5Ac已在大肠杆菌、枯草芽孢杆菌中实现异源从头合成。Neu5Ac的合成以N-乙酰甘露糖胺(N-acetyl-mannosamine,ManNAc)与磷酸烯醇式丙酮酸(phosphoenolpyruvic acid,PEP)为前体物。在中心碳代谢途径中,果糖-6-磷酸节点对于代谢流的分配具有非常重要的作用。一方面,前体物ManNAc的合成需要首先从果糖-6-磷酸合成N-乙酰氨基葡萄糖(N-acetyl-glucosamine,GlcNAc);另一方面,前体物PEP需要从果糖-6-磷酸进一步进行糖酵解过程获得。因此,碳源的代谢效率以及在果糖-6-磷酸节点处的碳代谢流分配,直接影响Neu5Ac合成中2个前体物的供应,进而影响Neu5Ac合成效率。
在微生物中,不同碳源具有不同的代谢速率与代谢特征,比如,葡萄糖作为大肠杆菌的最适碳源,具有代谢速度快,能够快速提供能量等特征。与葡萄糖相比,甘油进入糖酵解和三羧酸循环的途径更短,更有利于PEP的积累;甘油发酵可以获得额外的ATP,具有生物能优势。甘油作为一种高还原度碳源,可作为燃料和还原化学品发酵的碳源,并已在芳香族氨基酸的生产中广泛应用[9]。此外,有研究表明,以甘油作为发酵碳源,大肠杆菌可以减少乙酸与乳酸的积累[10]。因此,本研究分别探究了葡萄糖、甘油,以及葡萄糖甘油混合碳源,对Neu5Ac合成的影响。通过敲除糖酵解途径中的6-磷酸果糖激酶编码基因pfkA、引入甘油激酶突变glpK[G304S],进一步调控碳源利用速度。最终,菌株NEU5AC-2以单一葡萄糖为碳源在5 L发酵罐分批补料发酵38 h产生23.8 g/L Neu5Ac,获得了较高的发酵生产水平,具有较强的工业应用潜力。
1 材料与方法
1.1 实验材料
1.1.1 菌株与质粒
本研究所用的菌株与质粒信息如表1所示。
表1 本研究所用菌株与质粒
Table 1 Strains and plasmids used in this study

菌株/质粒特征来源菌株Escherichia coli DH5αCloning host本实验室NEAE.coli W3110,ΔlacIZ::PxylF-T7RNAP,Pmlc::Pmlc[M],ΔnagBAC,ΔmanXYZ,ΔnagE::PT7-Sc-gnal,yjiV::PT7-glmS,ycjV::PT7- glmS,gapC::PT7-bAGE,yeeP::PT7-neuB,mbhA::PT7-neuB,ΔptsG,rpH::Ptrc-glf,ycgh::Ptrc-glk,ΔpykA本实验室NEU5AC-1NEA,glpK::glpK[G304S]本研究NEU5AC-2NEU5AC-1,ΔpfkA本研究质粒pREDCas9SpeR,Cas9 and λ-Red recombinase expression vector天津大学pGRBAmpR,gRNA expression vector天津大学
1.1.2 试剂
100 mg/L氨苄青霉素、50 mg/L奇霉素,北京索莱宝科技有限公司;限制性内切酶、STAR HS DNA聚合酶、T4 DNA连接酶,日本TaKaRa公司;培养基所需原料,国药集团化学试剂有限公司;Neu5Ac、ManNAc,德国Sigma-Aldrich公司。
1.1.3 培养基
LB培养基(g/L):蛋白胨10、酵母粉5、NaCl 10,固体培养基则添加20 g/L的琼脂粉。
2×YT培养基(g/L):蛋白胨16、酵母粉10、NaCl 5。
固体斜面培养基(g/L):蛋白胨10、酵母粉5、NaCl 10、牛肉膏10、蔗糖1,溶解均匀后加入20 g/L琼脂粉并煮沸。
种子培养基(g/L):葡萄糖20、酵母粉3、KH2PO4 2、柠檬酸2、MgSO4·7H2O 1、(NH4)2SO4 2、FeSO4·7H2O 0.002 8、MnSO4·H2O 0.001 2、维生素B1 0.000 5、维生素H 0.000 1,微量元素混合液1 mL/L,消泡剂1滴,pH 7.0~7.2。
发酵培养基(g/L):碳源(葡萄糖、甘油,或葡萄糖/甘油混合)20、酵母粉3、KH2PO4 6.67、(NH4)2SO4 4、柠檬酸3.55、MgSO4·7H2O 2.5、NaCl 1、FeSO4·7H2O 0.01、CaCl2·2H2O 0.025、MnSO4·H2O 0.001 2、维生素B1 0.000 5、维生素H 0.000 1,微量元素混合液1 mL/L,消泡剂1滴,pH 7.0~7.2。
1.2 实验方法
1.2.1 基因编辑方法
本文采用CRISPR-Cas9基因编辑方法[11],对菌株E.coli基因组进行编辑,以获得相应的基因组修饰菌株。操作体系由目标重组DNA片段、提供gRNA片段的pGRB质粒和提供Cas9蛋白及RED重组酶的pREDCas9温敏性质粒构成。
首先,根据目的基因序列,合理设计引物(本研究所涉及引物信息如表2所示),通过PCR扩增获得目的基因片段。然后,通过CRISPR/Cas9在线工具(http://www.rgenome.net/cas-designer/)选择待整合/敲除位点附近的PAM序列(5′-NGG-3′)及其上游20 bp的基因序列,并通过引物合成将其引入单链DNA中,合成的单链通过PCR退火形成双链片段。将双链片段与线性化pGRB载体用同源重组的方法连接,化转至大肠杆菌DH5α感受态中,筛选阳性克隆并提取质粒。
表2 本研究所用引物
Table 2 Primers used in this study
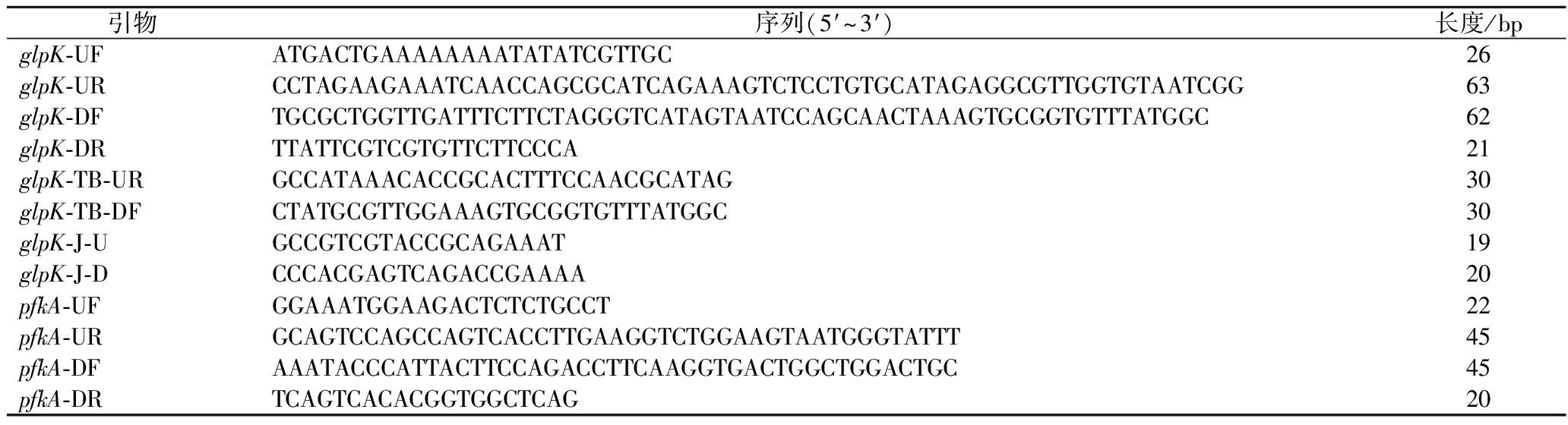
引物序列(5′~3′)长度/bpglpK-UFATGACTGAAAAAAAATATATCGTTGC26glpK-URCCTAGAAGAAATCAACCAGCGCATCAGAAAGTCTCCTGTGCATAGAGGCGTTGGTGTAATCGG63glpK-DFTGCGCTGGTTGATTTCTTCTAGGGTCATAGTAATCCAGCAACTAAAGTGCGGTGTTTATGGC62glpK-DRTTATTCGTCGTGTTCTTCCCA21glpK-TB-URGCCATAAACACCGCACTTTCCAACGCATAG30glpK-TB-DFCTATGCGTTGGAAAGTGCGGTGTTTATGGC30glpK-J-UGCCGTCGTACCGCAGAAAT19glpK-J-DCCCACGAGTCAGACCGAAAA20pfkA-UFGGAAATGGAAGACTCTCTGCCT22pfkA-URGCAGTCCAGCCAGTCACCTTGAAGGTCTGGAAGTAATGGGTATTT45pfkA-DFAAATACCCATTACTTCCAGACCTTCAAGGTGACTGGCTGGACTGC45pfkA-DRTCAGTCACACGGTGGCTCAG20
将pREDCas9质粒转化至待改造的E.coli感受态细胞中,然后使用电击转化仪将上述构建好的重组pGRB质粒和目的基因DNA片段同时电转化至含有pREDCas9质粒的待改造菌株感受态中,电转复苏完成后涂布于带有氨苄青霉素和奇霉素的固体平板培养皿中,32 ℃培养,筛选阳性克隆。将筛选到的阳性菌株在含2 g/L阿拉伯糖的LB培养基中培养,诱导pREDCas9中的pGRB消除系统,对pGRB质粒进行消除,在42 ℃过夜培养,消除pREDCas9质粒,即获得相应改造的无质粒工程菌株。
1.2.2 摇瓶发酵
首先在5 mL LB液体培养基中培养,其次利用固体斜面培养基传代2次,完成菌株活化。用接种环刮取菌体,接种于含30 mL种子培养基的500 mL圆底三角瓶中,在摇床中37 ℃、220 r/min培养8~10 h,测定OD600值。将培养好的种子培养液按照10%的接种量接种于含30 mL发酵培养基的500 mL挡板三角瓶中,在37 ℃、220 r/min条件下培养至发酵结束。发酵培养基中添加终质量浓度为8 mg/L的苯酚红作为酸碱指示剂,在发酵过程中,根据培养基颜色变化,及时添加氨水调整pH值至7.0左右,并根据耗糖情况及时补充1 mL 60 g/100 mL的碳源。
1.2.3 发酵罐分批补料发酵
菌株活化后,用无菌水将茄形瓶中的菌落冲洗下来制成菌悬液,全部接种到装有3 L种子培养基的5 L发酵罐中进行菌体扩大培养,发酵过程中控制pH 7.0左右,温度恒定在37 ℃,溶氧保持在25%~35%,至种子OD600值达到10~12时,按15%的接种量接入装有3 L发酵培养基的5 L发酵罐中进行发酵培养,发酵过程中维持pH 7.0左右,温度保持在37 ℃,溶氧控制在25%~35%。当罐中的葡萄糖耗尽时,开始以一定速率流加质量浓度80 g/100 mL的葡萄糖溶液,维持罐中葡萄糖质量浓度在0.1~1 g/L。
1.2.4 相关参数测定
本研究采用高效液相色谱法对发酵液中Neu5Ac、ManNAc、葡萄糖、甘油等组分进行测定分析。所用色谱柱为Aminex® HPX-87H色谱柱(7.8 mm×300 mm);检测器为RID-20A折光率检测器;流动相为5 mmol/L硫酸溶液,柱温设定37 ℃,流速设定0.5 mL/min。细胞干重(dry cell weight,DCW)的测定方法如下:取样并经合适比例稀释后用分光光度计测定发酵液的OD600值,按照公式(1)计算DCW:
DCW/(g/L)=0.382×OD600×稀释倍数
(1)
2 结果与分析
2.1 不同碳源对NEA菌株生长与Neu5Ac合成的影响
在Neu5Ac的合成中,N-乙酰葡萄糖胺2-差向异构酶可以催化GlcNAc异构化为ManNAc,然后以其为直接前体,PEP为共底物,通过Neu5Ac合成酶转化为Neu5Ac。在实验室前期的研究中,以一株GlcNAc生产菌GLA为底盘,引入来源于集胞藻Anabaena sp.CH1的N-乙酰葡萄糖胺2-差向异构酶编码基因bAGE,以及来源于脑膜炎奈瑟菌Neisseria meningitidis的Neu5Ac合成酶编码基因neuB,并利用T7启动子对两者进行强表达,实现了Neu5Ac的异源合成[12]。为了增强前体物PEP的供应,张颖[13]进一步敲除了ptsG基因,并引入来源于运动发酵单胞菌的葡萄糖易化转运蛋白编码基因glf,强化了葡萄糖激酶编码基因glk;在此基础上,通过敲除丙酮酸激酶编码基因pykA,进一步增强PEP供应,得到菌株NEA,有效增产Neu5Ac,该菌株摇瓶发酵36 h,产量12 g/L。前体物PEP的供应强化虽然提升了菌株NEA的Neu5Ac产量,然而,在发酵过程中,菌株NEA特别容易积累乙酸,导致细胞生长在发酵后期受到严重影响,成为限制Neu5Ac产量进一步提升的瓶颈。乙酸的过量积累说明中心碳代谢过程出现了失衡,上游糖酵解过程与下游TCA循环不匹配。虽然阻断ackA、pta、poxB等乙酸合成基因的表达,可以部分减少乙酸积累,但往往对细胞代谢产生不利影响,并且由于有未知途径仍然可以产生乙酸,单纯靠“阻断”的方式,并不能从根本上解决乙酸积累问题,而是需要进行碳代谢的平衡。中心碳代谢过程不仅对于细胞生长有重要作用,而且为产物合成过程提供直接前体,特别是对于具有2种前体物的Neu5Ac合成过程,碳代谢尤为重要。基于以上背景,本研究尝试从碳源代谢调控角度优化碳代谢过程,减少乙酸积累,提升Neu5Ac合成效率。
根据文献报道,相比于葡萄糖碳源,甘油的利用有利于减少大肠杆菌中乙酸的积累[14]。本研究分别以葡萄糖和甘油作为单一碳源对NEA进行摇瓶发酵,并对细胞生长与Neu5Ac产量进行了测定,摇瓶发酵32 h的结果如图1所示。由图1-a和图1-b中结果看出,在甘油唯一碳源的培养基中,菌株NEA的生物量明显高于葡萄糖单一碳源培养基,摇瓶发酵32 h时Neu5Ac的产量达到16.75 g/L,比葡萄糖培养基提高了38.54%;乙酸积累11.95 g/L,降低了55.82%,最终产生的前体物ManNAc也略高于葡萄糖培养基。可见,不同碳源代谢速率不同,导致前体物PEP与ManNAc的供应发生改变。另外在发酵过程中发现,不论在生长前期还是对数生长期,相同浓度的碳源补加,葡萄糖消耗速率始终大于甘油(图1-c)。甘油作为碳源提供生长的同时,需要进行糖异生补充上游果糖-6-磷酸,进而获得Neu5Ac的前体物ManNAc,相比于葡萄糖供应ManNAc的途径更长。由于菌株NEA在甘油培养基中发酵时,前体物ManNAc的含量不足1 g/L(图1-a),为了验证进一步增强甘油利用能否提升前体物供应,提高Neu5Ac合成效率,对甘油利用途径中的关键酶甘油激酶进行突变,以提高甘油利用效率。
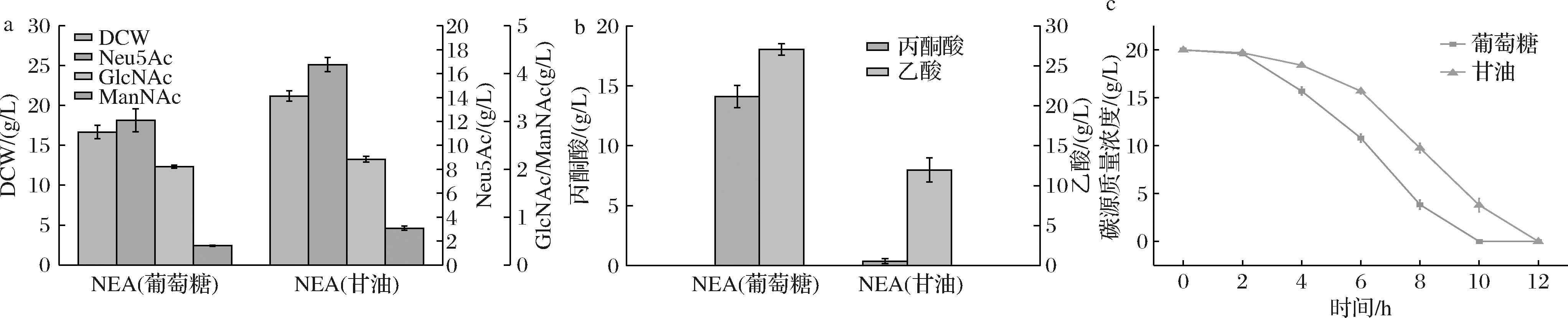
a-不同碳源下细胞生长与Neu5Ac生产情况;b-不同碳源下丙酮酸和乙酸积累情况;c-不同碳源消耗情况
图1 不同碳源条件下菌株NEA生长与Neu5Ac生产情况
Fig.1 Growth and Neu5Ac production of NEA using different carbon sources
2.2 甘油利用强化对NEU5AC-1菌株生长与Neu5Ac合成的影响
在甘油利用途径中,基因glpK编码的甘油激酶是甘油代谢中的限速酶。研究表明,甘油激酶可以受到糖酵解中果糖-1,6-二磷酸的反馈抑制,直接过表达glpK对菌体的生长速率以及甘油的利用率影响较小[15]。文献报道,glpK的突变可以有效缓解果糖-1,6-二磷酸的反馈抑制。PETTIGREW等[16]报道E. coli glpK突变基因编码的GlpK氨基酸列序列中304位(Gly→Ser)也能够有效降低果糖-1,6-二磷酸对甘油激酶的反馈抑制,提高甘油的利用效率。为了进一步增强甘油利用效率,在菌株NEA引入文献报道的突变体glpK[G304S][16]。突变体glpK[G304S]的引入过程如图2所示,首先在菌株NEA基因组上对glpK基因包含待突变位点的部分区域进行敲除,并引入优化的化脓性链球菌的原型间隔序列[17],作为突变序列插入的靶点;同时,通过设计突变引物并进行PCR重叠得到突变的glpK[G304S]目的基因片段,最后整合至菌株NEA基因组上,经过菌落PCR与基因测序验证,得到含突变体glpK[G304S]的菌株NEU5AC-1。以甘油为碳源对菌株NEA与NEU5AC-1进行摇瓶发酵实验,结果如图3所示。
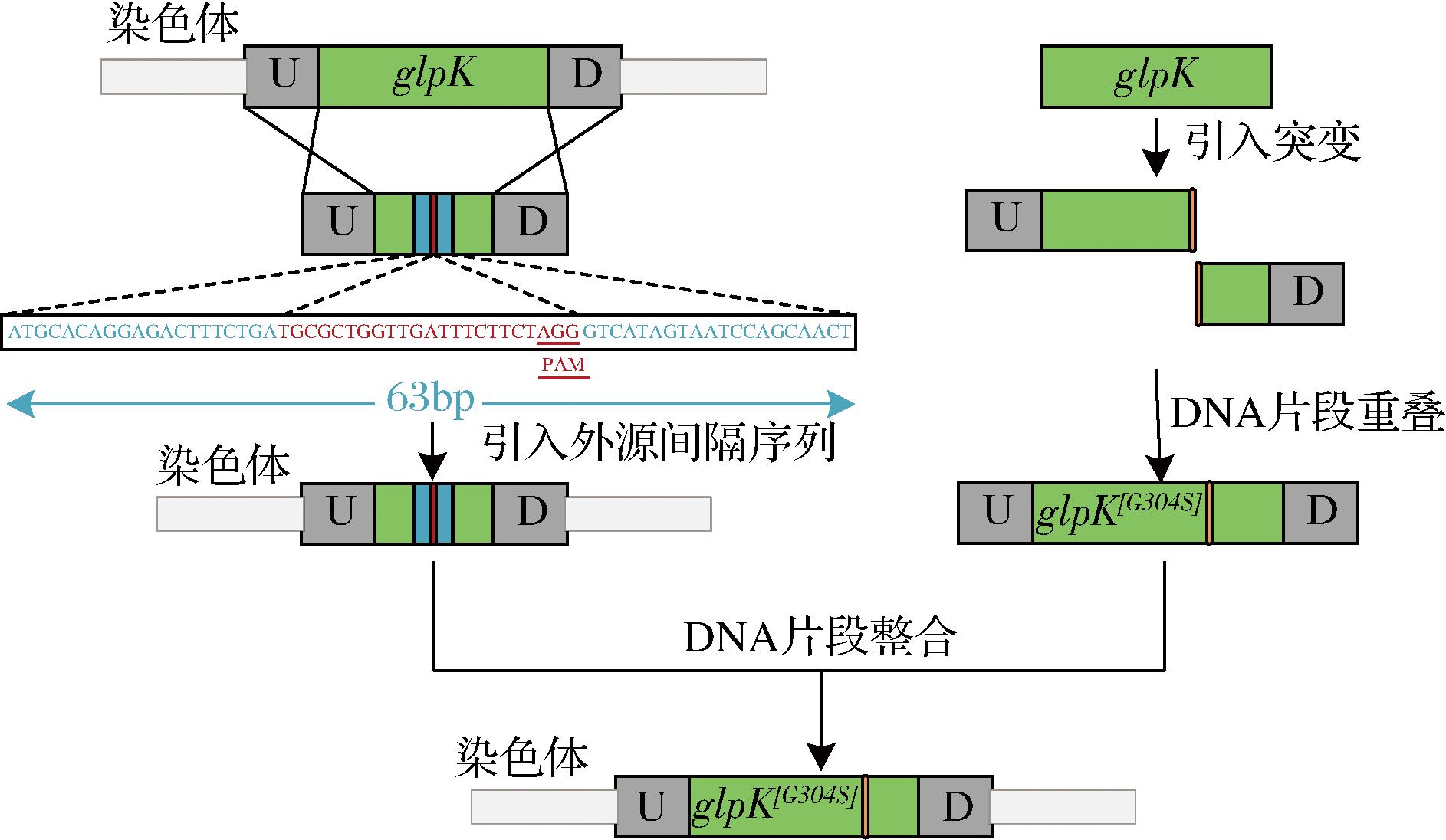
图2 glpK[G304S]突变基因在基因组上的整合
Fig.2 Strategy of integrating gene glpK[G304S] mutation into E. coli genome
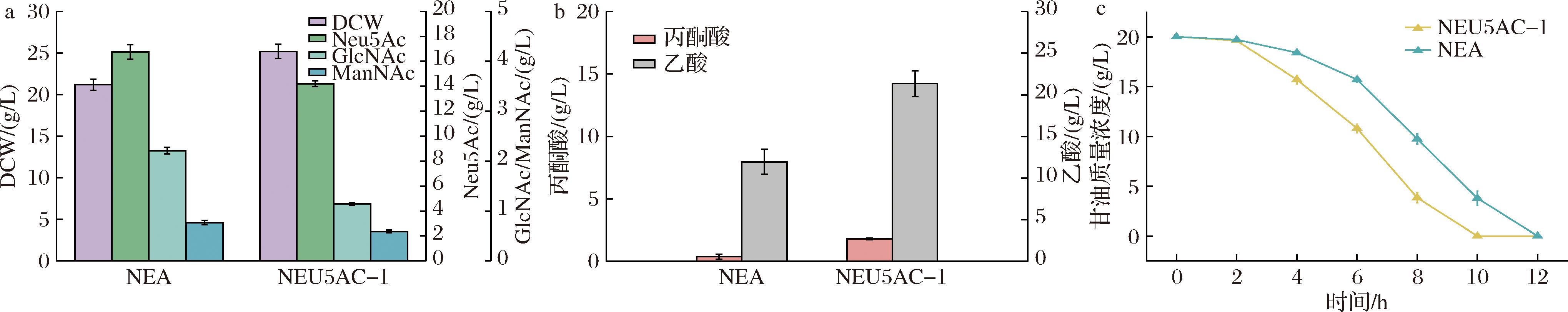
a-DCW和Neu5Ac生产情况;b-丙酮酸和乙酸积累情况;c-甘油消耗情况
图3 强化甘油利用后菌株的生长与Neu5Ac生产情况
Fig.3 Growth and Neu5Ac production of strains enhanced glycerol utilization pathway
从图3中可以看出,引入突变体glpK[G304S]的菌株NEU5AC-1,消耗甘油速率得到提高,菌株生物量进一步提升,然而Neu5Ac产量相比于未强化甘油利用的菌株NEA,下降了15.21%;前体物ManNAc也有不同程度下降;同时,NEU5AC-1中副产物乙酸的积累,较NEA提高了78.7%。以上结果表明,glpK[G304S]确实强化了甘油的代谢速度,但是过快的代谢速度,导致了糖酵解通量过强,副产物乙酸大量溢流,同时,从甘油进行糖异生合成GlcNAc与ManNAc的强度减弱,进而导致ManNAc与PEP之间不平衡,损害了Neu5Ac的合成效率。乙酸作为一种有毒物质,若在细胞内积累过多,很可能引起一系列的问题:如抑制菌体生长、抑制蛋白合成、发酵过程pH控制难等。因此,甘油利用途径过强,导致碳代谢流供应生长过强,不利于Neu5Ac的合成,需要对细胞生长与生产过程进行适当平衡,才能实现目标产物的高效率合成。
2.3 混合碳源对NEU5AC-2菌株生长与Neu5Ac合成的影响
上述不同碳源利用结果表明,甘油的适当速度代谢合成Neu5Ac比葡萄糖具有优势。然而,过强的甘油利用速度,导致菌株生长代谢过强,Neu5Ac产量下降。在实验室的前期研究中,葡萄糖、甘油混合碳源的利用对于促进GlcNAc合成具有显著作用,同时,完全不产生副产物乙酸,表明糖酵解与TCA循环达到了平衡。基于上述结果,为了进一步提高Neu5Ac合成的转化率,本研究对菌株NEU5AC-1中6-磷酸果糖激酶编码基因pfkA敲除得到NEU5AC-2菌株,尝试利用混合碳源进行代谢分工,如图4所示:甘油主要用于提供细胞生长的骨架与PEP供应,葡萄糖主要用于GlcNAc及ManNAc的合成,并进一步通过优化甘油与葡萄糖的比例,平衡前体物PEP与ManNAc的供应。

图4 混合碳源代谢分工进行Neu5Ac合成的策略示意图
Fig.4 Strategies for metabolic division in the utilization of mixed carbon sources for Neu5Ac synthesis
在E.coli中,存在葡萄糖的分解代谢阻遏,影响其他碳源的利用。在前期构建中,通过敲除ptsG,引入glf基因以及过表达glk基因,在不影响摄糖速率的情况下提高了PEP的积累[13]。ptsG的敲除解除了葡萄糖的分解代谢产物阻遏,因此,可实现混合碳源的共利用。分别在葡萄糖、甘油单一碳源以及葡萄糖/甘油混合碳源比例4∶1、1∶1、1∶4中,进行了NEU5AC-2菌株的摇瓶发酵,发酵结果如图5所示。

a-DCW和Neu5Ac生产情况;b-丙酮酸和乙酸积累情况;c-菌株NEU5AC-1与NEU5AC-2单一葡萄糖消耗情况
图5 混合碳源中葡萄糖/甘油比例对NEU5AC-2菌株生长和Neu5Ac合成的影响
Fig.5 Effects of the ratios of glucose/glycerol in the mixed carbon sources on cell growth and Neu5Ac production
在混合碳源中,甘油所占比列越高,最终样品中检测到的乙酸含量越高,单一甘油发酵时,乙酸最高达到31.62 g/L。乙酸的大量积累,对菌体产生毒害作用,使得最终菌体量较低。葡萄糖所占比例越高,GlcNAc与ManNAc积累越多,说明pfkA的敲除达到了预期的效果,使葡萄糖主要用于GlcNAc合成。然而,从图5结果来看,碳源的代谢分工对Neu5Ac的生产并没有发挥预期作用,与该策略在GlcNAc合成中的有益效果不同[18]。这可能是由于ptsG的敲除,与非磷酸转运途径的引入,对于中心碳代谢产生的影响比较大;同时,本研究中Neu5Ac的合成以PEP与ManNAc这2种代谢物作为前体物,二者的平衡尤为重要;除此之外,PEP作为中心碳代谢的关键代谢物,对中心碳代谢过程的多个酶具有调控作用。PEP的积累可以抑制pfkA编码的6-磷酸果糖激酶、pgi编码的6-磷酸葡萄糖异构酶、aceA编码的异柠檬酸裂解酶、icd编码的异柠檬酸脱氢酶等酶的活性,以减少中心碳代谢强度;同时,可以激活fbp编码的果糖-1,6-二磷酸酶、aceK编码的异柠檬酸脱氢酶激酶等酶的活性,增强糖异生过程。因此,PEP的过量积累对于细胞中心碳代谢,以及细胞生长产生不利影响,而积累量不足,又容易导致Neu5Ac合成效率降低。因此,PEP保持与ManNAc相平衡的适量供应,是Neu5Ac高效合成的关键。
图5结果表明,NEU5AC-2中pfkA的敲除使其在葡萄糖单一培养基中显著减少了丙酮酸与乙酸的积累。摇瓶发酵32 h,ManNAc积累3.01 g/L,Neu5Ac产量为15.05 g/L,菌体量明显高于单一甘油和混合碳源条件,同时副产物乙酸仅有4 g/L的积累;发酵36 h,Neu5Ac产量为16.74 g/L;发酵38 h,Neu5Ac产量高达18.41 g/L。由图5-c可知,在发酵前期,NEU5AC-2摄取葡萄糖速率明显降低,发酵8 h仅消耗了4 g/L的葡萄糖,而未敲除pfkA的菌株NEU5AC-1可以消耗16 g/L,但最终NEU5AC-1菌体量却能达到23.65 g/L,说明pfkA的敲除,有效调控了PEP的供应与消耗,充分供应合成需求的同时,缓慢供应生长代谢,乙酸积累得到缓解的同时,ManNAc也得到充足供应,Neu5Ac可以持续不断的合成,换言之,NEU5AC-2具有持续生产Neu5Ac的能力,这与MA等[18]在N-乙酰氨基葡萄糖生产中结论一致,敲除pfkA后,菌株生长显著变缓,有较长的延滞期,但在发酵后期有快速生长现象,最终菌体量甚至超过未敲除pfkA的对照菌株,N-乙酰氨基葡萄糖的生产也有类似规律,发酵前期低于对照菌株,而在发酵后期仍然有持续生产能力。由上述结论可知,相比于菌株NEA使用甘油发酵,菌株NEU5AC-2使用葡萄糖作为单一碳源,达到了PEP供应与消耗的更优平衡,可以产生更少的副产物乙酸,并且在后期仍具有持续生产能力。因此,NEU5AC-2在后续扩大生产上更具优势。
2.4 葡萄糖为碳源条件下的发酵放大试验
综合上述结果,NEU5AC-2菌株以葡萄糖为碳源发酵时,能够产生较少的副产物乙酸,Neu5Ac产量相对较高。为测试在放大规模发酵的情况,对其进行了5 L发酵罐分批补料发酵培养。发酵结果如图6所示,菌株NEU5AC-2以葡萄糖为碳源,整体生长较为缓和,最大DCW值为23.3 g/L,发酵过程无乙酸积累。虽然菌株NEU5AC-2在发酵前期利用葡萄糖速率较慢,产物合成与细胞生长相对较慢,但是在10 h后,Neu5Ac合成速度显著提升,并保持高速合成,发酵38 h,Neu5Ac产量达到23.8 g/L,糖酸转化率为0.116 g/g葡萄糖。
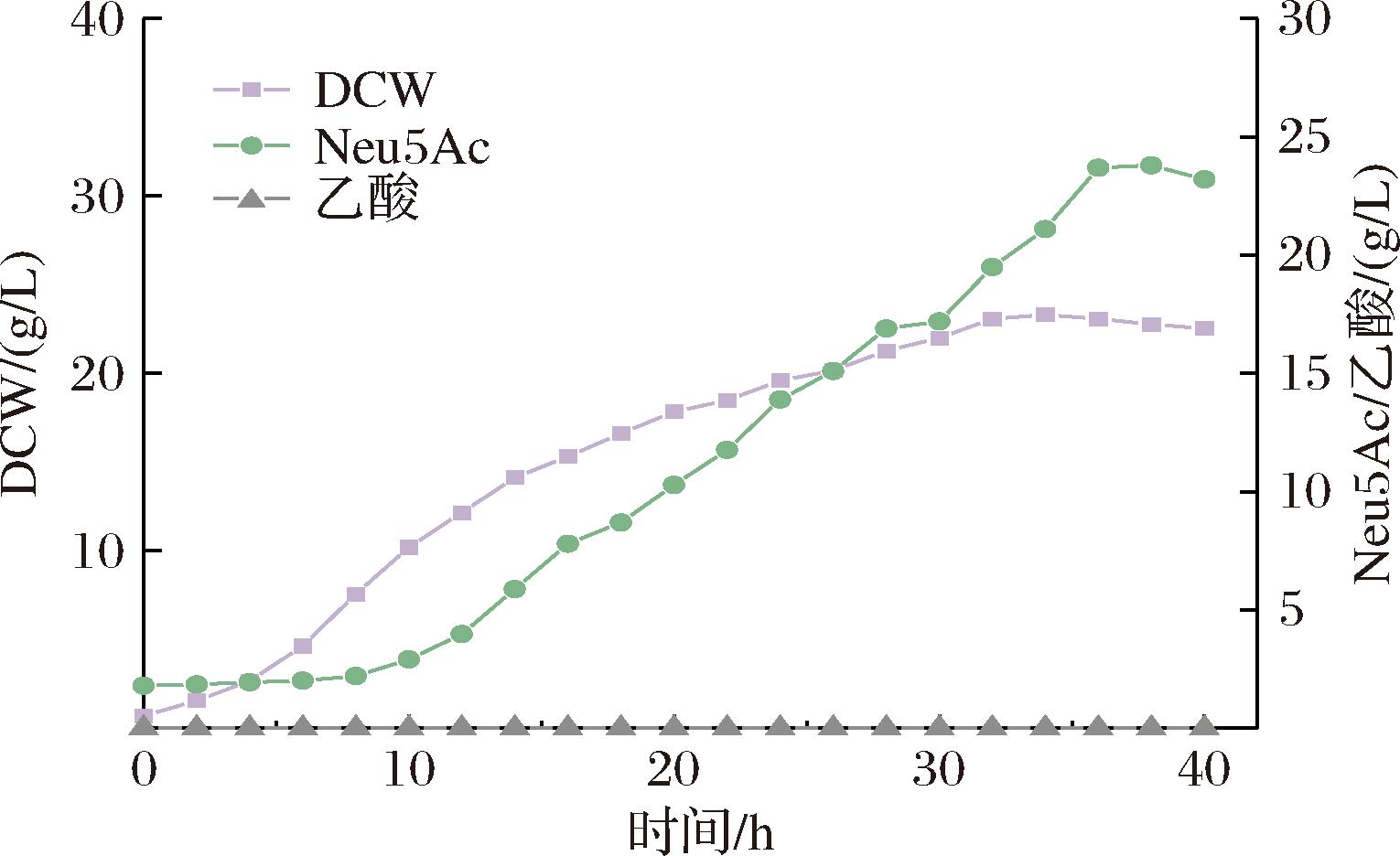
图6 工程菌株NEU5AC-2 5L发酵罐生产Neu5Ac
Fig.6 Production of Neu5Ac by the engineered strain NEU5AC-2 in a 5 L fermentor
3 讨论
随着合成生物学及系统代谢工程等技术手段的发展,微生物合成已成为提高Neu5Ac产量和降低生产成本的重要手段。然而,在工程菌株发酵过程中,如何协调碳源的利用和产物的合成这两个关键环节是需要进一步解决的难题。葡萄糖是大肠杆菌发酵常用碳源,代谢速度过快往往导致菌体生长与产物合成不平衡。为提高葡萄糖的利用率与目标产物的转化率,对葡萄糖代谢途径关键节点进行调控就变得尤为重要。
甘油是生物柴油炼制中的主要副产物,大约占据生物柴油产量的10%[19],随着生物柴油工业的蓬勃发展,大量的粗甘油出现剩余,作为廉价碳源,具有丰富的来源。E.coli具有利用甘油的途径,利用甘油进行E.coli中相关产品的生产已有较多报道。如BLANKSCHIEN等[20]在E.coli中利用甘油进行琥珀酸的生产,转化率达到0.69 g/g甘油。ZHANG等[21]构建了利用甘油进行E.coli中L-丝氨酸的高转化率生产。芳香族化合物生物合成途径中需要两分子PEP,与磷酸转移酶系统摄取葡萄糖相比,甘油摄取不需要PEP,WEINER等[9]利用大肠杆菌以甘油为碳源分批补料生产13.4 g/L L-苯丙氨酸。可见,甘油作为廉价碳源可以被E.coli高效利用。
在本研究中,首先使用甘油作为碳源,出发菌株NEA摇瓶发酵32 h产生16.75 g/L Neu5Ac,然而进一步增强甘油利用效率后,菌体生长与Neu5Ac生产出现失衡。为协调菌体生长与生产,进一步对菌株NEU5AC-1中6-磷酸果糖激酶编码基因pfkA进行敲除,尝试混合碳源策略实现生产与细胞生长中的代谢分工,而在对比中发现,单一葡萄糖碳源持续生产能力最强,摇瓶发酵38 h产生18.41 g/L Neu5Ac,且副产物乙酸含量显著下降。在实验室前期工作中,pfkA基因的敲除与glpK[G304S]的引入,使得大肠杆菌利用葡萄糖/甘油混合碳源生产GlcNAc的效率显著提升,在5 L发酵罐发酵72 h,GlcNAc产量达到179 g/L,并且发酵过程完全没有副产物乙酸的积累,发酵过程高效稳定[18]。然而,在本研究Neu5Ac的合成过程中,该策略并没有产生预想调控两种前体物的效果。主要原因在于Neu5Ac的合成需要以PEP为前体物,双碳源的引入,对于PEP的供应产生了过强的效果,从而导致丙酮酸的大量积累,进一步转化为乙酸,产生细胞毒害。本研究发现,具有pfkA敲除的菌株NEU5AC-2,在单一葡萄糖碳源培养基中,实现了PEP与ManNAc的协调优化,减少了乙酸的积累,使得细胞能够更加持久地合成目标产物。不过,该菌株在发酵前期仍然存在菌体生长缓慢的不足,关键酶的表达可能受到限制等问题。适应性进化作为一种强有力的工具,在工业微生物细胞工厂优化中具有重要地位,通过该策略,大肠杆菌和酿酒酵母在生产有机酸(如乳酸[22]、丙酮酸[23]、琥珀酸[24]等羧酸)的产量进一步提高。后续可使用该策略对菌株NEU5AC-2进行定向进化,强化其利用葡萄糖的能力,有望解决菌体前期生长过慢现象,进一步提升Neu5Ac合成效率。此外,可使用不同强度启动子调控pfkA基因表达,进一步优化关键节点处碳流的分配;还可以选用动态调控元件控制pfkA基因的表达,发酵前期开启pfkA基因表达,满足细胞生长需求;在发酵过程适当时期,减弱或关闭pfkA基因表达,使细胞高效进行目标产物合成。综上所述,本研究通过碳源利用调控,对中心碳代谢调控、关键代谢节点处的碳流分配进行了优化,减少了副产物乙酸的积累,实现了目标产物合成效率提升,并为目标产物合成效率的进一步提升指明了方向,可以为其他以糖酵解途径的中间代谢物为前体物的异源产物合成提供借鉴。
[1] HU S Y, CHEN J, YANG Z Y, et al.Coupled bioconversion for preparation of N-acetyl-D-neuraminic acid using immobilized N-acetyl-D-glucosamine-2-epimerase and N-acetyl-D-neuraminic acid lyase[J].Applied Microbiology and Biotechnology, 2010, 85(5):1383-1391.
[2] KRAGL U, GYGAX D, GHISALBA O, et al.Enzymatic two-step synthesis of N-acetyl-neuraminic acid in the enzyme membrane reactor[J].Angewandte Chemie International Edition in English, 1991, 30(7):827-828.
[3] ZHANG X L, LIU Y F, LIU L, et al.Microbial production of sialic acid and sialylated human milk oligosaccharides:Advances and perspectives[J].Biotechnology Advances, 2019, 37(5):787-800.
[4] LEE Y C, CHIEN H C R, HSU W H.Production of N-acetyl-D-neuraminic acid by recombinant whole cells expressing Anabaena sp.CH1 N-acetyl-D-glucosamine 2-epimerase and Escherichia coli N-acetyl-D-neuraminic acid lyase[J].Journal of Biotechnology, 2007, 129(3):453-460.
[5] MARU I, OHNISHI J, OHTA Y, et al.Why is sialic acid attracting interest now? Complete enzymatic synthesis of sialic acid with N-acylglucosamine 2-epimerase[J].Journal of Bioscience and Bioengineering, 2002, 93(3):258-265.
[6] ZHANG L, WEI T T, LI Y, et al.Functional metabolomics characterizes a key role for N-acetylneuraminic acid in coronary artery diseases[J].Circulation, 2018, 137(13):1374-1390.
[7] BONDIOLI L, RUOZI B, BELLETTI D, et al.Sialic acid as a potential approach for the protection and targeting of nanocarriers[J].Expert Opinion on Drug Delivery, 2011, 8(7):921-937.
[8] GAO X Y, ZHANG F F, WU M, et al.Production of N-acetyl-D-neuraminic acid by whole cells expressing Bacteroides thetaiotaomicron N-acetyl-D-glucosamine 2-epimerase and Escherichia coli N-acetyl-D-neuraminic acid aldolase[J].Journal of Agricultural and Food Chemistry, 2019, 67(22):6285-6291.
[9] WEINER M, ALBERMANN C, GOTTLIEB K, et al.Fed-batch production of L-phenylalanine from glycerol and ammonia with recombinant Escherichia coli[J].Biochemical Engineering Journal, 2014, 83:62-69.
[10] MURARKA A, DHARMADI Y, YAZDANI S S, et al.Fermentative utilization of glycerol by Escherichia coli and its implications for the production of fuels and chemicals[J].Applied and Environmental Microbiology, 2008, 74(4):1124-1135.
[11] LI Y F, LIN Z Q, HUANG C, et al.Metabolic engineering of Escherichia coli using CRISPR-Cas9 meditated genome editing[J].Metabolic Engineering, 2015, 31:13-21.
[12] 侯正杰. 大肠杆菌N-乙酰神经氨酸合成途径的构建与优化[D].天津:天津科技大学, 2020.
HOU Z J, Construction and optimization of N-acetylneuraminic acid pathway in Escherichia coli[D].Tianjin:Tianjin University of Science and Technology, 2020.
[13] 张颖. 代谢工程改造大肠杆菌高效生产N-乙酰神经氨酸[D].天津:天津科技大学, 2022.
ZHANG Y.Metabolic engineering transformation of Escherichia coli for efficient production of N-acetylneuraminic acid[D].Tianjin:Tianjin University of Science &Technology, 2022.
[14] CHENG K K, LEE B S, MASUDA T, et al.Global metabolic network reorganization by adaptive mutations allows fast growth of Escherichia coli on glycerol[J].Nature Communications, 2014, 5:3233.
[15] GOTTLIEB K, ALBERMANN C, SPRENGER G A.Improvement of L-phenylalanine production from glycerol by recombinant Escherichia coli strains:The role of extra copies of glpK, glpX, and tktA genes[J].Microbial Cell Factories, 2014, 13(1):96.
[16] PETTIGREW D W, MA D P, CONRAD C A, et al.Escherichia coli glycerol kinase.Cloning and sequencing of the glpK gene and the primary structure of the enzyme[J].Journal of Biological Chemistry, 1988, 263(1):135-139.
[17] LI Y J, YAN F Q, WU H Y, et al.Multiple-step chromosomal integration of divided segments from a large DNA fragment via CRISPR/Cas9 in Escherichia coli[J].Journal of Industrial Microbiology &Biotechnology, 2019, 46(1):81-90.
[18] MA Q, SUN Q W, TAN M, et al.Highly efficient production of N-acetyl-glucosamine in Escherichia coli by appropriate catabolic division of labor in the utilization of mixed glycerol/glucose carbon sources[J].Journal of Agricultural and Food Chemistry, 2021, 69(21):5966-5975.
[19] MEISWINKEL T M, RITTMANN D, LINDNER S N, et al.Crude glycerol-based production of amino acids and putrescine by Corynebacterium glutamicum[J].Bioresource Technology, 2013, 145:254-258.
[20] BLANKSCHIEN M D, CLOMBURG J M, GONZALEZ R.Metabolic engineering of Escherichia coli for the production of succinate from glycerol[J].Metabolic Engineering, 2010, 12(5):409-419.
[21] ZHANG X M, ZHANG D, ZHU J F, et al.High-yield production of L-serine from glycerol by engineered Escherichia coli[J].Journal of Industrial Microbiology &Biotechnology, 2019, 46(2):221-230.
[22] UTRILLA J, LICONA-CASSANI C, MARCELLIN E, et al.Engineering and adaptive evolution of Escherichia coli for D-lactate fermentation reveals GatC as a xylose transporter[J].Metabolic Engineering, 2012, 14(5):469-476.
[23] WANG Z K, GAO C J, WANG Q, et al.Production of pyruvate in Saccharomyces cerevisiae through adaptive evolution and rational cofactor metabolic engineering[J].Biochemical Engineering Journal, 2012, 67:126-131.
[24] WU M K, GUAN Z, WANG Y J, et al.Efficient succinic acid production by engineered Escherichia coli using ammonia as neutralizer[J].Journal of Chemical Technology &Biotechnology, 2016, 91(9):2412-2418.