中国对虾(Fenneropenaeus chinensis)是重要渔业资源之一,主要分布于中国、印度、越南等亚洲国家,是大型经济虾类。亚洲约占全球虾养殖业的80%,根据联合国粮食及农业组织(Food and Agriculture Organization of the United Nations, FAO)的数据,2022年全球虾产量达到501.10万t,超过2021年的456.90万t。其中,2022年中国海水养殖甲壳类总产量为195.25万t,同比上涨5.26%,且中国对虾产量同比上涨5.02%[1]。中国是虾类主要消费国,2022年上半年,虾类进口量增加25.80%,达到37.01万t。中国对虾富含优质蛋白、微量元素、脂肪酸、维生素及虾青素抗氧化剂等多种人体必需的营养成分[2]。目前,关于中国对虾的研究主要集中在免疫蛋白分析、育种方法和遗传连锁图谱构建以及保鲜技术等方面,而关于通过开发新技术来增强中国对虾虾肉生物活性、提高蛋白质品质方面还有待进一步研究。
高压脉冲电场(high intensity pulsed electric field, PEF)是一种新兴的、可持续的、环保的非热处理方法,被认为是21世纪食品加工技术领域的最新技术之一。目前,它被应用于食品科学的许多领域,包括食品保存和灭菌、生物活性成分提取、农药残留降解和食品安全等[3-4]。脉冲电场将电能以极短时间的高强度脉冲形式作用于放置在两极之间的样品,蛋白质的极性基团在吸收能量时产生自由基,导致蛋白质聚集和膨胀。PEF技术作为一种非热加工技术,具有加工时间短、温度变化小的特点。这样可以避免对材料性能和感官性能的负面影响,最大限度地保持食品原有的营养价值[5]。此外,与传统的化学方法相比,PEF处理不需要使用化学试剂,则不会在食品中留下任何化学残留物。NIU等[6]采用脉冲电场辅助提取柚皮苷时,不仅提高了提取率,还增强了其抗氧化活性。OMS-OLIU等[7]对西瓜汁进行了高强度脉冲电场处理,调整了工艺参数后可使西瓜汁番茄红素保留率和抗氧化能力提高。李迎秋等[8]发现高压脉冲电场会影响大豆分离蛋白结构,提高其疏水性和巯基含量。DONG等[9]证实脉冲电场处理后的肌肉肌原纤维蛋白的微观结构与未处理样品有明显不同,蛋白质凝胶网络之间的水通道被小水孔所取代。根据前人研究表明,高压脉冲电场处理会有效提高食品的抗氧化活性,影响蛋白质结构及特性。
因此,本研究将中国对虾于不同条件下高压脉冲电场处理后,对其抗氧化活性、蛋白质特性以及引起抗氧化活性变化的因素进行测定分析,探究这一方法对中国对虾虾肉抗氧化活性及蛋白质特性的影响,以期为中国对虾的加工方式和生物活性增强提供有益参考。
1 材料与方法
1.1 材料与试剂
中国对虾从中国上海浦东新区芦潮港海鲜市场购买。虾的平均长度和平均质量分别为(13.75±0.25) cm和(14.40±0.20) g。将虾去头、去壳、去虾线后留下可食用部分置于密封袋中,并保存在-20 ℃中备用。
主要试剂:菲咯嗪溶液、铁氰化钾、DPPH、虾青素标准品,上海麦克林生物科技有限公司;三氯乙酸(trichloroacetic acid,TCA)、FeCl2、FeCl3、乙醇,四川爱奇生物科技有限公司;FeSO4、盐酸(优级纯)、苯酚、乙腈(色谱级)、2,4,6-三吡啶-s-三嗪(2,4,6-tripyridyl-s-triazine,TPTZ)、甲醇(色谱级)、柠檬酸钠(优级纯)、印三酮溶液、BCA蛋白检测试剂盒,北京索莱宝科技有限公司。所用试剂均为分析纯试剂。
1.2 仪器与设备
LA8080日立全自动氨基酸分析仪,日本东京日立制造所;Z326K低温离心机、Multiskan Go全自动酶标仪,美国赛默飞世尔科技有限公司;UV-1800紫外可见分光光度计,日本岛津公司;DZF-6090减压干燥仪,上海徐爽电子公司;Waters高效液相色谱仪,沃特世科技(上海)有限公司;TR-3L旋转蒸发仪,上海泰坦科技股份有限公司;N5230C PNA-L网络分析仪、85070E同轴探针,安捷伦科技有限公司。
1.3 实验方法
1.3.1 高压脉冲电场处理
本实验设计并搭建了一套高压脉冲电场处理装置,如图1所示,主要包括升压变压器、整流模块、调压器、放电球隙以及处理腔。处理装置上下两极为铜板,通过20×20个钨针对样品溶液进行放电,钨针尖与下极板距离为0.4 cm。处理样品统一取虾肉第二节肌肉处。相关处理条件如下:(1)10 kV/cm-5 min (10-5);(2)10 kV/cm-10 min (10-10);(3)10 kV/cm-15 min (10-15);(4)15 kV/cm-5 min (15-5);(5)15 kV/cm-10 min (15-10);(6)15 kV/cm-15 min (15-15);(7)20 kV/cm-5 min (20-5);(8)20 kV/cm-10 min (20-10);(9)20 kV/cm-15 min (20-15);(10)以未处理样品为对照组,记为Con。处理后取出样品置于分隔盒中密封,-20 ℃保存备用。
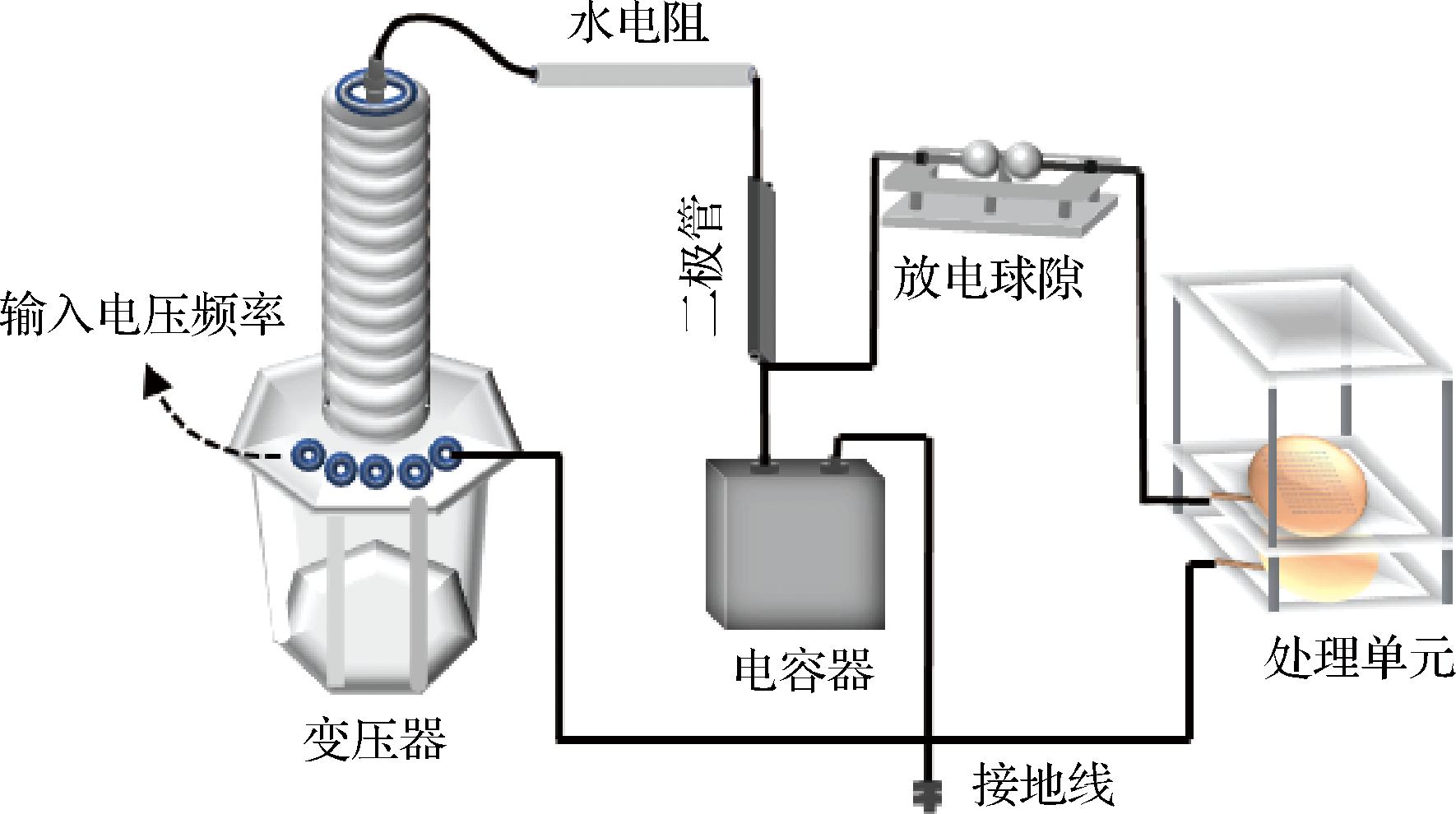
图1 实验装置接线图
Fig.1 Experimental device wiring diagram
1.3.2 总抗氧化活性
测定样品的总抗氧化能力方法如下[10]:将20 mmol/L的FeCl3溶液、10 mmol/L的TPTZ溶液和300 mmol/L的乙酸缓冲液按1∶1∶10的体积比混合,即为FRAP工作液。将1 g样品与10 mL乙醇混合均质,在4 ℃,8 500 r/min离心5 min后取上清液,即为样品提取液。取190 μL FRAP工作液与5 μL样品提取液加入96孔板中,37 ℃避光条件下孵育5 min后,采用酶标仪检测其吸光度变化(593 nm)。其中,以1 000 μmol/L硫酸亚铁溶液为标准溶液制备标准曲线。
1.3.3 DPPH自由基清除活性
本实验参照林晓彤等[11]的方法进行:称取2 mg DPPH溶于50 mL乙醇中配制成0.1 mmol/L的DPPH醇溶液。将相同体积的DPPH醇溶液与不同条件处理的样品提取液混合、涡旋,在25 ℃条件下避光孵育30 min,测其吸光度(517 nm),记为样品组As;对照组以相同体积水与DPPH醇溶液混合孵育,测定后记为Ac;空白组是取相同体积样品与无水乙醇混合孵育,记为Ab,其计算如公式(1)所示:
清除率![]()
(1)
1.3.4 亚铁离子螯合能力
采用张芷芸等[12]的方法,稍作修改后进行。取200 μL样品提取液,加入370 μL去离子水、10 μL FeCl2(2 mmol/L)混合后,滴加20 μL 5 mmol/L的菲咯嗪溶液,25 ℃孵育10 min后,测定吸光度(562 nm),记为A1。对照组以水代替样品,记为A0。其计算如公式(2)所示:
螯合率![]()
(2)
1.3.5 总还原能力
该实验测定方法如下[13]:取0.2 mL样品提取液与0.5 mL PBS溶液(200 mmol/L,pH 6.6)混匀,加入0.5 mL的10 g/L铁氰化钾混合,50 ℃孵育20 min,加入0.5 mL的10% TCA(体积分数)溶液,在8 500 r/min条件下离心5 min。取100 μL上清液,加入100 μL水和25 μL FeCl3(1 g/L)混合均匀后,测定其吸光度值(700 nm)。
1.3.6 虾青素含量
采用高效液相色谱法测定虾青素含量,参考刘增萌等[14]的方法并稍作修改。取2 g匀浆后的虾肉组织,加入Na2SO4(4 g)和10 mL乙醇,混匀。超声提取15 min,8 500 r/min离心5 min,收集上清液。残渣中加入10 mL乙醇按上述步骤重复提取3次,合并提取液定容至50 mL混匀。取出5 mL提取液并加入1 mL NaOH-乙醇溶液(20 mmol/L)混匀,4 ℃避光反应12 h,经0.22 μm微孔滤膜过滤后,待测。
1.3.7 游离氨基酸含量
称取2 g处理后的虾肉组织,加入15 mL 5%的TCA均质,4 ℃下8 500 r/min离心5 min,取上清液。沉淀物以上述步骤重复提取至样品无色,合并上清液,定容至50 mL。经0.22 μm微孔滤膜过滤后,待测。
1.3.8 总氨基酸含量
总氨基酸含量的测定参照GB 5009.124—2016《食品安全国家标准 食品中氨基酸的测定》的操作方法进行。简而言之,将不同处理后的虾肌肉组织样品(1 g)精确称量到水解管中,加入15 mL 6 mol/L HCl溶液,滴加3~4滴苯酚,充分混合溶解。对其抽真空10 min后,置于(105±5) ℃的烘箱中水解22 h。取出冷却至室温后移至50 mL容量瓶中定容,混匀。取出1 mL水解液转移至干燥皿中,使用减压干燥器在45 ℃,0 MPa下减压干燥。待水分蒸干后滴加1 mL超纯水继续干燥,直至完全蒸干后加入2 mL柠檬酸钠溶液(pH 2.2)溶解,通过0.22 μm微孔滤膜过滤后,待测。
1.3.9 可溶性蛋白质含量
本研究中蛋白质含量采用BCA蛋白检测试剂盒进行测定。以牛血清白蛋白(bovine serum albumin,BSA)为标准品制作标准曲线。
1.3.10 介电特性
介电性能的测定参照XU等[15]的方法,稍作修改。使用同轴探针连接性能网络分析测量样品蛋白质的介电特性。校准和测量前,打开测试系统,预热2 h。接着将同轴探头依次通过空气-短接块-去离子水三步骤对仪器进行校准。标定后,对去离子水的介电性能进行了测量,以验证标定的有效性。测量频率范围为1~10 GHz。将待测样品置于25 mL小烧杯中,插入探针,测量其介电常数和介电损耗。
1.3.11 统计分析
采用Excel 2016、SPSS 26.0、Origin 2018软件对实验中的相关图表进行分析。所有试验均进行3次。
2 结果与分析
2.1 总抗氧化能力
图2反映了高压脉冲电场处理对虾肉样品总抗氧化能力(total antioxidant capacity, TAC)的影响。总体来看,与未处理组相比(32.81 μmol/100 mg),冲击电压刚作用到虾样品时提高了总抗氧化能力,可能是由于冲击电压破坏了细胞结构和肌肉组织,导致抗氧化物质外溢,提高了其抗氧化能力[16-17]。随后增加处理时间和电场强度总抗氧化能力下降,在15 kV/cm的电场强度下处理5 min时,观察到其下降到最低(33.51 μmol/100 mg),但仍高于未处理组,可能是高强度脉冲引起的活性氧物质的生成参与了氧化反应的发生,致使抗氧化物质的损失与降解[18]。在15 kV/cm和20 kV/cm电场强度下,总抗氧化活性随作用时间增加呈现出上升的趋势,其中,在20 kV/cm下处理15 min时,虾的总抗氧化能力达到最高(38.02 μmol/100 mg),可能是细胞遭受氧化应激时,激活抗氧化酶,使抗氧化物质聚集重组与生成[19]。这些结果表明,采用高压脉冲电场方式处理虾有助于提高其总抗氧化能力。

图2 不同高压脉冲电场处理对虾样品TAC的影响
Fig.2 Effects of different high intensity pulsed electric fields on TAC of shrimp samples
注:图中标注不同字母的值表示存在差异显著(P<0.05)(下同)。
2.2 总还原能力
虾肉样品中含有还原性化合物,包括多酚类、硫醇类化合物等,它们可以中和自由基并减少氧化反应的发生,因此,可以通过测定总还原能力衡量样品的抗氧化能力强弱。如图3所示,高压脉冲电场处理使虾样品的总还原能力增强。未经处理的虾样品总还原能力约为0.24,经不同电场强度和时间处理后,最高达到0.33左右。与对照组相比较,在15 kV/cm和20 kV/cm电场强度下处理5、10、15 min时,样品的总还原能力逐渐增强,在10 kV/cm电场强度下随时间的延长呈现出先上升后下降的趋势,且均高于未处理组,这与测定的总抗氧化能力呈现趋势相似。
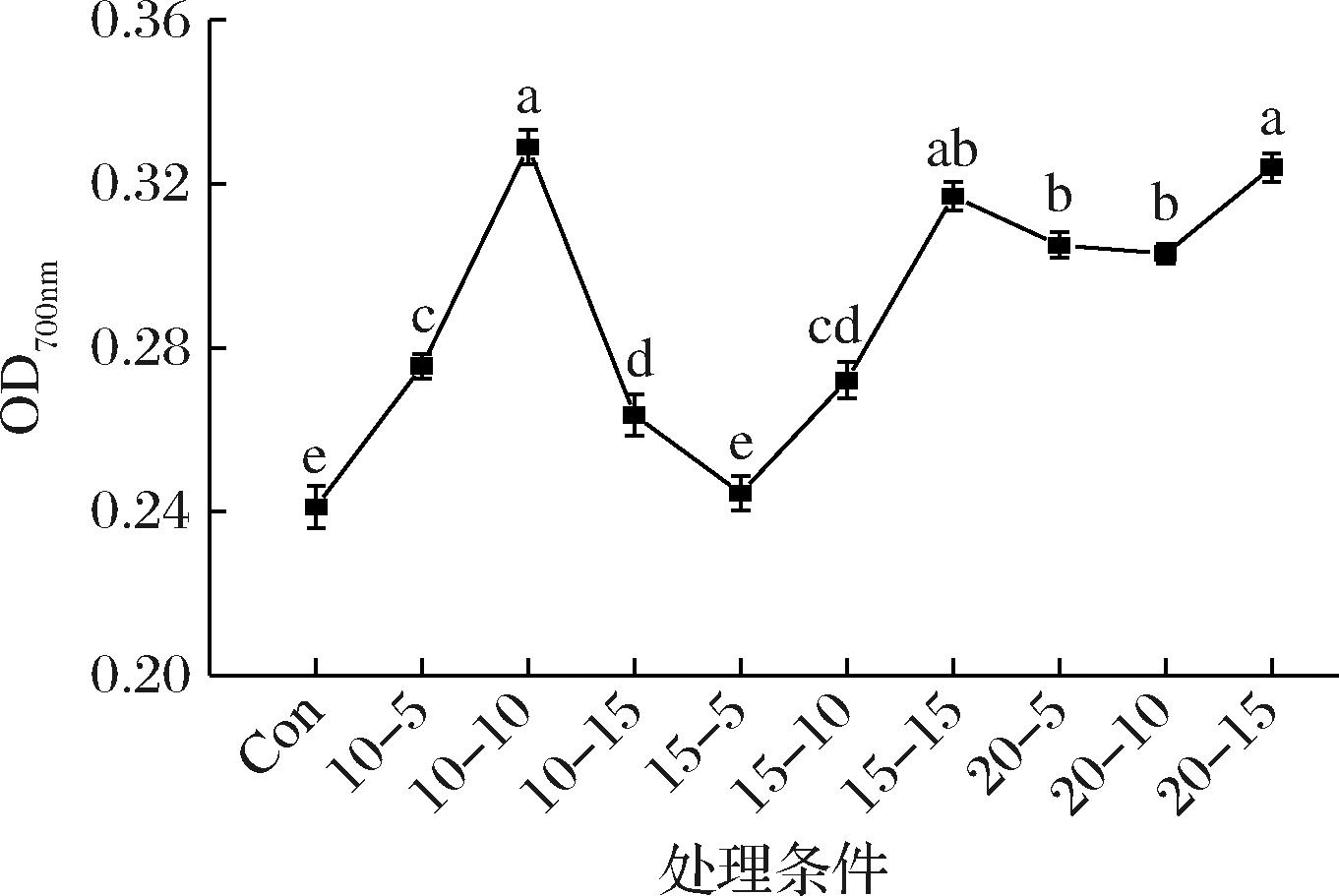
图3 不同高压脉冲电场处理对虾样品总还原能力的影响
Fig.3 Effects of different high intensity pulsed electric fields on the total reduction capacity of shrimp samples
虾样品的抗氧化能力是由其所含的抗氧化物质、可溶性蛋白质、氨基酸等影响的[13]。PEF处理过程中可能会产生自由基和活性氧物质,可以直接或间接与肌肉中的蛋白质分子发生反应,如氧化剪切、交联等[20]。其次,脉冲瞬间的冲击作用也可以破坏虾肉组织,使一些蛋白质发生裂解,增大肌纤维间隙。这些都可能导致虾肉样品还原能力的增加[20]。
2.3 DPPH自由基清除率
图4呈现出PEF处理对虾样品DPPH自由基清除率的影响。随着电场强度和处理时间的增加,自由基清除能力逐渐增加,在10 kV/cm电场强度下处理10 min,虾样品的自由基清除率约为65%。进一步处理呈现下降的趋势,但仍高于未处理组。在20 kV/cm电场强度下处理15 min达到最高(67%),显著提高了63.40%(P<0.05)。这与NIU等[6]在探究脉冲电场辅助处理对柚皮苷抗氧化活性的影响时研究现象一致,猜测可能与脉冲电场处理过程中分子的极化和结构变化有关。
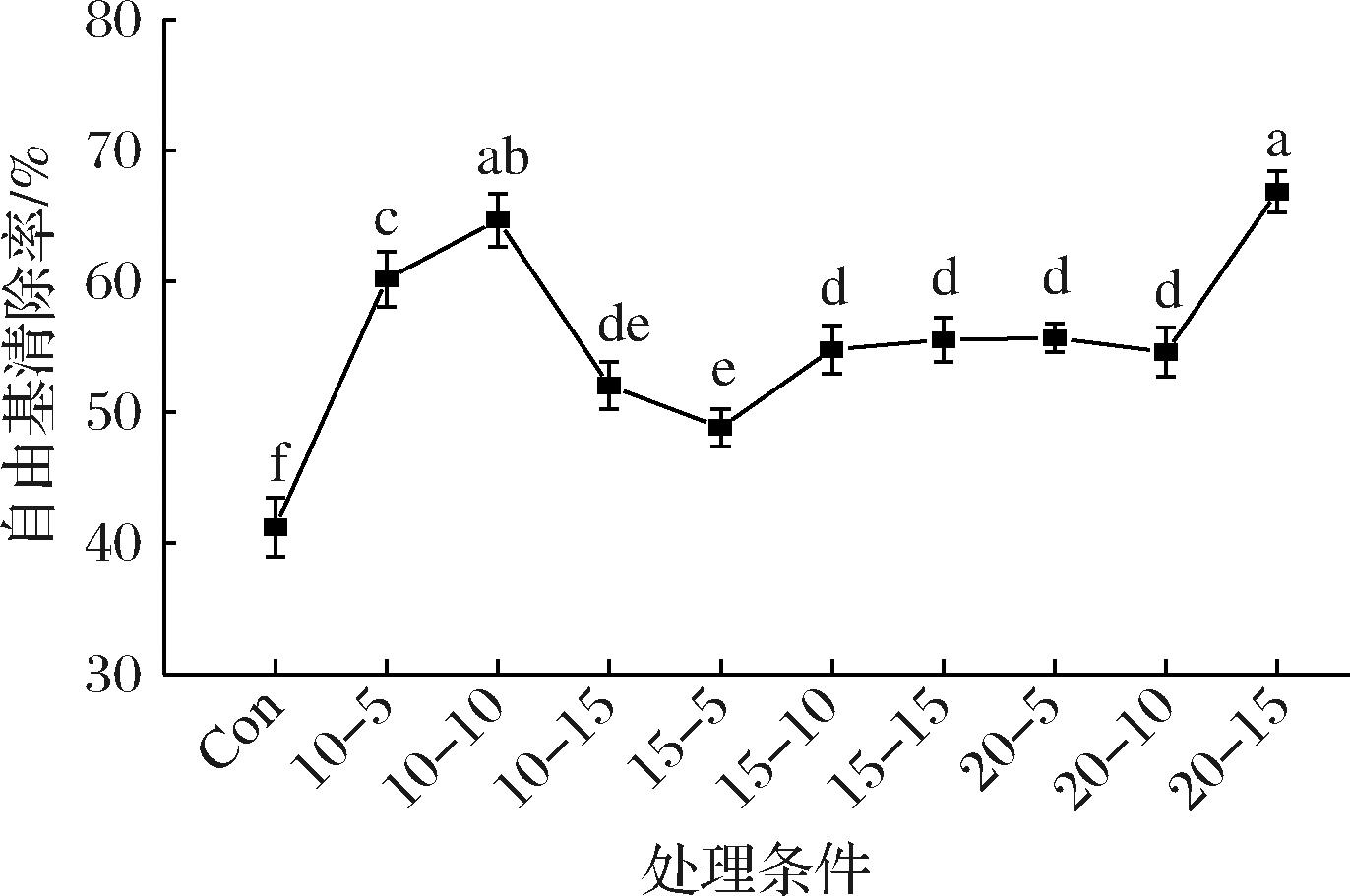
图4 不同条件高压脉冲电场处理对虾样品DPPH自由基清除率的影响
Fig.4 Effects of different high intensity pulsed electric fields on DPPH free radical clearance of shrimp samples
2.4 亚铁离子螯合能力
图5反映了不同条件高压脉冲电场处理对虾肉样品亚铁离子螯合能力的影响,Fe2+螯合能力可以用作衡量样品抗氧化能力的指标之一。未处理样品的Fe2+螯合率为20.59%,随着电场强度和处理时间的增加,螯合率最高提升了43.52%。虾样品亚铁离子螯合能力的变化可能与PEF处理过程中蛋白质氧化应激反应和氨基酸残基修饰有关[21]。
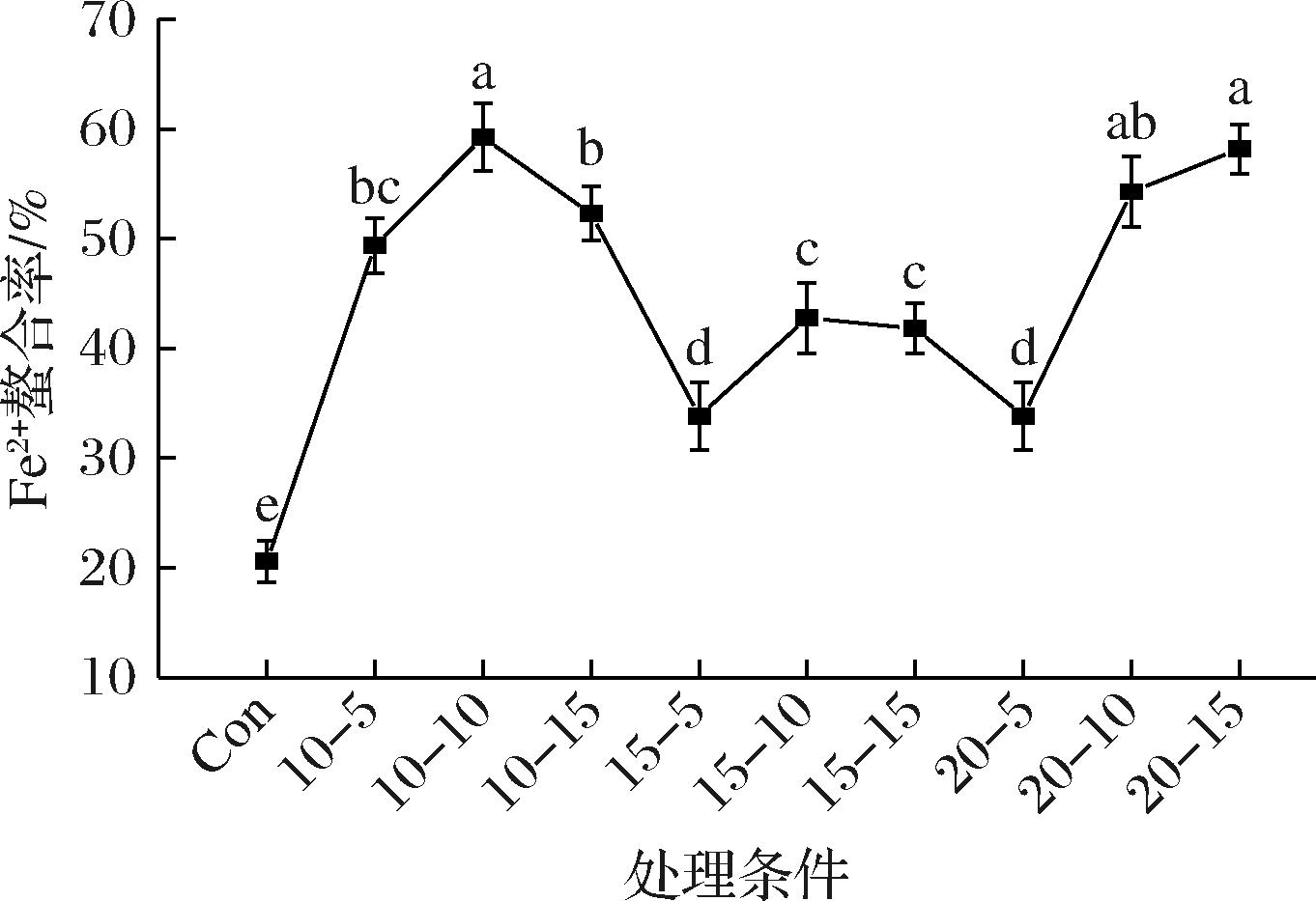
图5 不同高压脉冲电场处理对虾样品Fe2+螯合能力的影响
Fig.5 Effects of different high intensity pulsed electric fields on Fe2+ chelating ability of shrimp samples
2.5 虾青素含量
图6-a为虾青素标准品的重叠色谱图,图中峰群和出峰时间与陈晋明等[22]研究结果一致。以虾青素标准品的质量浓度X(μg/mL)为横坐标,峰面积Y为纵坐标进行线性拟合,获得回归方程y=19 036x-12 392,R2=0.993 2。
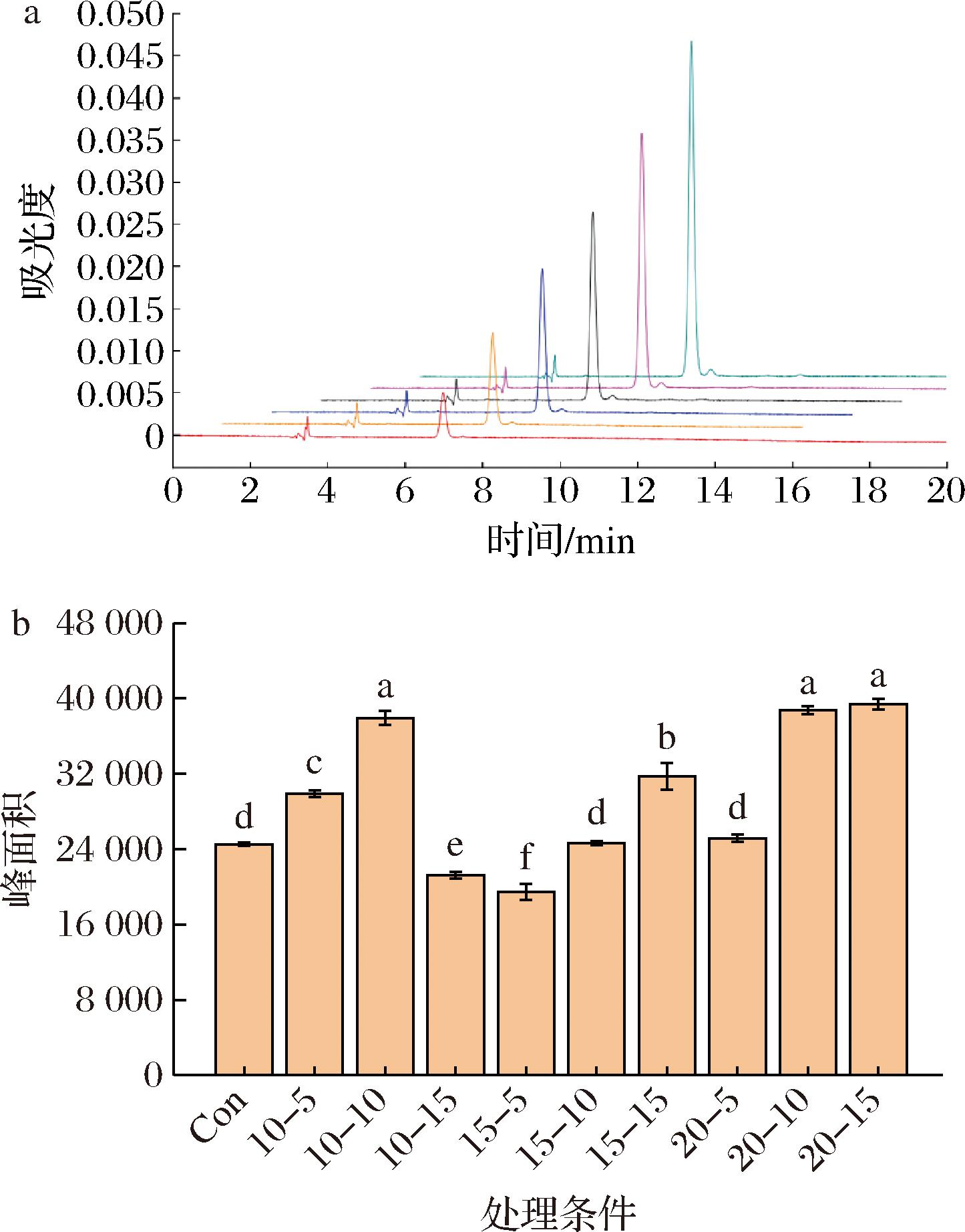
a-虾青素标准品的重叠色谱图;b-不同处理样品中虾青素含量(以峰面积表示)
图6 不同条件高压脉冲电场处理后虾肉中虾青素含量的变化
Fig.6 Changes of astaxanthin content in shrimp meat treated by high intensity pulsed electric field under different conditions
虾青素含量变化由图6-b所示,在较低电场强度和短时间处理下,虾青素含量上升,可能是在处理过程中,高压脉冲电场导致细胞膜的破裂或渗透性增加,细胞内的物质(包括虾青素)释放到外部环境[16]。进一步增强电场强度和延长处理时间,虾青素含量呈现降低趋势,可能是由于虾青素中含有丰富的电子共轭双键结构,对热、光、氧气较敏感,在高压脉冲处理过程中,会产生活性氧,易与样品中虾青素发生反应、降解,从而使虾青素含量降低[23]。在20 kV/cm电场强度下,随处理时间延长虾青素含量有上升的趋势,是由于全反式天然虾青素因其空间位阻原因而容易异构化为顺式异构体[24]。YANG等[25]指出,9-顺式(9-cis)和13-顺式(13-cis)异构体虾青素较全反式天然虾青素具有更强的抗氧化性。因此,虾肉样品抗氧化性增加可能受顺式异构体的形成有关。虾青素含量的变化趋势与抗氧化活性变化趋势类似,这也说明了虾青素含量的变化对虾总体抗氧化能力的变化有显著影响。
2.6 游离氨基酸含量
高压脉冲电场处理后虾肉样品游离氨基酸含量的变化如图7-a所示,未处理组以及不同条件下PEF处理后均检测出15种游离氨基酸,未经处理的样品氨基酸组成中,甘氨酸(Gly)、精氨酸(Arg)及丙氨酸(Ala)含量占比重较大,其中,精氨酸(Arg)含量高达857.71 mg/100 g。图7-b结果显示,脉冲电场可能引起虾蛋白质的部分降解,导致氨基酸的释放,从而与未处理组相比较,经过不同条件PEF处理后,游离氨基酸总含量均有所增加。
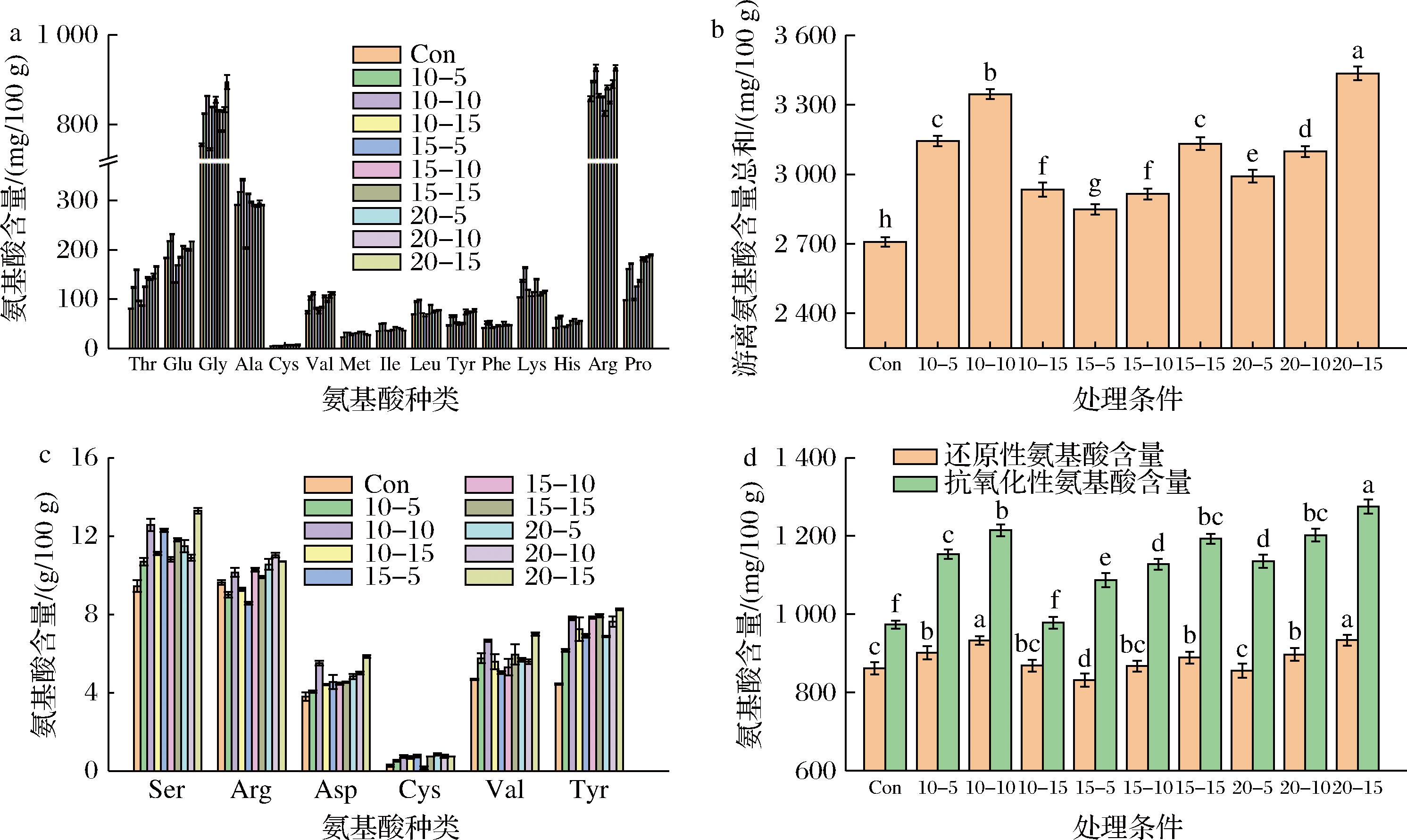
a-各种氨基酸含量变化;b-不同条件处理下游离氨基酸总含量变化;c-具有抗氧化性氨基酸和还原性氨基酸含量的变化;d-不同条件处理下具有抗氧化性氨基酸和还原性氨基酸总含量变化
图7 不同条件高压脉冲电场处理虾肉中游离氨基酸含量的变化
Fig.7 Changes of free amino acid content in shrimp meat treated by high intensity pulsed electric field under different condition
虾样品的抗氧化活性变化可能与相关氨基酸残基修饰有关,将游离氨基酸中具有抗氧化性和还原性氨基酸单独比较。如图7-c和图7-d所示,脉冲电场可增加各类氨基酸含量,在10 kV/cm电场强度下,氨基酸含量上升后又出现下降趋势,但含量值仍高于未处理组,出现这种现象的原因可能是PEF处理过程中产生的活性自由基攻击蛋白质所致,导致部分氨基酸残基被修饰,致使氧化还原反应的发生[21]。在15 kV/cm和20 kV/cm电场强度条件下分别处理5、10、15 min,还原性氨基酸和抗氧化性氨基酸总量均逐渐增加,可能是由于脉冲引起的冲击作用,释放了肌肉中部分水解酶类或脱氨酶类促进其水解,导致氨基酸含量升高[26],进而增加虾肉抗氧化能力,这与张鹰等[27]用高压脉冲电场处理脱脂牛乳研究结果一致。游离氨基酸含量以及其中具有抗氧化性和还原性氨基酸含量的变化趋势与虾肉抗氧化性变化趋势相似,从结果可推测其含量变化对虾肉抗氧化活性的变化有显著影响。
2.7 总氨基酸含量
高压脉冲电场对虾肉氨基酸含量的影响如表1所示。未经过处理的虾肉必需氨基酸含量和非必需氨基酸分别为7.38 g/100 g和14.2 g/100 g。氨基酸组成及品质是评价蛋白质品质的重要指标,可以观察到虾肉中谷氨酸(Glu)、甘氨酸(Gly)、丝氨酸(Ser)以及丙氨酸(Ala)占比重较大,含量丰富,是一种优质的蛋白质资源。
表1 不同条件高压脉冲电场处理下虾肉中氨基酸含量 单位:g/100 g
Table 1 Amino acid content in shrimp meat under different conditions of high intensity pulsed electric field

Con10-510-1010-1515-515-1015-1520-520-1020-15必需氨基酸Thr0.97±0.00c0.90±0.01d1.05±0.01b0.98±0.04c1.09±0.00b1.19±0.00a0.99±0.00c1.17±0.01a1.08±0.00b1.10±0.01`Val0.94±0.00a0.95±0.12a1.03±0.05a1.06±0.21a1.12±0.15a1.12±0.04a1.00±0.04a1.14±0.09a1.03±0.01a1.10±0.08aMet0.23±0.01c0.30±0.22c0.31±0.14c0.46±0.08b0.45±0.08b0.82±0.05a0.74±0.07a0.66±0.10a0.30±0.01c0.68±0.17aIle0.80±0.00a0.96±0.28a1.08±0.13a1.19±0.31a1.18±0.24a1.15±0.15a1.08±0.18a1.11±0.15a0.97±0.01a1.05±0.14aLeu1.64±0.00c1.79±0.21bc2.06±0.11ab2.15±0.26ab2.23±0.19a2.27±0.13a2.03±0.14ab2.20±0.12a1.98±0.02bc2.06±0.11abPhe0.96±0.00e1.31±0.19d1.71±0.08bc2.06±0.18a1.92±0.18ab1.81±0.17ab1.77±0.19ab1.45±0.11cd1.46±0.03cd1.35±0.09dLys1.86±0.01d2.26±0.12c2.65±0.03ab2.79±0.07a2.81±0.05a2.83±0.09a2.60±0.09ab2.67±0.05ab2.46±0.04bc2.48±0.06bcE7.39±0.02e8.47±0.47d9.89±0.55c10.70±0.31a10.80±0.26a11.19±0.64a10.21±0.43b10.39±0.48bc9.27±0.21c9.82±0.38c非必需氨基酸Asp2.66±0.01a0.81±0.01e0.97±0.01c0.91±0.04d1.00±0.01c1.08±0.00b0.91±0.00d1.06±0.01b0.99±0.01c1.01±0.01cSer2.13±0.01e2.14±0.02e2.51±0.03c2.36±0.09d2.56±0.01bc2.82±0.01a2.46±0.01cd2.90±0.03a2.56±0.02bc2.66±0.01bGlu3.42±0.01a0.43±0.01b0.42±0.01bc0.42±0.00cd0.43±0.00bc0.42±0.00bc0.40±0.00e0.40±0.00de0.42±0.00bc0.41±0.00deGly1.36±0.01a0.22±0.00e0.26±0.00c0.25±0.00d0.27±0.00c0.30±0.00b0.25±0.00d0.29±0.00b0.27±0.00c0.27±0.00cAla1.21±0.01a0.20±0.00e0.23±0.00c0.22±0.01d0.24±0.00c0.26±0.00b0.22±0.00d0.26±0.00b0.24±0.00c0.24±0.00cCys0.05±0.01a0.10±0.08a0.07±0.01a0.15±0.08a0.15±0.08a0.14±0.01a0.15±0.00a0.17±0.06a0.08±0.01a0.14±0.04aTyr0.89±0.01c1.23±0.24bc1.36±0.09ab1.57±0.20a1.53±0.08a1.45±0.06ab1.38±0.16ab1.37±0.13ab1.18±0.03bc1.25±0.11bcHis0.56±0.01f1.25±0.08cd1.39±0.01bc1.69±0.02a1.51±0.03b1.32±0.10c1.31±0.11c1.15±0.06de1.09±0.03e1.12±0.04eArg1.93±0.01e1.80±0.01f2.03±0.02cd1.98±0.08de2.20±0.01b2.35±0.01a1.92±0.01e2.31±0.03a2.06±0.01c2.14±0.02bN14.21±0.02a8.19±0.34e9.25±0.17cd9.53±0.22b9.89±0.32bc10.15±0.50bc9.00±0.24d9.92±0.18b8.90±0.11d9.25±0.23cdE/N0.52±0.12b1.03±0.15a1.07±0.03a1.12±0.11a1.09±0.06a1.10±0.07a1.13±0.08a1.05±0.07a1.04±0.06a1.06±0.05a
注:表中E表示必需氨基酸总含量;N表示非必需氨基酸总含量;E/N表示必需氨基酸和非必需氨基酸总含量比值。表中标注不同字母的值存在差异显著(P<0.05)。
不同条件脉冲电场处理后虾肉样品中必需氨基酸含量均增加,尤其是在15 kV/cm电场强度下处理10 min时,总必需氨基酸含量显著提高至11.73 g/100 g(P<0.05)。赖氨酸是衡量优质蛋白的一种重要氨基酸,可观的是经PEF处理后,赖氨酸含量增加,在15 kV/cm电场强度下作用5 min时显著提高了53.51%(P<0.05)。与未处理组相比较,经脉冲电场处理后虾肉的非必需氨基酸中天冬氨酸、谷氨酸、甘氨酸以及丙氨酸含量降低,其他氨基酸含量显著提高。其次,脉冲电场对虾肉样品蛋白质的影响可以通过氨基酸E/N比进一步分析。从表1中计算结果来看,PEF处理使虾肉氨基酸E/N比值均显著增加,说明脉冲电场处理可以提高虾肉的蛋白品质,增加其氨基酸的利用率。这可能是因为脉冲电场处理能够改变蛋白质的二级及三级结构,使蛋白质发生裂解,从而提高蛋白质的溶解性和消化率等[28]。
2.8 总可溶性蛋白质含量和介电特性
如图8-a所示,测定了样品处理前后的总可溶性蛋白质含量。经PEF处理的样品中可溶性蛋白质含量显著降低2.50%~12.35%。其中,在20 kV/cm电场强度下处理10 min后蛋白质含量达到最低水平(130.31 mg/g),可能是PEF处理过程中电场的冲击作用使蛋白质降解成小肽或氨基酸,导致蛋白质含量降低[29]。其次,高压脉冲电场提高蛋白质含量原因可能是脉冲电场使蛋白质变性,一些不可溶性蛋白转化成可溶性蛋白,提高了蛋白质溶解度[13],从而使蛋白质含量呈现上升的趋势,但值仍低于未处理样品。
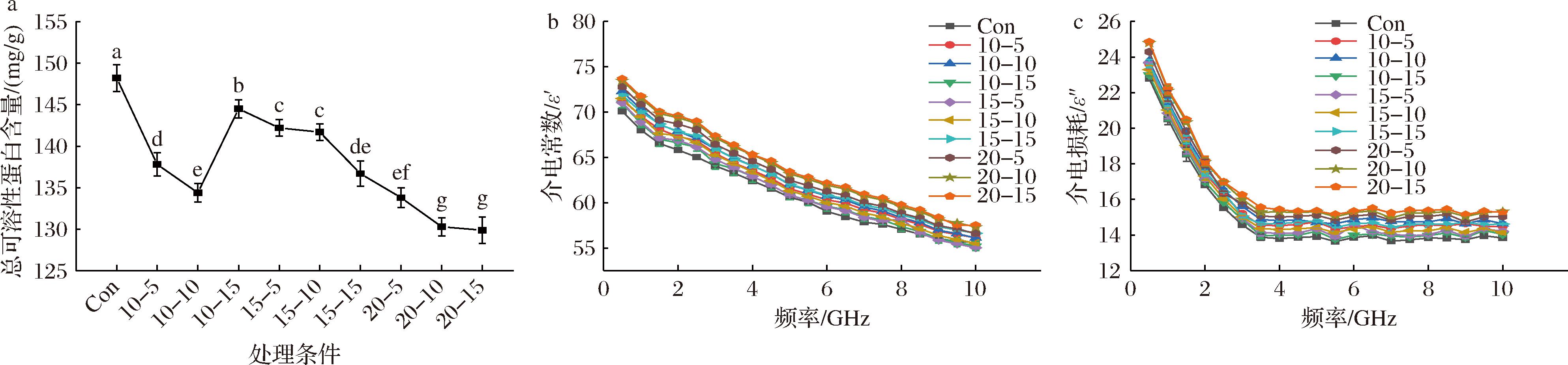
a-总可溶性蛋白含量变化;b-不同条件条件处理前后虾肉介电常数的变化;c-不同条件处理前后虾肉介电损耗的变化
图8 不同条件高压脉冲电场处理对虾肉中总可溶性蛋白含量和介电特性的影响
Fig.8 Effects of high intensity pulsed electric field on total soluble protein content and dielectric properties of shrimp meat under different conditions
蛋白质是具有导电性和介电常数特性的动态分子。样品经PEF处理后,在1~10 GHz范围内测量其介电常数和介电损耗,如图8-b和图8-c所示,介电常数及介电损耗在10 kV/cm电场强度作用下,其随处理时间的增加呈现出先上升后下降的趋势,在15 kV/cm和20 kV/cm条件下分别处理5、10、15 min,介电常数和介电损耗均逐渐上升。首先,介电常数的增加与降低可能与可溶性蛋白质含量变化相关,随着可溶性蛋白质含量的降低,介电常数逐渐增加,且介电损耗与介电常数变化趋势相同。蛋白质含量下降会增加水的流动性,导致介电常数增加,这与GUO等[30]在探究大豆分离蛋白分散体的介电性能时研究结果相似。其次,食物是复杂的多组分系统,当受到外部电场时,极性或带电粒子的电化学特性可以产生偶极振动、重新定向、平移和旋转,沿着电场的氢键被增强,而与电场正交的其他氢键被削弱,这会导致介电常数降低和水的表面张力增加[3]。因此,PEF处理可能会改变蛋白质结构或破坏其肽链,进一步影响其生物活性的变化。
3 结论
本研究探讨了不同条件高压脉冲电场处理对中国对虾抗氧化活性和蛋白质特性的影响。根据对PEF处理前后虾肉的总抗氧化能力、总还原能力、DPPH自由基清除能力以及亚铁离子螯合能力的测定可知,PEF处理可提高虾肉的抗氧化活性,这与所含虾青素含量、游离氨基酸含量,尤其是具有抗氧化性氨基酸和还原性氨基酸含量变化显著相关。脉冲电场处理后,虾青素含量和游离氨基酸含量随处理时间的增加逐渐上升,且虾青素含量最高增加了1.61倍。此外,脉冲电场处理后,虾肉中总必需氨基酸含量与非必需氨基酸含量比值显著增加,且高压脉冲电场产生的瞬间冲击作用可导致虾肉中可溶性蛋白质含量下降,增加水的流动性,使其介电常数增加。蛋白质是具有导电性和介电常数特性的动态分子,可见PEF处理时产生的电化学效应一定程度上改变了虾肉的蛋白质特性。综上所述,高压脉冲电场能够有效增强虾肉抗氧化活性,提高蛋白质品质和氨基酸利用率,为中国对虾的加工方式和生物活性增强提供了新思路,可提高渔业资源利用水平。
[1] 李洋. 中国对虾抗WSSV相关RNA的生物信息学研究[D].济南:山东大学, 2023.
LI Y.Bioinformatics studies on anti-WSSV-related RNA of Fenneropenaeus chinensis[D].Jinan:Shandong University, 2023.
[2] LIU Z Y, LIU Q M, ZHANG D, et al.Comparison of the proximate composition and nutritional profile of byproducts and edible parts of five species of shrimp[J].Foods, 2021, 10(11):2603.
[3] WANG Q J, LI Y F, SUN D W, et al.Enhancing food processing by pulsed and high voltage electric fields:Principles and applications[J].Critical Reviews in Food Science and Nutrition, 2018, 58(13):2285-2298.
[4] ZHU N, ZHU Y, YU N, et al.Evaluation of microbial, physicochemical parameters and flavor of blueberry juice after microchip-pulsed electric field[J].Food Chemistry, 2019, 274:146-155.
[5] BARBHUIYA R I, SINGHA P, SINGH S K.A comprehensive review on impact of non-thermal processing on the structural changes of food components[J].Food Research International, 2021, 149:110647.
[6] NIU D B, REN E F, LI J, et al.Effects of pulsed electric field-assisted treatment on the extraction, antioxidant activity and structure of naringin[J].Separation and Purification Technology, 2021, 265:118480.
[7] OMS-OLIU G, ODRIOZOLA-SERRANO I, SOLIVA-FORTUNY R, et al.Effects of high-intensity pulsed electric field processing conditions on lycopene, vitamin C and antioxidant capacity of watermelon juice[J].Food Chemistry, 2009, 115(4):1312-1319.
[8] 李迎秋, 陈正行.高压脉冲电场对大豆分离蛋白疏水性和巯基含量的影响[J].食品科学, 2006, 27(5):40-43.
LI Y Q, CHEN Z X.Effects of high power pulsed electric field on hydrophobicity and sulfhydry groups content of soybean protein isolated[J].Food Science, 2006, 27(5):40-43.
[9] DONG M, TIAN H X, XU Y J, et al.Effects of pulsed electric fields on the conformation and gelation properties of myofibrillar proteins isolated from pale, soft, exudative (PSE)-like chicken breast meat:A molecular dynamics study[J].Food Chemistry, 2021, 342:128306.
[10] DONG X, WANG J, RAGHAVAN V.Effects of high-intensity ultrasound processing on the physiochemical and allergenic properties of shrimp[J].Innovative Food Science &Emerging Technologies, 2020, 65:102441.
[11] 林晓彤, 李蒙, 张玉苍.虾壳蛋白质的提取、美拉德反应改性及抗氧化活性研究[J].食品与发酵工业, 2023, 49(7):218-224.
LIN X T, LI M, ZHANG Y C.Study on extraction and modification by Maillard reaction and antioxidant activity of shrimp shell protein[J].Food and Fermentation Industries, 2023, 49(7):218-224.
[12] 张芷芸, 姜启兴, 高沛, 等.热加工方式对斑点叉尾鮰鱼肉体外消化产物抗氧化活性的影响[J].食品与发酵工业, 2023, 49(11):163-169.
ZHANG Z Y, JIANG Q X, GAO P, et al.Effects of thermal treatment on antioxidant activity of in vitro digestion products of channel catfish (Ietalurus punetaus)[J].Food and Fermentation Industries, 2023, 49(11):163-169.
[13] 张意锋. 高静压对鱿鱼品质及原肌球蛋白、血蓝蛋白致敏性的影响研究[D].上海:上海交通大学, 2017.
ZHANG Y F.Effect of high hydrostatic pressure on squid (Todarodes pacificus) quality, and allergenicity of squid tropomyosin and hemocyanin[D].Shanghai:Shanghai Jiao Tong University, 2017.
[14] 刘增萌, 杨斌, 李良, 等.虹鳟鱼肌肉组织中虾青素含量的高效液相色谱检测方法的建立[J].动物医学进展, 2020, 41(5):50-55.
LIU Z M, YANG B, LI L, et al.Establishment of HPLC method for the determination of astaxanthin in muscle tissue of Oncorhynchus mykiss[J].Progress in Veterinary Medicine, 2020, 41(5):50-55.
[15] XU Y Y, XIANG P, QIU W Q, et al.Dielectric properties of the Maillard reaction solution formed between enzymatic hydrolysate of Antarctic krill and glucose under microwave heating[J].LWT, 2022, 161:113355.
[16] CARBONELL-CAPELLA J M, BUNIOWSKA M, BARBA F J, et al.Changes of antioxidant compounds in a fruit juice-Stevia rebaudiana blend processed by pulsed electric technologies and ultrasound[J].Food and Bioprocess Technology, 2016, 9(7):1159-1168.
[17] LI X, FARID M.A review on recent development in non-conventional food sterilization technologies[J].Journal of Food Engineering, 2016, 182:33-45.
[18] ZHU C, CHEN L H, ZENG X Y, et al.Effects of ultra high pressure-magnetic field treatment on protein properties and quality characteristics of stored shrimp (Litopenaeus vannamei)[J].LWT, 2022, 170:114070.
[19] OHSHIMA T, TAMURA T, SATO M.Influence of pulsed electric field on various enzyme activities[J].Journal of Electrostatics, 2007, 65(3):156-161.
[20] 李南, 李蛟龙, 李鹏鹏, 等.加工对肉类蛋白质氧化及肉品品质影响的研究进展[J].食品工业科技, 2024, 45(15):392-399.
LI N, LI J L, LI P P, et al.Research progress on the effects of processing conditions on the meat protein oxidation and meat quality[J].Science and Technology of Food Industry, 2024, 45(15):392-399.
[21] 徐彩娜, 殷涌光, 王二雷, 等.卵黄高磷蛋白及其磷酸肽稳定性和抗氧化性[J].吉林大学学报(工学版), 2013, 43(2):544-549.
XU C N, YIN Y G, WANG E L, et al.Stability and anti-oxidative abilities of phosvitin and phosvitin phosphopeptides[J].Journal of Jilin University (Engineering and Technology Edition), 2013, 43(2):544-549.
[22] 陈晋明, 王世平, 陈敏.反相高效液相色谱法检测虾青素[J].化学分析计量, 2006, 15(2):27-29.
CHEN J M, WANG S P, CHEN M.Determination of astaxanthin by reversed-phase high performance liquid chromatography[J].Chemical Analysis and Meterage, 2006, 15(2):27-29.
[23] 江嘉琦, 张旭飞, 吉宏武, 等.常压油炸与空气油炸对凡纳滨对虾中虾青素含量及抗氧化活性的影响[J].食品科学, 2022, 43(13):33-39.
JIANG J Q, ZHANG X F, JI H W, et al.Effects of deep frying and air frying on astaxanthin content and antioxidant activity of litopenaeus vannamei[J].Food Science, 2022, 43(13):33-39.
[24] 赵英源, 舒澳, 张胜梦, 等.高效液相色谱法分析鉴定虾青素全反式、9-顺式、13-顺式几何异构体[J].中国海洋药物, 2022, 41(5):73-81.
ZHAO Y Y, SHU A, ZHANG S M, et al.Analysis and identification of all-trans, 9-Cis and 13-Cis geometric isomers of astaxanthin by HPLC[J].Chinese Journal of Marine Drugs, 2022, 41(5):73-81.
[25] YANG C, ZHANG H, LIU R H, et al.Bioaccessibility, cellular uptake, and transport of astaxanthin isomers and their antioxidative effects in human intestinal epithelial Caco-2 cells[J].Journal of Agricultural and Food Chemistry, 2017, 65(47):10223-10232.
[26] 张铁华, 殷涌光.高压脉冲电场对食品中生物大分子的影响[J].食品科技, 2007, 32(7):16-20.
ZHANG T H, YIN Y G.Effect of high-intensity pulsed electric fields(PEF) on food biomacromolecule[J].Food Science and Technology, 2007, 32(7):16-20.
[27] 张鹰, 曾新安, 朱思明.高强脉冲电场处理对脱脂乳游离氨基酸和乳糖的影响研究[J].食品科技, 2004, 29(3):12-13;19.
ZHANG Y, ZENG X A, ZHU S M.Study on the effects of high intensity pulsed electric fields on the contents of free amino acids and lactose in skim milk[J].Food Science and Technology, 2004, 29(3):12-13;19.
[28] LI Y L, ZHANG S Y, JIANG P F, et al.Exploration of structure-activity relationship between IgG1 and IgE binding ability and spatial conformation in ovomucoid with pulsed electric field treatment[J].LWT, 2021, 141:110891.
[29] ZHANG Z Y, YANG Y L, ZHOU P, et al.Effects of high pressure modification on conformation and gelation properties of myofibrillar protein[J].Food Chemistry, 2017, 217:678-686.
[30] GUO C F, WANG X J, WANG Y Y.Dielectric properties of soy protein isolate dispersion and its temperature profile during radio frequency heating[J].Journal of Food Processing and Preservation, 2018, 42(7):e13659.