酵母在葡萄发酵过程中会产生多种香气化合物,决定着最终葡萄酒的品质[1]。商业酿酒酵母是葡萄酒生产的首选,以确保葡萄酒质量的稳定性和标准化的发酵过程[2]。然而,使用有限数量的商业酵母可能会削弱不同地区葡萄酒的区域性、独特性和香气复杂性[3]。因此,非酿酒酵母(non-Saccharomyces yeasts)在葡萄酒酿造中的作用也越来越受到重视[4-5],挖掘具有独特区域特征的本土非酿酒酵母也备受关注[6]。大量研究表明,非酿酒酵母菌株能高产香气化合物(酯类、高级醇和挥发酸等),使葡萄酒具有果香、花香或辛辣的香气[7-8],改善葡萄酒颜色和口感,提升葡萄酒的品质[9]。例如LAI等[10]使用酿酒酵母Gr112、葡萄汁有孢汉逊酵母pi235和克鲁维毕赤酵母pe114混合发酵,增强了葡萄酒中花香、红色果香和热带果香。LIU等[11]发现库氏毕赤酵母CCTCC2017759和酿酒酵母7VA混合发酵显著提高了黄烷-3-醇的含量,还增加了苯乙醇、异戊醇和乙酯的含量,增强了葡萄酒的玫瑰味和果味。ŽENI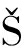 OV
OV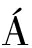 等[12]用美极梅奇酵母发酵的葡萄酒中2-苯乙醇和琥珀酸二乙酯的浓度增加,乙醛的浓度降低。王静尧等[13]将东方伊萨酵母F10酿酒酵母S15混合发酵提高了具有玫瑰香、蜂蜜香、梨香的癸酸乙酯和具有花香、果香的月桂酸乙酯含量。
等[12]用美极梅奇酵母发酵的葡萄酒中2-苯乙醇和琥珀酸二乙酯的浓度增加,乙醛的浓度降低。王静尧等[13]将东方伊萨酵母F10酿酒酵母S15混合发酵提高了具有玫瑰香、蜂蜜香、梨香的癸酸乙酯和具有花香、果香的月桂酸乙酯含量。
我国非酿酒酵母资源丰富,但目前国内葡萄酒生产企业使用的非酿酒酵母大多由国外进口。这种生产方式不但会增加企业的生产成本,还会严重影响我国葡萄酒酵母资源的多样性,降低葡萄酒的产区特色。为了获得本土的优良非酿酒酵母菌株,本研究以宁夏贺兰山东麓银川、玉泉营、青铜峡3个子产区中分离得到的112株非酿酒酵母为研究对象,通过葡萄糖、乙醇、pH、SO2等耐受性筛选,获得数株耐受性好的本土非酿酒酵母。以赤霞珠葡萄为原料,利用筛选出的优良非酿酒酵母进行发酵试验,对酿造的葡萄酒进行基础理化指标测定、感官评价和挥发性成分测定,得到具有良好发酵特性且能够酿造出具有产区特色风味葡萄酒的本土非酿酒酵母菌株。
1 材料与方法
1.1 材料
1.1.1 菌种与葡萄原料
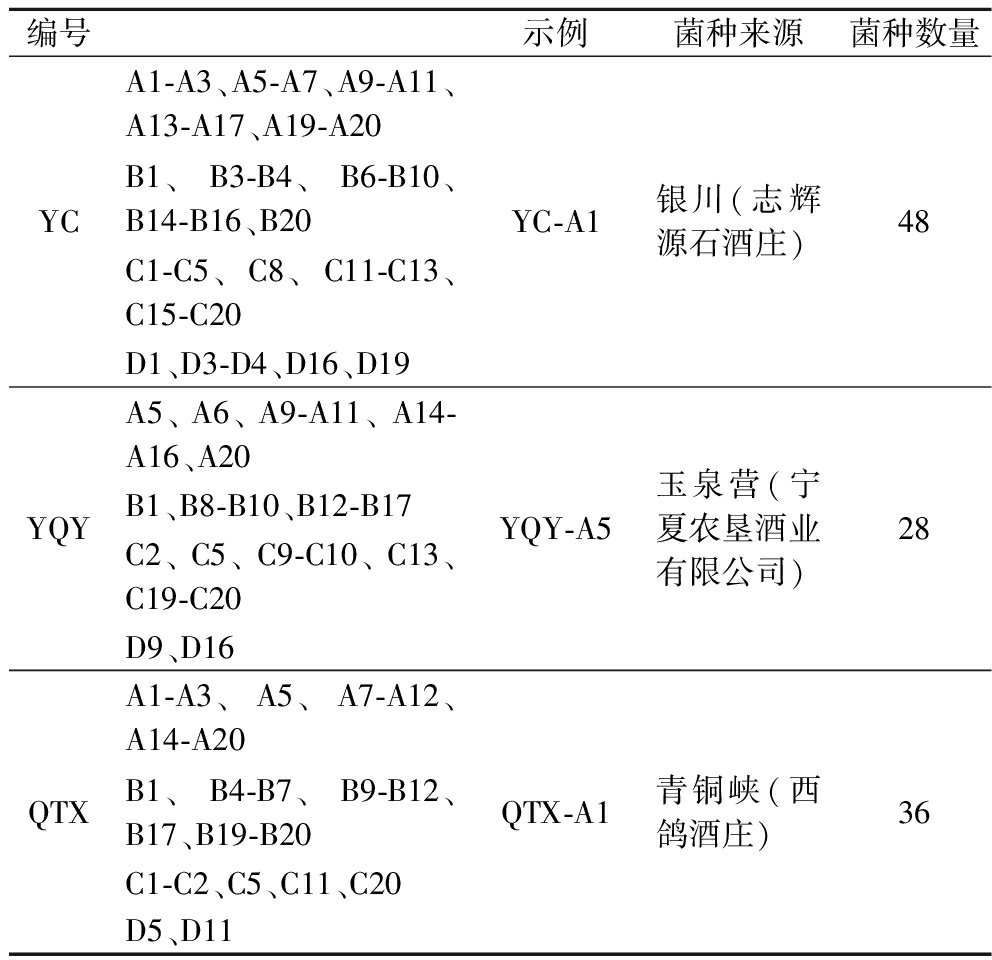
实验所用菌种分离自宁夏贺兰山东麓玉泉营、青铜峡、银川3个子产区赤霞珠自然发酵葡萄酒,现保藏在-80 ℃冰箱中。本实验所用的112株本土非酿酒酵母,包括有孢汉逊酵母(Hanseniaspora)80株、梅奇酵母(Metschnikowia)17株、泽普林假丝酵母(Starmerella bacillaris)15株,详见表1。
表1 菌种来源及编号
Table 1 Source and number of strains
编号示例菌种来源菌种数量YCA1-A3、A5-A7、A9-A11、A13-A17、A19-A20B1、B3-B4、B6-B10、B14-B16、B20C1-C5、C8、C11-C13、C15-C20D1、D3-D4、D16、D19YC-A1银川(志辉源石酒庄)48YQYA5、A6、A9-A11、A14-A16、A20B1、B8-B10、B12-B17C2、C5、C9-C10、C13、C19-C20D9、D16YQY-A5玉泉营(宁夏农垦酒业有限公司)28QTXA1-A3、A5、A7-A12、A14-A20B1、B4-B7、B9-B12、B17、B19-B20C1-C2、C5、C11、C20D5、D11QTX-A1青铜峡(西鸽酒庄) 36
商业酿酒酵母:XR,诺盟公司;F33,LAFFORT公司;CECA,安琪酵母股份有限公司。
葡萄原料:赤霞珠葡萄(2023年10月4日采摘于宁夏青铜峡西鸽酒庄)。除梗破碎后的葡萄汁卫生状况良好,还原糖为251.3 g/L,可滴定酸(以酒石酸计)为8.7 g/L,pH值为3.01。
1.1.2 培养基
YPD液体培养基:蛋白胨20.0 g,酵母浸粉10.0 g,葡萄糖20.0 g,加热溶解于1 L蒸馏水中,121 ℃高压灭菌15 min。
YPD固体培养基:蛋白胨20.0 g,酵母浸粉10.0 g,葡萄糖20.0 g,琼脂20.0 g,加热溶解于1 L蒸馏水中,121 ℃高压灭菌15 min。
蛋白胨、酵母浸粉、琼脂,青岛海博生物技术有限公司。
1.1.3 主要试剂和仪器
0.1 mol/L柠檬酸钠缓冲液:称取29.0 g柠檬酸钠,用蒸馏水定容至1 L。
柠檬酸钠、无水乙醇均为分析纯,上海广诺化学科技有限公司;葡萄糖、酒石酸、NaCl、NaOH、次甲基蓝、CuSO4等均为分析纯,天津市大茂化学试剂厂。
生化培养箱,常州诺基仪器有限公司;紫外可见分光光度计,北京普析公司;酶标仪,赛默飞世尔仪器有限公司;全自动葡萄酒分析仪,Biosystems公司;7890 B气相色谱-7000 D质谱仪、DB-Wax色谱柱(60 m×250 μm, 0.25 μm),美国Agilent公司。
1.2 实验方法
1.2.1 非酿酒酵母种子液的制备
将-80 ℃冰箱中保存的本土非酿酒酵母在YPD固体培养基上划线,28 ℃条件下倒置培养3~4 d,挑取单菌落放入YPD液体培养基中,在28 ℃、180 r/min条件下培养8~10 h后所得菌液作为该非酿酒酵母种子液。
1.2.2 非酿酒酵母耐受性筛选
以YPD固体培养基为基础培养基,分别添加不同质量浓度的葡萄糖(150、200、250、300、350、400、450、500 g/L),配制成高糖固体筛选培养基。用0.1 mol/L柠檬酸钠缓冲液调种子液OD600值为0.5(标记为样品100),梯度稀释制成10-4~10-1共4个浓度梯度的稀释样。分别取2.5 μL菌液点板于高糖固体筛选培养基,28 ℃静置培养2 d,观察菌斑生长情况。
以YPD液体培养基为基础培养基,分别添加不同体积分数(5%、7%、9%、11%、13%)的无水乙醇和不同质量浓度的SO2(以偏重亚硫酸钾添加)(50、100、150、200、250 mg/L),配制乙醇和SO2筛选培养基;使用酒石酸调节YPD液体培养基的pH(1.0、1.5、2.0、2.5、3.0),配制pH筛选培养基。用0.1 mol/L柠檬酸钠缓冲液将种子液OD600值调整为0.5(标记为菌液1),取250 μL菌液1加入到含有5 mL上述不同筛选培养基的离心管中,于28 ℃、180 r/min条件下振荡培养24 h(标记为菌液2)。分别取1 mL菌液2(标记为样品100),梯度稀释制成10-4~10-1共4个浓度梯度的稀释样。分别取2.5 μL菌液点板于YPD固体培养基,28 ℃静置培养2 d,观察菌斑生长情况。
1.2.3 非酿酒酵母生长曲线测定
用0.1 mol/L柠檬酸钠缓冲液调种子液OD600值为0.5,移取1 mL种子液到50 mL YPD液体培养基中,于28 ℃、180 r/min振荡培养,每隔2 h取样200 μL,用酶标仪测其OD600值,以培养时间为横坐标,OD600值为纵坐标,绘制生长曲线。
1.2.4 葡萄醪发酵试验
将保藏的酿酒酵母菌株解冻后在YPD固体培养基上划线,28 ℃条件下培养3 d。挑取单菌落于YPD液体培养基中,在28 ℃、180 r/min条件下培养10 h,在25 ℃、8 000 r/min条件下离心5 min收集菌体,用无菌水洗涤2次后,血细胞计数板计数,以1×106 cells/mL的接种量接入发酵罐中。
挑选果粒饱满、无病害的赤霞珠葡萄果实,除梗破碎后,按装液量90%分装于5 L玻璃发酵罐,加入60 mg/L偏重亚硫酸钾,搅拌后加入30 mg/L的果胶酶,常温浸渍24 h,接入相应酵母进行单菌发酵(发酵过程中检测比重和温度),待发酵液比重为0.992~0.996视酒精发酵结束,皮渣分离后加入60 mg/L偏重亚硫酸钾,静置澄清1个月后分离沉淀并装瓶,同时取样进行理化指标等测定。
1.2.5 葡萄酒理化指标测定
参照GB/T 15038—2006《葡萄酒、果酒通用分析方法(含第1号修改单)》测定酒精度、可滴定酸(g/L,以酒石酸计)、挥发酸(g/L,以乙酸计)、残糖、总SO2、游离SO2、甘油。使用pH计测定pH。理化指标测定重复3次计算平均值。
1.2.6 葡萄酒感官评价
参考李毅丽等[14]的方法,感官评价由18名具有丰富葡萄酒感官评价经验的宁夏大学师生(9男9女)组成。在(18±2) ℃的ISO标准品酒酒杯倒入约30 mL的葡萄酒样品。采用10分制评价葡萄酒感官属性强度,包括外观(颜色、澄清度)、香气(浓郁度、复杂度、协调性)、口感(香气浓郁度、酸甜平衡感、涩感、余味)和整体性。采用5分制评价葡萄酒香气描述强度,包括花香、绿色果香、红色果香、黑色果香、热带果香、核果类香气、柑橘类、草本味、香辛料味、坚果类香气、不良风味。感官评价结果为所有成员评价得分的平均值,并绘制雷达图。
1.2.7 葡萄酒挥发性物质测定
利用HS-SPME-GC-MS技术,使用7890 B气相色谱-7000 D质谱仪、DB-Wax色谱柱(60 m×250 μm, 0.25 μm),参照李亚军等[15]的方法进行测定。将1.5 g NaCl、5 mL酒样、10 μL 4-甲基-2-戊醇(1.008 3 g/L)依次加入顶空瓶中,250 r/min,40 ℃萃取30 min。色谱条件:进样口温度230 ℃,起始柱温50 ℃,恒温1 min,以3 ℃/min升到220 ℃,保持5 min。载气为高纯氦气(纯度≥99.999%),流速1 mL/min,不分流进样。质谱条件:传输线温度235 ℃,离子源温度230 ℃,电子能量70 eV。质量扫描范围m/z 29~350。将质谱图通过NIST检索,根据C8~C20烷烃混合标准品的保留时间进行定性分析。使用标准曲线对香气成分定量分析并对其香气活度值(odor activity value,OAV)进行计算。
1.2.8 数据分析
使用Office 2019、SPSS 26软件进行数据统计与分析,使用单因素ANOVA检验进行显著性分析;使用Origin 2022软件进行绘图。
2 结果与分析
2.1 非酿酒酵母耐受性筛选
由表2葡萄糖耐受性结果可知,QTX-A17葡萄糖耐受性为350 g/L,这与商业酿酒酵母CECA、XR、F33耐受性一致;QTX-A19葡萄糖耐受性为400 g/L;YC-B3等67株菌葡萄糖耐受性为450 g/L;而YC-A3等43株菌在葡萄糖质量浓度500 g/L时仍未受到胁迫作用,菌株生长旺盛,菌落明显。部分菌株葡萄糖耐受性生长情况见电子版增强出版附图1(https://doi.org/10.13995/j.cnki.11-1802/ts.038563)。因此筛选出111株可以耐受葡萄糖质量浓度400 g/L及以上的本土非酿酒酵母进行下一步乙醇耐受性试验。
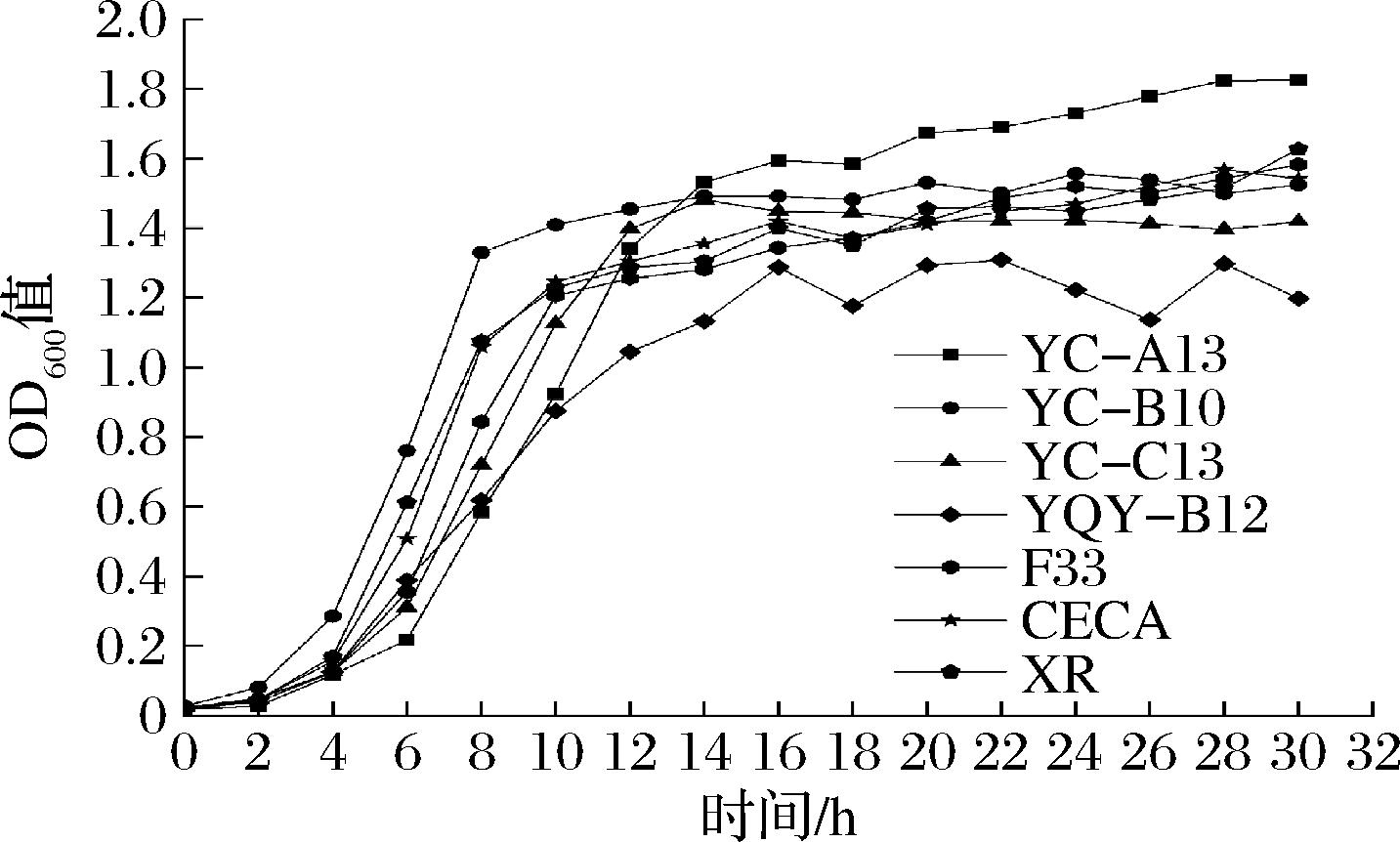
图1 不同酵母菌株的生长曲线
Fig.1 Growth curves of different yeast strains
表2 不同酵母菌株高糖耐受性结果
Table 2 Results of high glucose tolerance of different yeast strains

菌株编号数量葡萄糖质量浓度/(g/L)150200250300350400450500YC-A3、YC-A19、YC-B14、YQY-A16、YQY-A20、YC-A1、YC-A2、YC-A5、YC-A6、YC-A7、YC-A9、YC-A10、YC-A11、YC-A14、YC-A15、YC-A16、YC-A17、YC-B1、YC-B6、YC-B9、YC-B16、YC-C13、QTX-A2、QTX-A18、QTX-B6、QTX-B9、QTX-B11、QTX-B20、QTX-C1、QTX-C2、QTX-C5、QTX-C11、YQY-A14、YQY-A15、YC-A13、QTX-A3、QTX-A5、QTX-A20、YQY-B1、YQY-B8、YQY-B9、YC-A20、QTX-B143++++++++YC-B3、YC-B4、YC-B7、YC-B8、YC-C1、YC-C2、YC-C5、YC-C8、YC-C11、QTX-A10、QTX-A14、QTX-A16、QTX-C20、QTX-D5、QTX-D11、YQY-A9、YQY-A10、YQY-A11、YQY-B10、YQY-B13、YQY-B14、YQY-B15、YQY-C9、YC-B15、YC-B20、YC-C3、YC-C4、YC-C12、YC-C17、YC-D3、YC-D16、YC-D19、QTX-A1、QTX-A7、QTX-A8、QTX-A9、QTX-A11、QTX-A12、QTX-A15、QTX-B4、QTX-B5、QTX-B7、QTX-B10、QTX-B12、QTX-B17、QTX-B19、YQY-A6、YQY-B12、YQY-B16、YQY-B17、YQY-C2、YQY-C5、YQY-C10、YQY-C13、YQY-C19、YQY-C20、YQY-D9、YQY-D20、YC-C15、YC-C20、YC-D1、YQY-A5、YC-C18、YC-B10、YC-C16、YC-D4、YC-C1967+++++++-QTX-A191++++++--CECA、XR、F33、QTX-A174+++++---
注:“+”表示菌株在某特定浓度条件下能生长;“-”表示菌株在某特定浓度条件下不能存活(下同)。
由表3乙醇耐受性结果可知,YC-A9等16株菌乙醇耐受性为7%;YC-B20等44株菌乙醇耐受性为9%;YC-A3等33株菌乙醇耐受性为11%,这与商业酿酒酵母F33耐受性一致;而YC-B14等18株菌在乙醇含量13%时仍未受到胁迫作用,菌株生长旺盛,菌落明显,这与商业酿酒酵母XR、CECA耐受性一致。部分菌株乙醇耐受性生长情况见电子版增强出版附图2。因此筛选出51株可以耐受乙醇含量11%及以上的本土非酿酒酵母进行下一步pH耐受性试验。

a-感官属性强度评价;b-香气类型感官强度评价
图2 不同酵母发酵赤霞珠葡萄酒感官评价
Fig.2 Sensory evaluation of Cabernet Sauvignon wine fermented by different yeasts
注:*表示非酿酒酵母酒样的浓郁度显著高于酿酒酵母酒样。
表3 不同酵母菌株乙醇耐受性结果
Table 3 Results of ethanol tolerance of different yeast strains

菌株编号数量乙醇含量(体积分数)5%7%9%11%13%YC-B14、YC-C13、YC-B16、QTX-A10、QTX-A16、QTX-B11、YC-B10、YC-C16、YQY-A15、YQY-A20、YQY-B12、YQY-B14、QTX-A14、YC-A13、YQY-A16、QTX-A19、QTX-A20、QTX-A18、XR、CECA20+++++YC-A3、QTX-B6、QTX-B9、YC-A6、YC-B15、YQY-A10、YQY-B1、QTX-A2、QTX-A9、QTX-B1、QTX-B12、QTX-C11、YC-A1、YC-A5、YC-A10、YC-A11、YC-A16、YC-A17、YC-A19、YC-B6、YC-C2、YC-C20、YC-D3、YQY-A14、YQY-B10、YQY-B15、QTX-B7、QTX-C1、QTX-C20、QTX-D5、QTX-D11、YC-A14、QTX-B10、F3334++++-YC-B20、YQY-A5、QTX-B17、QTX-B19、QTX-B20、QTX-C2、YC-A2、YC-A7、YC-A15、YC-A20、YC-B1、YC-B3、YC-B7、YC-B9、YC-C4、YC-C12、YC-C15、YC-C19、YC-D1、YC-D4、YC-D19、YQY-A6、YQY-A9、YQY-A11、YQY-B8、YQY-B9、YQY-B13、YQY-B16、YQY-B17、YQY-C2、YQY-C5、YQY-C9、YQY-D9、YQY-D16、QTX-A1、QTX-A3、QTX-A7、QTX-A8、QTX-A11、QTX-A12、QTX-C5、YC-C1、YC-C18、YC-D1644+++--YC-A9、YC-B4、YC-C8、QTX-A15、QTX-A5、YC-B8、YC-C3、YC-C5、YC-C11、YC-C17、YQY-C10、YQY-C13、YQY-C19、YQY-C20、QTX-B4、QTX-B516++---
由表4 pH耐受性结果可知,QTX-A16等9株菌pH耐受性为2.0;这与商业酿酒酵母F33、CECA耐受性一致;YC-B14等20株菌pH耐受性为1.5,这与商业酿酒酵母XR耐受性一致;而YC-A3等22株菌在pH 1.0时仍未受到胁迫作用,菌株生长旺盛,菌落明显。部分菌株pH耐受性生长情况见电子版增强出版附图3。筛选出22株可以耐受pH 1.0及以上的本土非酿酒酵母进行下一步SO2耐受性试验。
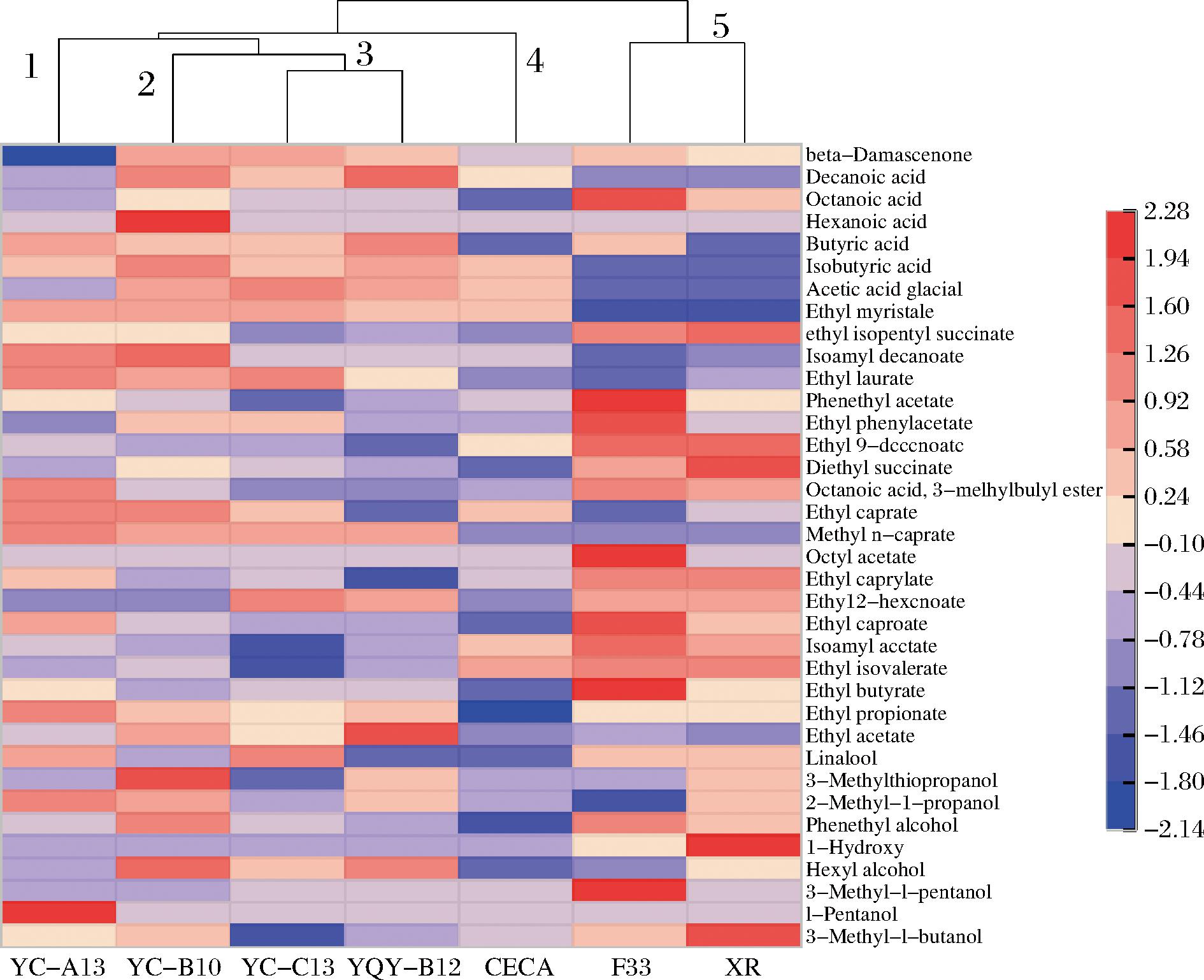
图3 不同酵母发酵赤霞珠葡萄酒挥发性成分聚类分析
Fig.3 Cluster analysis of volatile components in Cabernet Sauvignon wines fermented by different yeast
表4 不同酵母菌株pH耐受性结果
Table 4 Results of pH tolerance of different yeast strains

菌株编号数量pH1.01.52.02.53.0YC-A3、YC-A11、YC-B15、YC-D3、YQY-B1、YQY-B10、YC-B10、YC-C2、YC-C13、YQY-B12、QTX-A2、QTX-B1、QTX-B7、QTX-B9、QTX-C1、QTX-C20、YC-A5、YC-A6、YC-A10、YC-A13、YQY-A14、QTX-A922+++++YC-B14、YC-C16、YC-C20、YQY-B14、YQY-B15、YC-A14、YC-A16、YC-A19、YC-B16、QTX-A10、QTX-A14、QTX-B10、QTX-C11、YC-A1、YC-A17、YC-B6、YQY-A20、QTX-A18、QTX-A19、QTX-A20、XR21-++++QTX-A16、QTX-B6、QTX-B11、QTX-B12、QTX-D5、QTX-D11、YQY-A10、YQY-A15、YQY-A16、F33、CECA11--+++
由表5 SO2耐受性结果可知,YC-A3等22株菌在SO2质量浓度250 mg/L时仍未受到胁迫作用,生长旺盛,菌落明显。这与商业酿酒酵母F33、CECA、XR耐受性一致。部分菌株SO2耐受性生长情况见电子增强版附图4。
表5 不同酵母菌株SO2耐受性结果
Table 5 Results of SO2 tolerance of different yeast strains
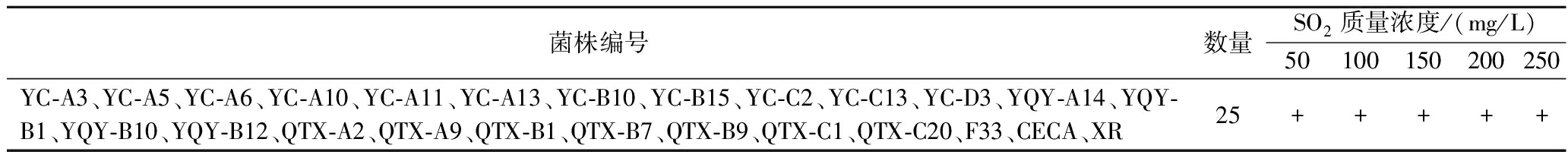
菌株编号数量SO2质量浓度/(mg/L)50100150200250YC-A3、YC-A5、YC-A6、YC-A10、YC-A11、YC-A13、YC-B10、YC-B15、YC-C2、YC-C13、YC-D3、YQY-A14、YQY-B1、YQY-B10、YQY-B12、QTX-A2、QTX-A9、QTX-B1、QTX-B7、QTX-B9、QTX-C1、QTX-C20、F33、CECA、XR25+++++
综合上述耐受性筛选结果,选择4株可以耐受葡萄糖质量浓度450 g/L、乙醇含量13%、pH 1.0、SO2质量浓度250 mg/L的本土非酿酒酵母进行发酵试验,分别为美极梅奇酵母YC-A13、葡萄汁有孢汉逊酵母YC-B10、YQY-B12和泽普林假丝酵母YC-C13。
2.2 生长曲线的测定
生长曲线能对微生物发酵和培养起到指导性意义。不同菌株的生长曲线如图1所示,4株非酿酒酵母和3株商业酿酒酵母在2 h时逐渐进入指数生长期,表明菌株对环境的适应性较强;在2~10 h完全进入指数生长期,表明菌株该阶段生长旺盛,繁殖速度快,其中,YC-B10在对数期的OD600值最高,其次是XR、CECA、F33,最后是YC-C13、YC-A13、YQY-B12;从10 h开始进入生长稳定期。总体来说,这4株非酿酒酵母和3株商业酿酒酵母的生长趋势基本保持一致。
2.3 葡萄酒感官评价
如图2-a所示,在颜色和透明度方面,各酒样之间的差异不显著,均澄清透亮有光泽。在香气浓郁度方面,4株非酿酒酵母发酵酒样显著高于酿酒酵母酒样;在复杂度和协调性方面,YC-A13、YC-B10、YC-C13发酵酒样明显高于商业酿酒酵母F33、CECA、XR酒样;YQY-B12发酵酒样与商业酿酒酵母酒样差异不大。在口感的大多数方面(香气浓郁度、酸甜平衡感、涩感、余味),YC-A13、YC-B10、YC-C13发酵酒样较高于YQY-B12和商业酿酒酵母F33、CECA、XR发酵酒样;在涩感方面,YC-B10、YQY-B12发酵酒样略高于其他菌株。从整体来看,对YC-C13的感官评分明显高于其他组别,YC-A13、YC-C13酒样与商业酿酒酵母酒样差异不大,而YQY-B12发酵酒样略低。如图2-b所示,YC-A13增加了葡萄酒花香;YQY-B12增加了绿色果香;在热带水果香气、红色果香等多方面,各组别之间差异不大。
2.4 葡萄酒理化指标分析
如表6所示,所有酒样理化指标均符合国家标准GB/T 19504—2008《地理标志产品 贺兰山东麓葡萄酒》。4株本土非酿酒酵母发酵酒样中,本土非酿酒酵母YC-C13发酵酒样残糖量最低,为9.75 g/L,高于商业酿酒酵母酒样,因此4株本土非酿酒酵母发酵酒样的酒精度显著低于商业酿酒酵母,可能是因为酿酒酵母比非酿酒酵母有较强的糖代谢能力造成的。总酸和挥发酸含量在9.27~10.05 g/L和0.42~0.70 g/L,菌种间总酸差异不显著,而适量的挥发酸会增加葡萄酒的香气,实验中发现本土非酿酒酵母发酵酒样的挥发酸含量显著高于商业酿酒酵母F33、XR。总SO2含量差异显著,商业酵母CECA发酵酒样的总SO2含量最高,其次是4株本土非酿酒酵母,含量最低的是商业酿酒酵母F33、XR。本土非酿酒酵母发酵的葡萄酒游离SO2含量在4.43~5.49 mg/L,显著低于商业酿酒酵母发酵酒样;所有酒样pH值在2.98~3.05,差异不显著。所有酒样甘油含量在6.75~10.37 g/L,差异显著,YC-C13菌株产生的甘油含量最高,可以增加葡萄酒口感的圆润度。
表6 不同酵母发酵赤霞珠葡萄酒样的基础理化指标
Table 6 Basic physicochemical indexes of Cabernet Sauvignon wine samples fermented by different yeast
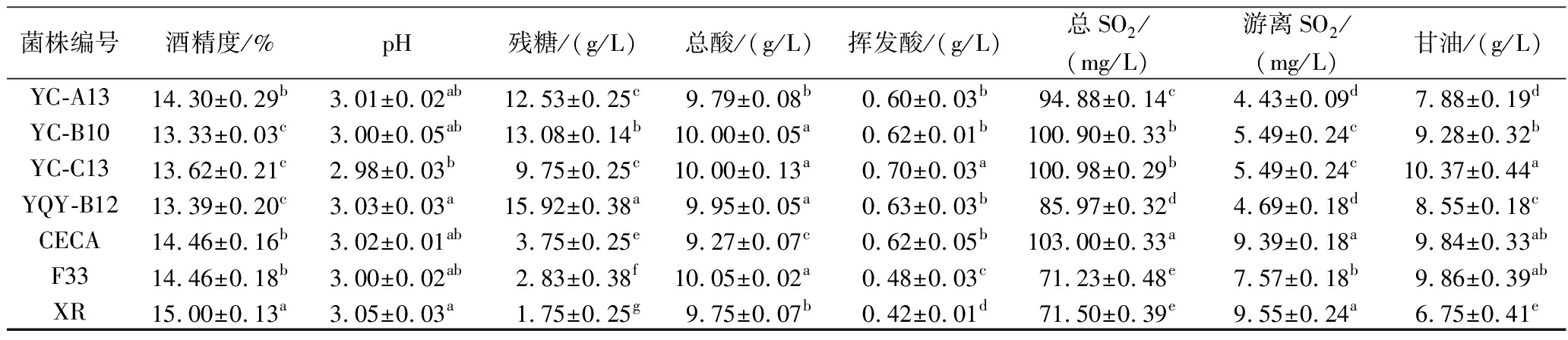
菌株编号酒精度/%pH残糖/(g/L)总酸/(g/L)挥发酸/(g/L)总SO2/(mg/L)游离SO2/(mg/L)甘油/(g/L)YC-A1314.30±0.29b3.01±0.02ab12.53±0.25c9.79±0.08b0.60±0.03b94.88±0.14c4.43±0.09d7.88±0.19dYC-B1013.33±0.03c3.00±0.05ab13.08±0.14b10.00±0.05a0.62±0.01b100.90±0.33b5.49±0.24c9.28±0.32bYC-C1313.62±0.21c2.98±0.03b9.75±0.25c10.00±0.13a0.70±0.03a100.98±0.29b5.49±0.24c10.37±0.44aYQY-B1213.39±0.20c3.03±0.03a15.92±0.38a9.95±0.05a0.63±0.03b85.97±0.32d4.69±0.18d8.55±0.18cCECA14.46±0.16b3.02±0.01ab3.75±0.25e9.27±0.07c0.62±0.05b103.00±0.33a9.39±0.18a9.84±0.33abF3314.46±0.18b3.00±0.02ab2.83±0.38f10.05±0.02a0.48±0.03c71.23±0.48e7.57±0.18b9.86±0.39abXR15.00±0.13a3.05±0.03a1.75±0.25g9.75±0.07b0.42±0.01d71.50±0.39e9.55±0.24a6.75±0.41e
注:不同小写字母代表不同显著差异(P<0.05)(下同)。
2.5 葡萄酒挥发性成分分析
所有葡萄酒样品经HS-SPME-GC-MS分析检测出78种香气物质(见电子版增强出版附表1),其中包括醇类物质15种、酯类物质39种、酮类物质5种、酸类物质6种及其他化合物13种。
醇类物质是酵母菌主要的代谢产物,7株菌发酵的葡萄酒中醇类物质总含量在500 929.9~680 578.4 μg/L,其中具有威士忌、香蕉香气的异戊醇含量最高,赋予良好的口感与香气。葡萄酒中酯类化合物大部分是酵母菌发酵的副产物,赋予葡萄酒独特的花香和果香,增加香气复杂性。所有酒样的酯类物质总含量在191 920.08~202 063.02 μg/L,其中大部分酯类物质的含量都高于其阈值,例如具有花香的十四酸乙酯、具有青苹果香气的正己酸乙酯、具有椰子香气的癸酸甲酯等。4株本土非酿酒酵母产生的酯类物质丰富程度均高于3株商业酿酒酵母,其中本土非酿酒酵母YQY-B12发酵的葡萄酒中酯类物质含量最高,其次是YC-B10,均高于3株商业酿酒酵母。非酿酒酵母YC-B10、YQY-B12酒样中检测到独有的己酸丁酯。乙酸是酸类物质中含量占比最高的挥发酸,其他酸类物质产生腐臭等不愉快气味的同时会增加葡萄酒香气的复杂性,例如具有奶酪香气的异丁酸、具有糖果香气的丁酸等。非酿酒酵母YC-A13、YC-C13酒样中检测出了其他菌株没有的2,3-丁二酮;非酿酒酵母YC-B10、YC-C13、YQY-B12酒样中检测出了其他菌株没有的香茅醇。
香气物质的OAV>1表明该物质在葡萄酒的香气中起决定性作用,而0.1
3 讨论与结论
酵母菌是影响葡萄酒品质最重要的因素,主要分为酿酒酵母和非酿酒酵母。酿酒酵母是主导葡萄酒酒精发酵的重要菌株,而非酿酒酵母具有某些酿酒酵母所不具备的酶学特征,可以促进大分子物质的分解及转化。此外,还有望改善葡萄酒的工艺过程及发酵品质,如提升发酵速率,降低乙醇含量,提高醛、酯、酚等风味成分的水平等[16]。本实验通过耐受性筛选,筛选出能耐受葡萄糖质量浓度400 g/L、乙醇含量13%、pH 1.0和SO2质量浓度250 mg/L的4株本土非酿酒酵母。王静尧[17]筛选出葡萄汁有孢汉逊酵母F3、异常汉逊酵母F12在pH 3.0和乙醇含量10%具有良好的耐受性。高娉娉[18]筛选出6株可以耐受350 g/L葡萄糖浓度、9%乙醇含量、pH 2.5和250 mg/L SO2的本土非酿酒酵母。马延琴等[19]筛选出非酿酒酵母CZ4葡萄糖耐受性达到200 g/L。董琦楠等[20]从本土非酿酒酵母菌中筛选出HU4能耐受乙醇含量6%、糖250 g/L及pH 2.75。GE等[21]筛选发现葡萄汁有孢汉逊酵母Z-2-5和LYQ-3可以耐受乙醇含量4%;Hanseniaspora Pseudoguilliermondii JCT1可以耐受乙醇含量8%。对比以上研究发现,大部分非酿酒酵母可以耐受SO2质量浓度250 mg/L,这与本试验筛选出的菌株耐受性一致。特别的是,王静尧[17]、高娉娉[18]、董琦楠等[20]筛选出的菌株能耐受葡萄糖质量浓度200~350 g/L、pH 2.5~3.0、乙醇含量4%~10%,而本实验筛选出的4株非酿酒酵母在葡萄糖质量浓度450 g/L、pH 1.0、乙醇含量13%的条件下依旧可以生长,说明这些菌株综合耐受性更强,在配合酿酒酵母混合发酵时不易受到环境的胁迫,从而在提高葡萄酒香气丰富度方面有着巨大的潜力。
本实验发现,非酿酒酵母YC-A13、YC-B10、YC-C13酒样中癸酸乙酯的含量均高于商业酿酒酵母。李红玉等[22]研究发现,将葡萄汁有孢汉逊酵母与安琪酿酒酵母混菌发酵使癸酸乙酯的含量增加,使脂肪香气大幅增加,这与本研究结果类似。综合对比分析所有挥发性成分,发现4株非酿酒酵母发酵的葡萄酒中乙酸乙酯、癸酸3-甲基丁酯的含量都高于商业酿酒酵母,增强了葡萄酒中香蕉味等果香;2-壬酮、芳樟醇的含量都高于商业酿酒酵母,使玫瑰花香、柑橘香等香气大幅度增加;月桂酸乙酯的含量可达到商业酿酒酵母的2倍以上,赋予了葡萄酒浓郁的花香。以上结果表明,使用非酿酒酵母参与发酵,可以增强葡萄酒的某种香气风格,使果香、花香等香气特征更为显著。在本实验中,4株本土非酿酒酵母发酵酒样的香气物质中还发现了商业酿酒酵母酒样中没有的癸酸甲酯、2-糠酸乙酯,赋予了脂香、花香、果香等香气。GE等[21]也发现有孢汉逊酵母PCT4和商业酿酒酵母CEC01的连续发酵产生了商业酵母中没有的特殊挥发性化合物(如庚酸乙酯、1-庚醇、乙酸庚酯和邻苯二甲酸二甲酯)。张鸣宇等[23]将美极梅奇酵母08与酿酒酵母F33顺序发酵增加了新的香气物质香叶醇、橙花醇、松油醇和玫瑰醚。罗来庆等[24]用克鲁维毕赤酵母HSX-5与酿酒酵母HSX-5进行发酵,产生了新的香气物质月桂醇、乙酸异丁酯。与本研究结果相似。以上结果说明,4株本土非酿酒酵母通过单菌发酵产生了商业酿酒酵母没有的香气物质,后续可以配合酿酒酵母开展混菌发酵实验,深入探究对葡萄酒香气物质的影响。此外,本实验在葡萄汁有孢汉逊酵母YQY-B12发酵酒样中检测出具有杏仁、菠萝香气的丙酸异戊酯;葡萄汁有孢汉逊酵母YC-B10发酵酒样中检测出具有奶酪味的己酸;YC-B10和YQY-B12发酵酒样中均检测出己酸丁酯;在美极梅奇酵母YC-A13发酵酒样中检测出具有扁桃仁、脂香气的1-戊醇;在美极梅奇酵母YC-A13和泽普林假丝酵母YC-C13发酵酒样中检测到具有脂香、黄油香气的2,3-丁二酮,在其他菌种发酵酒样中均未检出。以上研究结果表明,不同种属的非酿酒酵母可以产生菌种特有的香气物质,在进行不同风格葡萄酒酿造时,可以根据香气需求选择特殊种属的非酿酒酵母参与发酵过程。综上所述,筛选出的4株优良本土非酿酒酵母具有不同的发酵特性,在提升葡萄酒香气品质和丰富度方面都有着独特的贡献与优势,为酿造具有产区特色的葡萄酒提供了理论依据。
[1] 姚红红, 任学梅, 严幻汝, 等.甘肃河西走廊葡萄酒产区高产糖苷酶非酿酒酵母菌株筛选及其酿酒适应性分析[J].食品与发酵工业, 2023, 49(16):49-58.
YAO H H, REN X M, YAN H R, et al.Screening of non-Saccharomyces yeasts endowed with high glucosidase activity and their adaptability to wine biotope in Hexi Corridor of Gansu Province[J].Food and Fermentation Industries, 2023, 49(16):49-58.
[2] GE Q, GUO C F, YAN Y, et al.Contribution of non-Saccharomyces yeasts to aroma-active compound production, phenolic composition and sensory profile in Chinese Vidal icewine[J].Food Bioscience, 2022, 46:101152.
[3] LIN M M H, BOSS P K, WALKER M E, et al.Evaluation of indigenous non-Saccharomyces yeasts isolated from a South Australian vineyard for their potential as wine starter cultures[J].International Journal of Food Microbiology, 2020, 312:108373.
[4] 张博钦, 方梓庄, 成池芳, 等.5株低产乙醇的非酿酒酵母筛选及其酿造特性[J].食品科学, 2021, 42(8):114-121.
ZHANG B Q, FANG Z Z, CHENG C F, et al.Screening of five non-Saccharomyces strains with low ethanol yield and evaluation of their oenological properties[J].Food Science, 2021, 42(8):114-121.
[5] ZILELIDOU E A, NISIOTOU A.Understanding wine through yeast interactions[J].Microorganisms, 2021, 9(8):1620.
[6] FAZIO N A, RUSSO N, FOTI P L, et al.Inside current winemaking challenges:Exploiting the potential of conventional and unconventional yeasts[J].Microorganisms, 2023, 11(5):1338.
[7] BINATI R L, LEMOS W J F Jr, LUZZINI G, et al.Contribution of non-Saccharomyces yeasts to wine volatile and sensory diversity:A study on Lachancea thermotolerans, Metschnikowia spp.and Starmerella bacillaris strains isolated in Italy[J].International Journal of Food Microbiology, 2020, 318:108470.
[8] LI J C, YUAN M M, MENG N, et al.Influence of nitrogen status on fermentation performances of non-Saccharomyces yeasts:A review[J].Food Science and Human Wellness, 2024, 13(2):556-567.
[9] 战吉宬, 曹梦竹, 游义琳, 等.非酿酒酵母在葡萄酒酿造中的应用[J].中国农业科学, 2020, 53(19):4057-4069.
ZHAN J C, CAO M Z, YOU Y L, et al.Research advance on the application of non-Saccharomyces in winemaking[J].Scientia Agricultura Sinica, 2020, 53(19):4057-4069.
[10] LAI Y T, HOU C Y, LIN S P, et al.Sequential culture with aroma-producing yeast strains to improve the quality of Kyoho wine[J].Journal of Food Science, 2023, 88(3):1114-1127.
[11] LIU W H, JI R J, AIMAIER A, et al.Adjustment of impact phenolic compounds, antioxidant activity and aroma profile in Cabernet Sauvignon wine by mixed fermentation of Pichia kudriavzevii and Saccharomyces cerevisiae[J].Food Chemistry:X, 2023, 18:100685.
[12] ŽENI OV
OV K, CABICAROV
K, CABICAROV T, SIDARI R, et al.Effects of co-fermentation with Lachancea thermotolerans or Metschnikowia pulcherrima on concentration of aroma compounds in pinot Blanc wine[J].Journal of Food &Nutrition Research, 2021, 60(1):87-91.
T, SIDARI R, et al.Effects of co-fermentation with Lachancea thermotolerans or Metschnikowia pulcherrima on concentration of aroma compounds in pinot Blanc wine[J].Journal of Food &Nutrition Research, 2021, 60(1):87-91.
[13] 王静尧, 王文华, 王丽玲, 等.酿酒酵母与2株非酿酒酵母混酿培养中的增香特性[J].食品研究与开发, 2023, 44(11):60-66.
WANG J Y, WANG W H, WANG L L, et al.Aroma enhancement characteristics of Saccharomyces cerevisiae and two strains of non-Saccharomyces cerevisiae in mixed culture[J].Food Research and Development, 2023, 44(11):60-66.
[14] 李毅丽, 李红玉, 贺艳楠, 等.混菌发酵对昌黎赤霞珠葡萄酒品质的影响[J].食品与发酵工业, 2022, 48(21):54-60.
LI Y L, LI H Y, HE Y N, et al.Effect of mixed fermentation on quality of Cabernet Sauvignon wine in Changli region[J].Food and Fermentation Industries, 2022, 48(21):54-60.
[15] 李亚军, 郑明朋, 张众, 等.贺兰山东麓赤霞珠干红葡萄酒发酵过程中香气成分与感官特征的变化[J].食品与发酵工业, 2023, 49(24):118-124.
LI Y J, ZHENG M P, ZHANG Z, et al.Changes of aroma components and sensory characteristics of Cabernet Sauvignon dry red wine in Eastern Foothill of Helan Mountain during fermentation[J].Food and Fermentation Industries, 2023, 49(24):118-124.
[16] 李海峰, 李砷, 牟志勇, 等.非酿酒酵母在酒类酿造过程中的微生物相互作用及功能特性研究进展[J].食品与发酵工业, 2024, 50(7):313-323.
LI H F, LI S, MU Z Y, et al.Research progress on microbial interaction and functional characteristics of non-Saccharomyces yeasts in wine brewing process[J].Food and Fermentation Industries, 2024, 50(7):313-323.
[17] 王静尧. 高产酯非酿酒酵母筛选及在混菌发酵中的发酵特性研究[D].新疆:塔里木大学, 2023.
WANG J Y.Screening of non-Saccharomyces cerevisiae with high ester yield and its fermentation characteristics in mixed fermentation[D].Xinjiang:Tarim University, 2023.
[18] 高娉娉. 高产β-葡萄糖苷酶本土优良非酿酒酵母菌株筛选及应用效果评价[D].甘肃:甘肃农业大学, 2022.
GAO P P.Evaluation of the selection and application of indigenous high ß-glucosidase activity non-Saccharomyces yeast[D].Gansu:Gansu Agricultural University, 2022.
[19] 马延琴, 徐晓裕, 李甜, 等.酿酒葡萄表皮产酶非酿酒酵母的筛选及其产酶特性研究[J].中国酿造, 2021, 40(12):149-154.
MA Y Q, XU X Y, LI T, et al.Screening of non-Saccharomyces cerevisiae from wine grape epidermis and its enzyme-producing ability[J].China Brewing, 2021, 40(12):149-154.
[20] 董琦楠, 叶冬青, 梁艳英, 等.高产酸本土非酿酒酵母菌株的筛选及发酵性能研究[J].中国酿造, 2021, 40(8):70-75.
DONG Q N, YE D Q, LIANG Y Y, et al.Screening and fermentation performance of native non-Saccharomyces cerevisiae with high lactic acid production[J].China Brewing, 2021, 40(8):70-75.
[21] GE X X, WANG J, WANG X D, et al.Evaluation of indigenous yeasts screened from Chinese vineyards as potential starters for improving wine aroma[J].Foods, 2023, 12(16):3073.
[22] 李红玉, 贺艳楠, 李毅丽.混菌发酵对两个品种葡萄酒香气的影响[J].中外葡萄与葡萄酒, 2023(6):99-106.
LI H Y, HE Y N, LI Y L.Effect of mixed yeasts fermentation on aroma of wine from two grape varieties[J].Sino-Overseas Grapevine &Wine, 2023(6):99-106.
[23] 张鸣宇, 罗莉莎, 高特, 等.本土美极梅奇酵母对玫瑰香葡萄酒降醇及香气的影响[J].中国酿造, 2023, 42(1):133-141.
ZHANG M Y, LUO L S, GAO T, et al.Effects of indigenous Metschnikowia pulcherrima on alcohol reduction and aroma of Muscat wine[J].China Brewing, 2023, 42(1):133-141.
[24] 罗来庆, 林海明, 焦宇知, 等.非酿酒酵母与酿酒酵母混合发酵对葡萄酒香气的影响[J].中国酿造, 2022, 41(10):89-94.
LUO L Q, LIN H M, JIAO Y Z, et al.Effects of mixed-strain fermentation of non-Saccharomyces cerevisiae and Saccharomyces cerevisiae on wine aroma[J].China Brewing, 2022, 41(10):89-94.