罗望子(Tamarindus indica L.)又称酸角,主要分布在我国云南、海南、广西、广东、福建等热带和亚热带地区[1]。罗望子果实分为果肉、果皮和种子3部分,其中种子占果实重量的25%~40%。罗望子种仁富含多糖成分,含量高达50%。从种仁中分离出的罗望子多糖(tamarind seed polysaccharide,TSP)是一种半乳木葡聚糖,主链为β-1,4连接的葡聚糖,在O-6位置部分被α-D-木糖取代,侧链的木糖在O-2位置部分被β-D-半乳糖取代[2]。罗望子多糖亲水性强,易分散于冷水中,是一种性能优良的天然食品添加剂,具有良好的耐热、耐酸、耐冷冻性。例如,TSP可作为酸性乳液的稳定剂,维持乳液液滴的大小并提升其酸稳定性。但其在乳液中的分散性较差,尤其是高油相的乳液体系中[3-4]。因此,深入研究TSP的改性方法,通过对TSP改性修饰,探究改性后的TSP乳化能力和乳液稳定性,从而使TSP在饮料行业得到更加广泛的应用[5-6]。
辛烯基琥珀酸酐(octenyl succinic anhydride,OSA)是一种重要的精细化学品中间体,其分子中含有碳碳双键和羧酸配基,因此具有很高的化学反应活性[7]。OSA能够与多种物质反应,如醇、胺和淀粉等,进行加成、取代、还原、醋化、水解及聚合等一系列反应。在多糖改性的过程中,OSA主要与多糖中的羟基(—OH)发生酯化反应,形成酯键[8-9]。在这个过程中,OSA的疏水性长链烷基与多糖的亲水性糖链结合,赋予改性多糖两亲性(同时具有亲水和疏水性质)。经过OSA改性后的多糖,其分子结构和性质发生了显著变化。由于引入了OSA的疏水性长链烷基,改性多糖的乳化稳定性得到提高。改性后的多糖,如OSA-大豆多糖酯,被广泛应用于食品、医药、化妆品和化工等行业[10-11]。
本实验以罗望子多糖为研究对象,通过离子液体均相体系法以及常用酯化剂辛烯基琥珀酸酐对罗望子多糖进行酯化改性,探究辛烯基琥珀酸酐对罗望子多糖的改性及不同酯化度产物的乳化活性及乳液稳定性,为提高罗望子多糖的利用价值提供理论依据。
1 材料与方法
1.1 材料与设备
TSP(食品级),云南猫哆哩集团食品有限责任公司;无水乙醇、浓盐酸、NaOH、OSA、1-丁基-3-甲基咪唑氯盐离子液体、四二甲氨基吡啶(4-dimethylaminopyridine,DMAP)、酚酞,国药化学试剂有限公司;大豆油,金龙鱼粮油食品股份有限公司。
冷冻干燥机,美国Labconco公司;Discovery HR-3流变仪,美国TA Instruments公司;Nicolet傅里叶红外光谱仪,美国Thermo公司;DW-3数显电动搅拌器,山东省鄄城县嘉德仪器厂;GL-3型磁力搅拌器,河南巩义市英峪予华仪器厂;DHG-9240A型电热恒温鼓风干燥箱,上海精宏实验设备有限公司;AE240电子分析天平,梅特勒上海仪器有限公司;HH-S恒温水浴锅,金坛市荣华仪器厂;TDL80-2B型台式离心机,上海安亭科学仪器厂;Sigma 500场发射扫描电子显微镜,德国Zeiss公司;Nano ZS型号纳米粒度及zeta电位仪,英国Malvern公司;752型紫外可见分光光度计,上海光谱仪器有限公司。
1.2 实验方法
1.2.1 OSA-TSP的制备
1.2.1.1 滴定法
称取1.0 g TSP溶于100 mL去离子水中,用1.0 mol/L NaOH溶液调节pH值至8.5,再在10 min内缓慢加入OSA试剂(设置3个比例TSP∶OSA=1∶1、1∶2、1∶3,其中OSA用量是指OSA与干TSP的质量比),同时搅拌,加完后继续低速搅拌反应1 h,期间不断滴加NaOH溶液使整个体系的pH值维持在8.5。反应结束后用1.0 mol/L HCl溶液将体系pH调节至6.5,透析除去多余OSA并将样品放入冰箱预冻一夜,冷冻干燥后放入干燥箱保存[12]。
1.2.1.2 离子液体均相法
称取0.5 g TSP和7 g离子液体放入样品瓶中,70 ℃油浴至TSP完全溶解,再将0.175 g DMAP加入混合物中,至DMAP完全溶解后加入OSA(比例同1.2.1.1节),混合均匀后在121 ℃下酯化反应,2.2 h后停止反应,待冷却至室温,加入无水乙醇洗涤产物,再用纯水洗涤数次,放入45 ℃烘箱烘干后磨碎并放入干燥箱保存[13]。
1.3 OSA-TSP酯化度的测定
酯化度是每个TSP糖单位取代羟基的平均数。本文使用滴定法对取代度进行测定。称取0.5 g干样品加入到5 mL溶剂为体积分数为90%异丙醇的2.5 mol/L HCl溶液中,搅拌并加热到60 ℃保持3 h直至样品完全溶解。将样品转移到15 mL的离心管中,配平,再在25 ℃下以6 000 r/min的速度离心15 min,取出去除上层液体,加入5 mL体积分数为90%的异丙醇与残留物混合洗涤,再以相同的参数离心。洗涤离心重复3次后将残留物干燥去除多余异丙醇,再将产物溶于60 mL去离子水中,以酚酞为指示剂,使用0.002 5 mol/L NaOH溶液进行滴定,记录NaOH消耗体积为V1。以TSP为空白组,得到NaOH消耗体积V0。取代度(degree of Substitution,DS)的计算如公式(1)所示:
(1)
式中:DS,取代度,%;V0,空白组消耗的NaOH体积,mL;V1,样品组消耗的NaOH体积,mL;c,NaOH浓度,mol/L;m,样品质量,g[14]。
1.4 OSA-TSP结构表征
1.4.1 红外光谱分析
使用傅里叶红外光谱仪对样品进行红外光谱测定。将样品干燥粉碎后置于红外光谱仪上测试,扫描波数范围为4 000~400 cm-1,分辨率为4 cm-1,以空气为空白对照,每分钟扫描8次后取平均值得到样品的红外光谱图。
1.4.2 扫描电子显微镜检测
使用场发射扫描电子显微镜对不同用量OSA酯化的TSP进行表面观察[15]。用镊子夹取少量OSA-TSP,并用导电胶将OSA-TSP固定于样品台,然后对样品台进行喷金处理,喷金结束后取出样品台,放入预热好的扫描电子显微镜中,利用扫描电子显微镜系统软件观察样品表面形态,选择样品中具有代表性的颗粒,并使用软件调节图像亮度和对比度直至能清晰观察到样品,再从低倍到高倍观察样品并拍摄图像。
1.5 OSA-TSP乳液制备
将0.05 g OSA-TSP分散于10 mL超纯水中,搅拌并加热至沸腾,待OSA-TSP完全溶解后,再将溶液体积补至10 mL。将溶液转移到标记好的50 mL小烧杯中,将均质机转速调至12 000 r/min对其进行均质,期间向烧杯中缓慢加入10 mL大豆油,完全加入后等待均质乳化5 min制成乳液。
1.5.1 OSA-TSP乳液乳化活性
取10 mL制备好的OSA-TSP乳液放入15 mL标记好的离心管中,然后以3 000 r/min的速度离心5 min。记录乳化层高度(H1)和总液体高度(H),重复3次平行。
乳化活性(emulsifying capacity,EC)的计算如公式(2)所示:
(2)
式中:EC,样品乳化能力,%;H,总液体高度,cm;H1,乳化层高度,cm[13]。
再取上述已制备好的乳液放入15 mL标记好的离心管中,将上述乳液静置24 h后,以3 000 r/min的速度离心5 min。记录乳化层高度(H2)和总液体高度(H)。乳化稳定性(emulsion stability,ES)按公式(3)计算:
(3)
式中:ES,乳化稳定性,%;H,总液体高度,cm;H2,静置24 h后乳化层高度,cm[13]。
1.5.2 OSA-TSP乳液的流变学特性分析
使用Discovery HR-3流变仪测定OSA-TSP乳液的流变性质,采用直径为40 mm的不锈钢平板作夹具,所有测量间隙尺寸均为1.0 mm。通过测定小振幅振荡剪切来确定TSP和3种取代度OSA-TSP乳液的线性黏弹性行为。储能模量G′和损耗模量G″均有记录,由TRIOS软件进行实验数据的采集和分析。
1.6 OSA-TSP乳液的粒度和zeta电位测定
1.6.1 粒度分布
使用纳米粒度及zeta电位仪在室温下对乳液的液滴大小进行表征。将制得的乳液倒入石英比色皿中,置于激光粒度仪中,打开粒度分析软件,调整好各项参数,记录好样品信息,并设置平衡时间为120 s。等待仪器平行测试3次并记录数据。
1.6.2 zeta电位分析
使用规格为1 mL的注射器吸取TSP和不同比例酯化得到的OSA-TSP乳液样品,然后注射到zeta电位仪测量池中,戴好塞子放入电位仪。打开Zetasizer电位分析软件,设置测试折光指数为1.33,光束波长633 nm,测试温度25 ℃,点击开始测试乳液电位。等待仪器平行测试3次并记录数据。
1.6.3 OSA-TSP 乳液稳定性分析——光学显微镜分析
将100 μL乳液分散到1 mL pH分别为3、5和7的水溶液中(体积比1∶1)。充分混匀后,使用移液枪吸取20 μL溶液滴在载玻片上,用镊子夹住盖玻片的一端,另一端靠在载玻片液滴上,使盖玻片与载玻片呈45°角,缓慢放下盖玻片,使盖玻片缓慢接触样品,避免出现气泡。制好片后晾干至盖玻片固定,然后到光学显微镜载物台上观察乳滴状态,并选取视野进行拍摄。
1.7 数据分析
所有数据至少记录3次,结果以“平均值±标准差”表示。显著性差异分析使用SPSS软件中的Tukey检验(P<0.05)。
2 结果与分析
2.1 OSA-TSP的结构表征分析
2.1.1 红外光谱分析
利用滴定法和离子液体均相法制得的OSA-TSP样品红外光谱如图1所示。离子液体均相法制得的OSA-TSP红外光谱图中1 730 cm-1处出现了OSA分子结构中C![]() O键的伸缩振动峰[16],而对比滴定法同比例OSA酯化得到的TSP样品,该谱图在1 730 cm-1处特征峰较不明显,这表明同样剂量酯化剂条件下,离子液体均相法制得的TSP酯化程度和酯化效果优于滴定法。因此后续实验中不同取代度的OSA-TSP样品均使用离子液体均相法制得。
O键的伸缩振动峰[16],而对比滴定法同比例OSA酯化得到的TSP样品,该谱图在1 730 cm-1处特征峰较不明显,这表明同样剂量酯化剂条件下,离子液体均相法制得的TSP酯化程度和酯化效果优于滴定法。因此后续实验中不同取代度的OSA-TSP样品均使用离子液体均相法制得。
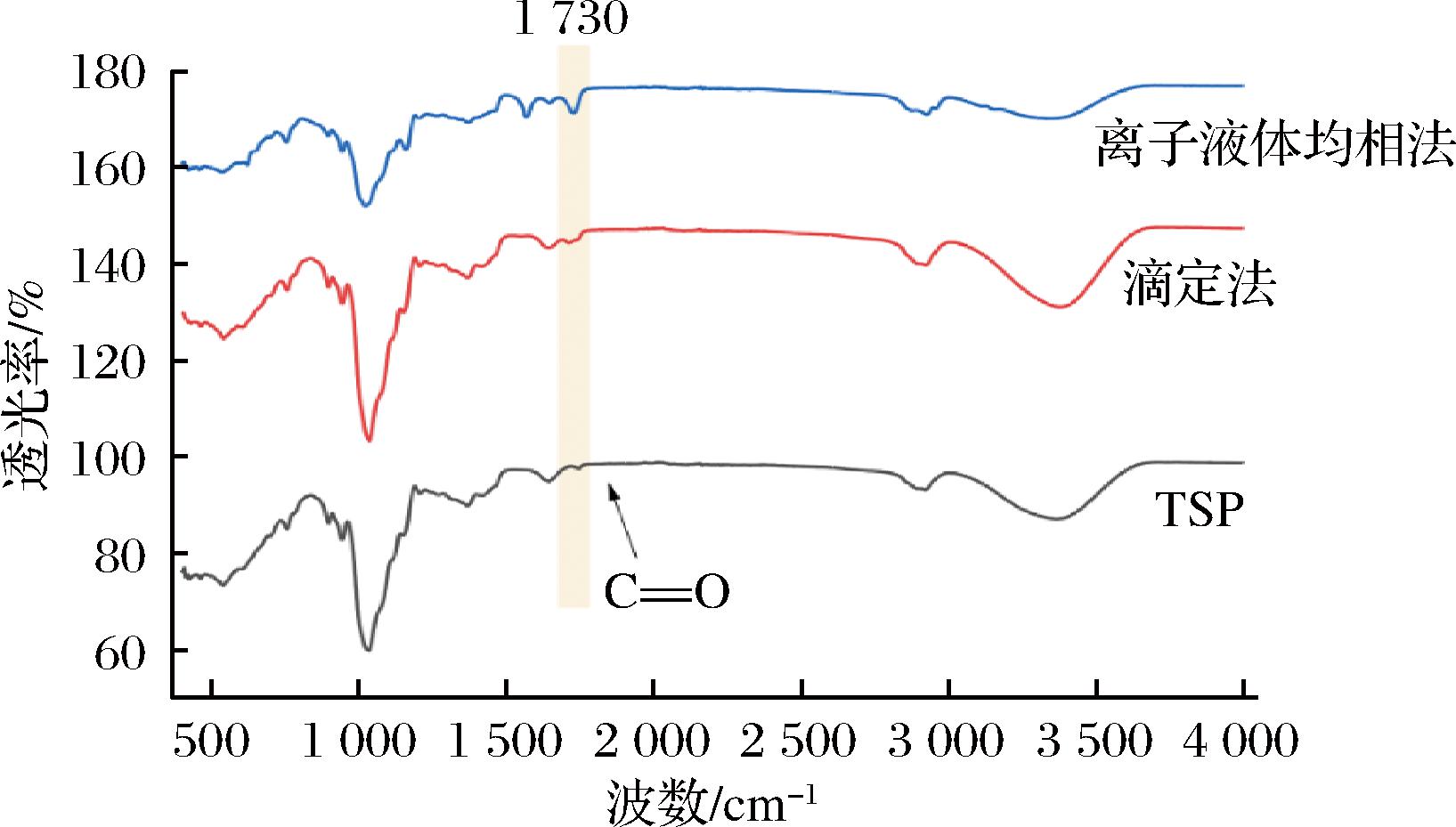
图1 两种方法制备的OSA-TSP的红外谱图
Fig.1 FTIR spectra of OSA-TSP prepared by the two methods
使用不同比例OSA酯化得到的OSA-TSP样品和TSP的红外谱图如图2所示。在OSA-TSP的红外光谱图中,1 730 cm-1处新出现的特征峰为OSA结构中C![]() O键的伸缩振动峰,此处C
O键的伸缩振动峰,此处C![]() O键的拉伸振动增强,说明OSA酯化TSP分子成功[16]。此外,不同酯化程度的OSA-TSP红外谱图在1 730 cm-1处吸收峰的强弱排序为:1∶3>1∶2>1∶1,表明随着OSA用量的增大,TSP的酯化程度增加[17]。3种OSA-TSP样品在1 140 cm-1的峰为C—O—C键的不对称拉伸振动,说明酯化后TSP的基本结构仍旧保持完整。
O键的拉伸振动增强,说明OSA酯化TSP分子成功[16]。此外,不同酯化程度的OSA-TSP红外谱图在1 730 cm-1处吸收峰的强弱排序为:1∶3>1∶2>1∶1,表明随着OSA用量的增大,TSP的酯化程度增加[17]。3种OSA-TSP样品在1 140 cm-1的峰为C—O—C键的不对称拉伸振动,说明酯化后TSP的基本结构仍旧保持完整。
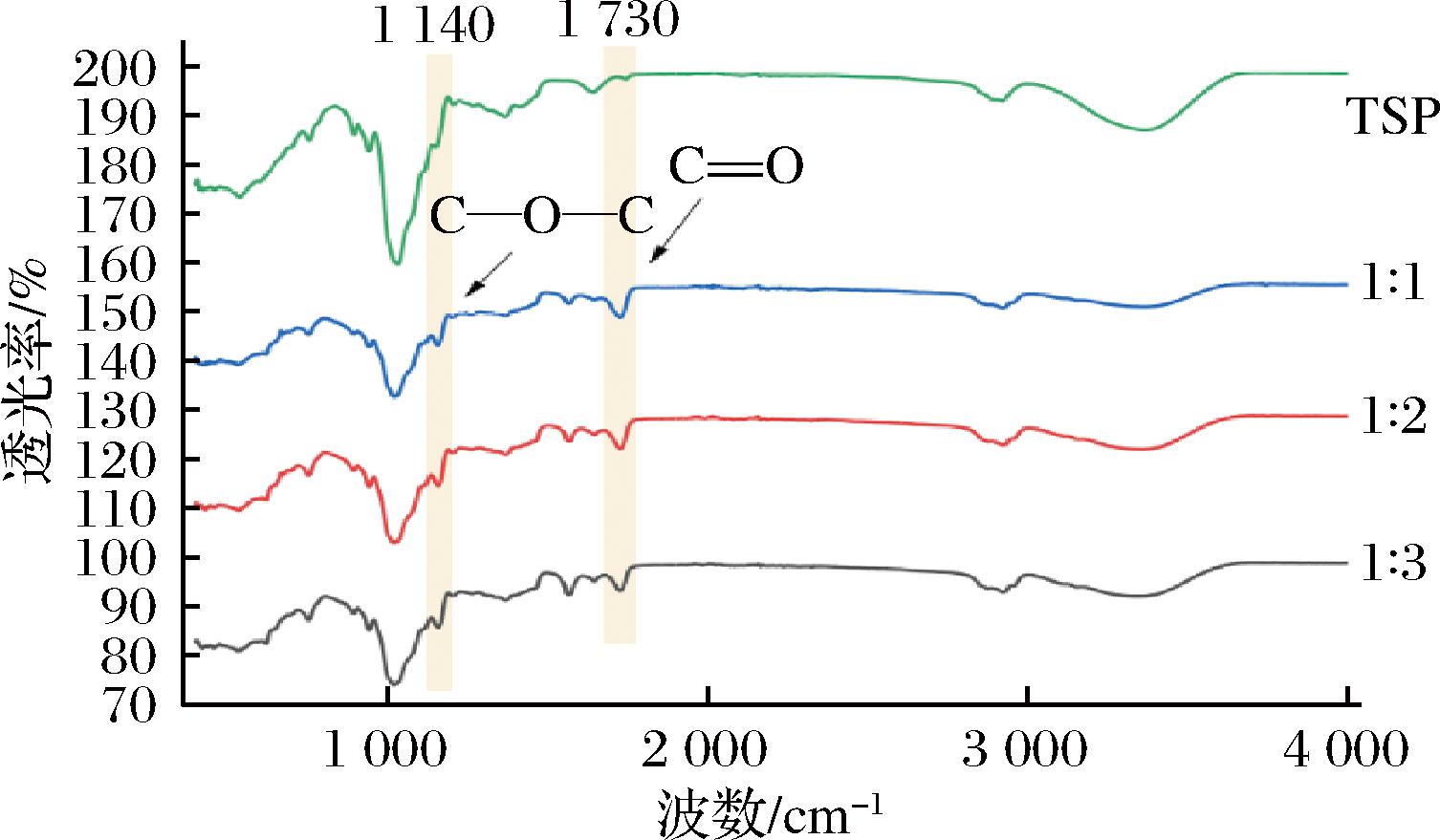
图2 不同比例酯化的OSA-TSP的红外光谱
Fig.2 FTIR spectra of OSA-TSP with different DS
2.1.2 OSA-TSP的酯化度测定
TSP和不同比例OSA酯化得到的OSA-TSP的DS分别为0.12 (OSA-TSP1∶1),0.21 (OSA-TSP2∶1),0.68 (OSA-TSP3∶1),结果表明随着样品酯化比例的增加,样品DS也有所提高,但OSA-TSP总体DS较低,且不成比例关系,这可能是因为利用离子液体均相法制备OSA-TSP样品时,罗望子多糖溶于离子液体形成的均相溶液黏度较大,搅拌困难,导致酯化反应不均匀[18]。
2.1.3 扫描电镜分析
TSP和不同比例酯化的OSA-TSP的电镜扫描分析如图3所示。TSP的颗粒呈现不规则的块状结构,表面较光滑。酯化后的OSA-TSP样品仍然呈现较大的块状结构,但表面变得粗糙,且有小颗粒附着,并且随着OSA用量的增大,OSA-TSP表面更加粗糙且有孔隙出现。引起TSP形态变化的原因是在酯化过程中,TSP在离子液体的作用下其分子间和分子内氢键断裂,活性羟基暴露并与长链OSA基团发生酯化反应,从而导致OSA-TSP表面的小颗粒聚集和粗糙现象,但对TSP的主体结构影响较小[19-20]。

a-TSP;b-TSP∶OSA=1∶1;c-TSP∶OSA=1∶2;d-TSP∶OSA=1∶3
图3 不同比例酯化的OSA-TSP的扫描电镜图
Fig.3 SEM of OSA-TSP with different DS
2.2 OSA-TSP乳化能力和乳化稳定性分析
OSA-TSP乳化能力和乳化稳定性分析结果见表1和图4。酯化后的3种OSA-TSP的EC和ES值要高于未经酯化处理的TSP乳液,且随着酯化程度升高,OSA-TSP样品的EC和ES值升高,说明OSA酯化可提升TSP的乳化能力。TSP虽有一定的乳化能力,但其ES较差,不能很好地稳定乳液。而酯化后的3种OSA-TSP的ES均能达到50%左右,这是因为OSA基团可以降低界面张力,在分散的液滴之间产生空间位阻或静电排斥,以达到稳定乳液的作用[21]。比较不同取代度的OSA-TSP的EC和ES发现,OSA-TSP的乳化能力和稳定性随取代度的增加而增加,这可能是因为取代度越高的OSA-TSP的样品含有更多的辛烯基长链基团,从而增强了样品的两亲性,表面张力变小,乳化能力增强。同时由于取代度越高,OSA-TSP孔隙结构越明显,形成的网状结构稳定性越强,其乳化稳定性也增强[22-23]。此外,从图4中可看出,离心后的TSP乳液出现明显的油水分离现象,说明TSP制备的乳液稳定性较差,OSA-TSP(1∶1)样品乳液也出现明显的油水分离现象,而OSA-TSP(2∶1)、OSA-TSP(3∶1)样品乳液未见油相析出,乳化层仍然存在,且OSA-TSP(3∶1)样品乳液乳化层体积较大。综上,TSP具有一定的乳化能力,但稳定性较差,而酯化后OSA-TSP的EC和ES都有所增强,且其EC和ES随酯化程度增加而增强,表明OSA酯化TSP可较好地提升其乳化能力。
表1 TSP和不同比例酯化的OSA-TSP的乳化特性(n=3)
Table 1 The EC and ES comparison of TSP and OSA-TSP with different DS(n=3)
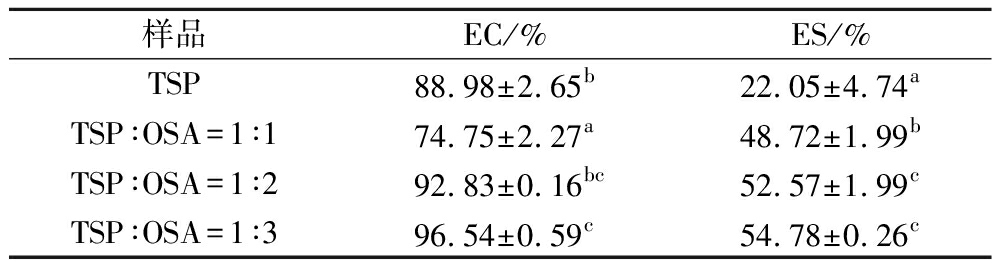
样品EC/%ES/%TSP88.98±2.65b22.05±4.74aTSP∶OSA=1∶174.75±2.27a48.72±1.99bTSP∶OSA=1∶292.83±0.16bc52.57±1.99cTSP∶OSA=1∶396.54±0.59c54.78±0.26c
注:不同列中字母表示显著性差异(P<0.05)(下同)。
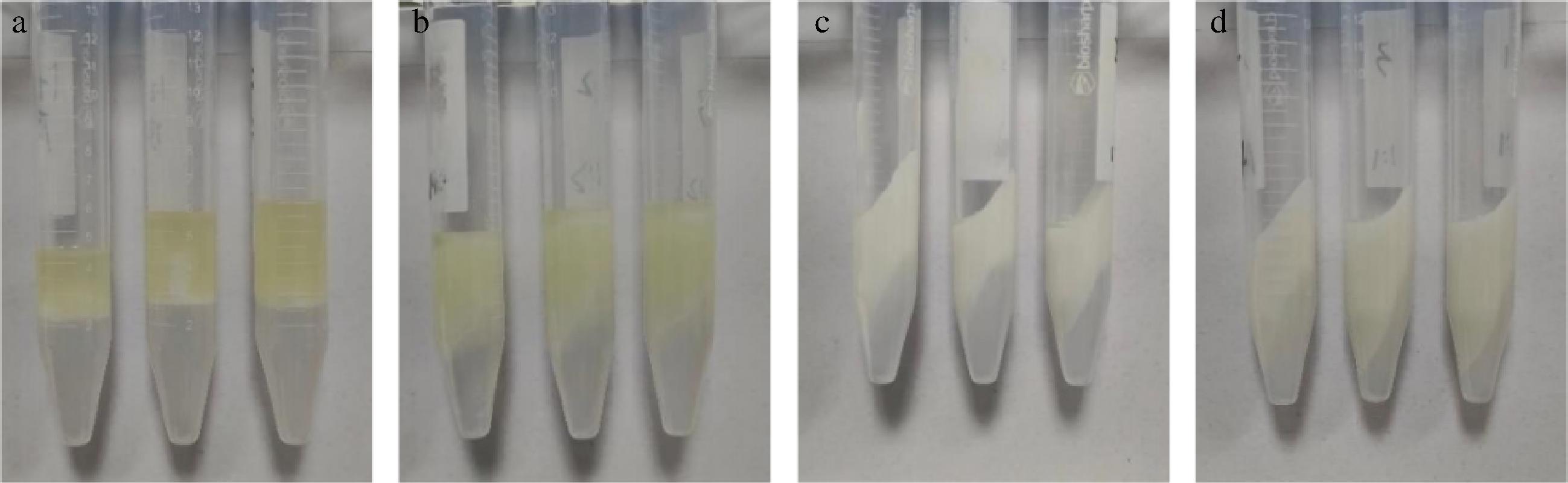
a-TSP;b-TSP∶OSA=1∶1;c-TSP∶OSA=1∶2;d-TSP∶OSA=1∶3
图4 离心后TSP和不同比例酯化的OSA-TSP的乳化稳定性
Fig.4 ES of TSP and OSA-TSP with different DS after centrifugation
2.3 OSA-TSP乳液流变学特性
2.3.1 静态流变学
如图5所示,4种TSP乳液的黏度随着剪切速率的增大而下降,表明4种乳液都是典型的非牛顿假塑性流体。这可能是由于OSA-TSP分散在水相剪切速率增大时,物理交联聚合物被分离,乳液体系的网络结构被破坏,导致乳液的剪切应力急剧增大,乳液黏度下降[24]。与TSP相比,当剪切速率较低时,OSA-TSP乳液的黏度要明显大于TSP乳液,这可能是OSA基团的引入使TSP具有双亲性,导致乳液更稳定,形成的乳液网状结构更强,在油水界面形成的界面膜黏弹性更好,所以在低速剪切时OSA-TSP乳液的黏度大于TSP乳液。对比不同取代度的OSA-TSP乳液发现,低速剪切时,取代度越高的OSA-TSP乳液黏度越大,这是因为OSA基团在TSP分子中的取代度变高,形成了更牢固的网状结构,致使乳液稳定性更高[8, 22]。
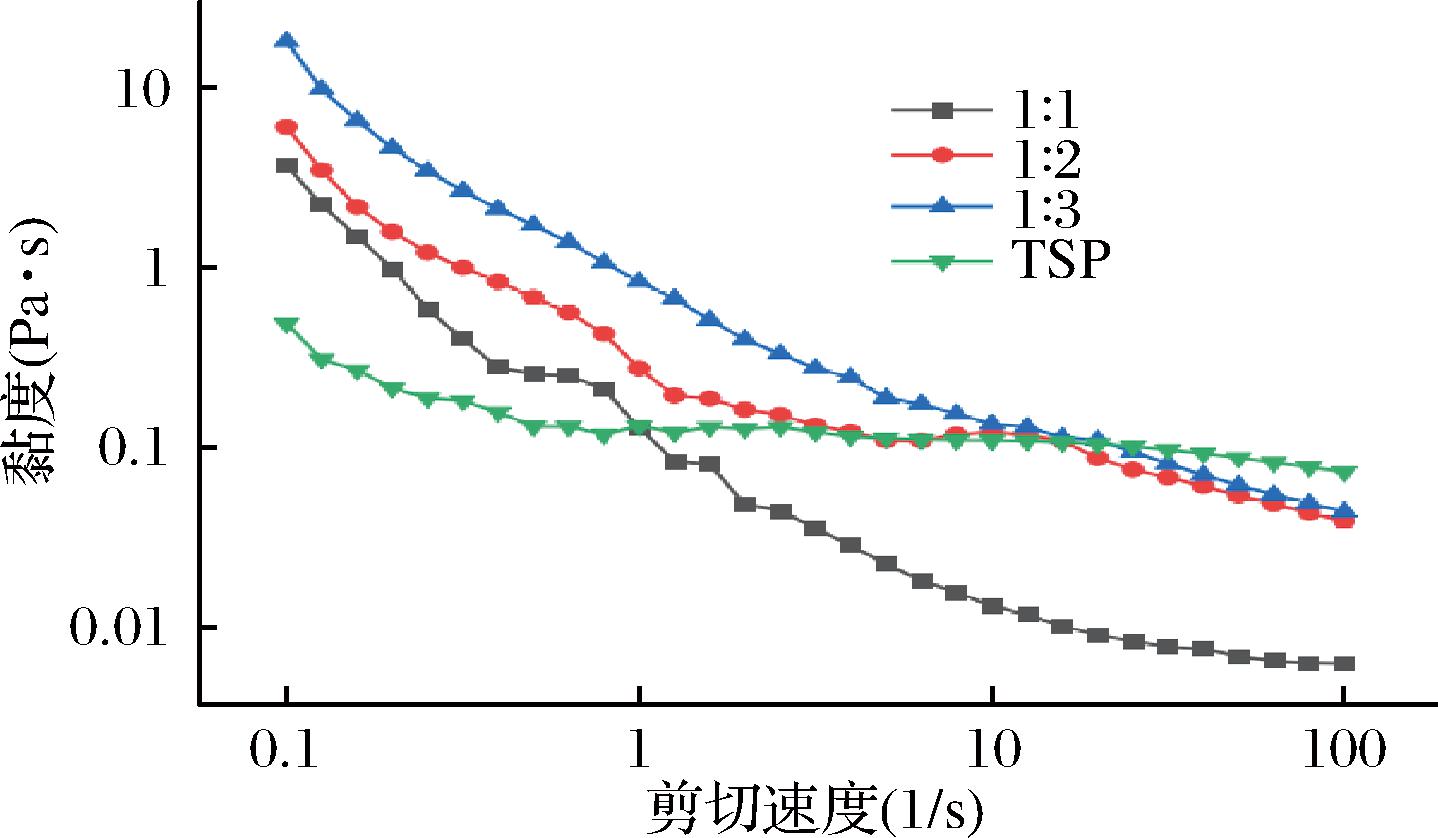
图5 不同酯化比例的OSA-TSP乳液的黏度变化
Fig.5 Effect of emulsion of OSA-TSP on viscosity
2.3.2 动态流变学
储能模量(G′)和损耗模量(G″)一般用于动态流变学中分析样品的黏弹性。G′表示当样品溶液发生形变时,由于弹性形变而储存能量的大小,用于反映材料弹性大小;G″表示当样品发生形变时,由不可逆形变引起的能量损失的大小[25]。当G′>G″时,样品主要表现出弹性行为的凝胶特性;当G′<G″时,样品主要表现出黏性行为的流体特性[21]。从图6中可看出,在测试频率范围内,TSP乳液的G′<G″,而3种OSA-TSP乳液样品在测试频率范围内G′>G″,表明TSP乳液主要表现出黏性行为的流体特性,而不同取代度的OSA-TSP乳液表现出弹性特性。对比不同取代度的OSA-TSP样品,取代度高的样品乳液的G′和G″较高,即样品更易形成强度更高的网状结构来防止破乳[26]。这说明高取代度的样品更有利于乳液的稳定,这与2.2节中结论一致。
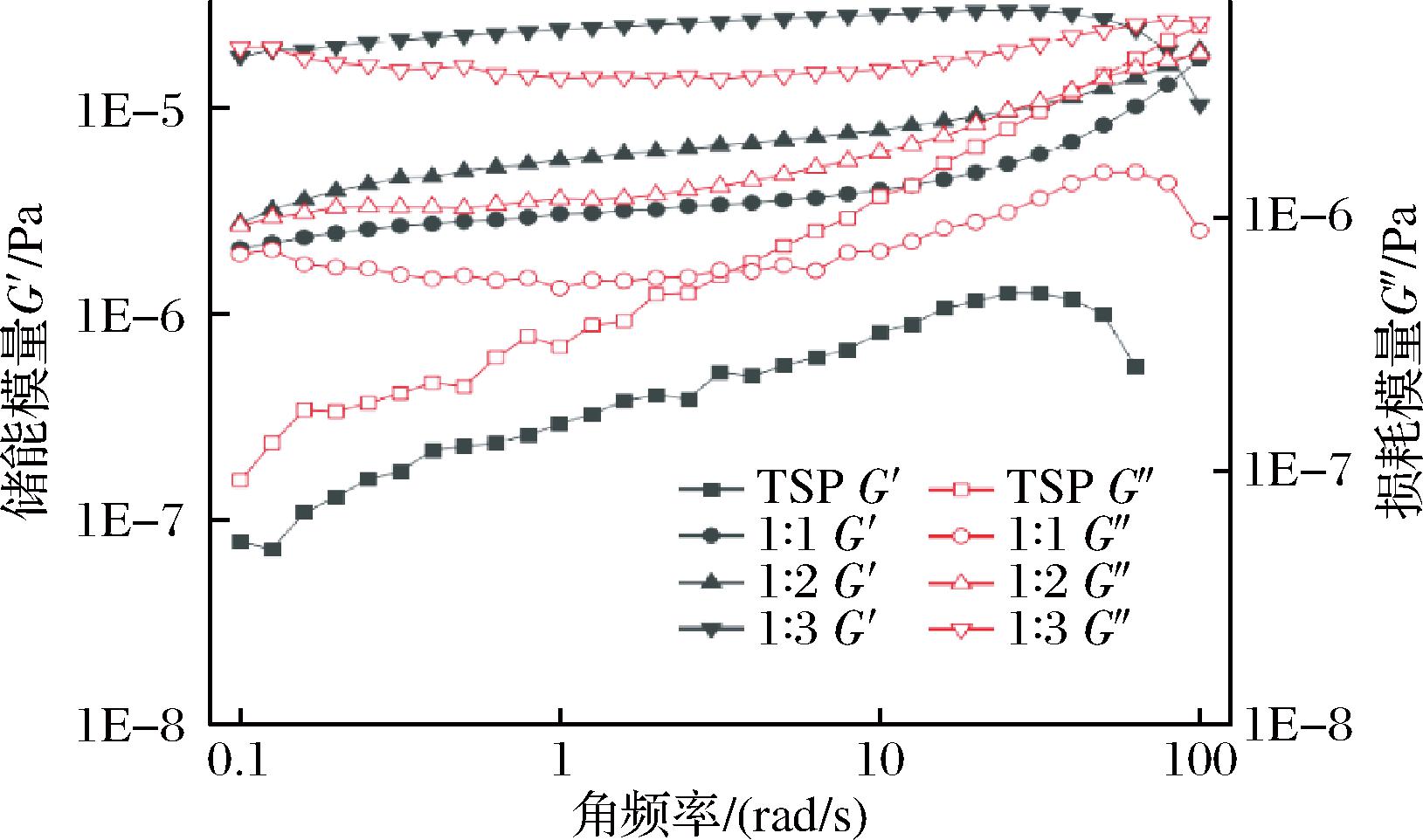
图6 不同酯化比例的OSA-TSP乳液的储能模量G′和损耗模量G″
Fig.6 Storage modulus G′ and loss modulus G″ of OSA-TSP with different DS
2.4 OSA-TSP乳液粒度和zeta电位分析
2.4.1 粒度分布
由图7可知,TSP乳液的粒度分布出现双峰,表示乳液中粒度分布不均匀,形成的乳液稳定性较差。对比不同取代度的OSA-TSP乳液粒径,随着取代度的提高,OSA-TSP乳液中乳滴的平均粒径逐渐变小,且粒度分布呈现正态分布,表明乳液较稳定。OSA长链基团进入TSP分子,形成了具有亲水性和疏水性链、能够稳定油水乳状液的网状结构,该结构能稳定包裹小乳滴防止破乳[13]。高取代度OSA-TSP乳液网状结构更加稳定,所以乳液粒径相对取代度低的样品粒径更小[26]。
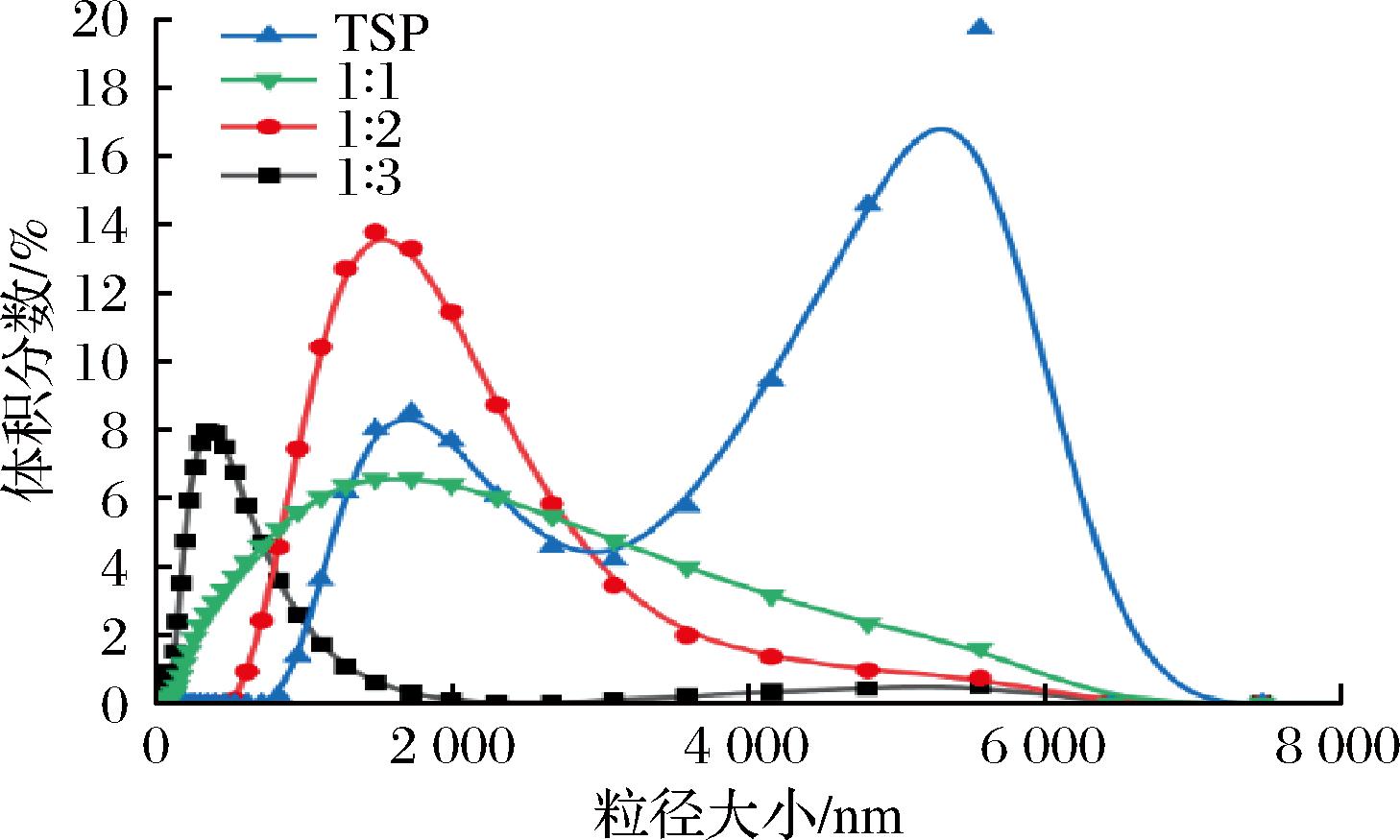
图7 不同酯化比例的OSA-TSP的粒度分布
Fig.7 Size distribution of OSA-TSP with different DS
2.4.2 zeta电位分析
zeta电位用于测量乳状液液滴的界面电性,其数值可反应分散体系的稳定性与乳液体系中分子间的静电相互作用的类型和强度,其中zeta电位的绝对值与胶态体系稳定性呈正相关[26-27]。如图8所示,在测试范围内,所有样品的zeta电位均为负值,且4种样品体系皆具有一定的稳定效果。比较4个样品的zeta电位绝对值可知,3种酯化后OSA-TSP乳液的zeta电位绝对值均大于TSP乳液,且OSA-TSP乳液zeta电位绝对值随样品的酯化程度增加而增大。这可能是因为OSA-TSP吸附在大豆油表面,改变了大豆油颗粒表面电荷密度,使其与体系中其他颗粒产生不同程度的静电排斥,并且随着OSA-TSP酯化程度增加,OSA基团数目增加,长链增多,电荷数增加导致静电排斥效果增强,从而使大豆油颗粒的聚集效果减弱,乳液的稳定性增强[28]。综上,TSP和3种OSA-TSP皆有一定能够稳定乳液的效果,3种酯化比例的OSA-TSP乳液稳定效果均强于TSP,且OSA-TSP稳定乳液的能力随酯化程度增加而增强。
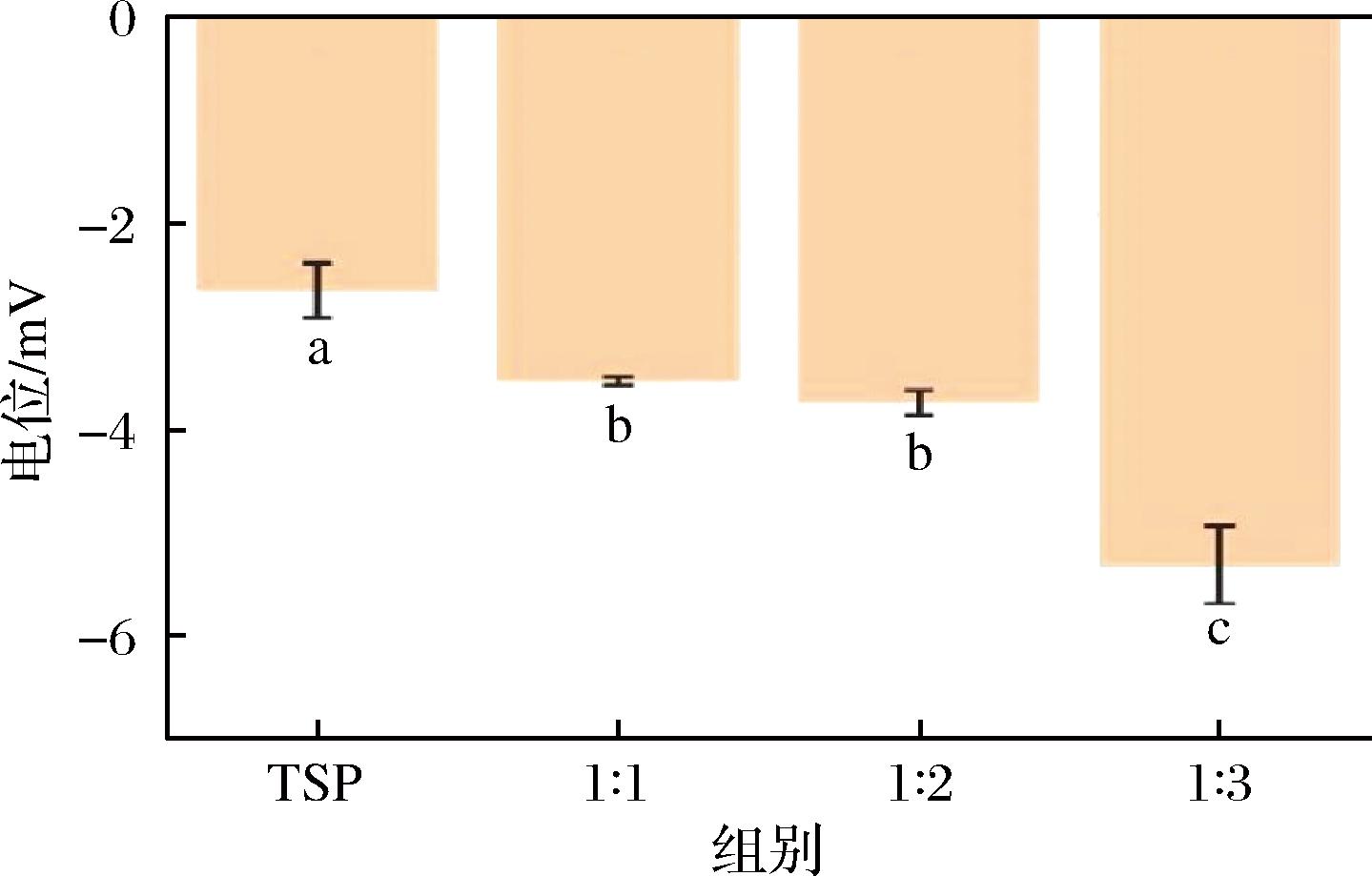
图8 不同酯化比例的OSA-TSP的zeta电位
Fig.8 Zeta potential of OSA-TSP with different DS

图9 不同酯化比例的OSA-TSP乳液在不同pH溶液中的乳滴变化
Fig.9 OSA-TSP with different DS emulsion in different pH solutions
2.4.3 OSA-TSP乳液酸稳定性分析——光学显微镜分析
TSP和不同比例酯化的OSA-TSP乳液分散在pH 7、5、3溶液中的光学显微镜图如9所示。同一样品中,乳滴粒径随着溶液pH的减小逐渐变大。在pH 3时,TSP和OSA-TSP(1∶1)乳液样品中出现明显的油相析出,而OSA-TSP(2∶1)、OSA-TSP(3∶1)乳液样品中仍能呈现较完整的乳球。这可能是因为TSP和不同取代度的OSA-TSP乳液在水溶液中能电离成亲油基和亲水基来降低油水界面张力,使溶液中存在电离平衡,而H+会有效抑制电离,所以溶液的pH值越小,样品电离程度降低,乳滴表面的油水界面张力减弱,导致界面张力不足以支撑乳滴。因此随着样品放置时间增加,溶液的界面张力减弱导致破乳,聚集形成了大乳滴[10]。故乳液的平均粒度变大,乳液稳定性降低。
对比同一pH下不同乳液的微观结构,可发现相比于TSP,OSA-TSP样品的乳滴表面有明显的黑色晕圈,这说明酯化后的TSP样品形成了能够稳定油水乳状液的网状结构[24]。对比不同酯化度的OSA-TSP,高酯化度样品的黑色晕圈更明显,这说明形成的网状保护膜稳定性更强,与2.2节中推测相符。此外,相较于TSP和OSA-TSP(1∶1)乳液样品,OSA-TSP(2∶1)、OSA-TSP(3∶1)乳液样品在同一pH下的乳球最小,充分说明高OSA取代度的TSP乳液具备较好的酸稳定性。
3 结论与讨论
本研究对比2种OSA改性TSP的方法,使用离子液体均相法酯化样品的酯化程度和酯化效果均优于滴定法。红外光谱证明OSA与TSP 发生了酯化反应,随着OSA用量的增加,OSA-TSP样品表面变得粗糙、有孔隙并伴随小颗粒附着聚集。OSA酯化TSP后其乳液的黏弹性变化明显,乳液耐剪切性提升、黏度增大,且取代度越高,OSA-TSP孔隙结构越明显,形成的网状结构稳定性越强,其乳化能力和乳化稳定性也增强。此外,取代度高的OSA-TSP乳液粒径更小,乳液Zeta电位绝对值更大,乳液的酸稳定性更好。因此,本研究所制得的OSA-TSP样品较TSP具有更好的乳化能力,且乳液具备较好的机械、酸稳定性,研究结果为罗望子多糖的酯化改性,应用范围拓宽奠定了理论基础。
[1] 王枫, 艾连中, 赖凤羲, 等.小分子糖-罗望子多糖复合凝胶特性研究[J].中国食品学报, 2024, 24(4):69-79.WANG F, AI L Z, LAI F X, et al.Studies on the gelling properties of complex between small molecular sugars and tamarind seed polysaccharide[J].Journal of Chinese Institute of Food Science and Technology, 2024, 24(4):69-79.
[2] XIE F, ZHANG H, NIE C Q, et al.Structural characteristics of tamarind seed polysaccharides treated by high-pressure homogenization and their effects on physicochemical properties of corn starch[J].Carbohydrate Polymers, 2021, 262:117661.
[3] REN X L, ZHENG W Q, LI L, et al.Effects of tamarind seed polysaccharides on physicochemical characteristics of frozen dough:Structure-function relationship[J].Journal of the Science of Food and Agriculture, 2023, 103(13):6574-6583.
[4] SUN X B, GUO R, ZHAN T J, et al.Self-assembly of tamarind seed polysaccharide via enzymatic depolymerization and degalactosylation enhanced ice recrystallization inhibition activity[J].International Journal of Biological Macromolecules, 2023, 252:126352.
[5] 赵一鹤, 杨时宇, 李昆.世界酸角研究现状及进展[J].云南农业大学学报, 2005, 20(1):65-72.ZHAO Y H, YANG S Y, LI K.Advances in the researches of Tamarindus indica Ⅰ.in the world[J].Journal of Yunnan Agricultural University, 2005, 20(1):65-72.
[6] SUN F S, PAN C X, LIU Y T, et al.Carboxymethyl tamarind seed polysaccharide/chitosan complexes through electrostatic interaction stabilize high internal phase emulsions:Roles of the mass ratio and oil-water interfacial activity[J].LWT, 2024, 195:115833.
[7] ZHAO L, TONG Q Y, GENG Z W, et al.Recent advances of octenyl succinic anhydride modified polysaccharides as wall materials for nano-encapsulation of hydrophobic bioactive compounds[J].Journal of the Science of Food and Agriculture, 2022, 102(14):6183-6192.
[8] KOU Y X, GUO R, LI X J, et al.Synthesis, physicochemical and emulsifying properties of OSA-modified tamarind seed polysaccharides with different degrees of substitution[J].International Journal of Biological Macromolecules, 2023, 253:127102.
[9] 田俊青, 赵丹, 马小涵, 等.辛烯基琥珀酸酐纤维素酯的合成及其结构表征[J].食品与发酵工业, 2017, 43(11):65-74.TIAN J Q, ZHAO D, MA X H, et al.Synthesis and structure characterization of octenyl succinic acid cellulose ester[J].Food and Fermentation Industries, 2017, 43(11):65-74.
[10] CHIVERO P, GOHTANI S, YOSHII H, et al.Assessment of soy soluble polysaccharide, gum Arabic and OSA-Starch as emulsifiers for mayonnaise-like emulsions[J].LWT, 2016, 69:59-66.
[11] 齐军茹, 赵如霞, 刘倩茹, 等.酯化大豆多糖的制备及其分散稳定特性[J].华南理工大学学报(自然科学版), 2019, 47(3):78-84.QI J R, ZHAO R X, LIU Q R, et al.On the preparation of esterified soybean polysaccharides and its dispersion stability[J].Journal of South China University of Technology (Natural Science Edition), 2019, 47(3):78-84.
[12] 杨静, 王洋, 孔祥智, 等.辛烯基琥珀酸大蒜多糖酯的制备[J].食品研究与开发, 2008, 29(6):184-187.YANG J, WANG Y, KONG X Z, et al.Preparation of garlic polysaccharide octenylsuccinate[J].Food Research and Development, 2008, 29(6):184-187.
[13] 王满鑫. 辛烯基琥珀酸酯化羟丙基酸解罗望子胶的制备及性能研究[D].沈阳:沈阳工业大学, 2023.WANG M X.Study on preparation and properties of octenyl succinate hydroxypropyl acidolysis tamarind gum[D].Shenyang:Shenyang University of Technology, 2023.
[14] 李帅, 艾连中, 张汇, 等.百香果果胶及其辛烯基琥珀酸酯化物对酸化脱脂乳饮料稳定性的影响[J].食品与发酵工业, 2020, 46(11):151-156.LI S, AI L Z, ZHANG H, et al.Study on the stabilizing effects of passion fruit pectin and its octenyl succinate anhydride product on acidified skim milk drink[J].Food and Fermentation Industries, 2020, 46(11):151-156.
[15] 高蔷, 冯柳, 穆洪亮, 等.扫描电子显微镜样品的制备[J].上海化工, 2022, 47(6):26-29.GAO Q, FENG L, MU H L, et al.Preparation of scanning electron microscopy samples[J].Shanghai Chemical Industry, 2022, 47(6):26-29.
[16] EENSCHOOTEN C, GUILLAUMIE F, KONTOGEORGIS G M, et al.Preparation and structural characterisation of novel and versatile amphiphilic octenyl succinic anhydride-modified hyaluronic acid derivatives[J].Carbohydrate Polymers, 2010, 79(3):597-605.
[17] ZHAO R X, QI J R, LIU Q R, et al.Fractionation and characterization of soluble soybean polysaccharide esterified of octenyl succinic anhydride and its effect as a stabilizer in acidified milk drinks[J].Food Hydrocolloids, 2018, 85:215-221.
[18] 闫溢哲, 冯琳琳, 周亚萍, 等.酸解时间对B型玉米微晶淀粉结构的影响[J].食品工业, 2019, 40(7):80-84.YAN Y Z, FENG L L, ZHOU Y P, et al.Effect of different acidic days on the structure of B-type corn microcrystal ine starch[J].The Food Industry, 2019, 40(7):80-84.
[19] WU D, LIN Q Q, SINGH H, et al.Complexation between whey protein and octenyl succinic anhydride (OSA)-modified starch:Formation and characteristics of soluble complexes[J].Food Research International, 2020, 136:109350.
[20] DING W, ZHOU J F, ZENG Y H, et al.Preparation of oxidized sodium alginate with different molecular weights and its application for crosslinking collagen fiber[J].Carbohydrate Polymers, 2017, 157:1650-1656.
[21] 黄敏杰, 马利锋, 尚福林.基于等效特征应变原理的复合材料有效模量细观力学分析[J].固体力学学报, 2022, 43(3):271-283.HUANG M J, MA L F, SHANG F L.Micro-mechanical analysis of effective moduli of composite materials based on the principle of equivalent eigenstrain[J].Chinese Journal of Solid Mechanics, 2022, 43(3):271-283.
[22] 石燕, 闫薇, 涂宗财, 等.辛烯基琥珀酸酐酯化改性阿拉伯胶的工艺优化[J].中国食品学报, 2021, 21(2):203-212.SHI Y, YAN W, TU Z C, et al.Process optimization of esterification modification of Arabic gum with octenyl succinic anhydride[J].Journal of Chinese Institute of Food Science and Technology, 2021, 21(2):203-212.
[23] 石燕, 李翠, 罗琦, 等.辛烯基琥珀酸-阿拉伯胶酯的合成工艺及乳化性能[J].食品科学, 2017, 38(4):211-216.SHI Y, LI C, LUO Q, et al.Synthesis and emulsification properties of octenyl succinic anhydride-modified gum Arabic[J].Food Science, 2017, 38(4):211-216.
[24] 田俊青. OSA疏水改性薯渣纤维素制备高分子吸附剂和Pickering乳液的研究[D].重庆:西南大学, 2019.TIAN J Q.Study of the preparation of polymer adsorbents and Pickering emulsion by OSA hydrophobic modified sweet potato residue cellulose[D].Chongqing:Southwest University, 2019.
[25] YAN C, MCCLEMENTS D J, ZHU Y Q, et al.Fabrication of OSA starch/chitosan polysaccharide-based high internal phase emulsion via altering interfacial behaviors[J].Journal of Agricultural and Food Chemistry, 2019, 67(39):10937-10946.
[26] BOULHAIA I, HADJSADOK A, MOULAI-MOSTEFA N, et al.Impact of octenyl succinic anhydride (OSA) modified starch on the particle size distribution and rheological properties of xanthan gum in aqueous solutions[J].International Journal of Food Engineering, 2020, 16(9):20190279.
[27] LIU Q R, QI J R, YIN S W, et al.Preparation and stabilizing behavior of octenyl succinic esters of soybean soluble polysaccharide in acidified milk beverages[J].Food Hydrocolloids, 2017, 63:421-428.
[28] 李昭成, 杨桂花.流动电位法zeta电位仪的测量原理及使用性能[J].纸和造纸, 2002, 21(4):29-30.LI Z C, YANG G H.Measuring principal and operating performance of zeta potential instrument based on streaming potential[J].Paper and Paper Making, 2002, 21(4):29-30.