便秘作为一种胃肠道症状,在全球的发病率约为10%,严重影响着人们的生产生活。迄今为止,便秘的致病机制仍然未得到明确解析,症状难以得到有效治疗[1]。尽管现有的药物疗法多样,但普遍存在有副作用、耐药性、价格昂贵以及难以长期使用等问题。近年来,肠道菌群已成为科研领域的研究热点,多数研究表明便秘与肠道菌群紊乱存在着紧密的联系,微生态疗法可能是缓解便秘的一个有效手段[2-3]。现有的研究报道了益生菌缓解便秘作用的有效性,可以显著降低肠道转运时间,增加大便次数,改善大便稠度[4]。相较于传统的泻药,益生菌安全且无副作用,因此是良好的替代品。
常见的益生菌包括乳杆菌和双歧杆菌,它们在缓解便秘上都取得了较好的作用,并且作用效果上存在种间差异[5]。本实验所用的两歧双歧杆菌B1是分离自健康人肠道的菌株,通过构建洛哌丁胺造成的便秘小鼠模型,研究其缓解便秘的能力,并初步探讨其机制,针对具有治疗便秘功能的产品开发提供更多思路,为益生菌生物活性疗法的开发和利用奠定基础。
1 材料与方法
1.1 菌株及材料
两歧双歧杆菌B1(CCFM1163)保藏于江南大学生物技术中心菌种保藏库;盐酸洛哌丁胺(loperamide hydrochloride)胶囊,西安杨森制药有限公司;比沙可啶,南京药大制药有限公司;阿拉伯树胶粉、乙酸、丙酸、丁酸、异丁酸、戊酸、异戊酸、活性炭粉,国药集团化学试剂公司;小鼠胃泌素(gastrin,Gas)、小鼠P物质(substance P,SP)、小鼠生长抑制素(somatostatin,SS)、小鼠乙酰胆碱(acetylcholine,Ach)、小鼠五羟色胺(5-hydroxy tryptamine,5-HT)、小鼠一氧化氮合酶(neuronal nitric oxide synthase,nNOS)ELISA试剂盒,南京森贝伽生物;总超氧化物歧化酶(superoxide dismutase,SOD)测定试剂盒、过氧化氢酶(catalase,CAT)测定试剂盒,南京建成生物工程研究所。
1.2 仪器与设备
真空冷冻干燥机,美国LABCONCO公司;Multiscan Go多功能酶标仪、1300-ISQ型Trace GC-MS、Sorvall MX120+型超高速离心机,美国Thermo公司;SCIENTZ-48型组织破碎仪,宁波新芝生物科技股份有限公司。
1.3 动物实验设计
本实验从维通利华实验动物有限公司采购了24只8周大的雄性SPF级C57BL/6 J小鼠。所有的动物程序都是按照江南大学《实验动物护理和使用指南》进行,并得到了江南大学实验动物动物伦理委员会的批准(合格编号:JN.No20220615c1501207[251])。动物饲养间保持在25~2 ℃的温度和50%~5%的相对湿度。所有的动物都能自由地食用标准饲料和饮用水,并在自适应喂养1周后开始动物实验。
参考李亦汉等[6]的实验方法,研究分组信息描述如下:自适应喂养1周后,双歧杆菌组每天灌胃0.2 mL菌悬液(5×109 CFU/mL),阳性对照组灌胃比沙可啶(10 mg/kg BW)持续4周,正常对照组和模型组的小鼠给予生理盐水。从第3周开始,除正常组外,其他各组的小鼠则给予0.2 mL溶解在生理盐水中的盐酸洛派丁胺(10 mg/kg BW),进行造模处理,第5周实验结束后,对体重进行称量,处死并收集相关的样本材料。
1.4 动物实验方法
1.4.1 粪便含水量测定
灌胃后,及时收集粪便并装于事先称重的无菌Eppendorf管中,随后称重获得湿重,后续进行冷冻干燥使水分挥发以得到粪便干重。粪便含水量按公式(1)计算:
粪便含水量![]()
(1)
1.4.2 首例黑便
在实验结束的前1天,灌胃0.2 mL盐酸洛哌丁胺和活性炭的混合物,完成灌胃和排出第一个黑色墨汁颗粒之间的时间间隔记录为每只小鼠的肠道通过时间。
1.4.3 小肠推进率
实验结束当天,除空白对照组灌胃无菌生理盐水和活性炭的混合物,其余各组均灌胃0.2 mL盐酸洛哌丁胺和活性炭的混合物。30 min后小鼠被处死。打开小鼠腹腔后,取出整个小肠段,记录活性炭前段与小肠总长度之间的距离(cm),并按公式(2)计算小肠推进率:
小肠推进率![]()
(2)
1.4.4 组织病理学分析
小鼠的结肠组织固定在4%(体积分数)的中性多聚甲醛溶液中,流水冲洗过夜,在梯度乙醇中脱水。随后,放入纯酒精和二甲苯混合液中进行透明处理。完成后,浸泡于二甲苯和石蜡的混合液中进行60 min浸蜡处理,以组织最大面在底层进行包埋,切片机进行切片并在40 ℃去离子水中进行展开,用载玻片捞出。最后用中性胶密封染色组织切片。中性胶完全凝固后,这些切片被放置在数字组织切片扫描仪中进行观察。
1.4.5 生化分析
用酶联免疫吸附法测定小鼠结肠组织中的中胃肠活性肽SP、SS、Gas的浓度,以及相关的神经递质包括5-HT、Ach、nNOS。用1∶9(质量比)的预冷生理盐水对大约20 mg的小鼠结肠组织进行称重和混合,然后在4 ℃ 下12 000×g进行均质化和离15 min,取组织上清液,采用相应的酶联免疫吸附测定试剂盒中的含量。
1.4.6 短链脂肪酸(short chain fatty acids,SCFA)分析
通过GC-MS测定小鼠粪便中6种短链脂肪酸的含量。称取冻干处理后的小鼠粪便30 mg于饱和氯化钠(0.5 mL)中,加入20 μL 10%硫酸,加入小磁珠在组织匀浆器作用下破碎混合。在通风橱中操作,添加1 mL乙醚萃取SCFA,充分混匀后在4 ℃下以14 000×g离心15 min弃上清液,然后将样品转移至离心管中,加入0.25 g无水硫酸钠脱去多余水分。离心后,取500 μL上清液移到气相小瓶中,利用气相色谱进行后续分析。气相色谱-质谱联用的条件如前文所述[7]。
1.4.7 16S菌群测定
使用Fast DNA Stool Kit(MP Biomedicals,Carlsbad,CA,USA)提取新鲜粪便中细菌的总DNA。使用通用引物(341正向:5′-CCTAYGGGRBGCASCAG-3′和806反向:5′-GGACTACNNGGGGTATCTAAT-3′)进行16S rDNA基因的PCR扩增。PCR产物使用TIAN gel Mini Purification Kit(天根,北京,中国)纯化。按照 Qubit dsDNA 检测试剂盒(Life Technologies,卡尔斯巴德,加利福尼亚州,美国)的说明对 DNA 进行定量并以等浓度汇集。对样品进行条形码标记,并最终按照制造商的方案在 Illumina MiSeq PE300 平台上进行配对末端测序。使用 Quantitative Insights into Microbial Ecology version 2 (QIIME2) 进行 16S rDNA 测序分析。根据采样深度,将每个样品中ASV数量抽平至10 000个。
1.5 统计分析
结果显示为每组的“平均值±标准差”(Mean±SD)。通过单因素方差分析(ANOVA) Dunnett检验进行差异分析。*表示与模型组相比有显著性差异,*:P<0.05,**:P<0.01,***:P<0.001,****:P<0.000 1。
2 结果与分析
2.1 两歧双歧杆菌B1可缓解便秘
在临床上,便秘的主要症状包括粪便传输困难,粪便过硬或过小以及排便次数过少[8]。洛哌丁胺为阿片类药物,可选择性与肠壁阿片受体结合,通过抑制兴奋性肠运动神经元来改变结肠运动,是一种常见的便秘造模方法[9]。在本研究中,如图1所示,在利用盐酸洛派丁胺造模及干预后,各组小鼠的体重和脏器指数无明显差异(P>0.05)与先前的报道一致[10]。从便秘的表观指标来看,根据《保健食品评价技术规范》2022版中缓解便秘阳性结果的评价标准可知,洛哌丁胺干预后,模型组的粪便含水量和小肠推进率均显著低于对照组,且在肠道转运时间上显著长于对照组,表明便秘模型构建成功。
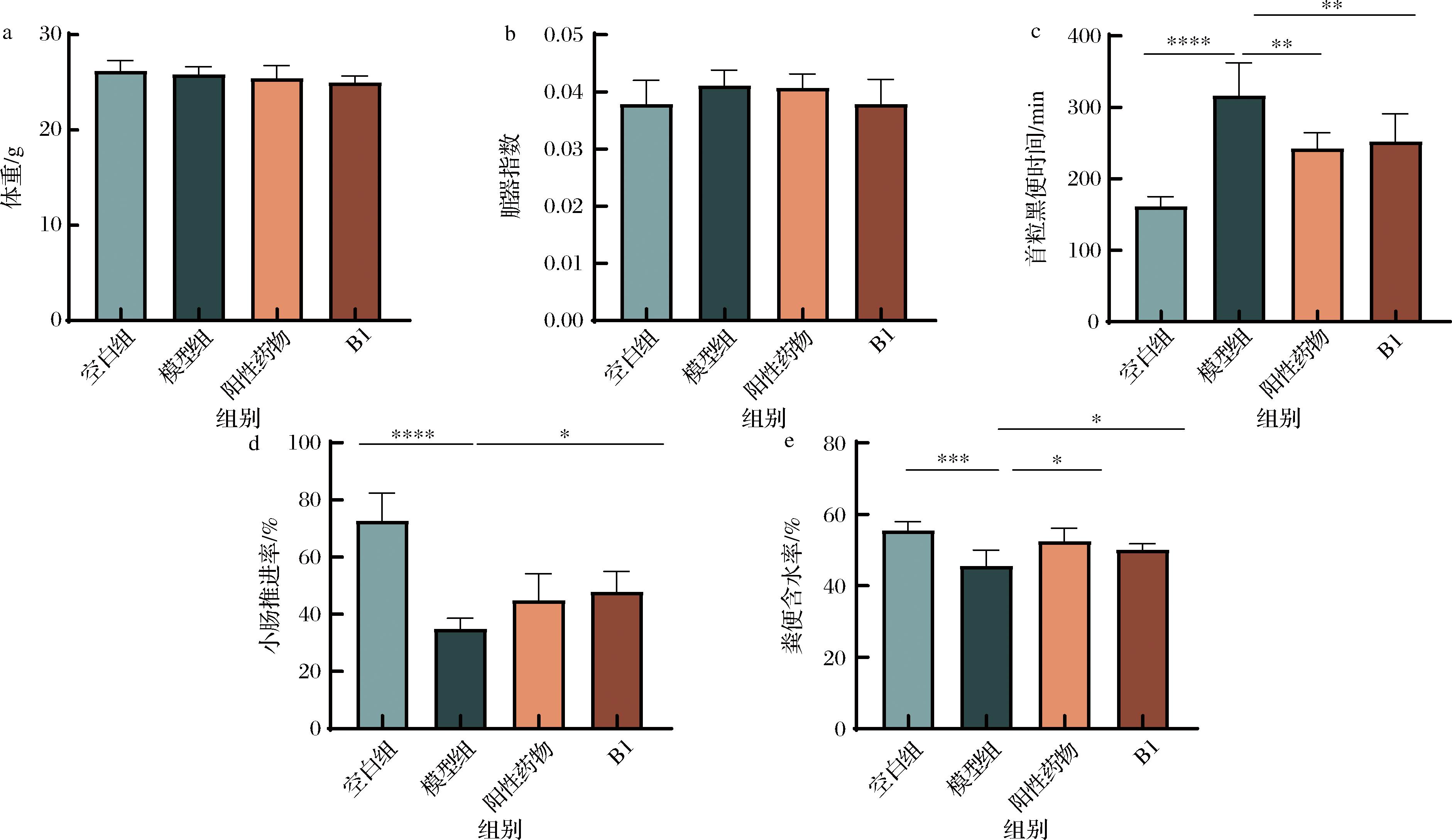
a-体重;b-脏器指数;c-首粒黑便时间;d-小肠推进率;e-粪便含水率
图1 两歧双歧杆菌B1对小鼠便秘相关指标的影响
Fig.1 The effect of Bifidobacterium bifidum B1 on constipation related indicators in mice
注:*表示P<0.05,**表示P<0.01,***表示P<0.001,****表示P<0.000 1(与模型组比较) (下同)。
在应用两歧双歧杆菌B1干预后,两歧双歧杆菌B1能够显著提高粪便含水量(P<0.05)和小肠推进率(P<0.05)并降低肠道转运时间(P<0.01)。基于此,本研究认为两歧双歧杆菌B1在缓解便秘上发挥着良好的功效。
2.2 两歧双歧杆菌B1缓解洛派丁胺诱导的结肠损伤
便秘引起的粪便硬结、肠道转运时间的延缓,很大程度上与结肠组织结构和完整性有关。如图2所示,结肠组织HE染色显示,正常小鼠结肠组织肠壁完整,具有清晰的隐窝结构和杯状细胞边界且组织层较厚,而长期摄入洛派丁胺使得模型组结肠组织出现炎症细胞浸润,隐窝萎缩,黏膜组织较薄并伴随着杯状细胞的减少。经两歧双歧杆菌B1和阳性药物干预后能够缓解便秘诱发的损伤,并提升结肠黏膜厚度。
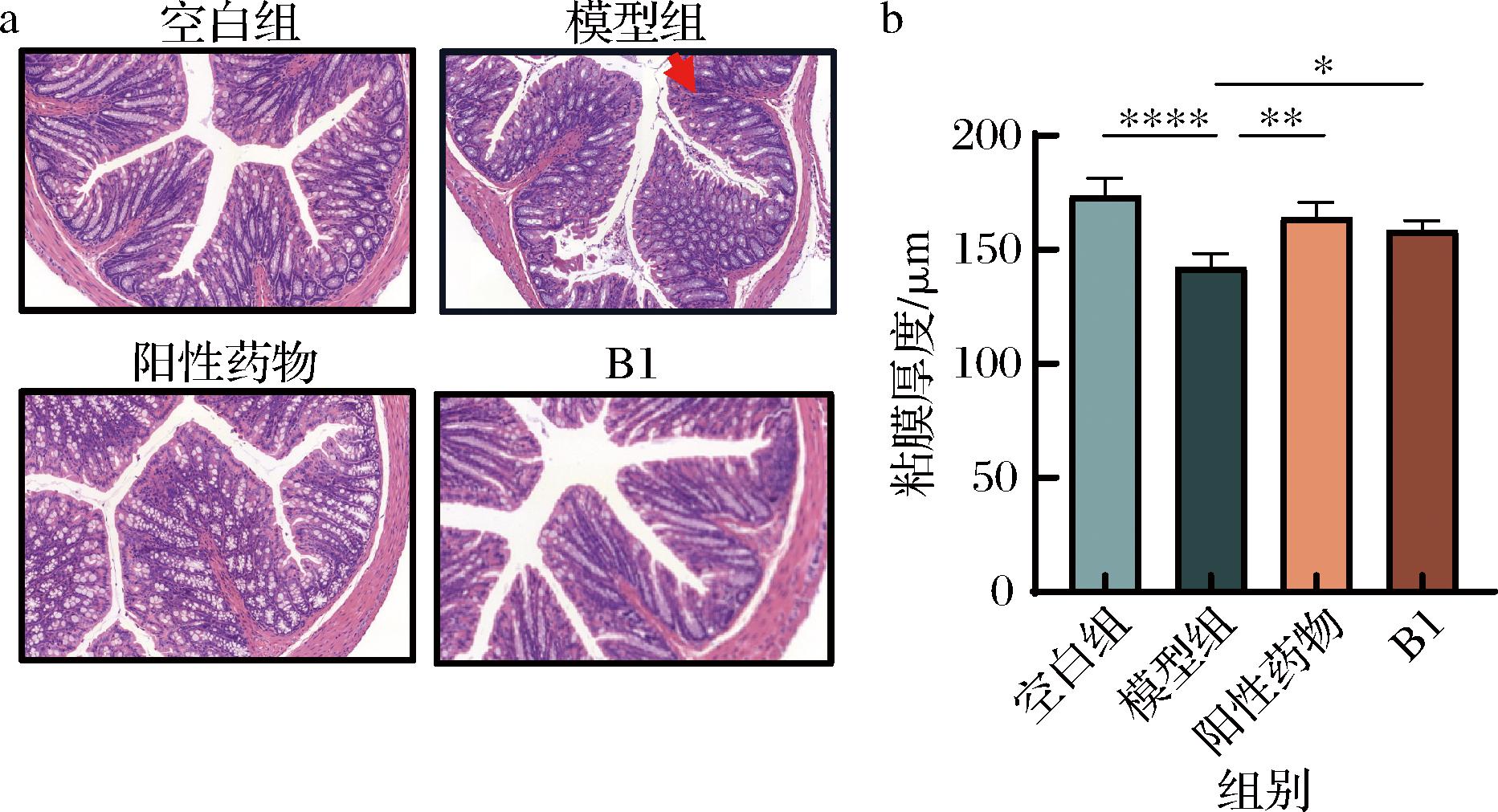
a-HE染色切片;b-黏膜厚度
图2 结肠切片HE染色
Fig.2 HE staining of colon sections
2.3 两歧双歧杆菌B1显著提高Gas的水平
胃肠活性肽在肠道转运中发挥着重要的作用。报道称,P物质(SP)在调节肠道、刺激肠道蠕动以及增加结肠收缩和蠕动方面发挥着重要的作用[11]。生长抑素(SS)能够抑制平滑肌收缩[12]。胃泌素(Gas)有助于促进幽门括约肌松弛和胃肠平滑肌收缩[13]。如图3所示,通过对结肠匀浆上清液胃肠活性肽的测定发现,便秘组小鼠结肠组织中SP(P<0.05)、和Gas(P<0.05)水平低于正常组,并伴随着SS水平升高(P>0.05)。说明两歧双歧杆菌B1提升了结肠组织中SP的水平,降低了SS水平,并显著性地提升了Gas水平(P<0.05)。
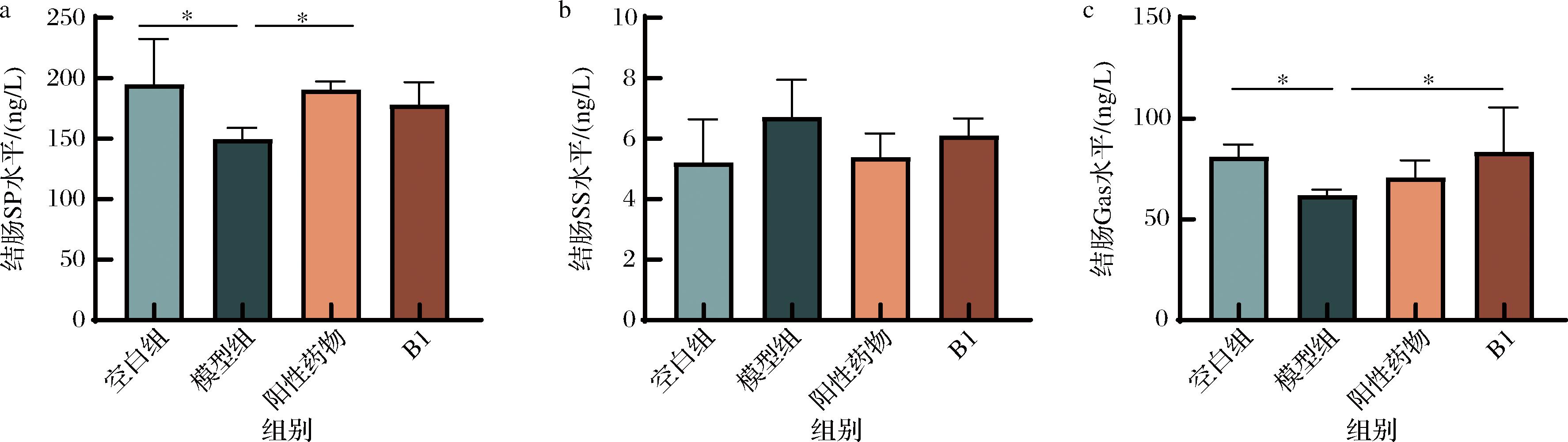
a- SP水平;b-SS水平;c-Gas水平
图3 两歧双歧杆菌B1对小鼠便秘相关胃肠活性肽的影响
Fig.3 The effect of Bifidobacterium bifidum B1 on constipation related gastrointestinal active peptides in mice
2.4 两歧双歧杆菌B1对小鼠便秘相关神经递质的影响
便秘引发的肠神经系统异常,导致肠神经递质释放异常,可能是便秘的主要原因之一[14]。结肠神经递质包括兴奋性神经递质和抑制性神经递质,常见的兴奋性神经递质Ach能够直接刺激平滑肌收缩,5-HT 能够与5-HTR4受体结合促进胃肠蠕动[15]。此外,神经元nNOS是负责释放抑制性神经递质NO的关键酶,通过释放NO抑制结肠蠕动[16]。如图4所示,相较正常组,模型组中nNOS含量上升(P<0.01),并伴随着5-HT(P<0.05)、Ach(P<0.05)水平的显著降低,两歧双歧杆菌B1的干预能够显著提升兴奋性神经递质5-HT(P<0.001)、Ach(P<0.01)的水平,并降低抑制性nNOS的水平。
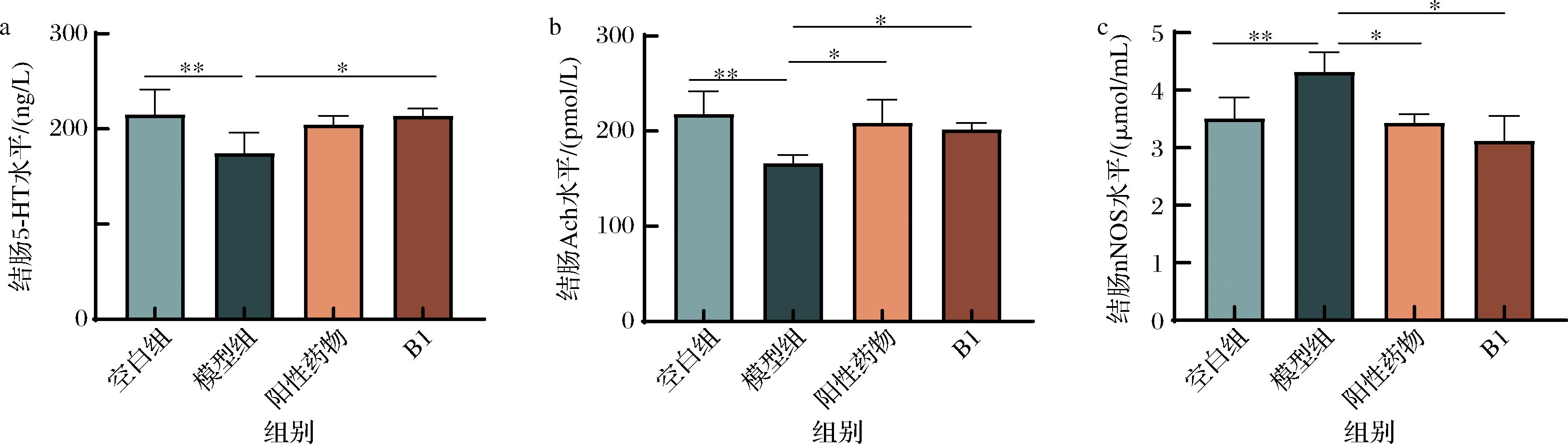
a-5-HT水平;b-Ach水平;c-nNOS水平
图4 两歧双歧杆菌B1对小鼠便秘相关神经递质的影响
Fig.4 The effect of Bifidobacterium bifidum B1 on constipation related neurotransmitters in mice
2.5 两歧双歧杆菌B1可显著提高SOD的水平
慢性便秘或引起潜在的氧化应激,对机体具有较强的细胞毒性作用,可损伤肠黏膜细胞,引起肠黏膜功能障碍,诱发或加重便秘[17]。SOD催化超氧化物自由基的歧化可清除自由基,并且CAT和SOD在增强自由基的作用中发挥协同作用[18]。通过对SOD和CAT两种抗氧化酶活力进行了测定发现,相较于正常组(图5),便秘小鼠在结肠组织中的SOD(P<0.001)和CAT(P<0.05)活力显著降低,而在阳性药物的干预下逆转了相应指标的变化,此外,长双歧杆菌B1提升了结肠SOD的活力。便秘会对机体造成氧化应激损伤,补充两歧双歧杆菌B1增强了结肠组织的内源性抗氧化能力。

a-SOD;b-CAT
图5 两歧双歧杆菌B1对小鼠便秘相关氧化应激的影响
Fig.5 The effect of Bifidobacterium bifidum B1 on constipation related oxidative stress in mice
2.6 两歧双歧杆菌B1可显著提高乙酸和异戊酸的水平
SCFA是由肠道微生物群发酵膳食纤维产生的,是肠腔环境中的一种重要的代谢物。由图6可知,相较正常组,模型组粪便中乙酸(P<0.001)和戊酸(P<0.05)含量显著降低,而阳性药物组和两歧双歧杆菌B1能够显著提升便秘小鼠粪便中乙酸的含量,此外两歧双歧杆菌B1还显著提升了异戊酸的水平(P<0.05)。临床研究显示,便秘患者粪便中乙酸含量会出现下调的情况,可能是引发便秘的潜在原因[19]。然而结肠靶向释放乙酸的实验发现,乙酸能够提升推进率和粪便含水量,以改善便秘[20]。因此,在这里乙酸可能是两歧双歧杆菌B1发挥作用的一个关键代谢物。
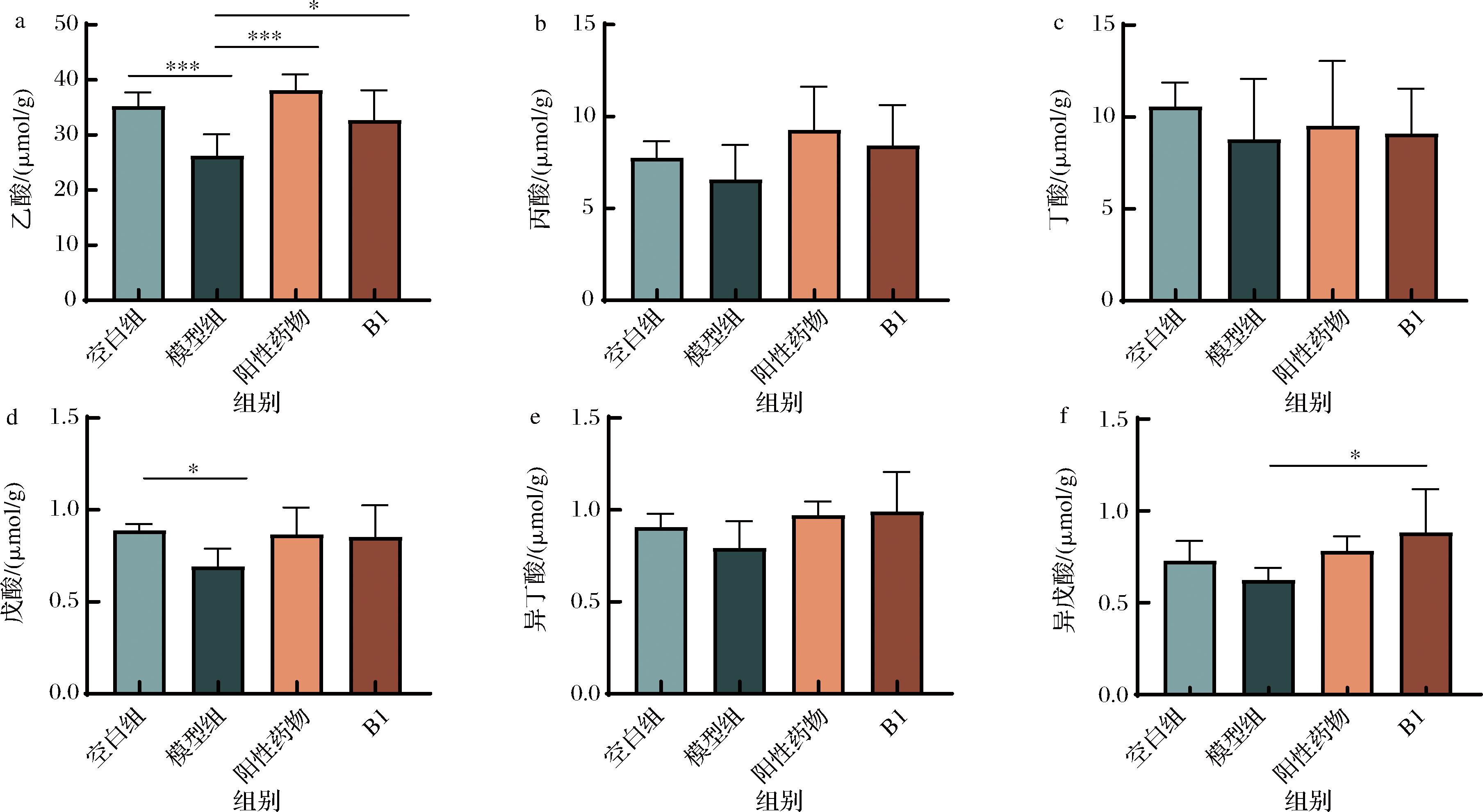
a-乙酸;b-丙酸;c-丁酸;d-戊酸;e-异丁酸;f-异戊酸
图6 两歧双歧杆菌B1对小鼠盲肠内容物中短链脂肪酸含量的影响
Fig.6 The effect of Bifidobacterium bifidum B1 on the content of short chain fatty acids in the cecal contents of mice
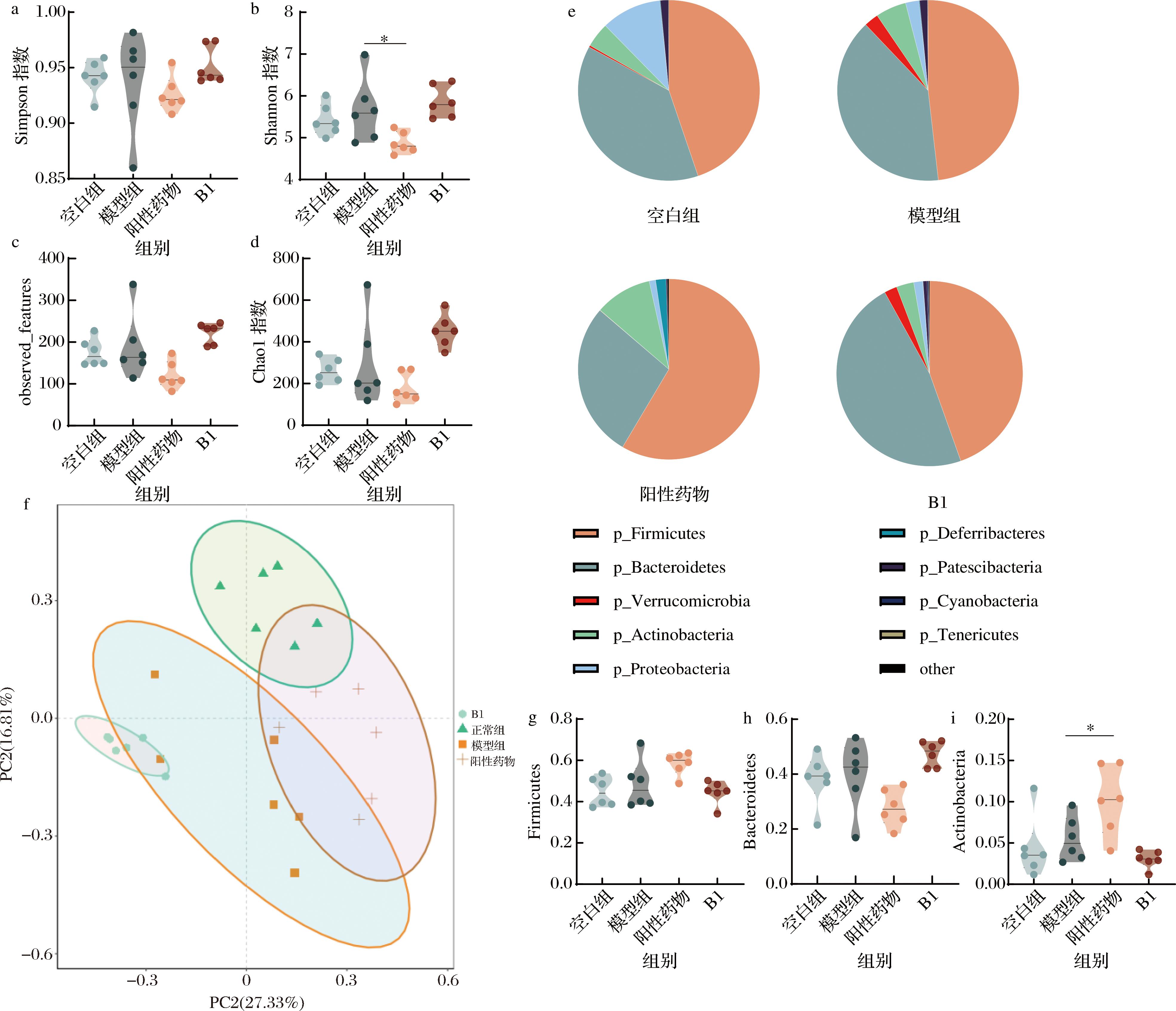
a-Simpson指数;b-Shannon指数;c-observed_features;d-Chao1指数;e-门水平;f-PCoa图;g-Firmicutes;h-Bacteroidetes;i-Actinobacteria
图7 两歧双歧杆菌B1对小鼠菌群多样性和门水平的影响
Fig.7 The effect of Bifidobacterium bifidum B1 on microbial diversity and phylum level in mice
2.7 两歧双歧杆菌B1调节肠道菌群
调节肠道菌群结构是益生菌发挥缓解便秘作用的一个重要的机制。本研究分析了阳性药物和两歧双歧杆菌B1干预对洛派丁胺便秘小鼠肠道微生物的影响。对Shannon指数、Chao1指数、observed_features以及Simpson指数进行分析显示,洛派丁胺和两歧双歧杆菌B1的干预均未能显著性改变肠道菌群的α多样性。然而,β多样性结果分析,正常和模型组小鼠的肠道菌群明显分离,而长双歧杆菌B1干预后偏离模型组,没有完全恢复粪便微生物群的结构,但有别于未干预的便秘小鼠的肠道菌群,并且阳性药物比沙可啶引起的菌群改变向正常组靠近。
如图7所示,进一步对菌群结构进行分析发现,门水平上,Firmicutes和Bacteroidetes在肠道菌群中占主导地位。洛派丁胺干预下的小鼠肠道菌群中的Firmicutes和Bacteroidetes的相对丰度均有一定程度上升,而双歧杆菌B1干预后显著下调了小鼠肠道中Firmicutes相对丰度,上调了Bacteroidetes相对丰度。需要注意的是各组之间的相对丰度差异并不显著(P>0.05)。
属水平上,如图8所示,相较正常组,洛派丁胺造模干预后小鼠肠腔内容物中的Lactobacillus、Staphylococcus、Alistipes、Enterorhabdus、Streptococcus、Faecalibaculum菌属丰度显著降低,而在 Parasutterella、lleibacterium、Romboutsia、Lachnospiraceae NK4B4 group、Muribaculum、[Eubacterium] fissicatena group菌属丰度上显著升高。
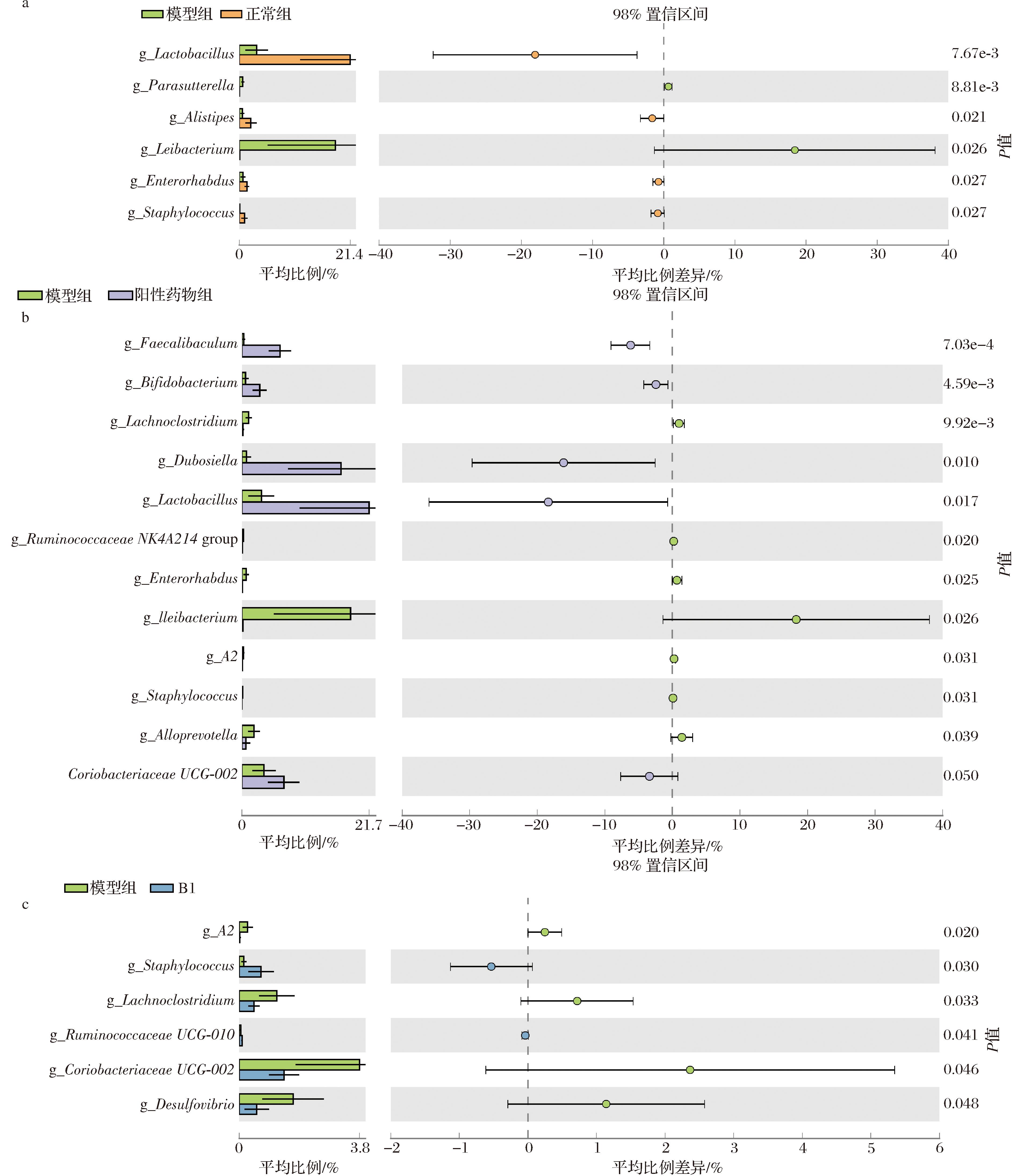
a-模型组vs正常组;b-模型组vs阳性药物组;c-模型组vs B1
图8 Stamp分析两歧双歧杆菌B1对便秘小鼠肠道菌群的影响
Fig.8 Stamp analysis of the effect of Bifidobacterium bifidum B1 on the microbiota of constipated mice
然而,在长双歧杆菌B1的干预下,Ruminococcaceae UCG-010、Staphylococcus菌属的丰度上升。而A2、Lachnoclostridium、Coriobacteriaceae UCG-002、Desulfovibrio菌属的丰度下降。在这里特别注意到,Ruminococcaceae UCG-010被报道称为一种乙酸细菌[21],Staphylococcus被报道可能与杂粮发酵产生的乳酸和醋酸盐相关[22]。因此,这2种菌丰度的增加可能是粪便中乙酸水平上升的原因。此外,在阳性药物比沙可啶的干预下,Faecalibaculum、Bifidobacterium、Dubosiella、Lactobacillus、Coriobacteriaceae UCG-002的丰度显著上升,而Lachnoclostridium、Ruminococcaceae NK4A214 group、Enterorhabdus、Ileibacterium、A2、Staphylococcus、Alloprevotella的丰度显著下降。这些结果表明两歧双歧杆菌B1的干预显著改变了肠道菌群。
3 结论
本研究从两歧双歧杆菌B1调节肠腔代谢物和肠道菌群的作用展开。结果发现两歧双歧杆菌B1能够显著改善便秘小鼠Ach、5-HT、nNOS、Gas的水平,并提升SOD、CAT活力,调节肠道菌群并促进肠道内 Ruminococcaceae UCG-010、Staphylococcus菌属的丰度上升,A2、Lachnoclostridium、Coriobacteriaceae UCG-002、Desulfovibrio菌属的丰度下降,并显著改善肠腔内容物短链脂肪酸乙酸的水平,以缓解便秘。
[1] ZHANG T, LIU W X, LU H M, et al.Lactic acid bacteria in relieving constipation:Mechanism, clinical application, challenge, and opportunity[J].Critical Reviews in Food Science and Nutrition, 2023:1-24.
[2] OHKUSA T, KOIDO S, NISHIKAWA Y, et al.Gut microbiota and chronic constipation:A review and update[J].Frontiers in Medicine, 2019, 6:19.
[3] YANG L, WANG Y, ZHANG Y, et al.Gut microbiota:A new avenue to reveal pathological mechanisms of constipation[J].Applied Microbiology and Biotechnology, 2022, 106(21):6899-6913.
[4] ZHANG C C, JIANG J C, TIAN F W, et al.Meta-analysis of randomized controlled trials of the effects of probiotics on functional constipation in adults[J].Clinical Nutrition, 2020, 39(10):2960-2969.
[5] WANG L L, HU L J, XU Q, et al.Bifidobacteria exert species-specific effects on constipation in BALB/c mice[J].Food &Function, 2017, 8(10):3587-3600.
[6] 李亦汉, 王琳琳, 赵建新,等.两歧双歧杆菌CCFM1167通过提升肠道中乙酸水平以抑制炎症从而缓解便秘[J].食品与发酵工业, 2023, 49(6):35-41.LI Y H, WANG L L, ZHAO J X, et al.Constipation relief by increasing intestinal acetate level to suppress inflammation using Bifidobacterium bifidum CCFM1167[J].Food and Fermentation Industries, 2023, 49(6):35-41.
[7] MEI L Y, CHEN Y, WANG J L, et al.Lactobacillus fermentum stimulates intestinal secretion of immunoglobulin a in an individual-specific manner[J].Foods,2022,11(9):1229.
[8] WALD A.JAMA PATIENT PAGE.Constipation[J].JAMA, 2016, 315(2):214.
[9] HEITMANN P T, KEIGHTLEY L, WIKLENDT L, et al.The effects of loperamide on excitatory and inhibitory neuromuscular function in the human colon[J].Neurogastroenterology and Motility, 2022, 34(11):e14442.[10] HE Y H, LIU G, XIA C, et al.Laxative effect of mulberry ferment on two models of constipated mice[J].Journal of Functional Foods, 2022, 90:104971.
[11] JIN X, GUAN Y T, BAI H, et al.Effects of sEA on slow transit constipation through the microbiota-gut-brain axis in rats[J].Evidence-Based Complementary and Alternative Medicine:eCAM, 2020, 2020:8828846.
[12] NIU Y Y, WANG J Y, WANG P Y, et al.Effect of Malus halliana koehne polysaccharides on functional constipation[J].Open Chemistry, 2018, 16(1):956-962.
[13] ZHOU X, MAO B Y, TANG X, et al.Exploring the dose-effect relationship of Bifidobacterium longum in relieving loperamide hydrochloride-induced constipation in rats through colon-released capsules[J].International Journal of Molecular Sciences, 2023, 24(7):6585.
[14] HOLLAND A M, BON-FRAUCHES A C, KESZTHELYI D, et al.The enteric nervous system in gastrointestinal disease etiology[J].Cellular and Molecular Life Sciences:CMLS, 2021, 78(10):4713-4733.
[15] HOFFMAN J M, TYLER K, MACEACHERN S J, et al.Activation of colonic mucosal 5-HT(4) receptors accelerates propulsive motility and inhibits visceral hypersensitivity[J].Gastroenterology, 2012, 142(4):844-854.
[16] NISHIZAKI K, NAKAO K, ISHII H, et al.Induction of neuronal nitric oxide synthase by sympathetic denervation is mediated via alpha 2-adrenoceptors in the jejunal myenteric plexus[J].Brain Research, 2003, 965(1-2):121-129.
[17] ZHOU J F, LOU J G, ZHOU S L, et al.Potential oxidative stress in children with chronic constipation[J].World Journal of Gastroenterology, 2005, 11(3):368-371.
[18] LIU B H, XIAO X, ZHOU X R, et al.Effects of Lactobacillus plantarum CQPC01-fermented soybean milk on activated carbon-induced constipation through its antioxidant activity in mice[J].Food Science &Nutrition, 2019, 7(6):2068-2082.
[19] WANG L Y, WANG L L, TIAN P J, et al.A randomised, double-blind, placebo-controlled trial of Bifidobacterium bifidum CCFM16 for manipulation of the gut microbiota and relief from chronic constipation[J].Food &Function, 2022, 13(3):1628-1640.
[20] WANG L L, CEN S, WANG G, et al.Acetic acid and butyric acid released in large intestine play different roles in the alleviation of constipation[J].Journal of Functional Foods, 2020, 69:103953.
[21] HAN X Y, LEI X J, YANG X X, et al.A metagenomic insight into the hindgut microbiota and their metabolites for dairy goats fed different rumen degradable starch[J].Frontiers in Microbiology, 2021, 12:651631.
[22] XU L, YU Q R, MA L X, et al.In vitro simulated fecal fermentation of mixed grains on short-chain fatty acid generation and its metabolized mechanism[J].Food Research International, 2023, 170:112949.