机体的免疫应答由多种细胞类型驱动,并由细胞因子介导,主要分为两大类:非特异性免疫和特异性免疫。非特异性免疫通过皮肤、黏膜、巨噬细胞、NK细胞、炎症因子等提供机体免疫的第1道防线。特异性免疫包括主要由T淋巴细胞介导的细胞免疫和B淋巴细胞介导的体液免疫[1]。脾脏是动物外周免疫器官,富含T淋巴细胞、B淋巴细胞和巨噬细胞,是体液免疫和细胞免疫的中心,而胸腺是机体的一级免疫器官,对T细胞成熟和分化起重要作用[1]。T淋巴细胞和B淋巴细胞活性和增殖分化能力可以通过免疫球蛋白和细胞因子水平反应。其中免疫球蛋白是机体在感染方面的重要屏障,分泌型IgA、IgG、IgM是血清中的主要抗体成分,通常这三类免疫球蛋白水平就可以代表免疫球蛋白的总体水平[2]。细胞因子中IL-12主要是激活的炎性细胞产生的,IFN-γ可介导细胞免疫功能,可通过调节巨噬细胞、NK细胞的生长增强免疫调节作用[1]。
近年来,由于慢性病、不健康生活方式等原因,免疫功能失调的发生率不断增加[3]。过敏性鼻炎是由IgE介导的鼻黏膜非传染性慢性炎症性疾病,当过敏个体暴露于刺激性过敏原后,大量炎性细胞浸润鼻炎膜组织,辅助性T细胞释放细胞因子(如IL-4和IL-5等),促进浆细胞产生大量IgE,肥大细胞与IgE结合会触发组胺等介质的释放,导致小动脉扩张、血管通透性增加、瘙痒、鼻漏、黏液分泌和肺平滑肌收缩等[4]。它的主要特征是鼻黏膜和分泌物中的嗜酸性粒细胞增多[5]。
为发挥免疫系统的最佳功能,合理的膳食是提高机体免疫力的有效方式,即可以通过蛋白质、脂质、碳水化合物、维生素等营养素的科学摄入来改善机体的免疫功能[6]。其中蛋白质不仅是构成机体免疫反应的基础物质,还是免疫器官、免疫细胞和免疫因子的主要成分。乳清蛋白来源于牛奶乳清,属于优质蛋白质,并具有独特的营养功能和生物活性;但因其分子质量大,需要水解为小分子短肽或游离氨基酸后,才能被机体吸收利用[7]。乳清蛋白肽(whey hydrolyzed peptides,WHPs)是通过水解技术从乳清蛋白中分离得到的小分子生物活性肽类混合物,其特点是蛋白吸收率高,有利于促进肌肉生长,并且具有低致敏和低抗原性,更适合过敏体质人群使用。曾志等[7]研究证明了水解乳清蛋白配方在过敏性婴幼儿中的应用能增加NK细胞亚群分布,抑制细胞因子释放等。
本文首先以WHPs为干预物,对WHPs干预后小鼠的特异性和非特异性免疫功能变化进行评价;其次建立小鼠过敏性鼻炎模型,测定血清及鼻腔灌洗液中的组胺水平、血清中细胞因子和免疫球蛋白水平,并进行病理组织染色观察,以评价WHPs对过敏症状的改善作用。同时将WHPs和乳清蛋白的免疫效果进行了比较。
1 材料与方法
1.1 材料与试剂
1.1.1 实验动物
健康6~8周龄BALB/c雌性小鼠250只,重18~22 g,北京大学医学部实验动物中心。小鼠分笼饲养于北京大学医学部实验动物部,每笼5只,饲养及试验期间饲料为SPF级基础饲料自由饮食和饮水。动物室温度(25±1) ℃,相对湿度50%~60%,室内照明控制在12 h/12 h光暗周期节律。动物喂养及实验设计严格按照《北京市实验动物管理条例》执行,并经过北京大学医学部伦理委员会审核通过。
1.1.2 实验材料
WHPs,乳白色固体粉末。本研究所用WHPs来自Hilmar公司生产的乳清蛋白肽(水解型)WHPs 8350,其水解度为12.5%,蛋白质含量82%,分子质量<1 000 Da的低聚肽占40.5%,分子质量<5 000 Da的低聚肽占67.2%。
1.1.3 实验试剂
刀豆蛋白A(concanavalin A,ConA),上海源叶有限公司;乳酸锂,郑州宇控生物科技有限公司;硝基氯化四氮唑,湖北广奥生物科技有限公司;氧化性辅酶I,上海康朗生物科技有限公司;甲基噻唑基四唑,上海源叶有限公司;胎牛血清,杭州江滨生物技术有限公司;姬姆萨染液,上海尚宝生物科技有限公司;绵羊红细胞(sheep red blood cell,SRBC),北京大学医学部实验动物中心;鼠T淋巴瘤细胞系(YAC-1细胞),北京大学毒理学系;氢氧化铝凝胶佐剂,上海迈弘生物科技有限公司;Elisa试剂盒,上海丽臣生物科技有限公司。
1.3 实验方法
1.3.1 分组及干预方式
将200只雌性小鼠经适应性喂养3 d后按体重随机分为5组,每组40只。组别分别为1个空白对照组(灌胃蒸馏水)、1个乳清蛋白对照组(灌胃1.5 g/kg·bw乳清蛋白溶液)、3个WHPs剂量组(分别灌胃0.3、1.5、3.0 g/kg·bw的WHPs溶液)。每组小鼠随机分为4个亚组,每个亚组进行不同的实验测定[8]。各组别灌胃液体量均为10 mL/kg·bw,以蒸馏水配制,每日1次经口给予,连续干预30 d。动物喂养及设计严格按照《北京市实验动物管理条例》执行,并经过北京大学生物医学伦理委员会审核通过,审核编号:LA2021477。
1.3.2 体重、摄食情况及免疫器官指数计算
体重及摄食情况:每周称量并记录小鼠体重和剩余饲料量,计算摄食量。在实验结束后,将小鼠称重后处死,取出脾脏和胸腺,称重并计算免疫器官指数。
1.3.3 小鼠特异性免疫功能评价
1.3.3.1 小鼠细胞免疫评价
通过迟发型变态反应和ConA诱导的小鼠淋巴细胞转化实验评价小鼠的细胞免疫功能改变。淋巴细胞的增殖能力以加ConA孔与不加ConA孔的光密度差值表示。在各组小鼠干预第26天时,通过SRBC诱导的小鼠迟发型变态反应(delayed type hypersensitivity,DTH),以第30天及第31天小鼠左后足跖的厚度差值来表示DTH的程度[8]。
1.3.3.2 小鼠血清细胞因子和免疫球蛋白水平的测定
试验结束后,小鼠内眦采血,经3 000 r/min离心10 min收集血清分装后贮存于-80 ℃冰箱中待测。采用液态悬浮芯片法和检测试剂盒[9],检测11种细胞因子免疫球蛋白IgA、IgM、IgG水平。
1.3.4 小鼠非特异性免疫应答评价
通过小鼠腹腔巨噬细胞吞噬鸡红细胞实验评价单核-巨噬细胞功能,计算吞噬百分率。通过乳酸脱氢酶法检测小鼠NK细胞活性[8]。
1.3.5 过敏性鼻炎小鼠模型建立及检测
1.3.5.1 过敏性鼻炎小鼠模型建立
本研究建立的模型为卵白蛋白联合4%(质量分数)氢氧化铝凝胶免疫佐剂致小鼠过敏性鼻炎模型。模型构建方法参照CHOI等[5]研究,对照组用生理盐水代替。每次鼻腔激发时的20 min内,观察小鼠打喷嚏和鼻腔瘙痒动作次数,模型组打喷嚏和鼻腔瘙痒次数显著大于对照组即视为模型建立成功。
之后将50只小鼠按体重随机分为5个组,每组10只,分别为空白对照组,模型对照组,WHPs低剂量组、WHPs中剂量组、WHPs高剂量组。空白对照组小鼠不经历造模过程,而其他组小鼠在模型建成后每日以固定时间灌胃给予各组相应受试物,干预周期为14 d。WHPs低剂量组给予0.3 g/kg·bw乳清蛋白肽,WHPs中剂量组给予1.5 g/kg·bw乳清蛋白肽,WHPs高剂量组给予3.0 g/kg·bw乳清蛋白肽。模型对照组和空白对照组均给予等量无菌蒸馏水。
1.3.5.2 过敏性鼻炎小鼠免疫功能检测
小鼠在灌胃14 d后,称小鼠体重,各脏器系数测定和计算方法同1.3.2节。之后参照CHOI等[5]测定小鼠血清及鼻腔灌洗液中组胺含、血清免疫蛋白以及血清炎症因子。参照JANG等[10]的方法将小鼠鼻腔组织进行HE和天狼猩红染色,对组织中嗜酸性粒细胞进行计数。
1.4 统计分析
采用IBM SPSS 24.0统计软件进行统计学分析,实验数据以“均数±标准差![]() 表示,对数据进行单因素方差分析或重复度量的方差分析;对非正态或方差不齐的数据进行适当的变量转换,待满足正态或方差齐要求后,用转换后的数据进行统计;若变量转换后未达到正态或方差齐的目的,对数据进行Kruskal-Wallis秩和检验。以P<0.05为差异显著性标准。采用Graphpad Prism 9.5.1软件作图。
表示,对数据进行单因素方差分析或重复度量的方差分析;对非正态或方差不齐的数据进行适当的变量转换,待满足正态或方差齐要求后,用转换后的数据进行统计;若变量转换后未达到正态或方差齐的目的,对数据进行Kruskal-Wallis秩和检验。以P<0.05为差异显著性标准。采用Graphpad Prism 9.5.1软件作图。
2 结果与分析
2.1 WHPs对小鼠体重及免疫器官指数的影响
WHPs干预的各组小鼠初始体重、终末体重、胸腺指数和脾脏指数均无统计学差异(P>0.05),见表1。
表1 WHPs对小鼠体重及免疫器官指数的影响(n=10)
Table 1 Effects of WHPs on body weight and immune organ index in mice(n=10)
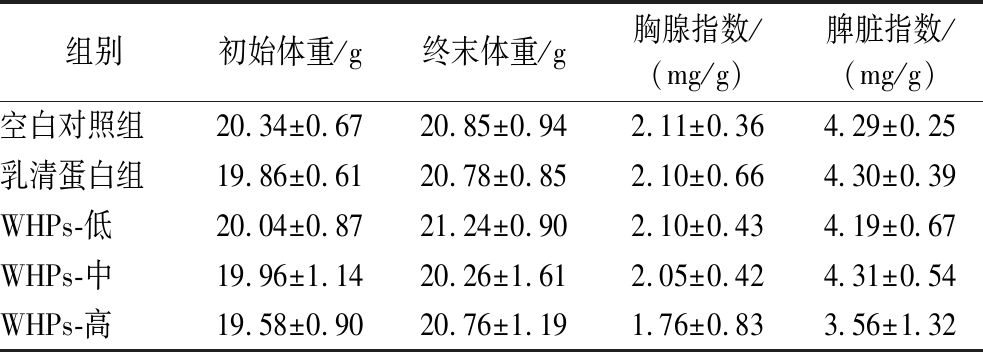
注:脾脏指数=脾脏/体重;胸腺指数=胸腺/体重。
组别初始体重/g终末体重/g胸腺指数/(mg/g)脾脏指数/(mg/g)空白对照组20.34±0.6720.85±0.942.11±0.364.29±0.25乳清蛋白组19.86±0.6120.78±0.852.10±0.664.30±0.39WHPs-低20.04±0.8721.24±0.902.10±0.434.19±0.67WHPs-中19.96±1.1420.26±1.612.05±0.424.31±0.54WHPs-高19.58±0.9020.76±1.191.76±0.833.56±1.32
2.2 WHPs对小鼠特异性免疫应答的影响
2.2.1 WHPs对小鼠细胞免疫的影响
如图1所示,脾淋巴细胞增殖能力的血清光密度差值在各组小鼠中无显著差异(P>0.05)。WHPs高剂量组干预小鼠的足跖增厚度较空白组显著高(P<0.05),且WHPs干预各组小鼠足跖厚度皆显著高于乳清蛋白对照组小鼠足跖厚度(P<0.05)。
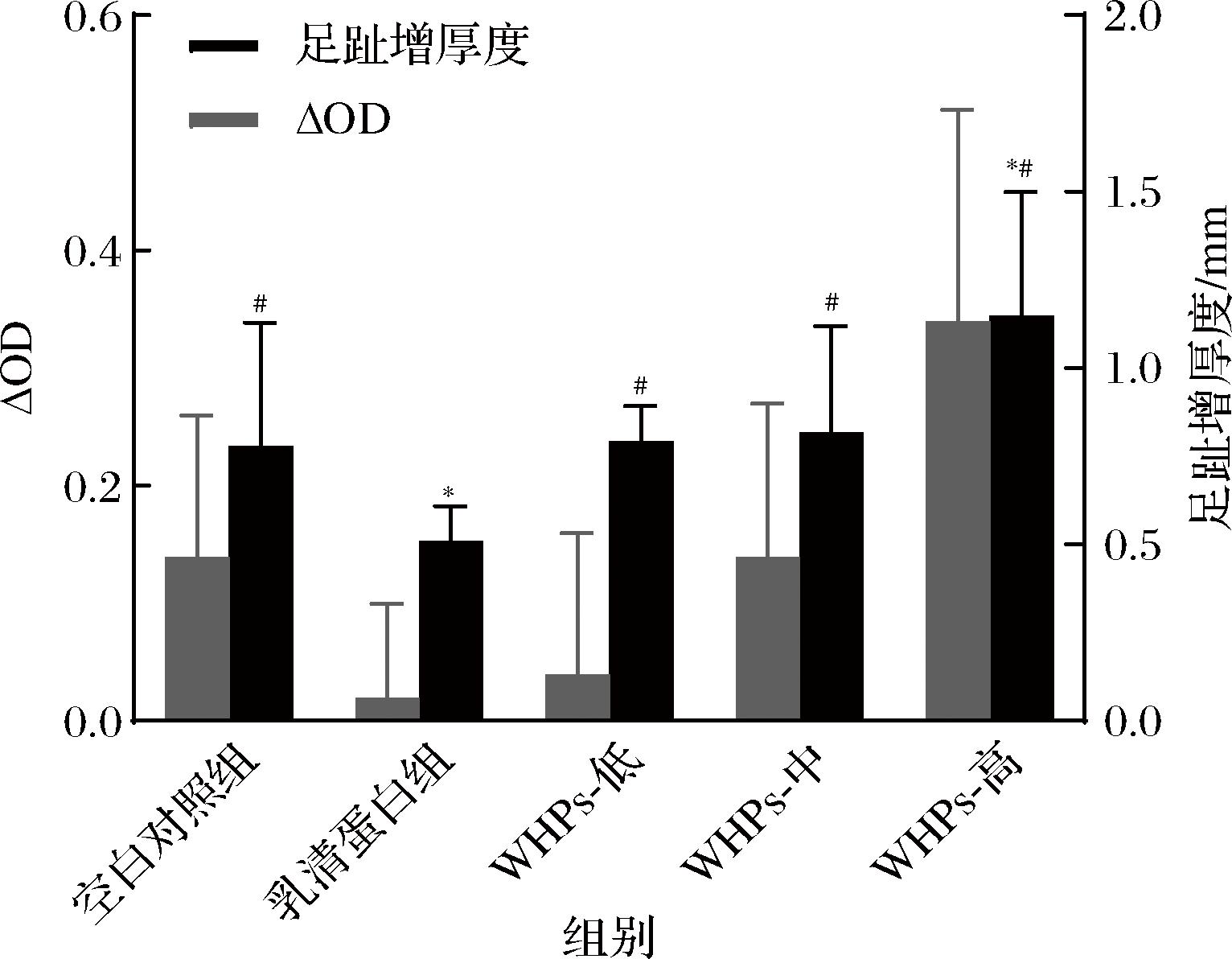
图1 WHPs对小鼠脾淋巴细胞增值和足跖增厚量的影响
Fig.1 Effect of WHPs on splenic lymphocyte proliferation and plantar thickening in mice
注:*表示与空白对照组相比,差异有统计学意义(P<0.05);#表示与乳清蛋白组相比,差异有统计学意义(P<0.05)。
2.2.2 WHPs对小鼠血清细胞因子和免疫球蛋白的影响
免疫球蛋白水平如表2所示,WHPs低剂量组小鼠血清IgM水平较空白对照组和乳清蛋白对照组均有显著提高(P<0.05)。WHPs高剂量组小鼠血清IgG水平较乳清蛋白对照组有显著提升(P<0.05),WHPs低剂量组小鼠血清IgA水平较乳清蛋白对照组有显著提升(P<0.05)。如表3所示,WHPs低剂量组干预小鼠血清IL-12水平较空白对照组显著增高(P<0.05),WHPs中剂量小鼠血清IFN-γ水平较空白对照组有显著增高(P<0.05),但是WHPs各干预组和乳清蛋白干预组小鼠的血清细胞因子水平之间均无显著性差异。
表2 WHPs对小鼠血清免疫球蛋白水平的影响
Table 2 Effect of WHPs on serum immunoglobulin levels in mice
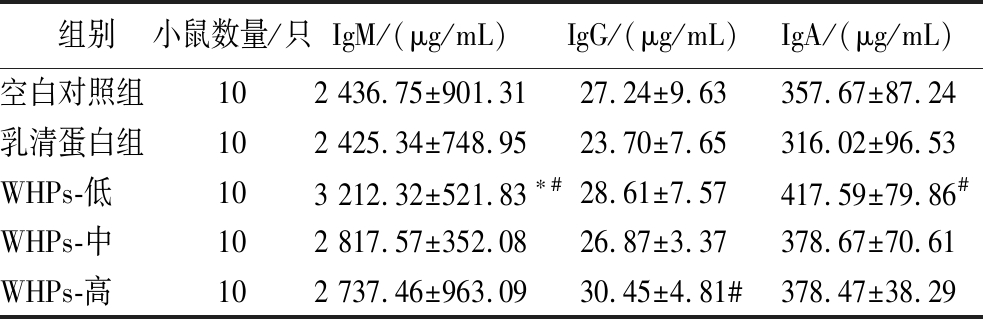
注:*表示与空白对照组相比,差异有统计学意义(P<0.05);#表示与乳清蛋白组相比,差异有统计学意义(P<0.05)(表3同)。
组别小鼠数量/只IgM/(μg/mL)IgG/(μg/mL)IgA/(μg/mL)空白对照组102 436.75±901.3127.24±9.63357.67±87.24乳清蛋白组102 425.34±748.9523.70±7.65316.02±96.53WHPs-低103 212.32±521.83∗#28.61±7.57417.59±79.86#WHPs-中102 817.57±352.0826.87±3.37378.67±70.61WHPs-高102 737.46±963.0930.45±4.81#378.47±38.29
表3 WHPs对小鼠血清细胞因子的影响
Table 3 Effect of WHPs on the content of serum cytokines in mice
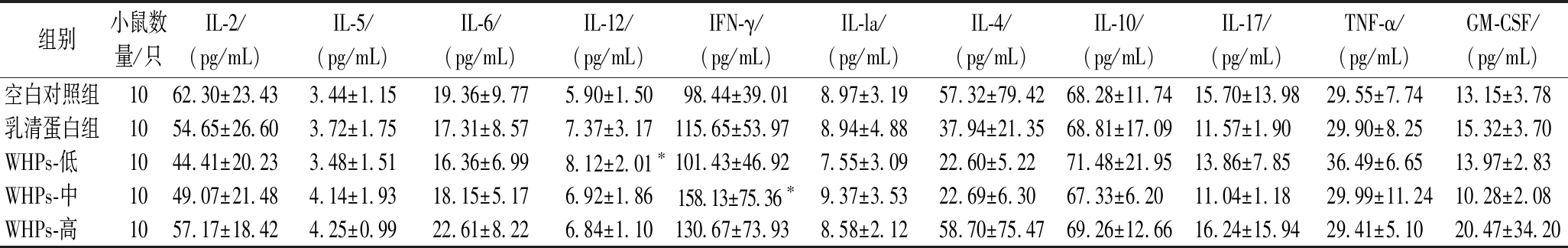
组别小鼠数量/只IL-2/(pg/mL)IL-5/(pg/mL)IL-6/(pg/mL)IL-12/(pg/mL)IFN-γ/(pg/mL)IL-la/(pg/mL)IL-4/(pg/mL)IL-10/(pg/mL)IL-17/(pg/mL)TNF-α/(pg/mL)GM-CSF/(pg/mL)空白对照组1062.30±23.433.44±1.1519.36±9.775.90±1.5098.44±39.018.97±3.1957.32±79.4268.28±11.7415.70±13.9829.55±7.7413.15±3.78乳清蛋白组1054.65±26.603.72±1.7517.31±8.577.37±3.17115.65±53.978.94±4.8837.94±21.3568.81±17.0911.57±1.9029.90±8.2515.32±3.70WHPs-低1044.41±20.233.48±1.5116.36±6.998.12±2.01∗101.43±46.927.55±3.0922.60±5.2271.48±21.9513.86±7.8536.49±6.6513.97±2.83WHPs-中1049.07±21.484.14±1.9318.15±5.176.92±1.86158.13±75.36∗9.37±3.5322.69±6.3067.33±6.2011.04±1.1829.99±11.2410.28±2.08WHPs-高1057.17±18.424.25±0.9922.61±8.226.84±1.10130.67±73.938.58±2.1258.70±75.4769.26±12.6616.24±15.9429.41±5.1020.47±34.20
2.3 WHPs对小鼠非特异性免疫应答的影响
小鼠巨噬细胞吞噬能力和NK细胞活性如图2所示。与空白对照组相比,WHPs中、高剂量组小鼠巨噬细胞吞噬能力均显著提高(P<0.05),且WHPs高剂量组吞噬率显著高于乳清蛋白组(P<0.05)。WHPs干预各组和乳清蛋白组小鼠NK细胞活性较空白对照组有增强的趋势,但无显著差异(P>0.05),表明WHPs对小鼠NK细胞活性的影响并不显著。
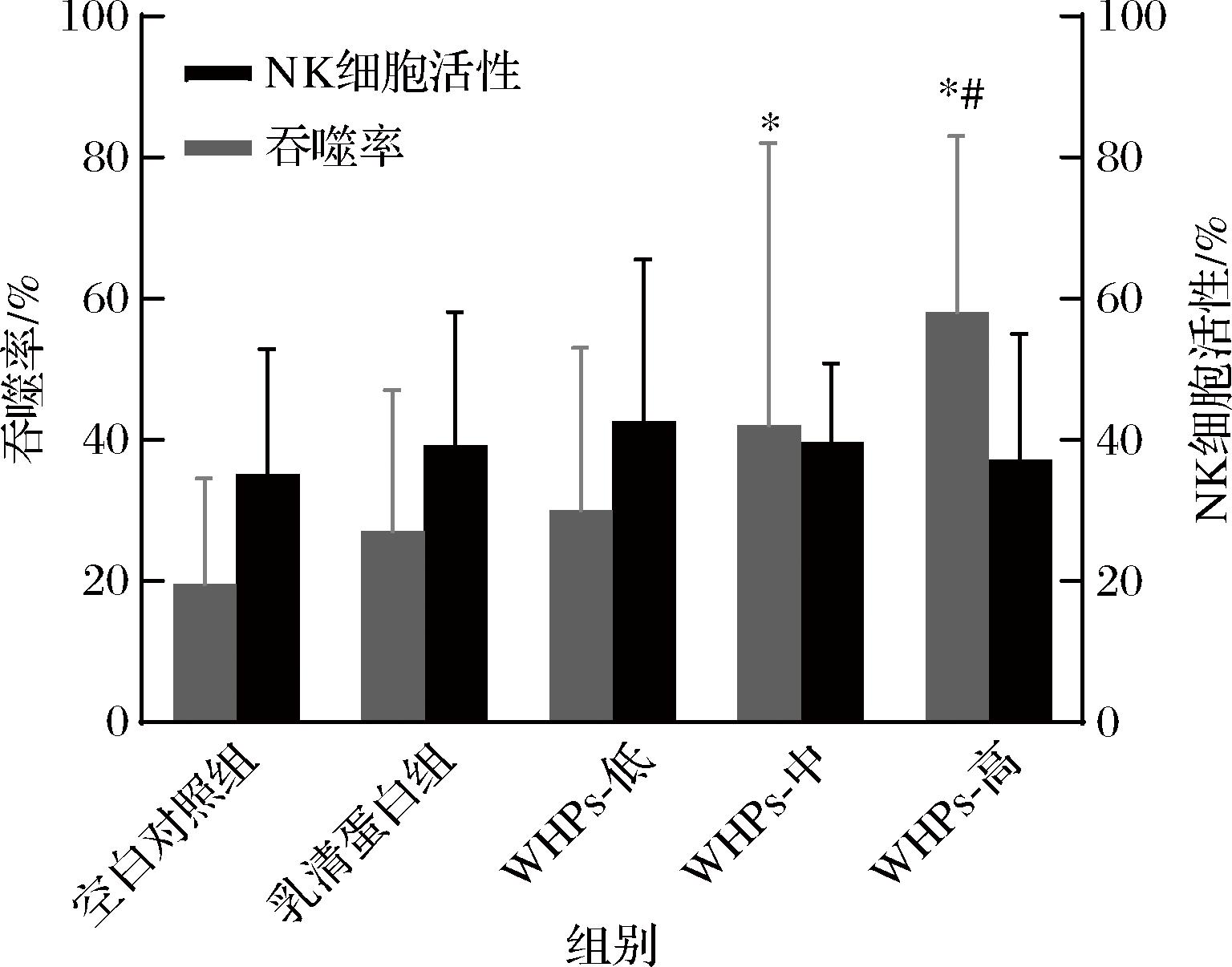
图2 WHPs对小鼠巨噬细胞吞噬率和NK细胞活性的影响(n=10)
Fig.2 Effects of WHPs on macrophage phagocytosis rate and NK cell activity in mice(n=10)
注:*表示与空白对照组相比,差异有统计学意义(P<0.05);#表示与乳清蛋白组相比,差异有统计学意义(P<0.05)。
2.4 WHPs对过敏性鼻炎小鼠体重及脏器系数的影响
由表4可见,各组小鼠的体重、肾脏系数、胸腺系数差异均无统计学意义,过敏模型性对照组肝脏系数较空白对照组有显著升高,而WHPs干预后的3个组小鼠肝脏系数均较模型对照组显著降低,接近空白对照组水平。说明WHPs干预可改善过敏小鼠可能发生的一些肝损伤症状。过敏模型小鼠脾脏系数均显著高于空白对照组,但未见各模型干预组脾脏系数有显著差异。
表4 WHPs对小鼠体重及重要脏器系数的影响(n=10)
Table 4 Effects of WHPs on body weight and vital organ coefficients in mice(n=10)
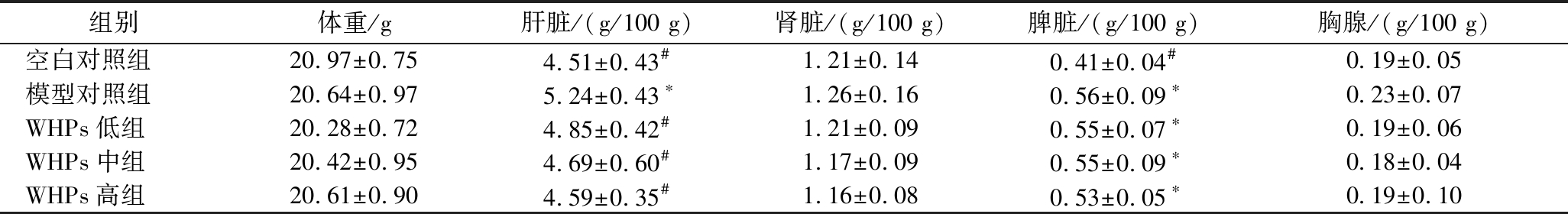
注:*表示与空白对照组相比有统计学差异(P<0.05);#表示与模型对照组相比有统计学差异(P<0.05)(表5同)。
组别体重/g肝脏/(g/100 g)肾脏/(g/100 g)脾脏/(g/100 g)胸腺/(g/100 g)空白对照组20.97±0.754.51±0.43#1.21±0.140.41±0.04#0.19±0.05模型对照组20.64±0.975.24±0.43∗1.26±0.160.56±0.09∗0.23±0.07WHPs低组20.28±0.724.85±0.42#1.21±0.090.55±0.07∗0.19±0.06WHPs中组20.42±0.954.69±0.60#1.17±0.090.55±0.09∗0.18±0.04WHPs高组20.61±0.904.59±0.35#1.16±0.080.53±0.05∗0.19±0.10
2.5 WHPs对过敏性鼻炎小鼠血清、鼻腔灌洗液中组胺(histamine,HIS)的影响
由图3可知,模型对照组血清及鼻腔灌洗液中的HIS含量均显著高于空白对照组,说明小鼠全身和局部过敏反应明显,模型建立成功。而WHPs干预的中剂量组和高剂量组小鼠均表现为血清HIS含量的显著降低,同时WHPs高剂量组小鼠的鼻腔灌洗液HIS含量也显著降低。
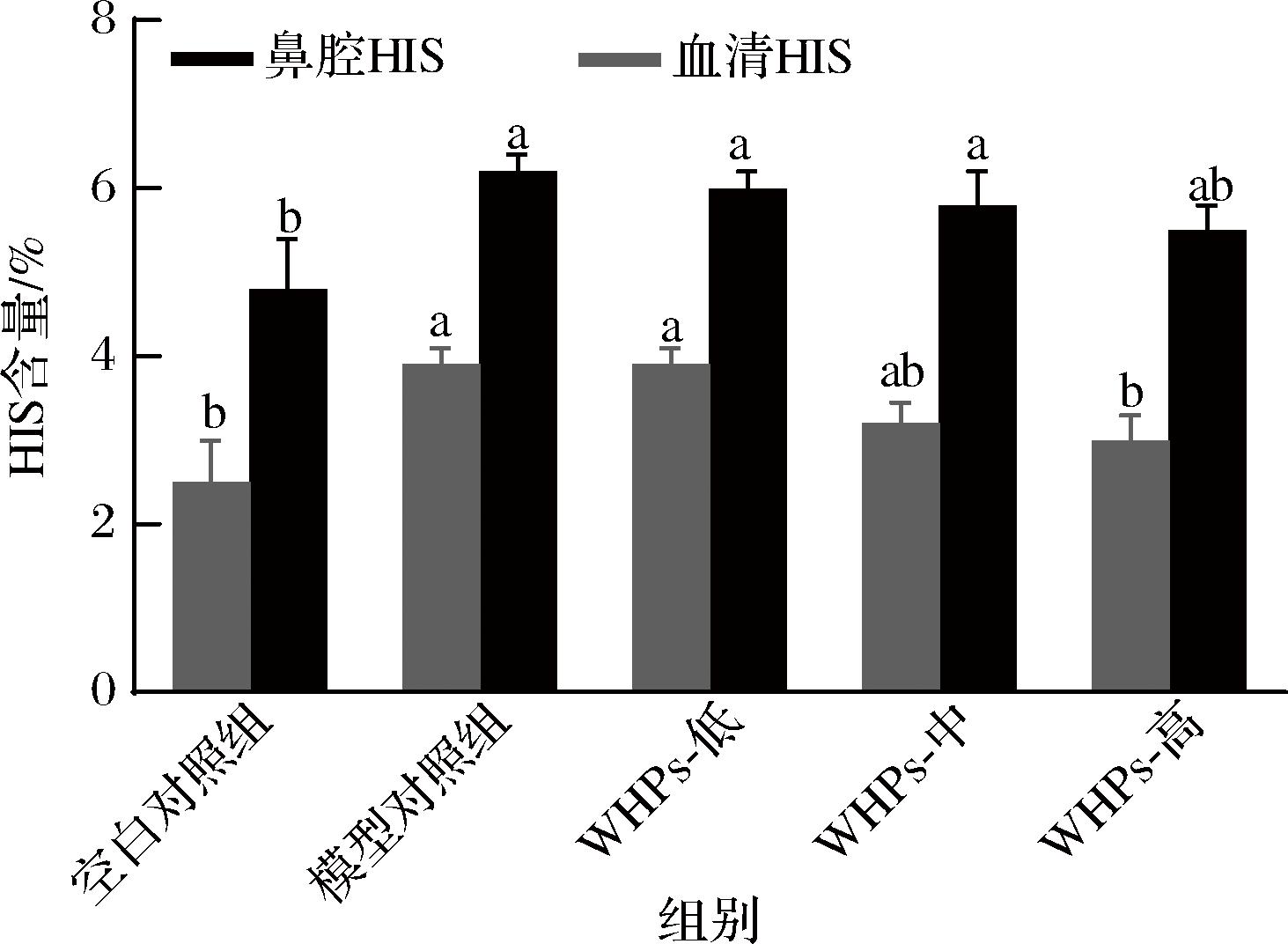
图3 WHPs对小鼠血清及鼻腔灌洗液中HIS含量的影响
Fig.3 Effect of WHPs on HIS content in serum and nasal lavage solution of mice
注:a表示与空白对照组相比有统计学差异(P<0.05);b表示与模型对照组相比有统计学差异(下同)。
2.6 WHPs对过敏性鼻炎小鼠血清炎症因子及免疫球蛋白的影响
由图4可知,与模型对照组比较,WHPs中剂量组和高剂量组均可显著降低系数血清中IgE及IgG含量。
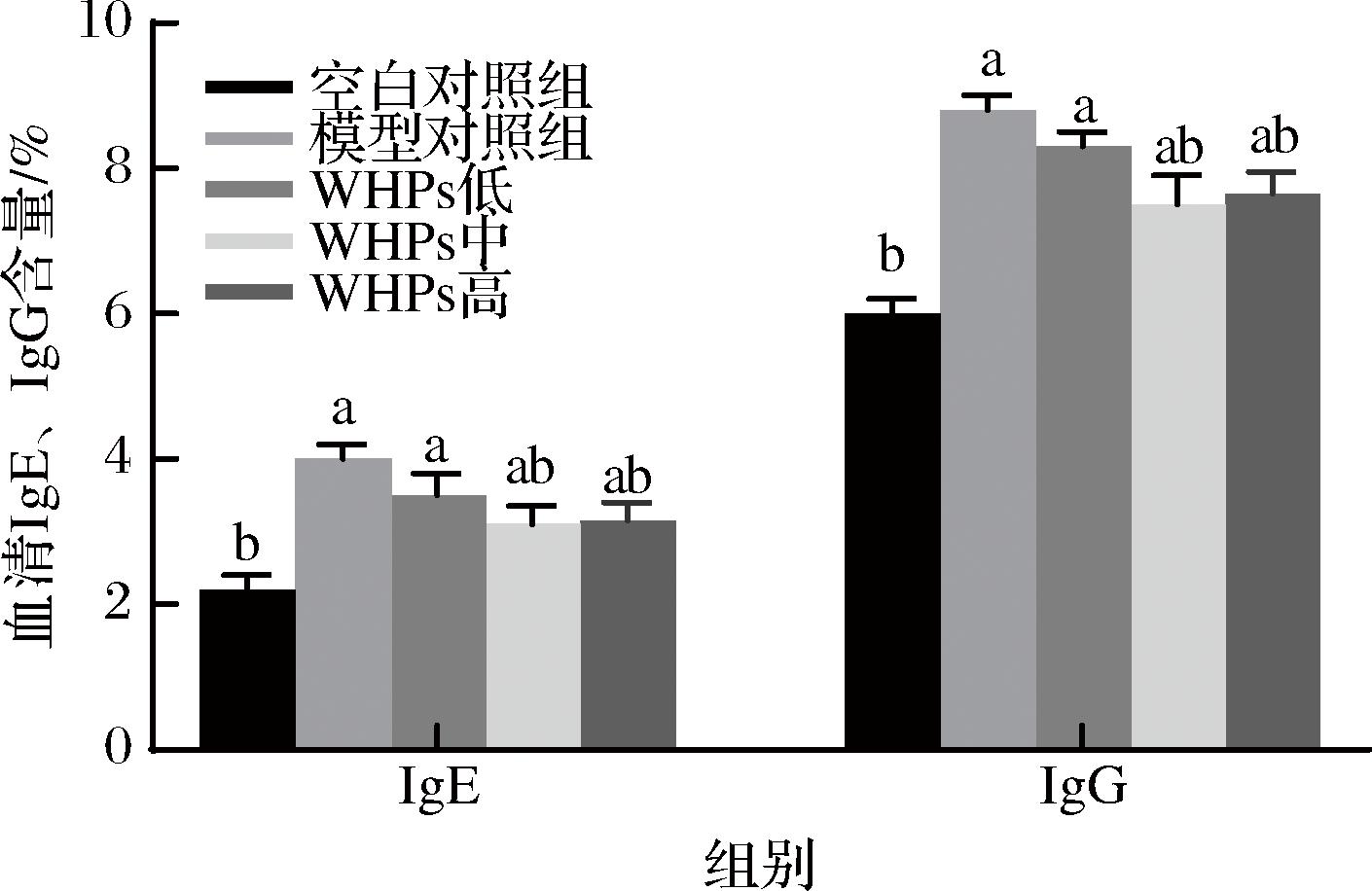
图4 WHPs对过敏性鼻炎小鼠血清IgE、IgG含量的影响
Fig.4 Effects of WHPs on serum IgE and IgG in mice with allergic rhinitis
由表5可知,WHPs中剂量和高剂量组可显著降低过敏型小鼠血清IL-4和IL-12的水平,与空白对照组相比模型对照组小鼠血清IL-10及IFN-γ显著降低,而WHPs高剂量组干预后小鼠血清IL-10水平显著高于模型对照组,WHPs中、高剂量组干预后小鼠血清IFN-γ含量显著高于模型对照组,且含量接近空白对照组健康小鼠。
表5 WHPs对小鼠血清炎症因子的影响(n=10)
Table 5 Effect of WHPs on serum inflammatory factors in mice(n=10)
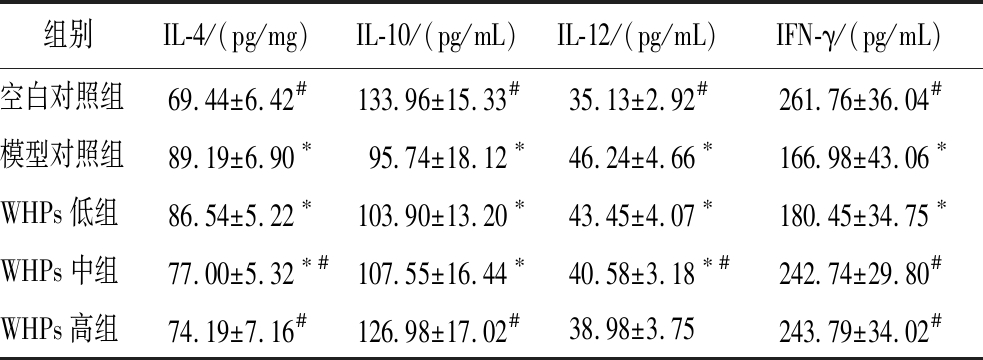
组别IL-4/(pg/mg)IL-10/(pg/mL)IL-12/(pg/mL)IFN-γ/(pg/mL)空白对照组69.44±6.42#133.96±15.33#35.13±2.92#261.76±36.04#模型对照组89.19±6.90∗95.74±18.12∗46.24±4.66∗166.98±43.06∗WHPs低组86.54±5.22∗103.90±13.20∗43.45±4.07∗180.45±34.75∗WHPs中组77.00±5.32∗#107.55±16.44∗40.58±3.18∗#242.74±29.80#WHPs高组74.19±7.16#126.98±17.02#38.98±3.75243.79±34.02#
2.7 过敏性鼻炎小鼠鼻腔病理结构变化
过敏性鼻炎模型组小鼠瘙痒及喷嚏行为均显著高于正常小鼠,另外血清及鼻腔灌洗液指标均有显著的疾病状态改变。同时,苏木精-伊红(hematoxylin-eosin,HE)染色观察到过敏性鼻炎小鼠的鼻腔黏膜结构发生显著变化,表现为大量嗜酸性粒细胞浸润、细胞轻度水肿、上皮细胞层变薄(图5,嗜酸性粒细胞以黑色箭头指出)。
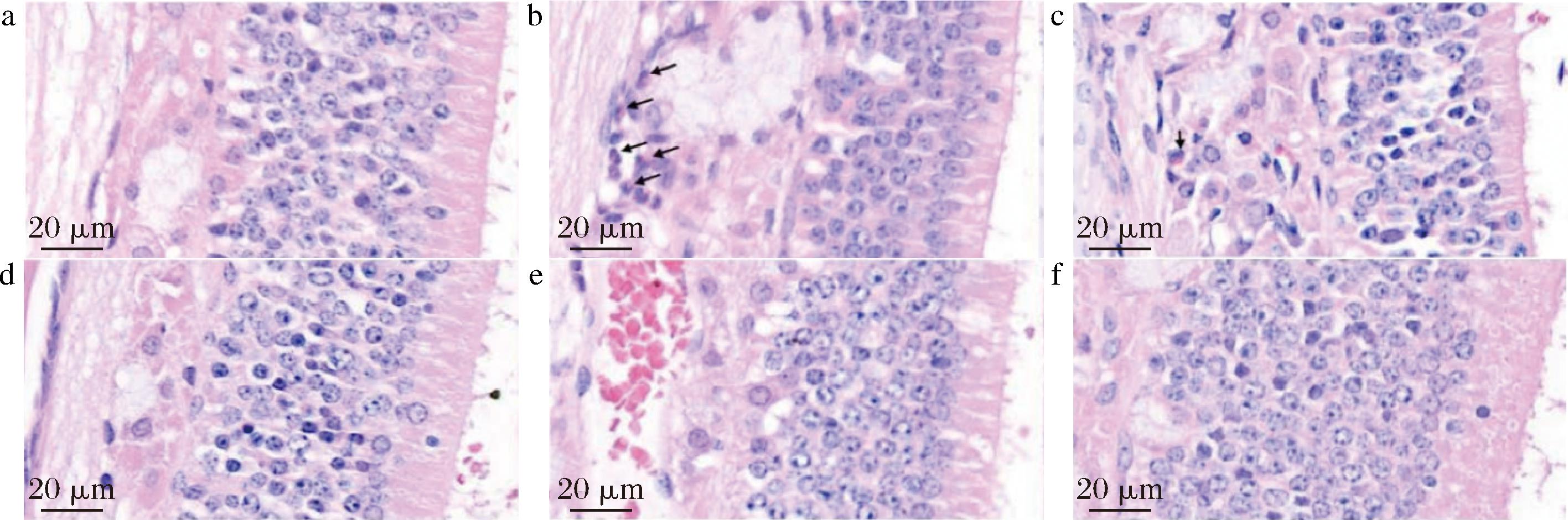
a-空白对照组;b-模型对照组;c-乳清蛋白对照组;d-WHPs低剂量组;e-WHPs中剂量组;f-WHPs高剂量组
图5 各组小鼠鼻腔黏膜病理结构图片(HE染色,40×)
Fig.5 Images of nasal mucosal pathological structures in each group of mice (HE staining, 40×)
注:嗜酸性粒细胞被染为鲜红色,以黑色箭头指出(下同)。
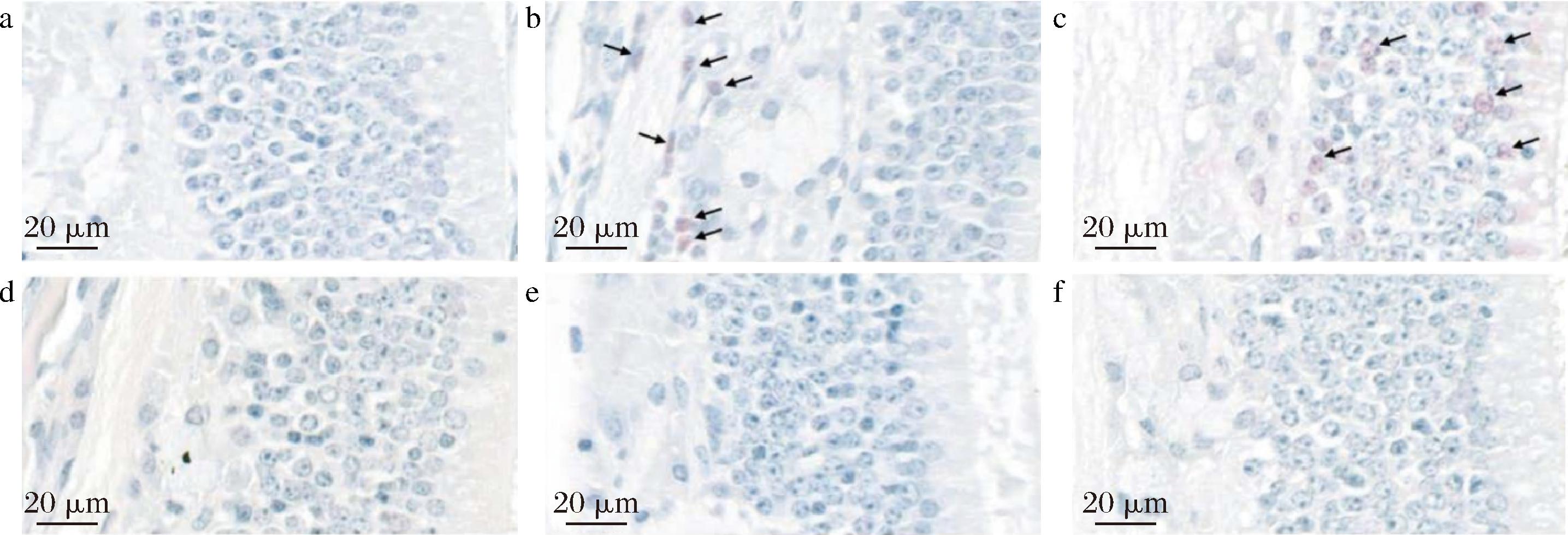
a-空白对照组;b-模型对照组;c-乳清蛋白对照组;d-WHPs低剂量组;e-WHPs中剂量组;f-WHPs高剂量组
图6 各组小鼠鼻腔黏膜细胞染色图片(天狼猩红染色,40×)
Fig.6 Images of nasal mucosal cell staining in each group of mice (sirius red staining, 40×)
进一步通过天狼猩红染色嗜酸性粒细胞也可以看出过敏性鼻炎小鼠的鼻腔病理结构发生了显著的改变,模型对照组小鼠和乳清蛋白组小鼠鼻腔黏膜有明显的嗜酸性粒细胞浸润(图6,以黑色箭头指出),而3组WHPs干预后的小鼠鼻腔黏膜中几乎未见嗜酸性粒细胞浸润。
3 结论与讨论
目前食品源的免疫活性物质已经得到广泛研究,KIEWIET等[11]研究证明给予小鼠乳清蛋白水解产物灌胃21 d可防止小鼠对β-乳球蛋白的过敏反应。KANG等[12]通过对80名参与者进行随机、双盲、安慰剂对照研究证明了补充发酵美拉德反应性乳清蛋白可显著增强NK细胞活性。CHUN等[13]证明β-乳球蛋白能够刺激小鼠多种免疫细胞,增强先天和适应性免疫反应的增殖和激活。而本研究旨在通过WHPs灌胃小鼠30 d后,从免疫器官指数、特异性免疫和非特异性免疫3个方面评价WHPs的免疫调节作用。同时,建立了小鼠过敏性鼻炎模型并给予14 d的WHPs灌胃干预,评价WHPs对小鼠过敏症状的改善作用。
免疫器官指数的变化可以反映机体的免疫能力,可作为反映免疫调节作用的初步指标。徐姗等[14]研究利用Con A作为刺激物,检测T淋巴细胞的增值能力,证明了蚕丝胶原蛋白对小鼠细胞免疫的促进作用。小鼠足跖肿胀程度反映的迟发型变态反应程度,也可作为细胞免疫能力的重要评价指标。本研究结果中各组小鼠免疫器官指数和淋巴细胞增值能力均无显著性差异,原因可能是作为一种营养物质,30 d的干预时间相对较短,WHPs未对小鼠体重和免疫器官发育产生明显影响。尽管如此,经过WHPs干预后小鼠的足跖厚度显著高于空白对照和乳清蛋白组,表明摄入高剂量WHPs可提高迟发型变态反应能力,提高小鼠细胞免疫功能。
MORIYA等[15]通过灌胃小鼠含有乳清蛋白的膳食后,测定免疫球蛋白的水平,结果表明乳清蛋白可显著提高免疫球蛋白的水平。本研究结果显示,经过WHPs干预组小鼠血清中IgA、IgG、IgM有明显提高,小鼠血清IL-12、IFN-γ水平较也较空白对照组小鼠血清水平显著提高。表明WHPs可能通过增加免疫球蛋白和上调IL-12、IFN-γ等细胞因子的表达而影响其介导的免疫反应,从而改善机体的免疫功能。同时,相较于乳清蛋白干预组小鼠,低剂量WHPs干预组小鼠的血清中免疫球蛋白IgM、IgA含量显著提高,但是血清细胞因子水平无显著性差异。WHPs较乳清蛋白对免疫球蛋白的显著提升可能是由于WHPs拥有小分子的肽段和氨基酸更有利于机体消化吸收。这一结论和张健等[16]得到的大豆低聚肽的营养补充对小鼠的免疫能力的提高大于大豆蛋白的结论相符合。
对于机体的非特异性免疫,已有大量研究证明可以通过摄入免疫活性蛋白类食品得到提高,如补充酪蛋白和其他乳制品、牡蛎和鱼类制成的多种蛋白质水解物可以增加小鼠的巨噬细胞和NK细胞活性[11]。本研究结果显示,乳清蛋白干预组小鼠的巨噬细胞活性与空白对照组无显著性差异,WHPs中剂量和高剂量干预组小鼠的巨噬细胞活性显著高于空白对照组,并且WHPs高剂量干预组小鼠的巨噬细胞活性也显著高于乳清蛋白干预组小鼠,但是NK细胞活性在各组小鼠中均无显著性差异。由此可见,WHPs可以一定程度地提高小鼠非特异性免疫应答,且主要是通过影响巨噬细胞吞噬能力来实现的[14]。这和CHUN等[17]研究得到的补充糖基化乳清蛋白浓缩物对巨噬细胞具有激活作用以及其可作为具有免疫调节作用的蛋白质来源的结论相一致。
补充免疫活性蛋白类食品同样可以缓解机体的过敏症状。WU等[18]通过对异基因抑制小鼠模型进行营养干预,证明了补充大豆-乳清蛋白混合物促进了小鼠体重、淋巴细胞、白细胞以及中性粒细胞的恢复,提高了血清免疫球蛋白水平。本研究结果显示,过敏模型组小鼠肝脏系数和脾脏系数较空白对照组有显著升高,而经过WHPs干预后,小鼠肝脏系数相较于过敏模型组显著降低,鼻腔和血清中HIS含量均有下降,IgE及IgG含量显著降低,血清炎症因子IL-4、IL-10、IL-12、IFN-γ更接近空白对照组的健康小鼠,说明WHPs干预可改善过敏小鼠的肝损伤症状,对降低小鼠HIS水平、纠正过敏小鼠血清炎症因子紊乱、缓解过敏症状以及免疫系统重建有很显著的作用。
进一步通过HE染色和天狼猩红染色观察小鼠鼻腔黏膜结构,过敏模型对照组小鼠和乳清蛋白组小鼠鼻腔黏膜有明显的嗜酸性粒细胞浸润,而WHPs干预后的小鼠鼻腔黏膜中几乎未见嗜酸性粒细胞浸润。这和JANG等[10]对过敏性哮喘和鼻炎小鼠进行木犀草素干预后观察到的单个支气管周围浸润的嗜酸性粒细胞数量显著减少的现象一致。这说明WHPs对过敏性鼻炎小鼠的过敏症状具有改善作用,并且改善效果优于乳清蛋白。
4 总结与展望
WHPs可以通过提高小鼠迟发型变态反应能力、上调IL-12、IFN-γ细胞因子水平和增加免疫球蛋白浓度的途径改善小鼠的特异性免疫应答,以及可以通过增强巨噬细胞吞噬能力来改善非特异性免疫应答,从而辅助提高机体免疫能力。针对过敏性鼻炎小鼠,WHPs可以显著降低血清和鼻腔灌洗液组胺水平、有效调节炎症因子、减轻嗜酸性粒细胞浸润,从而起到改善过敏性鼻炎的作用。并且,WHPs在提升小鼠迟发型变态反应能力、提高机体血清免疫蛋白IgA和IgM含量、增加巨噬细胞吞噬能力、改善过敏性鼻炎症状等方面的效果较乳清蛋白更为显著。
WHPs具有与乳清蛋白不同的加工特性,溶解性、热稳定性和免疫特性皆优于乳清蛋白,在开发免疫调节功能性食品中具有较大潜力,它作为功能性食品配料,已经被广泛应用于婴幼儿配方奶粉、特殊医学用途配方食品、功能性固体饮料与代餐食品、中老年食品等食品的开发。尽管关于WHPs的免疫效果研究结果比较明确且效果得到广泛认可,但是目前体外和动物研究偏多,而临床研究较少,因此,未来需要研究者开展更多类型和更大样本量的临床评价,以证明其安全性和有效性。同时,获取纯度较高的WHPs的提取工艺并未实现产业化,需要结合多种纯化手段和设备得到单一的目标肽。最后,作为肽类产品,WHPs的苦味等不良风味也制约了它的应用,目前可以通过吸附、萃取、包埋等手段去除或通过其他香精、香料等遮蔽不良风味。
[1] 李晋祯, 郑惠娜, 任鼎鼎, 等.牡蛎低分子肽LOPs对短期免疫抑制小鼠的免疫调节作用[J].中国食品学报, 2022, 22(10):143-152.LI J Z, ZHENG H N, REN D D, et al.Immunomodulatory effects of low molecular weight oyster peptides in short-term immunosuppressed mice[J].Journal of Chinese Institute of Food Science and Technology, 2022, 22(10):143-152.
[2] 张健, 李雯晖, 赵博雅, 等.大豆蛋白与大豆低聚肽对负氮平衡老年小鼠表皮创伤感染下的免疫调节作用[J].食品科学, 2018, 39(17):145-151.ZHANG J, LI W H, ZHAO B Y, et al.Immune modulation of soybean protein and soybean oligopeptides on epidermal trauma infection in aged mice with negative nitrogen balance[J].Food Science, 2018, 39(17):145-151.
[3] 李富强, 张廷新, 朱丽萍, 等.食物蛋白源免疫调节肽研究进展[J].食品与发酵工业, 2022, 48(1):308-314.LI F Q, ZHANG Y X, ZHU L P, et al.Advance of immunomodulatory peptides from dietary-protein source[J].Food and Fermentation Industries, 2022, 48(1):308-314.
[4] 邵深深, 张蔷蓉, 林希, 等.苍耳子水提液对过敏性鼻炎小鼠的治疗作用及机制研究[J].浙江中医药大学学报, 2023, 47(2):111-117.SHAO S S, ZHANG Q R, LIN X, et al.Study on the therapeutic effect and mechanism of Xanthii Fructus water extract on mice with allergic rhinitis[J].Journal of Zhejiang Chinese Medical University, 2023, 47(2):111-117.
[5] CHOI S, JUNG M A, HWANG Y H, et al.Anti-allergic effects of Asarum heterotropoides on an ovalbumin-induced allergic rhinitis murine model[J].Biomedicine &Pharmacotherapy, 2021, 141:111944.
[6] HA D J, KIM J, KIM S, et al.Dietary whey protein supplementation increases immunoglobulin G production by affecting helper T cell populations after antigen exposure[J].Foods, 2021, 10(1):194.
[7] 曾志, 赖远禄, 黄炳暖, 等.水解乳清蛋白配方对过敏性疾病婴幼儿NK细胞亚群分布的影响[J].齐齐哈尔医学院学报, 2020, 41(15):849-1 852.ZENG Z, LAI Y L, HUANG B N, et al.Effect of hydrolyzed protein formula on the distribution of NK cell subsets in infants with allergic diseases[J].Journal of Qiqihar University of Medicine, 2020, 41(15):1849-1852.
[8] 房军. 保健食品检验与评价技术规范[M].北京:中华书局, 2004.FANG J.Technical specifications for inspection and evaluation of health food[M].Beijing:Zhonghua Book Company, 2004.
[9] 司少艳, 尚颖, 马小淯, 等.胶原蛋白肽部分恢复辐射联合模拟失重模型小鼠的免疫功能[J].细胞与分子免疫学杂志, 2023, 39(11):967-972.SI S Y, SHANG Y, MA X Y, et al.Collagen peptide partially restores immune function in mice under the condition of X-ray irradiation combined with simulated weightlessness[J].Chinese Journal of Cellular and Molecular Immunology, 2023, 39(11):967-972.
[10] JANG T Y, JUNG A Y, KYUNG T S, et al.Anti-allergic effect of luteolin in mice with allergic asthma and rhinitis[J].Central European Journal of Immunology, 2017, 42(1):24-29.
[11] KIEWIET M B G, FAAS M M, DE VOS P.Immunomodulatory protein hydrolysates and their application[J].Nutrients, 2018, 10(7):904.
[12] KANG M, OH N S, KIM M, et al.Supplementation of fermented Maillard-reactive whey protein enhances immunity by increasing NK cell activity[J].Food &Function, 2017, 8(4):1718-1725.
[13] CHUN S H, LEE K W.Immune-enhancing effects of β-lactoglobulin glycated with lactose following in vitro digestion on cyclophosphamide-induced immunosuppressed mice[J].Journal of Dairy Science, 2022, 105(1):623-636.
[14] 徐姗, 杜双双, 阎昭.蚕丝蛋白肽对S180荷瘤小鼠免疫调节作用的研究[J].中国肿瘤临床, 2021, 48(1):1-7.XU S, DU S S, YAN Z.Immunoregulatory effect of silk fibroin peptide in S180 tumor-bearing mice[J].Chinese Journal of Clinical Oncology, 2021, 48(1):1-7.
[15] MORIYA T, FUKATSU K, NOGUCHI M, et al.Effects of semielemental diet containing whey peptides on Peyer’s patch lymphocyte number, immunoglobulin A levels, and intestinal morphology in mice[J].Journal of Surgical Research, 2018, 222:153-159.
[16] 张健, 李雯晖, 赵博雅, 等.大豆蛋白与大豆低聚肽对负氮平衡老年小鼠表皮创伤感染下的免疫调节作用[J].食品科学, 2018, 39(17):145-151.ZHANG J, LI W H, ZHAO B Y, et al.Immune modulation of soybean protein and soybean oligopeptides on epidermal trauma infection in aged mice with negative nitrogen balance[J].Food Science, 2018, 39(17):145-151.
[17] CHUN S H, KIM H H, KIM Y, et al.Characterization of macrophage stimulating compound in glycated whey protein concentrate[J].Food Science and Biotechnology, 2020, 29(8):1113-1123.
[18] WU X L, HOU Q H, ZHAO Z Y, et al.Effects of soy-whey protein nutritional supplementation on hematopoiesis and immune reconstitution in an allogeneic transplanted mice[J].Nutrients, 2022, 14(15):3014.