菠菜(Spinacia oleracea L.)富含类胡萝卜素和多种维生素及矿物质等,具有促进人体新陈代谢和生长发育、延缓衰老、增强抗病能力等多种功效[1]。上海青(Brassica chinensis L.)种植范围广、生长周期短,含有多种维生素和矿物质,营养丰富[2],深受消费者的喜爱。芹菜(Apium graveolens L.)在我国有着悠久的种植历史,因其重要的药用价值而备受古代医家推崇[3],研究表明芹菜中含有可预防心血管疾病、黄疸、痛风等疾病的功能性成分[4]。西兰花(Brassica oleracea L.var.Italica)主要食用部位是花茎和紧密集成球状的花蕾,除了包含人体必需的五大营养素之外,还含有丰富的葡糖异硫氰酸盐、类黄酮物质、膳食纤维等[5],营养价值高,被誉为“蔬菜皇冠”[6]。细香葱(Allium schoenoprasum)以嫩叶和假茎供食,《重庆草药》中记载:“味辛,性温,无毒,入肺,肝经”,具有发表散寒、祛风胜湿、解毒消肿等功效,是一种调味香料型蔬菜[7]。
鲜切蔬菜又称半加工蔬菜,是指以新鲜蔬菜为原料,经分级、清洗、整修、切分、保鲜、包装等一系列处理后,经冷链销售的即食蔬菜制品[8]。鲜切蔬菜既可以最大程度保留蔬菜原有的新鲜状态和营养品质,同时又具有清洁卫生、可利用程度高、食用方便等特点。但鲜切蔬菜加工过程中的清洗、切分等操作会破坏组织,产生组织液渗漏,极易导致微生物繁殖,从而变味和软腐,严重影响其货架期[9]。目前国内外关于鲜切蔬菜保鲜的研究主要集中在控制其衰老进程、抑制微生物繁殖、减少水分散失等方面[10],对微生物多样性和主要腐败菌鉴定方面的研究较少。这也导致了鲜切蔬菜保鲜技术的开发缺少足够的理论依据,不能针对鲜切蔬菜主要腐败菌开发出有效的抑菌技术。
本研究以菠菜、上海青、芹菜、西兰花和细香葱5种蔬菜为实验材料,探究了4 ℃冷藏条件下普通包装和真空包装的5种蔬菜的菌落总数变化规律、新鲜及腐败蔬菜的微生物多样性及相对丰度,并筛选、鉴定出了5种蔬菜中主要腐败菌。本研究可为鲜切蔬菜腐败变质机制研究和保鲜技术开发提供生物学依据。
1 材料与方法
1.1 材料与试剂
菠菜、上海青、芹菜、西兰花、细香葱,上海扬升农副产品专业合作社;平板计数琼脂(plate count agar,PCA)培养基、沙氏葡萄糖琼脂(Sabouraud dextrose agar)培养基,青岛海博生物技术有限公司;LB培养基,北京陆桥技术股份有限公司。
1.2 仪器与设备
AL204电子天平,瑞士Mettler Toledo公司;BCD-900A-2C冷柜,德玛仕公司;EQR/GL-41超净工作台,新加坡艺思高生物技术有限公司;HPP260恒温恒湿培养箱,德国Memmert公司;一次性无菌培养皿,海门市莱博尔实验器材有限公司;FKJ-E01A5真空封口机,小熊电器股份有限公司;Research Plus移液枪,德国Eppendorf公司;ABI3730-XL测序仪,上海派森诺生物科技股份有限公司。
1.3 实验方法
1.3.1 样品处理
取新鲜菠菜、上海青、芹菜、西兰花和细香葱,去除病虫害、机械损伤等不合格品,用自来水冲去表面的泥土,并用无菌水清洗3次、沥干。用75%酒精消毒过的锋利小刀对蔬菜进行分割:菠菜和上海青茎叶分割为4 cm × 4 cm的大小;芹菜茎叶分离,茎分割为5 cm长的小段;西兰花切分时要求切口平整,切分后大小基本一致,花球紧密、花蕾大小适中;细香葱茎叶分割为5 cm长的小段。分别使用普通包装袋(PE自封袋:200 mm×280 mm×0.08 mm)和真空包装袋(150 mm×200 mm×0.08 mm;真空度≥60 kPa)对蔬菜进行包装,每包质量约为50 g,置于4 ℃条件下冷藏至出现腐烂。
1.3.2 菌落总数
参考GB 4789.2—2022《食品安全国家标准 食品微生物学检验 菌落总数测定》。
1.3.3 微生物多样性
1.3.3.1 菌种总DNA提取
取5~10 g新鲜和腐败蔬菜样品,装入消毒小自封袋,冷冻送至上海派森诺生物科技股份有限公司进行DNA提取。
1.3.3.2 PCR扩增
以提取的真菌总DNA为模板,采用ITS_V1真菌通用引物进行PCR扩增:F:5′-CTACACGACGCTTCCGATCTCTTGGTCATTTAGAGGAAGTAA-3′,R:5′-CAGACGTGTGCTCTTCCGATCTGCTGCGTTCTTCATC GATGC-3′,下划线序列为测序接头。
以提取的细菌总DNA为模板,采用16SrDNA细菌引物进行PCR扩增:F:5′-CTACACGACGCTCTTCCGATCTAACMGGATTAGATACCCKG-3′,R:5′-CAGA CGTGTGCTCTTCCGATCTACGTCATCCCCACCTTCC-3′,下划线序列为测序接头。PCR反应参数如表1所示。
表1 PCR 扩增程序
Table 1 PCR amplification procedure
预变性变性退火延伸终延伸循环数95 ℃,5 min95 ℃,30 s58 ℃,30 s72 ℃,90 s72 ℃,7 min35
反应完成后,PCR产物用AxyPrep DNA凝胶回收试剂盒回收,然后取3 μL PCR产物进行1%琼脂糖凝胶电泳检测。
1.3.3.3 高通量测序数据分析
用Illumina平台对群落DNA片段进行双端测序,使用QIIME2和Vsearch软件对序列在98%相似度水平去噪聚类,获得操作性分类单元(operational taxonomic unit, OUT)。PCR扩增及测序由上海派森诺生物科技股份有限公司完成。
1.3.4 腐败菌分离
取25 g已腐败的蔬菜样品于均质袋中,按1.3.2节的方法对腐败样品中的微生物进行稀释、培养,不同样品所采用的培养基和培养条件如表2所示。
表2 腐败菌分离实验培养条件
Table 2 Culture conditions for the isolation of spoilage bacteria

编号培养菌种培养基培养条件1普通包装条件下的细菌PCA37 ℃,48 h2真空包装条件下的细菌PCA厌氧,37 ℃,48 h
1.3.5 腐败菌回接
将鲜切蔬菜样品放入150 mg/L次氯酸溶液中浸泡5 min,使用无菌水洗涤3次,沥干。分别挑取1.3.4节培养皿中具有不同特征的菌落涂抹在鲜切蔬菜的切口上,采用对应的包装方式包装,并置于4 ℃冰箱中冷藏至出现腐败特征。将致蔬菜腐败速度快的菌种,初步判断为该蔬菜的主要腐败菌。从切口挑起腐败菌在对应的培养基上划线,培养后观察菌落形态是否单一。
1.3.6 腐败菌鉴定
1.3.6.1 菌种DNA提取和PCR扩增
挑取PCA平板上单菌落于LB液体培养基中培养,按1.3.3节方法进行DNA提取和PCR扩增(引物不带测序接头)。
1.3.6.2 序列测定与分析
取各个菌种纯化后的PCR产物,送至上海派森诺生物科技股份有限公司进行DNA测序。用NCBI Blast程序将拼接后的序列文件与NCBI 16S数据进行比对,得到鉴定结果。
2 结果与分析
2.1 普通包装和真空包装对鲜切蔬菜菌落总数的影响
5种蔬菜贮藏过程中菌落总数变化如图1所示,真空包装和普通包装蔬菜样品中的菌落总数均随着贮藏时间的延长而持续升高。普通包装和真空包装菠菜的菌落总数分别在贮藏前7 d和前10 d,从7.4×105 CFU/g增长到2.2×106 CFU/g和2.9×106 CFU/g,速度相对较慢,而在第10天和第12天,菌落总数分别快速增长到2.5×108 CFU/g和1.8×107 CFU/g。普通包装和真空包装的上海青呈现出与菠菜相似的规律。普通包装和真空包装的芹菜和西兰花的菌落总数总体增长速度较缓,这可能是芹菜和西兰花在4 ℃条件下保质期较长的原因之一。而细香葱在贮藏过程中菌落总数呈现快速增长的趋势,普通包装和真空包装分别在贮藏第3天和第5天出现轻微的腐败现象,这与焦贺等[11]实验中细香葱保质期较短的结果相一致。

a-普通包装;b-真空包装
图1 五种蔬菜贮藏过程中菌落总数变化
Fig.1 Change in the aerobic plate count of five vegetables during storage
注:A1-普通包装菠菜;B1-普通包装上海青;C1-普通包装芹菜;D1-普通包装西兰花;E1-普通包装细香葱;A2-真空包装菠菜;B2-真空包装上海青;C2-真空包装芹菜;D2-真空包装西兰花;E2-真空包装细香葱(下同)。
在贮藏过程中,真空包装的菠菜、上海青和细香葱中的菌落总数显著低于普通包装,说明真空包装可以在一定程度上抑制微生物的生长。2种包装的芹菜中菌落总数没有显著差异,可能与芹菜中存在黄酮、皂苷和单宁等抑菌成分有关。研究表明,芹菜提取物具有一定的抑菌活性,可以有效抑制细菌的生长[12-13]。真空包装西兰花的菌落总数高于普通包装,这可能是因为真空包装会对西兰花造成机械损伤,导致西兰花组织液渗漏,高水分活度和丰富的营养物质为微生物提供了良好的生长繁殖条件[14]。
2.2 微生物多样性分析
2.2.1 微生物群落的丰度分析
5种蔬菜样品的细菌和真菌的物种多样性分析结果分别如图2和图3所示。由图2可知,各样品中主要细菌有假单胞菌属(Pseudomonas spp.)、黄杆菌属(Flavobacterium spp.)、黄假单胞菌属(Xanthonmonas spp.)、鞘脂单胞菌属(Sphingomonas spp.)、乳球菌属(Lactococcus spp.)、杜擀氏菌属(Duganella spp.)、异根瘤菌-新根瘤菌-副根瘤菌-根瘤菌属(Allorhizobium-Neorhizobium-Pararhizobium-Rhizobium spp.)、拉恩氏菌属(Rahnella spp.)、副球菌属(Paracoccus spp.)、肉杆菌属(Carnobacterium spp.)、魏斯氏属(Weissella spp.)、甲基杆菌-甲基红菌属(Methylobacterium-Methylorubrum spp.)、金黄杆菌属(Chryseobacterium spp.)、窄食单胞菌属(Stenotrophomonas spp.)、欧文氏菌属(Erwinia spp.)和泛菌属(Pantoea spp.)等。
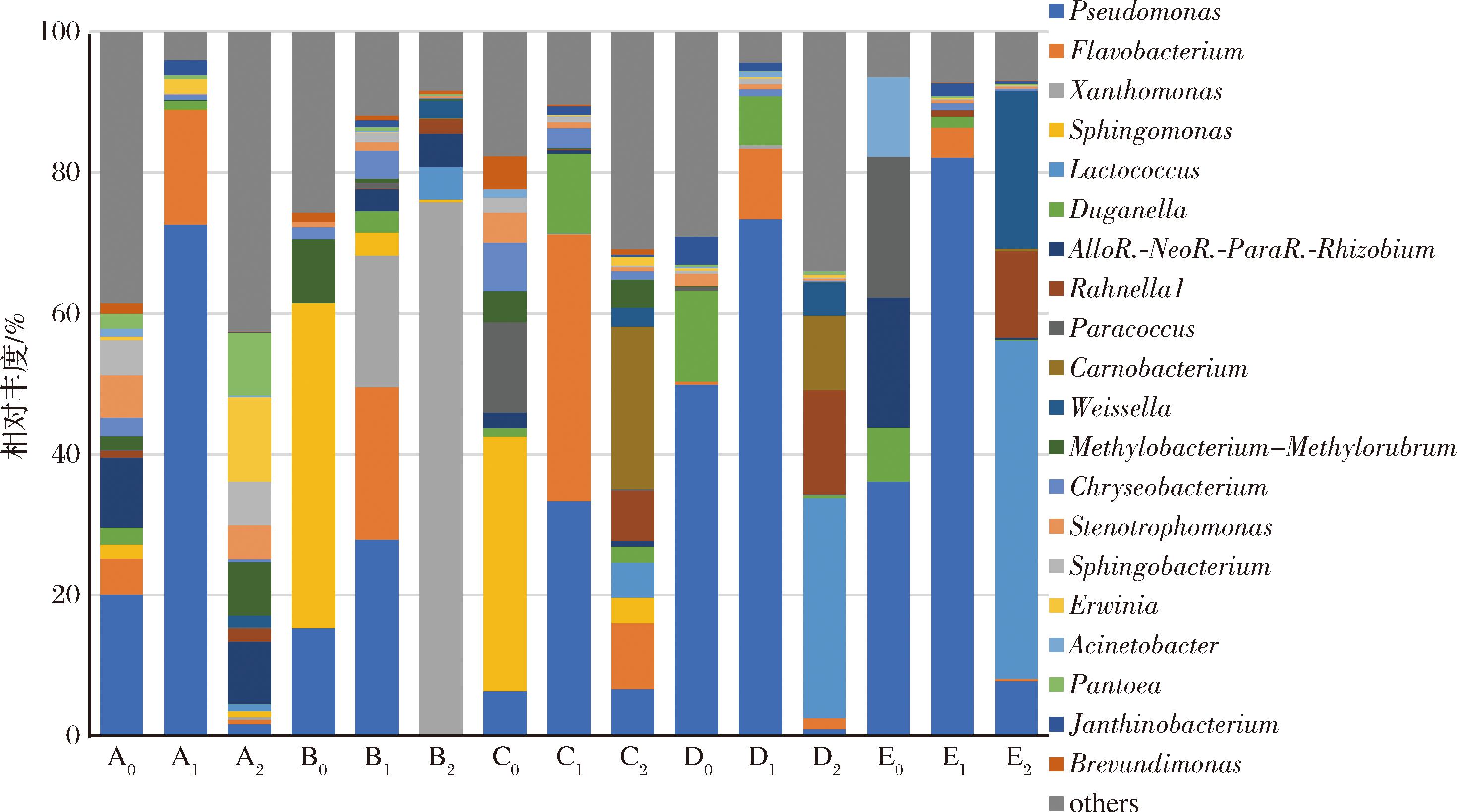
图2 各样品细菌丰度属水平分析
Fig.2 Bacterial abundance analysis of each sample at the genus level
注:A0-新鲜菠菜;B0-新鲜上海青;C0-新鲜芹菜;D0-新鲜西兰花;E0-新鲜细香葱;其他样品编号同图1。

图3 各样品真菌丰度属水平分析
Fig.3 Fungal abundance analysis of each sample at the genus level
新鲜样品细菌中,菠菜以假单胞菌属和异根瘤菌-新根瘤菌-副根瘤菌-根瘤菌属为主;上海青以鞘脂单胞菌属、假单胞菌属和甲基杆菌-甲基红菌属为主;芹菜以鞘脂单胞菌属、副球菌属和金黄杆菌属为主;西兰花以假单胞菌属和杜擀氏菌属为主;细香葱以假单胞菌属、副球菌属和异根瘤菌-新根瘤菌-副根瘤菌-根瘤菌属为主。
腐败样品中,普通包装的5种蔬菜中的细菌均以假单胞菌属、黄杆菌属、黄假单胞菌属和杜擀氏菌属为主;而真空包装蔬菜中,不同品种间显示了细菌群落结构的显著差异,菠菜以欧文氏菌属和肉杆菌属为主;上海青以黄假单胞菌属、欧文氏菌属和泛菌属为主;芹菜菌群较多样,以肉杆菌属、假单胞菌属和黄杆菌属为主;西兰花以乳球菌属、拉恩氏菌属和肉杆菌属为主,细香葱以乳球菌属、魏斯氏属和拉恩氏菌属为主。
由图3可知,各样品中主要真菌有篮状菌属(Talaromyces)、小不整球壳属(Plectosphaerella)、线黑粉酵母属(Filobasidium)、链格孢霉属(Alternaria)、新灰菌属(Neosetophoma)、孢子菌属 (Sporobolomyces)、莫氏黑粉菌属(Moesziomyces)、蝶形担孢酵母属(Papiliotrema)、维希尼克氏酵母属(Vishniacozyma)、枝顶孢霉属(Acremonium)、红酵母属(Rhodotorula)、汉纳酵母属(Hannaella)、帚枝霉属(Sarocladium)和布勒担孢酵母属(Bulleromyces)等。不同品种蔬菜携带的主要真菌丰度差异较大,其中,链格孢霉属和线黑粉酵母属等是常见的低温环境下导致果蔬等腐烂变质的微生物。
新鲜样品真菌中,菠菜以篮状菌属为主;上海青以小不整球壳属、链格孢霉属和莫氏黑粉菌属为主;芹菜以篮状菌属和蝶形担孢酵母属为主;西兰花以篮状菌属、小不整球壳属和线黑粉酵母属为主;细香葱以篮状菌属为主。腐败样品中,普通包装菠菜以小不整球壳属、维希尼克氏酵母属和布勒担孢酵母属为主,而真空包装菠菜以枝顶孢霉属、帚枝霉属和布勒担孢酵母属为主;普通包装上海青以小不整球壳属和链格孢霉属为主,而真空包装上海青以孢子菌属为主;普通包装芹菜以链格孢霉属和汉纳酵母属为主,真空包装芹菜以蝶形担孢酵母属、汉纳酵母属和链格孢霉属为主;普通包装西兰花以线黑粉酵母属和小不整球壳属为主,而真空包装西兰花以孢子菌属、红酵母属和莫氏黑粉菌属为主;普通包装细香葱以线黑粉酵母属、小不整球壳属和红酵母属为主,而真空包装细香葱中新灰菌属占绝对优势。
图2和图3结果显示,部分样品中others比例较高,主要由2部分构成:有明确注释但丰度较低的菌种和在所选分类水平下没有明确注释结果的菌种。通过查看完整注释结果可知,这部分样品中不明确注释的菌种比例较高,故出现others比例较高的现象。
2.2.2 α多样性分析
α多样性主要关注局域均匀生境下的物种数目,又被称为生境内的多样性,可以反映微生物群落的丰度和多样性。Chao1指数是反映物种丰度的指标,其值越大,OTU数目越多,说明该样本物种总数越多。Simpson指数和Shannon指数常用于估算样品中微生物菌群的丰富度以及均匀度,指数值越大,微生物种类丰富度越高[15]。
基于97%相似度水平的OTU数,对各样品的细菌α多样性指数值统计结果如表3和表4所示。各样品的Simpson指数和Shannon指数呈正相关,且新鲜蔬菜细菌α多样性指数中的Simpson指数和Shannon指数均小于2种包装的腐败蔬菜,说明在贮藏过程中,5种蔬菜的细菌多样性增加。这与大部分文献中细菌多样性随贮存时间延长而降低的规律不一致,少数研究报道,苹果[16]、芝麻菜[17-18]、红甜菜和菠菜[18]等果蔬的细菌多样性随着贮存时间的延长而呈现上升趋势,但文中并未对细菌多样性增加的原因进行深入分析,具体原因有待进一步的研究。而5种蔬菜中的真菌α多样性指数呈现出不同的规律,新鲜菠菜、上海青、芹菜的Simpson指数和Shannon指数均小于2种包装的腐败蔬菜,而新鲜西兰花和细香葱则相反。
表3 细菌α多样性指数统计
Table 3 Bacterial alpha diversity index statistics
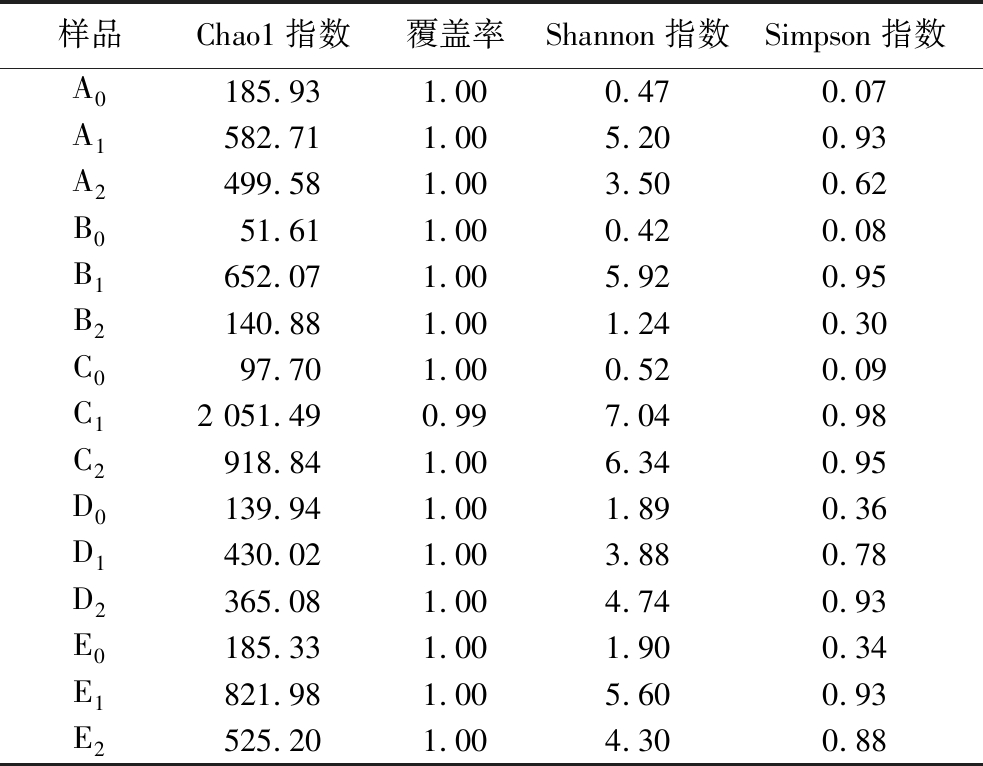
样品Chao1指数覆盖率Shannon指数Simpson指数A0185.931.000.470.07A1582.711.005.200.93A2499.581.003.500.62B051.611.000.420.08B1652.071.005.920.95B2140.881.001.240.30C097.701.000.520.09C12 051.490.997.040.98C2918.841.006.340.95D0139.941.001.890.36D1430.021.003.880.78D2365.081.004.740.93E0185.331.001.900.34E1821.981.005.600.93E2525.201.004.300.88
表4 真菌α多样性指数统计
Table 4 Fungal alpha diversity index statistics
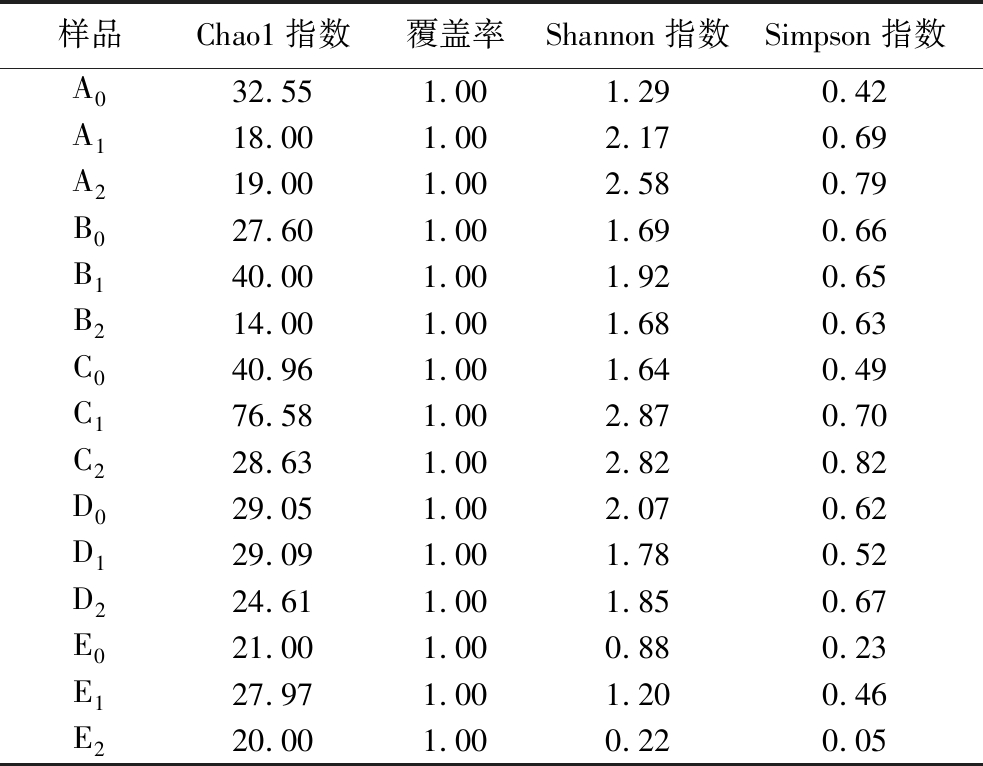
样品Chao1指数覆盖率Shannon指数Simpson指数A032.551.001.290.42A118.001.002.170.69A219.001.002.580.79B027.601.001.690.66B140.001.001.920.65B214.001.001.680.63C040.961.001.640.49C176.581.002.870.70C228.631.002.820.82D029.051.002.070.62D129.091.001.780.52D224.611.001.850.67E021.001.000.880.23E127.971.001.200.46E220.001.000.220.05
2.3 腐败菌鉴定
腐败菌的鉴定结果如表5所示。普通包装冷藏菠菜的主要腐败菌为四川肠杆菌(Enterobacter sichuanensis)和路氏肠杆菌(Enterobacter ludwigii),有研究表明果蔬组织发生腐败的过程与假单胞菌、肠杆菌和欧文氏菌等有关[19];真空包装冷藏菠菜的主要腐败菌为土生拉乌尔菌(Raoultella terrigena),该菌是从克雷伯菌属划分出来的一种革兰氏阴性兼性厌氧菌[20],曾在苍耳、芦苇[21]、紫苜蓿[22]等植物根际周围土壤中分离得到,但未见到土生拉乌尔菌引起蔬菜腐败的研究。
表5 鲜切蔬菜中主要的腐败菌
Table 5 Main spoilage bacteria in fresh-cut vegetables

品名包装 DNA鉴定结果同源性/%普通包装E.sichuanensis99.65菠菜 E. ludwigii99.44真空包装R.terrigena99.45西兰花普通包装P.azotoformans99.73真空包装R.ornithinolytica99.45普通包装L.amnigena99.44细香葱P. paralactis99.93真空包装B.cereus99.80上海青普通包装L.adecarboxylata99.17芹菜 真空包装B.cabrialesii99.66
普通包装冷藏上海青的主要腐败菌为非脱羧勒克菌(Leclercia adecarboxylata),该菌是肠杆菌科的一种革兰阴性杆菌,是非脱羧勒克菌属中唯一的种,生化特性与大肠埃希菌相似,是条件致病菌,可以引起败血症、伤口感染等,在凉拌菜中曾有检出[23]。
普通包装和真空包装的冷藏西兰花的主要腐败菌分别为产氮假单胞菌(Pseudomonas azotoformans)和解鸟氨酸拉乌尔菌(Raoultella ornithinolytica),前者在杂交石斑鱼[24]等食品中曾有检出,后者是从克雷伯菌中划分出来的一种需氧芽孢革兰氏阴性杆菌,可引起新生儿解鸟氨酸拉乌尔菌败血症[25]。
冷藏细香葱的主要腐败菌为河生莱略特氏菌(Lelliottia amnigena)和拟副乳假单胞菌(Pseudomonas paralactis),河生莱略特氏菌是一种革兰氏阴性植物致病菌,能够引起洋葱鳞茎[26]和马铃薯块茎[27]的软腐病;真空包装冷藏细香葱中分离到蜡样芽孢杆菌(Bacillus cereus),该菌是革兰氏阳性需氧芽孢杆菌,属于兼性好氧菌,能在厌氧的条件下生长,可以污染蔬菜、奶制品、肉制品[28]等多种类型的食物,有些菌株会引起食物中毒,例如“炒饭综合症”。真空包装冷藏芹菜的腐败菌为卡氏芽孢杆菌(Bacillus cabrialesii),该菌为2019年发现的新种[29],其性质有待进一步研究。
鲜切蔬菜中的腐败细菌主要为革兰氏阴性菌,这与蔬菜的贮藏条件有关,革兰氏阳性菌的最适生长温度一般为20~40 ℃,而很多革兰氏阴性菌则能够耐受较低温度并生长繁殖。假单胞菌在低温条件下生长速度较快,可以产生水解酶致使蔬菜软腐,一些种类还具有很强的产生氨等腐败产物的能力[30],是鲜切蔬菜的主要腐败菌之一。程媛媛等[9]对4 ℃条件下贮藏的鲜切西兰花进行了腐败菌的分离与鉴定,结果表明,鲜切西兰花在冷藏过程中的主要腐败细菌主要为恶臭假单胞杆菌等革兰氏阴性菌,与本实验鲜切西兰花和细香葱主要腐败菌有假单胞菌的结果一致。细菌多样性结果显示假单胞菌属在腐败样品中丰度较高,而其他分离得到的菌种在腐败样品中的丰度较低,表明腐败样品中的优势菌并不一定是腐败优势菌。
3 结论
鲜切蔬菜菌落总数的增长趋势表明,真空包装对菠菜、上海青、细香葱表现出明显的抑菌效果,菌落总数显著低于普通包装;但对芹菜未表现出显著的抑菌效果,可能与芹菜中的抑菌成分有关。真空包装西兰花菌落总数显著高于普通包装,这可能与真空包装造成西兰花组织液渗漏有关。
对5种蔬菜的微生物多样性和丰度进行分析,发现冷藏蔬菜中优势好氧真菌主要为线黑粉酵母属、小不整球壳属、链格孢霉属和维希尼克氏酵母属等;优势好氧细菌为假单胞菌属、黄杆菌属和杜擀氏菌属等;优势厌氧真菌主要为孢子属和新灰菌属等;优势兼性厌氧细菌主要为乳球菌属、魏斯氏属和欧文氏菌属等;优势厌氧细菌为泛菌属和拉恩氏菌属等。篮状菌属是最常见的真菌,存在于除上海青外其他4种新鲜蔬菜样品中,但在腐败样品中却丰度很低。小不整球壳属是最常见的主要腐败真菌,存在于上海青、西兰花新鲜样品和除芹菜外其他4种普通包装腐败蔬菜样品中。假单胞菌属是常见的果蔬腐败菌之一,在5种蔬菜的新鲜样品和普通包装腐败样品中丰度均较高;其他菌属在不同蔬菜中差异性较大。
对5种蔬菜中的主要腐败菌进行鉴定分析,发现主要的腐败菌以革兰氏阴性菌为主。其中普通包装菠菜、上海青、西兰花及细香葱的主要腐败菌分别为肠杆菌属、非脱羧勒克菌属、假单胞菌属、河生莱略特氏菌属;真空包装菠菜和西兰花的主要腐败菌为拉乌尔菌属,真空包装芹菜和细香葱的主要腐败菌为芽孢杆菌属。细菌多样性分析结果显示,上述腐败菌种在大部分样品中的丰度较低,即腐败样品中的优势菌不一定是主要腐败菌。
[1] 冯岩岩, 王庆国.鲜切菠菜和香菜专用自发气调包袋的研制[J].食品工业科技, 2020, 41(11):287-293.FENG Y Y, WANG Q G.Development of special modified atmosphere packaging of fresh-cut spinach and coriander[J].Science and Technology of Food Industry, 2020, 41(11):287-293.
[2] 安容慧, 陈皖豫, 胡花丽,等.贮藏温度对采后上海青叶片衰老及活性成分的影响[J].包装工程, 2020, 41(9):7-16.AN R H, CHEN W Y, HU H L, et al.Effects of storage temperature on senescence and contents of active components in postharvest leaves of pakchoi (Brassica chinensis L.)[J].Packaging Engineering, 2020, 41(9):7-16.
[3] 王高敏. 芹菜素的高效提取及健康芹菜制品的研制[D].青岛:青岛科技大学, 2021.WANG G M.Efficient extraction of apigenin and development of healthy celery products [D].Qingdao:Qingdao University of Science and Technology, 2021.
[4] KOOTI W, DARAEI N.A Review of the antioxidant activity of celery (Apium graveolens L)[J].Journal of Evidence-Based Complementary &Alternative Medicine, 2017, 22(4):1029-1034.
[5] 管玉格. 鲜切西兰花酚类物质生物合成机制及其抗氧化活性的研究[D].大连:大连理工大学, 2021.GUAN Y G.Study on biosynthesis mechanism of phenolic compounds in fresh-cut broccoli[D].Dalian:Dalian University of Technology, 2021.
[6] 叶保华, 赵继承, 朱胜龙.鲜切西兰花贮藏保鲜技术研究[J].包装与食品机械, 2009, 27(3):18-21.YE B H, ZHAO J C, ZHU S L.Studies on storing technology of fresh brassicao leraceav uitailca[J].Packaging and Food Machinery, 2009, 27(3):18-21.
[7] 郭元元, 张力, 蒋月喜, 等.细香葱种质资源花粉活力及测定方法的比较[J].中国瓜菜, 2020, 33(8):45-48.GUO Y Y, ZHANG L, JIANG Y X, et al.Comparison of pollen viability and determination methods of the germplasm resources of Allium schoenoprasum[J].China Cucurbits and Vegetables, 2020, 33(8):45-48.
[8] 王宏. 鲜切蔬菜保鲜工艺的研究[J].农业科技通讯, 2008(12):84-86.WANG H.Study on fresh-keeping technology of fresh-cut vegetables[J].Bulletin of Agricultural Science and Technology, 2008(12):84-86.
[9] 程媛媛, 古静燕, 陈宇航, 等.鲜切西兰花贮藏过程中腐败细菌的多样性分析[J].中国果菜,2019, 39(7):1-5,11.CHENG Y Y, GU J Y, CHEN Y H, et al.The diversity analysis of dominant spoilage microbial flora in fresh-cut broccoli during storage[J].China Fruit &Vegetable, 2019, 39(7):1-5, 11.
[10] 冯晓汀. 鲜切西兰花保鲜及机理研究[D].武汉:华中农业大学, 2016.FENG X T.Study on preservation and mechanism of fresh-cut broccoli[D].Wuhan:Huazhong Agricultural University, 2016.
[11] 焦贺, 孟敌, 韩颖, 等.微酸性电解水对采后香葱抑菌特性及贮藏品质的影响[J].食品科学, 2024,45(9):197-203.JIAO H, MENG D, HAN Y, et al.Effect of slightly acidic electrolyzed water treatment on antibacterial properties and storage quality of postharvest chives[J].Food Science, 2024,45(9):197-203.
[12] PRAKOSO Y A, RINI C S, RAHAYU A, et al.Celery (Apium graveolens) as a potential antibacterial agent and its effect on cytokeratin-17 and other healing promoters in skin wounds infected with methicillin-resistant Staphylococcus aureus[J].Veterinary World, 2020, 13(5):865-871.
[13] 闫亚茹. 三种绿色蔬菜多酚的分离鉴定及生物活性研究[D].西安:西安工程大学, 2018.YAN Y R. Isolation, identification and biological activities of polyphenols from three green vegetables[D]. Xi’an: Xi’an Polytechnic University, 2018.
[14] MART NEZ-HERN
NEZ-HERN NDEZ G B, G
NDEZ G B, G MEZ P A, PRADAS I, et al.Moderate UV-C pretreatment as a quality enhancement tool in fresh-cut Bimi® broccoli[J].Postharvest Biology and Technology, 2011,62(3):327-337.
MEZ P A, PRADAS I, et al.Moderate UV-C pretreatment as a quality enhancement tool in fresh-cut Bimi® broccoli[J].Postharvest Biology and Technology, 2011,62(3):327-337.
[15] 王斐, 刘慧君, 陈湘宁, 等.次氯酸钠对鲜切洋葱品质与微生物多样性影响研究[J].河北农业大学学报, 2021, 44(1):75-84.WANG F, LIU H J, CHEN X N, et al.Effect of sodium hypochlorite on safe nutrition quality and microbial diversity of fresh-cut onions[J].Journal of Hebei Agricultural University, 2021, 44(1):75-84.
[16] MADUREIRA J, GONÇALVES S, SANTOS-BUELGA C, et al.Microbiota assessment of fresh-cut apples packaged in two different films[J].Microorganisms, 2023, 11(5):1157.
[17] MANTHOU E, COEURET G, CHAILLOU S, et al.Metagenetic characterization of bacterial communities associated with ready-to-eat leafy vegetables and study of temperature effect on their composition during storage[J].Food Research International, 2022, 158:111563.
[18] SHANG H S, TAN B Z, DAKWA V, et al.Effect of pre-harvest sanitizer treatments on Listeria survival, sensory quality and bacterial community dynamics on leafy green vegetables grown under commercial conditions[J].Food Research International, 2023, 173:113341.
[19] MILLER L G, KASPAR C W.Escherichia coli O157:H7 acid tolerance and survival in apple cider[J].Journal of Food Protection, 1994, 57(6):460-465.
[20] DRANCOURT M, BOLLET C, CARTA A, et al.Phylogenetic analyses of Klebsiella species delineate Klebsiella and Raoultella gen.nov., with description of Raoultella ornithinolytica comb.nov., Raoultella terrigena comb.nov.and Raoultella planticola comb.nov[J].International Journal of Systematic and Evolutionary Microbiology, 2001, 51(Pt3):925-932.
[21] 贺字典, 闫立英, 石延霞, 等.产生ACC脱氨酶的PGPR种衣剂对黄瓜细菌性茎软腐病的防治效果[J].中国生物防治学报, 2017, 33(6):817-825.HE Z D, YAN L Y, SHI Y X, et al.Bio-control of PGPR seed coating producing ACC deaminase to cucumber bacterial stem soft rot disease[J].Chinese Journal of Biological Control, 2017, 33(6):817-825.
[22] PAWLICKI-JULLIAN N, COURTOIS B, PILLON M, et al.Exopolysaccharide production by nitrogen-fixing bacteria within nodules of Medicago plants exposed to chronic radiation in the Chernobyl exclusion zone[J].Research in Microbiology, 2010, 161(2):101-108.
[23] 李晓路, 张巍, 廖文, 等.凉拌菜中检出2株非脱羧勒克菌的鉴定与分析[J].预防医学论坛, 2019,25(10):785-787,790.LI X L, ZHANG W, LIAO W, et al.Identification and analysis on 2 strains Leclercia adecarboxylata detected in salad[J].Preventive Medicine Tribune, 2019, 25(10):785-787, 790.
[24] HUANG W B, XIE J.Characterization of the volatiles and quality of hybrid grouper and their relationship to changes of microbial community during storage at 4 ℃[J].Molecules (Basel, Switzerland), 2020, 25(4):818.
[25] YAPRAK D, MISIRLIGIL M, BOZAT A D, et al.Neonatal community-acquired Raoultella ornithinolytica septicemia:A case report and review of the literature[J].The Pediatric Infectious Disease Journal, 2021, 40(10):e370-e373.
[26] LIU S Y, TANG Y X.Identification and characterization of a new Enterobacter onion bulb decay caused by Lelliottia amnigena in China[J].Applied Microbiology:Open Access, 2016, 2(2):1000114.
[27] OSEI R, YANG C D, CUI L X, et al.Isolation, identification, and pathogenicity of Lelliottia amnigena causing soft rot of potato tuber in China[J].Microbial Pathogenesis, 2022, 164:105441.
[28] 孔丽. 肉与肉制品源蜡样芽胞杆菌的风险评估与防控技术研究[D].广州:暨南大学, 2019.KONG L.Risk assessment and prevention and control technology of Bacillus cereus from meat and meat products [D].Guangzhou:Jinan University, 2019.
[29] DE LOS SANTOS VILLALOBOS S, ROBLES R I, PARRA COTA F I, et al. Bacillus cabrialesii sp.nov., an endophytic plant growth promoting bacterium isolated from wheat (Triticum turgidum subsp.durum) in the Yaqui Valley, Mexico[J].International Journal of Systematic and Evolutionary Microbiology, 2019, 69(12):3939-3945.
[30] CUI S Q, YU X L, CHEN Y, et al.Bacterial diversity and dominant spoilage microorganisms in fresh-cut broccoli[J].Applied Sciences, 2022, 12(7):3370.