芜菁[(Brassica rapa spp.rapa)]又名蔓菁,为十字花科(Brassicaceae)芸薹属二年生蔬菜作物[1],其肉质根含有丰富的硫代葡萄糖苷、多糖以及黄酮类物质,具有抗缺氧、抗氧化、调节血糖以及预防癌症等功能[2-3]。芜菁因较高的营养价值得到越来越多消费者的青睐,但新鲜的芜菁水分含量高,贮藏过程容易发生糠心、萎蔫和霉变,极大限制了芜菁的开发和利用。干燥是十字花科类蔬菜深加工的重要方式之一,真空冷冻干燥是一种新型优质的干燥方式[4],该技术可保留食品中热敏性物质及营养成分[5],真空冷冻干燥技术大幅降低原料质量,便于运输,适合长期保存[6]。目前已经实现了芜菁冻干片的产业化生产。风味是芜菁冻干片品质评价的重要指标,直接影响消费者的接受和喜爱程度。高琦等[7]综合评价了4种干燥方式对芜菁脆片香气品质的影响,结果表明真空冷冻干燥的芜菁脆片香气品质最佳。
目前,研究食品风味的技术手段主要有气相色谱-质谱联用(gas chromatography-mass spectrometry,GC-MS)[8]和气相色谱-离子迁移谱(gas chromatography-ion mobility spectrometry,GC-IMS)等[9]。GC-MS结合了气相色谱的高分离能力和质谱的高鉴定能力,但是该方法对低分子质量物质和微量挥发性物质的灵敏度较低,导致样品中此类挥发性化合物容易被忽视[10]。GC-IMS通过离子漂移时间的差异来检测挥发性物质,适用于低浓度挥发性物质的痕量检测[11-12],弥补了GC-MS技术的不足,具有检测速度快、无需样品前处理、分辨率高、操作简便、数据可视化、灵敏度高和分析速度快等优点[13]。近年来,GC-IMS技术在食品风味分析、质量检测等领域得到了广泛的应用,但是数据库的局限性阻碍了挥发性化合物的定性测定。已有研究证实,多种仪器结合使用可为食品风味特征评估提供快速全面的方法[14-15]。然而,目前鲜见GC-MS和GC-IMS相结合分析芜菁冻干片风味的研究。本研究将顶空-固相微萃取-气相色谱-质谱(headspace solid phase microextraction gas chromatography-mass spectrometry,HS-SPME-GC-MS)与顶空-气相色谱-离子迁移谱(headspace gas chromatography-ion mobility spectrometry,HS-GC-IMS)相结合,对芜菁冻干片中挥发性有机物(volatile organic compounds,VOCs)进行全面分析,并结合主成分分析(principal component analysis,PCA)、偏最小二乘判别法(partial least squares-discriminant analysis,PLS-DA)等化学计量法,基于变量投影重要度(variable importance in projection,VIP)值探究不同品种芜菁冻干片VOCs的差异,研究可为芜菁深加工产品的开发与利用提供数据支持。
1 材料与方法
1.1 材料
实验所用芜菁由新疆艾力努尔有限公司柯坪县芜菁种植基地种植。
1.2 仪器与设备
FD5-4 型冷冻干燥机,美国GOLD SIM公司;FlavourSpec气相色谱离子迁移谱联用仪,德国 G.A.S 公司;QP 2020 NX气相色谱-质谱联用仪(GC-MS),日本岛津公司;AL104分析天平,梅特勒-托利多仪器(上海)有限公司。
1.3 实验方法
1.3.1 样品的制备
将新鲜芜菁切片,均匀平铺在冷冻干燥机托盘上,冷冻温度为-50 ℃,冷冻时间36 h。不同品种芜菁冻干片的外观如图1所示。干燥后将芜菁冻干片粉碎,过40目筛混合均匀,密封备用。

图1 不同品种芜菁冻干片外观
Fig.1 Appearance of turnip freeze-dried slices with different varieties
注:ZD、HD、BD 分别代表紫色冻干片、黄色冻干片、白色冻干片(下同)。
1.3.2 HS-SPME-GC-MS分析条件
HS-SPME萃取条件:采用SPME Arrow萃取头,先在260 ℃下老化10 min;然后60 ℃恒温振荡20 min,转速250 r/min,称0.5 g样品于顶空瓶中70 ℃萃取 45 min,并于250 ℃下解析5 min进行GC-MS分析。
色谱条件:PolarWAX柱(30 m×0.25 mm×0.25 μm),载气为高纯氦气,进样口温度250 ℃,不分流进样,溶剂延迟3 min。程序升温:40 ℃保持3 min,以5 ℃/min升至200 ℃后保持5 min,再以10 ℃/min升至230 ℃后保持5 min。
质谱条件:电子轰击离子源,离子源温度200 ℃,质谱接口温度250 ℃,全扫描m/z 35~550。
基于NIST的数据库进行比对,保留匹配度>80%的物质,采用面积归一化法计算相对含量。
1.3.3 顶空气相色谱-离子迁移谱分析条件
色谱柱为MXT-5(15 m×0.53 mm×1 μm),漂移气和载气为高纯氮(99.999%)。取0.3 g样品于20 mL顶空瓶中,80 ℃孵育20 min。色谱柱温度60 ℃,漂移气的流量为75 mL/min,载气的流速设置:0~2 min为2.00 mL/min,2 min~10 min由2.00 mL/min升高至10.00 mL/min,10 min~20 min增至100.00 mL/min,20 min~30 min增加至150.00 mL/min,分析时间为30 min,顶空进样针温度85 ℃、进样量300 μL。
定性分析:基于GC保留指数和IMS相对迁移时间,与内置的NIST数据库和IMS数据库进行匹配。
定量分析:基于峰信号值强度,通过quantification功能进行半定量,按照面积归一法计算各组分的相对含量。
1.4 数据处理
利用Origin 2022软件绘制桑基图、韦恩图和PCA图,GraphPad Prism 8软件绘制柱形图;采用SIMCA 14.1软件进行PLS-DA,计算预测VIP值;并结合SPSS 25.0软件进行单因素ANOVA分析。
2 结果与分析
2.1 HS-SPME-GC-MS 分析
采用HS-SPME-GC-MS对3种芜菁冻干片的VOCs进行测定。芜菁冻干片中共检出96种VOCs,其中白色冻干片中65种,黄色冻干片中81种,紫色冻干片中69种。挥发性化合物的定性结果如表1所示,共含有16种醛类、11种醇类、10种酮类、14种酯类、5种酸类、14种含硫化合物、8种烷烃类、5种腈类及13种杂环类。由表1可知,3种芜菁冻干片中主要挥发性风味物质种类和含量之间存在明显差异。整体而言,黄色芜菁冻干片中挥发性物质种类比白色和紫色冻干片多。
表1 芜菁冻干片中挥发性物质的含量和种类HS-SPME-GC-MS 分析结果
Table 1 The contents and types of volatile organic compounds in turnip freeze-dried slices by HS-SPME-GC-MS

类别序号名称CAS号ZDHDBD气味描述醛类12-丁烯醛4170-30-30.85±0.020.20±0.011.54±0.01辛辣味2己醛66-25-10.09±0.010.37±0.020.16±0.01草腥味3反式-2-己烯醛6728-26-30.08±0.020.26±0.020.07±0.01青草味、果香味4壬醛124-19-60.27±0.020.53±0.020.25±0.01具有果香5(E,E)-2,4-己二烯醛142-83-6——0.19±0.016(E,E)-2,4-庚二烯醛4313-03-50.07±0.010.21±0.000.04±0.017苯甲醛100-52-70.08±0.010.16±0.010.14±0.00苦杏仁气味85-甲基-2-噻吩甲醛13679-70-4——0.20±0.01杏仁味9糠醛98-01-10.10±0.000.17±0.020.04±0.00焦糖、烤面包102-己烯醛505-57-7—0.27±0.01—青草香味113-糠醛498-60-20.16±0.000.18±0.00—杏仁味12反-2-壬烯醛18829-56-6—0.28±0.01—脂肪香、黄瓜味13(E, Z)-2,6 -壬二烯醛557-48-2—0.10±0.00—辛辣味14苯乙醛122-78-10.26±0.040.59±0.01—有杏仁、樱桃香15(E)-3,7-二甲基-2,6-辛二烯醛141-27-5—0.24±0.00—16正二十六烷醛26627-85-0—0.22±0.01—醇类1乙醇64-17-52.05±0.018.10±0.154.77±0.08甜香22,3-丁二醇24347-58-8——1.07±0.03黄油、奶酪香3辛醇111—87-50.11±0.010.19±0.000.13±0.01坚果、蘑菇4丙二醇57-55-6——1.03±0.125十九醇1454-84-80.06±0.010.08±0.000.12±0.006苯甲醇100-51-6——0.10±0.01水果香气7苯乙醇60-12-80.88±0.012.11±0.023.20±0.00花香、蜜香8十三醇112-70-9—0.18±0.020.07±0.00香料91-辛烯-3-醇3391-86-40.05±0.020.10±0.01—蘑菇味103-十四炔-1-醇55182-74-6—0.27±0.02—111-(2-丁氧基乙氧基)乙醇54446-78-50.16±0.03——酮类12,3-丁二酮431-03-80.48±0.010.80±0.021.59±0.03乳香味23-戊烯-2-酮625-33-20.35±0.02—1.09±0.02水果香气3羟基丙酮116-09-60.09±0.010.09±0.010.09±0.01焦糖味46-甲基-5-庚烯-2-酮110-93-00.04±0.002.69±0.050.07±0.00果香味和芳香味53,5-辛二烯-2-酮38284-27-40.19±0.010.64±0.010.47±0.02水果香6香叶基丙酮3796-70-10.24±0.011.49±0.050.22±0.01清甜香、花香72,3-二氢-3,5-二羟基-6-甲基-4(H)-吡喃-4-酮28564-83-20.18±0.010.53±0.130.25±0.0485-甲基-5-庚烯-3-酮1190-34-70.14±0.011.61±0.010.10±0.049反式-3-戊烯-2-酮3102-33-8—0.11±0.02—水果香气106-甲基-3,5-庚二烯-2-酮1604-28-0—0.49±0.01—酯类1二十二酸乙酯5908-87-2——0.10±0.0024-羟基丁酸乙酰酯591-81-10.41±0.060.93±0.010.07±0.013肉豆蔻酸乙酯124-06-10.04±0.010.12±0.010.06±0.00芹菜或黄油味4苯甲酸2-乙基己酯5444-75-70.68±0.030.71±0.020.98±0.045棕榈酸乙酯628-97-70.63±0.021.80±0.020.73±0.04果香味69-十六碳烯酸乙酯54546-22-40.06±0.010.20±0.030.07±0.017酞酸二甲酯131-11-3—0.06±0.010.04±0.01芳香味8亚油酸乙酯544-35-40.22±0.021.15±0.110.24±0.02果香、花香9邻苯二甲酸二异丁酯84-69-59.71±0.4416.12±0.1016.75±0.23芳香味10亚麻酸乙酯1191-41-90.44±0.021.65±0.060.72±0.01蜡味11邻苯二甲酸二丁酯84-74-20.08±0.000.22±0.030.09±0.02芳香味12癸酸乙酯110-38-3—0.17±0.01—脂肪香、果香13水杨酸甲酯119-36-8—0.34±0.02—草药香气14月桂酸乙酯106-33-2—0.36±0.02—花香果香
续表1

注:—表示样品中未检测到该物质。空白值表示未查到相关数据。
类别序号名称CAS号ZDHDBD气味描述酸类1乙酸64-19-75.95±0.026.33±0.2014.16±0.08醋酸味2壬酸112-05-00.46±0.040.66±0.061.24±0.14绿色、脂肪3癸酸334-48-50.14±0.010.16±0.010.25±0.02馊、脂肪4苯甲酸65-85-00.26±0.090.23±0.051.02±0.305丙酸79-09-40.13±0.010.21±0.00—酸味含硫化合物1二甲基三硫醚3658-80-80.16±0.000.25±0.010.09±0.00鱼肉、卷心菜22-甲硫基乙醇5271-38-5——0.07±0.003正辛基丙基硫醚3877-15-40.34±0.02—0.20±0.024甲酰甲基二甲基砜31043-74-0——0.20±0.0254-甲硫基丁醇20582-85-80.78±0.010.27±0.003.23±0.08洋葱、泥土65-甲硫基-戊腈59121-25-430.78±0.0517.69±0.5618.70±0.49辛辣味7氰基-3,4-环硫丁烷54096-45-61.80±0.051.60±0.080.19±0.0186-甲硫基己腈72931-29-410.47±0.144.17±0.203.33±0.1694-甲硫基丁基芥子油4430-36-87.48±0.041.07±0.043.76±0.2010异硫氰酸苯乙酯2257-09-24.47±0.061.04±0.072.97±0.12115-甲硫基丁基芥子油4430-42-61.59±0.030.16±0.010.4±0.0312二甲基二硫醚624-92-0—0.09±0.01—洋葱、卷心菜13环硫醚异构体30381-35-2—0.76±0.00—143-丁烯基芥子油3386-97-81.35±0.08——辛辣味烷烃类12,6,10,14-四甲基十五烷1921-70-60.11±0.02—0.1±0.01青草味、甜味2十七烷629-78-70.33±0.010.31±0.040.29±0.07燃料味33-甲基十七烷6418-44-60.09±0.030.08±0.010.06±0.014二苯基二乙氧基硅烷2553-19-70.62±0.020.68±0.040.90±0.015戊三氪烷630-04-60.08±0.070.06±0.050.09±0.0062,6,10-三甲基十三烷3891-99-4—0.22±0.01—72-甲基二十六烷1561-02-0—0.11±0.01—81-氰基-4,5-环噻吩戊烷58130-94-20.30±0.01——腈类1甲基丙烯腈4786-19-00.49±0.03—0.25±0.0222-甲基-5-己烯腈30316-00-80.10±0.010.14±0.000.07±0.013苯代丙腈645-59-010.54±0.029.33±0.145.52±0.30辛辣味43-甲基-2-丁烯腈4786-24-7—1.60±0.03—清香味52-戊烯腈13284-42-9—0.08±0.03—杂环类1乙偶姻513-86-00.32±0.011.20±0.051.17±0.03牛奶香气2N-(1-甲基亚庚基)甲胺18641-72-0——0.16±0.023二丙二醇丁醚29911-28-20.10±0.000.14±0.020.1±0.014邻苯二甲醚91-16-7—0.13±0.010.08±0.01香草味5苯并噻唑95-16-90.30±0.010.47±0.020.62±0.02橡胶味6乙二醇苯醚122-99-60.13±0.010.17±0.030.05±0.0174-(1,1-二甲基庚基)苯酚0.08±0.000.19±0.050.06±0.008己烯雌酚,O-(正丙氧基羰基)0.08±0.000.14±0.060.06±0.019二十烷基辛基醚—0.31±0.01—10二乙二醇丁醚112-34-5—0.15±0.02—112-乙酰基吡咯1072-83-9—0.26±0.02—坚果、核桃126-甲氧基喹啉氮氧化物6563-13-9—0.26±0.03—13癸醚2456-28-20.10±0.02——
为直观观察芜菁冻干片VOCs种类及相对含量,绘制热图、韦恩图和桑基图,如图2所示。由图2-a可以看出,不同品种芜菁冻干片中主要挥发性化合物种类及相对含量存在差异,乙酸、5-甲硫基-戊腈、邻苯二甲酸二异丁酯相对含量较高。5-甲硫基-戊腈是芜菁冻干片中相对含量最高的挥发性化合物,主要呈辛辣味,在白色、黄色、紫色芜菁冻干片中相对含量分别为19.19%、17.69%、30.78%。由图2-b可知,黄色冻干片中VOCs种类最多,共81种,以醛类、酯类为主;白色冻干片中含硫化合物和酯类种类最多;紫色冻干片中酯类、含硫化合物种类居多。结合图2-c可知,3种芜菁冻干片共有的VOCs有51种,仅存在于白色冻干片中的VOCs有9种,分别是(E,E)-2,4-己二烯醛、2,3-丁二醇、丙二醇、苯甲醇、二十二酸乙酯、2-甲硫基乙醇、甲酰甲基二甲基砜、N-(1-甲基亚庚基)甲胺、5-甲基-2-噻吩甲醛;仅存在于黄色冻干片中的VOCs有21种,即2-己烯醛、反-2-壬烯醛、(E,Z)-2,6-壬二烯醛、(E)-3,7-二甲基-2,6-辛二烯醛、正二十六烷醛、3-十四炔-1-醇、反式-3-戊烯-2-酮、6-甲基-3,5-庚二烯-2-酮、癸酸乙酯、水杨酸甲酯、月桂酸乙酯、二甲基二硫醚、环硫醚异构体、2,6,10-三甲基十三烷、2-甲基二十六烷、3-甲基-2-丁烯腈、2-戊烯腈、二十烷基辛基醚、二乙二醇丁醚、2-乙酰基吡咯、6-甲氧基喹啉氮氧化物;仅存在于紫色冻干片中的挥发性化合物有4种,即1-(2-丁氧基乙氧基)乙醇、3-丁烯基芥子油、1-氰基-4,5-环噻吩戊烷、癸醚。由图2-d可知,芜菁冻干片VOCs中醛类占比1.95%~3.74%、酮类占比1.77%~8.95%、醇类占比3.30%~11.01%、酯类占比12.32%~24.19%、酸类占比6.92%~16.3%、杂环类占比1.10%~3.38%、含硫化合物占比27.07%~59.19%、烷烃类占比1.45%~1.52%、腈类占比6.16%~11.14%。虽然3种芜菁冻干片中各类挥发性物质的相对含量差别较大,但3种芜菁冻干片中主要挥发性物质均为含硫化合物。

a-聚类分析热图;b-种类Sankey图;c-韦恩图;d-相对含量桑基图
图2 HS-SPME-GC-MS分析芜菁冻干片中VOCs的种类及含量
Fig.2 Types and contents of VOCs in turnip freeze-dried slices detected by HS-SPME-GC-MS
注:a图中HD、ZD、BD各重复3次实验;b图中不同颜色表示不同品种,带的粗细表示该组分含量的高低。
研究表明,挥发性含硫化合物广泛存在于多种食品中,具有阈值极低的特点,对食品感官品质具有重要贡献,在形成食品独特风味中至关重要[16]。芜菁独特的辛辣味主要来源于含硫化合物。3种芜菁冻干片中均检出4-甲硫基丁基芥子油、5-甲硫基丁基芥子油和3-丁烯基芥子油等硫代葡萄糖苷。硫代葡萄糖苷在芥子酶或热诱导下降解形成腈类和异硫氰酸化合物,并产生天然活性物质[17]。芜菁冻干片中检出5-甲硫基戊腈、6-甲硫基己腈2种含硫腈类,其中5-甲硫基戊腈是芜菁冻干片中相对含量最高的VOCs,这一结果与之前的研究一致,即5-甲硫基戊腈是芜菁粉中的主要挥发性物质[18]。由表1可知,在3种芜菁冻干片中均检测到了异硫氰酸苯乙酯,异硫氰酸苯乙酯是先前报道的白菜中含量较高的化合物。已有研究表明异硫氰酸酯是十字花科植物产生刺激性气味的主要原因[19-20]。此外,在芜菁冻干片中还检出了二甲基二硫醚和二甲基三硫醚,已有研究表明这2种物质主要呈现出硫化物异味及新鲜洋葱味,是十字花科植物特有的香味活性物质[21]。
分析芜菁冻干片中相对含量排名前10的挥发性化合物(图3-a~图3-c)可知,不同品种冻干片中含量排名前十的挥发性化合物种类及相对含量不同,其中乙醇、乙酸、5-甲硫基-戊腈、苯代丙腈、6-甲硫基己腈、邻苯二甲酸二异丁酯是3种芜菁冻干片共有且相对含量排名前10的化合物。

a-HS-SPME-GC-MS, BD;b-HS-SPME-GC-MS, HD; c-HS-SPME-GC-MS, ZD; d-HS-GC-IMS, BD; e-HS-GC-IMS, HD; f-HS-GC-IMS, ZD
图3 HS-SPME-GC-MS和HS-GC-IMS检测到相对含量排名前10的化合物
Fig.3 The top 10 volatiles in sample detected by HS-SPME-GC-MS and HS-GC-IMS
2.2 HS-GC-IMS分析
对3种芜菁冻干片进行HS-GC-IMS测定,结果如图4所示。图中X、Y和Z轴分别代表离子迁移时间、保留时间和峰强度,图中的点代表芜菁冻干片中的挥发性化合物,点的颜色代表峰值强度,颜色越深,峰值的强度越高。图4-a直观地反映了3种芜菁冻干片中挥发性物质的差别,黄色冻干片中挥发性化合物种类多于其他2种样品。由图4-b可以看出,3种芜菁冻干片的挥发性成分分离程度较好,大多数峰的保留时间为100~800 s,漂移时间为1.0~1.5 s。为确定3种芜菁冻干片中挥发性化合物种类,根据保留时间和迁移时间对挥发性化合物进行定性分析,一共鉴定出94种VOCs,其中27种化合物未能定性,定性出67种,包括醇类7种、醛类23种、酮类7种、酯类12种、酸类4种、含硫化合物3种、杂环类11种。
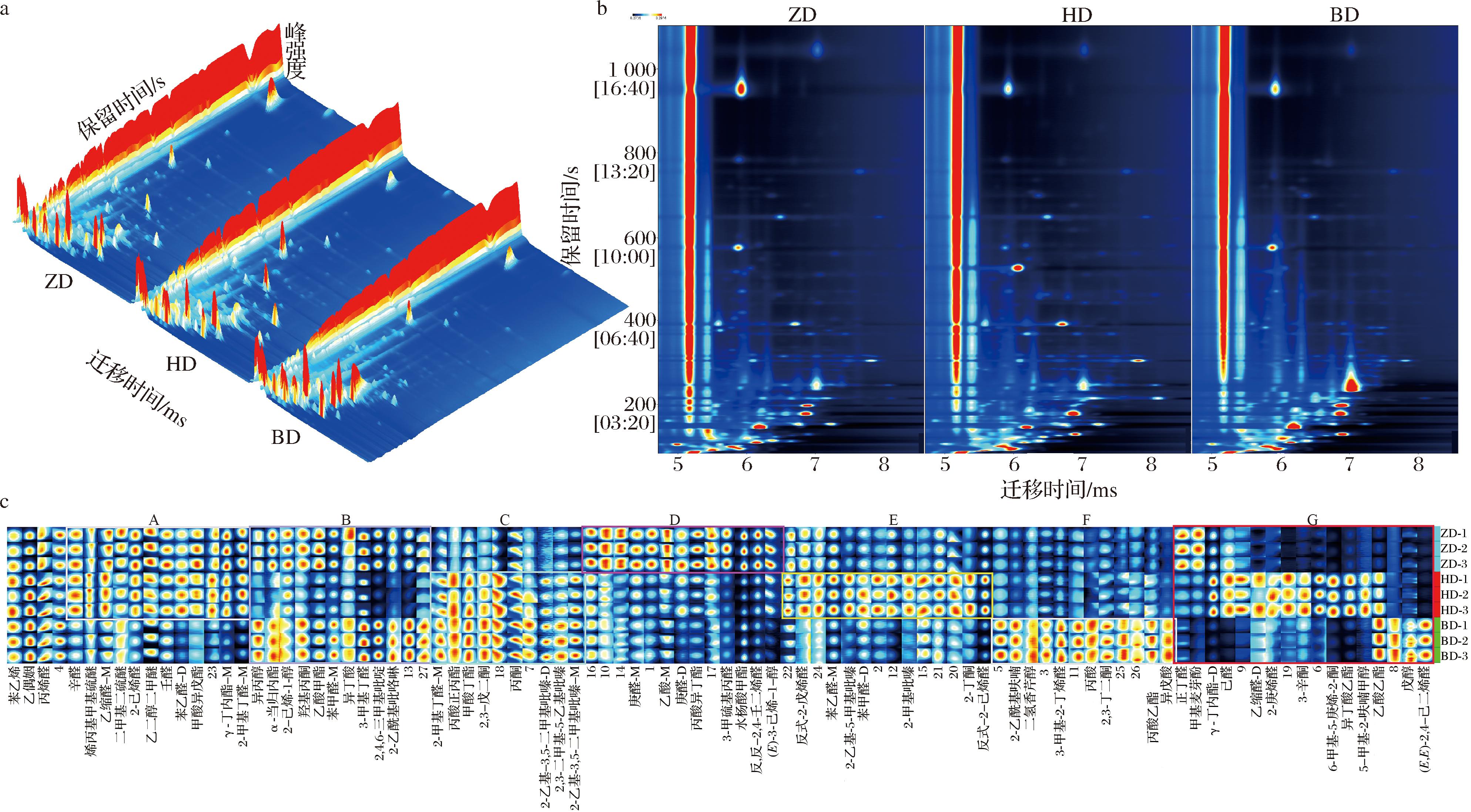
a-三维图谱;b-二维图谱;c-指纹图谱
图4 芜菁冻干片中挥发性化合物的HS-GC-IMS谱图
Fig.4 Volatile organic compounds in different turnip freeze-dried slices detected by HS-GC-IMS
为进一步比较不同芜菁样品VOCs的差异,利用Gallery Plot插件生成指纹图谱,结果如图4-c所示。每一行代表一个样本,每一列代表一个化合物。一些挥发性化合物由于性质和浓度不同,可能会产生多个信号(单体和二聚体)[22],部分物质后面的M和D分别代表其单体和二聚体。已定性的化合物用物质名称标记,未定性出的化合物用数字标记。对比图4-c可以看出,不同品种芜菁冻干片含有共同的VOCs,也有各自的特征VOCs。A框为3种芜菁冻干片共有且在紫色、黄色冻干片中相对含量较高的特征峰区域,有12种化合物,主要为醛类化合物,包括2-甲基丁醛-D、γ-丁内酯-M、甲酸异戊酯、苯乙醛-D、壬醛、辛醛、乙二醇二甲醚、乙缩醛-M、2-己烯醛以及二甲基二硫醚、烯丙基甲基硫醚等。B框为紫色、白色冻干片共有且相对含量高于黄色冻干片的物质,主要是2-乙酰基吡咯啉、2,4,6-三甲基吡啶、3-甲基丁醛、异丁酸、苯甲醛-M、乙酸甲酯、羟基丙酮、2-己烯-1-醇、α-当归内酯、异丙醇等物质。C框为白色、黄色芜菁冻干片中相对含量显著高于紫色芜菁冻干片的物质,如2-乙基-3,5-二甲基吡嗪、2,3-二甲基-5-乙基吡嗪、丙酮、2,3-戊二酮、甲酸丁酯、丙酸正丙酯、2-甲基丁醛-M等。D框为紫色芜菁冻干片样品含量较高的化合物,包括(E)-3-己烯-1-醇、(E,E)-2,4-己二烯醛、水杨酸甲酯、3-甲硫基丙醛、丙酸异丁酯、庚醛、乙酸-M等。E框为黄色芜菁冻干片样品含量较高的化合物,包括反式-2-己烯醛、2-丁酮、2-甲基吡嗪、苯甲醛-D、2-乙基-5-甲基吡嗪、苯乙醛-M、反式-2-戊烯醛等。F框为白色芜菁冻干片中含量较高的化合物,包括异戊酸、丙酸乙酯、2,3-丁二酮、丙酸、3-甲基-2-丁烯醛、二氢香芹醇、2-乙酰基呋喃等化合物。G框中的挥发性化合物仅在1或2种芜菁冻干片中存在,分别为(E,E)-2,4-己二烯醛、戊醇、乙酸乙酯、5-甲基-2-呋喃甲醇、异丁酸乙酯、6-甲基-5-庚烯-2-酮、3-辛酮、2-庚烯醛、乙缩醛-D、己醛、γ-丁内酯-D、甲基麦芽酚、正丁醛。
由图5-a可以看出,3种芜菁冻干片中挥发性化合物的含量差异很大,其中乙偶姻、3-甲基丁醛、水杨酸甲酯、3-甲基-2-丁烯醛等化合物相对含量较高。结合3种芜菁冻干片中相对含量前10的挥发性化合物(图3-d~图3-f)可知,水杨酸甲酯、3-甲基-2-丁烯醛、乙偶姻、3-甲基丁醛和丙酮在3种芜菁冻干片共有且相对含量排名前10。其中,白色冻干片中3-甲基-2-丁烯醛相对含量最高,为15.78%;紫色冻干片中水杨酸甲酯相对含量最高,为14.72%;黄色冻干片中水杨酸甲酯和3-甲基-2-丁烯醛相对含量较高,分别为6.63%、6.91%。

a-聚类分析热图;b-种类桑基图;c-韦恩图;d-相对含量桑基图
图5 HS-GC-IMS分析芜菁冻干片中VOCs的种类及含量
Fig.5 Types and contents of VOCs in freeze-dried turnip slices detected by HS-GC-IMS
综合图5-b~图5-d结果可知,3种芜菁冻干片中种类较多的挥发性化合物是酯类、醛类和杂环类,其中醛类是最主要的挥发性化合物。黄色冻干片中VOCs种类最多,为91种;紫色冻干片中化合物种类最少。由图5-c可知,3种芜菁冻干片共有VOCs有78种,黄色芜菁冻干片特征VOCs有4种,分别为6-甲基-5-庚烯-2-酮、6、异丁酸乙酯和5-甲基-2-呋喃甲醇。白色芜菁冻干片特征VOCs有3种,分别为(E,E)-2,4-己二烯醛、8、戊醇。芜菁冻干片中醛类相对含量最高,为28.31%~35.13%;酯类相对含量次之,为17.30%~24.51%;酮类相对含量为6.70%~12.61%,醇类相对含量为3.78%~4.66%,酸类相对含量为2.66%~4.14%,杂环类相对含量为9.34%~11.04%,含硫化合物1.55%~2.10%和未定性18.76%~20.67%。
对比HS-SPME-GC-MS和HS-GC-IMS的结果发现,二者共同检测出来的挥发性物质有醛类、酮类、醇类、酯类、酸类、杂环类、含硫化合物,其中2,3-丁二酮、己醛、反式-2-己烯醛、乙偶姻、羟基丙酮、6-甲基-5-庚烯-2-酮、壬醛、(E,E)-2,4-己二烯醛、乙酸、苯甲醛、二甲基二硫醚、2-己烯醛、丙酸、苯乙醛和水杨酸甲酯为共同检测出的VOCs,虽然2种方法测定的挥发性物质种类和含量不同,但黄色芜菁冻干片中VOCs的种类最多,紫色芜菁冻干片VOCs种类最少这个结果相同。HS-SPME-GC-MS单独检测出了烷烃类物质,这可能是由于2种方法检测原理不同,HS-GC-IMS 主要依靠化合物的质子亲和力,烷烃类物质的质子亲和力比水弱,因此无法检测出烷烃类物质[23]。由于IMS数据库不够完善,利用HS-GC-IMS检测出的芜菁冻干片挥发性物质种类比HS-SPME-GC-MS少,但HS-GC-IMS 技术的高灵敏度可以弥补HS-SPME-GC-MS 无法检测痕量物质的不足,同时可以检测出以单体和二聚体形式存在的挥发性物质,2种检测方法互相补充。2种方法的结合可以更全面地定性芜菁冻干片中挥发性成分。
2.3 芜菁冻干片中差异挥发性化合物
为了揭示不同品种芜菁冻干片挥发性化合物的差异,分别对HS-SPME-GC-MS和HS-GC-IMS测定的挥发性化合物进行主成分分析,结果如图6-a、图6-b所示,第一主成分的贡献率分别为63%、51.4%,第二主成分的贡献率分别为32%、40.5%,两者的累计贡献率均超过90%,表明PC1和PC2这2个主成分可以较好地解释3种芜菁冻干片挥发性化合物的信息。从图6可以看出不同品种芜菁冻干片分散在不同的象限距离较远,说明3种芜菁冻干片的挥发性化合物存在较大差异。

a-GC-MS PCA得分;b-GC-IMS PCA得分;c-GC-MS差异挥发物;d-GC-IMS差异挥发物;e-GC-MS VOCs的PLS-DA分析;f-GC-IMS VOCs的PLS-DA分析;g-GC-MS交叉验证;h-GC-IMS交叉验证
图6 三种芜菁冻干片VOCs的多元统计分析
Fig.6 Multivariate statistical analysis of VOCs of three kinds of turnip freeze-dried slices
PLS-DA 是一种具有监督判别模式的统计方法,可以有效解释观测值并进行相应变量预测,通过R2和Q2对模型的可靠性和预测能力进行评估,R2和Q2均大于 0.5表示模型拟合度可接受,越接近 1 表示预测能力越强[24]。分别以GC-MS和GC-IMS检测结果中的VOCs相对含量为因变量,不同品种芜菁冻干片为自变量进行PLS-DA分析。不同颜色的点代表不同样品,结果表明PLS-DA分析可用于不同品种芜菁冻干片挥发性成分鉴别分析。如图6-e~图6-h所示,GC-MS中R2x为0.822,R2y为0.994,Q2为0.958;GC-IMS的PLS-DA分析中R2x为0.976,R2y为0.997,Q2为0.992,R2、Q2均大于0.5表示该模型具有较好的预测特性,经200次置换检验,分析结果中Q2与纵轴的相交点均小于0,说明模型有效,不存在过拟合。
为了进一步衡量每个变量的贡献,基于PLS-DA模型预测了各挥发性成分VIP值,当VIP值>1表明该变量对整体判别模型的贡献度高[25]。筛选VIP值>1的化合物作为差异挥发性化合物(图6-c~图6-d)。在GC-MS结果中,VIP值>1的VOCs有59种,包括6种醇类、9种醛类、8种酮类、3种烷烃、10种酯类、9种含硫化合物、5种酸类和9种其他挥发性化合物。VIP值排名前10的挥发性化合物包括苯乙醇、苯并噻唑、十九醇、2,3-丁二酮、苯代丙腈、邻苯二甲酸二异丁酯、6-甲硫基己腈、二苯基二乙氧基硅烷、氰基-3,4-环硫丁烷、癸酸。在GC-IMS结果中,VIP值>1的VOCs有23种,包括1种醇类、5种醛类、2种酮类、6种酯类、1种酸类、2种杂环和6种未定性化合物。VIP值排名前10的挥发性化合物包括3-甲基-2-丁烯醛、水杨酸甲酯、6-甲基-5-庚烯-2-酮、3-甲基丁醛、13、乙酸乙酯、18、γ-丁内酯-D、2,4,6-三甲基吡啶、反,反-2,4-壬二烯醛。
3 结论
本实验采用HS-SPME-GC-MS和 HS-GC-IMS技术鉴定了3种芜菁冻干片的VOCs,结合PCA、PLS-DA等化学计量法分析了不同品种芜菁冻干片的VOCs差异。通过HS-SPME-GC-MS共鉴定出96种VOCs,通过HS-GC-IMS技术检出94种VOCs,因2种技术的检测原理、灵敏度、萃取方式、检测温度等条件不同,检测结果存在一定的差异,共同检测到的VOCs仅15种。PCA分析结果表明,HS-GC-IMS和HS-SPME-GC-MS均能有效区分3种芜菁冻干片。在PLS-DA分析结果的基础上通过VIP确定了芜菁冻干片的差异挥发性化合物。HS-SPME-GC-MS和HS-GC-IMS技术联合使用可以最大限度地提高结果准确性,全面表征不同品种芜菁冻干片的挥发性成分差异,有助于进一步了解芜菁冻干片风味形成的机理,为芜菁冻干片产品风味质量调控提供依据。
[1] PAUL S, GENG C G, YANG T H, et al.Phytochemical and health-beneficial progress of turnip (Brassica rapa)[J].Journal of Food Science, 2019, 84(1):19-30.
[2] LIN S E, MIAO Y J, SU S W, et al.Comprehensive analysis of Ogura cytoplasmic male sterility-related genes in turnip (Brassica rapa ssp.rapifera) using RNA sequencing analysis and bioinformatics[J].PLoS One, 2019, 14(6):e0218029.
[3] ZHANG H Y, SCHONHOF I, KRUMBEIN A, et al.Water supply and growing season influence glucosinolate concentration and composition in turnip root (Brassica rapa ssp.rapifera L.)[J].Journal of Plant Nutrition and Soil Science, 2008,171(2):255-265.
[4] 刘野婷. 西洋参冻干片工艺及质量标准研究[D].长春:长春中医药大学, 2022.LIU Y T.Study on technology and quality standard of ginseng freeze-dried American tablets[D].Changchun:Changchun University of Chinese medicine, 2022.
[5] HU L N, BI J F, JIN X, et al.Study on the rehydration quality improvement of shiitake mushroom by combined drying methods[J].Foods, 2021, 10(4):769.
[6] 李宝磊, 张丽, 陈苏, 等.真空冷冻干燥技术在食品和中草药行业的应用[J].饮料工业, 2019,22(6):71-74.LI B L, ZHANG L, CHEN S, et al.Application of freeze-drying technology in food and Chinese herbal medicine industry[J].Beverage Industry, 2019,22(6):71-74.
[7] 高琦, 韩昊廷, 李加恒, 等.基于主成分分析法综合评价四种干燥方式对芜菁脆片香气品质的影响[J].食品工业科技, 2018,39(22):212-218; 224.GAO Q, HAN H T, LI J H, et al.Comprehensive evaluation of four drying methods on aroma quality of turnip chips based on principal component analysis[J].Science and Technology of Food Industry, 2018,39(22):212-218; 224.
[8] LI Y, YUAN L, LIU H J, et al.Analysis of the changes of volatile flavor compounds in a traditional Chinese shrimp paste during fermentation based on electronic nose, SPME-GC-MS and HS-GC-IMS[J].Food Science and Human Wellness, 2023, 12(1):173-182.
[9] ZHANG X X, DAI Z, FAN X J, et al.A study on volatile metabolites screening by HS-SPME-GC-MS and HS-GC-IMS for discrimination and characterization of white and yellowed rice[J].Cereal Chemistry, 2020,97(2):496-504.[10] CHEN Y, LI P, LIAO L Y, et al.Characteristic fingerprints and volatile flavor compound variations in Liuyang Douchi during fermentation via HS-GC-IMS and HS-SPME-GC-MS[J].Food Chemistry, 2021,361:130055.
[11] LIU N F, SHEN S S, HUANG L F, et al.Revelation of volatile contributions in green teas with different aroma types by GC-MS and GC-IMS[J].Food Research International, 2023,169:112845.
[12] SORRIBES-SORIANO A, DE LA GUARDIA M, ESTEVE-TURRILLAS F A, et al.Trace analysis by ion mobility spectrometry:From conventional to smart sample preconcentration methods.A review[J].Analytica Chimica Acta, 2018,1026:37-50.
[13] XIAO Y, HUANG Y X, CHEN Y L, et al.Discrimination and characterization of the volatile profiles of five Fu brick teas from different manufacturing regions by using HS-SPME/GC-MS and HS-GC-IMS[J].Current Research in Food Science, 2022,5:1788-1807.
[14] CHI X L, ZHANG Y D, ZHENG N, et al.HS-GC-IMS and HS-SPME/GC-MS coupled with E-nose and E-tongue reveal the flavors of raw milk from different regions of China[J].Current Research in Food Science, 2024,8:100673.
[15] FENG T, SUN J Q, SONG S Q, et al.Geographical differentiation of Molixiang table grapes grown in China based on volatile compounds analysis by HS-GC-IMS coupled with PCA and sensory evaluation of the grapes[J].Food Chemistry:X, 2022,15:100423.
[16] 王蓓, 韩兆盛, 杨智杰, 等.6类常见食品中含硫化合物风味特征及形成机理研究进展[J].食品科学技术学报, 2022,40(6):13-25.WANG B, HAN Z S, YANG Z J, et al.Research progress on flavor characteristics and formation mechanism of sulfur compounds in six common foods[J].Journal of Food Science and Technology, 2022,40(6):13-25.
[17] MAO X H, ZHAO X Z, HUYAN Z Y, et al.Relationship of glucosinolate thermal degradation and roasted rapeseed oil volatile odor[J].Journal of Agricultural and Food Chemistry, 2019,67(40):11 187-11 197.
[18] 王静, 吴江超, 李汴生.不同干燥方式制得的新疆恰玛古粉的成分、加工特性和香气比较[J].食品工业科技, 2023,44(22):257-265.WANG J, WU J C, LI B S.Components, processing characteristics and aroma of Xinjiang Qiamagu (Brassica rapa L.) powder prepared by different drying methods[J].Science and Technology of Food Industry, 2023, 44(22):257-265.
[19] BELL L, KITSOPANOU E, OLOYEDE O O, et al.Important odorants of four brassicaceae species, and discrepancies between glucosinolate profiles and observed hydrolysis products[J].Foods, 2021,10(5):1055.
[20] BODDUPALLI S, MEIN J.R, LAKKANNA S, et al.Induction of phase 2 antioxidant enzymes by broccoli sulforaphane:Perspectives in maintaining the antioxidant activity of vitamins A, C, and E[J].Frontiers in Genetics, 2012,3:7.
[21] 张越. 植物精油天然防腐剂制备及其在发酵蔬菜中的应用研究[D].南昌:南昌大学, 2023.ZHANG Y. Study on preparation of natural preservatives for plant essential oil and its application in fermented vegetables[D]. Nanchang: Nanchang University, 2023.
[22] 金文刚, 别玲玲, 裴金金, 等.基于GC-IMS技术分析炖煮过程中大鲵头汤挥发性风味物质[J].食品工业科技, 2021,42(19):307-313.JIN W G, BIE L L, PEI J J, et al.Volatile flavor compounds of giant salamander (Andrias davidianus) head soup during stewing based on GC-IMS technology[J].Science and Technology of Food Industry, 2021, 42(19):307-313.
[23] 夏兰欣, 周贵华, 王广, 等.GC-MS和GC-IMS分析食用油对熟炕马铃薯挥发性成分的影响[J].中国粮油学报,2022,37(12):236-245.XIA L X,ZHOU G H,WANG G, et al.Conjoint analysis of effects of edible oil on volatile components of cooked Kang potatoes by GC-MS and GC-IMS[J].Journal of the Chinese Cereals and Oils Association,2022,37(12):236-245.
[24] 夏诗琪, 周成钏, 郭昌庆, 等. 基于广泛靶向代谢组学分析花榈木不同部位挥发性代谢物差异[J]. 天然产物研究与开发, 2023, 35(12):2027-2039.XIA S Q, ZHOU C C, GUO C Q, et al. Differential analysis of volatile metabolites in different parts of Ormosia henryi by using widely-targeted volatilomics method[J]. Natural Product Research and Development, 2023, 35(12):2027-2039.
[25] OLIVEIRA L F C, TEGA D U, DUARTE G H B, et al. Foodomics for agroecology: Differentiation of volatile profile in mint (Mentha×gracilis Sole) from permaculture, organic and conventional agricultural systems using HS-SPME/GC-MS[J]. Food Research International, 2022, 155:111107.