随着生活水平的提高,人们对调味品的品质要求精益求精,而风味是消费者选择产品最直观的要求。人们常使用增味剂以改变和提升食物的风味[1],增味剂属于调味品的一种,主要用于增强食品的感官特性特别是其味道和风味[2]。这些能够增强食物风味的物质天然存在于某些食物中,其特征是谷氨酸或核苷肌苷酸和鸟苷酸的呈现,以谷氨酸为原料制备的增味剂为代表[3]。谷氨酸是在自然界广泛分布的一种常见的酸性氨基酸,是食品香精的重要来源之一。葡萄糖是一种在自然界中分布范围很广且十分重要的单糖,在食品、生物和医药等领域都有着广泛的用途。目前以谷氨酸为原料的美拉德反应产物主要应用于增强食物的风味[4]。
美拉德反应是指在一定加热条件下氨基化合物与羰基化合物之间所发生的羰-氨反应[5]。1909年有研究者通过研究来自海带的谷氨酸对食品风味的影响,将鲜味确定为第5种基本味道,这种化合物是最常用的增味剂之一。对于具有鲜味活性的化合物,首先发现的成分是L-谷氨酸,L-抗坏血酸/L-谷氨酸体系可以产生强烈的烘烤香气和坚果香气,糠醛是具有浓郁的烘焙、杏仁风味的挥发性化合物,它是由谷氨酸和还原糖经美拉德反应产生的风味化合物之一[7],但是一定剂量的糠醛或5-羟甲基糠醛物质被人体吸收后,会对身体健康产生一定的负面影响[8]。PAN等[9]研究发现谷氨酸的加入可以增强谷氨酸-半乳糖Amadori重排产物中的牛奶风味和烘焙风味,谷氨酸-半乳糖Amadori重排产物有希望可以制成具有牛奶香味和烘焙香味的产物,谷氨酸与羰基化合物发生的美拉德反应具有令食品增香的巨大应用潜力。LUAN等[10]在阿拉斯加鳕鱼骨架与葡萄糖发生美拉德反应制备调味粉的研究中发现反应温度过高,会产生强烈的气味,并降低食物中氨基酸和还原糖的营养价值,温度过低则反应程度不够、产生的香气也不够浓郁,因此美拉德反应还需控制在合适的温度范围内。目前研究风味物质的技术主要有电子鼻、气相色谱闻香、GC-MS以及气相离子迁移色谱(gas chromatography-ionmobilityspectrometry,GC-IMS)等,其中最常用的是GC-MS以及GC-IMS,其特点是检测范围广、准确性高。DENG等[11]通过结合GC-MS和GC-IMS技术对粗核桃油和软精核桃油中存在的挥发性化合物评估可知,GC-IMS可快速追踪挥发性化合物的风味特征,强调独特的香气细微差别,而GC-MS则精确定位单个化合物,所以结合2种技术可为各种食物提供更详细的香气特征。
因此,本研究利用GC-MS和GC-IMS相结合,对不同温度下谷氨酸-葡萄糖美拉德反应生成产物中的挥发性风味物质进行检测,比较其挥发性香气成分差异,可以为新型调味品和食品添加剂的开发提供理论指导。
1 材料与方法
1.1 材料与试剂
L-谷氨酸(98%)、D-无水葡萄糖(98%),上海麦克林生化科技有限公司;磷酸二氢钠、磷酸氢二钠、甲醇,北京化学试剂公司;1,2-邻二氯苯标准品、正构烷烃(C7~C30),美国Sigma公司。
1.2 仪器与设备
BSA224S-CW电子天平,赛多利斯科学仪器(北京)有限公司;ZNCL-GS190×90恒温油浴锅,巩义市科瑞仪器有限公司;GCMS-TQ8040三重四极杆型气相色谱-质谱联用仪,日本岛津公司;FlavourSpec®气相色谱-离子迁移谱仪,济南海能仪器股份有限公司;50/30 μm DVB/CAR/PDMS萃取头固相微萃取装置,美国Supelco公司。
1.3 实验方法
1.3.1 美拉德反应产物制备
参考吴若彤等[12]方法适当修改。称取0.2 g谷氨酸和0.3 g葡萄糖溶解于10.0 mL 0.2 mol/L的磷酸盐缓冲溶液(pH=6)中,混合均匀,加入20.0 mL耐压瓶中,在180 ℃油浴锅中反应90 min。将制备的美拉德反应产物在-80 ℃进行预冻24 h后,再经过低温冷冻干燥,在4 ℃冰箱冷藏备用。
1.3.2 GC-MS分析
参照文献[13]方法稍作修改。称取0.5 g样品并加入20 mL顶空瓶中。将老化完成的50/30 μm DVB/CAR/PDMS萃取头扎进顶空中,对每个样品进行固相微萃取,样品在50 ℃下平衡10 min,顶空吸附20 min,每种样品进行3次平行实验。
GC条件:色谱柱DB-WAX毛细管柱(30 m×250 μm,0.25 μm);氦气作为载气,流速设置为1.0 mL/min,进样口温度250 ℃;升温程序:0~2 min,40 ℃,40~80 ℃以3 ℃/min的速率升温,保持3 min,80~120 ℃以4 ℃/min的速率升温,保持2 min,120~230 ℃以10 ℃/min的速率升温;不分流。MS条件:电子能量70 eV;四极杆温度150 ℃;离子源温度230 ℃;质量扫描范围40~450 u,全扫描模式。每种样品平行测定3次。
采用内标定量:将2 μL的1,2-二氯苯(50 μg/mL,甲醇溶液中)作为内标添加到每个样品中,挥发性化合物的浓度计算如公式(1)所示:
(1)
式中:Cv 代表挥发性化合物的质量浓度,mg/L;Ci,内标物的质量浓度,mg/L;Sv,挥发性化合物的峰面积;Si,内标物的峰面积。
定性分析:挥发性物质的定性是根据其质谱数据与NIST17数据库进行匹配得出,仅将相似度>80%的化合物进行定性,然后,测定每种化合物的线性保留指数(retention index,RI),以确认鉴定出的化合物。
定量分析:挥发物定量采用内标半定量法进行,含量表示为μg/kg。
1.3.3 GC-IMS分析
参照文献[14]方法稍作修改。称取2 mL的美拉德反应产物,置于20 mL顶空进样瓶中密封60 ℃孵化15 min,孵化速度为500 r/min;样品针温度为65 ℃;样品体积为200 μL。
GC条件:色谱柱选用MXT-5(15 m×0.53 mm,1 μm);膜厚0.25 μm;柱温设置为60 ℃;分析时间为20 min;载气为N2(纯度≥99.999%),载气流量:0~2 min,2 mL/min;2~20 min,2~100 mL/min。IMS条件:漂移管长度为5 cm;管线性电压设置为400 V/cm;漂移气体选用N2(纯度≥99.999%);流速为150 mL/min;IMS温度设置为45 ℃。每种样品平行测定3次。
1.4 气味活性值计算
通过气味活性值(odor active value,OAV)的大小来确定关键风味物质,利用各挥发性物质含量与阈值间的比值计算。若OAV≥0.1则对整体风味有修饰作用,OAV≥1则对整体风味贡献较大,挥发物的OAV越大,则对整体风味的影响就越大。OAV通过公式(2)进行计算:
(2)
式中:C,挥发性化合物含量,μg/kg;OT,该化合物阈值,μg/kg。
1.5 数据分析
使用Origin 2022绘制理化指标差异性对比图、雷达图、聚类热图。采用SPSS Statistics 23.0对单因素方差进行统计分析,结果显示P<0.05,为显著性水平。全部试验数据表示为平均值±标准偏差,每组重复3次。使用NIST 17数据库,通过比较线性保留指数和质谱来鉴定GC-MS数据中的化合物。GC-IMS分析结果采用仪器自带的LAV(Laboratory Analytical Viewer)软件的Gallery插件程序进行不同样品谱图差异比较,主成分分析(principal component analysis,PCA)绘图。
2 结果与分析
2.1 GC-MS分析
采用GC-MS对美拉德反应产物在160、170、180 ℃ 温度条件下挥发性化合物进行分析。
结果如表1所示,在3个不同温度下的美拉德反应产物中共鉴定出72种化合物,包括醇类10种、酸类8种、酯类8种、醛类7种、烷烃类7种、酮类4种、酚类4种、醚类2种、其他类22种,并利用内标法对每种化合物进行相对定量,具体结果如表3所示。
表1 不同反应温度对挥发性成分的影响
Table 1 Effect of different reaction temperatures on volatile components

化合物类别化合物名称CAS号RI相对含量/(μg/mL)计算值参考值160 ℃170 ℃180 ℃风味描述醇类 1-壬醇143-08-81 1591 1730.06±0.06a1.17±0.15c0.09±0.02b肉香1-十一醇112-42-51 3571 3870.28±0.04c1.04±0.21a0.45±0.05b肉香1-癸醇112-30-11 2581 2560.55±0.03a1.22±0.02b1.06±0.13c花甜香十二醇112-53-81 4571 4730.33±0.25b0.66±0.02c0.62±0.06a花香味1-辛烯-3-醇3391-86-41 7901 4510.11±0.04b3.11±0.12a1.30±0.06c蘑菇味赤藓糖醇149-32-61 229-0.17±0.06c2.15±1.020.88±0.01a甜味丙三醇56-81-51 115-23.75±0.32a32.70±0.95b21.30±0.06c甜味5-甲基-2-呋喃甲醇3857-25-81 732-1.45±0.05c1.55±0.01a1.73±0.04b肉香1-戊醇71-41-01 4577660.55±0.02a0.85±0.05b0.44±0.01c清香、木香山梨醇50-70-41 752-0.01±0.01b0.11±0.01a0.07±0.01c甜味噻唑类2-甲基噻唑28588-74-11 265-4.48±0.05c5.91±0.02a5.03±0.01b卷心菜味2-乙酰基噻唑7774-74-57 906-3.32±0.02a5.41±0.06b5.42±0.04c烤肉味、肉味醛类 壬醛124-19-61 1041 4000.15±0.05b0.31±0.03c0.22±0.04a柑橘香癸醛112-31-21 2041 2060.19±0.03c0.27±0.04c0.21±0.02b柑橘香、脂肪香辛醛124-13-01 0051 0000.06±0.03c0.23±0.02a0.09±0.01a清香味3-糠醛498-60-28318322.42±0.05a0.12±0.02b2.16±0.03b焦香5-甲基呋喃醛620-02-09201 6183.53±0.07b3.30±0.07c2.80±0.14c焦糖味苯乙醛122-78-11 0811 0450.19±0.04c4.39±0.04a0.32±0.03a青香香气苯甲醛100-52-71 601-16.07±0.09c16.51±0.02b15.04±0.02b油脂味、鸢尾似香呋喃类3,4-环氧四氢呋喃85-69-82 370-0.13±0.05a0.41±0.06a0.64±0.02b甜香2-戊基呋喃534-22-5642-2.55±0.04b0.76±0.03c3.83±0.03c泥土味、豆腥味、果蔬味2-甲基-3-(甲硫基)呋喃63012-97-5907-0.14±0.12b3.66±0.02a0.13±0.02a肉香、甜香2,5-二甲酰基呋喃823-82-52 586-0.22±0.03c0.35±0.03c0.53±0.02b -酚类 2,4-二叔丁基苯酚96-76-41 5551 5120.09±0.03c0.38±0.01a0.11±0.05b -1,4-苯二酚123-31-91 122-0.08±0.04a1.53±0.08a1.15±0.02b -2,4-二氨基苯酚95-86-31 094-0.22±0.03a0.67±0.02c0.65±0.01c -1,3-苯二酚108-46-31 290-0.21±0.03c0.51±0.02b0.65±0.03a甜味酚类 2-糠酸甲酯611-13-21 654-0.10±0.04b0.30±0.04b0.07±0.03c -癸酸乙酯110-38-31 3811 6310.15±0.01a0.55±0.01a0.21±0.04c梨香乙酸四氢-2-呋喃甲酯637-64-91 016-0.14±0.03b0.31±0.02b0.21±0.04c水果风味乙酸乙酯142-77-82 3838800.19±0.02c0.22±0.06a0.24±0.02b水果香味甘油脂肪酸酯542-44-92 482-0.09±0.02a0.45±0.03b0.30±0.01b -乙酸壬酯143-13-51 2821 5340.18±0.03b0.12±0.02c0.12±0.03a蘑菇、栀子花香硬脂酸乙酯111-61-52 1772 1282.60±0.04c0.31±0.03c3.16±0.02b略呈蜡香邻苯二甲酸二乙酯84-66-21 6391 8831.56±0.01c3.20±0.18a2.55±0.02a芳香味吡唑类3,5-二甲基吡唑67-51-61 010-1.58±0.05a2.32±0.07b1.56±0.03c -1,3-二甲基吡唑694-48-4804-0.90±0.04c2.13±0.02b0.36±0.06b -3-甲基吡唑1453-58-31 913-1.70±0.03b1.37±0.11a1.52±0.05c -
续表1

注:-代表该物质未检测到;不同字母代表不同反应温度下样品的相对含量存在显著差异(P<0.05)(表3同)。
化合物类别化合物名称CAS号RI相对含量/(μg/mL)计算值参考值160 ℃170 ℃180 ℃风味描述吡啶类3-羟基吡啶109-00-21 823-0.21±0.02c3.35±0.03a0.53±0.03a -4-羟基吡啶626-64-2674-1.12±0.01a0.49±0.07b1.64±0.03c -烯类 正癸烯872-05-9907-0.08±0.03b2.46±0.06b0.04±0.01c -1-十一烯821-95-41 320-0.8±0.02c1.55±0.01a1.31±0.04b -3-溴-3,3-二氟丙烯420-90-61 437-0.43±0.02a0.56±0.02b0.74±0.04c -环庚三烯544-25-22 480-0.09±0.02c0.89±0.02b1.23±0.02a -2,3,4-三甲基-2-戊烯565-77-51 447-0.16±0.09c2.09±0.11a1.11±0.12b -醚类 苄丁醚588-67-01 447-0.04±0.02a0.35±0.02c0.06±0.04b玫瑰花、老鹳草花香气二癸基硫醚693-83-42 260-0.04±0.01b0.26±0.04a0.05±0.02c -噻吩类2-噻吩甲醛98-03-32 618-1.53±0.05c0.73±0.05a2.51±0.10b类似杏仁气味5-甲基-2-噻吩甲醛13679-70-41 715-2.32±0.04a2.33±0.02b2.44±0.03c焦糊味2-正丁基噻吩1455-20-51 954-1.76±0.02b5.41±0.07c1.55±0.04a杏仁味吡嗪类2-乙酰基吡嗪109-08-01 8239152.87±0.03a3.35±0.04b1.39±0.05c坚果味、烤肉味2,5-二甲基吡嗪123-32-0--1.45±0.10b2.01±0.35a2.14±0.23c烤香、奶油味吡咯类2,5-二甲基-1H-吡咯625-84-31 7781 9780.79±0.06c1.67±0.03a1.25±0.02b -酮类 丙酮67-64-19747920.25±0.03c0.42±0.01b0.54±0.07a -2-丁酮78-93-31 1739060.05±0.05a0.09±0.04c0.09±0.02b -苯乙酮98-86-21 3721 6240.17±0.05b0.23±0.04c0.25±0.01a呈强烈金合欢似甜香3-巯基-2-丁酮40789-98-81 576-15.24±0.15a15.29±0.43c14.35±0.14b韭菜、香葱味烷烃类2,2-二氯丙烷594-20-7686-0.06±0.04c1.54±0.03b0.36±0.02a -三氧杂环己烷110-88-32 036-0.33±0.01b0.22±0.01a0.22±0.01c -氯代十八烷3386-33-21 015-0.04±0.03c0.63±0.01a0.14±0.03b -癸烷124-18-51 2311 0000.04±0.01c0.55±0.03b0.27±0.04a -顺-1,3-二甲基环己烷638-04-01 439-0.11±0.01a0.07±0.02c0.42±0.02b -二甲苯1330-20-71 032-0.25±0.04b0.53±0.02c0.42±0.01a烟熏香味邻二甲苯95-47-61 852-0.06±0.02a0.04±0.01b0.04±0.02c甜糖果味酸类 甲酸64-18-60-0.05±0.02b0.05±0.02a0.04±0.03c -辛酸124-07-2-2 0890.10±0.07a0.21±0.03c0.11±0.04b -癸酸334-48-5-2 2911.27±0.04c2.31±0.21a2.11±0.06b -月桂酸143-07-71 570-19.49±0.05c22.90±0.57b23.48±0.12a月桂油香山梨酸110-44-19901 0520.29±0.02a0.33±0.02b0.22±0.03c -花生酸506-30-92 366-0.14±0.04b0.14±0.03c0.21±0.02a -3-甲基戊酸105-43-19108841.16±0.02a0.99±0.45b0.94±0.04c -2,4-己二烯酸110-44-1990-0.14±0.01a0.11±0.01c0.15±0.02b水果香气
聚类热图可以阐明美拉德反应产物中挥发性成分的分布和相对丰度,在聚类热图中,从绿色到红色的过渡表示相对强度从低到高的变化。结合表1和图1可知,挥发性化合物的种类和含量随着反应温度变化而有所差异。

图1 不同温度美拉德反应产物风味物质聚类热图
Fig.1 Cluster heat map of flavor substances in Maillard reaction product at different temperatures
图1为通过GC-MS分析不同温度下美拉德反应产物的主要风味物质。其中醛类物质气味阈值较低,具有脂香气味。有研究[15]表明,许多Strecker醛本身及其反应产物对于食品香料有着非常重要的作用。本研究中鉴定的醛类化合物主要有壬醛、3-糠醛、5-甲基呋喃醛和苯乙醛等,结合表1可知壬醛含量最高,且在180 ℃的含量要高于160、170 ℃(P<0.05),与前人研究结果一致[16]。壬醛具有玫瑰、柑橘等香气,有强的油脂气味,多项研究证明壬醛可以伴随其他香味产生肉香风味[17]。糠醛含量是表征食品变质程度、食品贮藏时间长短的一项重要指标,糠醛也是许多风味物质及美拉德体系褐变的前体物质[18]。5-甲基呋喃醛和苯甲醛分别提供甜香、焦糖样和青香香气的气味,醛类物质在180 ℃时整体含量较高,说明随着温度的升高更有利于风味的形成。
醇类化合物的风味阈值与其他羰基化合物相比较高,通常对美拉德反应体系风味的香气贡献很小。本研究中鉴定出10种醇类物质且含量都较低,通常情况下,直链醇风味阈值较高,相对气味较弱,但随着碳链增长其气味也增强,主要呈现花香、蘑菇香、清甜香味,如 1-壬醇、1-戊醇等具有青气和木香的特征,1-辛烯-3-醇具有蘑菇和干草香气[19]。
吡嗪类化合物一般具有烤香、坚果香、爆米花香、咖啡香等风味特征,它是由Strecker醛、酮缩合而形成的挥发性风味物质,其风味阈值较低[20]。共检测到2种吡嗪类物质:2-乙酰基吡嗪、2,5-二甲基吡嗪,且含量都较低,可能是因为谷氨酸的氨基会发生质子化,无法进行亲核攻击,从而导致吡嗪类化合物的种类和含量较低[21]。
呋喃类物质是由美拉德反应和焦糖化反应生成的一种含氧杂环化合物。呋喃具有独特的感官特性,可以显著提高食品的风味[22]。ZHENG等[23]的研究中发现呋喃类物质是美拉德反应过程中非常重要的风味物质,可提供盐味、烧烤味。共鉴定出4种呋喃类物质:3,4-环氧四氢呋喃、2-甲基呋喃、2-甲基-3-(甲硫基)呋喃和2,5-二甲酰基呋喃,其中3,4-环氧四氢呋喃含量较高可赋予食品甜香风味。
2.2 挥发性风味物质PCA
PCA可用于概述挥发性成分的差异并评估样品之间的规律性和差异性,是一种无监督的多元统计分析方法[24],PCA图中图案相互靠近甚至重叠说明其样品具有相似香气特征,若分离则说明样品香气特征不同有差异[25]。不同温度下样品中挥发性化合物的PCA如图2所示,PC1(54.7%)和PC2(32.9%)的累积方差贡献为87.6%,说明此PCA分离模型是有效的。根据样品间的分布特征,可以了解到不同样品与风味物质间的关系。由图2可知,3种不同温度下样品分布较分散,说明美拉德反应产物在不用温度下产生的风味差异较大。
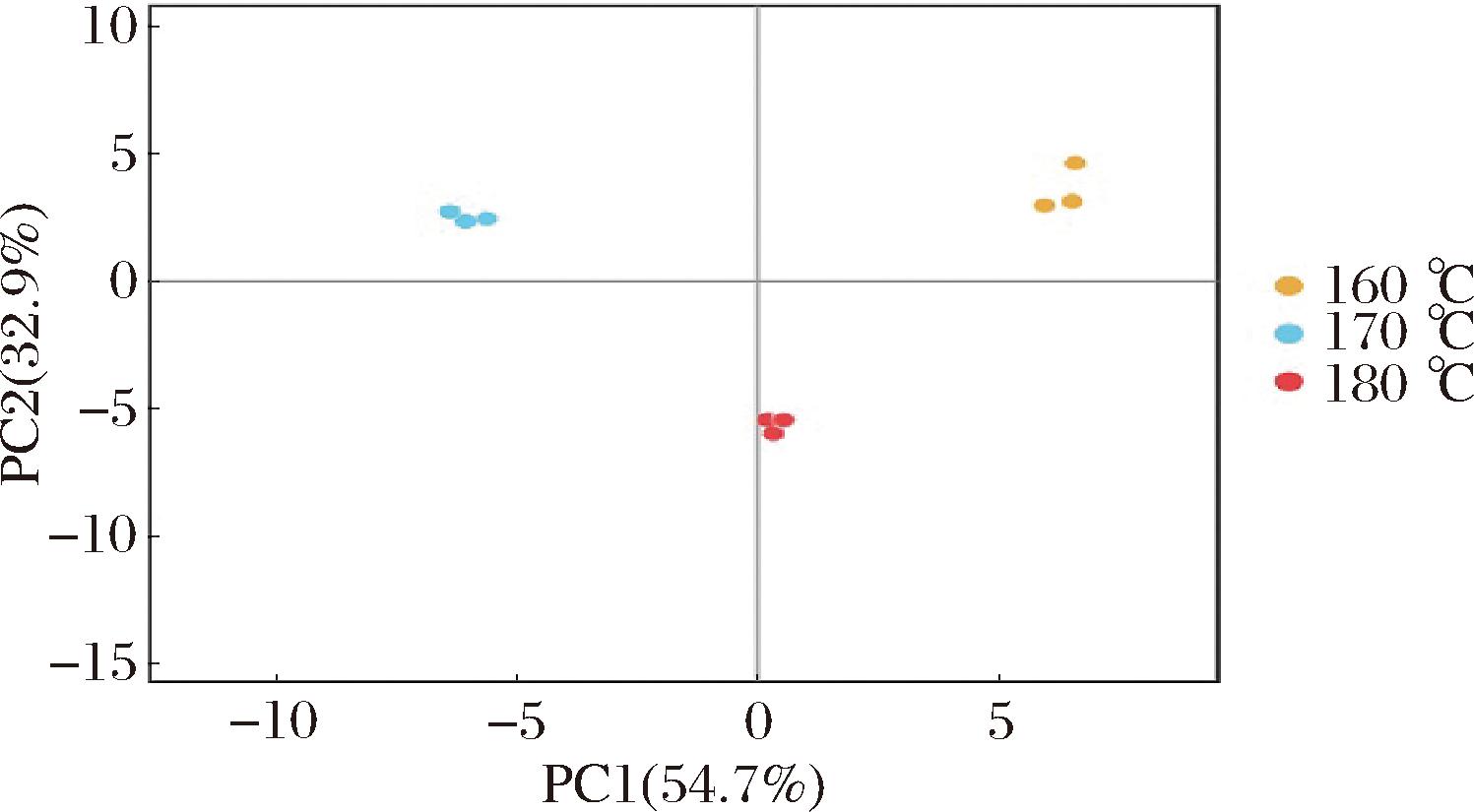
图2 不同反应温度挥发性风味物质主成分分析评分图
Fig.2 Principal component analysis scoring diagram of volatile flavor compounds at different reaction temperatures
2.3 不同反应温度美拉德产物关键风味成分的确定
挥发性化合物的含量不能准确反映挥发性化合物对香气的贡献。因此评价其贡献还需要与每个挥发性成分的香气阈值相结合。OAV是挥发性化合物质量浓度与其香气阈值的比值,用来评价单一香气化合物对整体香气的贡献程度的指标,OAV>1则表示该物质是关键风味成分,在风味中起主要作用。
通过对GC-MS鉴定出的挥发性成分进行计算,由表2可知6种关键风味物质(OAV>1)(壬醛、2-乙酰基吡嗪、苯甲醛、2-甲基呋喃、苯乙醛和5-甲基呋喃醛)在反应过程中的含量变化,这些挥发性成分被认为是美拉德反应产物风味的主要组成部分,对食物的整体香气或风味贡献最大,主要提供焦香、焙烤香、甜香气味。关键风味成分的含量随反应温度不同而发生不同程度的变化,随着温度的不断升高,部分关键风味物质的含量整体也不断增高。主要是醛类和吡嗪类化合物,醛类在美拉德反应产物风味成分中发挥主要作用以增加其甜味、咸味、鲜味[26],吡嗪类主要增加焙烤、焦香气味。
表2 反应过程中的关键风味物质
Table 2 Key flavor substances in the reaction process

注:-表示未检测到该物质。
序号化合物名称风味描述阈值/(μg/kg)OAV/(μg/kg)160 ℃170 ℃180 ℃1壬醛柑橘香、橙花香0.232.541.973.0222-乙酰基吡嗪烤肉味0.06246.3054.0322.413苯甲醛苦杏仁、樱桃及坚果香6.42.52.62.342-戊基呋喃泥土味、豆腥味、果蔬味0.604.251.276.385苯乙醛青香香气45.926.437.7265-甲基呋喃醛焦糖味0.57.066.65.67十二醇花香味0.2320.6241.255.6381-戊醇清香、木香0.153.665.662.9391-辛烯-3-醇蘑菇味1-3.111.310壬醛柑橘香0.23-1.340.9611癸醛柑橘香、脂肪香0.11.92.72.1123-糠醛焦香0.124.21.221.613苯乙酮山楂味0.0652.613.543.84143-甲基戊酸-0.285.73.543.34
2.4 GC-IMS分析结果
为了确定特征风味成分的保留时间和迁移时间,使用GC-IMS对美拉德反应产物中的挥发性物质进行了鉴定。在不同温度阶段的美拉德反应过程中,共鉴定出53种化合物。结果如表3所示,其中包括酮类10种、醇类10种、酯类10种、醛类10种、杂环类5种、烯烃类2种、硫化类2种和其他类4种物质,与GC-MS分析结果类似,区别在于挥发性化合物的种类,特别是2种检测方法对化合物的结果存在显著差异。
表3 不同反应温度产物的GC-IMS参数
Table 3 GC-IMS parameters of products with different reaction temperatures

序号化合物CAS号分子式相对分子质量RI风味描述相对含量/(μg/mL)160 ℃170 ℃180 ℃1四甲基吡嗪C1124114C8H12N2136.21 105.9坚果香、咖啡样香气81.73±43.35a85.03±12.44b112.45±54.43c2庚酸乙酯C106309C9H18O2158.21 104.8果香、青香426.06±235.32b687.83±87.24c496.47±23.46a32-甲基-2-戊烯醛C623369C6H10O98.11 155.2青草青香,水果香气833.10±23.76a905.65±98.43b990.21±146.38c42-甲基丙醇C78922C4H10O74.11 053.4葡萄酒气味143.79±87.68c258.38±13.47b1 477.03±463.34a52(E)-己烯酸C13419697C6H10O2114.11 045.1油脂香气322.24±23.34a369.15±64.76c497.87±167.47b6异戊醇C123513C5H12O88.11 232.8苹果白兰地香气1 227.71±932.32b1 381.01±254.64c1 725.65±256.86a7辛烷-2-酮C111137C8H16O128.2988.3霉香、乳蘑菇味147.28±12.03a164.78±12.31b236.07±44.75c8苯甲醛C100527C7H6O106.1945.1苦杏仁、樱桃及坚果香704.73±34..21c686.84±54.43a738.72±25.65b9庚醛C111717C7H14O114.2921.9甜杏、坚果果实香气7 331.42±693.92b8 222.09±867.78a11 493.19±325.43c104-异丙基甲苯C99876C10H14134.21 000.1芳香气味445.98±56.47c435.99±24.54b483.02±45.34a11醋酸异丙酯C108214C5H10O2102.1900.7水果香气649.71±223.02a951.34±121.99b587.49±134.89c122-丙醇C67630C3H8O60.1888.0 -67.63±10.34b53.79±9.63a106.60±54.25c13月桂烯C123353C10H16136.2988.6香脂香气690.74±129.97c687.59±12.25b694.72±25.44a142-乙酰基吡嗪C22047252C6H6N2O122.1988.3爆米花、烘烤味81.73±10.32a85.03±52.45c112.45±25.77b155-甲基糠醛C620020C6H6O2110.1955.2辛香、甜香、焦糖香味138.09±22.20b157.55±24.35c250.56±56.22a16丁酸丙酯C105668C7H14O2130.2880.8霉气味、香蕉、菠萝和杏香气605.37±95.75b589.41±354.46a529.53±65.34c17己腈C628739C6H11N97.2879.8不愉快气味654.90±383.21a688.40±32.54c716.70±97.75b182-呋喃甲醇C98000C5H6O298.1879.4苦辣气味96.14±18.12c111.15±10.55a126.30±41.87b192-糠醛C98011C5H4O296.1847.7杏仁味55.17±12.20c60.70±23.36b68.97±13.43a202-甲基-1-戊醇C105306C6H14O102.2835果香和花香味143.79±34.59a258.38±65.33b1 477.03±354.76c21硫代环戊烷C110010C4H8S88.2837.3水果果香及葡萄酸香6 951.70±350.76c7 146.25±633.67a7680.35±265.39b222-甲基-1-丁醇C137326C5H12O88.1783.8果香和花香的气味567.38±83.04b755.27±23.67c1 569.93±93.65a233(2H)-呋喃酮,二氢,2-甲基C3188009C5H8O2100.1745.2 -226.58±54.35a290.56±57.83c704.47±13.57b243-羟基-2-丁酮C513860C4H8O288.1744.1奶油、脂肪、奶香气1 197.89±129.76a1 269.88±227.87c1 503.81±213.38b254-甲基-2-戊酮C108101C6H12O100.2714.6酮样香味200.88±38.53a199.51±56.55b173.53±13.75c262-己酮C591786C6H12O100.2746.8 -432.70±135.87b427.50±34.68a412.52±43.32c27丁醛C123728C4H8O72.1580.7 -407.18±48.92b485.51±57.32c1 006.05±254.23a281-丁醇C71363C4H10O74.1640.5芳香气味35.75±1.24c46.68±6.86a95.72±6.39b29乙醇C64175C2H6O46.1417.1 -1 326.68±42.76b1 226.75±264.88a1 154.33±78.43c303-丁烯腈C109751C4H5N67.1670.5 -200.92±98.34a293.69±23.68c710.15±346.52b313-戊酮C96220C5H10O86.1697.9丙酮气味223.80±56.74b191.76±76.46c295.93±45.75a32异丁醇C78831C4H10O74.1584.6甜香220.21±24.67c220.96±35.56a275.37±23.38b332-甲基丙醛C78842C4H8O72.1580.7麦芽香48.19±6.36c64.74±14.83b248.03±34.23a34甲酸乙酯C109944C3H6O274.1499.3果香香气402.84±63.68b450.36±93.53c461.06±23.32a35醋酸C64197C2H4O260.1609.4白葡萄酒或柠檬汁气味262.06±34.67a236.04±42.32c207.13±55.28b362-己酮C591786C6H12O100.2786.6 -1 378.62±235.75b1 610.16±291.58a2 579.51±238.34c372-甲基噻吩C554143C5H6S98.2744.1 -1 525.63±34.76c1 388.79±122.27a1 404.46±65.64b38二甲基二硫C624920C2H6S294.2742.9大蒜气味292.72±37.57b414.41±54.82a281.82±76.23c39丙烯醛C107028C3H4O56.1830.7 -519.81±139.23a610.22±43.89b935.85±43.54c40Z-己-3-烯-1-醇乙酸酯C3681718C8H14O2142.21 327.4青香香气637.60±36.97a3 697.85±823.21c744.58±89.47b41壬醛C124196C9H18O142.21 105.5油脂气息195.11±32.91c259.16±23.45a809.96±34.65b42甲酸异戊酯C110452C6H12O2116.21 058.8水果香气326.20±34.45a330.81±74.15b372.84±43.34c432-庚酮C110430C7H14O114.2898香蕉及药香气味49.49±3.67b87.13±13.21c64.53±24.43a44丙酸丁酯C590012C7H14O2130.2912苹果香味1 411.85±787.3b1 290.37±412.17a1 184.40±552.22c45巴豆酸乙酯C623701C6H10O2114.1833.4焦香和水果香气 1 330.56±46.67a1 456.12±234.53c1 293.26±110.23b46醋酸甲酯C79209C3H6O274.1521.1芳香味515.63±36.20c542.25±92.54a623.45±142.99b47(E)-壬-2-烯醛C18829566C9H16O140.21 138.2油脂 气息419.71±98.32b349.77±45.24a323.99±35.86c48二丙烯基二硫C2179579C6H10S2146.31 083.7大蒜特殊气味539.09±24.54c575.25±97.27a963.09±44.66b491-丙醇C71238C3H8O60.11 001.7 -229.20±121.04a338.78±23.43c642.00±45.64b504-戊内酯C108292C5H8O2100.1977.2香兰素和椰子香气96.72±4.25c110.60±13.43b115.61±32.53a512-甲基四氢呋喃-3-酮C3188009C5H8O2100.1785坚果香、奶油香70.91±16.97b76.83±13.65a67.53±7.47c52二氢-2-甲基-3(2H)-呋喃酮C3188009C5H8O2100.1829.4坚果香、奶油香223.80±35.89c191.76±12.33a295.93±25.65b53环戊酮C120923C5H8O84.1780.8木香和霉腐香气154.18±55.87a163.22±32.54b274.54±29.32c
由表3可知,GC-IMS主要鉴定出的酮类物质有辛烷-2-酮、3(2H)-呋喃酮,二氢,2-甲基、3-羟基-2-丁酮、4-甲基-2-戊酮等,主要提供一些特殊的水果香气、强烈的奶油、脂肪、奶香气等风味,常用于烘烤食品、肉制品、糖果饮料等。这些具有特征气味的酮类物质对食品风味的形成有着重要的意义,它们不仅能够影响食品风味的风味,还能提高其营养价值和质量[27]。醇类物质主要鉴定出2-甲基丙醇、2-呋喃甲醇、2-甲基-1-丁醇等,由于醇类物质阈值相对较高,因此对风味的影响不够突出,其具有霉香、酮香,并有牛奶、乳酪、蘑菇的气味。酯类化合物风味阈值较低,酯类物质的产生可能来源于醇和酸之间发生的酯化反应,主要包括丁酸丙酯、甲酸乙酯、Z-己-3-烯-1-醇乙酸酯等,赋予一定的水果果香风味。醛类物质是主要呈味成分,对食品风味具有重要的作用,其风味阈值较低,不仅直接影响风味物质的形成,还是其他芳香化合物的前体物质。GC-IMS中鉴定出的物质主要包括苯甲醛、2-糠醛、庚醛等,其中苯甲醛呈苦杏仁、樱桃及坚果香,是苦杏仁油的主要成分,是世界上使用最多的风味化合物之一[28]。杂环类物质主要有四甲基吡嗪、2-乙酰基吡嗪、2-甲基噻吩,吡嗪类化合物阈值较低,被视为焙烤食品、肉制品中的重要风味化合物,通常被描述为坚果香和烧烤香。酸类物质中只发现醋酸,一般认为对风味的形成直接贡献较小。
通过与GC-MS检测结果对比发现2种方法对酮类和酸类物质检测结果存在显著差异,GC-MS中酮类物质检测到4种,酸类物质8种,而GC-IMS中检测到酮类物质11种,酸类物质1种,这可能是由于GC-IMS和GC-MS技术在检测物质时灵敏度不同所致[29]。
如图3所示,为了比较直观和全面地展示风味物质的差异,本研究采用GC-IMS中reporter插件绘制了二维谱图,以蓝色为背景,纵坐标为挥发性物质分离时的保留时间,横坐标为相对于反应离子峰(横坐标0.5处的红色竖线)的迁移时间。通过离子峰的位置、数量、强度和时间来反映不同反应温度的样品之间挥发性风味化合物的差异[30]。反应离子峰右侧的每一个点都代表一种气味物质,通过颜色深浅表示物质浓度高低,红色表示该气味物质浓度较高,白色则表示浓度较低。

图3 不同反应温度美拉德产物中挥发性化合物GC-IMS差异图谱
Fig.3 GC-IMS differential chromatogram of volatile compounds in Maillard products at different reaction temperatures
由图3可知,3个温度样品的风味相似,但在气味强度方面有所不同,在100~400 s的保留时间和0.5~1.5 s的漂移时间中大多数化合物产生,由于物质的极性不同,导致了保留时间有一定差异。温度反应后期时,样品的保留时间延长到800 s,根据信号和颜色的变化,香气分布存在显著差异,热处理明显改善了香气化合物的信号。结合上述描述可以直观地比较不同样品间挥发性物质的组成,3种不同样品的风味特征相似,风味物质浓度相对接近。但170 ℃时样品的风味物质数量有所增加,少数风味物质的浓度也有所增加,一些挥发性化合物在170 ℃时含量显著高于160 ℃时,如四甲基吡嗪、Z-己-3-烯-1-醇乙酸酯、甲酸异戊酯、2-庚酮,180 ℃时样品的光谱显示挥发性物质含量最高。
为直接反映不同温度下美拉德反应产物中挥发性成分含量差异,构建并分析了挥发性指纹图谱。选取所有峰,利用GalleryPlot插件绘制挥发性物质的指纹图谱,可以更直观、清晰观察到不同加热温度下所得到的美拉德反应产物中挥发性化合物的变化规律[31]。指纹图谱中同一行代表一个加热温度选择的所有峰的3个平行,同一列代表某种挥发性物质在不同样品中的信号峰;信号峰的颜色明、暗代表该物质含量的高、低,图谱中红色点状越明显则样品中含该风味物质的含量越高[32]。
由图4可知,170、180 ℃时挥发性物质的种类明显比160 ℃时挥发性风味物质的种类多,如5-甲基糠醛、2-呋喃甲醇、2-甲基-1-戊醇等物质,这可能是因为反应温度较低时,反应不充分,生成的风味前体物质较少,从而导致无法进行下一阶段的美拉德反应[33];随着反应温度的不断升高,异丁醇、环戊酮、庚醛、3-羟基-2-丁酮、辛烷-2-酮等信号峰颜色逐渐变亮,说明这些物质的含量随加热温度的升高而增加,高温有利于以上物质的进一步生成;在170 ℃时四甲基吡嗪、Z-己-3-烯-1-醇乙酸酯、甲酸异戊酯等物质信号峰亮度更进一步增亮,其呈现焦香、果香风味,说明此温度下更有利于此类风味的形成;180 ℃时异丁醇、2-甲基四氢呋喃-3-酮、2-丁醇、2-糠醛等呈味物质信号峰亮度最高,说明在此阶段美拉德反应产物的风味物质含量明显增多,较其他温度段更加浓郁丰富,但5-羟甲基糠醛等致癌化合物的含量一同增加,这些物质会对人体健康产生负面影响,因此美拉德反应温度需控制在合适的温度范围内。
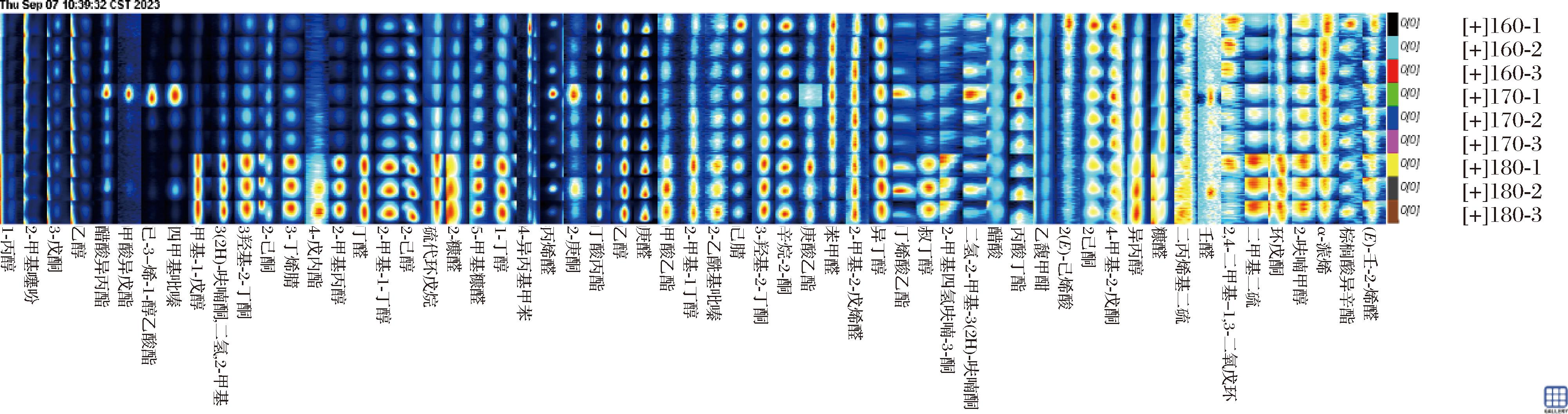
图4 不同反应温度美拉德产物挥发性化合物指纹图谱
Fig.4 Fingerprint of volatile compound of maillard products at different reaction temperature
为了更好地呈现和区分用3个温度美拉德反应产物的差异,使用GC-MS鉴定的挥发物进行了PCA。图5为全部样品的PCA结果。PCA是通过降维将多变量变为少变量的一种简化原始数据的统计分析方法[34]。样本越近,风味化合物的组成和含量越相似。根据GC-IMS结果分析,PC1(69%)和PC2(14%)的累积方差贡献率为83%,表明PCA分离模型是有效的。不同温度下美拉德反应产物可以很容易地区分为3个部分。180 ℃下样品较于其他温度差异较大,主要集中在左侧区域,160、170 ℃的样品之间差异较小,主要集中位于右侧区域。总体来说,不同温度下美拉德反应产物之间的差异较大,但组内的重复性较好,表明反应温度对美拉德反应产物风味物质影响较大,GC-IMS可以很好地表征不同样品中风味物质的差异。
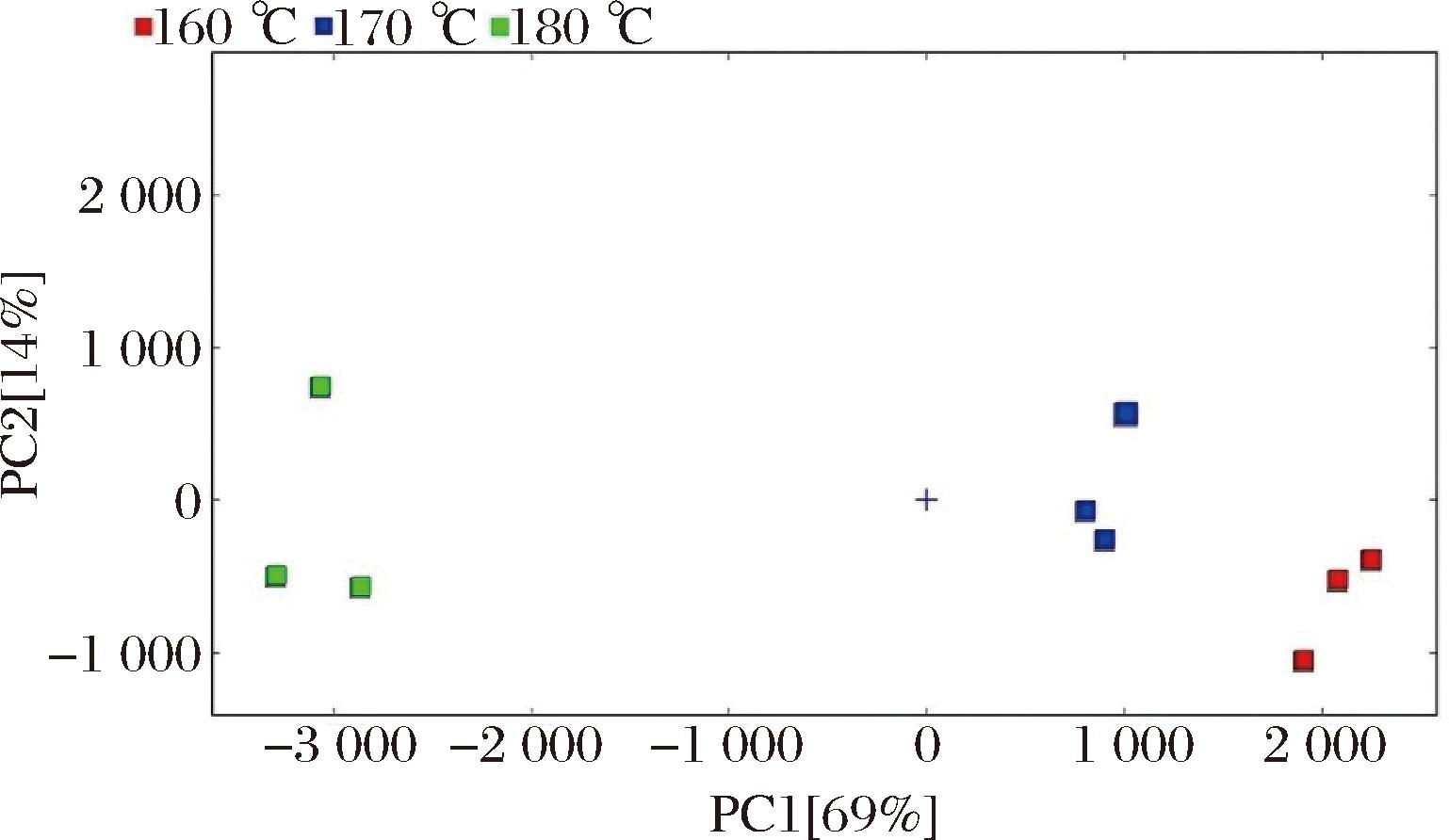
图5 挥发性化合物的主成分分析
Fig.5 PCA of volatile compounds
2.5 GC-MS和GC-IMS检测结果比较
通过Venn图比较了GC-MS和GC-IMS在检测风味物质方面的差异。由图6可知,通过GC-MS和GC-IMS在整个反应过程中,分别鉴定出72、53种风味化合物,通过2种方法共同鉴定出4种化合物,分别是壬醛、3-糠醛、2-呋喃甲醇和2-乙酰基吡嗪。
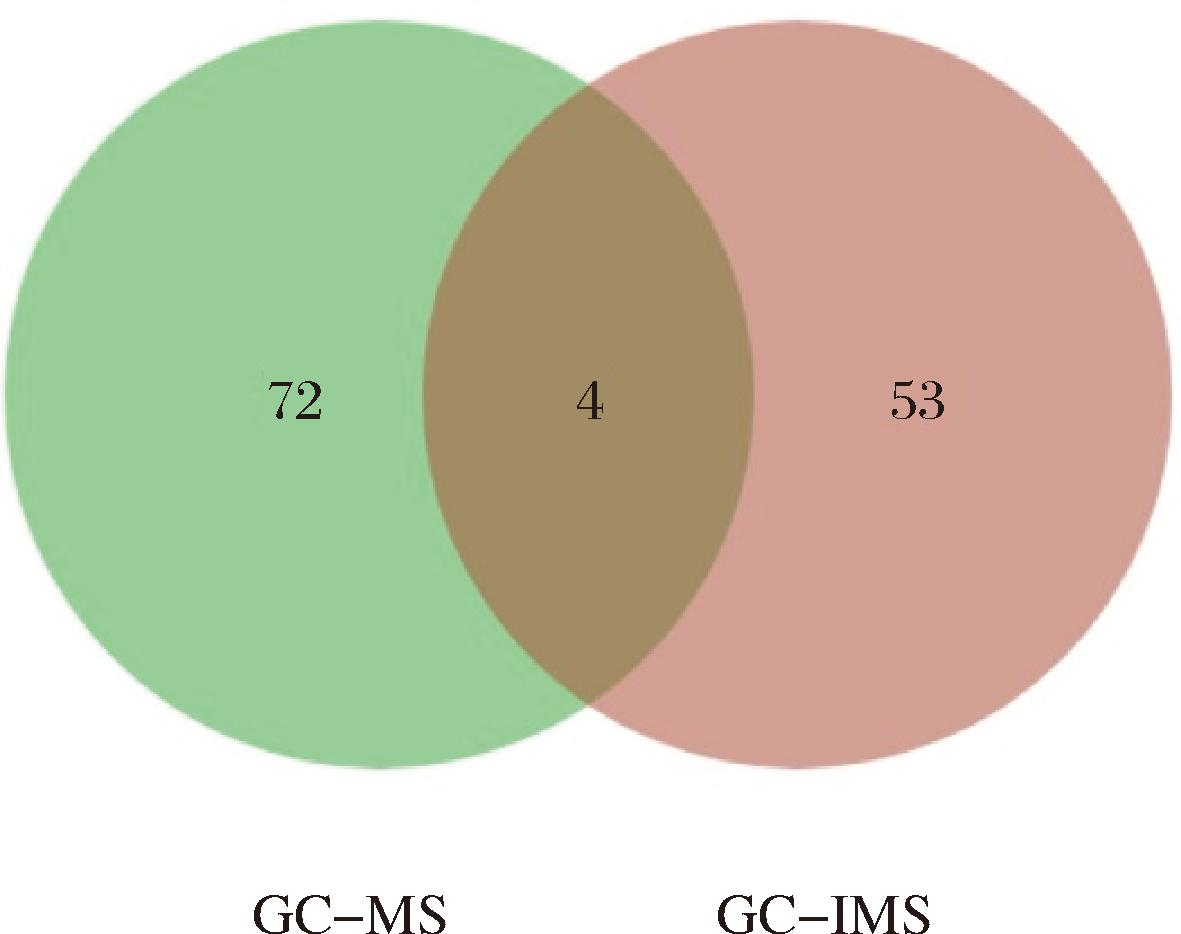
图6 两种鉴定方式下风味挥发性成分种类差异图
Fig.6 Difference diagram of volatile components of flavor under two identification methods
2种方法鉴定出的挥发性物质不同,主要是由于仪器对于挥发性物质的敏锐程度不同。GC-MS利用气相色谱分离混合物中的组分,通过质谱仪进行分析。气相色谱分离后的组分依次进入质谱仪,在离子源中被电离成离子后通过质量分析器和检测器检测并记录离子的质量数和丰度,最后通过计算机处理得到化合物的分子量和结构信息。该技术具有高分离能力和高灵敏度,适用于分析复杂的混合物。GC-IMS利用气相色谱分离后的组分依次进入质谱仪,在离子迁移谱仪中进行分析。离子迁移谱仪中含有一个离子源和一个迁移管,离子源产生的离子在迁移管中受到电场和磁场的作用,根据离子的质量和电荷不同,离子在迁移管中移动的距离也不同,从而被分离和检测,因此其具有更高的灵敏度和更快的分析速度。GC-MS适用于分析低极性、热稳定的化合物,如多环芳烃、药物等,可以分析极性化合物和热不稳定化合物。测样时需要逐步升温以对样品中的风味物质进行更全面的检测,并且可以更准确地量化,分辨率高、鉴定能力精确,在挥发性成分的定性上与GC-IMS技术互补[30]。GC-IMS更适用于分析高极性、热不稳定的化合物,如醇类、醛类、酮类、酯类、胺类等。具有无需样品前处理、高灵敏度、低检出限等优势,检测出的风味物质更接近实际嗅觉感受到的风味,因此其具有更高的灵敏度和更快的分析速度[35]。本研究中使用GC-MS鉴定到的化合物主要以醇类、醛类、酯类和酸类为主;使用GC-IMS鉴定到的化合物主要以酮类、醇类、酯类、醛类为主,对酸类物质不敏感只鉴定到一种酸类物质。因此使用GC-MS和GC-IMS技术相结合的方法可以更全面地检测美拉德反应过程中不同温度下风味物质的变化,最大程度保留了美拉德反应过程中挥发性成分的整体信息。
3 结论
本研究通过OAV、PCA结合GC-MS和GC-IMS等方法对不同温度下生成的美拉德反应产物挥发性风味物质进行综合鉴定分析。结果表明,通过GC-MS共鉴定出72种挥发性化合物,醛类、醇类和酯类化合物的种类含量最多,其中OAV>1的物质有14种,2-乙酰基吡嗪、2-戊基呋喃等物质对形成的风味具有突出贡献,提供花果、甜香以及焦香风味,GC-IMS共鉴定出53种挥发性化合物。2种方法共同鉴定出4种化合物,分别是壬醛、3-糠醛、2-呋喃甲醇和苯甲醛,主要表现出油脂、杏仁、樱桃及坚果香等。在160 ℃下样品反应不完全风味不明显,170 ℃样品中物质种类及含量最丰富浓郁,而180 ℃样品中会产生较多对人体健康有害产物。
采用GC-MS和GC-IMS方法相结合,可以最大程度保留美拉德反应产物挥发性成分的整体信息。以上结果均表明,在合适的温度范围内谷氨酸-葡萄糖美拉德反应产物可以给食物带来更好更愉悦的口感,能有效地增强食物中的鲜甜气味,使食物中的风味更丰富明显,为我国食品调味料的发展提供了一个新的参考方向。
[1] WANG K, ZHUANG H N, BING F L, et al.Evaluation of eight kinds of flavor enhancer of umami taste by an electronic tongue[J].Food Science &Nutrition, 2021, 9(4):2095-2104.
[2] STAROWICZ M, ![]() H.How Maillard reaction influences sensorial properties (color, flavor and texture) of food products?[J].Food Reviews International, 2019, 35(8):707-725.
H.How Maillard reaction influences sensorial properties (color, flavor and texture) of food products?[J].Food Reviews International, 2019, 35(8):707-725.
[3] REIS ROCHA R A, REIS ROCHA L C, RIBEIRO M N, et al.Effect of the food matrix on the capacity of flavor enhancers in intensifying salty taste[J].Journal of Food Science, 2021, 86(3):1022-1032.
[4] WIJAYASEKARA K N, WANSAPALA J.Comparison of a flavor enhancer made with locally available ingredients against commercially available Mono Sodium Glutamate[J].International Journal of Gastronomy and Food Science, 2021, 23:100286.
[5] GAO P, ZHANG W Y, ZHAO X X, et al.The effect of Maillard reaction on flavour development of protein hydrolysates from cheese[J].Food Chemistry, 2024, 437:137569.
[6] MORITA R, OHTA M, HAYABUCHI H, et al.Quantitative verification of the effect of using an umami substance (L-glutamate) to reduce salt intake[J].Hypertension Research, 2020, 43(6):579-581.
[7] AGCAM E.A kinetic approach to explain hydroxymethylfurfural and furfural formations induced by Maillard, caramelization, and ascorbic acid degradation reactions in fruit juice-based mediums[J].Food Analytical Methods, 2022, 15(5):1286-1299.
[8] SHAPLA U M, SOLAYMAN M, ALAM N, et al.5-hydroxymethylfurfural (HMF) levels in honey and other food products:Effects on bees and human health[J].Chemistry Central Journal, 2018, 12(1):35.
[9] PAN C, CUI H, HAYAT K, et al.Exogenous glutamic acid effectively involved in N-(1-deoxy-D-galulos-1-yl)-glutamic acid degradation for simultaneous improvement of both milk-like and baking flavor[J].Food Bioscience, 2022, 47:101697.[10] LUAN H W, ZHU W H, LI Y, et al.Preparation and flavor characteristics of alaska pollock frame seasoning powder by solid-phase Maillard reaction[J].Journal of Aquatic Food Product Technology, 2020, 29(1):15-27.
[11] DENG J K, ZHAO H B, QI B, et al.Volatile characterization of crude and refined walnut oils from aqueous enzymatic extraction by GC-IMS and GC-MS[J].Arabian Journal of Chemistry, 2024, 17(1):105404.
[12] ZHANG K Y, GAO L L, ZHANG C, et al.Analysis of volatile flavor compounds of corn under different treatments by GC-MS and GC-IMS[J].Frontiers in Chemistry, 2022, 10:725208.
[13] 吴若彤, 王兴伟, 夏书芹, 等.外源氨基酸对牡蛎肽美拉德反应产物风味特性的调控作用[J].食品与生物技术学报, 2023, 42(3):30-37.WU R T, WANG X W, XIA S Q, et al.Flavor characteristics of oyster peptide Maillard reaction products regulated by exogenous amino acids[J].Journal of Food Science and Biotechnology, 2023, 42(3):30-37.
[14] LI W D, LI J J, QIN Z, et al.Insights into the composition and antibacterial activity of Amomum tsao-ko essential oils from different regions based on GC-MS and GC-IMS[J].Foods, 2022, 11(10):1402.
[15] 赵景丽, 赵改名, 柳艳霞, 等.谷氨酸美拉德反应在金华火腿挥发性风味物质形成中的作用[J].中国食品学报, 2014, 14(9):110-115.ZHAO J L, ZHAO G M, LIU Y X, et al.The role of Maillard reaction about glutmate in the generation of volatile flavor compounds of Jinhua ham[J].Journal of Chinese Institute of Food Science and Technology, 2014, 14(9):110-115.
[16] DENG J Y, XU H, LI X M, et al.Correlation of characteristic flavor and microbial community in Jinhua ham during the post-ripening stage[J].LWT, 2022, 171:114067.
[17] 翟昀. 半胱氨酸Maillard中间体示踪制备转化机制与加工风味色泽受控形成[D].无锡:江南大学, 2022.ZHAI Y, Tracer-preparation transformation mechanism of cysteine Maillard intermediates and controlled formation of processed flavor and color[D].Wuxi:Jiangnan University, 2022.
[18] 魏代巍. “半胱氨酸—木糖—谷氨酸”美拉德反应体系烤肉/肉汤风味形成途径与调控[D].银川:宁夏大学, 2022.WEI D W.Pathway and regulation of flavor formation of roasted meat/broth by "cysteine-xylose-glutamic acid" melad reaction system[D].Yinchuan:Ningxia University, 2022.
[19] 孙艺飞. 美拉德反应与鸡脂对松蘑菌汤风味影响及产品开发[D].泰安:山东农业大学, 2022.SUN Y F.Effect of Maillard reaction and chicken fat on the flavor of matsutake mushroom soup and product development[D].Taian:Shandong Agricultural University, 2022.
[20] YU H, ZHANG R Y, YANG F W, et al.Control strategies of pyrazines generation from Maillard reaction[J].Trends in Food Science &Technology, 2021, 112:795-807.
[21] ZHANG Z W, JI H W, ZHANG D, et al.The role of amino acids in the formation of aroma-active compounds during shrimp hot air drying by GC-MS and GC-IMS[J].Foods, 2022, 11(20):3264.
[22] SHEN M Y, LIU Q, JIA H B, et al.Simultaneous determination of furan and 2-alkylfurans in heat-processed foods by automated static headspace gas chromatography-mass spectrometry[J].LWT-Food Science and Technology, 2016, 72:44-54.
[23] ZHENG Z L, ZHANG M, LIU W C, et al.Effect of beef tallow, phospholipid and microwave combined ultrasonic pretreatment on Maillard reaction of bovine bone enzymatic hydrolysate[J].Food Chemistry, 2022, 377:131902.
[24] GENG D C, CHEN X Y, LU D L, et al.Discrimination of different edible vegetable oils based on GC-IMS and SIMCA[J].CyTA-Journal of Food, 2023, 21(1):49-56.
[25] GAO L L, ZHANG L H, LIU J, et al.Analysis of the volatile flavor compounds of pomegranate seeds at different processing temperatures by GC-IMS[J].Molecules, 2023, 28(6):2717.
[26] YAMAMOTO T, INUI-YAMAMOTO C.The flavor-enhancing action of glutamate and its mechanism involving the notion of kokumi[J].NPJ Science of Food, 2023, 7(1):3.
[27] MAN L M, REN W, SUN M Q, et al.Characterization of donkey-meat flavor profiles by GC-IMS and multivariate analysis[J].Frontiers in Nutrition, 2023, 10:1079799.
[28] LI C, AL-DALALI S, WANG Z P, et al.Investigation of volatile flavor compounds and characterization of aroma-active compounds of water-boiled salted duck using GC-MS-O, GC-IMS, and E-nose[J].Food Chemistry, 2022, 386:132728.
[29] ZHANG L C, SHI P X, SUN J, et al.Analysis of roasted peanuts based on GC-MS combined with GC-IMS[J].Food Science &Nutrition, 2023, 12(3):1888-1901.
[30] ZHANG K Y, ZHANG C, GAO L L, et al.Analysis of volatile flavor compounds of green wheat under different treatments by GC-MS and GC-IMS[J].Journal of Food Biochemistry, 2022, 46(6):e13875.
[31] LI X J, ZENG X Q, SONG H L, et al.Characterization of the aroma profiles of cold and hot break tomato pastes by GC-O-MS, GC×GC-O-TOF-MS, and GC-IMS[J].Food Chemistry, 2023, 405(Part A):134823.
[32] YU X Y, CHEN X C, LI Y T, et al.Effect of drying methods on volatile compounds of citrus reticulata ponkan and chachi peels as characterized by GC-MS and GC-IMS[J].Foods, 2022, 11(17):2662.
[33] YIN X C, WEI Y M, LI T H, et al.Heterocyclic compounds formation in large-leaf yellow tea induced by the Maillard reaction at different roasting temperatures[J].LWT, 2023,182:114856.
[34] GUO X Y, SCHWAB W, HO C T, et al.Characterization of the aroma profiles of oolong tea made from three tea cultivars by both GC-MS and GC-IMS[J].Food Chemistry, 2022, 376:131933.
[35] NIE S, LI L H, WANG Y Q, et al.Discrimination and characterization of volatile organic compound fingerprints during sea bass (Lateolabrax japonicas) fermentation by combining GC-IMS and GC-MS[J].Food Bioscience, 2022, 50:102048.