随着社会工业的发展,塑料因防水、耐用、质轻、易塑性等优点在食品包装领域被广泛应用[1]。然而,目前滥用塑料包装情况普遍,尤其大量的食品包装膜拆封(如聚丙烯、聚乙烯膜)丢弃后,难以被环境降解,造成严重的白色污染;同时,化石燃料全球储量告急,塑料包装也不利于可持续发展[2-3]。因此开发绿色环保,低成本的可降解食品包装材料日益重要。其中淀粉来源广泛,价格低廉,可再生且可被生物完全降解是最具潜力的食品包装材料[4]。板栗作为河北的特色农产品,其质量产量均为全国第一,是典型的淀粉类食物。板栗淀粉(chestnut starch, CS)纯度较高,具有较低的糊化温度、较高的糊化黏度和稳定性,具有很大开发潜力。然而在板栗生产、销售过程中,许多破损、虫蛀、尺寸不合格等缺陷的板栗果实被废弃,间接造成资源浪费。因此选择废弃板栗作为淀粉的原材料,可提高板栗生产的经济效益[5-6]。
由于淀粉是多羟基聚合物,分子内和分子间可形成大量的氢键,导致淀粉基材料的耐水性、力学性能都较差,玻璃化转变温度较高,无法进行熔融挤出等热塑性加工,通常需要对其进行热塑改性[7]。刘鹏飞等[8]采用甘油作为塑化剂制备热塑性甘薯淀粉膜,热塑性得到了改善。KOH等[9]将甘油、山梨醇、果糖及其组合作为塑化剂,制备热塑性西米淀粉,研究发现淀粉热塑改性后淀粉薄膜的机械性能增强,但其在水中的溶解度仍然较高。多元醇类塑化剂制备的热塑性淀粉具有一定的韧性可改善力学性能,但亲水性较强,易回生,不耐贮存。甲酰胺等酰胺类塑化剂可与淀粉形成较稳定的氢键,有效防止淀粉回生,但热塑性淀粉材料韧性较差[10]。因此本文选用废弃板栗果实作为原料,制备板栗淀粉,通过引入二羟甲基脲[1,3-bis(hydroxymethyl)urea,DMU]对板栗淀粉进行热塑改性,得到热塑性淀粉,并将两者按照一定比例混合,进一步制备出具有良好成膜性、疏水性及一定可降解性的改性板栗淀粉薄膜,以期将其应用于绿色食品包装材料。该研究不仅为可降解食品包装材料提供新的思路,也进一步实现板栗生物质资源的再利用,提高其经济价值。
1 材料与方法
1.1 材料与试剂
板栗于中国河北省迁西所购(板栗淀粉的基本信息见表1);无水乙醇,天津市永大化学试剂有限公司;石油醚,天津市津东天正精细化学试剂厂;柠檬酸,天津市大茂化学试剂厂;DMU,上海阿拉丁生化科技股份有限公司;其他化学品为分析试剂级,由本地供应商提供。
表1 板栗淀粉的成分 单位:%
Table 1 Composition of chestnut starch

成分淀粉含量(以千重计)直链淀粉含量(以千重计)支链淀粉含量(以千重计)游离水板栗淀粉92.8529.4370.577.15
1.2 仪器与设备
ZNCL-GS智能磁力搅拌器,巩义市予华仪器有限责任公司;N&DN系列超声波细胞粉碎机,宁波新芝生物科技股份有限公司;PH-3C型pH计,上海仪电科学仪器股份有限公司;SmartLab9KW型X射线粉末衍射仪,日本理学Rigaku;Spectrum 3型傅里叶变换红外光谱仪,美国PerkinElmer;Setline DSC型差示扫描量热仪、Setline STA型同步热分析仪,法国塞特拉姆;UV-5100B紫外可见分光光度计,上海元析仪器有限公司;CMT-4502全能试验机,珠海市三思泰捷电器设备有限公司。
1.3 实验方法
1.3.1 CS与酯化板栗淀粉(esterified chestnut starch, ERCS)的制备
CS的制备按照HU等[11]的方法制备。
将CS与蒸馏水均匀混合成一定的溶液,置于超声波细胞粉碎仪,处理时间为30 min,处理后的超声板栗淀粉(ultrasonic chestnut starch,UCS)样品冷冻干燥备用。将占若干比重的柠檬酸分别溶解在10 mL 的蒸馏水中,并用10 mol/L NaOH溶液将柠檬酸溶液的pH值调节至3.0[12]。然后将5 g UCS分散在柠檬酸溶液中,搅拌均匀,在室温下平衡一定时间,再置于45 ℃烘箱中干燥至恒重。将混合物研磨后在一定温度烘箱中反应一定的时间。分别用蒸馏水、无水乙醇洗涤2次。洗涤后离心,冷冻干燥得到ERCS。
1.3.2 热塑性淀粉薄膜的制备
将1 g CS与蒸馏水混合配制成质量分数为10%的溶液,在80 ℃下热搅拌90 min,得到糊化淀粉,将糊化淀粉倒入内衬聚四氟乙烯的平底培养皿中在40 ℃下干燥1 h得到淀粉薄膜(chestnut starch film, CSF)[13];
将制得的CS和ERCS按照质量比5∶2配制成质量分数为10%的溶液,于80 ℃下热搅拌90 min,得到糊化淀粉,将糊化淀粉倒入内衬聚四氟乙烯的平底培养皿中在40 ℃下干燥1 h得到酯化淀粉薄膜(esterified chestnut starch film, ERCSF);
将制得的CS和ERCS按照质量比5∶2配制成5组质量分数为10%的溶液,分别加入占淀粉总质量的15%、20%、25%、30%、35%的DMU,于80 ℃下热搅拌90 min,得到糊化淀粉,冷冻干燥可得热塑性淀粉;将糊化淀粉倒入内衬聚四氟乙烯的平底培养皿中在40 ℃下干燥1 h得到热塑性淀粉薄膜。实验组别如表2所示。
表2 实验组别
Table 2 Experimental groups
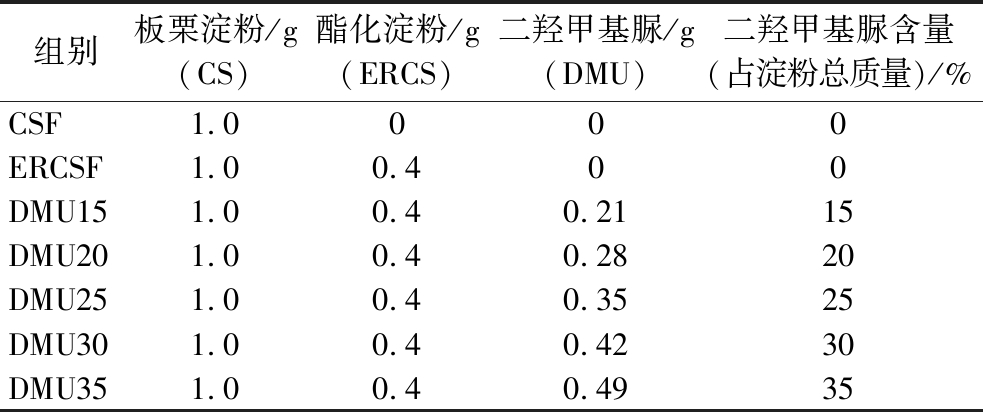
组别板栗淀粉/g(CS)酯化淀粉/g(ERCS)二羟甲基脲/g(DMU)二羟甲基脲含量(占淀粉总质量)/%CSF1.0000ERCSF1.00.400DMU151.00.40.2115DMU201.00.40.2820DMU251.00.40.3525DMU301.00.40.4230DMU351.00.40.4935
1.3.3 红外光谱测试
采用傅里叶变换红外光谱对CS、ERCS、热塑性淀粉进行红外测试。测试分辨率设定:4 cm-1,扫描32,测定波数范围4 000~400 cm-1,采用Origin软件进行谱图拟合。
1.3.4 X-射线衍射测试
采用X-射线衍射仪对CS、ERCS、热塑性淀粉样品进行结晶结构表征,采用Cu靶,ka辐射,管压/管流40 kV/30 mA,速度为8°/min,扫描频率为0.02°,扫描范围为5°~40°。使用MDI jade 6.0软件计算淀粉样品的相对结晶度(relative crystallinity,RC)。
1.3.5 差示扫描量热仪测试
用差示扫描量热分析仪测定CSF、ERCSF、热塑性淀粉薄膜的玻璃化转变温度。将薄膜剪裁成2 cm×2 cm的样品,放在仪器的样品架上,通入氮气,进行升温测试,升温速率5 ℃/min,温度34~200 ℃,通入氮气速率30 mL/min。
1.3.6 热重测试
利用热分析仪测定复合膜热重,测试温度范围0~550 ℃,升温速率为5 ℃/min。
1.3.7 扫描电镜测试
对CSF、ERCSF、热塑性淀粉薄膜采用扫描电子显微镜检测。在喷金和真空后,用日立S-4800电子显微镜对样品进行扫描和拍照。
1.3.8 薄膜透光率的测定
使用UV-5100B紫外可见分光光度计测定复合膜透光率。将测试薄膜样品裁剪为 4 cm×1 cm的长条,测试波长为400、600、800 nm。每个样品重复测试3次,取平均值[14]。
1.3.9 薄膜耐水性的测定
将制备出的复合膜裁剪成长条状(4 cm×1 cm)保存于实验室环境(20~25 ℃,相对湿度为35%~45%,避光保存),称量并记录(m1)。再将薄膜在100 mL去离子水室温浸泡24 h后取出,使用滤纸吸去复合膜表面多余水分,称重(m2)。最后薄膜在105 ℃ 下再次干燥1 h,然后称重(m3)。薄膜的吸水率(water absorption,WA)和水溶率(water solubility,WS)计算如公式(1)和公式(2)所示[15]:
(1)
(2)
式中:m1,初始质量,g;m2,吸水之后的质量,g;m3,干燥之后的质量,g。
1.3.10 薄膜力学性能的测定
复合膜的力学性能使用全能试验机测定膜的抗拉强度(tensile strength,TS)和断裂伸长率(elongation at break,EAB)。将复合膜裁剪成长条状(4 cm×1 cm),并在测试前放置在23 ℃和相对湿度为53%环境中放置72 h。设置初始夹距为50 mm,测试速度为100 mm/min。样品的厚度通过螺旋测微器测量。每个膜样品重复测试3次,取平均值[16]。
1.3.11 薄膜可降解性能的测定
将复合膜裁剪成长条状(4 cm×1 cm)并在烘箱中干燥至恒重,称重并标记为W0。再放入土壤中进行降解,待测样条分别于10、20、30 d取出用无水乙醇和蒸馏水进行洗涤,放入干燥箱中干燥至恒重记为W1,降解率计算如公式(3)所示[17]:
降解率![]()
(3)
式中:W0,初始质量,g;W1,降解之后的质量,g。
2 结果与分析
2.1 红外光谱分析
由图1可以看出,在3 100~3 500 cm-1间有一强吸收峰形较宽,是O—H峰经氢键缔合而成[18]。加入DMU之后在1 665 cm-1处出现酰胺基团中的C![]() O键吸收峰,在1 557 cm-1处出现了N—H键的吸收峰,在1 417 cm-1处出现了C—N键的吸收峰。在低波数范围内,波数越低,DMU与淀粉之间的氢键相互作用越强[19]。由图1可以看出,CS和ERCS在1 025.4 cm-1处出现C—O—C基的C—O伸缩振动峰,当DMU的添加量为15%、20%、25%、30%、35%则C—O伸缩振动峰分别为1 024.5、1 024.2、1 021.6、1 022.8、1 023 cm-1、也就是说随着DMU的加入,DMU与淀粉之间的氢键作用增大,破坏了淀粉分子内和分子间的氢键作用,在添加量为25%时DMU与淀粉的氢键作用达到了最大值,当DMU含量为30%、35%时,峰值有所回升,这是由于DMU过量会导致淀粉团聚,从而削弱了DMU对淀粉的氢键作用。
O键吸收峰,在1 557 cm-1处出现了N—H键的吸收峰,在1 417 cm-1处出现了C—N键的吸收峰。在低波数范围内,波数越低,DMU与淀粉之间的氢键相互作用越强[19]。由图1可以看出,CS和ERCS在1 025.4 cm-1处出现C—O—C基的C—O伸缩振动峰,当DMU的添加量为15%、20%、25%、30%、35%则C—O伸缩振动峰分别为1 024.5、1 024.2、1 021.6、1 022.8、1 023 cm-1、也就是说随着DMU的加入,DMU与淀粉之间的氢键作用增大,破坏了淀粉分子内和分子间的氢键作用,在添加量为25%时DMU与淀粉的氢键作用达到了最大值,当DMU含量为30%、35%时,峰值有所回升,这是由于DMU过量会导致淀粉团聚,从而削弱了DMU对淀粉的氢键作用。
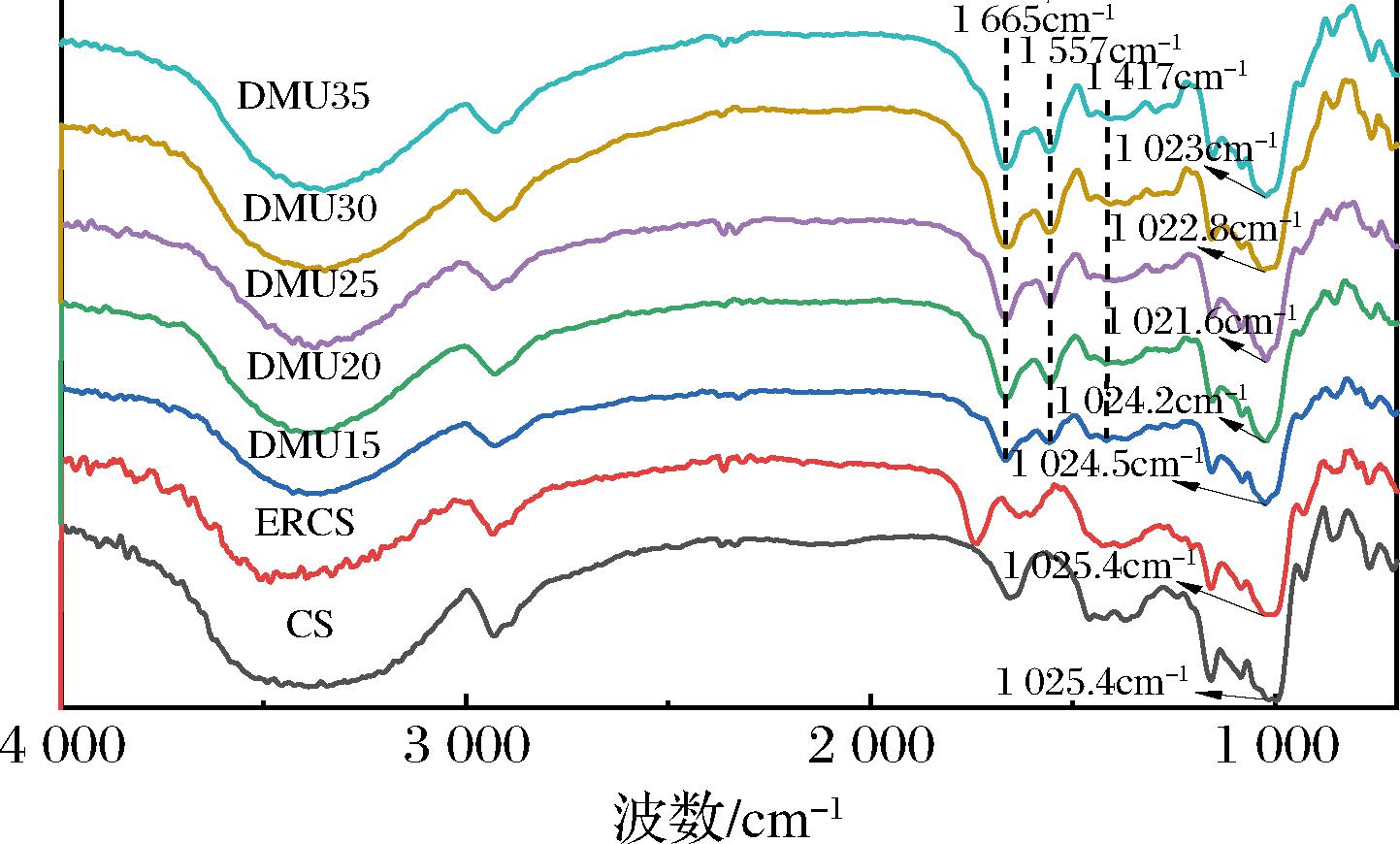
图1 CS、ERCS和热塑性淀粉红外光谱图
Fig.1 The FTIR spectra of CS, ERCS, and thermoplastic starch
2.2 X-射线衍射分析
如图2所示,CS在15.1°、17.2°和23.2°时均有衍射峰可判断晶型为C型[20]。ERCS因为酯基的取代衍射峰减弱,塑化过程中淀粉的衍射峰也在20°左右发生了明显的变化,为淀粉的V型结晶;说明小分子DMU进入淀粉的结晶区取代淀粉分子原有的氢键,与之形成新的氢键,使天然淀粉由原有的C型结晶转变为V型结晶。在加入DMU之后相对结晶度先降低后增加,在DMU含量为25%时结晶度最低;这是由于DMU渗透到淀粉分子内,削弱了淀粉分子间和分子内的作用,破坏了淀粉的双螺旋结构,从而破坏了淀粉结晶区,导致结晶度降低;当DMU过多时,会导致淀粉团聚,从而促使淀粉分子的重结晶,结晶度升高。
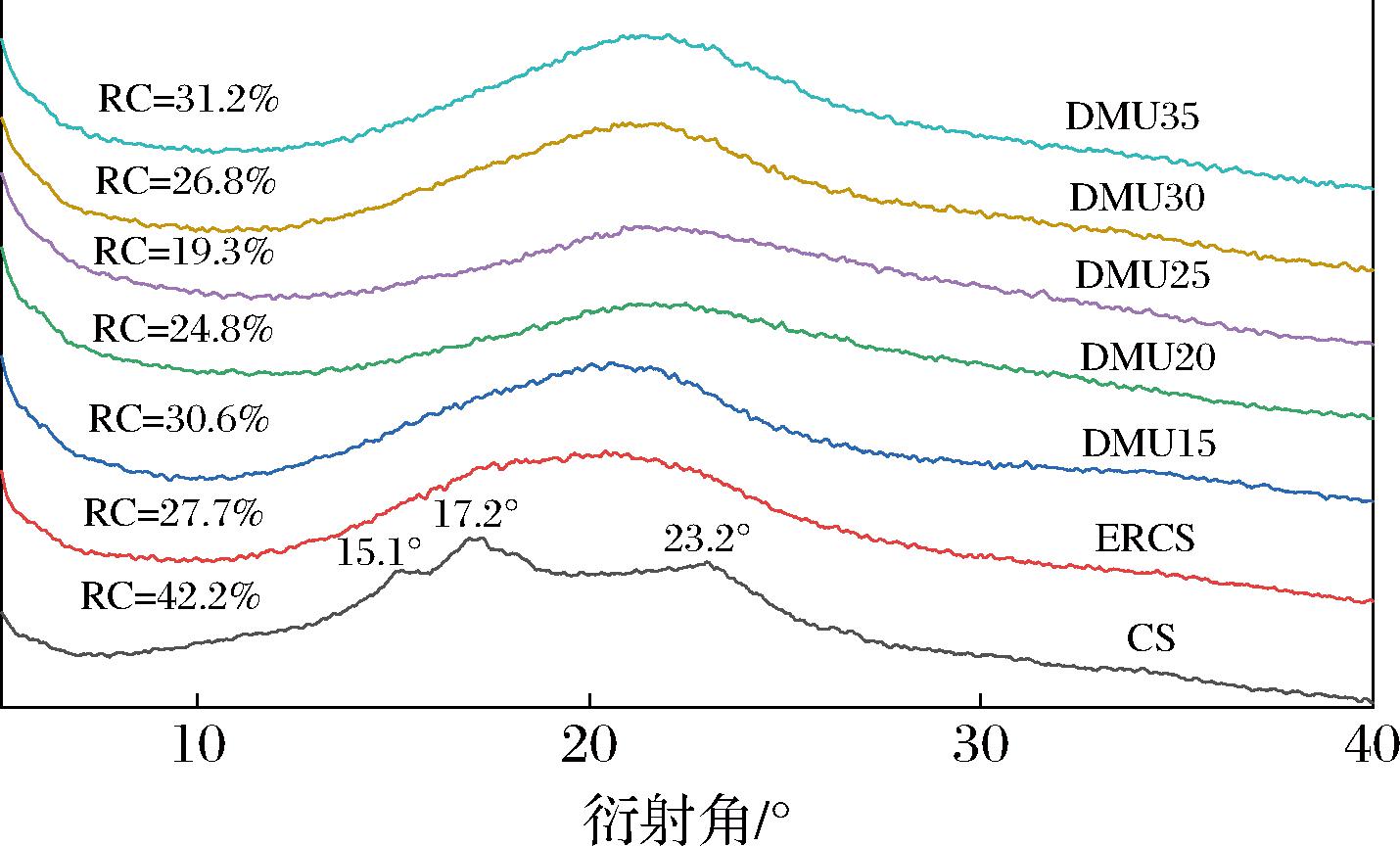
图2 CS、ERCS和热塑性淀粉X-射线衍射图
Fig.2 The XRD analysis of CS, ERCS, and thermoplastic starch
2.3 差示扫描量热分析
玻璃化转变主要是由非晶聚合物(线性的,例如直链淀粉)引起的,其中分子在热能作用下相互滑动,导致聚合物变得更柔韧,黏性和橡胶性,这样的性能更利于热塑加工[21]。如图3所示,随着DMU加入,DMU与淀粉之间氢键的生成削弱了淀粉分子间和分子内作用,淀粉薄膜的玻璃化转变温度逐渐降低,在DMU含量为25%时玻璃化转变温度达到最低值;当淀粉分子中含有过量的DMU,会导致淀粉团聚,从而导致淀粉分子链的重组,玻璃化转变温度就会升高。也进一步验证了红外光谱的氢键作用。
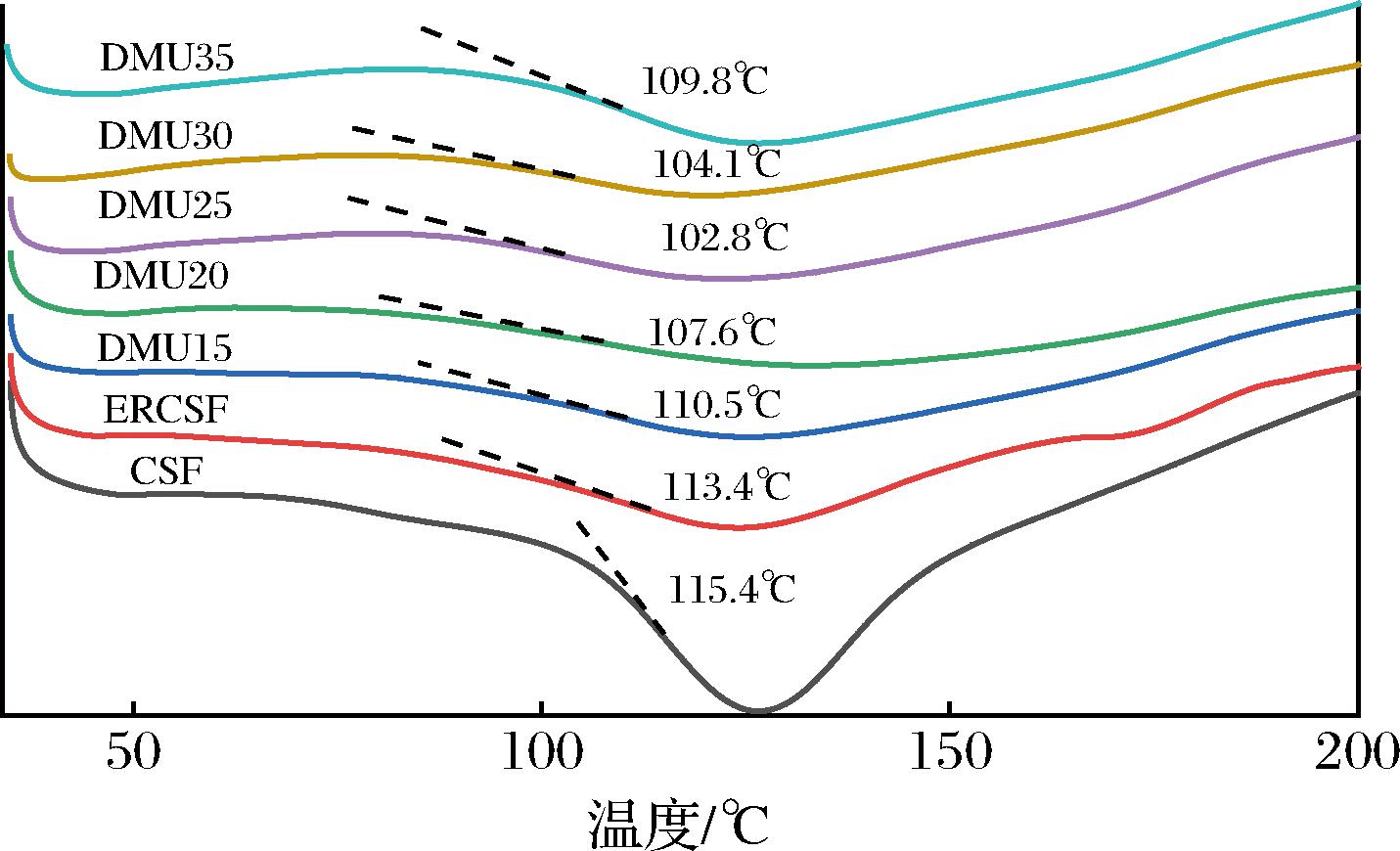
图3 CSF、ERCSF和热塑性淀粉薄膜的玻璃化转变温度
Fig.3 The DSC analysis of CSF, ERCSF, and thermoplastic starch films
2.4 热重分析
如热重(thermal gravity, TG)图4-a显示,样品存在三步降解过程。第一步在37~113 ℃,这一步主要是样品中自由水的挥发,重量减轻;第二步降解在113~232 ℃,这一阶段主要与样品中的可挥发物,结合水以及部分DMU的分解有关;第三失重阶段主要是淀粉聚合物中的直链淀粉和支链淀粉糖苷键的分解[22]。如微分热重(differential thermal gravity,DTG)图4-b所示,CSF的热分解温度为296.26 ℃,ERCSF的分解温度略低于CSF,这是由于部分酯基取代了羟基,减小淀粉分子内的氢键键能,而随着DMU含量的增加,热分解温度逐渐减小,在DMU含量为25%时最低,由此可以推断出DMU25中淀粉分子间和分子内的氢键作用最小。
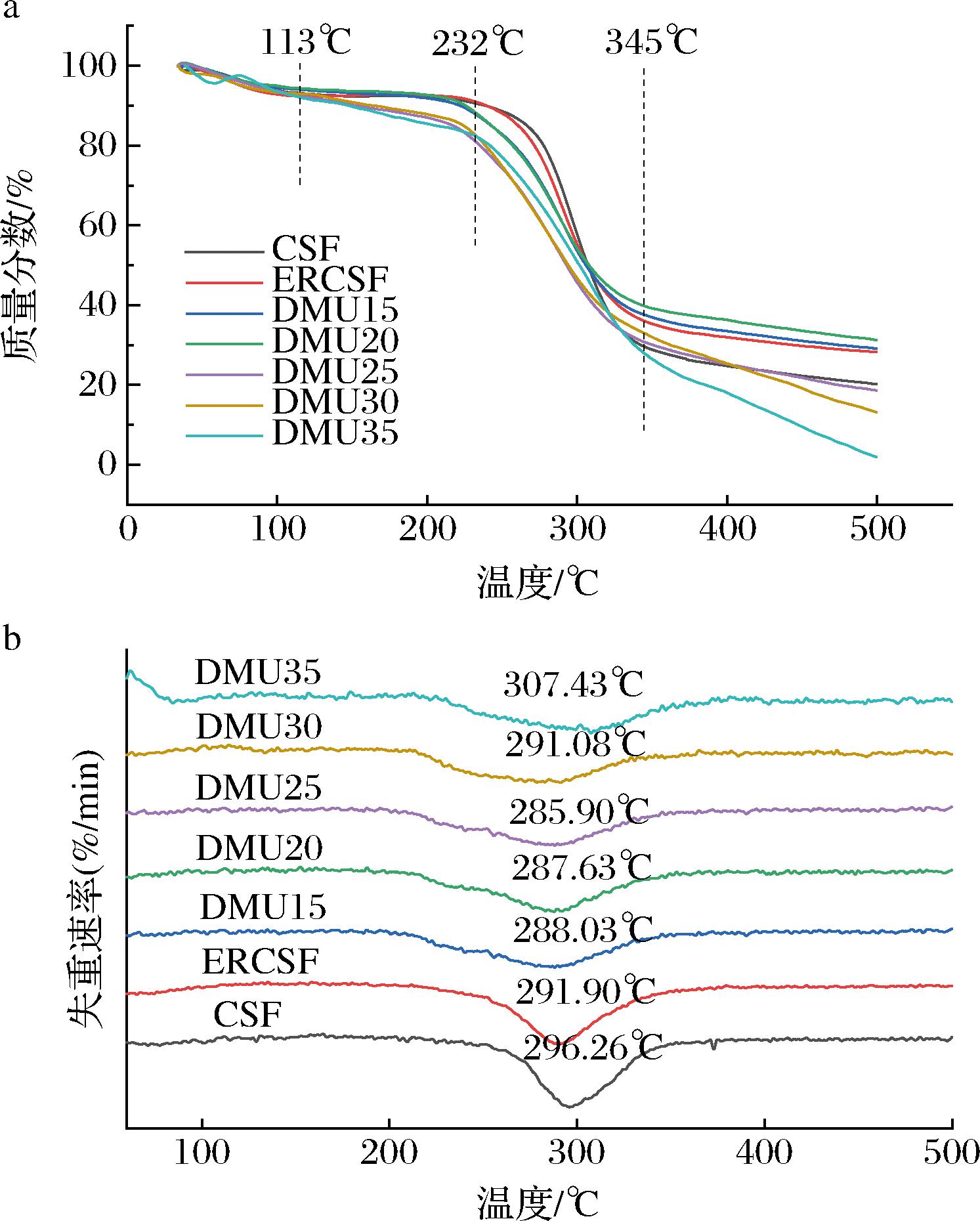
a-TG图;b-DTG图
图4 CSF、ERCSF和热塑性淀粉薄膜的热重图
Fig.4 The TG and DTG analysis of CSF, ERCSF, and thermoplastic starch films
2.5 扫描电镜图分析
如图5所示,CSF电镜图中小颗粒淀粉部分聚集形成大颗粒且形成的薄膜不连续,分布不均匀;添加ERCS制备出的ERCSF颗粒更加明显,因为ERCS的溶胀度低,糊化效果不好,导致颗粒增多;随着DMU的添加,淀粉膜表面变得平整光滑,颗粒减少,分布均匀,当DMU含量为25%时热塑性淀粉薄膜既连续又均匀,塑化效果最好,而添加过量DMU时,薄膜表面会有DMU颗粒。

a-CSF;b-ERCSF;c-DMU15;d-DMU20;e-DMU25;f-DMU30;g-DMU35
图5 CSF、ERCSF和热塑性淀粉薄膜的扫描电镜图
Fig.5 The SEM analysis of CSF, ERCSF, and thermoplastic starch films
2.6 薄膜透光率分析
如图6-a所示,随着波长的增加,薄膜的透光率整体是增加的;薄膜的透光率与薄膜材料的结晶度,淀粉的糊化程度以及膜结构有关[8]。CSF的结晶度最高且淀粉糊化程度最好,从而导致透光率最低;疏水性的酯化淀粉的加入,总体淀粉的溶胀度变低,糊化程度减弱,透光率有所提升;随着DMU的加入及反应,削弱了淀粉分子内的氢键,结晶度降低,形成的薄膜又连续又均匀,颗粒数量减小从而导致透光率增加,在DMU含量为25%的时透光率最大,塑化效果最好;而过量的DMU会提高结晶度,导致透光率减小。如图6-b所示,透光率越大,成膜物质的相容性越好。
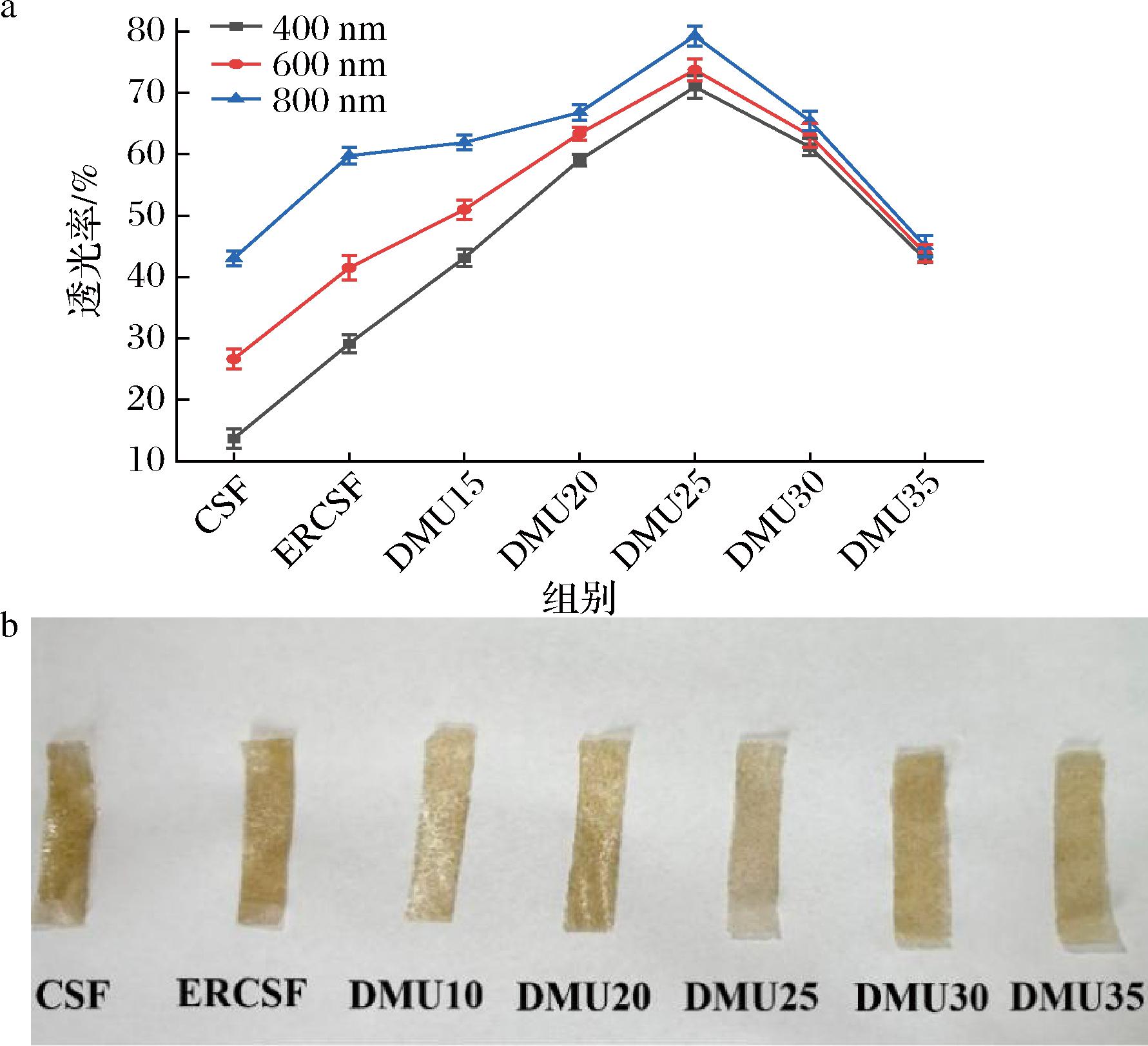
a-透光率折线图;b-透光率实物图
图6 CSF、ERCSF和热塑性淀粉薄膜的透光率
Fig.6 The transmittance of CSF, ERCSF, and thermoplastic starch films
2.7 薄膜耐水性分析
水溶率是材料在水中溶解的质量百分比,水溶率与材料的亲水性有关。如图7所示,添加ERCS后,薄膜材料的疏水性增强,所以ERCSF的水溶率降低,而随着亲水性DMU的添加,薄膜的水溶率逐渐增大。薄膜的吸水率是指材料吸收水分占总质量的百分比,薄膜的吸水率不仅与薄膜材料的亲水性有关,还与薄膜的结构形态有很大的关系[23]。薄膜的结构越连续越紧密,水分越不易吸附在薄膜上。ERCSF是由于材料疏水性增强所以吸水率相较CSF减小;如电镜图5-c~图5-e所示,随着DMU的添加,增加了基质的相容性,增强了基质的内聚力,使得薄膜变得更加致密,制备出的薄膜又连续又均匀,抑制了薄膜的持水性,DMU25薄膜连续性最好,所以吸水率最低;而当DMU添加量继续增加时,薄膜表面会分布亲水性的DMU,在薄膜结构形态相同的条件下,表面亲水性物质越多,吸水率就越大,因此导致DMU30、DMU35薄膜的吸水率增加。
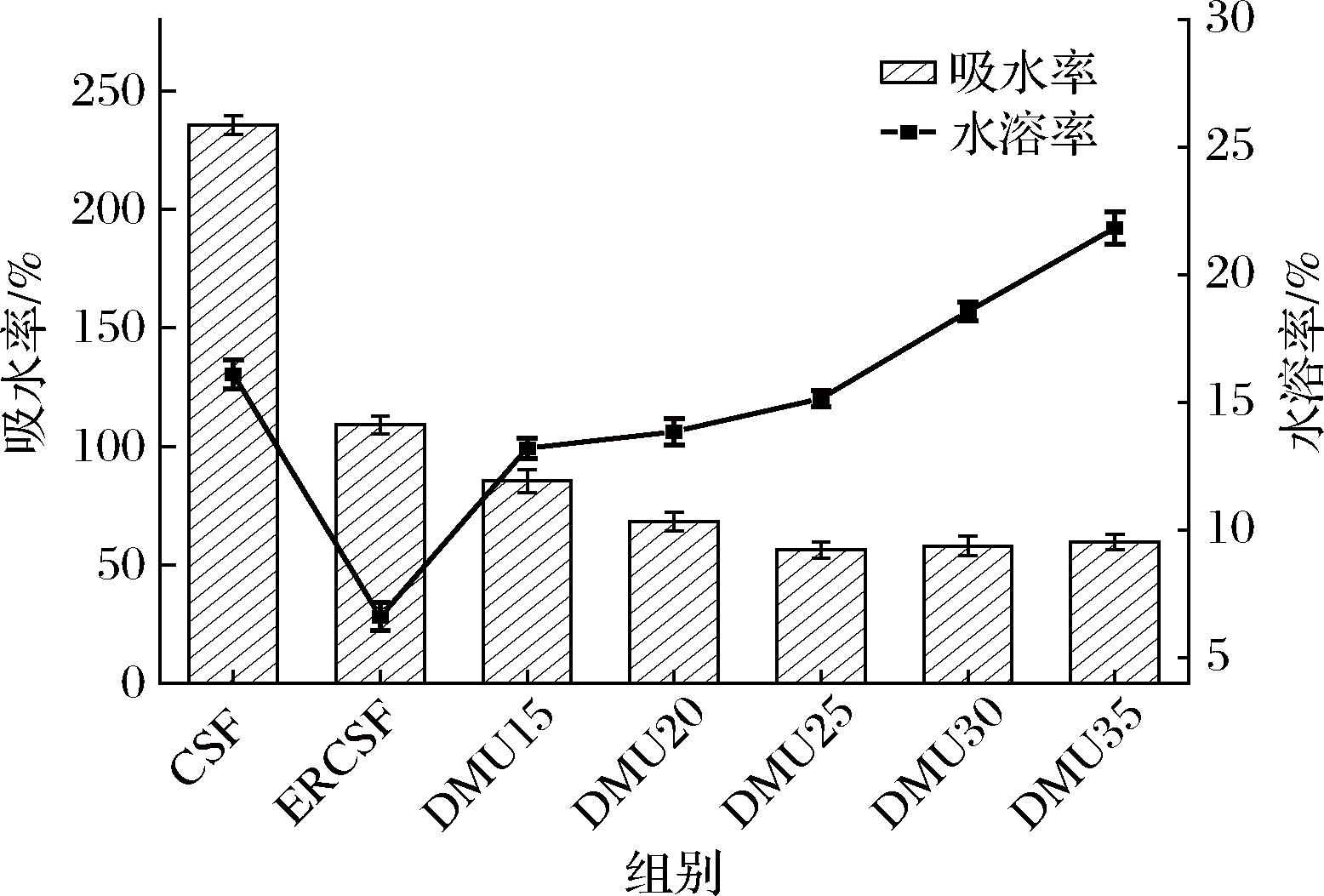
图7 CSF、ERCSF和热塑性淀粉薄膜的耐水性
Fig.7 The waterproof of CSF, ERCSF, and thermoplastic starch films
2.8 薄膜力学性能分析
图8结果表明,相比较CSF,ERCSF的拉伸强度增加,断裂伸长率降低,因为ERCS的添加减少了水分子的进入,减弱了淀粉分子链的相对运动。随着DMU用量的增加薄膜的拉伸强度逐渐降低,断裂伸长率逐渐升高;这是由于DMU分子与淀粉分子之间相互作用的面积增加,从而加大了DMU对淀粉分子间作用的削弱程度,降低了淀粉分子间强的氢键相互作用力;而DMU的亲水性,在糊化过程中也促进水分子的进入,进一步增加了淀粉分子链的相对运动使膜的拉伸强度降低。同时DMU的加入提高了淀粉链段的移动性,增大了薄膜的断裂伸长率。
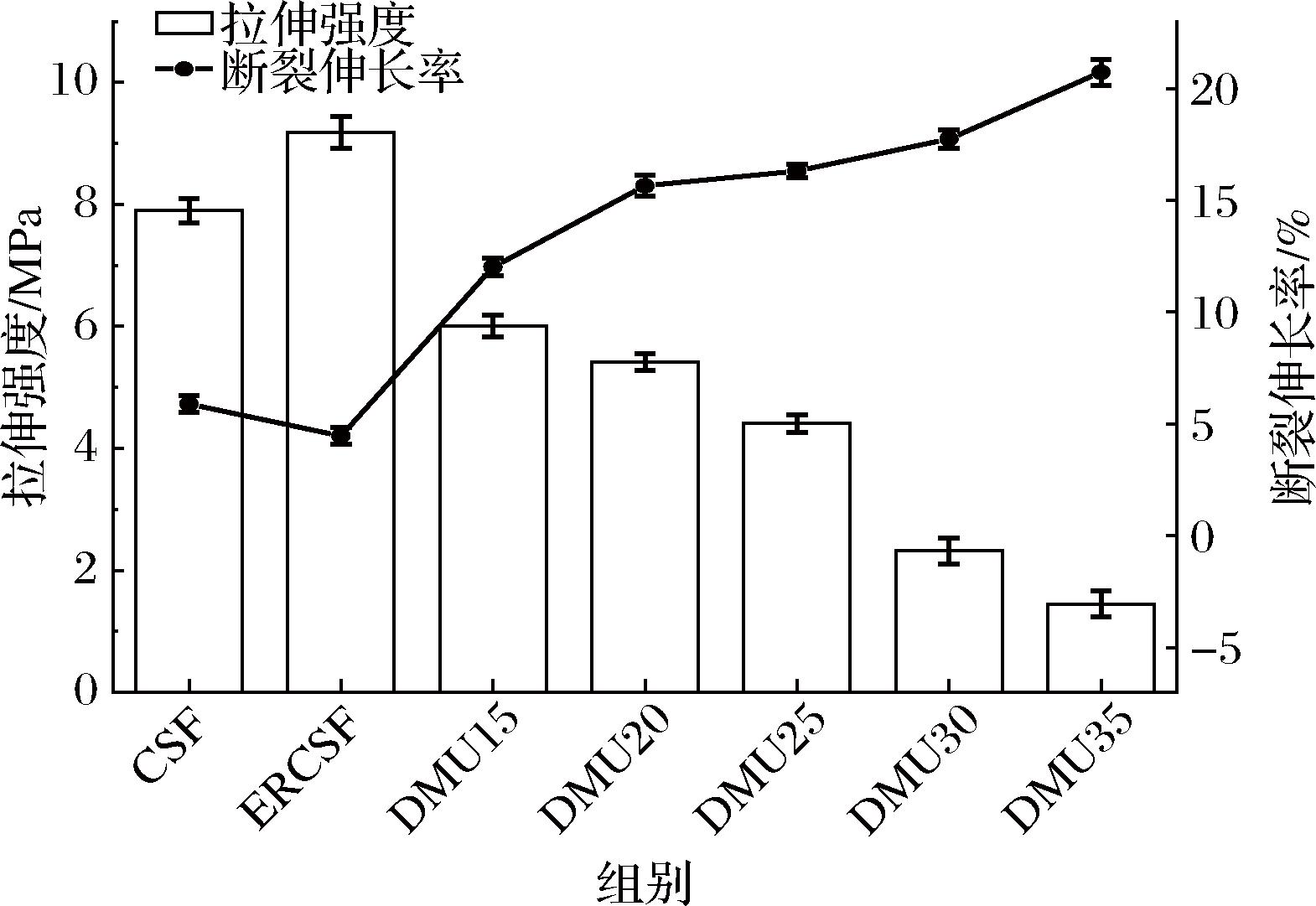
图8 CSF、ERCSF和热塑性淀粉薄膜的力学性能
Fig.8 The mechanical property of CSF, ERCSF, and thermoplastic starch films
2.9 薄膜可降解性能分析
由图9可以看出,对比CSF,ERCSF的降解率下降,这是由于ERCS的加入,薄膜的耐水性增强,土壤中的水分难以进入薄膜,降低了水分对薄膜的作用。随着DMU含量的增加,薄膜的降解率逐渐下降,这是由于DMU的作用,使得热塑性淀粉薄膜形成均匀连续相,土壤中的水分和微生物难以进入,进一步增加了热塑性淀粉薄膜的稳定性。保持淀粉薄膜高降解率,DMU不宜添加过多。DMU25薄膜的热塑性最佳,结合电镜测试结果,该薄膜的连续性及基质的相容性最好、且薄膜的透光率最大、吸水率最低,因此选择DMU含量为25%,改性淀粉薄膜的综合性能达到了最优。
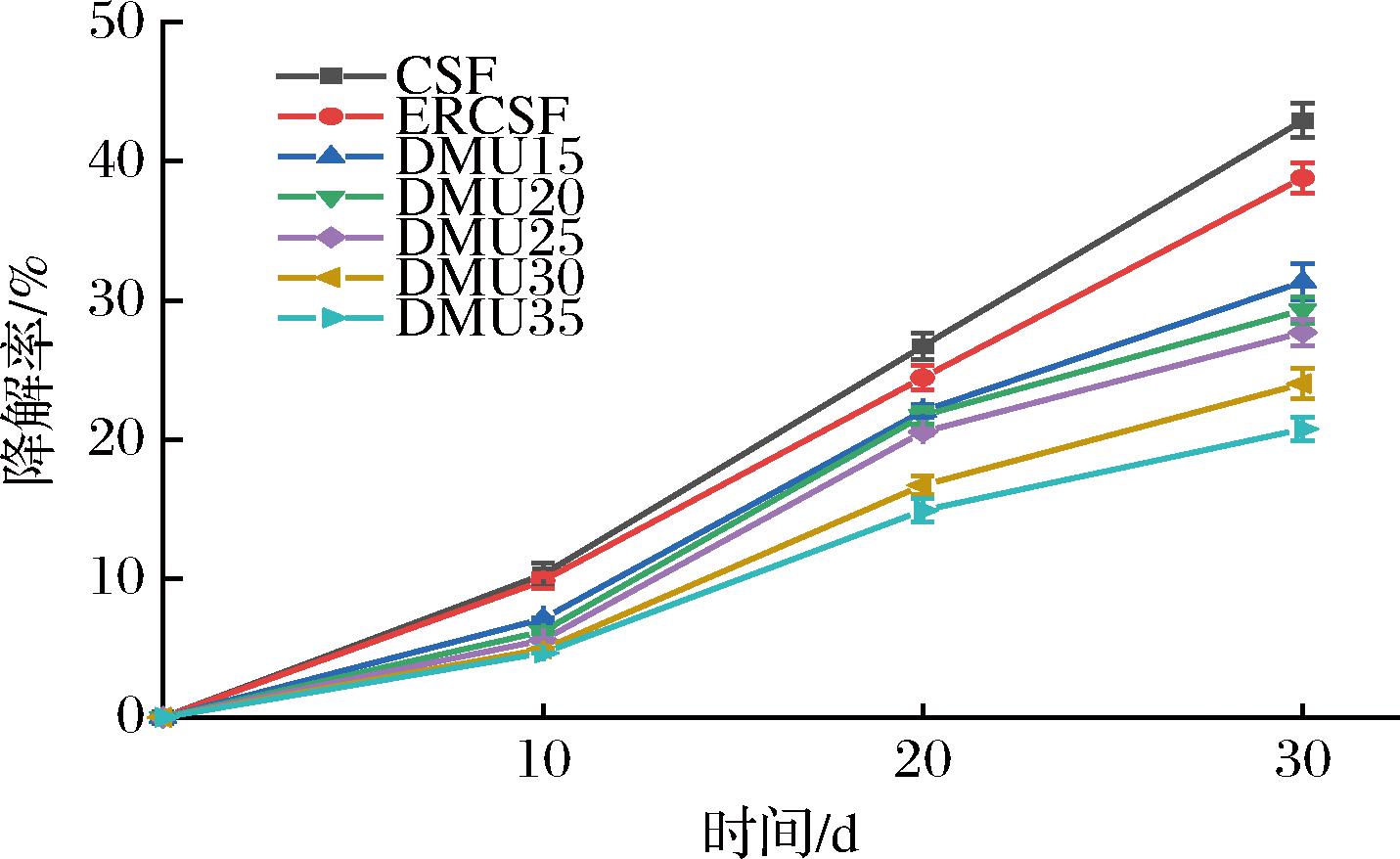
图9 CSF、ERCSF和热塑性淀粉薄膜的降解率
Fig.9 The degradation rate of CSF, ERCSF, and thermoplastic starch films
3 结论
塑化剂DMU的加入增强了板栗淀粉的热塑性能,在DMU含量为25%时,塑化剂DMU与淀粉分子间的氢键作用最强,玻璃化转变温度达到了最低,更利于热塑加工。塑化剂DMU的氢键作用破坏了板栗淀粉颗粒的内部结构使其结晶度降低,形成的热塑性板栗淀粉薄膜更具连续、均匀和紧密性,进一步增强了改性淀粉薄膜的透光率、耐水性及相容性;随着塑化剂DMU用量的增加,断裂伸长率递增,拉伸强度降低,表明塑化作用增强了热塑性板栗淀粉薄膜的韧性。因此,热塑性板栗淀粉作为一种环境友好、生物可降解的优质生物基材料为绿色食品包装领域所使用的膜材料提供一种新的选择。
[1] ZHANG K, HAMIDIAN A H, ![]() A, et al.Understanding plastic degradation and microplastic formation in the environment:A review[J].Environmental Pollution, 2021, 274:116554.
A, et al.Understanding plastic degradation and microplastic formation in the environment:A review[J].Environmental Pollution, 2021, 274:116554.
[2] WANG W, ZHANG W W, LI L, et al.Biodegradable starch-based packaging films incorporated with polyurethane-encapsulated essential-oil microcapsules for sustained food preservation[J].International Journal of Biological Macromolecules, 2023, 235:123889.
[3] 王雅荭, 谢京颖, 高彦祥.生物基材料及其在食品包装中的研究进展[J].中国食品添加剂, 2024, 35(11):238-248.WANG Y H, XIE J Y, GAO Y X.Research progress of bio-based materials and their applications in food packaging[J].China Food Additives, 2024, 35(11):238-248.
[4] POUDEL R, DUTTA N, KARAK N.A mechanically robust biodegradable bioplastic of citric acid modified plasticized yam starch with anthocyanin as a fish spoilage auto-detecting smart film[J].International Journal of Biological Macromolecules, 2023, 242:125020.
[5] BAO W J, LI Q, WU Y W, et al.Insights into the crystallinity and in vitro digestibility of chestnut starch during thermal processing[J].Food Chemistry, 2018, 269:244-251.
[6] WANG S, HU N, TANG E J, et al.Optimization of porous phosphorylated chestnut starch synthesis by response surface methodology and characterization of its properties[J].Starch-Stärke, 2023,75(7-8):2200179.
[7] 孙万海, 董海洲, 侯汉学, 等.熔融挤出法制备热塑性羟丙基交联淀粉可食膜的研究[J].食品与发酵工业, 2010, 36(11):53-57.SUN W H, DONG H Z, HOU H X, et al.Study on preparation of thermoplastic hydroxypropylated cross-linked edible starch film with melt-extrusion[J].Food and Fermentation Industries, 2010, 36(11):53-57.
[8] 刘鹏飞, 孙圣麟, 王文涛, 等.增塑剂甘油对甘薯淀粉膜性能的影响研究[J].中国粮油学报, 2015, 30(10):15-20.LIU P F, SUN S L, WANG W T, et al.Effect of glycerol plasticizer on the properties of sweet potato starch-based films[J].Journal of the Chinese Cereals and Oils Association, 2015, 30(10):15-20.
[9] KOH A Y M, NOR F M, RAMESH S, et al.Plasticisers for edible packaging made of thermoplastic sago starch[J].Materials Today:Proceedings, 2023, 4:523.
[10] 李泽坤. 热塑性淀粉及其复合材料的制备与性能研究[D].石家庄:石家庄铁道大学, 2023.LI Z K.Preparation and properties of thermoplastic starch and its composites[D].Shijiazhuang:Shijiazhuang Tiedao University, 2023.
[11] HU N, LI L N.Optimization of chestnut starch acetate synthesis by response surface methodology and its effect on dough properties[J].Journal of Food Processing and Preservation, 2021, 45(5):e15431.
[12] LYU X F, GUO C S, MA Y X, et al.Effect of citric acid esterification on the structure and physicochemical properties of tigernut starch[J].International Journal of Biological Macromolecules, 2022, 222:2833-2842.
[13] YANG N, GAO W, ZOU F X, et al.The relationship between molecular structure and film-forming properties of thermoplastic starches from different botanical sources[J].International Journal of Biological Macromolecules, 2023, 230:123114.
[14] 姜俊志. 淀粉/PBAT/纤维素复合膜的制备及其性能研究[D].泰安:山东农业大学, 2023.JIANG J Z.Preparation of starch/PBAT/cellulose composite membrane and its performance study[D].Taian:Shandong Agricultural University, 2023.
[15] PATIL S, BHARIMALLA A K, NADANATHANGAM V, et al.Nanocellulose reinforced corn starch-based biocomposite films:Composite optimization, characterization and storage studies[J].Food Packaging and Shelf Life, 2022, 33:100860.
[16] ADJOUMANE M M A, EDJA A F, DOE-MENSAH J, et al.Effect of cardanol-based plasticizers on thermoplastic cassava (Manihot esculenta) starch properties[J].Industrial Crops and Products, 2023, 203:117145.
[17] SHEN L X, ZHANG Y M, LAN Y C, et al.Effects of degradable films with different degradation cycles on soil temperature, moisture and maize yield[J].International Journal of Agricultural and Biological Engineering, 2019, 12(3):36-44.
[18] 孙秋月, 王若桦, 吴非.超声波和酯化复合处理马铃薯淀粉的性质分析[J].食品研究与开发, 2023, 44(14):119-124.SUN Q Y, WANG R H, WU F.Properties analysis of potato starch treated by ultrasonic and esterification[J].Food Research and Development, 2023, 44(14):119-124.
[19] 黄娜, 杨晋辉.二羟甲基脲塑化马铃薯淀粉膜的性能研究[J].塑料工业, 2012, 40(S1):79-83.HUANG N, YANG J H.Study on the properties of dihydroxyl-methyl-urea plasticized potato starch film[J].China Plastics Industry, 2012, 40(S1):79-83.
[20] 刘天祥. 板栗C型淀粉的结构和特性[D].扬州:扬州大学, 2020.LIU T X.Structure and properties of chestnut C-type starch[D].Yangzhou:Yangzhou University, 2020.
[21] 唐康康. 淀粉生物降解材料的分子模拟与制备研究[D].石家庄:石家庄铁道大学, 2016.TANG K K.Molecular modeling and preparation of starch biodegradable materials[D].Shijiazhuang:Shijiazhuang Tiedao University, 2016.
[22] MA H P, QIN W B, GUO B, et al.Effect of plant tannin and glycerol on thermoplastic starch:Mechanical structural, antimicrobial and biodegradable properties[J].Carbohydrate Polymers, 2022, 295:119869.
[23] PROMSORN J, HARNKARNSUJARIT N.Oxygen absorbing food packaging made by extrusion compounding of thermoplastic cassava starch with gallic acid[J].Food Control, 2022, 142:109273.