苦荞是一种中国传统农作物,含有多酚、蛋白质和多糖等多种生物活性物质,以黄酮含量高而出名[1]。黄酮类物质可以清除体内的自由基,减轻氧化应激反应,保护细胞免受氧化损伤[2]。在食品、药品和保健品领域具有良好的开发前景。苦荞中含有多种黄酮类物质,并以自由和结合两种形式存在。结合形式的黄酮多酚类物质与脂肪酸、糖、蛋白质或其他大分子形成不溶状态的复合体,不易被人体吸收[3]。促进苦荞中结合形式的黄酮多酚类物质转变为可溶性或游离黄酮多酚类物质具有一定的学术及应用价值。
微生物发酵可使不溶性结合黄酮多酚类物质变为可溶性结合黄酮多酚类物质或游离黄酮多酚类物质,从而有效提高天然产物的生物活性。如经黑曲霉发酵的豆荚、柑橘粉,经米曲霉发酵的黑米皮和经红曲霉发酵的番石榴均可提高酚类/黄酮类物质的提取率[4-7]。红曲霉(Monascus ssp.)是一种丝状真菌,在我国的生产和使用已有1 000多年历史。随着国内外学者对经红曲霉发酵产生的有效生理活性物质的深入研究,越来越多具有药用价值、营养价值的代谢产物被发现,如莫纳可林K、红曲霉色素、γ-氨基丁酸等活性物质[8-9]。近些年来,越来越多的红曲霉发酵基质被开发利用,奶酪、青稞等发酵基质和红曲霉结合产生新的功能性食品[10-11]。同样的有研究观察红曲霉固态发酵前后苦荞中酚类物质的变化,研究结果表明发酵后总酚和总黄酮含量分别增加约1.4倍和2.2倍,膳食添加发酵产物可改善小鼠血脂、糖耐量和抗氧化酶活性[12]。
通过红曲霉发酵苦荞,提高生苦荞中黄酮类物质生物含量以及产生具有降血脂作用的莫纳可林K具有较好的研究和开发价值。本研究从市售红曲米中筛选高产莫纳可林K的红曲霉菌株,并且以该红曲霉为发酵菌株,苦荞为发酵基质,莫纳可林K为主要指标,发酵产物黄酮提取量、色价、抗氧化活性作为参考指标,通过单因素试验确定影响因子,再运用响应面试验优化发酵工艺,为开发红曲苦荞茶产品提供实践基础。
1 材料与方法
1.1 材料与试剂
1.1.1 菌种及培养基
发酵菌株为从市售红曲米中筛选出的3株菌株,命名HQ-1、HQ-0、HQ-QZ。马铃薯葡萄糖琼脂培养基(PDA)培养基(g/L):马铃薯200,葡萄糖20,琼脂粉20。种子培养基(g/L):葡萄糖60,蛋白胨25,苦荞粉20,NaNO3 2,MgSO4·7H2O 1,KH2PO3 1,ZnSO4 1,pH值自然,分装至250 mL摇瓶,装液量30 mL,灭菌条件121 ℃,20 min。固态发酵培养基:市售苦荞25 g,蒸馏水20 mL,pH自然,灭菌条件121 ℃,20 min。
1.1.2 主要试剂
市售红曲米,古田县闵妃食品有限公司、古田帝元红曲厂、安徽德昌药业股份有限公司;市售苦荞,山东莘县睿翼食品有限公司;莫纳可林K(纯度98%),东京化成工业株式会社;DPPH(98%)、ABTS(98%)、芦丁(97%)、槲皮素(97%)、山奈酚(97%)、绿原酸(98%)、阿魏酸(99%),上海麦克林生化科技有限公司;抗坏血酸(99%),北京索莱宝科技有限公司。
1.2 仪器与设备
UV-5500PC紫外可见分光光度计,上海元析仪器有限公司;LC-2030高效液相色谱仪,日本岛津株式会社;ZQZY-78BN振荡培养箱,上海楚知仪器有限公司;S-4800扫描电镜,株式会社日立制作所。
1.3 实验方法
1.3.1 红曲霉菌株筛选与鉴定
称取市售红曲米5.0 g于250 mL灭菌药瓶中,加入45 mL无菌生理盐水,放入温度30 ℃,转速200 r/min摇床中,活化40 min。吸取1 mL液体进行梯度稀释,涂布PDA平板,30 ℃培养3~5 d。观察菌落生长,选取具有红曲霉菌落特征的单菌落用接种环挑取,在PDA培养基上划线,如有杂菌需要再次进行分离纯化,4 ℃保藏。
取PDA平板培养4 d菌种于1 mL离心管中,按照林琳等[13]方法进行戊二醇固定,冷冻干燥24 h进行扫描电镜检测。分子生物学鉴定参考文献[14],以红曲霉菌株HQ-1、HQ-0、HQ-QZ的DNA为模板,使用通用引物ITS1和ITS4作为引物进行PCR实验,测序后进行BLAST比对。
1.3.2 红曲苦荞发酵方法
取红曲霉菌株于PDA培养基中划线,用5 mL无菌水洗出孢子液。振荡混匀,取1 mL孢子悬浮液,接种于30 mL种子培养基中,37 ℃、200 r/min培养2 d。取培养过的种子液5 mL(接种量按总发酵体系10%计),加入至固体发酵培养基中,0~2 d,30 ℃静置培养,2~15 d 25 ℃静置培养,每天均匀充分摇晃1次,发酵结束置于60 ℃烘箱,烘至恒重,打成粉过40目筛,-4 ℃备用。
1.3.3 发酵条件优化
依次以不同氮源((NH4)2SO4、NaNO3、NH4Cl、NH4NO3、酵母膏、牛肉膏、蛋白胨、黄豆饼粉,添加量3 g/L),氮源添加量(NH4NO3添加量为1、2、3、4、5 g/L),无机盐[MgSO4·7H2O、KH2PO3、ZnSO4、Fe2(SO4)3,添加量1 g/L],无机盐添加量(ZnSO4添加量1、1.5、2、2.5、3 g/L),溶液初始pH(2.5、4、5.5、6.5、8.0),料液比(液体添加量为10、15、20、25、30 mL)作为唯一变量进行单因素试验,以其发酵产物莫纳可林K作为主要评比指标,黄酮类物质含量、色价和抗氧化活性为次要指标,优化发酵培养基。
以单因素结果为依据,采用Box-Behnken中心组合设计,设置pH值(X1)、料液比(X2)、NH4NO3含量(X3)、ZnSO4含量(X4)为自变量,莫纳可林K产量(Y1)为响应值,以此来设计四因素四水平实验,其他次要条件不变,具体数值如表1所示。
表1 实验设计及结果
Table 1 Experimental design and results

试验号pH值X1含水率X2/%NH4NO3含量X3/(g/L)ZnSO4含量X4/(g/L)莫纳可林K含量Y1/(mg/100 g)114032104.445254032101.425316032107.360456032109.935535011120.295635051117.800735013121.730835053139.420915031117.8851055031123.8551115033124.7851255033132.455133401295.8801436012116.1601534052104.6751636052110.6801715012131.9751855012119.5901915052120.1302055052115.8052134031102.1752236031113.5352334033102.3952436033112.8852535032157.1752635032150.6202735032161.5352835032163.8052935032152.395
1.3.4 莫纳可林K含量、黄酮类物质和抗氧化活性测量
精密称量1.000 g红曲苦荞粉,置于50 mL离心管中,添加25 mL甲醇,超声波30 min,用0.22 μm超滤膜过滤,得到待测液。采用HPLC法进行莫纳可林K含量测定,色谱条件[15]:C18色谱柱,流动相:V(乙腈)∶V(0.01%磷酸水溶液)=40∶60,检测波长238 nm;进样体积20 μL;流速1 mL/min;柱温25 ℃。采用抗坏血酸为标准品,进行DPPH抗氧化活性和ABTS抗氧化活性测定[16]。以芦丁为标品采用AlCl3法测定总黄酮含量[17]。
1.3.5 色价测量
参照国标GB 1886.19—2015《食品国家安全标准 食品添加剂 红曲米》。
1.3.6 芦丁、槲皮素、山奈酚、阿魏酸、绿原酸含量测定
精密称量1.000 g红曲苦荞粉,置于50 mL离心管中,添加25 mL甲醇,超声波30 min,用0.22 μm超滤膜过滤,得到待测液。芦丁、阿魏酸、绿原酸测定色谱条件:C18色谱柱;流动相:V(乙腈)∶V(0.01%磷酸水溶液)=20∶80;检测波长329 nm;进样体积20 μL;流速1 mL/min;柱温25 ℃。槲皮素、山奈酚测定色谱条件:C18色谱柱。流动相:V(乙腈)∶V(0.01%磷酸水溶液)=40∶60;检测波长370 nm;进样体积20 μL;流速1 mL/min;柱温25 ℃。
1.4 数据处理
每个实验进行3个平行,结果取均值。使用Origin 2018软件分析作图;SPSS 22.0软件进行单因素方差分析及显著性差异分析;Design Expert 12.0软件进行响应面优化试验设计及分析。
2 结果与分析
2.1 红曲霉菌株筛选及鉴定
实验共筛选出HQ-0、HQ-1、HQ-QZ 3株菌株,颜色均为橙色或者偏棕红色,菌落中间凸起,气生菌丝被茸毛状至被卷棉毛状,菌丝具隔膜,多分枝,分生孢子连续分生呈链,6~8 μm。子囊孢子呈圆形,光滑,5~6 μm,符合紫色红曲霉的形态学特征[18](图1)[19]。对3株菌株进行5.8 s ITS rDNA测序,通过NCBI数据库进行比较,并构建系统发育树。HQ-0与Monascus purpureus strain BHQ33.M03(MW581232.1)处于同一分支,HQ-1与Monascus sp.(MW527421.1)处于同一分支,HQ-QZ与Monascus purpureus isolate 2010F16(MT5583931.1)处于同一分支(图2)。根据形态学特征、5.8 s ITS rDNA测序,可以初步确定,3株菌株均属于紫色红曲霉(Monascus purpureus)。
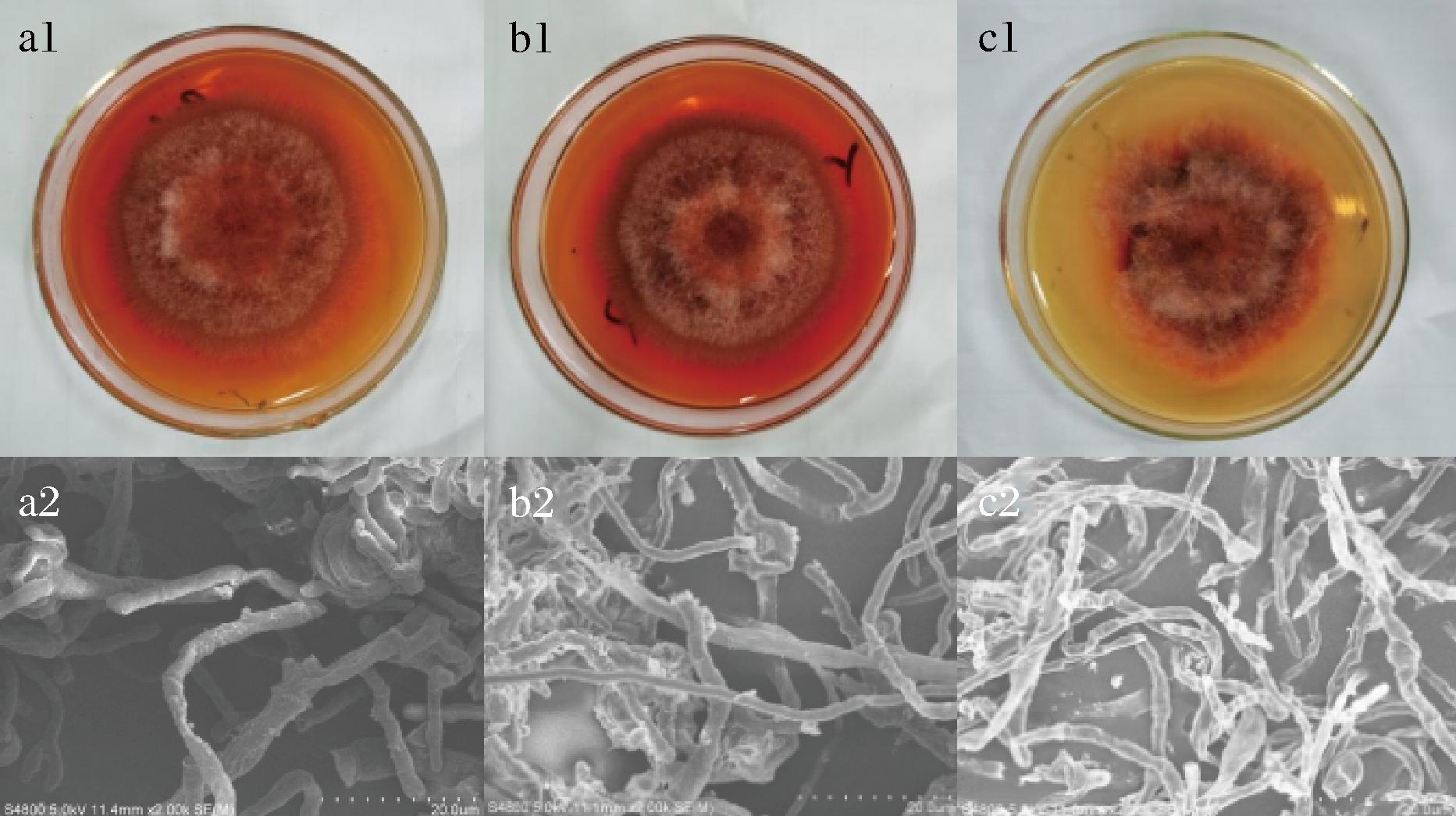
a1-HQ-0号菌株菌落照片;b1-HQ-1号菌株菌落照片;c1-HQ-QZ号菌株菌落照片;a2-HQ-0号菌株菌丝体电镜照片;b2-HQ-1号菌株菌丝体电镜照片;c2-HQ-QZ号菌株菌丝体电镜照片
图1 菌落照片及菌丝体电镜照片
Fig.1 Colony photo and electron microscopy photo of mycelium
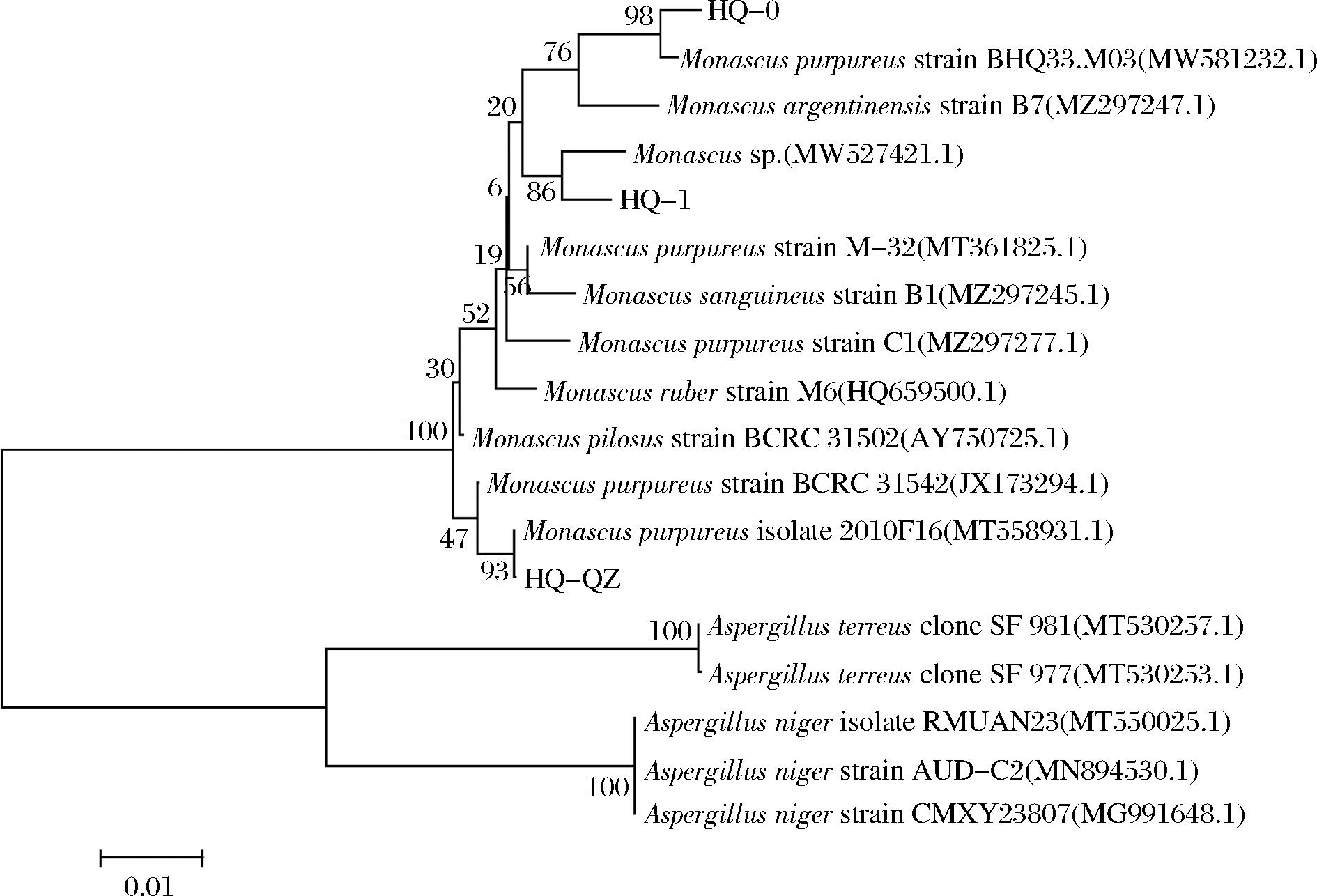
图2 HQ-1、HQ-0、HQ-QZ菌株基于ITS序列建立的系统发育树
Fig.2 The phylogenetic trees of HQ-1, HQ-0, and HQ-QZ strains were established based on ITS sequences
2.2 菌株发酵菌株选定
3株菌株中HQ-1菌株其发酵的莫纳可林K产量(显著P<0.05)及ABTS抗氧化活性最高,达到了140.36 mg/100 g、1 655.8 μg vc/gdw,色价基本与HQ-0持平,为335.5 μ/g,DPPH抗氧化活性以及发酵产物的黄酮提取量略逊于HQ-QZ,后续实验选择HQ-1作为发酵优化菌株(图3)。

a-莫纳可林K产量和色价;b-DPPH和ABTS抗氧化活性以及发酵产物的黄酮提取量
图3 三株红曲霉发酵产物的产量、对其发酵过苦荞的抗氧化活性以及黄酮提取量的影响
Fig.3 The production from three strains of Monascus purpureusand the antioxidant properties, in addition to detailing the quantity of flavonoids extracted from fermented tartary buckwheat
注:相同颜色图案数据上标字母不同表示差异显著(P<0.05)(下同)。
2.3 单因素优化
2.3.1 添加不同外源氮源对红曲霉发酵的影响
发酵体系中添加NH4NO3作为外源氮源其莫纳可林K产量最高,达到了145.6 mg/100 g,其色价仅次于添加(NH4)2SO4样品,尽管其抗氧化活性以及发酵产物的黄酮提取量不是添加7种外源氮源中最高的,但是考虑其综合指标,最终选择NH4NO3作为外源氮源添加(图4)。

a-莫纳可林K产量和色价;b-DPPH和ABTS抗氧化活性以及发酵产物的黄酮提取量
图4 添加不同外源氮源对红曲霉发酵产物产量、对发酵过苦荞的抗氧化活性以及其黄酮提取量的影响
Fig.4 Effect of adding different exogenous nitrogen sources on the fermentation yield ,the antioxidant properties and the quantity of flavonoids extracted from fermented tartary buckwheat

a-莫纳可林K产量和色价;b-DPPH和ABTS抗氧化活性以及发酵产物的黄酮提取量
图5 不同的硝酸铵添加浓度对红曲霉发酵产物产量、对发酵过苦荞的抗氧化活性以及其黄酮提取量的影响
Fig.5 Effect of different ammonium nitrate addition concentrations on the fermentation yield ,the antioxidant properties and the quantity of flavonoids extracted from fermented tartary buckwheat

a-莫纳可林K产量和色价;b-DPPH和ABTS抗氧化活性以及发酵产物的黄酮提取量
图6 添加无机盐对红曲霉发酵产物产量、对发酵过苦荞的抗氧化活性以及其黄酮提取量的影响
Fig.6 Effect of adding inorganic salts on the fermentation yield,the antioxidant properties and the quantity of flavonoids extracted from fermented tartary buckwheat
2.3.2 不同的NH4NO3质量浓度对发酵的影响
当NH4NO3质量浓度达到3 g/L时,其莫纳可林K、色价、抗氧化活性、发酵产物的黄酮提取量均为最高,分别达到了178.58 mg/100 g、345.33 μ/g、2 059.2 μg vc/gdw、1 687.43 μg vc/gdw、41.78 mg/g(图5)。SU等[19]研究发现,添加适量的NH4NO3可以促进红曲霉的生长,从而提高莫纳可林K的产量。
2.3.3 添加不同无机盐对发酵的影响
红曲霉生长同样不可缺少无机盐的参与。如图6所示,添加ZnSO4的样品其莫纳可林K产量及色价产量最高,达到了102.71 mg/100 g、534.00 μ/g。SEENIVASAN等[20]研究表明,Zn2+可以促进红曲霉产生莫纳可林K。因此后续实验将选取最佳的ZnSO4添加量。
2.3.4 不同的ZnSO4质量浓度对发酵的影响
ZnSO4的质量浓度达到2 g/L时,其莫纳可林K产量和色价最高,其产量分别达到了72.63 mg/100 g、336.33 μ/g,添加质量浓度1.5~2.0 g/L时,显著(P<0.05)高于其他添加量。而添加不同质量浓度ZnSO4对发酵产物的抗氧化活性及其黄酮提取量的影响不显著(图7)。因此,推测添加适量的ZnSO4促进红曲霉菌株的色素和莫纳可林K产生,而不是促进红曲霉菌株生长从而提高其代谢产物的产量[20]。

a-莫纳可林K产量和色价;b-DPPH和ABTS抗氧化活性以及发酵产物的黄酮提取量
图7 不同的硫酸锌添加浓度对红曲霉发酵产物产量、对发酵过苦荞的抗氧化活性以及其黄酮提取量的影响
Fig.7 Effect of different zinc sulfate addition concentrations on the fermentation yield ,the antioxidant properties and the quantity of flavonoids extracted from fermented tartary buckwheat
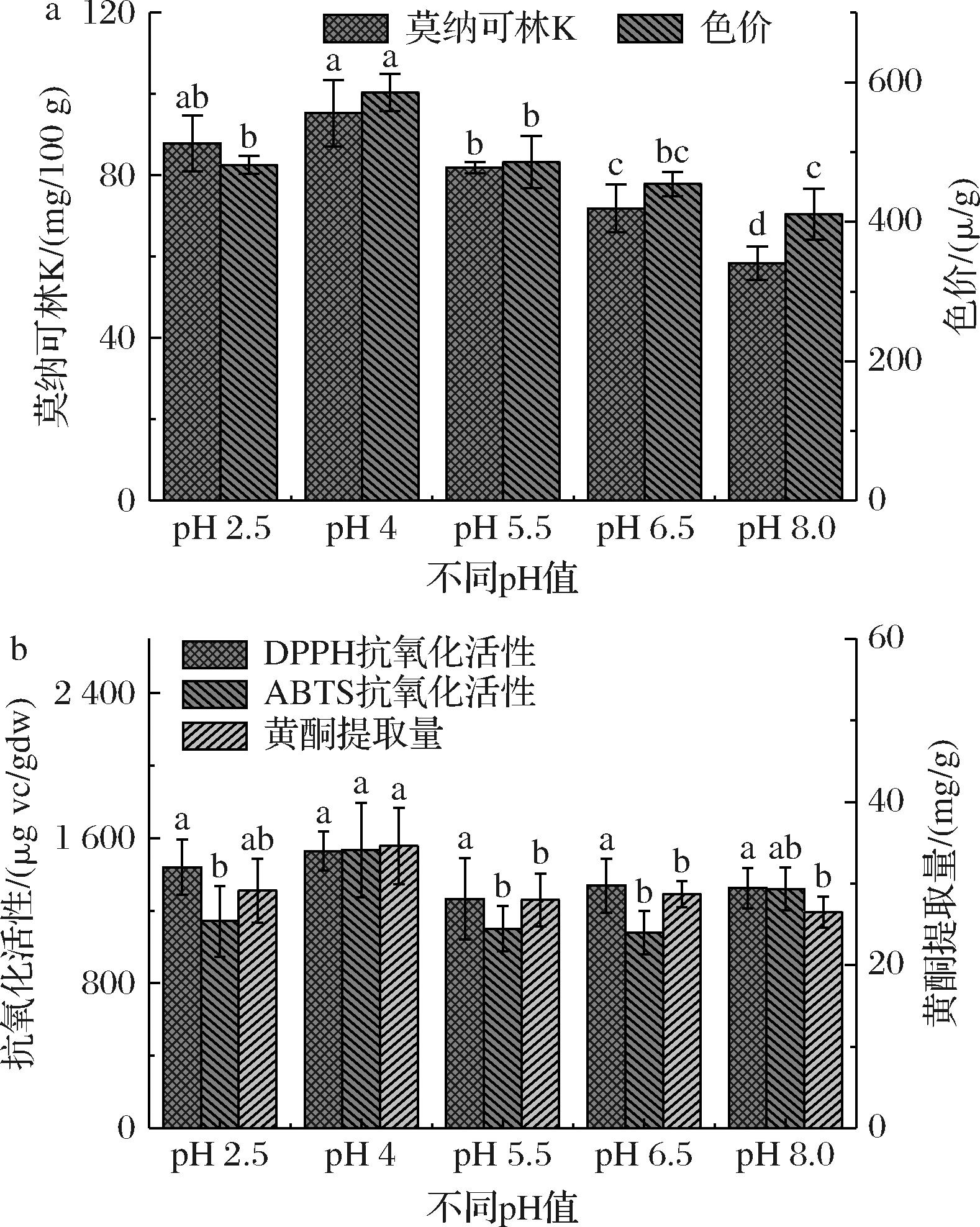
a-莫纳可林K产量和色价;b-DPPH和ABTS抗氧化活性以及发酵产物的黄酮提取量
图8 不同pH值对红曲霉发酵产物产量、对发酵过苦荞的抗氧化活性以及其黄酮提取量的影响
Fig.8 Effect of different pH concentrations on the fermentation yield,the antioxidant properties and the quantity of flavonoids extracted from fermented tartary buckwheat
2.3.5 不同pH值对红曲霉发酵的影响
在固体发酵中,不同pH值的搅拌水对红曲霉的生长有很大的影响。如图8所示,在pH值为4的条件下,样品中的莫纳可林K产量、色价、DPPH及ABTS抗氧活性、发酵产物的黄酮提取量均达到了最高,分别达到了95.31 mg/100 g、585.33 μ/g、1 528.69 μg vc/gdw、1 535.16 μg vc/gdw、34.59 mg/g。实验结果显示,酸性条件下,红曲霉莫纳可林K产量、色价显著提高(P<0.05),这与LEE等[21]的研究结果相类似,他们发现以山药做发酵基质时,pH值在3的条件下,莫纳可林K的产量更高;同时RATROVSKY等[22]研究发现,摇瓶发酵时pH值为2.5的时候,色素产量最高。因此,培养基为酸性条件可能更有利于红曲霉生长以及其代谢产物的生成。
2.3.6 不同料液比对红曲霉发酵的影响
发酵初始时料液比为5∶5的样品其莫纳可林K的产量、色价最高、ABTS抗氧活性、发酵产物的黄酮提取量最高,达到了135.51 mg/100 g、521 μ/g、1 740.03 μg vc/gdw、44.6 mg/g,而DPPH抗氧活性在料液比为5∶4时最高,为1 615.21 μg vc/gdw(图9)。有研究推断[23-24],当料液比中液体比较低时,红曲霉由于没有充足的水分从而导致其定殖苦荞表面的难度增大,影响苦荞的发酵。而当液体比重较高时,由于高温灭菌的作用,导致苦荞颗粒之间的黏度增大,再加上苦荞本身的吸水涨大,导致整个发酵环境中的空隙变小,空气流动性降低,导致红曲霉在增殖过程中无法获得足够多的O2,进而影响其生长发育。

a-莫纳可林K产量和色价;b-DPPH和ABTS抗氧化活性以及发酵产物的黄酮提取量
图9 料液比对红曲霉发酵产物产量、对发酵过苦荞的抗氧化活性以及其黄酮提取量的影响
Fig.9 Effect of material liquid ratio concentrations on the fermentation yield,the antioxidant properties and the quantity of flavonoids extracted from fermented tartary buckwheat
2.4 响应面法优化发酵条件
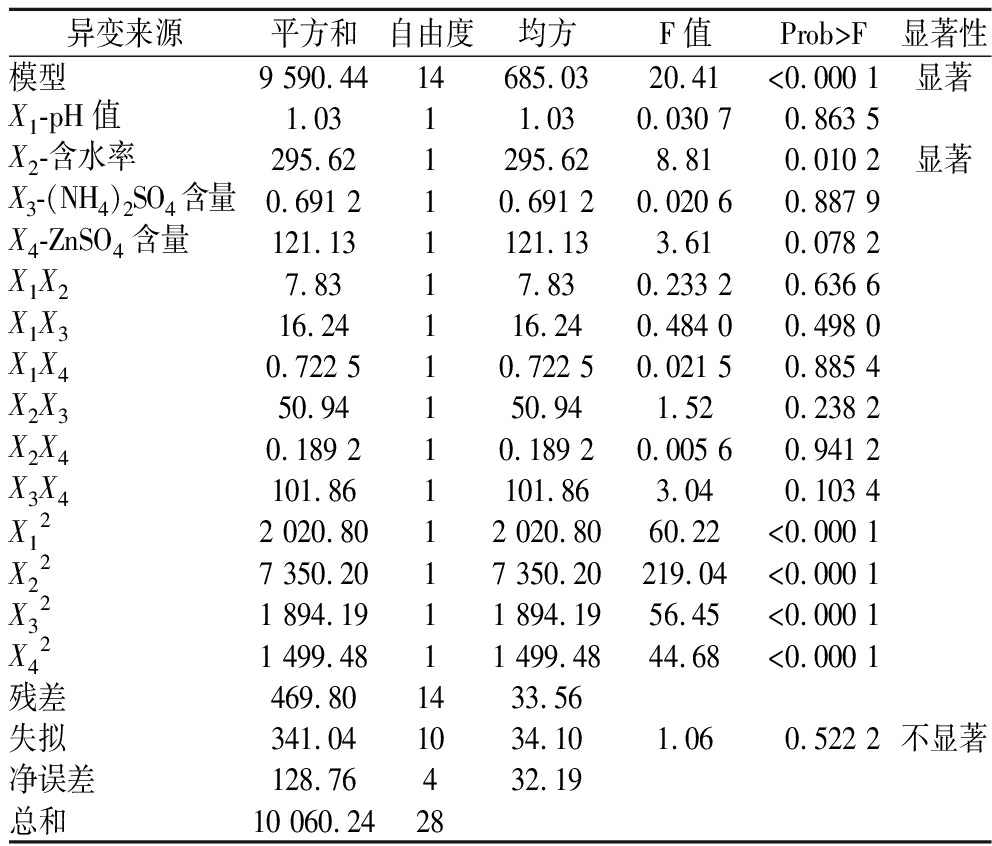
方差分析结果显示(表2),含水率对莫纳可林K产量有显著性影响,其余因素影响均显著。通过各因素F值可知,各因素对莫纳可林K的产量影响大小顺序为:含水率(X2)>ZnSO4质量浓度(X4)>搅拌水pH值(X1)>NH4NO3质量浓度(X3)。响应面结果表明,红曲霉固态发酵苦荞的最优发酵工艺条件:pH值为2.583,搅拌水添加量为每25 g苦荞添加21 mL,搅拌水NH4NO3质量浓度为2.766 g/L,搅拌水ZnSO4质量浓度为1.821 g/L(图10)。采用上述优化后的发酵条件,红曲霉发酵莫纳可林K产量为162.26 mg/100 g,发酵产物的黄酮提取量为50.2 mg/g,色价为724.33 μ/g,DPPH抗氧化活性和ABTS抗氧化活性分别为4 259.12 μg vc/gdw和2 391.86 μg vc/gdw。
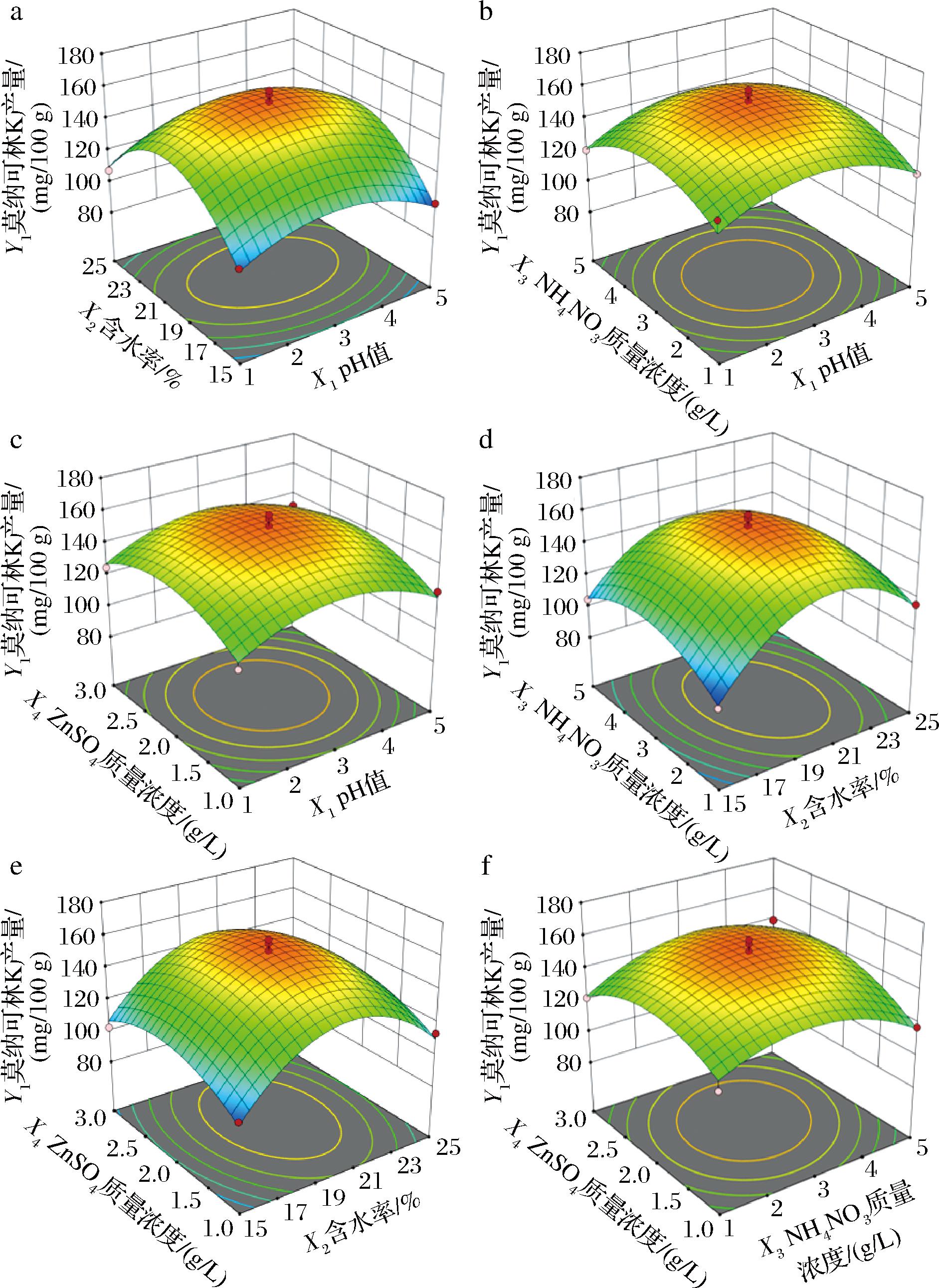
a-含水率和pH值交互作用对莫纳可林K产量影响的响应面图;b-NH4NO3质量浓度和pH值交互作用对莫纳可林K产量影响的响应面图;c-ZnSO4质量浓度和pH值交互作用对莫纳可林K产量影响的响应面图;d-NH4NO3质量浓度和含水率交互作用对莫纳可林K产量影响的响应面图;e-ZnSO4质量浓度和含水率交互作用对莫纳可林K产量影响的响应面图;f-ZnSO4质量浓度和NH4NO3质量浓度交互作用对莫纳可林K产量影响的响应面图
图10 响应面分析莫纳可林K产量的最优条件
Fig.10 Effect of various factors on MK yield
表2 回归方程(Y1)的方差分析表
Table 2 Analysis of variance table for regression equation (Y1)
异变来源平方和自由度均方F值Prob>F显著性模型9 590.4414685.0320.41<0.000 1显著X1-pH值1.0311.030.030 70.863 5X2-含水率295.621295.628.810.010 2显著X3-(NH4)2SO4含量0.691 210.691 20.020 60.887 9X4-ZnSO4含量121.131121.133.610.078 2X1X27.8317.830.233 20.636 6X1X316.24116.240.484 00.498 0X1X40.722 510.722 50.021 50.885 4X2X350.94150.941.520.238 2X2X40.189 210.189 20.005 60.941 2X3X4101.861101.863.040.103 4X122 020.8012 020.8060.22<0.000 1X227 350.2017 350.20219.04<0.000 1X321 894.1911 894.1956.45<0.000 1X421 499.4811 499.4844.68<0.000 1残差469.801433.56失拟341.041034.101.060.522 2不显著净误差128.76432.19总和10 060.2428
2.5 最优条件下各检测指标随时间变化
按最优实验条件发酵,红曲霉发酵所得产物莫纳可林K产量和色价如表3所示,其莫纳可林K产量在第13天趋于平稳,最大值在第15天,产量为187.10 mg/100 g;而其色价在第9天开始趋于稳定,最大值同样在第15天达到最大,达到733.33 μ/g。莫纳可林K的产量随时间变化趋势和SURAIYA等[25]研究结果相似且产量更高。由表4可知,随着发酵时间增长,芦丁、槲皮素、山奈酚、绿原酸、阿魏酸这些黄酮多酚类物质的萃取量显著(P<0.05)提高,分别提高了68%、159%、688%、244%、65%。丝状真菌产生的一些酶如淀粉酶、木聚糖酶、蛋白酶和β-葡萄糖苷酶等有助于改变谷类物质的组成,并释放结合的酚类黄酮类化合物[26]。黄酮多酚类物质的释放提高,提升了苦荞发酵提取液的抗氧化能力,DPPH抗氧化活性和ABTS抗氧化活性均随发酵时间增长,分别提高了202%和80%(表3)。综合考虑各检测指标随发酵时间变化情况以及发酵成本,确定最佳发酵时间为11 d。
表3 红曲霉发酵产物随时间变化
Table 3 Changes of Monascus purpureus fermentation products over time

天数莫纳可林K产量/(mg/100 g)色价/(μ/g)DPPH抗氧化活性/(μg vc/gdw)ABTS抗氧化活性/(μg vc/gdw)0001 443.63±25.46e1 443.63±25.46f 311.16±1.18e88.00±6.56d3 262.18±95.60d1 585.66±166.11e560.03±6.07d427.67±6.11c3 588.38±114.59c1 926.74±144.65d7113.12±9.04c598.67±8.74b4 010.40±114.26b2 106.98±18.69c9149.30±8.84b712.33±20.84a4 032.82±94.82b2 291.09±18.69b11158.58±9.53b724.33±1.53a4 259.12±79.59a2 391.86±139.90b13184.83±17.71a726.00±16.46a4 383.49±165.59a2 566.28±55.46a15187.10±10.08a733.33±26.35a4 361.06±183.72a2 605.04±39.57a
注:同列肩标小写字母不同表示差异显著(P<0.05)(下同)。
表4 发酵苦荞中黄酮多酚物质的提取量
Table 4 Changes in extraction quantity of flavonoids from fermented tartary buckwheat

天数芦丁萃取量/(mg/g)槲皮素萃取量/(μg/g)山奈酚萃取量/(μg/g)绿原酸萃取量/(μg/g)阿魏酸萃取量/(μg/g)027.9±0.63f225.26±11.28g7.45±0.67f91.66±3.88f304.52±5.01e335.31±0.25e310.98±13.94f8.60±2.80f137.64±3.88e374.71±0.93d538.18±1.63d381.69±38.15e12.77±1.01e165.41±9.66d393.28±29.38d740.72±0.76c426.04±41.34d30.42±1.63d224.97±10.25c424.57±20.03c943.08±0.82b436.34±16.99d45.09±5.00c256.37±17.88b449.58±11.81b1145.46±1.33a473.49±14.21c51.66±1.20b268.14±5.46b478.14±17.24a1346.28±0.88a541.55±5.11b55.25±2.53ab302.82±10.82a489.47±10.10a1547.06±0.77a585.25±6.52a58.77±0.49a316.13±9.11a501.95±8.79a
3 结论
研究通过单因素及响应面方法对筛选得到的红曲霉菌株HQ-1发酵苦荞实验条件进行了优化,最优发酵条件为:25 g苦荞添加搅拌水21 mL,搅拌水配方为NH4NO3 2.77 g/L,ZnSO4 1.82 g/L,MgSO4·7H2O 1.00 g/L,KH2PO4 1.00 g/L,pH 2.58,接种量为10%,发酵11 d,30 ℃培养2 d,25 ℃培养9 d,每天充分摇瓶1次。发酵产物中,莫纳可林K产量为162.26 mg/100 g,比优化前(140.36 mg/100 g)提高了15%。样品色价为724.33 μ/g,比优化前(335.5 μ/g)提高了115%。样品DPPH抗氧化活性和ABTS抗氧化活性分别为4 259.12 μg vc/gdw和2 391.86 μg vc/gdw,较之前(DPPH抗氧化活性1 284.40 μg vc/gdw、ABTS抗氧化活性1 655.80 μg vc/gdw)分别提高了232%、44%。发酵产物总黄酮提取量达到了50.2 mg/g,其中芦丁、槲皮素、山奈酚、绿原酸、阿魏酸含量从原本的27.9 mg/g、225.26 μg/g、7.45 μg/g、91.66 μg/g、304.52 μg/g提升至45.46 mg/g、473.49 μg/g、51.66 μg/g、268.14 μg/g、478.14 μg/g,分别提升了63%、110%、593%、192%、57%。
[1] LIU B G, ZHU Y Y.Extraction of flavonoids from flavonoid-rich parts in Tartary buckwheat and identification of the main flavonoids[J].Journal of Food Engineering, 2007, 78(2):584-587.
[2] DA PORTO A, CAVARAPE A, COLUSSI G, et al.Polyphenols rich diets and risk of type 2 diabetes[J].Nutrients, 2021, 13(5):1445.
[3] VERARDO V, ARR EZ-ROM
EZ-ROM N D, SEGURA-CARRETERO A, et al.Identification of buckwheat phenolic compounds by reverse phase high performance liquid chromatography-electrospray ionization-time of flight-mass spectrometry (RP-HPLC-ESI-TOF-MS)[J].Journal of Cereal Science, 2010, 52(2):170-176.
N D, SEGURA-CARRETERO A, et al.Identification of buckwheat phenolic compounds by reverse phase high performance liquid chromatography-electrospray ionization-time of flight-mass spectrometry (RP-HPLC-ESI-TOF-MS)[J].Journal of Cereal Science, 2010, 52(2):170-176.
[4] SHIN H Y, KIM S M, LEE J H, et al.Solid-state fermentation of black rice bran with Aspergillus awamori and Aspergillus oryzae:Effects on phenolic acid composition and antioxidant activity of bran extracts[J].Food Chemistry, 2019, 272:235-241.
[5] L PEZ-C
PEZ-C RDENAS F, OCHOA-REYES E, BAEZA-JIMÉNEZ R, et al.Solid-state fermentation as a sustainable tool for extracting phenolic compounds from cascalote pods[J].Fermentation, 2023, 9(9):823.
RDENAS F, OCHOA-REYES E, BAEZA-JIMÉNEZ R, et al.Solid-state fermentation as a sustainable tool for extracting phenolic compounds from cascalote pods[J].Fermentation, 2023, 9(9):823.
[6] WANG L, WEI W H, TIAN X F, et al.Improving bioactivities of polyphenol extracts from Psidium guajava L.leaves through co-fermentation of Monascus anka GIM 3.592 and Saccharomyces cerevisiae GIM 2.139[J].Industrial Crops and Products, 2016, 94:206-215.
[7] MAMY D, HUANG Y Y, AKPABLI-TSIGBE N D K, et al.Valorization of Citrus reticulata peels for flavonoids and antioxidant enhancement by solid-state fermentation using Aspergillus niger CGMCC 3.6189[J].Molecules, 2022, 27(24):8949.
[8] NIMNOI P, LUMYONG S.Improving solid-state fermentation of Monascus purpureus on agricultural products for pigment production[J].Food and Bioprocess Technology, 2011, 4(8):1384-1390.
[9] LI Y G, ZHANG F, WANG Z T, et al.Identification and chemical profiling of monacolins in red yeast rice using high-performance liquid chromatography with photodiode array detector and mass spectrometry[J].Journal of Pharmaceutical and Biomedical Analysis, 2004, 35(5):1101-1112.
[10] 胡久平, 鄢平, 戚珊珊, 等.发酵条件对青稞红曲中Monacolin K和β-葡聚糖的影响[J].食品与发酵工业, 2017, 43(3):134-139.HU J P, YAN P, QI S S, et al.The effect of fermentation conditions on the production of Monacolin K and β-glucan of hullesbarley Monascus[J].Food and Fermentation Industries, 2017, 43(3):134-139.
[11] 徐杏敏, 郑远荣, 刘振民, 等.奶酪发酵剂红曲霉的筛选及其对奶酪理化、质构和抗氧化性的影响[J].食品与发酵工业, 2023, 49(17):127-135.XU X M, ZHENG Y R, LIU Z M, et al.Screening of Monascus as cheese starter and its effects on physicochemical, texture and antioxidant properties of cheese[J].Food and Fermentation Industries, 2023, 49(17):127-135.
[12] REN R, ZENG H Y, MEI Q, et al.Effects of Monascus purpureus-fermented Tartary buckwheat extract on the blood lipid profile, glucose tolerance and antioxidant enzyme activities in KM mice[J].Journal of Cereal Science, 2022, 105:103465.
[13] 林琳, 王昌禄, 李贞景, 等.mok E基因过表达对红曲霉Monacolin K产量、菌丝及孢子形态的影响[J].食品科学, 2018, 39(8):45-49.LIN L, WANG C L, LI Z J, et al.Effect of mok E overexpression on monacolin K production and morphology of mycelia and spores in Monascus[J].Food Science, 2018, 39(8):45-49.
[14] 毛继龙, 张建辉, 王璨, 等.一株高产莫纳可林K红曲霉的筛选与液态发酵条件优化[J].微生物学通报, 2022, 49(6):2221-2232.MAO J L, ZHANG J H, WANG C, et al.Screening and liquid fermentation condition optimization of a high lovastatin producing Monascus[J].Microbiology China, 2022, 49(6):2221-2232.
[15] 陈景智, 王力超, 李亮, 等.红曲霉莫纳可林K的液态发酵及其分离纯化研究[J].食品与发酵工业, 2019, 45(2):31-38.CHEN J Z, WANG L C, LI L, et al.Fermentation conditions and separation of lovastatin for Monascus[J].Food and Fermentation Industries, 2019, 45(2):31-38.
[16] 仇菊, 朱宏, 吴伟菁.苦荞中可溶性及不可溶性膳食纤维调控糖尿病小鼠糖脂代谢的功效[J].食品科学, 2021, 42(15):129-135.QIU J, ZHU H, WU W J.Regulatory effect of soluble and insoluble dietary fiber from Tartary buckwheat on glucose and lipid metabolism in diabetic mice[J].Food Science, 2021, 42(15):129-135.
[17] WU N N, LI H H, TAN B, et al.Free and bound phenolic profiles of the bran from different rice varieties and their antioxidant activity and inhibitory effects on ɑ-amylose and α-glucosidase[J].Journal of Cereal Science, 2018, 82:206-212.
[18] 李钟庆, 郭芳.红曲菌的形态与分类学[M].北京:中国轻工业出版社, 2003.LI Z Q, GUO F.Morphology and Taxonomy of Monascus spp[M].Beijing:China Light Industry Press, 2003.
[19] SU Y C, WANG J J, LIN T T, et al.Production of the secondary metabolites γ-aminobutyric acid and monacolin K by Monascus[J].Journal of Industrial Microbiology and Biotechnology, 2003, 30(1):41-46.
[20] SEENIVASAN A, VENKATESAN S, PANDA T.Cellular localization and production of lovastatin from Monascus purpureus[J].Indian Journal of Pharmaceutical Sciences, 2018, 80(1):85-98.
[21] LEE C L, HUNG H K, WANG J J, et al.Improving the ratio of monacolin K to citrinin production of Monascus purpureus NTU 568 under Dioscorea medium through the mediation of pH value and ethanol addition[J].Journal of Agricultural and Food Chemistry, 2007, 55(16):6493-6502.
[22] PATROVSKY M, SINOVSKA K, BRANSKA B, et al.Effect of initial pH, different nitrogen sources, and cultivation time on the production of yellow or orange Monascus purpureus pigments and the mycotoxin citrinin[J].Food Science &Nutrition, 2019, 7(11):3494-3500.
[23] SRIANTA I, Harijono.Monascus-fermented Sorghum:Pigments and monacolin K produced by Monascus purpureus on whole grain, dehulled grain and bran substrates[J].International Food Research Journal, 2015, 22:377-382.
[24] PANSURIYA R C, SINGHAL R S.Response surface methodology for optimization of production of lovastatin by solid state fermentation[J].Brazilian Journal of Microbiology, 2010, 41(1):164-172.
[25] SURAIYA S, KIM J H, TAK J Y, et al.Influences of fermentation parameters on lovastatin production by Monascus purpureus using Saccharina japonica as solid fermented substrate[J].LWT, 2018, 92:1-9.
[26] TU Y, HUANG S X, CHI C D, et al.Digestibility and structure changes of rice starch following co-fermentation of yeast and Lactobacillus strains[J].International Journal of Biological Macromolecules, 2021, 184:530-537.