阴道加德纳菌(Gardnerella vaginalis,GV)等条件致病菌在阴道的异常增殖[1],会破坏由乳杆菌主导的阴道微生物群落的动态平衡,从而导致细菌性阴道炎(bacterial vaginosis,BV)的发生与进展[2]。GV生物膜的形成,以及唾液酸苷酶、溶细胞素等代谢产物的分泌,是BV发病机制中的关键因素。例如,GV生物膜能够保护病原菌的生长[3];唾液酸苷酶通过水解阴道分泌物中的唾液酸聚糖,进而降解阴道黏液层[4];溶细胞素则具有穿孔毒性,可导致阴道上皮细胞等靶细胞凋亡[5]。在阴道上皮屏障受损的过程中,细胞内的线粒体、微粒体及细胞质酶等位点或细胞器,其维持正常氧化还原平衡的功能发生紊乱,导致活性氧(reactive oxygen species,ROS)大量积累,引发氧化应激[6]。
临床上,硝基咪唑类药物是治疗BV的常用方法。然而,这类抗生素不仅会无选择性地消灭阴道的原生菌群[7],而且也无法修复氧化损伤。CHEN等[8]发现在小鼠模型中,通过下调氧化产物并提升抗氧化酶的活性,对BV的恢复具有显著作用。此外,大量研究亦表明[9-11],口服益生菌能够通过产生抗氧化物质,与宿主相互作用激活抗氧化途径、调节抗氧化酶的活性,从而调节体内的抗氧化反应,维持宿主健康。因此,开发具有抗氧化能力的菌株,对于促进BV氧化应激的恢复具有重要意义。
机体氧化还原系统的平衡及氧化应激状态的调节,与Kelch样ECH关联蛋白1(Kelch-like ECH-associated protein 1,Keap1)/核因子红细胞系2相关因子2(Nuclear factor erythroid 2-related factor 2,Nrf2)信号通路息息相关[12]。在正常条件下,Keap1与Nrf2结合;而在氧化损伤出现时,Keap1会发生变性并与Nrf2解离,随后Nrf2转入细胞核内,调控多种抗氧化酶的表达,以维持体内氧化还原平衡[13]。LONG等[14]研究表明,发酵乳杆菌CQPC08可以激活Keap1/Nrf2信号通路,减轻炎症。因此,开发调控Keap1/Nrf2信号通路的菌株,改善氧化应激损伤,是加速BV恢复的重要因素。
鉴于上述情况,本研究旨在筛选具有良好抗氧化特性的乳杆菌,并评估其对小鼠BV的缓解效果,期望为开发治疗BV的益生菌制剂提供新的研究思路。
1 材料与方法
1.1 实验材料与试剂
40只雌性Balb/c小鼠(7周龄),北京维通利华实验动物技术有限公司。
副干酪乳酪杆菌CCFM1317、VCQWX4103L1,卷曲乳杆菌QJSWX196M1,约氏乳杆菌QJSWX307M32,鼠李糖乳杆菌FNMGHLBE18L5和格氏乳杆菌QJSWX195M1、QJSWX310M13分离自健康人群的粪便或阴道分泌物样本,保存于江南大学食品生物技术菌种保藏中心。徳氏乳杆菌DM8909从内蒙古双奇药业股份有限公司定君生商品中分离得到,作为阳性对照。
阴道上皮细胞(VK2/E6E7)由无锡市人民医院妇产科惠赠。
阴道加德纳菌(Gardnerella vaginalis,GV)ATCC14018,广东省微生物保藏中心。
Nrf2 ELISA试剂盒,南京森贝伽生物科技有限公司;实时荧光定量PCR引物,上海生工生物工程有限公司;土壤DNA提取试剂盒,美国MP Biomedicals公司;DMEM培养液,美国Thermo Fisher Scientific公司;胎牛血清、胰酶,美国Gibco公司;6孔细胞培养板,德国Greiner公司;脂多糖(lipopolysaccharide,LPS),默克生物公司;Cell Counting Kit-8 (CCK-8)试剂盒、实时荧光定量PCR(quantitative real-time PCR,qPCR)及反转录试剂盒,南京诺唯赞生物科技股份有限公司;Trizol试剂,美国Life Technology公司。
1.2 主要仪器与设备
ULT1386-3-V31超低温冰箱、二氧化碳细胞培养箱,美国Thermo Fisher科技公司;ME-T精密天平,梅特勒-托利多仪器(上海)有限公司;SW-CJ-1 CV型微生物操作超净工作台,安泰空气技术有限公司;隔水式恒温培养箱,上海跃进医疗器械厂;高速冷冻离心机,德国Eppendorf;高压均质机,意大利GEA机械设备公司;Multiscan Go全波长酶标仪,美国Thermo公司;高通量组织研磨机,宁波新芝生物科技股份有限公司;切片电子扫描仪,匈牙利3DHISTECH公司;Nano Photometer超微量分光光度计,德国Implen公司;PCR扩增仪T100、实时荧光定量PCR仪、PCR仪、核酸电泳仪、凝胶成像仪,美国Bio-Rad公司。
1.3 主要培养基和菌悬液
MRS液体培养基(g/L):葡萄糖20.0、牛肉膏10.0、蛋白胨10.0、酵母粉5.0、三水合磷酸氢二钾2.6、无水乙酸钠2.0、柠檬酸氢二胺2.0、七水合硫酸镁0.5、一水合硫酸锰0.25,吐温-80 1.0 mL。115 ℃高压灭菌20 min。
MRS固体培养基,向已配好的液体培养基中添加18 g/L的琼脂,115 ℃高压灭菌20 min。
BHI液体培养基(g/L):胰蛋白胨10.0、牛心浸粉17.5、氯化钠5.0、磷酸氢二钠2.5、葡萄糖2.0,再额外添加10%酵母提取物,0.1%麦芽糖,0.1%葡萄糖,调节pH值至7.4。115 ℃高压灭菌20 min。使用前,向培养基中添加10%(体积分数)无菌胎牛血清。
BHI固体培养基则向已配好的液体培养基中添加20 g/L琼脂,115 ℃高压灭菌20 min。使用前,待温度降至50 ℃左右,向其中添加10%无菌脱纤维绵羊血。
菌体裂解液:将活化3代的菌株菌悬液以3%~5%(体积分数)接种于MRS液体培养基中进行扩培,于温度为37 ℃培养18~24 h后,将菌液于高压均质机高压均质(800~1 200 MPa,5次)获得菌体裂解液。
细胞培养基:89%(体积分数)DMEM培养基+10%(体积分数)胎牛血清+1%(体积分数)100×青霉素(100 U/mL)和链霉素(100 μg/mL)混合溶液。
乳杆菌菌悬液:将徳氏乳杆菌DM8909、副干酪乳酪杆菌CCFM1317和格氏乳杆菌QJSWX195M1在MRS液体培养基中活化3代后,按3%(体积分数)的比例转接到MRS培养基中扩大培养,18 h后收集菌泥,用PBS溶液重悬。通过MRS平板计数计算乳杆菌的细菌浓度,调整菌悬液浓度为109 CFU/mL。
阴道加德纳菌菌悬液:将阴道加德纳菌在BHI液体培养基中厌氧培养,活化3代后,按3%(体积分数)的比例转接到BHI液体培养基扩大培养,24 h后收集菌泥,用PBS溶液重悬。通过BHI平板计数计算细菌浓度,调整菌悬液浓度为1010 CFU/mL。
1.4 细胞实验
VK2/E6E7细胞复苏后在37 ℃,5% CO2环境下,于细胞培养基中培养。传代3次后将阴道上皮细胞浓度调整至2.5×105个/mL,于96孔板中每孔接种100 μL细胞悬液,培养24 h。设置对照组、LPS处理组和菌体裂解液处理组,除对照组外,其他组别用1.25 μg/mL的LPS(溶解于无血清细胞培养液中)干预。24 h后用PBS溶液清洗2次,对照组与LPS处理组加入含5%的MRS的细胞培养液;菌体裂解液处理组分别加入含5%徳氏乳杆菌DM8909、副干酪乳酪杆菌CCFM1317、VCQWX4103L1,卷曲乳杆菌QJSWX196M1,约氏乳杆菌QJSWX307M32,鼠李糖乳杆菌FNMGHLBE18L5和格氏乳杆菌QJSWX195M1、QJSWX310M13菌体裂解液的细胞培养液。
1.5 细胞活力检测
干预24 h后,按照CCK-8溶液∶DMEM培养基=1∶9的配比配制溶液,每孔加100 μL后,放入细胞培养箱中按照CCK-8试剂盒说明书进行避光孵育,用酶标仪检测450 nm的OD值,每组至少3次重复。按照公式(1)计算细胞存活率。
细胞存活率![]()
(1)
1.6 动物实验设计
小鼠放置于20~22 ℃,湿度(50±10)%,光照/黑暗周期为12 h的交替循环环境中。所有实验均按照江苏省寄生虫病研究所实验动物护理和使用指南进行,并得到江苏省寄生虫病研究所实验动物护理和使用委员会的批准(IACUC-JIPD—2023102)。1周适应期后,40只小鼠随机分为5组,如图1所示:空白对照组、模型组、实验组——徳氏乳杆菌DM8909组(DM8909),副干酪乳酪杆菌CCFM1317组(CCFM1317)和格氏乳杆菌QJSWX195M1组(QJSWX195M1)。
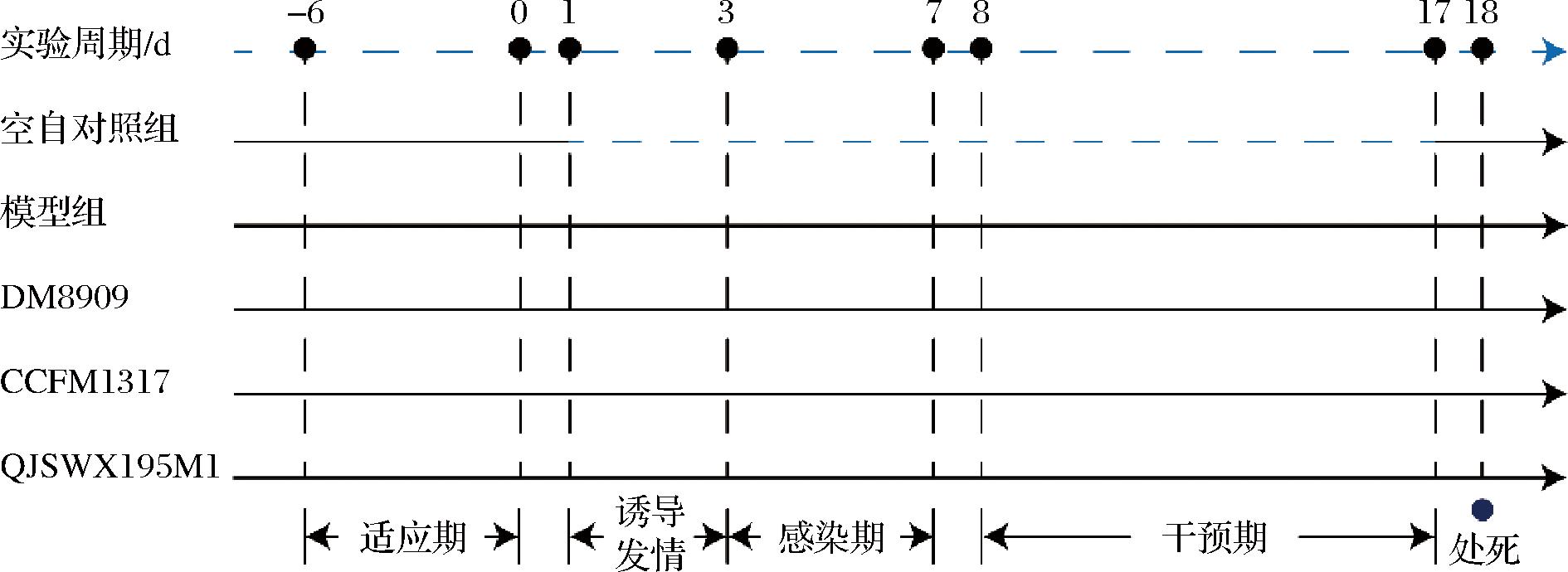
图1 动物实验设计方案流程图
Fig.1 Flow chart of animal experiment design scheme
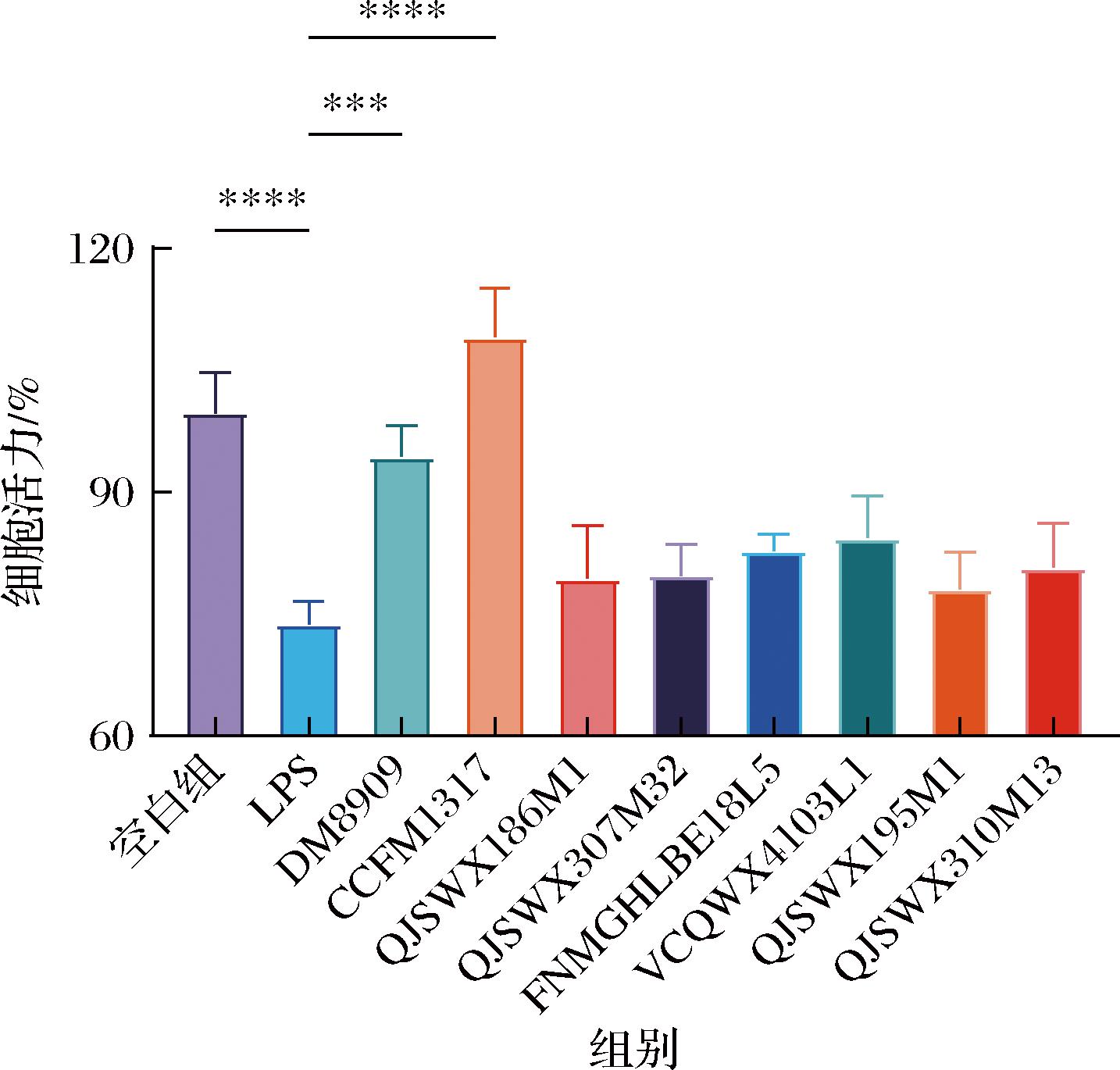
图2 不同细胞裂解液对VK2/E6E7细胞的影响
Fig.2 Effect of different cell lysates on VK2/E6E7 cells
注:与LPS处理组比较,***表示P<0.001,****表示P<0.000 1(下同)。
参考ZHANG等[15]的方法,除空白对照组外,其余小鼠均连续3 d(第1~3天)颈部皮下注射100 μL戊酸雌二醇溶液(5 mg/mL芝麻油)诱导发情。随后连续5 d(第3~7天),用枪头吸取20 μL浓度为1010CFU/mL的GV菌悬液,缓缓注入小鼠阴道内,并将小鼠倒立,停留1~2 min,以防止菌液流出。
将过夜培养的徳氏乳杆菌DM8909、副干酪乳酪杆菌CCFM1317和格氏乳杆菌QJSWX195M1,调节菌悬液浓度为109 CFU/mL。在第8~17天,实验组分别灌胃100 μL乳杆菌悬液,对照组和模型组灌胃等体积PBS溶液。实验结束后(第18天),处死实验小鼠并剥离阴道组织用于病理学分析,以及抗氧化指标的检测等。
1.7 小鼠阴道灌洗液阴道加德纳菌载量检测
在感染期和干预期结束的当天,即第7天和第17天,用300 μL无菌PBS冲洗阴道,收集阴道洗液。根据说明书,使用土壤DNA提取试剂盒提取阴道洗液中的DNA。随后,利用试剂盒进行定量聚合酶链式反应,对阴道加德纳菌数量进行定量分析,根据细菌16S rRNA序列选择引物(表1)。
表1 阴道加德纳菌实时定量PCR检测引物序列
Table 1 Real time quantitative PCR detection primer sequence of GV
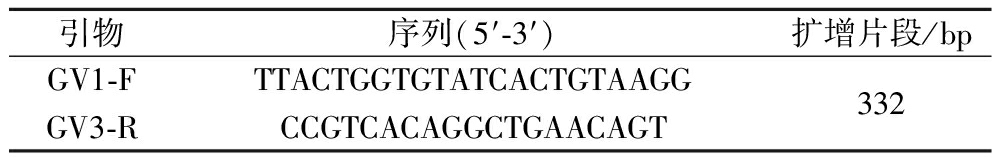
引物序列(5′-3′)扩增片段/bpGV1-FTTACTGGTGTATCACTGTAAGGGV3-RCCGTCACAGGCTGAACAGT332
qPCR反应体系(10 μL)如表2所示:反应程序设置为95 ℃预变性30 s,95 ℃变性5 s和60 ℃退火30 s,反应40次循环。另一个步骤,从65 ℃增加到95 ℃,每5 s增加0.5 ℃,以建立熔化曲线。确定阈值周期值(cycle threshold,CT),并根据标准曲线(对数拷贝数/μL与CT值)计算拷贝数。每个样品测3次。
表2 实时荧光定量PCR反应体系
Table 2 Real time fluorescent quantitative PCR reaction system

组分加样量/μLTaq Pro Universal SYBR qPCR Master Mix5正向引物(10 μmol/L)0.5正向引物(10 μmol/L)0.5模板DNA(10 ng/μL)1双蒸馏水3
1.8 小鼠阴道病理组织分析
剥离小鼠阴道组织,取2~3 mm的片段完全浸泡在4%中性多聚甲醛固定液中进行保存与固定。之后参照LI等[16]的方法,经脱水、包埋和切片后,用苏木精和伊红(hematoxylin eosin stain,HE)染色。切片标本使用切片电子扫描仪,放大20倍进行观察。
1.9 小鼠阴道组织Nrf2含量检测
取20 mg小鼠阴道组织,加入180 μL预冷的PBS对阴道组织进行匀浆处理。在4 ℃下,以3 000 r/min对样品离心15 min,取阴道组织上清液按试剂盒说明书进行Nrf2浓度测定。
1.10 小鼠阴道组织Keap1/Nrf2 mRNA表达检测
使用Trizol试剂提取总RNA,用Nanodrop检测OD260/OD280的数值,用反转录试剂盒完成反转录后,将cDNA样品稀释10倍,用q-PCR试剂盒进行荧光实时定量反应,引物如表3所示。
表3 引物及序列
Table 3 Primers and sequences
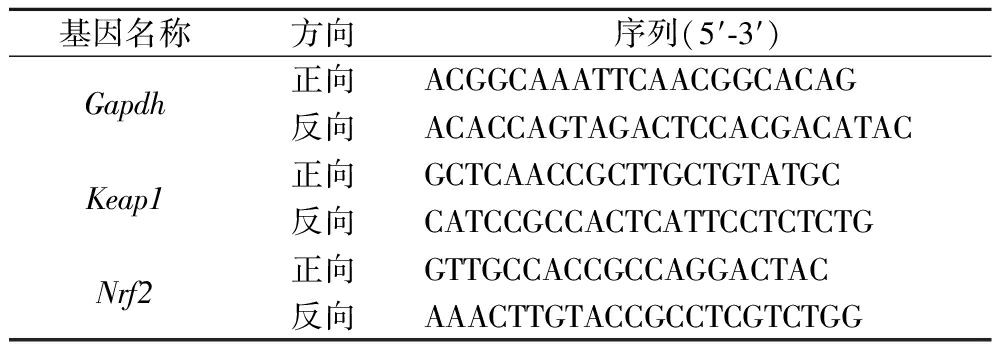
基因名称方向序列(5′-3′)Gapdh正向ACGGCAAATTCAACGGCACAG反向ACACCAGTAGACTCCACGACATACKeap1正向GCTCAACCGCTTGCTGTATGC反向CATCCGCCACTCATTCCTCTCTGNrf2正向GTTGCCACCGCCAGGACTAC反向AAACTTGTACCGCCTCGTCTGG
qPCR反应体系(10 μL)如表4所示,反应程序设置为95 ℃预变性30 s,95 ℃变性10 s和60 ℃退火10 s,反应30次循环。另一个步骤,从65 ℃增加到95 ℃,每5 s增加0.5 ℃,以建立融解曲线,每个样品测3次。
表4 实时荧光定量PCR反应体系
Table 4 Real time fluorescent quantitative PCR reaction system

组分加量/μLTaq Pro Universal SYBR qPCR Master Mix5正向引物(10 μmol/L)0.25正向引物(10 μmol/L)0.25模板DNA(10 ng/μL)1双蒸馏水3.5
1.11 统计学方法
采用Graphpad Prism 9.0软件对数据进行绘图和分析。将实验数据进行正态分布检验,对符合正态分布的数据进行多组数据采用单因素方差分析组间差异性分析,数据以均数±标准误差表示。P<0.05认为有统计学意义。
2 结果与分析
2.1 阴道上皮细胞VK2/E6E7活力
本研究采用体外细胞培养实验,对不同组别细胞活力的变化进行了检测。实验结果表明,经LPS处理后,VK2/E6E7细胞的活力显著下降至73.7%(P<0.000 1)。此外,不同菌体裂解液对细胞活力的影响各不相同,其中部分菌株的裂解液处理能显著提升VK2/E6E7细胞的活力。特别是德氏乳杆菌DM8909与副干酪乳酪杆菌CCFM1317的处理,显著提高了VK2/E6E7细胞的活力,分别达到94.4%(P<0.001)和109.0%(P<0.000 1)。然而,QJSWX195M1的处理仅使细胞活力轻微提升了4.4%,显示出最小的上调程度。
综上所述,本研究发现CCFM1317在体外细胞实验中具有显著上调VK2/E6E7细胞活力的能力,而抗氧化酶活力提升往往使细胞获得增殖优势。故而,CCFM1317显示出其调节阴道组织抗氧化系统的潜在作用。基于此,DM8909被选定为阳性参照菌株,而QJSWX195M1则作为阴性参照,以进一步探讨其在动物模型中的作用。
2.2 小鼠阴道中致病菌载量
在小鼠实验中,观察到小鼠的日常活动表现正常,而建模后,在阴道口可明显观察到扩张和分泌物异常增多的现象。为了评估实验建模的成功与否以及不同菌株干预的效果,本研究采用了GV的载量作为评价指标。如图3-a所示,除空白组外,在第7天,所有实验组别均能检测到约3.7 lg拷贝数/μL的GV载量,且各组之间没有显著的差异,这表明GV已成功定殖于小鼠阴道。
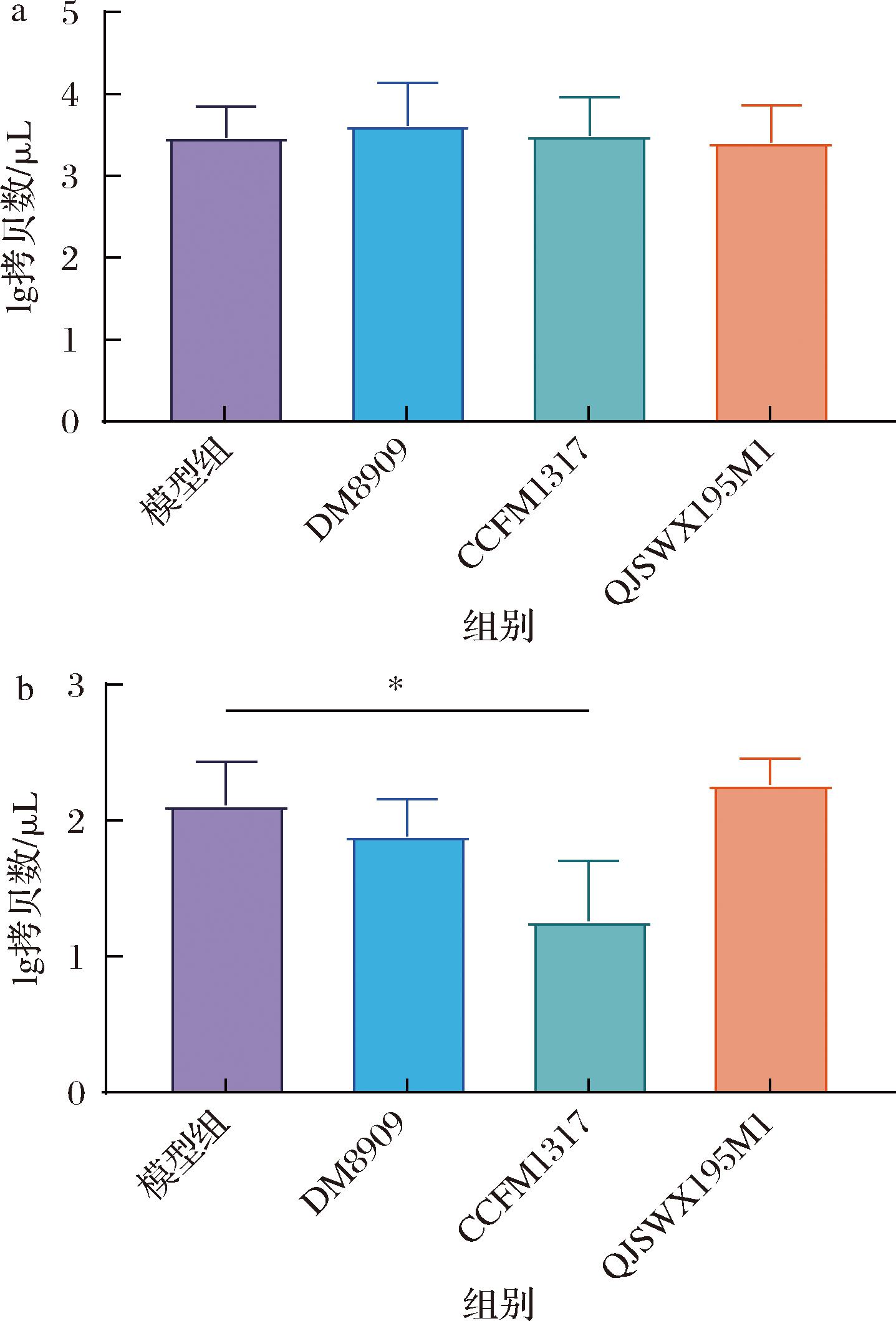
a-第7天阴道加德纳菌定植的情况;b-第17天阴道加德纳菌定植的情况
图3 小鼠阴道中阴道加德纳菌的定植情况
Fig.3 Colonization of GV in mice vagina
注:*表示P<0.05(下同)。
进一步的分析如图3-b所示,在干预期结束后,与模型组相比,仅副干酪乳酪杆菌CCFM1317干预组GV的定植量显著降低(P<0.05),检测到的GV载量为1.3 lg拷贝数/μL,相比模型组下降了40.6%。空白对照组在整个实验期间均未检出GV。这一结果表明,口服副干酪乳酪杆菌CCFM1317能够有效减少GV在小鼠阴道的定殖。
2.3 小鼠阴道组织病理评价
为了评估小鼠阴道组织的炎症情况,本研究采用HE染色对阴道组织进行了显微观察。如图4所示,空白对照组的小鼠阴道上皮光滑且连续,组织结构保持完整,未见明显的炎性细胞浸润。相比之下,模型组阴道黏膜上皮连续性较差,表层细胞出现糜烂并形成孔洞,黏膜下间质出现充血现象,且大量炎性细胞浸润于上皮和间质之中。
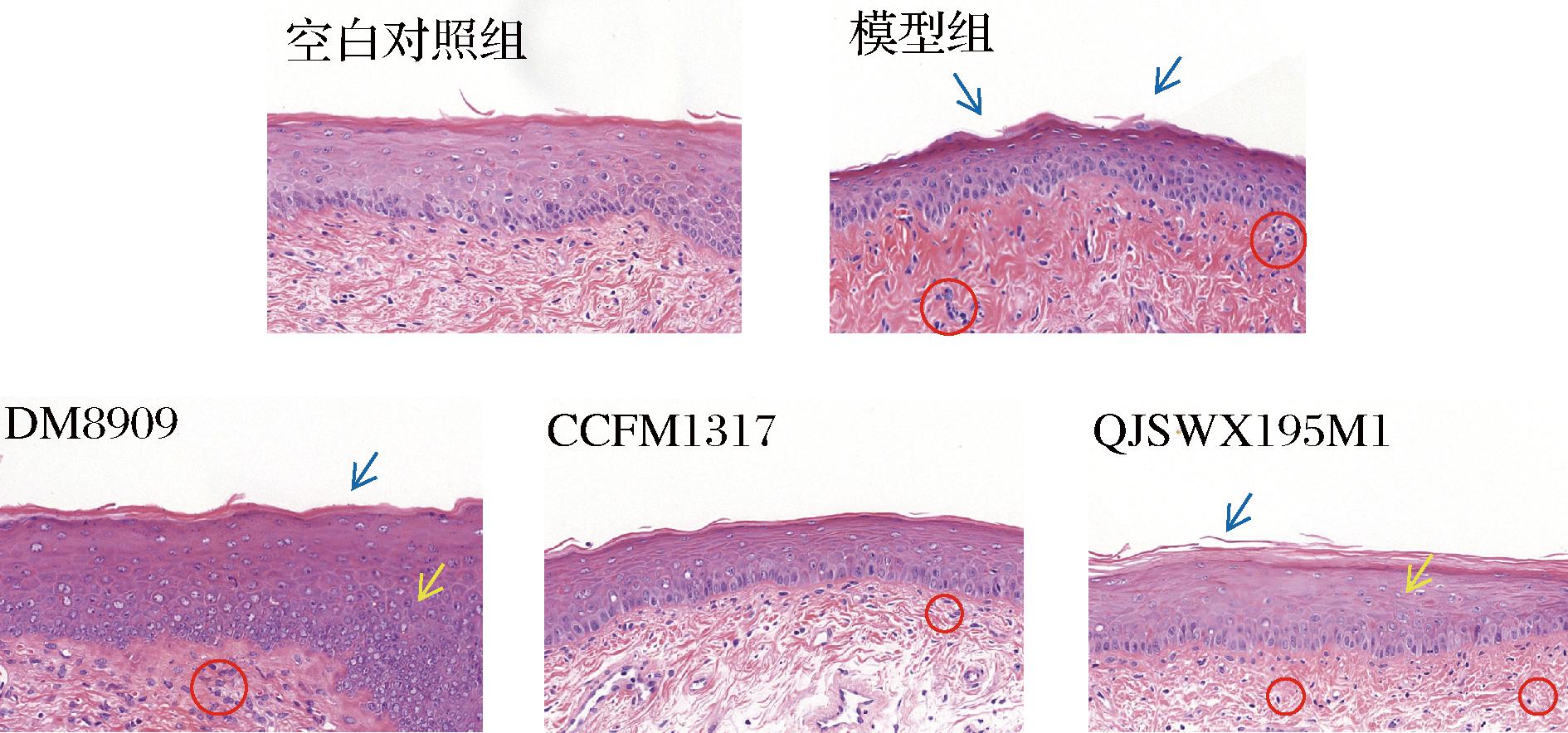
图4 小鼠阴道组织病理学评价图
Fig.4 HE of mice vagina
注:蓝色箭头指示上表皮;黄色箭头指示鳞状上皮;红色圆圈指示炎性细胞。
经过适当的益生菌干预后,德氏乳杆菌DM8909组的炎症细胞浸润数量较模型组减少,但仍有明显的鳞状上皮增生现象。副干酪乳酪杆菌CCFM1317干预组在病理组织层面显示出更为显著的改善效果,如上皮连续性的恢复和炎症细胞浸润的减少。与此同时,格氏乳杆菌QJSWX195M1干预组的上皮松散,鳞状上皮有一定程度的增生,其炎症细胞浸润情况相较于CCFM1317组略显严重。
综上所述,在益生菌干预后,副干酪乳酪杆菌CCFM1317组小鼠阴道组织的恢复情况优于德氏乳杆菌DM8909组和格氏乳杆菌QJSWX195M1组,表明CCFM1317在改善小鼠阴道炎症方面具有更为显著的效果。
2.4 细菌性阴道炎小鼠阴道组织抗氧化相关指标
Keap1蛋白通过与Nrf2蛋白的结合来调控Nrf2的活性。在细胞遭受氧化应激损伤时,Keap1与Nrf2的结合减弱,导致Nrf2蛋白稳定并转位至细胞核内,进而启动一系列抗氧化应激反应基因的转录,从而保护细胞免受氧化应激的损害。在此过程中,Keap1蛋白的表达下调,可以减少Nrf2的泛素化修饰,增强细胞的抗氧化能力。
如图5-a所示,与空白对照组相比,模型组小鼠阴道组织中Nrf2的含量显著下降(P<0.000 1)至20.9 μg/mL。与模型组相比,德氏乳杆菌DM8909和副干酪乳酪杆菌CCFM1317干预后,Nrf2的含量显著上升(P<0.000 1),分别是模型组的3.3倍和1.9倍。如图5-b所示,与空白对照组相比,模型组Keap1的表达显著上升了1.2倍。干预后,CCFM1317显著下调了Keap1的表达,与模型组相比下调了48.6%。如图5-c所示,模型组相比空白对照组,Nrf2的表达下调了89.4%(P<0.001)。与DM8909相比,CCFM1317和QJSWX195M1显著上调了Nrf2的表达(P<0.000 1)。

a-阴道组织Nrf2含量;b-阴道组织Keap1 mRNA水平表达;c-阴道组织Nrf2 mRNA水平表达
图5 阴道组织Keap1/Nrf2信号通路表达
Fig.5 Expression of keap1/nrf2 signaling pathway in vaginal tissue
综上所述,副干酪乳酪杆菌CCFM1317显著调节了阴道组织的Keap1/Nrf2信号通路,这可能是其发挥抗氧化作用的重要机制之一。
3 结论与讨论
CCK-8试剂中的WST-8在电子耦合载体的作用下,可被线粒体内的脱氢酶还原成橙黄色的甲臜染料。生成的甲臜量与活细胞数成正比,因此可以间接测定活细胞数量,反映细胞活力[17]。细胞活力与细胞抗氧化能力密切相关[18],抗氧化酶活力的增高可以使细胞获得增殖优势,而ROS的堆积则具有抑制作用。因此,检测细胞活力可以在一定程度上反映细胞的抗氧化能力。在本研究中,副干酪乳酪杆菌CCFM1317显著提升了细胞活力,推测其对氧化应激的缓解具有潜力。
正常健康女性的阴道菌群以乳杆菌为主,含有大约1010~1011个细菌[19],是阴道抵御病原微生物的第一道防线。GV的强黏附能力使其更容易形成生物膜[20],长时间驻留并分泌毒素,造成细胞损伤,在BV的发病机制中起着关键作用。本研究通过检测小鼠阴道中GV的载量发现,口服副干酪乳酪杆菌CCFM1317可以显著下调GV的载量。同时,分析病理组织切片发现,CCFM1317干预组炎症表征得到改善,上表皮的连续性得到恢复,炎性细胞的浸润程度下降,同时也没有表现出异常的鳞状上皮增生。这表明CCFM1317有助于加速阴道炎病程的结束,而德氏乳杆菌DM8909与格氏乳杆菌QJSWX195M1则并未有效降低GV的载量,改善阴道病理表征。
阴道细胞受损会影响细胞中维持正常氧化还原系统平衡的位点或细胞器,如线粒体,导致氧化呼吸链与电子传递链功能受阻,ROS产生增多,机体的氧化还原系统失衡,造成氧化损伤。Nrf2是参与氧化应激的关键转录因子,Keap1通过与Nrf2结合,抑制其活性并促进其降解。当Nrf2与Keap1解离后,Nrf2会进入细胞核,与抗氧化响应元件结合,促进抗氧化蛋白的表达,从而缓解氧化应激[21]。本研究检测阴道组织Keap1/Nrf2信号通路表达情况发现,CCFM1317可以显著降低Keap1 mRNA的表达水平,上调Nrf2 mRNA的表达水平,并增加Nrf2在阴道中的含量。已有研究表明[22],通过调控Nrf2/HO-1信号通路,增强抗氧化酶表达,可以增强清除ROS的能力,抑制IL-1β诱导的细胞凋亡。GE等[23]发现植物乳杆菌NJAU-01可以提升包括SOD在内的抗氧化酶活性,降低氧化应激产物丙二醛的含量,从而提高小鼠抗氧化能力。ZHANG等[24]发现发酵乳杆菌JX306可显著降低丙二醛水平,提高血清、肾脏和肝脏谷胱甘肽过氧化物酶活性和总抗氧能力。以上研究结果与本研究的结果一致,因此,本研究认为CCFM1317可以通过激活Keap1/Nrf2信号通路,增加Nrf2含量,进一步调控抗氧化酶系统的表达,缓解小鼠BV炎症,加速病程结束。
综上所述,与其他菌株相比,CCFM1317可以更好地提升细胞活力,表现出更强的抗氧化潜力。BV小鼠口服副干酪乳酪杆菌CCFM1317后,相比DM8909和QJSWX195M1,阴道GV的载量显著下降,炎性细胞浸润、上皮破碎以及鳞状上皮增生的情况得到更好的改善。与此同时,CCFM1317可显著降低阴道组织Keap1 mRNA的表达水平,同时上调Nrf2 mRNA的表达水平及Nrf2的含量,这对BV小鼠炎症的改善具有重要意义。然而,口服CCFM1317如何经肠道在阴道发挥作用的具体途径仍有待进一步探究。
[1] ABOU CHACRA L, FENOLLAR F, DIOP K.Bacterial vaginosis:What do we currently know?[J].Frontiers in Cellular and Infection Microbiology, 2022, 11:672429.
[2] BILARDI J, WALKER S, MOONEY-SOMERS J, et al.Women’s views and experiences of the triggers for onset of bacterial vaginosis and exacerbating factors associated with recurrence[J].PLoS One, 2016, 11(3):e0150272.
[3] CASTRO J, FRANÇA A, BRADWELL K R, et al.Comparative transcriptomic analysis of Gardnerella vaginalis biofilms vs.planktonic cultures using RNA-seq[J].NPJ Biofilms and Microbiomes, 2017, 3:3.
[4] AGARWAL K, ROBINSON L S, AGGARWAL S, et al.Glycan cross-feeding supports mutualism between Fusobacterium and the vaginal microbiota[J].PLoS Biology, 2020, 18(8):e3000788.
[5] PAWLEY D C, DIKICI E, DEO S K, et al.Rapid point-of-care test kit for bacterial vaginosis:Detection of vaginolysin and clue cells using paper strips and a smartphone[J].Analytical Chemistry, 2022, 94(33):11619-11626.
[6] WANG X D, ZHANG G Y, DASGUPTA S, et al.ATF4 protects the heart from failure by antagonizing oxidative stress[J].Circulation Research, 2022, 131(1):91-105.
[7] LING Z X, LIU X, CHEN W G, et al.The restoration of the vaginal microbiota after treatment for bacterial vaginosis with metronidazole or probiotics[J].Microbial Ecology, 2013, 65(3):773-780.
[8] CHEN L, WANG F, QU S, et al.Therapeutic potential of perillaldehyde in ameliorating vulvovaginal candidiasis by reducing vaginal oxidative stress and apoptosis[J].Antioxidants, 2022, 11(2):178.
[9] AABED K, SHAFI BHAT R, MOUBAYED N, et al.Ameliorative effect of probiotics (Lactobacillus paracaseii and Protexin®) and prebiotics (Propolis and bee pollen) on clindamycin and propionic acid-induced oxidative stress and altered gut microbiota in a rodent model of autism[J].Cellular and Molecular Biology, 2019, 65(1):1-7.
[10] WANG M Q, FENG X Y, ZHAO Y, et al.Indole-3-acetamide from gut microbiota activated hepatic AhR and mediated the remission effect of Lactiplantibacillus plantarum P101 on alcoholic liver injury in mice[J].Food &Function, 2023, 14(23):10535-10548.
[11] FENG T, WANG J.Oxidative stress tolerance and antioxidant capacity of lactic acid bacteria as probiotic:A systematic review[J].Gut Microbes, 2020, 12(1):1801944.
[12] BAIRD L, YAMAMOTO M.The molecular mechanisms regulating the KEAP1-NRF2 pathway[J].Molecular and Cellular Biology, 2020, 40(13):e00099-20.
[13] YAMAMOTO M, KENSLER T W, MOTOHASHI H.The KEAP1-NRF2 system:A thiol-based sensor-effector apparatus for maintaining redox homeostasis[J].Physiological Reviews, 2018, 98(3):1169-1203.
[14] LONG X Y, SUN F J, WANG Z Y, et al.Lactobacillus fermentum CQPC08 protects rats from lead-induced oxidative damage by regulating the Keap1/Nrf2/ARE pathway[J].Food &Function, 2021, 12(13):6029-6044.
[15] ZHANG Q X, CHENG Q H, CUI S M, et al.Inhibitory effect of Lactobacillus gasseri CCFM1201 on Gardnerella vaginalis in mice with bacterial vaginosis[J].Archives of Microbiology, 2022, 204(6):315.
[16] LI W Q, WU D W, TAN J W, et al.A gene-activating skin substitute comprising PLLA/POSS nanofibers and plasmid DNA encoding ANG and bFGF promotes in vivo revascularization and epidermalization[J].Journal of Materials Chemistry B, 2018, 6(43):6977-6992.
[17] NI M W, ZHOU J, ZHU Z H, et al.Shikonin and cisplatin synergistically overcome cisplatin resistance of ovarian cancer by inducing ferroptosis via upregulation of HMOX1 to promote Fe2+ accumulation[J].Phytomedicine, 2023, 112:154701.
[18] POULOSE S M, MILLER M G, SCOTT T, et al.Nutritional factors affecting adult neurogenesis and cognitive function[J].Advances in Nutrition, 2017, 8(6):804-811.
[19] CHEN C, SONG X L, WEI W X, et al.The microbiota continuum along the female reproductive tract and its relation to uterine-related diseases[J].Nature Communications, 2017, 8(1):875.
[20] ZHANG K D, LU M Y, ZHU X X, et al.Antibiotic resistance and pathogenicity assessment of various Gardnerella sp.strains in local China[J].Frontiers in Microbiology, 2022, 13:1009798.
[21] TOSSETTA G, FANTONE S, MONTANARI E, et al.Role of NRF2 in ovarian cancer[J].Antioxidants (Basel), 202, 11(4):663.
[22] CHEN B H, HE Q, CHEN C Y, et al.Combination of curcumin and catalase protects against chondrocyte injury and knee osteoarthritis progression by suppressing oxidative stress[J].Biomedicine &Pharmacotherapy, 2023, 168:115751.
[23] GE Q F, YANG B, LIU R, et al.Antioxidant activity of Lactobacillus plantarum NJAU-01 in an animal model of aging[J].BMC Microbiology, 2021, 21(1):182.
[24] ZHANG D I, LI C, SHI R R, et al.Lactobacillus fermentum JX306 restrain D-galactose-induced oxidative stress of mice through its antioxidant activity[J].Polish Journal of Microbiology, 2020, 69(2):205-215.