牛磺酸,化学名为2-氨基乙磺酸,又称牛黄酸、牛胆酸,是一种以游离状态存在的含硫β-氨基酸,分子式C2H7NSO3,分子质量125.15,广泛存在于动物机体中,因其最初由牛黄中分离得到,故而得名[1]。牛磺酸具有多种生理药理活性,如抗炎、抗氧化、解除肝脏毒素、调节细胞内离子水平、提高机体免疫力等[2]。人体可进行自身生物合成牛磺酸,主要途径是蛋氨酸和半胱氨酸代谢的中间产物半胱亚磺酸经半胱亚磺酸脱羧酶(cysteine sulfonic acid decarboxylase,CSAD)脱羧成亚牛磺酸,再经氧化成牛磺酸[3]。半胱亚磺酸脱羧酶是该反应过程中的关键因素,人类体内半胱亚磺酸脱羧酶的活性较其他哺乳动物低,尤其是新生儿和老龄群体自身合成牛磺酸的能力较弱,因此需从饮食中补充牛磺酸以满足机体的正常生理功能需求。作为一种营养强化剂,牛磺酸被广泛应用于奶粉、含乳饮料、功能性饮料及保健食品等多种类型食品中[4]。牛磺酸对生物体的生理活动影响具有双面性,摄入适量的牛磺酸可保障与之相关的各项生理活动正常进行,但摄入过量的牛磺酸则会抑制机体对其他种类营养素的吸收,进而导致机体的营养失衡,因此牛磺酸的添加使用量需得到严格把控。与牛磺酸含量检测相关的文献层出不穷,但针对特殊医学用途配方食品(特医食品),尤其是特殊医学用途配方奶粉(特医奶粉)中牛磺酸含量测定的研究还为数不多。
特医奶粉依照水解程度主要分为部分水解、深度水解和全氨基酸水解配方奶粉3种类型。在不影响蛋白质营养的前提下,特医奶粉中原料奶的蛋白质被部分或完全水解,进而降低了牛奶蛋白对婴幼儿的潜在致敏性[5]。但在此过程中产生的大量氨基酸会对待测样本中牛磺酸的定量测定产生干扰影响。目前牛磺酸测定的方法主要有高效液相色谱法[6]、高效液相色谱-串联质谱法[7]、高效液相色谱-高分辨质谱法[8]、氨基酸分析仪法[9]、分光光度法[10]、近红外光谱法[11]、核磁共振法[12]等。其中,高效液相色谱法和高效液相色谱-串联质谱法应用相对广泛。但受牛磺酸分子中缺少能够产生紫外特征吸收的共轭双键的生色团结构的限制,直接利用高效液相色谱法的检测灵敏度较低;而高效液相色谱-串联质谱法则存在着设备昂贵、操作费时且重复性不佳的缺点。因此针对牛磺酸的检测,大多数色谱分析方法均会在进行衍生之后上机测定。文献报道的用于牛磺酸衍生化的试剂主要有邻苯二甲醛(ortho phthalaldehyde,OPA)[13]、2,4-二硝基氟苯(2,4-dinitrofluorobenzene,NDFB)[14]、异硫氰酸苯酯(phenyl isothiocyanate,PITC)[15]、丹磺酰氯(dansyl chloride,dansyl-Cl)[16]等。在碱性环境和还原剂存在的条件下,OPA与牛磺酸反应生成取代的异吲哚产物,该过程反应灵敏,响应强度高,但对反应时间要求严格。NDFB与牛磺酸反应需避光进行且其水解产物对测定有干扰。PITC具有挥发性,需加入过量试剂参与反应,反应后剩余的试剂需利用真空蒸发装置除去,且该试剂毒性较强,衍生产物也不太稳定。dansyl-Cl作为一种荧光试剂,与牛磺酸反应迅速,灵敏度高,但该反应的衍生副产物会对测定结果形成干扰,需在反应一定时间后使用盐酸甲胺终止反应[17]。
本方法以GB 5009.169—2016《食品安全国家标准 食品中牛磺酸的测定》第一法OPA柱后衍生高效液相色谱法为基础,利用高效液相色谱仪的自动进样器进行进样程序设定,严格控制衍生反应的时间和条件。使用单因素法对OPA用量、衍生时间、流动相比例、流速、混合次数进行优化,并利用优化后的实验条件对两种特医奶粉中的牛磺酸含量进行了测定分析,同时还考察了测定方法的精密度、重复性和加标回收率。本研究通过建立特殊医学用途奶粉中牛磺酸测定的柱前衍生-高效液相色谱法,为特殊医学用途奶粉中牛磺酸含量的检测提供参考。
1 材料与方法
1.1 材料与试剂
牛磺酸标准品(纯度≥99%,CAS:107-35-7),SIGMA-ALDRICH公司;两款特殊医学用途配方奶粉(安儿宁能恩婴儿无乳糖配方奶粉、早启能恩早产/低出生体重婴儿配方奶粉),瑞士雀巢产品有限公司;甲醇(梯度级),德国Merck公司;OPA(纯度>99%),南京都莱生物技术有限公司;亚铁氰化钾、乙酸锌、硼酸、NaOH、巯基乙醇(均为分析纯),国药集团化学试剂有限公司;试验用水为自制超纯水。
1.2 仪器与设备
Agilent 1260高效液相色谱仪(配可变波长紫外检测器),美国安捷伦科技公司;MS403TS/02电子分析天平,梅特勒-托利多仪器(上海)有限公司;KQ-800DE超声波清洗仪,昆山市超声仪器有限公司;Milli-Q Integral 5超纯水系统,德国默克公司。
1.3 实验方法
1.3.1 溶液配制
牛磺酸标准液(1 mg/mL):准确称取0.1 g牛磺酸标准品,超纯水溶解并定容至100 mL。硼酸钠缓冲液:准确称取2.48 g硼酸和1.41 g NaOH,定容至100 mL容量瓶中备用。OPA衍生试剂:准确称取0.1 g OPA,用10 mL甲醇溶解后加入0.1 mL巯基乙醇,用前述配制的硼酸钠缓冲液定容至100 mL。沉淀剂I和沉淀剂II:分别准确称取亚铁氰化钾15 g和乙酸锌30 g,加水溶解后各自定容至100 mL。
1.3.2 牛磺酸分析方法的建立
所有反应液经0.45 μm微孔滤膜过滤后迅速放置于样品盘并依照设定程序完成自动进样。以衍生物紫外吸收峰的峰形和峰面积为对应指标,分别对衍生剂用量、衍生时间和流动相比例等参数进行优化。初始色谱条件为:Agilent C18色谱柱;流动相:V(甲醇+乙腈)∶V(水)=20∶80(在本研究中甲醇和乙腈体积保持相同);流速0.6 mL/min;反应液在自动进样器中的混合次数及混合完成后等待时长:6次、0.1 min;进样体积10 μL;检测波长335 nm。
1.3.3 牛磺酸标准曲线的绘制
取10 mL牛磺酸标准液定容至100 mL,配制得到0.1 mg/mL的牛磺酸中间液。取适量体积中间液依次稀释成50、30、20、10、5、1、0.5、0.1 μg/mL 8个质量浓度梯度,依照优化后的实验参数上机测定。以牛磺酸浓度作为横坐标,衍生物吸收峰面积作为纵坐标绘制标准曲线。
1.3.4 精密度测试
选择3种质量浓度的牛磺酸标准液(1、20、50 μg/mL),依照优化后的实验参数上机测定,每个标准液分别测定6次,并计算峰面积的平均值,标准偏差和相对标准偏差(relative standard deviation,RSD)。
1.3.5 样品中牛磺酸含量测定
准确称取待测样品2 g于50 mL离心管中,加入超纯水涡旋均匀溶解后超声波辅助提取(800 W,10 min),加入亚铁氰化钾溶液和乙酸锌溶液各1 mL,涡旋混合定容至50 mL后离心(5 000 r/min,10 min),取上清液过0.45 μm微孔滤膜,依照优化后的实验参数上机测定。
1.3.6 重复性测试
准确称取两种待测样品各6份,经1.3.5节方法处理后按照优化后的实验参数上机测定,并计算峰面积的平均值,标准偏差和RSD。
1.3.7 加标回收率测试
准确称取两种待测样品各10份,一份用于测定本底值,将剩余9份样品分为3份并向其中加入三水平的牛磺酸标准液,经1.3.5节处理后上机测定。分别计算2种样品的加标回收率及回收率的标准偏差和RSD。
1.4 数据处理
采用Excel 2019,SPSS 22.0和Origin 2019b对测定所得数据进行分析处理和作图。
2 结果与分析
2.1 HPLC条件的优化
2.1.1 衍生试剂使用量
衍生剂使用量对牛磺酸检测结果有重要影响,衍生剂使用量不足,会导致反应进行不完全,影响测定结果的准确定性;衍生试剂过量则会影响吸收峰形。本实验固定流动相比例为20∶80,流速0.6 mL/min,混合次数6次,等待时间0.1 min,进样体积10 μL,调整了衍生试剂的进样量(5、10、20、30、40、50 μL),综合考虑峰面积和峰形(图1-a),最终确定衍生剂使用量为30 μL。
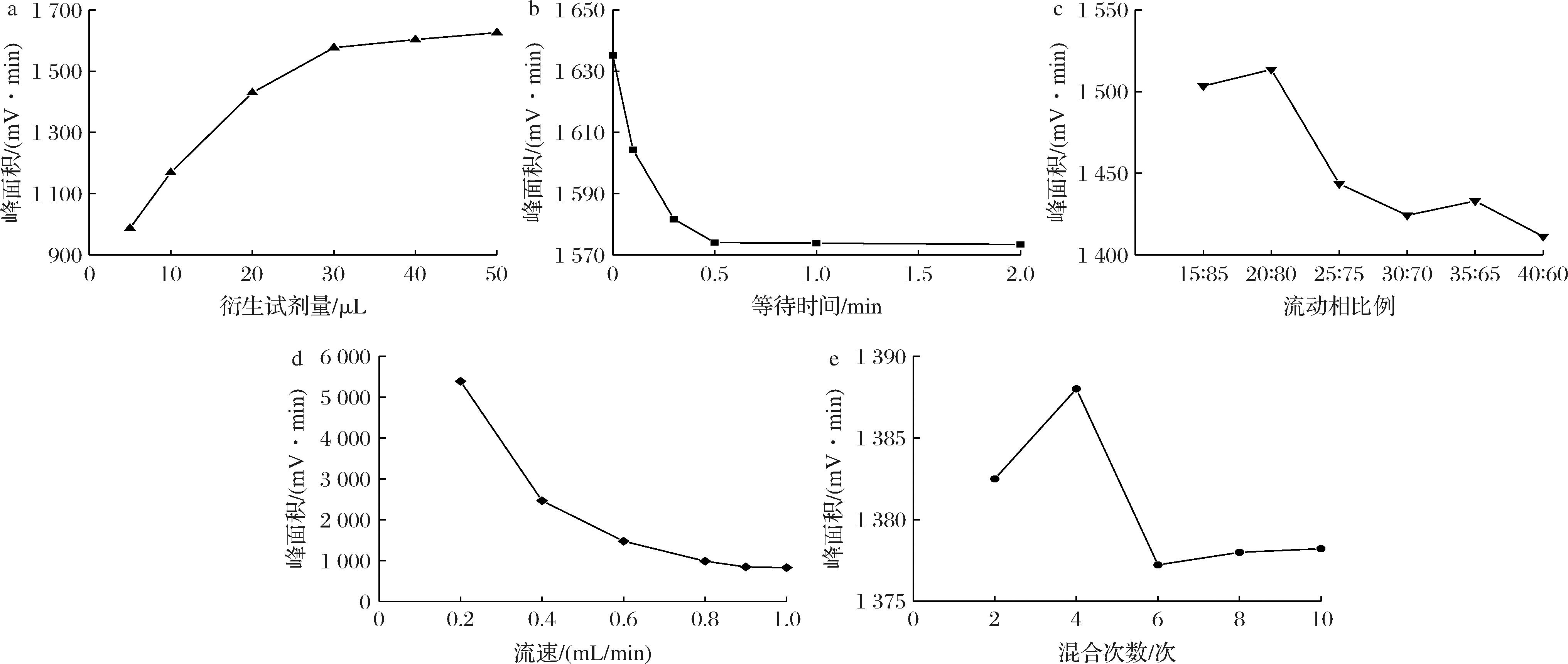
a-衍生试剂量;b-等待时间;c-流动相比例;d-流速;e-混合次数
图1 色谱条件优化
Fig.1 Optimization of chromatographic conditions
2.1.2 等待时间
固定流动相比例为20∶80,流速0.6 mL/min,混合次数6次,进样体积10 μL,衍生试剂30 μL,调整待测样品与衍生试剂在进样环中混合后的等待时间(0、0.1、0.3、0.5、1、2 min),结果显示峰面积随等待时间的延长而减小(图1-b)。这与柳小英等[18]的研究结论相一致,可能是由于牛磺酸与衍生试剂OPA反应迅速,灵敏度高,但衍生产物不稳定,会随着衍生时间的延长而分解,进而导致峰面积减小。因此,确定等待时间为0 min,即待测样品与衍生试剂混合后直接进样测定。
2.1.3 流动相比例
固定流速0.6 mL/min,混合次数6次,进样体积10 μL,衍生试剂30 μL,待测样品与衍生试剂混合后直接进样,调整流动相比例(15∶85、20∶80、25∶75、30∶70、35∶65、40∶60)。随流动相比例的改变,保留时间呈现缩短趋势,吸收峰面积和峰形也随之改变。在流动相比例为20∶80时得到最大的峰面积和半峰宽最窄的峰形(图1-c)。因此确定流动相比例为20∶80。
2.1.4 流速
固定流动相比例为20∶80,混合次数6次,进样体积10 μL,衍生试剂30 μL,待测样品与衍生试剂混合后直接进样,调整流动相流速(0.2、0.4、0.6、0.8、0.9、1.0 mL/min)后发现,随着流速的降低,保留时间延长,峰形变宽;流速过快则易导致目标物质检测不完全,峰面积减少(图1-d)。该结果和秦梦然等[19]的研究结论相吻合。综合考虑峰面积和保留时间,由此确定流速为0.6 mL/min。
2.1.5 混合次数
固定流动相比例为20∶80,流速0.6 mL/min,进样体积10 μL,衍生试剂30 μL,待测样品与衍生试剂被进样针吸入样品环中,由进样装置以空气为介质驱动混合,完成设定的混合次数后进样测定。探究不同混合次数(2、4、6、8、10次)对牛磺酸检测的影响。结果显示,混合次数对峰面积和峰形影响较小(图1-e),因牛磺酸与OPA反应灵敏,结合峰面积选定混合6次后进样测试。
2.2 牛磺酸标准曲线
在上述最优实验条件下,牛磺酸标准品及2种样品中牛磺酸的衍生色谱如图2所示。测定不同浓度的牛磺酸标准溶液记录峰面积,分别以牛磺酸标准溶液浓度和吸收峰面积作为横坐标和纵坐标绘图,得到牛磺酸标准曲线如图3所示。牛磺酸质量浓度在0.5~50 μg/mL时,牛磺酸浓度与峰面积呈现良好的线性关系,拟合方程为y=100.034 2x-2.333 5,R2=0.999 9。以3倍信噪比对应方法的检出限,经计算方法检出限为0.58 mg/100 g;以10倍信噪比对应方法的定量限,经计算方法定量限为2 mg/100 g。
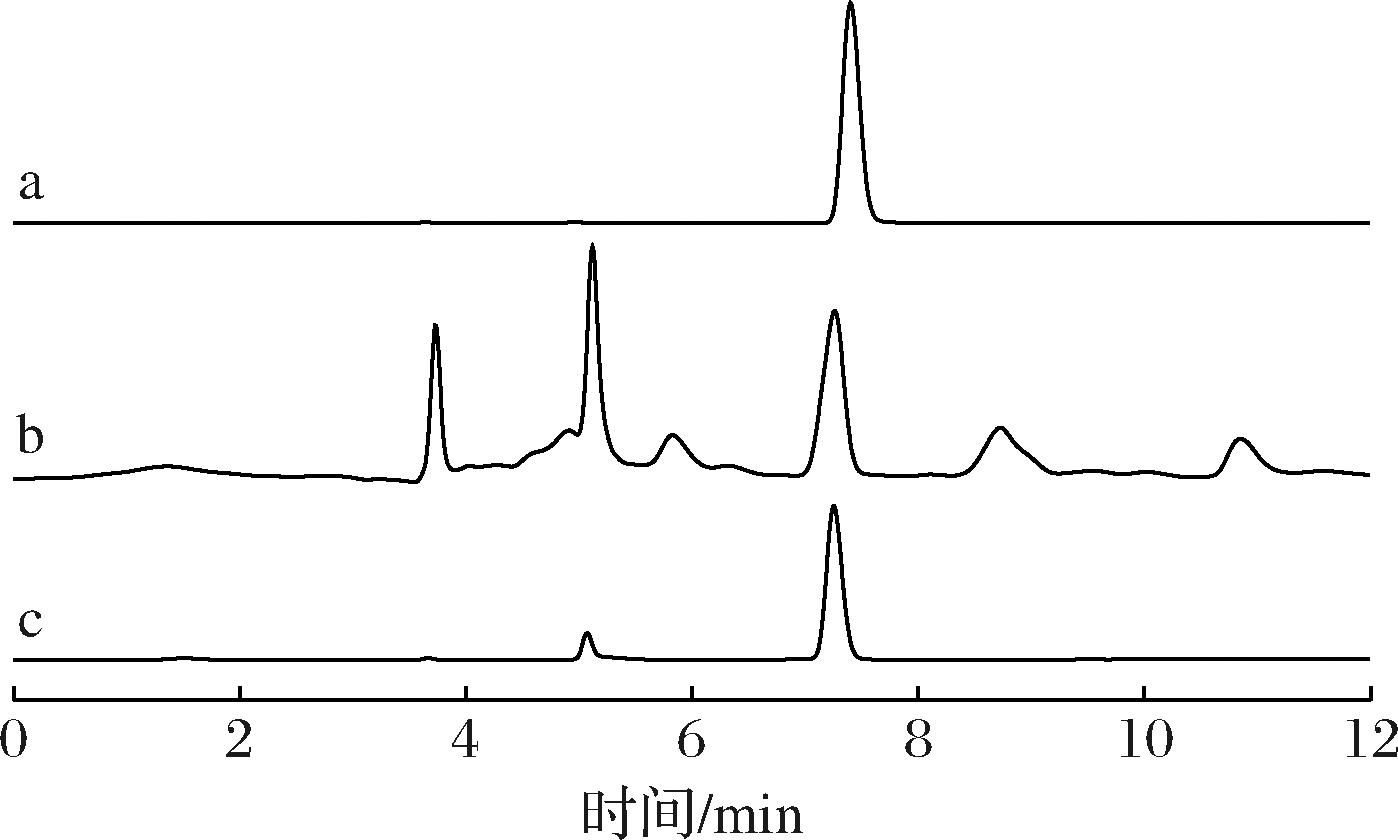
a-牛磺酸标准品;b-早启能恩;c-安儿宁能恩
图2 牛磺酸标准品及样品中牛磺酸色谱图
Fig.2 Chromatogram of taurine standard and samples
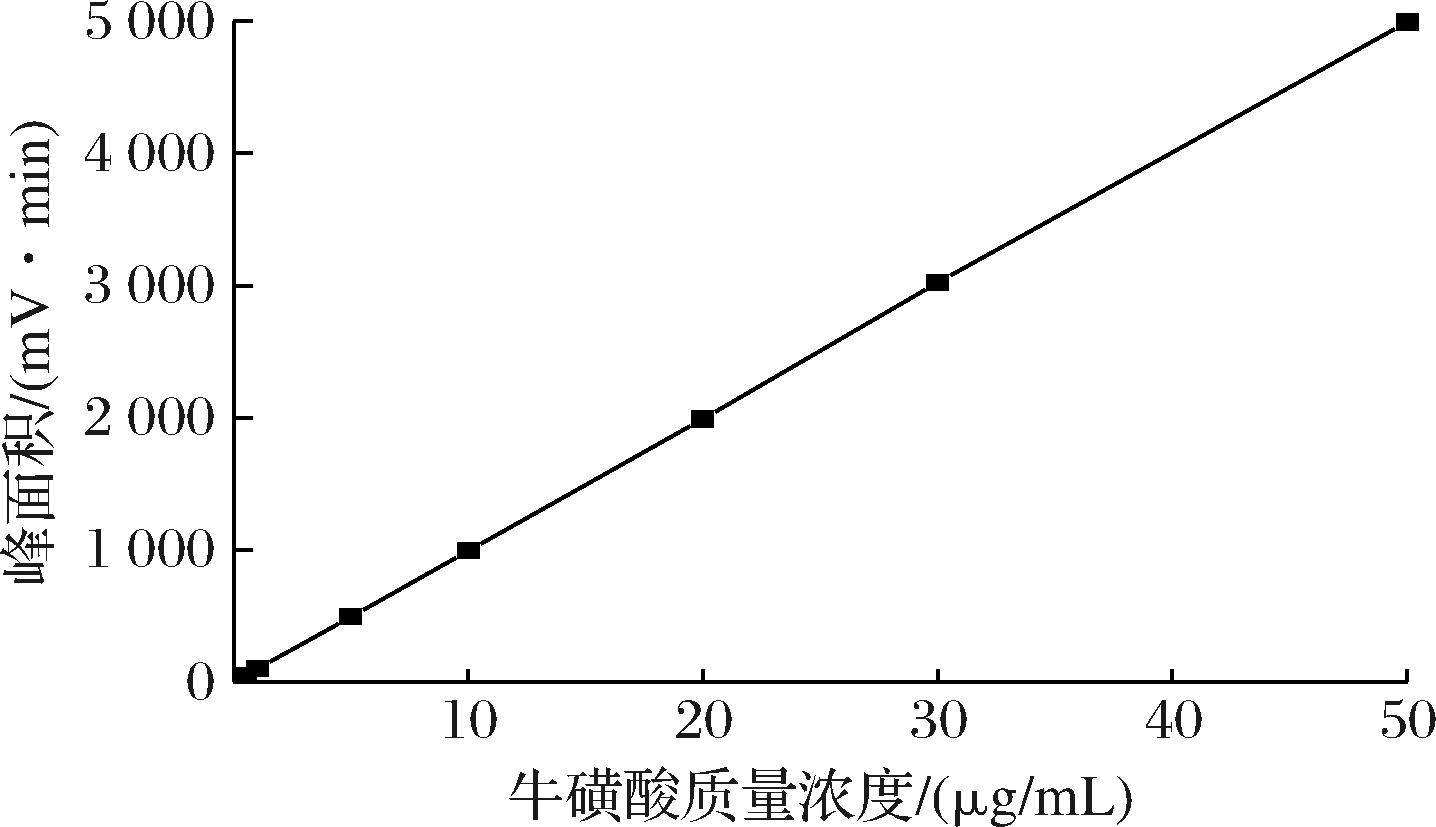
图3 牛磺酸标准曲线
Fig.3 Standard curve of taurine
2.3 精密度测定
选择3种质量浓度的牛磺酸标准液(1、20、50 μg/mL)上机测试,每一样品平行测定6次,所得结果如表1所示。3种不同浓度牛磺酸标样的精密度测定结果的RSD分别为0.75%、0.63%和0.08%,说明该柱前衍生-程序进样测定牛磺酸含量的方法精密度高。
表1 不同浓度牛磺酸样品精密度实验(n=6)
Table 1 Precision of taurine at different concentrations(n=6)
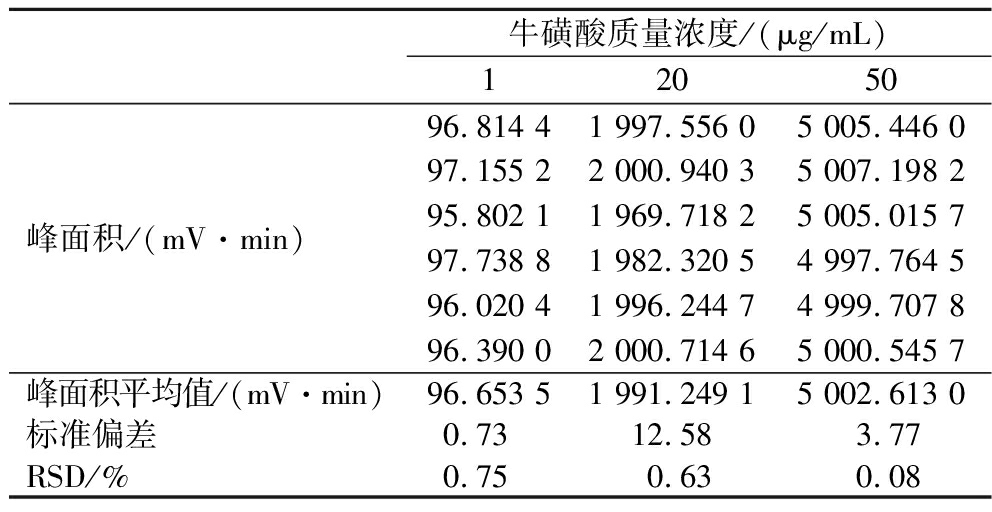
牛磺酸质量浓度/(μg/mL)12050峰面积/(mV·min)96.814 41 997.556 05 005.446 097.155 22 000.940 35 007.198 295.802 11 969.718 25 005.015 797.738 81 982.320 54 997.764 596.020 41 996.244 74 999.707 896.390 02 000.714 65 000.545 7峰面积平均值/(mV·min)96.653 51 991.249 15 002.613 0标准偏差0.7312.583.77RSD/%0.750.630.08
2.4 重复性测定
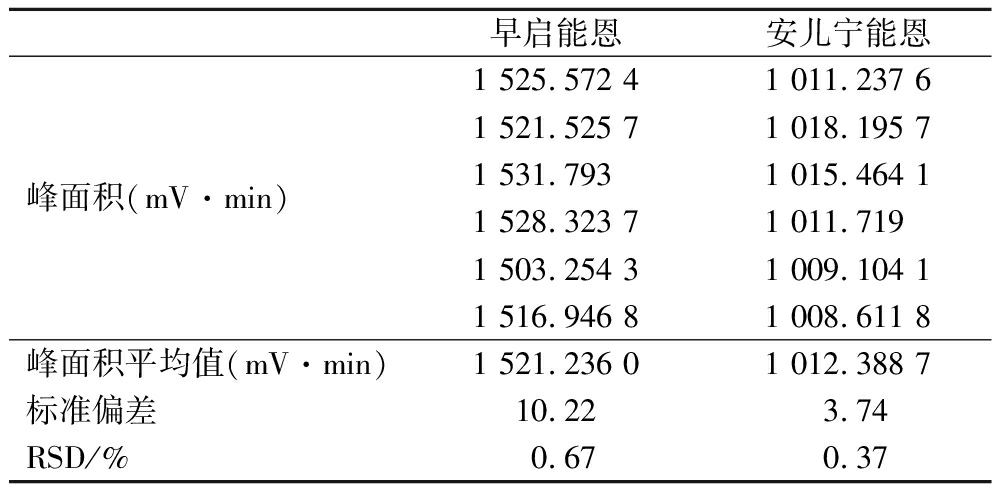
准确称取2种待测样品各6份,按照进行样品处理后上机测定。测定结果如表2所示。同种样品测定得到的峰面积相差不大,则说明在实验过程中出现的误差较小,说明该方法的可信度和有效性高。2种样品中,早启能恩峰面积平均值为1 521.236 0,RSD为0.67%;安儿宁能恩峰面积平均值为1 012.388 7,RSD为0.37%。
表2 重复性实验结果(n=6)
Table 2 Test results of repeatability (n=6)
早启能恩安儿宁能恩峰面积(mV·min)1 525.572 41 011.237 61 521.525 71 018.195 71 531.7931 015.464 11 528.323 71 011.7191 503.254 31 009.104 11 516.946 81 008.611 8峰面积平均值(mV·min)1 521.236 01 012.388 7标准偏差10.223.74RSD/%0.670.37
2.5 加标回收率实验测定
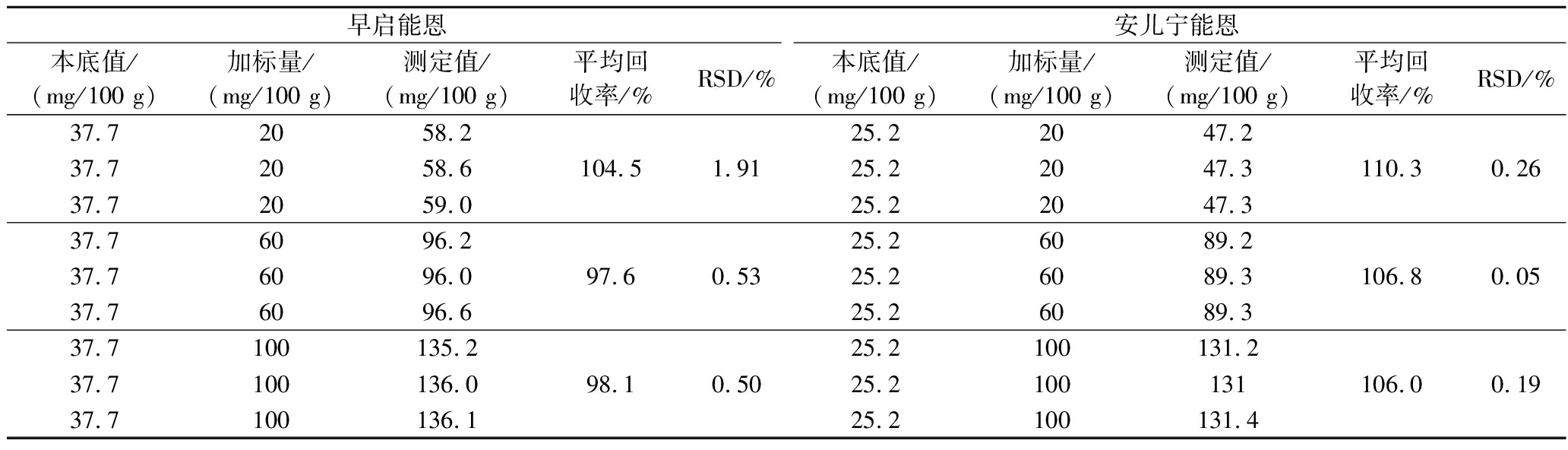
向2种待测特医奶粉中分别加入3种不同浓度的牛磺酸标准液,每种浓度水平测定3次并计算回收率,测定结果如表3所示。早启能恩的平均回收率为97.6%~104.5%,RSD为0.50%~1.91%;安儿宁能恩的平均回收率为106.0%~110.3%,RSD为0.05%~0.26%。证明利用本研究所使用的方法对2种特殊医学用途奶粉中牛磺酸含量进行测定具有很好的适用性和可行性。
表3 加标回收率实验结果
Table 3 Test results of spiked recovery rate
早启能恩安儿宁能恩本底值/(mg/100 g)加标量/(mg/100 g)测定值/(mg/100 g)平均回收率/%RSD/%本底值/(mg/100 g)加标量/(mg/100 g)测定值/(mg/100 g)平均回收率/%RSD/%37.72058.237.72058.637.72059.0104.51.9125.22047.225.22047.325.22047.3110.30.2637.76096.237.76096.037.76096.697.60.5325.26089.225.26089.325.26089.3106.80.0537.7100135.237.7100136.037.7100136.198.10.5025.2100131.225.210013125.2100131.4106.00.19
3 结论与讨论
本研究建立了一种利用自动进样器设定程序进样,OPA为衍生试剂的柱前衍生高效液相色谱法测定特殊医学用途奶粉中牛磺酸含量的方法。通过控制变量法确定了实验条件,并对测定方法的精密度、两种奶粉样品中牛磺酸含量测定的重复性和加标回收率进行了考察。该方法精密度高、重复性稳定、回收率良好、反应条件温和且操作性强,适用于特殊医学用途奶粉中牛磺酸含量的测定。
[1] 陈丽丽, 白春清, 袁美兰, 等.高效液相色谱法测定鱼露中章鱼胺和牛磺酸[J].食品与发酵工业, 2020, 46(2):261-265.CHEN L L, BAI C Q, YUAN M L, et al.Determination of octopamine and taurine in fish sauce by HPLC[J].Food and Fermentation Industries, 2020, 46(2):261-265.
[2] ALI OMER M M, ALI OMAR M M, ABDELAZIZ M A, et al.Liquid chromatographic and spectrophotometric determination of taurine in energy drinks based on O-phthalaldehyde-sulfite derivatization[J].Journal of Food Chemistry &Nanotechnology, 2019, 5(1):1-7.
[3] 谢昭鹏, 姚昱锟, 刘斌雄, 等.牛磺酸提取及检测方法的研究进展[J].食品工业科技, 2019, 40(24):323-331.XIE Z P, YAO Y K, LIU B X, et al.Research progress on extraction and detection methods of taurine[J].Science and Technology of Food Industry, 2019, 40(24):323-331.
[4] 徐彬, 李飞, 赵海萍, 等.柱前衍生法测定功能性饮料与口服液中的牛磺酸[J].食品研究与开发, 2019, 40(10):145-151.XU B, LI F, ZHAO H P, et al.Determination of taurine in energy drinks and oral liquids by pre-column derivatization[J].Food Research and Development, 2019, 40(10):145-151.
[5] 卞华, 翁史昱, 王亮.基于二维液相色谱体系分析特殊医学用途奶粉中的牛磺酸含量[J].中国食品学报, 2022, 22(3):288-296.BIAN H, WENG S Y, WANG L.Analysis on the taurine in the milk powder with special medical purpose based on the two-dimensional liquid chromatography system[J].Journal of Chinese Institute of Food Science and Technology, 2022, 22(3):288-296.
[6] MEHDINIA A, ROSTAMI S, DADKHAH S, et al.Simultaneous screening of homotaurine and taurine in marine macro-algae using liquid chromatography-fluorescence detection[J].Journal of the Iranian Chemical Society, 2017, 14(10):2135-2142.
[7] GILL B D, WOOD J E.Rapid analysis of taurine in infant formula and adult nutritionals by hydrophilic interaction liquid chromatography-mass spectrometry[J].Journal of AOAC International, 2023, 106(2):384-388.
[8] 张婷, 陈雷, 刘芸, 等.高效液相色谱-高分辨质谱法测定乳粉中的牛磺酸[J].食品安全质量检测学报, 2017, 8(6):2086-2090.ZHANG T, CHEN L, LIU Y, et al.Determination of taurine in milk powder by high performance liquid chromatography-high resolution mass spectrometry[J].Journal of Food Safety &Quality, 2017, 8(6):2086-2090.
[9] 严俊, 徐柏杨, 颜琳琦, 等.L-8900氨基酸分析仪检测不同形态保健食品中牛磺酸含量[J].食品工业, 2019, 40(11):341-344.YAN J, XU B Y, YAN L Q, et al.Determination of taurine in different forms health food by L-8900 amino acid analyzer[J].The Food Industry, 2019, 40(11):341-344.
[10] MOHAMED S, ELBASHIR A, ABOUL-ENEIN H.Spectrophotometric method for determination of taurine in energy drinks[J].Current Pharmaceutical Analysis, 2016, 13(1):11-17.
[11] GONZ LEZ-V
LEZ-V ZQUEZ M, MEZA-M
ZQUEZ M, MEZA-M RQUEZ O G, GALLARDO-VEL
RQUEZ O G, GALLARDO-VEL ZQUEZ T, et al.Simultaneous determination of caffeine and taurine in energy drinks by FT-MIR spectroscopy coupled with multivariate analysis[J].Journal of Spectroscopy, 2020, 2020:8835846.
ZQUEZ T, et al.Simultaneous determination of caffeine and taurine in energy drinks by FT-MIR spectroscopy coupled with multivariate analysis[J].Journal of Spectroscopy, 2020, 2020:8835846.
[12] LEE I, VO J, GAO Q Y, et al.Single-laboratory validation study of a proton NMR method for the determination of L-arginine, L-citrulline, and taurine contents in dietary supplements[J].Journal of AOAC International, 2020, 103(4):1140-1147.
[13] 吴海智, 肖玥惠子, 朱礼, 等.程序进样-柱前衍生-高效液相色谱法测定乳制品中牛磺酸含量[J].食品研究与开发, 2021, 42(21):116-120.WU H Z, XIAO Y, ZHU L, et al.Determination of taurine content in dairy products using program sampling-precolumn derivatization-high performance liquid chromatography[J].Food Research and Development, 2021, 42(21):116-120.
[14] 黄丽丹, 邢亚东, 王玲玲, 等.2, 4-二硝基氟苯柱前衍生化HPLC法测定保健食品中牛磺酸含量[J].药物分析杂志, 2016, 36(1):171-175.HUANG L D, XING Y D, WANG L L, et al.Determination of taurine in health food by RP-HPLC with pre-column derivatization[J].Chinese Journal of Pharmaceutical Analysis, 2016, 36(1):171-175.
[15] 赵超敏, 蒋颖婕, 曾静, 等.高效液相色谱法测定乳粉及液态奶中牛磺酸含量[J].现代食品科技, 2019, 35(1):252-256;205.ZHAO C M, JIANG Y J, ZENG J, et al.Determination of taurine content in milk powder and liquid milk by high performance liquid chromatography[J].Modern Food Science and Technology, 2019, 35(1):252-256;205.
[16] 姚程晨, 杨丽梅, 林立.特殊医学用途婴儿配方食品中牛磺酸含量的测定[J].中国乳品工业, 2022, 50(12):44-48.YAO C C, YANG L M, LIN L.Detection of taurine in formulas for special medical purposes intended for infants[J].China Dairy Industry, 2022, 50(12):44-48.
[17] 李宇, 张乃合, 刘洪海.牛磺酸分析方法的研究进展[J].中国卫生检验杂志, 2021, 31(17):2167-2173.LI Y, ZHANG N H, LIU H H.Research progress on analytical methods of taurine[J].Chinese Journal of Health Laboratory Technology, 2021, 31(17):2167-2173.
[18] 柳小英, 毛丽沙, 鲍敏洁, 等.高效液相色谱法测定海洋生物中牛磺酸的含量[J].安徽农业科学, 2017, 45(31):1-3;11.LIU X Y, MAO L S, BAO M J, et al.Detection of taurine in marine life by high performance liquid chromatography[J].Journal of Anhui Agricultural Sciences, 2017, 45(31):1-3;11.
[19] 秦梦然, 张伟, 吴凤明, 等.高效液相色谱法检测5种市售鸡蛋中牛磺酸含量[J].食品研究与开发, 2022, 43(1):167-172.QIN M R, ZHANG W, WU F M, et al.Determination of taurine content in five brands of commercially available eggs by high performance liquid chromatography[J].Food Research and Development, 2022, 43(1):167-172.