白酒是中国的传统酒种,具有独特的酿造工艺和酒体风格,深受饮用者的喜爱。回顾白酒的酿造历史,可以发现制曲技术的出现使白酒走上了快速发展之路,也将白酒与酒曲绑定在了一起,形成了“曲乃酒之骨”的说法。在众多酒曲中,大曲凭借易培养、功能多、内涵复杂等特点,成为大多数名优白酒的糖化发酵剂。大曲主要为白酒发酵提供微生物和功能酶,两者的共同作用保证了白酒发酵过程中原料降解、乙醇发酵和风味化合物代谢的顺利进行。因此,大曲内的微生物和功能酶一直是白酒产业界和科技界关注的重点和热点。目前,对大曲内微生物群落组成和关键微生物作用的研究较多,认识也较完善。由于大曲组分复杂、研究手段有限等问题,直到近年来测序技术和质谱技术快速发展,大曲的酶系组成和功能才得到深入的剖析。本文聚焦大曲酶系的研究进展,对目前常用于分析大曲酶系的先进技术手段进行了介绍,并对低温大曲、中温大曲和高温大曲的功能酶组成进行了总结,以期为白酒大曲的功能酶研究、质量监测控制和制作工艺优化提供参考。
1 白酒大曲及其组成
大曲是粮谷经过长时间的自然堆积发酵得到的一种含有多菌类、多酶类的复合制剂,是白酒发酵过程中菌系、酶系和物系的重要来源,具有糖化、发酵、投粮和生香的功能。不同大曲的区别主要体现在工艺、原料配比和发酵温度不同。其中,品温是微生物群落演替的重要驱动因素之一,品温的改变影响大曲内部微生物群落及代谢活性的变化,进而影响功能酶和风味化合物的组成[1]。大曲根据品温主要分为三类,即低温大曲、中温大曲和高温大曲(图1)。低温大曲多以大麦、豌豆为原料,最高品温不超过50 ℃,主要用于生产清香型白酒。中温大曲以小麦为主要原料,辅以大麦或豌豆,最高品温控制在60 ℃以下,为加强白酒的风味,部分中温大曲的制曲品温有所提高,形成了中高温大曲,中温及中高温大曲主要用于生产浓香型白酒。高温大曲多以纯小麦制成,接种一定比例的母曲,最高品温控制在60~65 ℃,是3种大曲中糖化力、液化力和发酵力最低的大曲,主要用于生产酱香型白酒或浓香型调味酒。
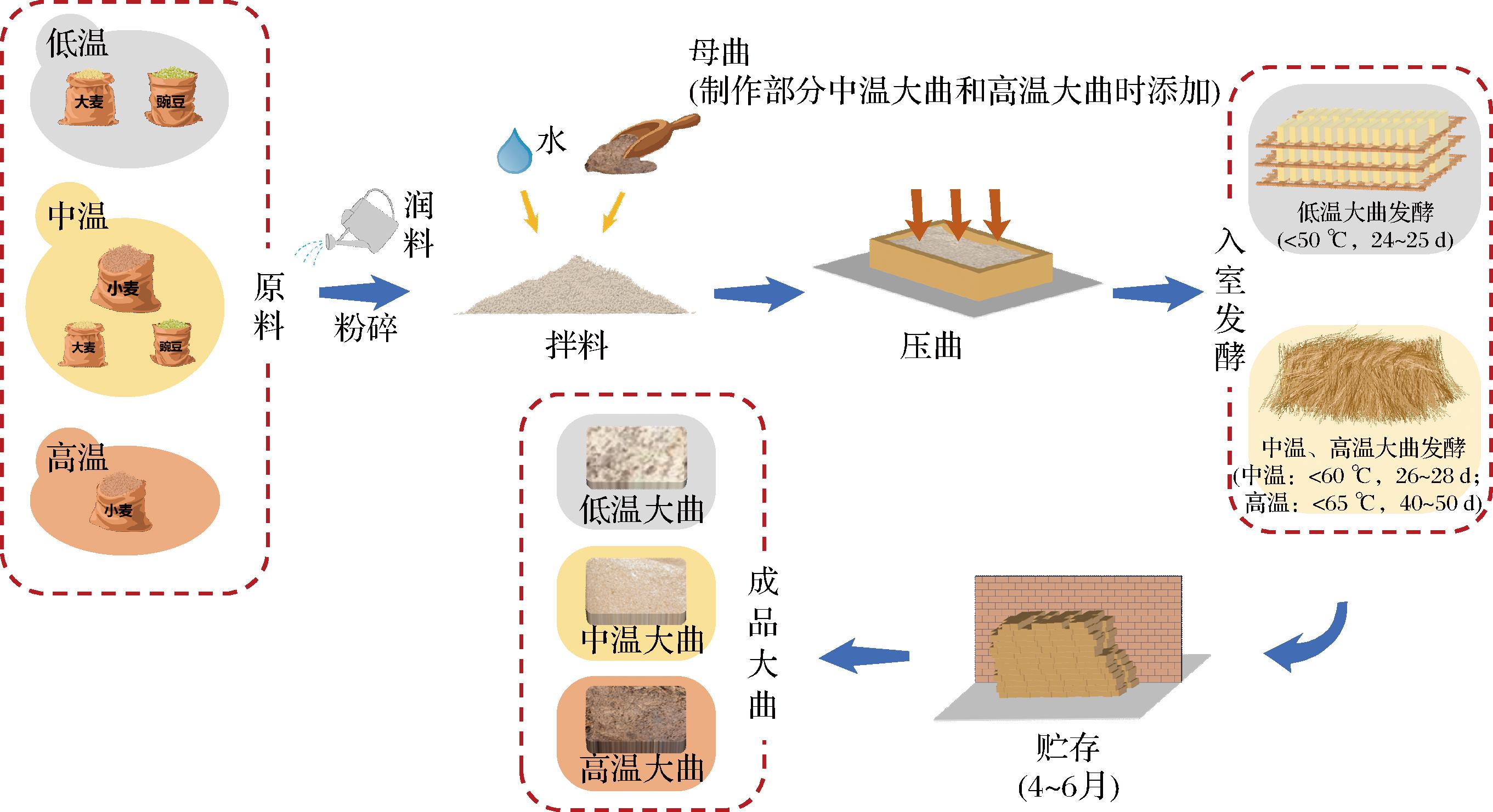
图1 低温大曲、中温大曲和高温大曲的生产工艺示意图
Fig.1 Schematic diagram of the production process for low-temperature Daqu, medium-temperature Daqu, and high-temperature Daqu
大曲经过长时间的自然发酵,组成十分复杂,现在一般将大曲的组分分为3个部分,即菌系、酶系和物系(图2)。菌系主要包括细菌、霉菌、酵母菌和放线菌等,其代谢活动和群落演替是决定大曲质量的关键之一。物系主要是微生物和功能酶降解原料后的代谢产物,不仅可以为后续白酒发酵提供关键前体物质,还可以直接将风味化合物带入到基础酒中[2]。酶系主要包括由微生物代谢产生的酶,以及少部分由原料和环境带入的酶,它们直接影响大曲的质量,并能为酒体香气的构成做出巨大贡献[3]。目前,已在大曲中鉴定出1 000余种酶,其中功能酶包括淀粉酶、纤维素酶、蛋白酶和酯化酶等。酶的作用主要有两个方面,一是在大曲自身发酵过程中,将原料降解为微生物需要的营养小分子,保证大曲内微生物的正常代谢活动,同时可以作为菌系代谢风味化合物的关键中间者;二是在白酒发酵中为糖化、乙醇发酵和风味化合物代谢等途径提供重要的功能酶[4]。因此,探究大曲中酶系的组成和功能,对于大曲的质量控制及提升和白酒的风味解析具有重要意义。

图2 大曲内部组成及酶系作用示意图
Fig.2 Schematic diagram of the internal composition of Daqu and the function of enzymes in Daqu
2 大曲中酶系的研究技术手段
在大曲的生产中,酶活力(糖化力、液化力、发酵力、蛋白酶活力和酯化力等)是判断成品大曲质量的重要指标。在部分大曲研究中,酶活力被用于表征大曲内功能酶的表达程度和微生物的产酶效果[5-7]。采用酶活力可以简单、快速且准确地表征大曲内各种功能酶的作用效果。但是,仅仅检测大曲的酶活力,并不能解析酶系的来源,且无法深入分析各类功能酶的组成和功能。随着检测技术的快速发展和各类数据库的补充,现有研究通过基因组、转录组和蛋白质组分析大曲,获得了大曲内的酶系来源、组成和功能。相应的技术手段主要有高通量测序技术(包括扩增子测序、宏基因组学和宏转录组学)和宏蛋白组学技术(表1)。
表1 大曲酶系研究的主要技术手段
Table 1 Main technologies for analyzing the enzymes in Daqu

方法主要优点主要缺点文献扩增子测序检测快速,检测成本低无法检测基因是否表达、是否有活性,测序深度不足,功能预测误差大[8-11]宏基因组学检测快速,测序深度高,检测范围广无法检测基因是否表达、是否有活性,存在功能预测误差[12-15]宏转录组学检测结果具有时空特异性,能够排除基因表达程度不同带来的误差RNA提取困难,易降解,存在功能预测误差[16-19]宏蛋白质组学能够直接检测酶系的种类及丰度检测成本较高,蛋白质提取困难[20-26]
2.1 高通量测序
高通量测序技术近年来愈发成熟,已广泛用于大曲的微生物群落研究中,该技术可以对大曲样品中微生物的基因片段进行快速且较准确的测序,为解析大曲内部微生物群落组成提供了重要帮助。随着各类数据库,如NCBI数据库、UniProt数据库、KEGG数据库等的补充,目前可以通过基因组和转录组在数据库中完成功能注释,预测蛋白表达,实现对大曲内酶系的解析。
基因组测序方法主要有两种,即扩增子测序和宏基因组测序。扩增子测序是利用引物扩增大曲内微生物的16S rDNA和ITS高度保守区,再对扩增产物进行测序,进而鉴定出大曲内部的微生物组成和丰度,还可以通过PICRUST 2对大曲内微生物进行功能预测。HE等[27]通过扩增子测序,分析了强化大曲中涉及糖化、乙醇发酵和风味化合物代谢的功能酶,发现上述代谢途径中相关功能酶的编码基因丰度明显增加。宏基因组测序可以对大曲内部所有微生物的基因组进行非靶向测序。相较于扩增子测序,宏基因组测序的深度更深,不仅能更大范围地检测出大曲内微生物的组成和丰度,还可以通过对DNA长序列的功能注释,更准确地预测大曲内部的功能酶组成[28]。ZHANG等[13]采用宏基因组测序对不同发酵过程中的大曲进行了研究,结果表明α-葡萄糖苷酶(EC 3.2.1.20)和β-葡萄糖苷酶类(EC 3.2.1.21)是大曲内碳水化合物代谢途径中的关键功能酶。但扩增子测序和宏基因组测序在大曲酶系研究中仍有不足。其中PICRUST 2是一种基于某段基因序列的系统发育关系预测功能的方法,本身存在一定的偏差,预测结果不能准确表征微生物的功能表达。宏基因组测序虽避免了PICRUST 2带来的误差,但仍是从DNA层面来进行功能预测,不能得到基因是否有表达、是否有活性等信息,且其利用功能基因丰度对功能酶进行定量分析,不能准确表征功能酶的丰度。
由于大曲内部组成复杂,目前多使用宏转录组学对大曲内的转录组进行测序。宏转录组学可以通过高通量测序技术得到大曲内部微生物的全部基因转录情况以及转录调控规律。宏转录组学是从RNA出发对蛋白表达进行预测,其预测信息具有时空特异性,可以对活性微生物、活性转录本以及活性功能进行研究。YI等[19]通过宏转录组学对中温大曲和高温大曲内功能基因的表达程度进行了对比,发现高温大曲中多数碳水化合物代谢途径的功能酶表达量低于中温大曲,同时发现高温大曲中存在独有的生香功能酶。但由于RNA提取技术受限,且大曲组成复杂,导致大曲内部RNA提取难度较大,同时受限于RNA易降解,影响了宏转录组学的检测范围及准确性。
要克服上述的高通量测序技术缺陷,关键依赖于组学技术的升级,通过多组学联合分析的方式可以减小实验结果的误差。如LIU等[29]等使用宏基因组学和宏转录组学结合的方式解析大曲酶系,不仅可以深入分析基因丰度与基因表达上的关系,还可以在宏基因组学的基础上分析功能基因的表达情况,并在宏转录组学的基础上判断具有活性的基因序列和捕捉微生物群落中基因表达瞬间变化,两种结果相互结合佐证可提高分析的准确性。
2.2 宏蛋白质组学
宏蛋白质组学是一种通过质谱技术对样品内微生物表达的所有蛋白质进行大规模的定性和定量的方法,可以直观表征大曲内酶系的组成情况,直接消除了由基因组和转录组预测蛋白表达带来的误差[30]。随着质谱技术的发展和相关数据库的补充,在大曲的酶系研究中宏蛋白质组学技术的应用也逐渐增多。采用宏蛋白质组学技术进行大曲酶系分析的路线如图3所示,包括蛋白质提取、蛋白质的酶解及分析纯化、肽段的质谱检测和数据库检索分析。需要指出的是,目前使用宏蛋白质组学检测大曲内的低丰度蛋白仍然存在困难,难点主要集中在蛋白质的提取、肽段的质谱检测和数据库检索分析方面。
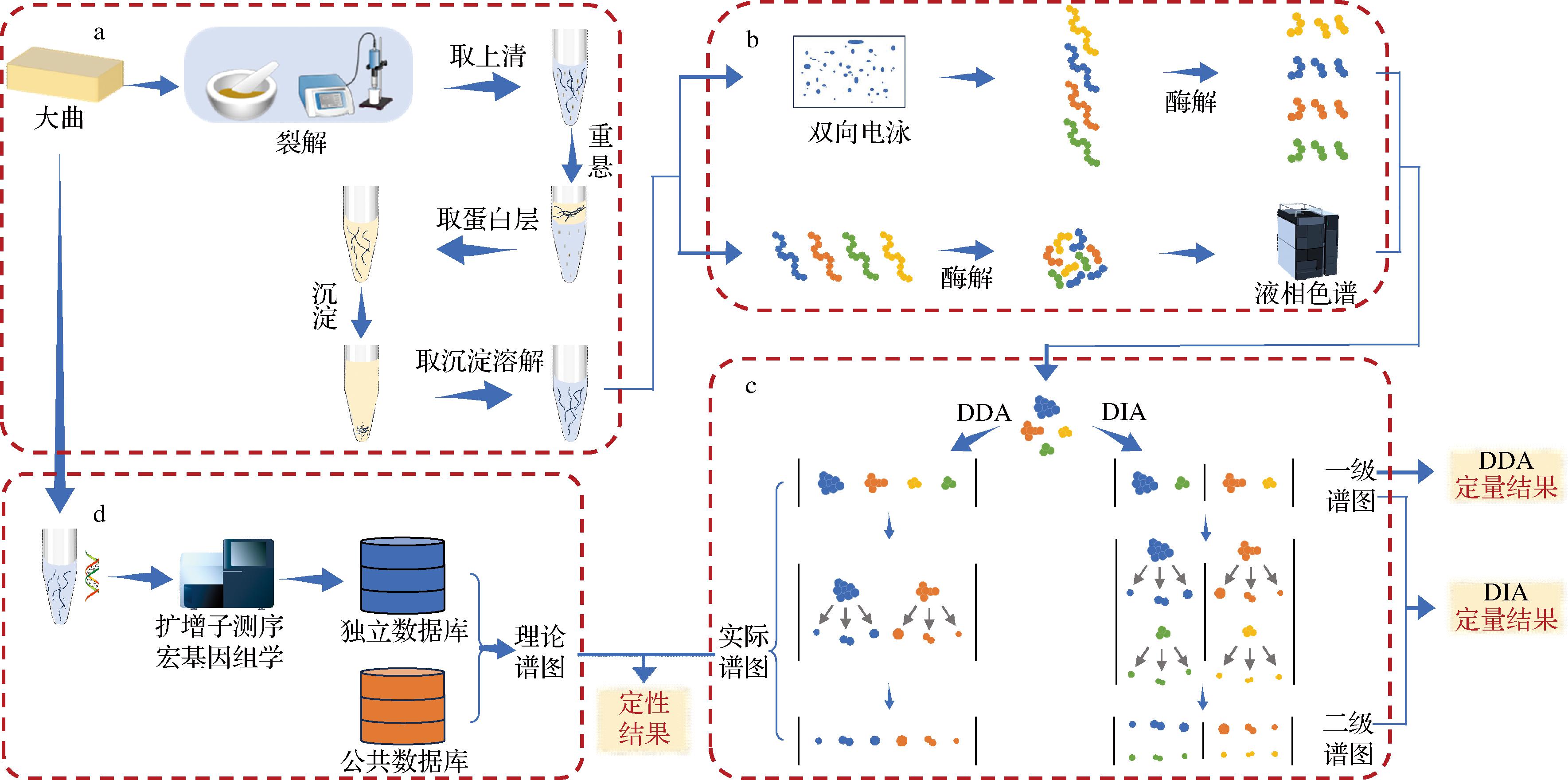
a-蛋白质的提取;b-蛋白质的酶解及分离纯化;c-肽段的质谱检测;d-数据库的选择
图3 宏蛋白质组学技术路线示意图
Fig.3 Schematic diagram of the technical route of metaproteomic
2.2.1 蛋白质的提取
有效提取大曲样品中所有蛋白质是确保宏蛋白质组学实验结果准确的关键,由于大曲含有丰富的微生物,各微生物的细胞壁结构和细胞抗裂解性不同,这在一定程度上影响了大曲中蛋白质的提取效果,而且大曲内部的高酸、高醇环境还会增大蛋白质的提取难度。目前,关于大曲中蛋白质的提取还没有统一的方法,但主要步骤为:1)加入裂解液,然后辅以研磨、匀浆和超声破碎仪等物理手段进行裂解;2)加入重悬液将蛋白质重悬;3)加入沉淀剂后离心取沉淀,得到待测蛋白质样品(图3-a)。其中,裂解液、重悬液和沉淀剂的选择对蛋白质的提取效果影响较大,因此在提取大曲蛋白质时,需要系统优化上述条件,以减小由于蛋白提取不全而带来的误差。
2.2.2 蛋白质的酶解及分离纯化
由于待测样品中蛋白质的相对分子质量较大、种类较多,因此在进行质谱检测前必须进行酶解和分离纯化。多使用胰蛋白酶进行酶解,因为胰蛋白酶的专一性较强,且酶解后的肽段具有较高的离子化效率。现有的蛋白质分离纯化方式有双向凝胶电泳法和液相色谱法(图3-b)。其中双向凝胶电泳法需要手动选择蛋白质点,各点需要单独酶解和上机,操作较繁琐,难以对样品进行快速检测,目前已很少用于大曲内蛋白质的分离纯化。液相色谱法要求先将蛋白质统一酶解成肽段,再通过液相色谱仪对所有肽段进行分离纯化,该方法降低了实验的繁琐度,更适合大曲这种含有大量蛋白质的样品。其中反向液相色谱法因具有良好的分离度和可重复性,是目前进行多肽分离纯化的主要方法。该方法的固定相通常为C18修饰的硅球,流动相包括水溶性缓冲液(如甲酸和水的混合物)和有机溶剂(如甲酸和乙腈的混合物)[31]。而且反向液相色谱法可以连接各种离子源,因此当肽段从色谱柱洗脱后,它们可以直接转移到质谱分析中,进一步简化了实验操作。
2.2.3 肽段的质谱检测与数据库检索分析
质谱分析的原理是将两次质谱得到的一二级谱图与数据库中的理论谱图进行匹配,以完成蛋白质的定性分析,再通过计算谱图丰度完成蛋白质的定量分析。在对大曲内蛋白质的质谱检测中,主要用到数据依赖性采集(data-dependent acquisition, DDA)模式或数据独立采集(data-independent acquisition, DIA)模式,其中DDA模式在质谱检测时选择一次质谱中丰度较大的肽段进行二次质谱,DIA模式对一次质谱后的所有肽段都进行二次质谱,这使得DIA模式对大曲内丰度较低的蛋白质有更好的检测效果(图3-c)。大曲中蛋白质组成复杂且含量差异较大,DDA模式因难以检测低丰度蛋白而无法获得大曲蛋白质的完全解析结果。DIA模式中进行二次质谱的肽段过多,会导致二级谱图与一级谱图的对应关系变得复杂,搜库定性较困难[32]。现有解决方案是配合使用DDA模式,以提高DIA模式的准确性,即可以先通过DDA模式确定好一级和二级谱图的对应关系,再进行DIA模式的定性分析,但该方案的检测成本过高,故仍需优化升级。
在分析质谱结果时,数据库的选择决定了定性分析结果的准确性,目前可以使用公共数据库或通过基因组学结果构建数据库(图3-d)。其中,使用公共数据库更方便,实验成本更低。但是,对于大曲这种含有复杂微生物群落的样品,使用公共数据库难以确保检测结果的准确度,因此多使用独立数据库完成大曲内蛋白质的定性分析。总体而言,各大数据库尚不足以满足大曲内蛋白质的完全检索需求,加强相关数据库的建设对实现大曲酶系的完全解析具有重要意义。
3 大曲内酶系研究进展
由于大曲的糖化、发酵和生香功能与大曲内部的酶系组成紧密相关,现有研究开始更多地探究大曲内的糖化酶系、乙醇发酵酶系和风味化合物代谢酶系。梳理现有的大曲酶系研究文献,可以发现低温、中温和高温大曲内糖化酶系与乙醇发酵酶系的相似度较高,但生香功能酶系差异较大。这可能是导致3种典型大曲所产成品酒风格差异较大的重要原因(图4)。

图4 低温大曲、中温大曲和高温大曲的功能酶组成
Fig.4 Composition of functional enzymes in low-temperatureDaqu, medium-temperature Daqu, and high-temperature Daqu
3.1 低温大曲
低温大曲较低的品温使其具有较高的糖化力、液化力和发酵力,并在清香型大曲酒发酵过程中主要起糖化和发酵的作用。目前对低温大曲的酶系研究较少,且集中于分析糖化酶系和乙醇发酵酶系的组成及功能,因此本文主要对两篇代表性文章进行简要介绍。关于糖化酶系,ZHENG等[4]通过扩增子测序与宏蛋白质组学结合的方法,发现低温大曲的主要糖化功能酶包括α-淀粉酶(EC 3.2.1.1)和葡聚糖-1,4-α-葡萄糖苷酶(EC 3.2.1.3);HUANG等[33]补充了低温大曲的糖化酶系组成,通过宏基因组学研究发现山西汾阳低温大曲的糖化酶系主要由淀粉降解功能酶构成,包括糖原磷酸化酶(EC 2.4.1.1)、α-淀粉酶(EC 3.2.1.1)、蔗糖磷酸化酶(EC 2.4.1.7)、4-α-葡聚糖转移酶(EC 2.4.1.25)、β-呋喃果糖苷酶(EC 3.2.1.26)和葡糖淀粉酶(EC 3.2.1.3)。在对乙醇发酵酶系的分析中,ZHENG等[4]发现大曲在白酒初始发酵阶段为乙醇发酵提供了乙醇脱氢酶(EC 1.1.1.1),但HUANG等[33]在研究中未发现乙醇脱氢酶,认为丙酮酸合酶(EC 1.2.7.1)、乙酸-辅酶A连接酶(EC 6.2.1.1)、乙醛脱氢酶(乙酰化/ NAD(+))(EC 1.2.1.10/ EC 1.2.1.3)、乙醇脱氢酶(NADP(+))(EC 1.1.1.2)是乙醇发酵的主要功能酶。这可能是两者的研究样品或检测方式有所差异而导致的。两篇文章对低温大曲内的生香功能酶系也进行了研究,发现乳酸脱氢酶(EC 1.1.1.27)是乳酸代谢的主要功能酶,羧酸酯酶(EC 3.1.1.1)和三酰甘油脂肪酶(EC 3.1.1.3)是酯类合成的主要功能酶。
3.2 中温大曲
目前对中温大曲糖化酶系的认识较为清晰。多个研究分别通过基因组[12,29,33-35]和蛋白组[21-23]证实了中温大曲的糖化酶系由淀粉降解酶系和纤维素降解酶系组成。其中,淀粉降解酶系主要包括葡糖淀粉酶(EC 3.2.1.3)、α-淀粉酶(EC 3.2.1.1)、α-葡萄糖苷酶(EC 3.2.1.20)、糖原磷酸化酶(EC 2.4.1.1)和低聚-1,6-葡糖苷酶(EC 3.2.1.10);纤维素降解酶系主要包括1,4-β-纤维二水解酶(EC 3.2.1.91)、β-葡萄糖苷酶(EC 3.2.1.21)和内切葡聚糖酶(EC 3.2.1.4)。这两种酶系通过降解淀粉和纤维素为白酒发酵提供葡萄糖。在后续的乙醇发酵途径中乙醇脱氢酶(EC 1.1.1.1)、乙醇脱氢酶(EC 1.1.1.2)和乙醛脱氢酶(EC 1.2.1.3)是中温大曲的关键功能酶[22,29,33-36]。
中温大曲内丰富的挥发性物质是影响白酒风味的重要因素之一,因此大曲的生香功能酶引起了研究人员的关注。酯类物质是白酒香味的关键成分,己酸乙酯更是浓香型白酒中的典型风味物质[37]。HUANG等[33]通过扩增子测序发现羧酸酯酶(EC 3.1.1.1)、酰基甘油脂肪酶(EC 3.1.1.23)和三酰甘油脂肪酶(EC 3.1.1.3)是中温大曲内酯类合成的关键功能酶,FAN等[21]通过宏蛋白质组学证实了3-羟基丁基-CoA脱氢酶(EC 1.1.1.157)是己酸乙酯合成途径中的重要功能酶。酸类物质不仅是白酒中的重要风味化合物,也是许多风味化合物的前体物质。HE等[36]利用扩增子测序发现丙酮酸脱氢酶(EC 1.2.4.1)、乙醛脱氢酶(EC 1.2.1.10)、磷酸转乙酰酶(EC 2.3.1.8)和乙酸激酶(EC 2.7.2.1)是乙酸代谢过程中的相关功能酶。FAN等[21]通过宏蛋白组学发现L-乳酸脱氢酶(EC 1.1.1.27)和乳酸脱氢酶(EC 1.1.2.4)是乳酸代谢的关键功能酶。TONG等[38]通过扩增子测序发现反式肉桂酸4-单加氧酶(EC 1.14.14.91)、苯丙氨酸氨裂解酶(EC 4.3.1.24)、酪氨酸氨裂解酶(EC 4.3.1.25)和咖啡酸O-甲基转移酶(EC 2.1.1.68)是咖啡酸代谢的相关功能酶。研究者也对其他风味化合物代谢途径中的功能酶进行了解析。FAN等[21]通过宏蛋白组学解析异丁醇的途径,验证了酮酸还原异构酶(EC 1.1.1.86)、二羟基酸脱水酶(EC 4.1.1.9)和支链氨基酸氨基转移酶(EC 2.6.1.42)是中温大曲中参与异丁醇代谢的关键酶。TONG等[39]发现阿魏酰-CoA 水合酶/裂解酶(EC 4.1.2.61)和酰氨基酶(EC 3.5.1.4)是香兰素合成的相关功能酶。MU等[40]发现乙酰乳酸合酶(EC 2.2.1.6)和乙酰乳酸脱羧酶(EC 4.1.1.5)是中温大曲内川芎嗪和2,3-丁二醇合成的相关功能酶。
3.3 高温大曲
高温大曲的糖化酶系组成与中温大曲类似,主要由淀粉降解酶系和纤维素降解酶系组成。其中,淀粉降解酶系主要包括α-淀粉酶(EC 3.2.1.1)、α-葡萄糖苷酶(EC 3.2.1.20)、葡糖淀粉酶(EC 3.2.1.3)和糖原磷酸化酶(EC 2.4.1.1)[11,12,19,33]。ZHU等[26]还通过宏蛋白组学在高温大曲内发现了来源于小麦的β-淀粉酶(EC 3.2.1.2),认为其对淀粉降解有重要作用。纤维素降解酶系包括内切葡聚糖酶(EC 3.2.1.4)、1,4-β-纤维二水解酶(EC 3.2.1.91)和β-葡萄糖苷酶(EC 3.2.1.21)[12,19,33]。ZHAO等[24]通过宏蛋白质组学进一步解析了季节和颜色对高温大曲内糖化酶系的影响,发现夏季黄色高温大曲中α-淀粉酶、1,4-β-纤维二水解酶、葡糖淀粉酶和β-葡萄糖苷酶的含量高于其他季节及颜色的高温大曲,这使得夏季黄色高温大曲拥有较高的糖化力。在乙醇发酵途径中,乙醇脱氢酶(EC 1.1.1.1)、乙醇脱氢酶(NADP(+))(EC 1.1.1.2)、乙醛脱氢酶(NAD(+))(EC 1.2.1.3)和丙酮酸脱羧酶(EC 4.1.1.1)是高温大曲内部的关键功能酶[19,33]。
由于高温大曲在酱酒发酵过程中具有独特的添加方式和较大的添加量,因此高温大曲的生香功能更为显著,多篇文章对高温大曲的生香功能酶进行了解析。HUANG等[33]通过宏基因组学发现十二烷酰基-[酰基载体蛋白]水解酶(EC 3.1.2.21)、三酰甘油脂肪酶(EC 3.1.1.3)、脂肪酸合酶(EC 2.3.1.85)、羧酸酯酶(EC 3.1.1.1)是高温大曲内酯类合成的关键功能酶。LYU等[18]通过转录组证实了高温大曲内参与乙酸合成的关键功能酶是丙酮酸脱羧酶(EC 4.1.1.1)和乙醇脱氢酶(EC 1.1.1.1),参与乳酸合成的功能酶是D-乳酸脱氢酶(EC 1.1.1.28)、乳酸脱氢酶(EC 1.1.2.4)和L-乳酸脱氢酶(EC 1.1.1.27)[18]。SHI等[11]通过对不同颜色高温大曲进行PICRUST 2功能预测,发现高温大曲内部的乙酰乳酸合成酶(EC 2.2.1.6)是川芎嗪合成的相关功能酶。
3.4 三种典型大曲关键功能酶系的差异分析
结合前文对低温、中温和高温大曲内部关键功能酶的梳理,可将大曲的功能酶系分为糖化酶系、乙醇发酵酶系和生香酶系。低温大曲的糖化酶系和乙醇发酵酶系的组成和含量与其他两种大曲呈现出一定的差异性,这可能是低温大曲较低的发酵温度影响了功能微生物的繁殖和代谢而导致的。中温和高温大曲的糖化酶系组成基本相同,主要包括淀粉降解酶系和纤维素降解酶系,但YI等[19]和HUANG等[33]分别通过转录组和基因组分析发现,高温大曲中糖化酶的功能基因丰度和表达程度均低于中温大曲,这也解释了高温大曲糖化能力较低的原因。在乙醇发酵途径中,高温大曲的关键功能酶与中温大曲类似[19],但高温大曲中丙酮酸脱羧酶的功能基因丰度显著高于中温大曲[33]。相比于糖化途径和乙醇发酵途径,3种典型大曲内风味化合物代谢途径的功能酶系组成差异较大。在酯类化合物代谢功能酶中,高温大曲内部检测出独有的十二烷酰基-[酰基载体蛋白]水解酶和脂肪酸合酶,这可能与高温大曲内鸡葡萄球菌的含量有关[33]。在乳酸代谢途径中,高温大曲内部的L-乳酸脱氢酶表达量比中温大曲低,而D-乳酸脱氢酶的表达量比中温大曲高[19]。此外,YI等[19]通过转录组在高温大曲内部检测到大量中温大曲中未被检测出的酶,包括2-脱氧-D-葡糖酸3-脱氢酶(EC 1.1.1.125)、2-羟基色烯-2-羧酸异构酶(EC 5.99.1.4)、苯甲醛脱氢酶(NAD)(EC 1.2.1.28)、D-3-磷酸甘油酸脱氢酶(EC 1.1.1.95)、醌氧化还原酶(EC 1.6.5.5)、L-肌醇2-脱氢酶(EC 1.1.1.14)、5-羧甲基-2-羟基粘酸异构酶(EC 5.3.3.10)和醛还原酶(EC 1.1.1.21),这可能与酱香型白酒的独特风味有关。
4 总结与展望
大曲的酶系组成不仅决定了大曲和白酒发酵时的糖化效果,还对最终成品酒的风味有重要影响。组学技术的快速发展为深刻认识大曲的功能酶提供了可能性。如扩增子测序、宏基因组学和宏转录组可以分别通过DNA和RNA片段预测大曲内酶系的表达情况,宏蛋白质组学可以直接检测大曲内的酶蛋白组成。但各种技术手段目前仍存在不足,如扩增子测序和宏基因组学无法避免由基因表达和基因活性情况导致的误差;宏转录组学难以提取大曲内的全部RNA,且RNA不能准确表征蛋白质的表达情况;宏蛋白质组学难以准确提取和检索大曲内的全部蛋白质。在未来的大曲酶系研究中,尚需针对不同的研究目的选择合适的组学技术进行检测和分析,还可以进一步采用多组学技术结合的模式,充分发挥各组学技术的优势,并通过结果互佐的方式提高酶系研究的准确性。通过对低温大曲、中温大曲和高温大曲中关键功能酶系的总结,可以发现葡糖淀粉酶和α-淀粉酶是糖化途径中的关键功能酶,乙醇脱氢酶和乙醛脱氢酶是乙醇发酵途径的关键功能酶;各典型大曲中功能酶系的差异主要集中于风味化合物代谢途径的相关酶,这应该是影响白酒风格的重要因素。由于现有技术对低丰度功能酶类的检测效果不佳,而且大曲内生香功能酶含量低、组成复杂,因此目前对各大曲风味化合物代谢途径的研究还不够深入。相信随着分析检测技术的不断发展,宏蛋白质组学、宏基因组学、宏转录组学等多组学分析技术将在大曲酶系研究中有更广泛的应用,为大曲内关键生香功能酶的认识和挖掘提供更多帮助。
[1] 杨阳, 禄凌飞, 刘光钱, 等.不同发酵顶温大曲中细菌群落结构的差异性分析[J].食品与发酵工业, 2023, 49(13):70-77.YANG Y, LU L F, LIU G Q, et al.Difference analysis of bacterial community structure in Daqu with different peak temperatures achieved during fermentation[J].Food and Fermentation Industries, 2023, 49(13):70-77.
[2] 张清玫, 赵鑫锐, 李江华, 等.不同香型白酒大曲微生物群落及其与风味的相关性[J].食品与发酵工业, 2022, 48(10):1-8.ZHANG Q M, ZHAO X R, LI J H, et al.The relationship between microbial community and flavors of three types of Daqu[J].Food and Fermentation Industries, 2022, 48(10):1-8.
[3] 柳习月, 朱琪, 杨帆, 等.蛋白组学揭示苯丙氨酸代谢对酱香大曲风味影响[J].食品科技, 2021, 46(8):1-6.LIU X Y, ZHU Q, YANG F, et al.Proteomics reveals the effect of phenylalanine metabolism on the flavor of Daqu [J].Food Science and Technology, 2021, 46(8):1-6.
[4] ZHENG Y F, LIANG F, WU Y, et al.Unraveling multifunction of low-temperature Daqu in simultaneous saccharification and fermentation of Chinese light aroma type liquor[J].International Journal of Food Microbiology, 2023, 397:110202.
[5] ZHU Q, CHEN L Q, PENG Z, et al.Analysis of environmental driving factors on Core Functional Community during Daqu fermentation[J].Food Research International, 2022, 157:111286.
[6] GUAN T W, YANG H, OU M Y, et al.Storage period affecting dynamic succession of microbiota and quality changes of strong-flavor Baijiu Daqu[J].LWT, 2021, 139:110544.
[7] JIANG X Y, PENG Z, ZHU Q, et al.Exploration of seasonal fermentation differences and the possibility of flavor substances as regulatory factors in Daqu[J].Food Research International, 2023, 168:112686.
[8] WANG Z M, WANG C T, SHEN C H, et al.Microbiota stratification and succession of amylase-producing Bacillus in traditional Chinese Jiuqu (fermentation starters)[J].Journal of the Science of Food and Agriculture, 2020, 100(8):3544-3553.
[9] XU B Y, XU S S, CAI J, et al.Analysis of the microbial community and the metabolic profile in medium-temperature Daqu after inoculation with Bacillus licheniformis and Bacillus velezensis[J].LWT, 2022, 160:113214.
[10] CHEN L H, LIU B, FENG S B, et al.Correlation between microbe, physicochemical properties of Jiuqu in different plateau areas and volatile flavor compounds of highland barley alcoholic drink[J].Food Bioscience, 2023, 51:102276.
[11] SHI W, CHAI L J, FANG G Y, et al.Spatial heterogeneity of the microbiome and metabolome profiles of high-temperature Daqu in the same workshop[J].Food Research International, 2022, 156:111298.
[12] XIA Y, ZHOU W, DU Y K, et al.Difference of microbial community and gene composition with saccharification function between Chinese nongxiangxing Daqu and jiangxiangxing Daqu[J].Journal of the Science of Food and Agriculture, 2023, 103(2):637-647.
[13] ZHANG Y T, DENG Y K, ZOU Y F, et al.Linking microbial functional gene abundance and Daqu extracellular enzyme activity:Implications for carbon metabolism during fermentation[J].Foods, 2022, 11(22):3623.
[14] YANG Y, WANG S T, LU Z M, et al.Metagenomics unveils microbial roles involved in metabolic network of flavor development in medium-temperature Daqu starter[J].Food Research International, 2021, 140:110037.
[15] ZHANG J, LIU S P, SUN H L, et al.Metagenomics-based insights into the microbial community profiling and flavor development potentiality of Baijiu Daqu and Huangjiu wheat Qu[J].Food Research International, 2022, 152:110707.
[16] CHEN L C, YI Z L, FANG Y, et al.Biochemical and synergistic properties of a novel alpha-amylase from Chinese Nong-flavor Daqu[J].Microbial Cell Factories, 2021, 20(1):80.
[17] ALI B, YI Z L, FANG Y, et al.Characterization of a fungal thermostable endoglucanase from Chinese Nong-flavor Daqu by metatranscriptomic method[J].International Journal of Biological Macromolecules, 2019, 121:183-190.
[18] LYU W Z, LI F, LI C G.Effect of inoculated Daqu on the spontaneous fermentation of Chinese liquor[J].Food Research International, 2023, 173:113321.
[19] YI Z L, JIN Y L, XIAO Y, et al.Unraveling the contribution of high temperature stage to Jiang-flavor Daqu, a liquor starter for production of Chinese Jiang-flavor Baijiu, with special reference to metatranscriptomics[J].Frontiers in Microbiology, 2019, 10:472.
[20] FAN Z B, JIA W.Extracellular proteolytic enzyme-mediated amino exposure and β-oxidation drive the raspberry aroma and creamy flavor formation[J].Food Chemistry, 2023, 424:136442.
[21] FAN W Y, ZHAO X R, DU G C, et al.Metaproteomic analysis of enzymatic composition in Baobaoqu fermentation starter for Wuliangye Baijiu[J].International Journal of Food Science &Technology, 2021, 56(8):4170-4181.
[22] HE M W, JIN Y, LIU M M, et al.Metaproteomic investigation of enzyme profile in Daqu used for the production of Nongxiangxing Baijiu[J].International Journal of Food Microbiology, 2023, 400:110250.
[23] XIA Y, ZHU M, DU Y K, et al.Metaproteomics reveals protein composition of multiple saccharifying enzymes in nongxiangxing Daqu and jiangxiangxing Daqu under different thermophilic temperatures[J].International Journal of Food Science &Technology, 2022, 57(8):5102-5113.
[24] ZHAO J Z, YANG Y, CHEN L Q, et al.Quantitative metaproteomics reveals composition and metabolism characteristics of microbial communities in Chinese liquor fermentation starters[J].Frontiers in Microbiology, 2023, 13:1098268.
[25] WANG Y, QUAN S K, ZHAO Y J, et al.The active synergetic microbiota with Aspergillus as the core dominates the metabolic network of ester synthesis in medium-high temperature Daqu[J].Food Microbiology, 2023, 115:104336.
[26] ZHU Q, CHEN L Q, PENG Z, et al.The differences in carbohydrate utilization ability between six rounds of Sauce-flavor Daqu[J].Food Research International, 2023, 163:112184.
[27] HE G Q, DONG Y, HUANG J, et al.Alteration of microbial community for improving flavor character of Daqu by inoculation with Bacillus velezensis and Bacillus subtilis[J].LWT, 2019, 111:1-8.
[28] 侯强川, 王玉荣, 田龙新, 等.基于宏基因组测序技术解析市售强化酒曲微生物群落结构和功能特征[J].食品与发酵工业, 2023, 49(10):100-107.HOU Q C, WANG Y R, TIAN L X, et al.Microbial community structure and functional characteristics of commercial intensified Jiuqu based on metagenomic sequencing technology[J].Food and Fermentation Industries, 2023, 49(10):100-107.
[29] LIU W H, CHAI L J, WANG H M, et al.Bacteria and filamentous fungi running a relay race in Daqu fermentation enable macromolecular degradation and flavor substance formation[J].International Journal of Food Microbiology, 2023, 390:110118.
[30] YANG L, FAN W L, XU Y.Metaproteomics insights into traditional fermented foods and beverages[J].Comprehensive Reviews in Food Science and Food Safety, 2020, 19(5):2506-2529.
[31] 赵鑫锐, 李江华, 范伟业, 等.基于宏蛋白质组学技术对浓香大曲进行酶系结构解析的方法:CN112899344A[P].2021-06-04.ZHAO X R, LI J H, FAN W Y, et al. Analyzing the enzyme structure of Luzhou Daqu based on the macroproteomics technology, comprises extracting the crude enzyme solution of Luzhou Daqu and measuring various enzyme activities in the crude enzyme solution: China, CN112899344A[P]. 2021-06-04.
[32] GUAN S H, TAYLOR P P, HAN Z W, et al.Data dependent-independent acquisition (DDIA) proteomics[J].Journal of Proteome Research, 2020, 19(8):3230-3237.
[33] HUANG Y, LI D, MU Y, et al.Exploring the heterogeneity of community and function and correspondence of “species-enzymes” among three types of Daqu with different fermentation peak-temperature via high-throughput sequencing and metagenomics[J].Food Research International, 2024, 176:113805.
[34] ZHU M, ZHENG J, XIE J, et al.Effects of environmental factors on the microbial community changes during medium-high temperature Daqu manufacturing[J].Food Research International, 2022, 153:110955.
[35] HE M W, JIN Y, ZHOU R Q, et al.Dynamic succession of microbial community in Nongxiangxing Daqu and microbial roles involved in flavor formation[J].Food Research International, 2022, 159:111559.
[36] HE G Q, XIE F, REN X, et al.Revealing the functional microbiota for acetic acid formation in Daqu starter for Chinese Nong-Xiang baijiu fermentation[J].Food Bioscience, 2023, 53:102782.
[37] XU Y Q, ZHAO J R, LIU X, et al.Flavor mystery of Chinese traditional fermented Baijiu:The great contribution of ester compounds[J].Food Chemistry, 2022, 369:130920.
[38] TONG W H, LI Y Y, YANG Y, et al.Dynamic analysis caffeic acid production driven by the key physicochemical factor and microbial community succession in Baijiu Daqu:A multi-microorganism fermentation of solid-state fermentation system[J].LWT, 2023, 190:115542.
[39] TONG W H, WANG S Q, YANG Y, et al.Insights into the dynamic succession of microbial community and related factors of vanillin content change based by high-throughput sequencing and Daqu quality drivers[J].Foods, 2023, 12(23):4312.
[40] MU Y, HUANG J, ZHOU R Q, et al.Comprehensive analysis for the bioturbation effect of space mutation and biofortification on strong-flavor Daqu by high-throughput sequencing, volatile analysis and metabolomics[J].Food Chemistry, 2023, 403:134440.