单增李斯特菌(Listeria monocytogenes)是革兰氏阳性兼性厌氧菌,是一种危害性很大的食源性致病菌,广泛存在于日常的环境和食品中,同时孕妇、儿童等高风险人群极易感染单增李斯特菌[1-2];在食品加工过程中,单增李斯特菌可在复杂的食品环境中形成生物被膜,黏附在玻璃、不锈钢和塑料等表面上难以被清理,污染可持续数年之久[3];与浮游状态下的细菌相比,形成生物被膜的细菌通过聚集、相互作用和产生胞外聚合物(多糖、蛋白质等)从而对环境的抵抗能力更强,例如对消毒剂和抗生素的抗性、抵抗干燥等[4]。单增李斯特菌的致病性主要与多种毒力岛基因有关,其中包括LIPI-1、LIPI-2两种主要毒力岛基因[5],LIPI-1中含有prfA、actA等毒力基因,prfA能促进单增李斯特菌生物被膜的形成,actA能影响单增李斯特菌的黏附性和生物膜形成;LIPI-2含有inlA、inlB、inlC等毒力基因,LIPI-2毒力岛基因产生的膜蛋白Inl A、Inl B等是单增李斯特菌在感染宿主时所必须的,并且能促进单增李斯特菌生物被膜的形成,提高其对复杂环境的抗逆性[6]。
群体感应(quorum sensing,QS)是一种细菌通讯现象,细菌分泌QS信号分子(quorum sensing molecules,QSM),其随着细菌密度的增长而增加,当信号分子到达阈值时,信号分子则能与受体结合并通过一系列的反应调控生理活动,例如生物被膜形成,各种抗菌物质形成等[7]。单增李斯特菌QS系统主要有2种:(a)由自诱导剂-2(autoinducer-2,AI-2)介导的QS系统;(b)由自诱导肽(autoinducer peptide,AIP)介导的QS系统[8];AI-2是单增李斯特菌主要的QS信号分子,是由luxS基因编码产生的[9]。因此可以通过影响单增李斯特菌的QS系统来抑制AI-2的产生,从而抑制生物被膜形成[10]。
乳酸菌(lactic acid bacteria,LAB)是一种被食品行业公认安全的有益菌,在人体肠道中普遍存在,是人体不可缺少的重要菌群[11]。乳酸菌分泌的乳酸、胞外多糖、细菌素等物质能够对致病菌的生长和生物被膜的形成产生一定的抑制作用[12]。GÖKSEL等[13]制备植物乳杆菌M16、双栖乳杆菌M24、长双歧杆菌M23等的无细胞上清液,能够抑制鼠伤寒沙门氏菌14028生物被膜的形成;KIYMACI等[14]从新生物粪便中分离的乳酸片球菌M17,从其发酵液中提取的乳酸能够抑制铜绿假单胞菌QS系统信号分子的产生,从而抑制其生物被膜产生,具有良好QS淬灭作用。与传统抗生素相比,乳酸菌源QS淬灭剂效果好且不容易产生菌株耐药性。因此,本研究通过制备戊糖乳杆菌Z097的乙酸乙酯提取物(Z097-E),考察其对单增李斯特菌的QS系统和生物被膜的抑制效果,为开发抗单增李斯特菌的天然抑菌剂提供数据参考。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株
单增李斯特菌ATCC19115、哈维氏弧菌(Vibrio harveyi)BB170,广东省微生物研究所微生物菌种保藏中心;戊糖乳杆菌Z097为实验室前期分离纯化鉴定和保藏的菌株。以上所用菌株均保藏于-80 ℃冰箱中。
1.1.2 主要实验材料与试剂
胰蛋白胨、脑心浸出液肉汤(brain heart infusion,BHI)、牛肉膏、酵母粉、琼脂粉,广东环凯生物技术有限公司;酸水解酪蛋白、结晶紫,上海麦克林生化科技有限公司;Bradford蛋白质浓度测定试剂盒,北京索莱宝科技有限公司;FITC-ConA染料,西格玛奥德里奇(上海)贸易有限公司;细菌活力/毒性检测试剂盒,苏州优逸兰迪生物科技有限公司。
1.2 仪器与设备
1285型生物安全柜,美国Thermo Electron公司;TS-200B恒温摇床,上海天呈实验仪器制造有限公司;5417R超高速冷冻离心机,德国Eppendorf公司;R1001-VN旋转蒸发仪,郑州长城科工贸有限公司;Scientz-12 N冷冻干燥机,宁波新芝生物科技股份有限公司;IVD型Multiskan酶标仪,赛默飞世尔(上海)仪器有限公司;Axio Observer A1荧光倒置显微镜,德国Zeiss公司。
1.3 实验方法
1.3.1 培养基的配制
MRS培养基(g/L):葡萄糖20、胰蛋白胨10、牛肉膏5、酵母粉4、K2HPO4 1.52、乙酸钠3.53、柠檬酸三胺2、MgSO4 0.2,MnSO4 0.003 8;吐温-80 1.0 mL,pH值为6.0,121 ℃灭菌30 min。
AB培养基(g/L):MgSO4 26、NaCl 17.5、酸水解酪蛋白2;用NaOH溶液调节pH值为7.5,121 ℃灭菌30 min。冷却后,加入无菌的10 mL 1 mol/L K2HPO4溶液(pH值为7.5)、10 mL 0.1 mol/L的L-精氨酸溶液(pH值为7.5)和20 mL体积分数为50%甘油。
BHI培养基(g/L):BHI培养基粉末37.6;调整pH值至7.4±0.2(制备固体培养基加入琼脂粉15~20 g),121 ℃灭菌30 min。
1.3.2 菌株活化
戊糖乳杆菌Z097按2%体积比接种于MRS培养基中,37 ℃静置培养12 h;单增李斯特菌按2%体积比接种于BHI培养基,37 ℃、150 r/min振荡培养24 h,哈维氏弧菌BB170按2%体积比接种于AB培养基,30 ℃、90 r/min振荡培养12 h。所有实验菌株均活化3代后使用。
1.3.3 戊糖乳杆菌Z097乙酸乙酯提取物的制备
参照MOMO等[15]的方法制备Z097的乙酸乙酯提取物。Z097经活化后,接种于200 mL的新鲜MRS培养基,37 ℃培养24 h。在4 ℃、12 000 r/min条件下离心30 min,过0.45 μm滤膜除菌,得到Z097无细胞上清溶液。将Z097上清液和乙酸乙酯等比例混合,180 r/min振荡混匀2 h后倒入分液漏斗中静置30 min,收集有机相,此操作重复3次。将多次分离后的有机相合并后,在旋转蒸发器中除去乙酸乙酯,收集剩余溶液进行冻干后为戊糖乳杆菌Z097乙酸乙酯提取物,记为Z097-E。
1.3.4 Z097-E对单增李斯特菌生长的最小抑菌浓度(minimum inhibitory concentration,MIC)测定影响
单增李斯特菌活化培养后调整菌浓度为106 CFU/mL,将冻干后的乳酸菌乙酸乙酯提取物Z097-E溶于BHI培养基中,配制成25.6 mg/mL的工作液,将工作液通过二倍稀释法稀释成6.4、3.2、1.6、0.8、0.4、0.2 mg/mL的BHI培养基,过0.22 μm滤膜除菌后各取200 μL于96孔板中,将调整好菌浓度的单增李斯特菌按2%体积比接入孔板中,以不接种单增李斯特菌的BHI培养基作阴性对照。37 ℃静置培养24 h测定OD595nm。以抑制单增李斯特菌生长的最小浓度为MIC。
1.3.5 Z097-E对单增李斯特菌自聚性和细胞表面疏水性的影响
单增李斯特菌活化后接种于含有不同质量浓度Z097-E(3.2、1.6、0.8、0 mg/mL)的BHI培养基中37 ℃培养24 h。于4 ℃、12 000 r/min条件下离心10 min,用无菌PBS溶液重悬菌体2次,此时菌液的OD595nm读数记作H0或A0。将菌液分为两部分,一部分振荡混匀后于37 ℃恒温水浴锅静置2 h,测定菌液OD595nm,记作At,并按照公式(1)计算其自动聚集性。
自聚率![]()
(1)
式中:A0,初始菌悬液的吸光度;At,静置后菌悬液的吸光度。
另一部分与二甲苯振荡混匀,于37 ℃恒温水浴锅静置15 min,移液枪吸取水相测定OD595nm并记作Ht,并按照公式(2)计算细胞疏水性。
疏水率![]()
(2)
式中:H0,初始菌悬液的吸光度;Ht,加入二甲苯混合后水相的吸光度。
1.3.6 Z097-E对单增李斯特菌运动性的影响
在试管内配制琼脂含量为0.4%、添加不同质量浓度的Z097-E(3.2、1.6、0.8、0 mg/mL)的BHI半固体培养基,将单增李斯特菌穿刺接种于半固体培养基中,在25 ℃下培养48 h,观察其对单增李斯特菌运动性的影响[16]。
1.3.7 Z097-E对单增李斯特菌生物被膜形成的影响
采用结晶紫染色法[17]测定生物被膜的生物量,在96孔板中分别添加200 μL含有3.2、1.6、0.8、0 mg/mL(对照)Z097-E的BHI培养基,在培养基中按2%体积比接种单增李斯特菌(终浓度为106 CFU/mL),在37 ℃下静置培养24和48 h,将培养完成后的中上层浮游菌液吸出,用PBS溶液洗涤孔板3次,于60 ℃烘箱干燥固定30 min,用质量分数为0.1%的结晶紫染色5 min,用PBS溶液洗涤孔板3次,用330 g/L冰乙酸脱色10 min后,酶标仪测定OD595nm并记录,按照公式(3)计算抑制率。
抑制率![]()
(3)
式中:OD对照组,未用Z097-E处理生物被膜的吸光度;OD处理组,Z097-E处理后生物被膜的吸光度。
1.3.8 Z097-E对单增李斯特菌胞外多糖的影响
采用苯酚-硫酸法测定胞外多糖[18],将1 mL不同质量浓度的Z097-E(3.2、1.6、0.8、0 mg/mL)加入24孔板中,将单增李斯特菌接种于孔内(终浓度为106 CFU/mL),并加入无菌盖玻片(12 mm×12 mm),37 ℃静置培养24 h后用镊子取出盖玻片放置于50 mL离心管中,加入1 mL生理盐水振荡洗脱30 s,经超声波处理30 s后二次振荡洗脱30 s,在8 000 r/min条件下离心30 min,收集上清液。取1 mL上清液加入等量质量分数为5%苯酚溶液,混匀后加入5 mL的浓硫酸,避光反应10 min后测定OD490nm,按照公式(3)计算抑制率。
1.3.9 Z097-E对单增李斯特菌胞外蛋白的影响
使用Bradford蛋白质浓度测定试剂盒测定单增李斯特菌胞外蛋白含量[19]。调整活化后单增李斯特菌浓度至106 CFU/mL,按2%体积比接种于含不同质量浓度Z097-E(3.2、1.6、0.8 mg/mL)的BHI培养基中,37 ℃培养24 h后,在12 000 r/min条件下离心10 min,过0.22 μm滤膜收集上清液。取20 μL制备的上清液加入96孔板,再添加200 μL考马斯亮蓝G-250染料,室温下静置5 min测定OD595nm,按照公式(3)计算抑制率。
1.3.10 Z097-E对单增李斯特菌AI-2信号分子的影响
采用哈维氏弧菌BB170生物发光法检测AI-2信号分子。哈维氏弧菌活化后培养至12 h,用新鲜AB培养基按1∶5 000体积比例稀释菌液形成菌悬液。单增李斯特菌活化后接种于含有不同质量浓度Z097-E的BHI培养基中37 ℃培养24 h,在4 ℃、12 000 r/min条件下离心10 min,过0.22 μm滤膜收集上清液,然后与哈维氏弧菌悬液按照1∶50体积比例混合。30 ℃,100 r/min孵育3~4 h,取200 μL于96孔黑色酶标板中,以哈维氏弧菌无细胞上清液为阳性对照,无菌AB培养基为阴性对照,无菌BHI为介质对照。使用连续波长多功能微孔板检测平台测定哈维氏弧菌生物发光情况,按照公式(4)计算抑制率。
抑制率![]()
(4)
1.3.11 Z097-E对单增李斯特菌成熟生物被膜的清除能力
将单增李斯特菌(终浓度为106CFU/mL)按2%体积比接种于含新鲜无菌BHI培养基的96孔板中,37 ℃培养48 h形成成熟生物被膜,培养结束后除去上层菌液,用PBS溶液洗去96孔板表面的浮游菌。再加入200 μL质量浓度为25.6、12.8、6.4、3.2 mg/mL的Z097-E于37 ℃下孵育24 h和48 h,再以1.3.7节的结晶紫染色法测定生物被膜量,按照公式(5)计算清除率。
清除率![]()
(5)
式中:OD对照组,未用Z097-E处理生物被膜的吸光度;OD处理组,Z097-E处理后生物被膜的吸光度。
1.3.12 倒置荧光显微镜观察生物被膜中细菌和胞外多糖的变化
单增李斯特菌活化后(菌液终浓度为106CFU/mL)取12 μL接种于600 μL含有不同质量浓度Z097-E(3.2、1.6、0.8、0 mg/mL)的BHI培养基中,于8室细胞培养玻片中37 ℃下培养24 h。用PBS溶液轻轻洗去附着在玻片表面的浮游菌,使用活/死细菌染料和伴刀豆蛋白分别染色菌体和胞外多糖,避光处理15 min后使用倒置荧光显微镜观察,绿色荧光使用硫氰酸荧光素(fluorescein isothiocyanate,FITC)适用滤光片观察,红色荧光采用碘化丙啶(propidium iodide,PI)适用滤光片观察,观察胞外多糖的激发波长和发射波长分别为546 nm和575~640 nm。
1.4 数据处理
所有实验重复3次,实验数据以“平均值±标准差”表示,实验结果利用GraphPad Prism 8.0绘图,以SPSS 25.0进行统计学分析,P<0.05为差异具有统计学意义。
2 结果与分析
2.1 Z097-E对单增李斯特菌的MIC值测定
采用96微孔板法测定Z097-E对单增李斯特菌的MIC值,结果如图1所示。单增李斯特菌在含有6.4 mg/mL的Z097-E的BHI培养基中培养24 h后,培养液仍澄清透明,与不含菌的空白培养基(对照)一致,说明Z097-E对单增李斯特菌的MIC值为6.4 mg/mL,具有良好的抑菌性能。相似地,范祥昊等[20]使用乳酸链球菌素对单增李斯特菌的MIC值为3.125 μg/mL;HOSSAIN等[21]以植物乳杆菌M.2和弯曲乳杆菌B.67制得的后生元对单增李斯特菌的MIC值分别为70 mg/mL和80 mg/mL。
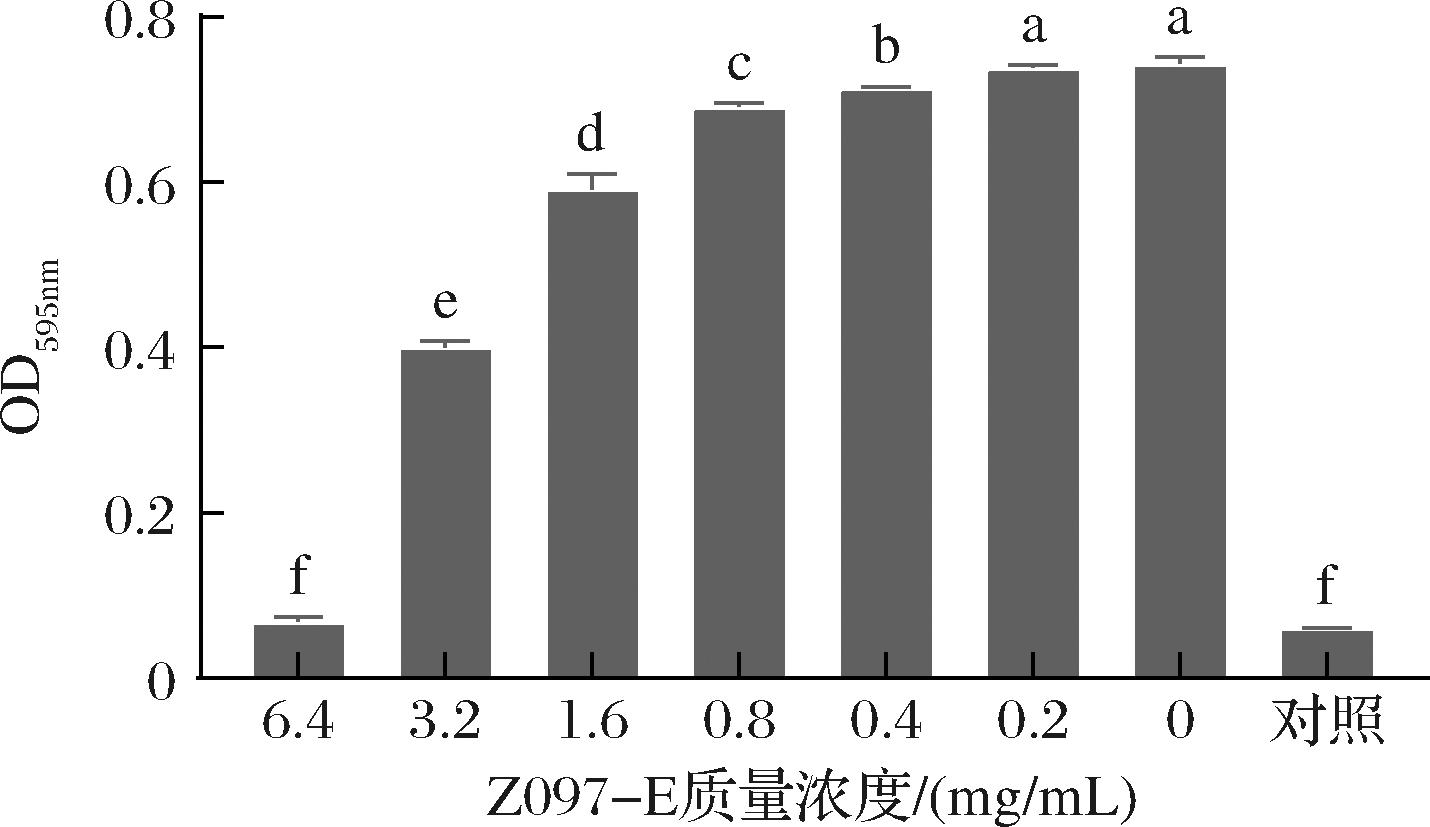
图1 Z097-E对单增李斯特菌的生长的影响
Fig.1 Effects of Z097-E on the growth of L.monocytogenes
注:图柱上方的小写字母相同表示差异不显著(P>0.05),小写字母不同表示差异显著(P<0.05)(图2,图4~图7同)。
2.2 Z097-E对单增李斯特菌自聚性和细胞表面疏水性的影响
食源性致病菌的自动聚集性是食源性致病菌的毒力因子之一,自聚性是构建微生物被膜的第一步,聚集体沉聚在底部启动生物被膜形成[22]。食源性致病菌的细胞表面疏水性是影响初始细胞黏附和生物被膜形成的重要因素,疏水性越高细菌越容易发生黏附效应和形成生物膜[23];通过图2可以看出,经过不同质量浓度Z097-E处理后的单增李斯特菌自动聚集性和细胞表面疏水性均显著下降。经过3.2 mg/mL的Z097-E处理后,细胞的自动聚集率由20.74%下降至5.48%;细胞的表面疏水性由71.72%下降至7.44%。所以,经过Z097-E处理后能显著降低单增李斯特菌的细胞自动聚集性和细胞表面疏水性,降低了致病菌的黏附侵袭能力,且具有量效关系。这一结果与MAO等[24]研究的结果类似,他们发现乳酸菌的无细胞上清液能够降低金黄色葡萄球菌的疏水性。
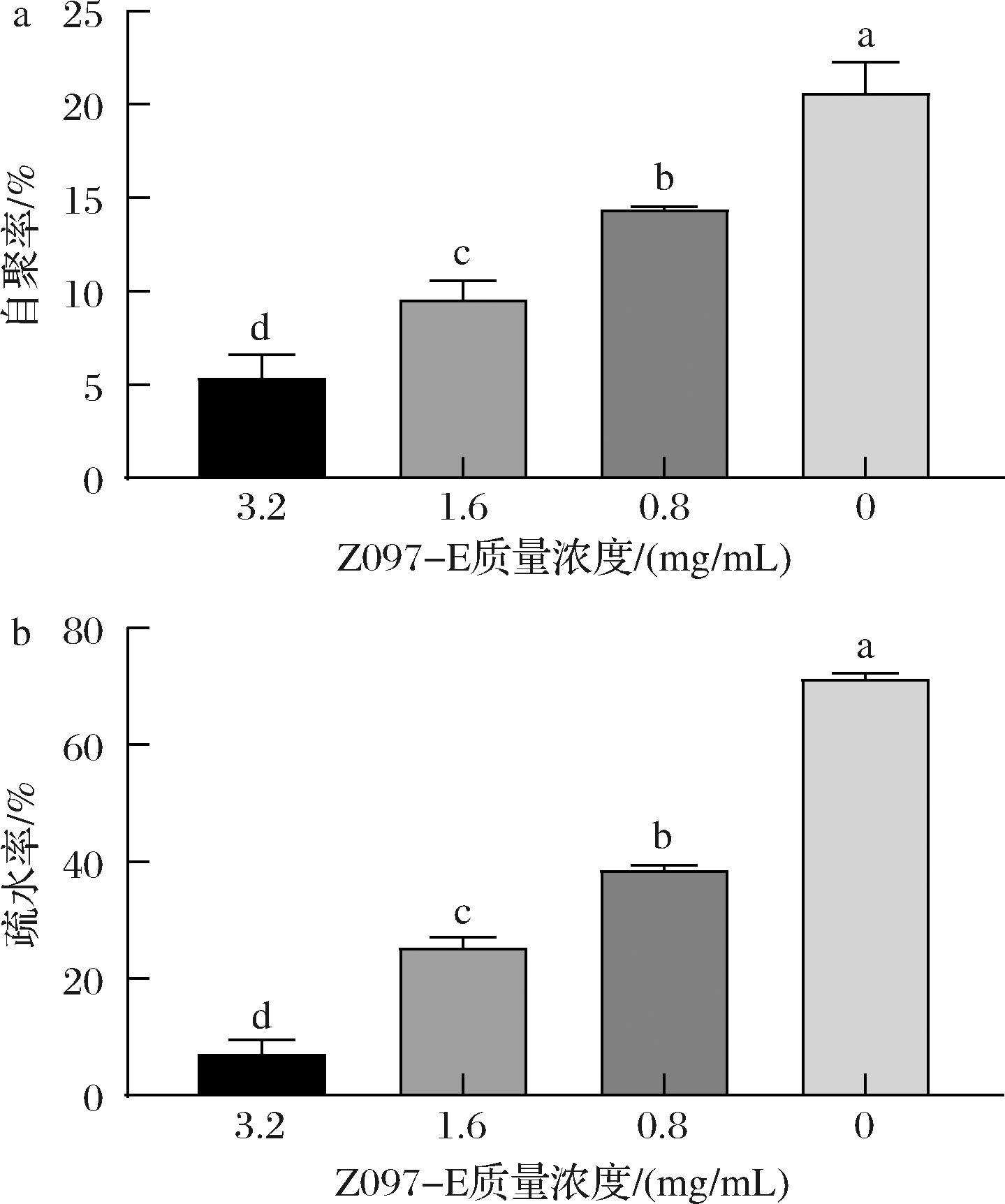
a-自聚性;b-疏水性
图2 Z097-E对单增李斯特菌自聚性和疏水性的影响
Fig.2 Effects of Z097-E on the auto-aggregation and hydrophobicity of L.monocytogenes
2.3 Z097-E对单增李斯特菌运动性的影响
单增李斯特菌是一种周身鞭毛细菌,鞭毛是细菌的运动器官,主要介导细菌的运动、黏附等,帮助细菌附着于生物或非生物表面并迁移到适合自己生长的位置,鞭毛介导的运动性影响生物被膜的形成[25]。由图3可见,添加了Z097-E的培养基中,单增李斯特菌与对照组相比形成的伞状生长线较小,表明Z097-E可以有效抑制单增李斯特菌的运动性。这一结果与黄湘媚等[26]的研究结果相符。
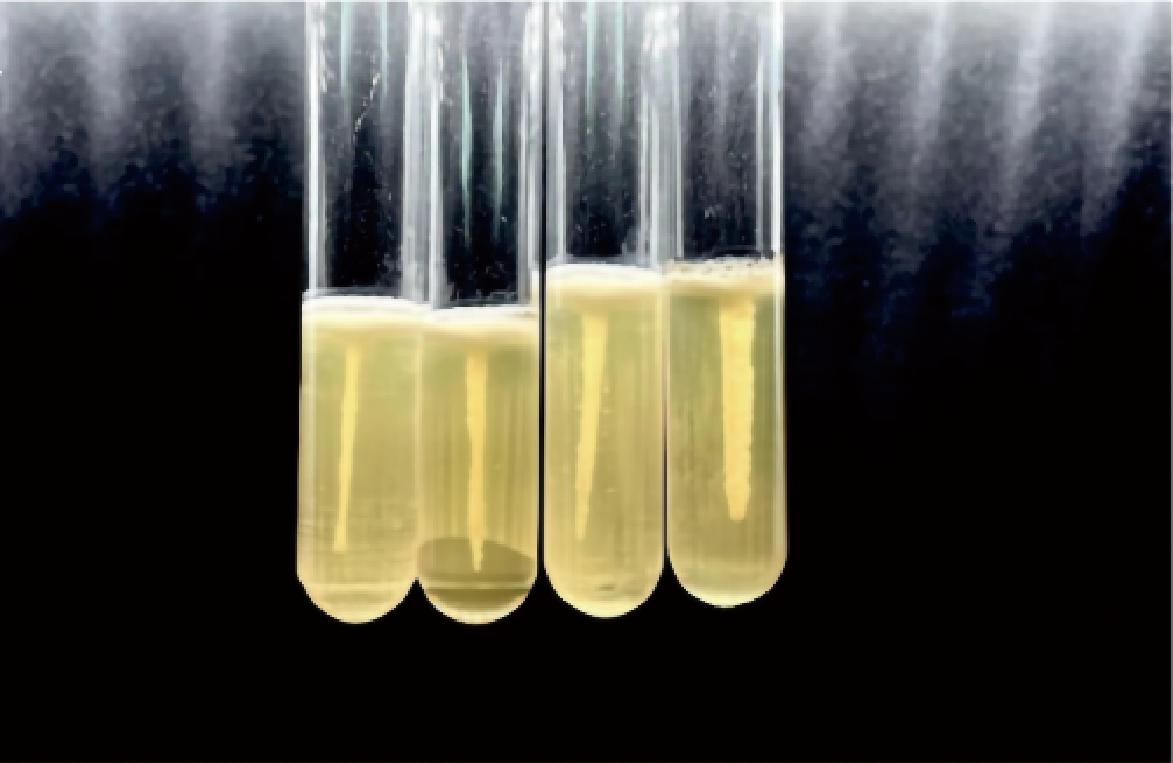
图3 Z097-E对单增李斯特菌运动性的影响
Fig.3 Effects of Z097-E on motility of L.monocytogenes
注:从左到右Z097-E的添加量分别为3.2、1.6、0.8、0 mg/mL。
2.4 Z097-E对单增李斯特菌生物被膜的影响
如图4所示,不同质量浓度的Z097-E能够显著抑单增李斯特菌生物被膜的生成,可以降低生物被膜的生物量并显示出量效关系,但研究发现Z097-E随着作用时间的延长并未出现抑制率明显升高的现象。随着Z097-E质量浓度的增加,抑制效果逐渐增大,在3.2和1.6 mg/mL的Z097-E处理单增李斯特菌24 h后,生物被膜量分别降低52.76%、41.81%;当处理时间达到48 h时,对生物被膜的抑制率为53.77%、41.91%。孙梦桐等[27]发现从传统腌菜中分离的乳酸菌的乙酸乙酯粗提物在16 mg/mL时对嗜水气单胞菌的生物被膜的抑制率为40.9%。
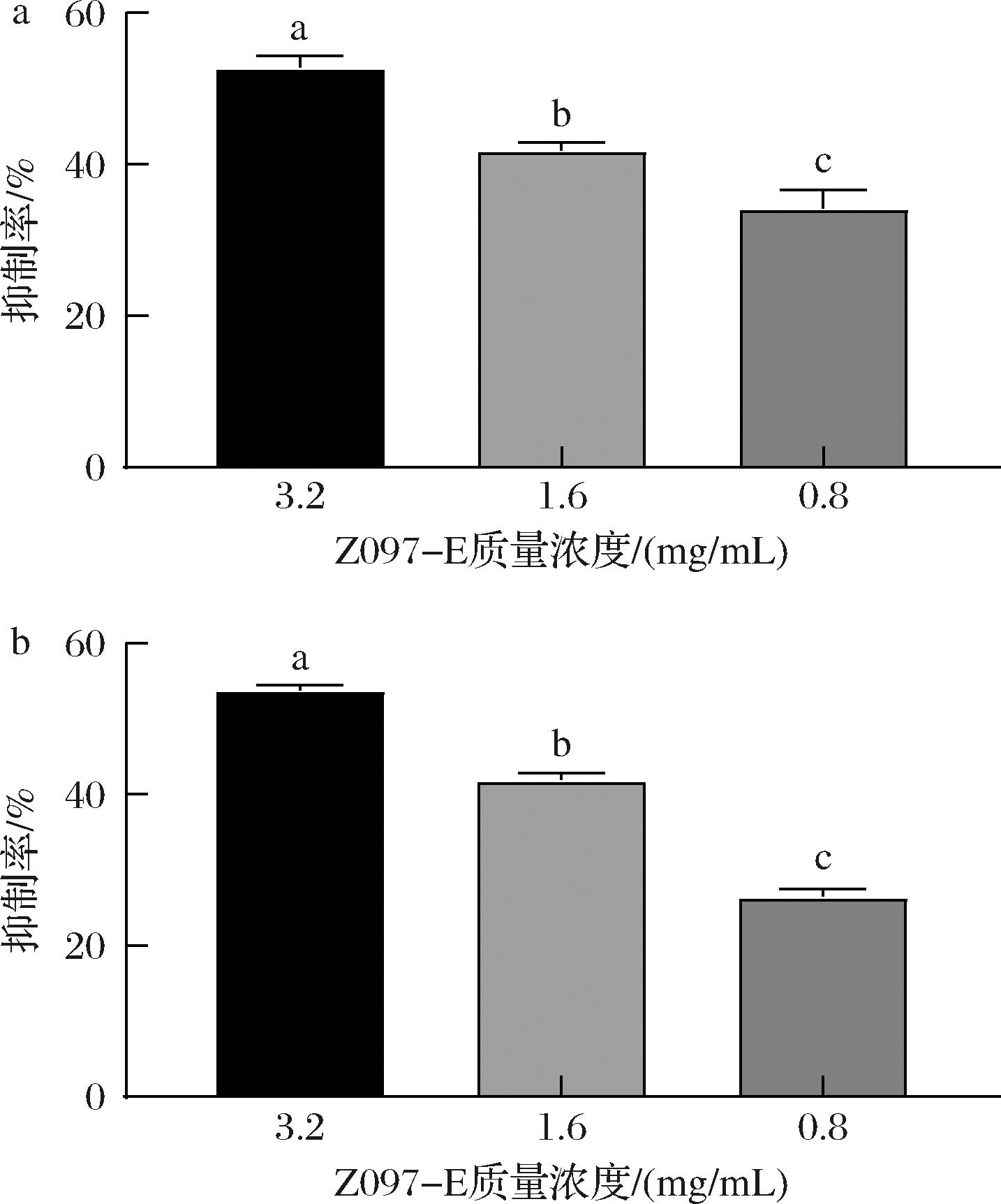
a-24 h;b-48 h
图4 Z097-E对单增李斯特菌生物被膜形成的抑制作用
Fig.4 Inhibitory effects of Z097-E on biofilm formation ofL.monocytogenes
2.5 Z097-E对单增李斯特菌胞外多糖和胞外蛋白的影响
胞外多糖是生物被膜基质的主要成分,能够促进细菌生物被膜快速形成[28]。本研究采用苯酚硫酸法测定多糖含量,得到苯酚硫酸法的标准曲线Y=0.005 3X+0.049 9(R2=0.999 8)。由图5-a可知,随着Z097-E质量浓度的增加,单增李斯特菌胞外多糖含量逐渐减小。在Z097-E添加量分别为3.2和1.6 mg/mL下,对胞外多糖的抑制率分别为80.03%、67.51%。由于细菌分泌的多糖等生物大分子物质是构成生物被膜的关键组分,因此,推测Z097-E通过抑制胞外多糖产生对单增李斯特菌生物被膜的形成产生影响。ADNAN等[29]报道了一种戊糖片球菌产生的表面活性剂,其通过影响生物被膜内细菌细胞的活力和完整性并降低胞外多糖含量以影响生物被膜基质的结构。胞外蛋白的存在是有助于生物被膜结构的稳定性,缺少胞外蛋白会降低生物被膜稳定性并改变生物被膜结构[30]。本研究以Bradford蛋白质浓度试剂盒测定单增李斯特菌胞外蛋白含量,得到蛋白质标准曲线为Y=0.002 227 5X+0.552 5(R2=0.998 8)。由图5-b可知,不同质量浓度的Z097-E作用于单增李斯特菌后能抑制其胞外蛋白的产生,当Z097-E添加量为3.2、1.6、0.8 mg/mL时,对其胞外蛋白抑制率分别为34.23%、26.32%和14.97%。
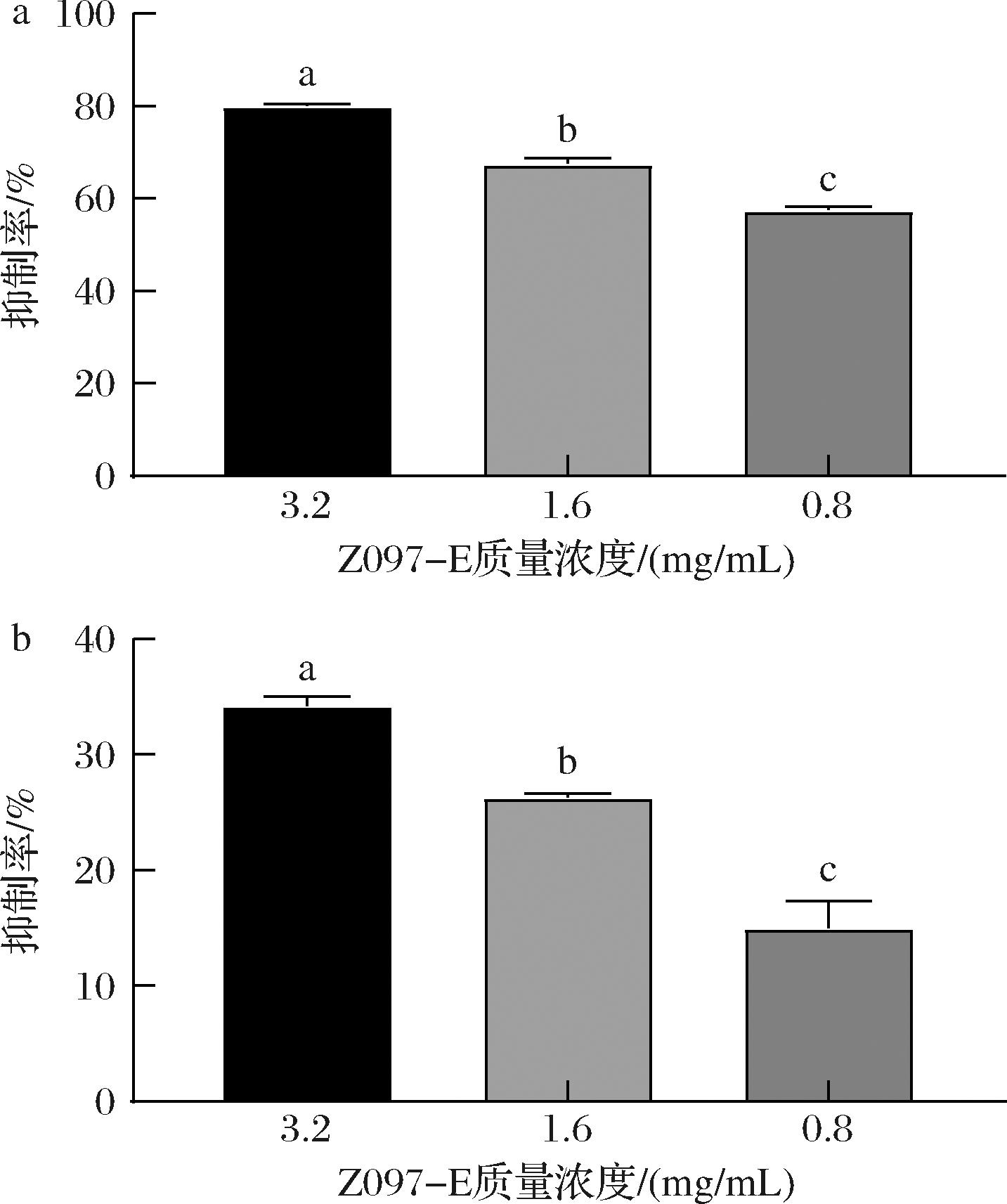
a-菌胞外多糖;b-胞外蛋白
图5 Z097-E对单增李斯特菌胞外多糖和胞外蛋白的抑制作用
Fig.5 Inhibitory effects of Z097-E on extracellular polysaccharide and extracellular proteins of L.monocytogenes
2.6 Z097-E对单增李斯特菌AI-2活性的影响
AI-2是革兰氏阴性与阳性菌共有的QS信号分子,也是促进生物被膜形成的重要因素之一。单增李斯特菌会产生AI-2,使作为标准发光菌株的哈维氏弧菌BB170发光[31]。本研究利用哈维氏弧菌BB170的发光特性,通过发光强度的变化测定不同浓度的Z097-E作用后单增李斯特菌上清液中AI-2信号分子的变化。由图6所示,经过不同质量浓度Z097-E处理后,单增李斯特菌产AI-2信号分子受到抑制,从而减少生物被膜的形成,并随着作用的质量浓度增大表现出量效关系。在Z097-E添加量分别为3.2 mg/mL和1.6 mg/mL下,对单增李斯特菌产AI-2信号分子的抑制率分别为84.43%和60.18%。相似地,YAN等[32]发现从植物乳杆菌17172和乳酸片球菌27167中获得的表面活性剂粗提取物能干扰金黄色葡萄球菌CMCC 26003信号分子AI-2的释放,对其具有良好的抗生物被膜活性。
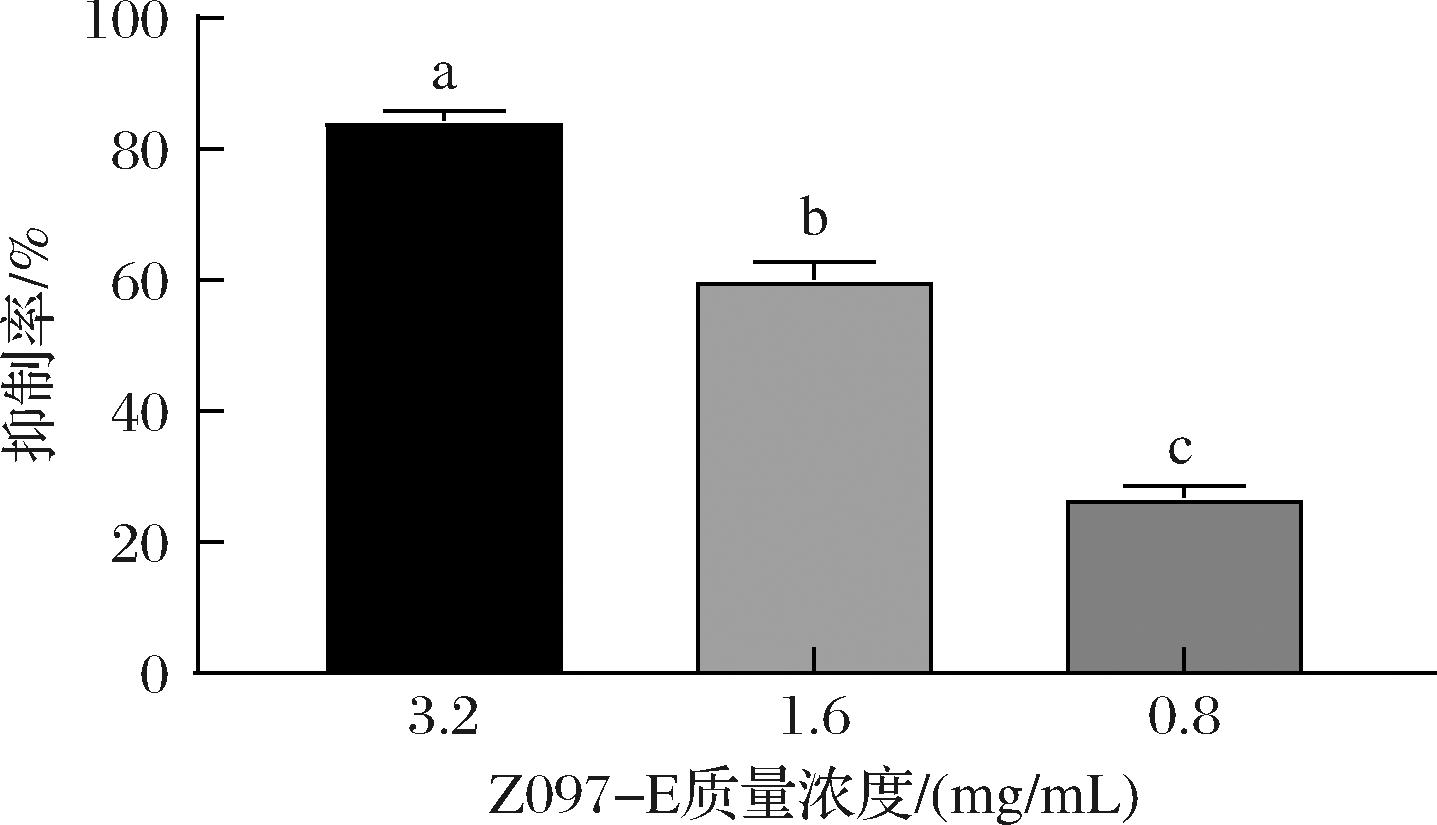
图6 Z097-E对单增李斯特菌AI-2信号分子的影响
Fig.6 Effects of Z097-E on AI-2 signaling molecules ofL.monocytogenes
2.7 Z097-E对单增李斯特菌成熟生物被膜的清除能力
从图7可知,Z097-E对单增李斯特菌生物被膜具有清除效果,当Z097-E的质量浓度为25.6、12.8 mg/mL时,在24 h时的生物被膜清除率分别是36.60%、30.08%;在48 h时的生物被膜清除率分别是76.14%、62.07%。以上结果表明,Z097-E能有效清除单增李斯特菌预成型生物被膜,在48 h时有较好的清除效果,且清除率与Z097-E的质量浓度以及对单增李斯特菌的作用时间呈正相关。
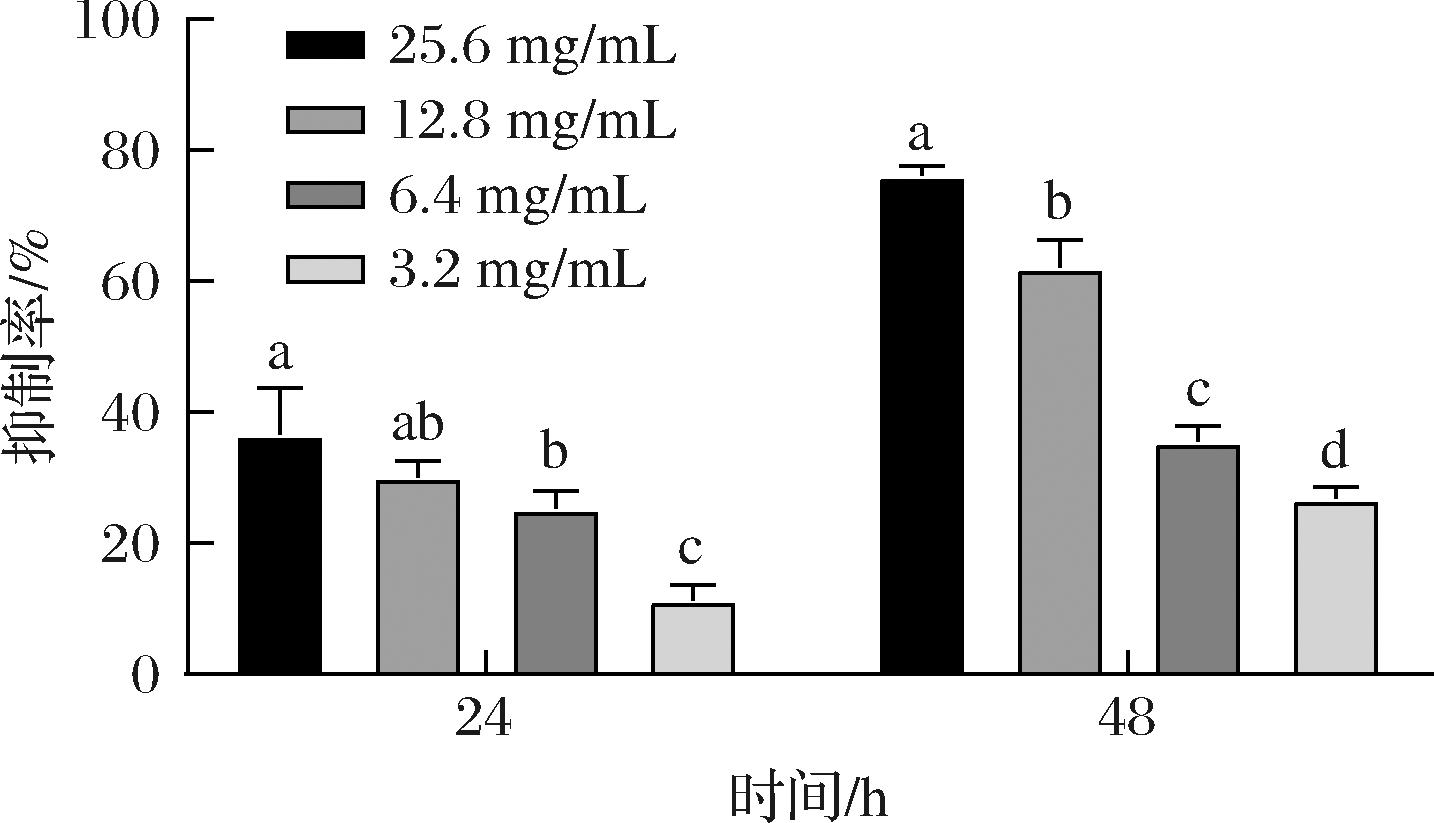
图7 Z097-E对单增李斯特菌成熟生物被膜的清除作用
Fig.7 Elimination effects of Z097-E on mature biofilm ofL.monocytogenes
2.8 倒置荧光显微镜观察生物被膜中细菌和胞外多糖的变化
利用活/死细菌染色试剂盒和伴刀豆蛋白可以直观地观察经Z097-E处理后的单增李斯特菌被膜菌的存活以及生物被膜变化情况。由图8所示,对照组中的生物被膜菌体活性良好,胞外多糖产量高,菌体周围被大量的胞外多糖所包围,生物被膜结构完整,生物被膜致密且厚。经过不同质量浓度的Z097-E处理之后,菌体的存活率大幅度下降,死菌的数量增加,胞外多糖量显著下降。结果表明Z097-E能有效抑制单增李斯特菌胞外多糖产生和生物被膜形成,引起细胞死亡。
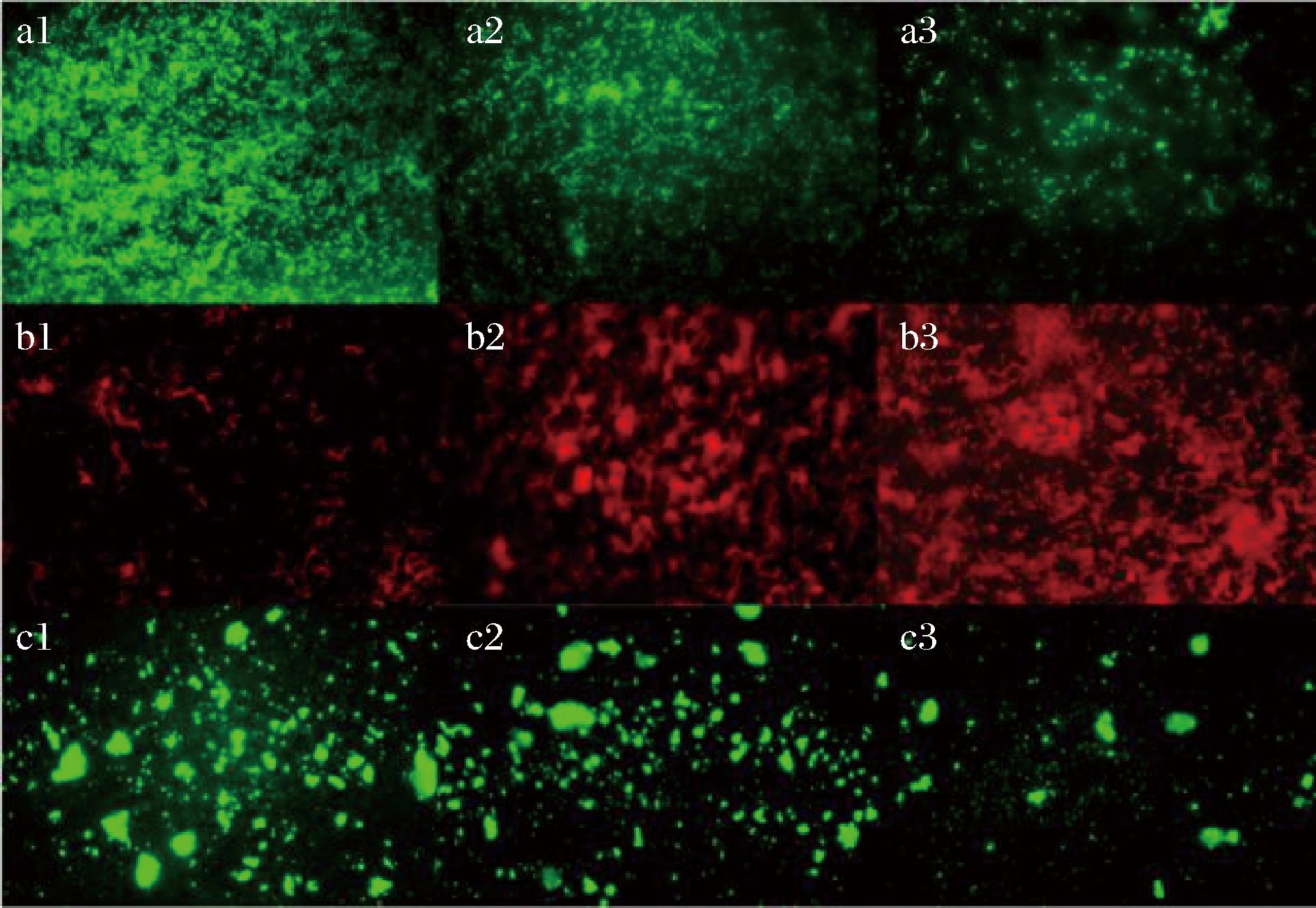
a-活菌;b-死菌;c-EPS
图8 Z097-E对单增李斯特菌生物被膜中的细胞和EPS的影响
Fig.8 Effects of Z097-E on cells and EPS inL.monocytogenes biofilm
注:下标1-3表示Z097-E的添加量分别为0、1.6、3.2 mg/mL。
3 结论与讨论
已有研究发现,一些乳酸菌的乙酸乙酯提取物质对致病菌具有抑制作用,例如AMAN等[33]发现发酵乳杆菌BM-2和戊糖片球菌BS-2的乙酸乙酯提取物具有一定的群体感应抑制剂(quorum sensing inhibitors,QSIs)特性,抑制了铜绿假单胞菌株JUPG01的生长;ABDEL-NASSER等[34]发现植物乳杆菌DSM20、鼠李糖乳杆菌ATCC 7468的乙酸乙酯提取物都表现出了不同程度的抗真菌活性。本研究发现Z097-E对单增李斯特菌的MIC值为6.4 mg/mL,具有良好的抑菌活性。
细菌形成生物被膜增强其对高温、高压、低温和抗生素等不良环境的抗性,而细菌的生物被膜形成是受QS调控的,QS通过特定的信号分子和调节因子来调控细菌的生物被膜形成[35],所以基于QS开发群体感应抑制剂,能够有效地抑制生物被膜的形成[36]。生物被膜的形成是一个动态变化的过程,胞外聚合物为生物被膜提供稳定性并调节细胞之间的相互作用,胞外多糖和胞外蛋白是胞外聚合物的主要成分并构成细胞的保护屏障[37]。本研究结果发现Z097-E能显著抑制单增李斯特菌胞外多糖和胞外蛋白的产生,并抑制和清除其生物被膜。
消毒剂和抗生素的过度使用导致多种耐药菌株的产生,生物被膜的形成也导致致病菌对消毒剂和抗生素的抗性上升,而以群体感应为靶标干扰细菌不会引起细菌产生耐药性,群体感应抑制剂能以较低的剂量干扰病原菌的QS系统,避免了高剂量使用抗菌剂而对人体产生副作用和危害。乳酸菌对病原微生物常见的应用是利用其无细胞上清液中的有机酸、细菌素、生物表面活性剂等活性物质来控制病原微生物及其生物被膜的形成[38]。KOWSALYA等[39]提取的植物乳杆菌PRK7和PRK11的胞外多糖能够抑制金黄色葡萄球菌和铜绿假单胞菌的生物被膜。NATARAJ等[40]研究报道了嗜酸乳杆菌和鼠李糖乳杆菌产生的生物表面活性剂对耐甲氧西林的金黄色葡萄球菌具有抗生物被膜作用。本研究结果发现不同质量浓度的Z097-E能够显著抑制和清除单增李斯特菌生物被膜,同时还能抑制其胞外多糖、胞外蛋白、AI-2活性、自聚性、疏水性、运动性以抑制其生物被膜的形成,并存在量效关系。因此,Z097-E对单增李斯特菌是一种良好的QSI,其可干扰单增李斯特菌的QS系统以控制生物被膜,适宜开发为单增李斯特菌的天然抗菌剂。
[1] 吕素玲, 何源, 周莹冰, 等.食源性单增李斯特菌感染的检测与防控专家共识[J].中国卫生工程学, 2023, 22(3):430-432.LYU S L, HE Y, ZHOU Y B, et al.Expert consensus on the detection and prevention of food-borne Listeria monocytogenes infection [J].Chinese Journal of Public Health Engineering, 2023, 22(3):430-432.
[2] FERRI G, LAUTERI C, FESTINO A R, et al.ARGs detection in Listeria monocytogenes strains isolated from the Atlantic salmon (Salmo salar) food industry:A retrospective study[J].Microorganisms, 2023, 11(6):1509.
[3] MANVILLE E, KAYA E C, YUCEL U, et al.Evaluation of Listeria monocytogenes biofilms attachment and formation on different surfaces using a CDC biofilm reactor[J].International Journal of Food Microbiology, 2023, 399:110251.
[4] PANEBIANCO F, RUBIOLA S, CHIESA F, et al.Effect of gaseous ozone on Listeria monocytogenes planktonic cells and biofilm:An in vitro study[J].Foods, 2021, 10(7):1484.
[5] 李红欢, 陈朔, 康立超, 等.食源性单增李斯特菌毒力岛基因检测与致病性[J].江苏农业科学, 2019, 47(14):193-196.LI H H, CHEN S, KANG L C, et al.Pathogenicity island gene detection and pathogenicity of food-borne Listeria monocytogenes[J].Jiangsu Agricultural Sciences, 2019, 47(14):193-196.
[6] 郝歌, 钱映, 李蓉, 等.单核细胞增生李斯特菌毒力基因及其致病机制的研究进展[J].中国食品卫生杂志, 2023, 35(3):481-486.HAO G, QIAN Y, LI R, et al.Research progress on virulence genes and pathogenesis of Listeria monocytogenes[J].Chinese Journal of Food Hygiene, 2023, 35(3):481-486.
[7] ZENG X Y, ZOU Y M, ZHENG J, et al.Quorum sensing-mediated microbial interactions:Mechanisms, applications, challenges and perspectives[J].Microbiological Research, 2023, 273:127414.
[8] 胡丽丽, 董庆利, 夏阳, 等.单增李斯特菌生物膜形成及其调控机制研究进展[J].食品与发酵工业, 2021, 47(8):276-282.HU L L, DONG Q L, XIA Y, et al.Advances on the formation and regulation mechanism of Listeria monocytogenes biofilm[J].Food and Fermentation Industries, 2021, 47(8):276-282.
[9] BANERJI R, KARKEE A, KANOJIYA P, et al.Bacterial communication in the regulation of stress response in Listeria monocytogenes[J].LWT, 2022, 154:112703.
[10] OLOKETUYI S F, KHAN F.Inhibition strategies of Listeria monocytogenes biofilms—Current knowledge and future outlooks[J].Journal of Basic Microbiology, 2017, 57(9):728-743.
[11] ZAPA NIK A, SOKO
NIK A, SOKO OWSKA B, BRY
OWSKA B, BRY A M.Role of lactic acid bacteria in food preservation and safety[J].Foods, 2022, 11(9):1283.
A M.Role of lactic acid bacteria in food preservation and safety[J].Foods, 2022, 11(9):1283.
[12] 蒋大成, 郝沛研, 程文, 等.发酵食品中乳酸菌的作用探讨[J].食品安全导刊, 2023(7):99-101.JIANG D C, HAO P Y, CHENG W, et al.Discussion on the function of lactic acid bacteria in fermented food[J].China Food Safety Magazine, 2023(7):99-101
[13] GÖKSEL  , AKÇELIK N, ÖZDEMIR C, et al.The effects of lactic acid bacteria on Salmonella biofilms[J].Microbiology, 2022, 91(3):278-285.
, AKÇELIK N, ÖZDEMIR C, et al.The effects of lactic acid bacteria on Salmonella biofilms[J].Microbiology, 2022, 91(3):278-285.
[14] KIYMACI M E, ALTANLAR N, GUMUSTAS M, et al.Quorum sensing signals and related virulence inhibition of Pseudomonas aeruginosa by a potential probiotic strain’s organic acid[J].Microbial Pathogenesis, 2018, 121:190-197.
[15] MOMO C H K, MBOUSSAAH A D K, FRANÇOIS ZAMBOU N, et al.New pyran derivative with antioxidant and anticancer properties isolated from the probiotic Lactobacillus plantarum H24 strain[J].Natural Product Research, 2022, 36(4):909-917.
[16] 吴雅茜. 单增李斯特菌群体感应抑制剂的筛选及控制效应研究[D].湛江:广东海洋大学, 2019.WU Y Q.Screening and control effects of quorum sensing inhibitors of Listeria monocytogenes[D].Zhanjiang:Guangdong Ocean University, 2019.
[17] NGUYEN TRANG P, THI ANH NGOC T, MASUDA Y, et al.Biofilm formation from Listeria monocytogenes isolated from Pangasius fish-processing plants[J].Journal of Food Protection, 2023, 86(3):100044.
[18] WANG J B, YU L Y, ZENG X, et al.Screening of probiotics with efficient α-glucosidase inhibitory ability and study on the structure and function of its extracellular polysaccharide[J].Food Bioscience, 2022, 45:101452.
[19] 韩翔鹏, 陈清莹, 张杏果, 等.粪肠球菌Z096对副溶血弧菌生物被膜及群体感应的抑制作用[J].食品工业科技, 2022, 43(19):167-176.HAN X P, CHEN Q Y, ZHANG X G, et al.Inhibitory effects of Enterococcus faecalis Z096 on biofilm and quorum sensing of Vibrio parahaemolyticus[J].Science and Technology of Food Industry, 2022, 43(19):167-176.
[20] 范祥昊, 李金兰, 房帅虎, 等.乳酸链球菌素对单增李斯特菌生物膜的杀灭效果研究[J].中国消毒学杂志, 2023, 40(10):725-727;732.FAN X H, LI J L, FANG S H, et al.Study on the killing effect of nisin on Listeria monocytogenes biofilm[J].Chinese Journal of Disinfection, 2023, 40(10):725-727;732.
[21] HOSSAIN M I, MIZAN M F R, ROY P K, et al.Listeria monocytogenes biofilm inhibition on food contact surfaces by application of postbiotics from Lactobacillus curvatus B.67 and Lactobacillus plantarum M.2[J].Food Research International, 2021, 148:110595.
[22] TRUNK T, KHALIL H S, LEO J C.Bacterial autoaggregation[J].AIMS Microbiology, 2018, 4(1):140-164.
[23] KIM B R, BAE Y M, HWANG J H, et al.Biofilm formation and cell surface properties of Staphylococcus aureus isolates from various sources[J].Food Science and Biotechnology, 2016, 25(2):643-648.
[24] MAO Y N, WANG Y X, LUO X F, et al.Impact of cell-free supernatant of lactic acid bacteria on Staphylococcus aureus biofilm and its metabolites[J].Frontiers in Veterinary Science, 2023, 10:1184989.
[25] 李孟华, 闫帅帅, 李德志, 等.单增李斯特菌生物膜形成调控机制的研究进展[J].生物工程学报, 2021, 37(9):3151-3161.LI M H, YAN S S, LI D Z, et al.Advances on the mechanisms regulating the formation of the biofilm of Listeria monocytogenes[J].Chinese Journal of Biotechnology, 2021, 37(9):3151-3161.
[26] 黄湘湄, 吴雅茜, 刘颖, 等.海洋源乳酸菌AI-2类群体感应抑制剂对单增李斯特菌抑制效果研究[J].生物技术通报, 2019, 35(4):36-42.HUANG X M, WU Y Q, LIU Y, et al.Inhibitory effects of AI-2 quorum sensing inhibitors from marine lactic acid bacteria on Listeria monocytogenes[J].Biotechnology Bulletin, 2019, 35(4):36-42.
[27] 孙梦桐, 吕欣然, 林洋, 等.传统腌渍蔬菜中抑制嗜水气单胞菌群体感应及生物膜形成乳酸菌的筛选[J].中国食品学报, 2020, 20(7):172-180.SUN M T, LYU X R, LIN Y, et al.Screening of lactic acid bacteria inhibiting quorum sensing and biofilm of Aeromonas hydrophila in Chinese traditional pickled vegetables[J].Journal of Chinese Institute of Food Science and Technology, 2020, 20(7):172-180.
[28] ZHANG J C, WU H J, WANG D, et al.Intracellular glycosyl hydrolase PslG shapes bacterial cell fate, signaling, and the biofilm development of Pseudomonas aeruginosa[J].eLife, 2022, 11:e72778.
[29] ADNAN M, SIDDIQUI A J, HAMADOU W S, et al.Functional and structural characterization of Pediococcus pentosaceus-derived biosurfactant and its biomedical potential against bacterial adhesion, quorum sensing, and biofilm formation[J].Antibiotics, 2021, 10(11):1371.
[30] FONG J, YILDIZ F.Biofilm matrix proteins[J].Microbiology Spectrum, 2015, 3(2):10-26.
[31] 张君怡, 王静怡, 郑学琪, 等.AI-2信号分子对单增李斯特菌生物被膜形成过程的影响[J].食品科技, 2021, 46(8):319-324.ZHANG J Y, WANG J Y, ZHENG X Q, et al.Effects of AI-2 signaling molecules on the formation of Listeria monocytogenes biofilm[J].Food Science and Technology, 2021, 46(8):319-324.
[32] YAN X, GU S S, CUI X Y, et al.Antimicrobial, anti-adhesive and anti-biofilm potential of biosurfactants isolated from Pediococcus acidilactici and Lactobacillus plantarum against Staphylococcus aureus CMCC26003[J].Microbial Pathogenesis, 2019, 127:12-20.
[33] AMAN M, ANEEQHA N, BRISTI K, et al.Lactic acid bacteria inhibits quorum sensing and biofilm formation of Pseudomonas aeruginosa strain JUPG01 isolated from rancid butter[J].Biocatalysis and Agricultural Biotechnology, 2021, 36:102115.
[34] ABDEL-NASSER A, HATHOUT A S, BADR A N, et al.Extraction and characterization of bioactive secondary metabolites from lactic acid bacteria and evaluating their antifungal and antiaflatoxigenic activity[J].Biotechnology Reports, 2023, 38:e00799.
[35] 刘雪晴, 吕欣然, 白凤翎, 等.基于群体感应的弧菌生物膜形成、耐药性及其控制研究进展[J].食品工业科技, 2023, 44(2):445-452.LIU X Q, LYU X R, BAI F L, et al.Biofilm formation, antimicrobial resistance and control of Vibrio based on quorum sensing:A review[J].Science and Technology of Food Industry, 2023, 44(2):445-452.
[36] VASHISTHA A, SHARMA N, NANAJI Y, et al.Quorum sensing inhibitors as therapeutics:Bacterial biofilm inhibition[J].Bioorganic Chemistry, 2023, 136:106551.
[37] PINTO R M, SOARES F A, REIS S, et al.Innovative strategies toward the disassembly of the EPS matrix in bacterial biofilms[J].Frontiers in Microbiology, 2020, 11:952.
[38] MGOMI F C, YANG Y R, CHENG G, et al.Lactic acid bacteria biofilms and their antimicrobial potential against pathogenic microorganisms[J].Biofilm, 2023, 5:100118.
[39] KOWSALYA M, VELMURUGAN T, MYTHILI R, et al.Extraction and characterization of exopolysaccharides from Lactiplantibacillus plantarum strain PRK7 and PRK 11, and evaluation of their antioxidant, emulsion, and antibiofilm activities[J].International Journal of Biological Macromolecules, 2023, 242:124842.
[40] NATARAJ B H, RAMESH C, MALLAPPA R H.Characterization of biosurfactants derived from probiotic lactic acid bacteria against methicillin-resistant and sensitive Staphylococcus aureus isolates[J].LWT, 2021, 151:112195.