两歧双歧杆菌(Bifidobacterium bifidum)是无芽孢、不运动、异型发酵的革兰氏阳性细菌,作为人类肠道中常见的双歧杆菌之一,在母乳喂养婴儿肠道中相对丰度较高(10.7%),通常被认为可以促进人类健康并可被用作益生菌[1-2]。联合国粮食及农业组织(Food and Agriculture Organization,FAO)和世界卫生组织(World Health Organization,WHO)将益生菌定义为“当摄取足够数量时,能够给予宿主健康益处的活的微生物”[3]。益生菌通常在宿主营养、肠道pH、细胞增殖分化和免疫等方面发挥积极作用。
B.bifidum作为从人体肠道中分离出来的益生菌物种之一,多项动物和临床研究表明B.bifidum通过调节肠上皮紧密连接(tight junctions, TJ)屏障,保护其免受肿瘤坏死因子(tumornecrosisfactor,TNF)-α诱导的破坏,维持上皮TJ的完整性,增强肠上皮屏障功能,从而发挥对宿主的益生作用(如减少肠综合征、改善免疫、抑制病原菌感染等)[4-6]。这种增强主要通过增加Toll样受体(toll-like receptor, TLR)2介导Toll相互作用蛋白(toll-interacting protein,TOLLIP)实现[5]。在Caco-2 细胞上进行的研究表明,B.bifidum可通过增加激活芳香烃受体(aryl hydrocarbon receptor, AHR)通路的吲哚-3-乳酸的产生,激活AHR,上调附属蛋白-1和claudin蛋白4,从而增强上皮屏障功能[4]。此外,B.bifidum上调短链脂肪酸的产生也有助于恢复上皮TJ屏障[4]。一些B.bifidum菌株,如BGN4、TMC3115已经进行了充分的体外、体内和临床研究,证实了在生物催化、细胞黏附、免疫调节等方面的作用,并且B.bifidum BGN4被用作营养保健品和乳制品发酵剂主要成分[6-7]。B.bifidum B1628从健康婴儿粪便样本中分离得到,具有较好的耐酸性和胆盐耐受性,动物实验表明其能够有效地改善葡聚糖硫酸钠(dextran sulfate sodium, DSS)诱导的结肠炎小鼠的炎症状态和组织损伤[8],但其基因组还未得到全面解析。
本研究对B.bifidum B1628进行全基因组测序、组装,结合来自多个国家和地区的B.bifidum菌株进行比较基因组分析,探究其遗传背景和进化历程,通过与充分研究的B.bifidum BGN4和TMC3115进行基因组功能注释比较,探究3株菌的功能差异,并解析B1628的功能基因图谱,挖掘其潜在益生基因,为菌株进一步开发及产业化提供数据参考。
1 材料与方法
1.1 细菌菌株培养、DNA提取和基因组测序
B.bifidum B1628最初是从健康婴儿粪便样本中分离出来,保存于内蒙古农业大学乳酸菌菌株资源库(Lactic Acid Bacteria Collection Center, LABCC),并由中国微生物菌种保藏管理中心保藏(CGMCC 22598)。菌株在37 ℃ RCM液体培养基厌氧条件培养48 h,4 000×g离心5 min收集菌体,磷酸盐缓冲盐溶液洗涤两次。使用STE法进行DNA提取,使用NanoDrop紫外-可见分光光度计在260 nm处测定DNA浓度。构建文库,通过Illumina NovaSeq 6000和Oxford Nanopore PromethION 24平台进行二代和三代全基因组测序。
1.2 基因组测序组装及下载
将Nanopore测序所得到的原始数据进行质控,获得高质量序列,通过NextDenovo[9]对B.bifidum B1628序列进行基因组组装,使用Circlator(V1.5.5)[10]对组装完成的基因组进行环化,并利用Pilon软件[11]通过二代数据对组装结果进行校正,从而得到B.bifidum B1628全基因组完成图。
119株B.bifidum 全基因组序列从NCBI Refseq数据库下载(2023年5月8日),120株B.bifidum全基因组序列基本信息见电子增强出版附表1(https://doi/org/10.13995/j.cnki.11-1802/ts.038536)。
表1 三株B.bifidum.基因组原噬菌体
Table 1 Genomic prophages of three B.bifidum strains
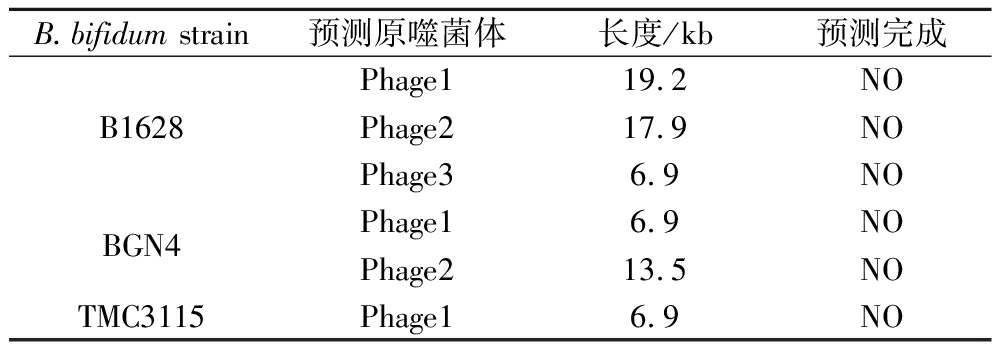
B.bifidum strain预测原噬菌体长度/kb预测完成B1628Phage119.2NOPhage217.9NOPhage36.9NOBGN4Phage16.9NOPhage213.5NOTMC3115Phage16.9NO
1.3 分析方法与可视化
1.3.1 遗传进化分析
通过fastANI[12]进行B.bifidum基因组成对ANI值计算。基因组注释通过默认参数的Prokka[13]软件进行,并使用roary[14]软件进行泛基因组和核心基因组分析,所有参数均为默认值。基于核心基因的系统发育树由Treebest软件(http://www.mybiosoftware.com/treebest)采用邻接法构建,bootstrap值1 000。使用CAZys数据库(http://csbl.bmb.uga.edu/dbCAN/)进行碳水化合物活性酶(carbohydrate-active enzymes, CAZys)注释。
1.3.2 基因组比较分析
使用具有默认参数的Mauve软件进行基因组共线性分析与同源区图谱绘制。利用EggNOG数据库(http://eggnog-mapper.embl.de/)和RAST(https://rast.nmpdr.org/)数据库进行全基因组功能注释。CRISPR-Cas系统鉴定由CRISPRCasFinder(https://crisprcas.i2bc.paris-saclay.fr/CrisprCasFinder/)完成[15]。噬菌体序列检测、注释和完整性评估通过在线网站PHASTER进行(http://phaster.ca/)[16]。
1.3.3 统计分析及数据可视化
基因组可视化图谱由在线网站Proksee(https://proksee.ca/)绘制。ANI热图、CAZys热图及PCA图使用联川生物云平台绘制(https://www.omicstudio.cn/tool/)。用TBtools软件计算并可视化B.bifidum基因存在与缺失热图。泛-核心基因趋势图由R(v.4.3.1)通过ggplot2绘制。系统发育树可视化在iTol在线网站(https://itol.embl.de/)中进行。基因组功能分类图由Excel统计并绘制。CRISPR-Cas结构由CRISPRCasTyper网站 (https://crisprcastyper.crispr.dk/)绘制。
2 结果与分析
2.1 B.bifidum遗传与发育分析
2.1.1 B.bifidum基因组特征结合NCBI Refseq数据库119株和B.bifidum B1628的基因组分析显示,120株的基因组大小在2.14~2.55 Mb,平均为(2.23±0.06) Mb,每个基因组平均包含(1 813±62)个编码序列(Coding Sequences,CDS),GC含量为61.33%~62.94%,平均(62.66±0.19)%。B1628基因组(图1)大小为2 234 414 bp,GC含量62.40%,预测到1 769个CDS;BGN4基因组大小为2 223 664 bp,GC含量62.65%,预测到1 788个CDS;TMC3115基因组大小为2 178 894 bp,GC含量62.79%,预测到1 761个CDS。菌株的基因组特征反映其生活方式和环境生态位,游牧生活菌株具有较大的基因组和较低的GC含量,而宿主适应性菌株由于其基因丢失而具有更小的基因组和更高的GC含量[17]。
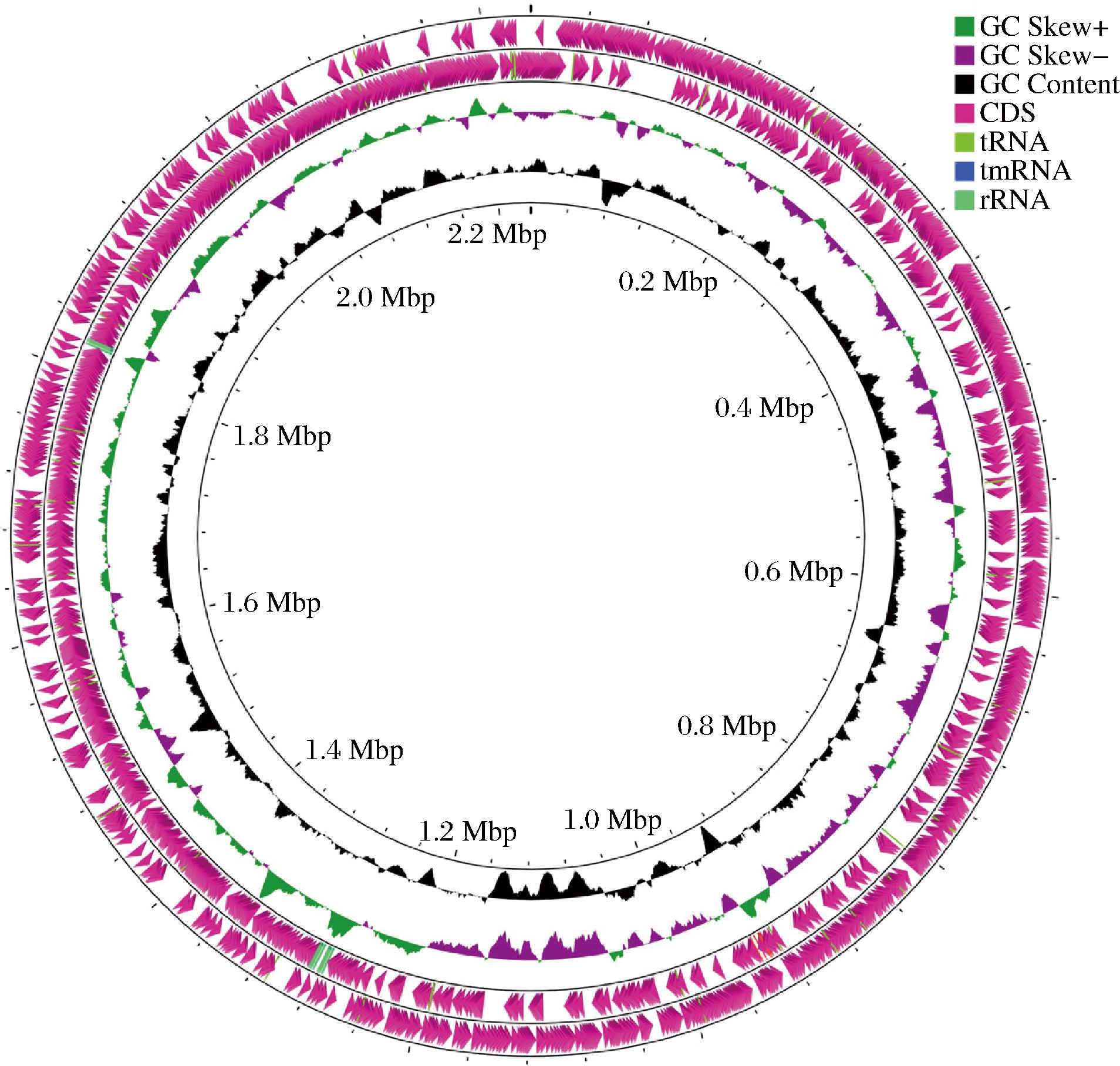
图1 B.bifidum B1628基因组图谱
Fig.1 Genome map of B.bifidum B1628
2.1.2 平均核苷酸同一性
平均核苷酸同一性(average nucleotide identity,ANI)值可以在基因组水平上确定菌株间遗传序列的相似程度,作为物种分类学鉴定中确定菌株是否属于参考物种或是否存在亚种的标准方法,使用96%的阈值作为物种边界[18]。119个基因组与模式株B.bifidum JCM1255T 基因组ANI值范围在98.38%~99.99%(图2-a),这验证了所有120株菌均为同一物种,并且B.bifidum基因组之间存在较小的差异。聚类结果显示不同国家和地区分离株存在一定的区域聚类趋势,其中中国和美国分离株聚集在不同的分支,这表明其具有地域间的菌株基因组多样性,同时在洲际分布上,同一区域内不同国家聚集在一起,表明其较高的相似性。
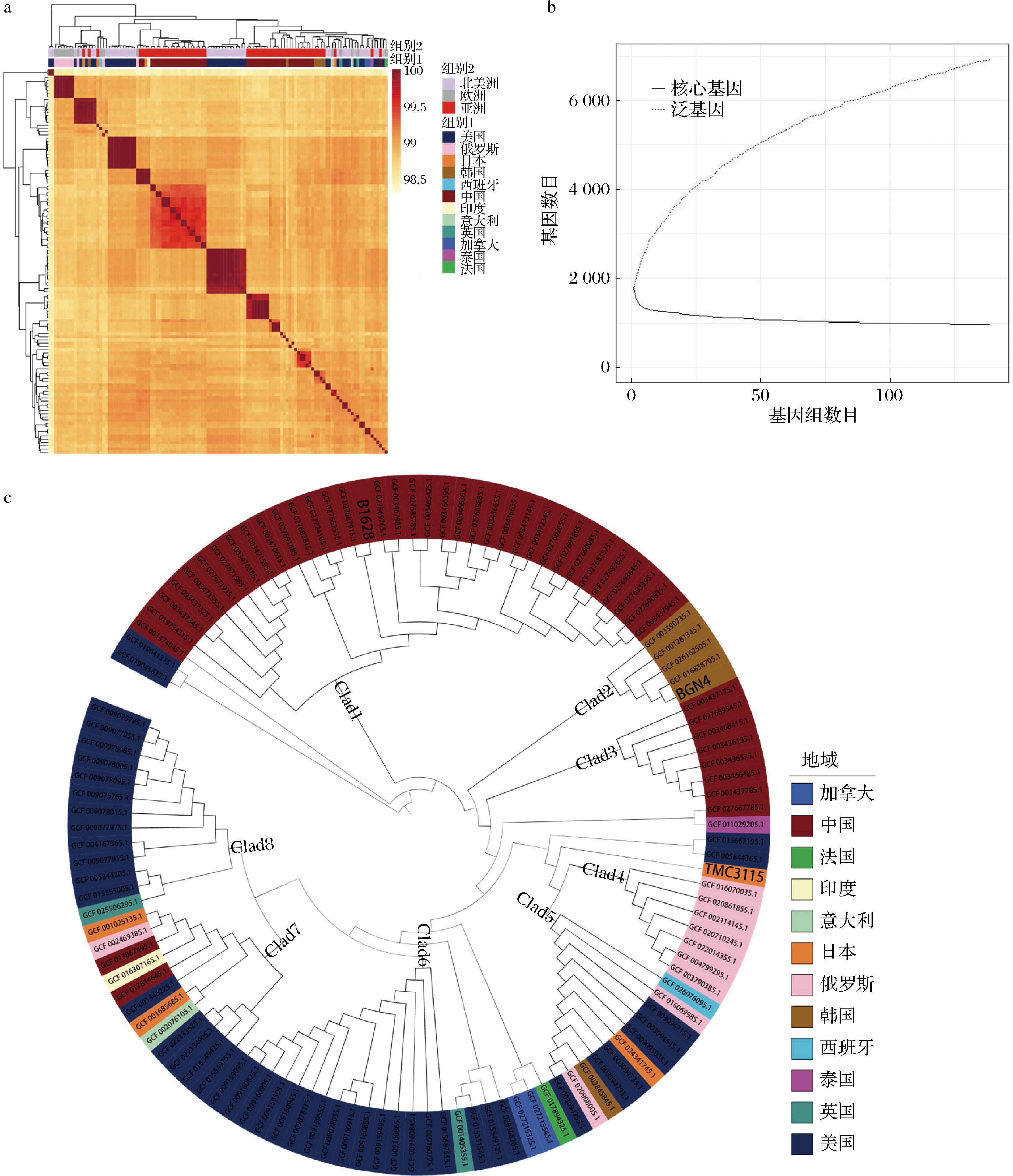
a-聚类热图;b-泛-核心基因趋势;c-系统发育树
图2 120株B.bifidum ANI 值聚类热图,泛-核心基因趋势,和基于987个核心基因构建的系统发育树
Fig.2 Heatmap of ANI based on the genome sequences, representation of gene content according to how the pan and core genes varies, phylogenetic tree based on 987 core genes in 120 B.bifidum
2.1.3 泛基因组分析
一个物种的所有基因被定义为该物种的泛基因集(包括核心基因和非核心基因),构建完整的泛基因图谱可以更加丰富物种的遗传信息[19]。核心基因集包含一个物种所有菌株的保守同源基因,它与该物种的生物功能和主要表型特征有关,反映了该物种的稳定性。本研究120株不同地区B.bifidum基因组序列提供相对全面的泛基因信息。分析发现,泛基因数量为6 554个,其中987个核心基因,占比15.1%;软核心基因308个,占比4.7%;壳基因876个,占比13.4%;云基因4 383个,占比66.9%。较低的核心基因比例和较高的云基因比例,表明了B.bifidum具有较高的遗传多样性。随着基因组数量的增加,核心基因组曲线趋于平稳,泛基因数量曲线则没有达到平台期(图2-b),这表明B.bifidum泛基因集仍处于开放状态,泛基因数量将随新基因组的加入而不断增加。
2.1.4 系统发育分析
基于987个核心基因的系统发育树(图2-c)显示,120株B.bifidum基本以地理单元聚类,其中105株分为8个较大的分支,其余15个菌株被分为几个包含1~4个不等的小分支,B1628位于分支1,BGN4位于分支2,TMC3115位于一个单独的小分支。分支1和分支3均为中国分离株;韩国分离株主要聚于分支2,与中国分离株发育关系较近;俄罗斯分离株聚于分支4;美国分离株则主要分布于分支5、分支6和分支8,其中分支6和分支8的分布比例在92%以上,与欧洲分离株亲缘关系较近。这表明,B.bifidum的系统发育可能与其分离源的地理位置有关,并且同一地区的B.bifidum分离株也存在遗传多样性。之前一项关于B.bifidum中国与美国分离株的基因组研究显示了其系统发育与其分离源的地理特征的关系,并且菌株特异性基因的数量与其所处生态位有一定关系[20],本研究也支持这一结果。
2.1.5 碳水化合物利用能力分析
碳水化合物利用能力是决定宿主体内双歧杆菌种类和数量的重要因素,双歧杆菌基因组中13%的同源基因家族与碳水化合物代谢相关[21]。120株B.bifidum基因组共预测到61种CAZys (图3-a),包括14种碳水化合物结合模块(carbohydrate-binding modules,CBMs)、7种碳水化合物酯酶家族(carbohydrate esterases,CEs)、29种糖苷水解酶家族(glycoside hydrolases,GHs),11种糖基转移酶家族(glycosyl transferases, GTs),其中GHs和CBMs最为丰富,其次是GTs。GHs是碳水化合物利用的关键酶,120株B.bifidum均编码GH2、GH13、GH36、GH42和GH77家族,参与降解主食和乳制品中不可消化碳水化合物,丰富的GH13(平均7个/株)参与ɑ-多糖(ɑ-glycans)代谢和糖原分解[22]。CBM通过与GH结构域肽链串联,从而增加GHs对碳水化合物的亲和性,CBMs较高的数量代表了B.bifidum碳水化合物利用偏好的基础,数量最多的CBM32(平均21个/株)结构域与乳糖、半乳糖及其衍生物的识别特异性相关[23]。B.bifidum丰富的GHs和CBMs充分印证了其对宿主来源的碳水化合物的利用能力,特别是难以被人体消化吸收的母乳低聚糖和黏蛋白。

a-CAZys基因数量;b-CAZys PCA;c-CAZys 差异
图3 120株B.bifidum菌株CAZys基因数量,不同地区CAZys PCA分析, 3个地区B.bifidum CAZys 差异
Fig.3 Number of genes in the carbohydrate-active enzyme family, CAZys PCA analysis of by region 120 B.bifidum strains, differences in B.bifidum CAZys in the three regions
120株B.bifidum CAZys聚类显示存在地区聚集性,主成分分析(principal component analysis,PCA)显示不同地区CAZys分布相似性较低(P=0.001)(图3-b),由于B.bifidum绝大多数寄居在人体肠道这一特性,因此这可能和不同地区宿主的饮食结构相关。进一步比较发现不同地区间CAZys类存在差异(P<0.05)(图3-c),包括CBM13、CBM32、CBM50、CE3、GH1、GH16、GH2、GH25、GH33、GH42、GH43、GT2、GT39、GT4、GT8、GT81等,主要表现在植物和乳制品来源碳水化合物的降解利用上。亚洲分离株呈现出较高的多样性,其中CBM13、GH1、GH16、GH43、GT8、GT81较高,表现出膳食纤维方面的降解优势,而北美和欧洲分离株在GH25、GT2、GT39、GT2、GH42中较高,具有乳制品来源碳水化合物利用方面的利用优势,这可能与亚洲人普遍的蔬菜、水果摄入,而欧美以奶制品、精制谷物为主的饮食结构存在联系[24-25]。
2.2 三株B.bifidum基因组比较分析
2.2.1 共线性分析
不同地区和分离源菌株因其自然选择和进化,基因组结构往往不同。通过与分离自韩国和日本人肠道的B.bifidum BGN4和B.bifidum TMC3115基因组进行比较分析,以进一步了解B.bifidum B1628的基因组特征。3株B.bifidum全基因组完成图通过MAUVE软件进行结构比较发现,3株B.bifidum间存在22个局部共线块(图4-a),不同菌株区块均存在未识别的基因组特异性序列,且不同菌株共线块间存在局部易位与重排,研究显示,位于易位边缘的基因片段容易被打断而改变编码区域[26]。共线性结果表明3株B.bifidum间存在基因组结构差异。

a-BGN4和 TMC3115基因组结构比较;b、c-COG与RAST 功能类别比较;d-CRISPR-Cas位点
图4 B.bifidum B1628,BGN4和 TMC3115基因组结构比较,COG与RAST 功能类别比较,B.bifidum B1628中CRISPR-Cas位点
Fig.4 Comparison of the genome structure and functional gene classes based on the COG database and RAST database ofB.bifidum B1628,BGN4 and TMC3115 gene map of the CRISPR-Cas loci in B.bifidum B1628
2.2.2 基因组功能注释
对3株B.bifidum基因组中功能基因分布进行注释和统计(图4-b、图4-c)。在同源蛋白质组(clusters of orthologous groups of proteins, COG)分布中,B.bifidum基因组功能分配的S(未知功能)、L(参与复制、重组与修复)、K(转录)、J(翻译、核糖体结构)、G(碳水化合物运输与代谢)、E(氨基酸运输与代谢)基因类较高,其中B1628中L类的数量高于BGN4和TMC3115。RAST功能注释中,3株B.bifidum均注释到22个功能大类。其中参与蛋白质代谢(protein metabolism)和氨基酸及其衍生物合成与降解(amino acids and derivatives)的基因数量最多,其次是碳水化合物代谢(carbohydrates metabolism)相关基因。3株B.bifidum比较显示, B1628在细胞壁和细胞膜合成,碳水化合物代谢和DNA修复方面具有一定的优势。
2.2.3 CRISPR-Cas与原噬菌体
CRISPR-Cas作为侵入性遗传元件抵抗系统而存在细菌和古菌中,其结构由重复间隔序列和Cas基因组成,一项对140株B.bifidum基因组评估中,仅56株具有CRISPR-Cas系统,这表明大多数B.bifidum不具备这种抵御能力[20]。本研究3株B.bifidum基因组评估中发现B1628存在II型CRISPR-Cas系统(图4-d),包括43个间隔序列,BGN4和TMC3115不含Cas基因。CRISPR间隔序列代表了对外源片段入侵的记忆,大量的间隔序列表明B1628具有较强的外源片段识别能力。
噬菌体作为细菌病毒广泛存在,溶原性噬菌体整合到细菌染色体后随宿主染色体复制而复制,这种溶原性噬菌体在人类肠道双歧杆菌中普遍存在,环境应激(紫外线、诱变剂)以及肠道炎症可引起原噬菌体的诱导和释放[27],其在人体肠道释放,可能对肠道微生态造成潜在影响,所以益生菌菌株基因组中应尽可能地避免噬菌体的存在。使用PHASTR软件对3株B.bifidum基因组中噬菌体序列的存在进行预测。发现3株菌共预测到6个不完整的噬菌体序列片段(表1),并且大多数片段没有已知编码功能,表明3株B.bifidum中几乎没有功能性噬菌体,这对B.bifidum菌株的开发具有指导意义。
2.3 B.bifidum B1628益生特性分析
2.3.1 母乳低聚糖利用
母乳低聚糖(human milk oligosaccharides, HMOs)是母乳中聚合度≥3的低聚糖的统称,是仅次于乳糖和脂类的母乳中第三大固体成分,不易被胰腺消化[28]。研究发现婴儿肠道相关双歧杆菌存在两种不同的HMOs降解策略:第一种是细胞外水解酶依赖型,其途径是在由细胞外被锚定在细胞壁上的分泌糖苷酶将HMOs水解为单糖和双糖,然后被细胞吸收;第二种是寡糖转运依赖型,通过ATP结合盒转运体将HMOs转运到胞内进行胞内水解利用[28]。B.bifidum HMOs利用通过第一种胞外水解酶途径,此外B.bifidum在生长过程中会留下一些HMOs降解糖而不被吸收,如乳糖-N-二糖I(LNB:Galβ1-3GlcNAc)、乳糖(Lac:Galβ1-4Glc)和半乳糖(galactose,Gal),这些HMOs降解物可作为良好的碳源由肠道中不同的双歧杆菌吸收利用,促进双歧杆菌属水平的丰度[29]。通过与HMOs利用菌B.bifidum JCM1254基因组比较分析显示,B.bifidum B1628包含编码HMOs降解酶的最低全套基因,并且其基因序列比对相似度大于98%(表2),这表明B.bifidum B1628具有HMOs降解能力,使得其在宿主肠道中具有一定的选择优势,并促进双歧杆菌属水平的优势地位。
表2 B.bifidum B1628中HMO降解酶
Table 2 HMO-degrading enzymes in B.bifidum B1628

酶[29]JCM1254B1628基因(GenBank ID)核酸序列一致性/%位置1,2-α-l-fucosidase (AfcA) afcA(AAQ72464)99.0908260 9141391,3-1,4-α-l-fucosidase (AfcB) afcB(BAH80310)98.31801484 1805840lacto-N-biosidase (LnbB) lnbB(ABZ78855)98.01721554 1724895β-galactosidase III (BbgIII) bbgIII(BAI94821)99.3535953 541760β-N-acetylglucosaminidase I (BbhI) bbhI(BAI94822)99.61598006 1602889solute-binding protein (GL-BP) of the GNB/LNB transportergltA(AEP83683)98.92173151 2174458GNB/LNB phosphorylase (GLNBP) lnpA1(BAD80752)98.82176809 2179064
2.3.2 B.bifidum B1628潜在益生基因与抗应激基因
对B.bifidum B1628基因组全面的潜在益生特性和抗应激功能基因挖掘和定位发现,B.bifidum B1628具有叶酸、色氨酸和乳酸等益于宿主健康的活性物质合成基因(表3)。乳酸是B.bifidum利用宿主碳水化合物的产物之一,可提供肠腔微酸化环境,促进电解质吸收和抑制病原菌生长,高水平的乳酸有助于巨噬细胞的突起和决定双歧杆菌的免疫调节特性[30]。色氨酸和叶酸是合成神经代谢物的关键物质,肠道细菌产生的色氨酸脱羧形成的色胺随血液输送到大脑,发挥神经递质前体的功能;叶酸是循环系统和免疫系统发育所必需的水溶性维生素,主要来自果蔬和人体肠道菌群,缺乏可导致妊娠期胎儿神经管缺陷,肠道细菌合成是人体重要的叶酸补充途径[31]。
表3 B.bifidum B1628潜在益生和抗应激相关基因
Table 3 Anti-stress and probiotic-related genes in B.bifidum B1628 strain

功能基因基因ID位置注释叶酸合成[31]folDB1628_00198227851 228726双功能蛋白FolD蛋白folCB1628_00368429789 431417二氢叶酸合成酶/叶酸多谷氨酸合成酶folAB1628_013611683066 1683725二氢叶酸还原酶folEB1628_013911716101 1716667 GTP环水解酶1folP1B1628_013921716733 1717605 二氢蝶酸合成酶色氨酸合成[31]trpBB1628_000099611 11698 色氨酸合成酶β亚基trpAB1628_0001011731 12603 色氨酸合成酶α亚基trpGB1628_008451032853 1033497 安息香酸合成酶组分2trpS2B1628_009521163457 1164554 色氨酸-tRNA连接酶2trpDB1628_015621930843 1931889 安息香酸磷酸核糖转移酶trpEB1628_017762171045 2172658 安息香酸合成酶组分1乳酸[31]pykB1628_00193220388 221830 丙酮酸激酶ldhB1628_018012203629 2204579L-乳酸脱氢酶耐酸[32]argCB1628_016752061140 2062234N-乙酰-γ-谷氨酰磷酸还原酶argHB1628_016892080717 2082204 精氨酸琥珀酸裂解酶dapAB1628_00508607785 608675 4-羟基四氢二吡咯酸合成酶PPKB1628_010721340585 1342822 多聚磷酸激酶pepPIB1628_00371432569 434167 Xaa-Pro氨基肽酶1耐胆盐[32]cbhB1628_0008496862 97812 胆酸甘氨酸水解酶glyQSB1628_00460534257 535777 甘氨酸-tRNA连接酶purDB1628_015121863491 1864756 磷酸核糖胺-甘氨酸连接酶gcvHB1628_00556679921 680328 甘氨酸裂解系统H蛋白氧化应激[32]SdhAB1628_016191995153 1997144 琥珀酸脱氢酶黄素蛋白亚基SdhBB1628_016141989872 1990843 琥珀酸脱氢酶铁硫亚基
益生菌功能具有菌株依赖性,并非所有菌株都能作为益生菌,益生菌在生产、储存和给药过程中暴露于多种压力源,包括O2、酸和胆汁盐等,但它们仍需要存活并发挥益生作用[32]。因此理想的益生菌菌株应具备对这些压力源的耐受能力,才能在胃肠道中保持活性,发挥益生功能。B1628功能基因解析发现其存在相关酸和胆盐耐受基因,这与其表型结果一致,同时还存在氧化应激相关基因(表3),这为其在宿主体内存活并发挥益生功能奠定了基础。未来还需继续通过小鼠和临床试验进一步探究B1628的潜在益生功能。
3 结论
本研究以1株由本实验室分离并测序和119株NCBI Refseq数据库公开发表的B.bifidum全基因组为基础进行比较基因组学研究。研究发现,B.bifidum基因组具有广泛的遗传多样性和地区特性。B.bifidum B1628、BGN4和TMC3115基因组功能基因分布趋同,B1628具有外源片段抵御能力。B.bifidum B1628编码多种潜在益生功能基因和环境抗应激基因。综合表明B.bifidum B1628经历了特定的遗传适应,具有良好的宿主环境生存能力,是一株潜在的功能性益生菌株。
[1] TURRONI F, PEANO C, PASS D A, et al.Diversity of bifidobacteria within the infant gut microbiota[J].PLoS One, 2012, 7(5):e36957.
[2] ZENDEBOODI F, KHORSHIDIAN N, MORTAZAVIAN A M, et al.Probiotic:Conceptualization from a new approach[J].Current Opinion in Food Science, 2020, 32:103-123.
[3] AAVV U.Health and nutritional properties of probiotics in food including powder milk with live lactic acid bacteria[J].Fao &Who, 2001(October):1-34.
[4] ABDULQADIR R, ENGERS J, AL-SADI R.Role of Bifidobacterium in modulating the intestinal epithelial tight junction barrier:Current knowledge and perspectives[J].Current Developments in Nutrition, 2023, 7(12):102026.
[5] ABDULQADIR R, AL-SADI R, MA T.Bifidobacterium bifidum causes an enhancement of the intestinal epithelial tight junction barrier is mediated by TLR-2 dependent increases of Toll-interacting protein (TOLLIP) expression in a MYD88 independent manner[J].Physiology, 2023, 38(S1):5734013.
[6] CHENG R Y, ZHANG Y J, YANG Y, et al.Maternal gestational Bifidobacterium bifidum TMC3115 treatment shapes construction of offspring gut microbiota and development of immune system and induces immune tolerance to food allergen[J].Frontiers in Cellular and Infection Microbiology, 2022, 12:1045109.
[7] KU S, PARK M S, JI G E, et al.Review on Bifidobacterium bifidum BGN4:Functionality and nutraceutical applications as a probiotic microorganism[J].International Journal of Molecular Sciences, 2016, 17(9):1544.
[8] FENG C J, ZHANG W Q, ZHANG T, et al.Heat-killed Bifidobacterium bifidum B1628 may alleviate dextran sulfate sodium-induced colitis in mice, and the anti-inflammatory effect is associated with gut microbiota modulation[J].Nutrients, 2022, 14(24):5233.
[9] KOREN S, WALENZ B P, BERLIN K, et al.Canu:Scalable and accurate long-read assembly via adaptive k-mer weighting and repeat separation[J].Genome Research, 2017, 27(5):722-736.
[10] HUNT M, SILVA N D, OTTO T D, et al.Circlator:Automated circularization of genome assemblies using long sequencing reads[J].Genome Biology, 2015, 16:294.
[11] WALKER B J, ABEEL T, SHEA T, et al.Pilon:An integrated tool for comprehensive microbial variant detection and genome assembly improvement[J].PLoS One, 2014, 9(11):e112963.
[12] JAIN C, RODRIGUEZ-R L M, PHILLIPPY A M, et al.High throughput ANI analysis of 90K prokaryotic genomes reveals clear species boundaries[J].Nature Communications, 2018, 9(1):5114.
[13] SEEMANN T.Prokka:Rapid prokaryotic genome annotation[J].Bioinformatics, 2014, 30(14):2068-2069.
[14] PAGE A J, CUMMINS C A, HUNT M, et al.Roary:Rapid large-scale prokaryote pan genome analysis[J].Bioinformatics, 2015, 31(22):3691-3693.
[15] COUVIN D, BERNHEIM A, TOFFANO-NIOCHE C, et al.CRISPRCasFinder, an update of CRISRFinder, includes a portable version, enhanced performance and integrates search for Cas proteins[J].Nucleic Acids Research, 2018, 46(W1):W246-W251.
[16] ARNDT D, MARCU A, LIANG Y J, et al.PHAST, PHASTER and PHASTEST:Tools for finding prophage in bacterial genomes[J].Briefings in Bioinformatics, 2019, 20(4):1560-1567.
[17] DUAR R M, LIN X B, ZHENG J S, et al.Lifestyles in transition:Evolution and natural history of the genus Lactobacillus[J].FEMS Microbiology Reviews, 2017, 41(Supp_1):S27-S48.
[18] CIUFO S, KANNAN S, SHARMA S, et al.Using average nucleotide identity to improve taxonomic assignments in prokaryotic genomes at the NCBI[J].International Journal of Systematic and Evolutionary Microbiology, 2018, 68(7):2386-2392.
[19] CAPUTO A, FOURNIER P E, RAOULT D.Genome and pan-genome analysis to classify emerging bacteria[J].Biology Direct, 2019, 14(1):5.
[20] LU W W, PEI Z M, ZANG M N, et al.Comparative genomic analysis of Bifidobacterium bifidum strains isolated from different niches[J].Genes, 2021, 12(10):1504.
[21] SELA D A, CHAPMAN J, ADEUYA A, et al.The genome sequence of Bifidobacterium longum subsp.infantis reveals adaptations for milk utilization within the infant microbiome[J].Proceedings of the National Academy of Sciences of the United States of America, 2008, 105(48):18964-18969.
[22] WEI X J, YU L L, ZHANG C, et al.Genetic-phenotype analysis of Bifidobacterium bifidum and its glycoside hydrolase gene distribution at different age groups[J].Foods, 2023, 12(5):922.
[23] FICKO-BLEAN E, BORASTON A B.Insights into the recognition of the human glycome by microbial carbohydrate-binding modules[J].Current Opinion in Structural Biology, 2012, 22(5):570-577.
[24] KHAKIMOV B, POULSEN S K, SAVORANI F, et al.New Nordic diet versus average Danish diet:A randomized controlled trial revealed healthy long-term effects of the new Nordic diet by GC-MS blood plasma metabolomics[J].Journal of Proteome Research, 2016, 15(6):1939-1954.
[25] 南开. 中国人的膳食结构[J].中国食物与营养, 2006, 12(6):55-57.NAN K.Summarization on the dietary pattern of Chinese residents[J].Food and Nutrition in China, 2006, 12(6):55-57.
[26] 邢锋. 籼稻珍汕97和明恢63基因组的注释和比较分析[D].武汉:华中农业大学, 2016.XING F.Genome annotation and comparative analysis of zhenshan 97 and minghui 63 [D].Wuhan:Huazhong Agricultural University, 2016.
[27] BUCKLEY D, ODAMAKI T, XIAO J Z, et al.Diversity of human-associated bifidobacterial prophage sequences[J].Microorganisms, 2021, 9(12):2559.
[28] KATAYAMA T.Host-derived glycans serve as selected nutrients for the gut microbe:Human milk oligosaccharides and bifidobacteria[J].Bioscience, Biotechnology, and Biochemistry, 2016, 80(4):621-632.
[29] GOTOH A, KATOH T, SAKANAKA M, et al.Sharing of human milk oligosaccharides degradants within bifidobacterial communities in faecal cultures supplemented with Bifidobacterium bifidum[J].Scientific Reports, 2018, 8(1):13958.
[30] MORITA N, UMEMOTO E, FUJITA S, et al.GPR31-dependent dendrite protrusion of intestinal CX3CR1+ cells by bacterial metabolites[J].Nature, 2019, 566:110-114.
[31] TOCHILINA A G, BELOVA I V, ILYICHEVA T N, et al.Genome features of probiotic bifidobacteria determining their strain-specific properties[J].Sovremennye Tekhnologii v Meditsine, 2022, 14(5):36-43.
[32] SCHÖPPING M, VESTH T, JENSEN K, et al.Genome-wide assessment of stress-associated genes in bifidobacteria[J].Applied and Environmental Microbiology, 2022, 88(7):e0225121.