1,6-己二胺(1,6-hexanediamine)是三大尼龙原材料之一,主要用于生产尼龙66[1]。作为重要的化工生产中间体,1,6-己二胺还可用于制备1,6-己二异氰酸酯(hexamethylene diisocyanate,HDI)和有机交联剂[2-3]。当前,工业上常采用己二腈催化加氢的化学法来制备1,6-己二胺[4-5],但是其化学合成存在原料高毒性导致的安全风险,而且反应条件严苛、副产物多、三废处理困难。此外,己二腈生产技术[6-9]被少数跨国公司垄断[10-11],国内己二腈供给受到制约,市场严重依赖进口。
相比于化学合成,生物法合成1,6-己二胺具有绿色无污染、反应条件温和等优点。到目前为止,只有部分研究通过酶催化合成了1,6-己二胺,生物法合成1,6-己二胺的研究仍处于起步阶段[12-13]。2019年,FEDORCHUK等[12]首次正式报道了己二酸至1,6-己二胺的生物转化途径,成功在体外合成了1,6-己二胺。ZHANG等[14]采用多级酶联反应,实现了由环己烷或环己醇到1,6-己二胺的生物转化。石焜等[15]对羧酸还原酶(carboxylic acid reductase, CAR)系统发育、结构与催化机理、蛋白质工程和固定化进行了研究,揭示其在己二胺合成中的重要作用。
6-氨基己酸是一种单氨基羧酸,主要由己内酰胺水解制得,也可以通过微生物代谢获得[16],具有原料来源广泛、制备工艺成熟等优点。本研究通过构建工程菌株,打通了从6-氨基己酸到1,6-己二胺的生物合成路线。相比于生物酶催化的高昂成本,全细胞生物合成不仅能避免酶的纯化,还能提供大量的辅因子,更符合工业化生产的需求。在此基础上,通过发酵强化进一步提高了1,6-己二胺的产量,为其生物法合成提供了新思路。
1 材料与方法
1.1 材料
1.1.1 菌株
本研究所用菌株DAH1~DAH37均基于本实验室保藏的菌株Escherichia coli BL21(DE3)/ΔsthA构建,所用质粒为pRSFDuet-1、pETDuet-1、pACYCDuet-1,具体信息如表1所示。
表1 菌株和质粒
Table 1 Strains and plasmids

名称基因型来源菌株BL21(DE3)/ΔsthAE.coli BL21(DE3)敲除基因sthA本实验室保藏DAH1BL21(DE3)/ΔsthA pRSF-MAB CAR L342E, pACYC-PatA本研究DAH2BL21(DE3)/ΔsthA pRSF-MAB CAR L342E, pACYC-SPTA本研究DAH3BL21(DE3)/ΔsthA pRSF-MAB CAR L342E, pACYC-GabT本研究DAH4BL21(DE3)/ΔsthA pRSF-MAB CAR L342E, pACYC-HATA本研究DAH5BL21(DE3)/ΔsthA pRSF-MAB CAR L342E, pACYC-CVTA本研究DAH6BL21(DE3)/ΔsthA pRSF-MAB CAR L342E, pACYC-VFTA本研究DAH7BL21(DE3)/ΔsthA pRSF-MAB CAR L342E, pACYC-STTA本研究DAH8BL21(DE3)/ΔsthA pRSF-MAB CAR L342E, pACYC-PDTA本研究DAH9BL21(DE3)/ΔsthA pRSF-MAB CAR L342E, pACYC-PatA, pET-puc-SPTA本研究DAH10BL21(DE3)/ΔsthA pRSF-MAB CAR L342E, pACYC-PatA, pET-puc-GabA本研究DAH11BL21(DE3)/ΔsthA pRSF-MAB CAR L342E, pACYC-PatA, pET-puc-HATA本研究DAH12BL21(DE3)/ΔsthA pRSF-MAB CAR L342E, pACYC-PatA, pET-puc-CVTA本研究DAH13BL21(DE3)/ΔsthA pRSF-MAB CAR L342E, pACYC-PatA, pET-puc-VFTA本研究DAH14BL21(DE3)/ΔsthA pRSF-MAB CAR L342E, pACYC-PatA, pET-puc-STTA本研究DAH15BL21(DE3)/ΔsthA pRSF-MAB CAR L342E, pACYC-PatA, pET-puc-PDTA本研究DAH16BL21(DE3)/ΔsthA pRSF-MAB CAR L342E, pACYC-SPTA, pET-puc-GabT本研究DAH17BL21(DE3)/ΔsthA pRSF-MAB CAR L342E, pACYC-SPTA, pET-puc-HATA本研究DAH18BL21(DE3)/ΔsthA pRSF-MAB CAR L342E, pACYC-SPTA, pET-puc-CVTA本研究DAH19BL21(DE3)/ΔsthA pRSF-MAB CAR L342E, pACYC-SPTA, pET-puc-VFTA本研究DAH20BL21(DE3)/ΔsthA pRSF-MAB CAR L342E, pACYC-SPTA, pET-puc-STTA本研究DAH21BL21(DE3)/ΔsthA pRSF-MAB CAR L342E, pACYC-SPTA, pET-puc-PDTA本研究DAH22BL21(DE3)/ΔsthA pRSF-MAB CAR L342E, pACYC-GabT, pET-puc-HATA本研究DAH23BL21(DE3)/ΔsthA pRSF-MAB CAR L342E, pACYC-GabT, pET-puc-CVTA本研究DAH24BL21(DE3)/ΔsthA pRSF-MAB CAR L342E, pACYC-GabT, pET-puc-VFTA本研究DAH25BL21(DE3)/ΔsthA pRSF-MAB CAR L342E, pACYC-GabT, pET-puc-STTA本研究DAH26BL21(DE3)/ΔsthA pRSF-MAB CAR L342E, pACYC-GabT, pET-puc-PDTA本研究
续表1

名称基因型来源DAH27BL21(DE3)/ΔsthA pRSF-MAB CAR L342E, pACYC-HATA, pET-puc-CVTA本研究DAH28BL21(DE3)/ΔsthA pRSF-MAB CAR L342E, pACYC-HATA, pET-puc-VFTA本研究DAH29BL21(DE3)/ΔsthA pRSF-MAB CAR L342E, pACYC-HATA, pET-puc-STTA本研究DAH30BL21(DE3)/ΔsthA pRSF-MAB CAR L342E, pACYC-HATA, pET-puc-PDTA本研究DAH31BL21(DE3)/ΔsthA pRSF-MAB CAR L342E, pACYC-CVTA, pET-puc-VFTA本研究DAH32BL21(DE3)/ΔsthA pRSF-MAB CAR L342E, pACYC-CVTA, pET-puc-STTA本研究DAH33BL21(DE3)/ΔsthA pRSF-MAB CAR L342E, pACYC-CVTA, pET-puc-PDTA本研究DAH34BL21(DE3)/ΔsthA pRSF-MAB CAR L342E, pACYC-VFTA, pET-puc-STTA本研究DAH35BL21(DE3)/ΔsthA pRSF-MAB CAR L342E, pACYC-VFTA, pET-puc-PDTA本研究DAH36BL21(DE3)/ΔsthA pRSF-MAB CAR L342E, pACYC-STTA, pET-puc-PDTA本研究DAH37BL21(DE3)/ΔsthA pRSF-MAB CAR L342E, pACYC-VFTA-PatA本研究质粒pRSFDuet-1RSF ori, lacI, T7lac, KanR本实验室保藏pETDuet-1ColE1 ori, lacI, T7lac, AmpR本实验室保藏pACYCDuet-1p15A ori, lacI, T7lac, ChlR本实验室保藏pET-pucpETDuet-1的多克隆位点被pACYCDuet-1的多克隆位点取代本实验室保藏
1.1.2 培养基
LB培养基(g/L):蛋白胨10,酵母提取物5,NaCl 10,添加2%(质量分数)琼脂粉,根据需要加入相应浓度抗生素。
1.1.3 试剂与仪器
葡萄糖、NaCl、NaHCO3,上海国药集团化学试剂有限公司;胰蛋白胨、酵母粉,英国oxoid公司;硫酸卡那霉素、氯霉素、氨苄青霉素,上海生工生物工程有限公司。
PCR仪和高速离心机,德国Eppendorf公司;蛋白电泳仪、GelDoc凝胶成像系统,美国Bio-Rad公司;DYY-6C型电泳仪,北京六一电泳仪厂;Y15全自动分析仪,上海佰三思生物科技有限公司;超低温冰箱、ST 16R高速冷冻离心机,美国Thermo Fisher公司;Cytation 3多功能酶标仪,美国BioTek公司。
1.2 实验方法
1.2.1 己二胺合成羧酸还原酶同工酶筛选
根据文献报道,选择了5种羧酸还原酶来优化1,6-己二胺人工合成途径中的羧酸还原效率,分别是:MAB CAR及其突变体MAB CAR L342E(来自Mycobacteroides abscessus)[12]、NI CAR(来自Nocardia iowensis)[17]、MAV CAR(来自Mycobacterium avium subsp.paratuberculosis)[18]和MSM CAR(来自Mycolicibacterium smegmatis MC2 155)[19],均构建在质粒pRSF Duet中,并通过E.coli BL21(DE3)进行表达。蛋白纯化按照上海生工的1 mL Ni-NTA 6FF预装重力柱说明书操作步骤进行。
1.2.2 培养条件
种子液培养:将低温冷冻保藏的菌株划线接种在LB固体培养基中,于37 ℃培养箱培养10~12 h,挑取单菌落接种到10 mL的LB液体培养基中,转移至37 ℃,250 r/min摇床培养10~12 h,得到种子液。
摇瓶发酵培养:将种子液按照2%的接种量转接到50 mL的LB液体培养基中(使用250 mL摇瓶)培养。在37 ℃,250 r/min的摇床中培养3 h后,添加异丙基-β-D-硫代半乳糖苷(isopropyl-beta-D-thiogalactopyranoside,IPTG)诱导,并将培养温度降至30 ℃表达蛋白,继续培养至72 h。
1.2.3 己二胺合成单转氨酶筛选
根据催化底物相似性,从生物酶数据库(BRENDA)中筛选了8种转氨酶,包括:PatA(GenBank ID:NP_417544)、SPTA(GenBank ID:WP_011049154)、GabT(GenBank ID:BAC70294)、HATA(GenBank ID:SCM51866)、CVTA(GenBank ID:6S4G_D)、VFTA(GenBank ID:5ZTX_A)、STTA(GenBank ID:XP_006351980)和PDTA(GenBank ID:WP_011747074)。分别将羧酸还原酶MAB CAR L342E突变体和8种转氨酶结合构建菌株DAH1~DAH8,摇瓶发酵72 h,取样品进行衍生化处理后使用HPLC进行分析。
1.2.4 己二胺合成双转氨酶筛选
在羧酸还原酶MAB CAR L342E突变体的基础上,将8种转氨酶两两结合,构建了28株菌株DAH9~DAH36,进行摇瓶发酵至72 h,取样品进行衍生化处理后使用HPLC进行分析。
1.2.5 己二胺合成发酵强化
底物浓度优化:为了优化底物浓度对1,6-己二胺生产的影响,控制底物6-氨基己酸添加浓度,分别在诱导后添加底物终质量浓度至2、4、6、8、10、12 g/L生产1,6-己二胺。然后,进行摇瓶发酵至72 h,取样品进行衍生化处理后使用HPLC进行分析。
初始糖浓度优化:在现有优化基础上,设置葡萄糖质量浓度梯度为0、2、4、6、8、10 g/L进行摇瓶发酵生产1,6-己二胺。然后,进行摇瓶发酵至72 h,取样品进行衍生化处理后使用HPLC进行分析。
诱导时间优化:在现有优化基础上,调整菌体诱导时间分别在0、0.5、1.0、1.5、2.0、2.5、3.0、3.5、4.0、4.5 h诱导生产1,6-己二胺。然后,进行摇瓶发酵至72 h,取样品进行衍生化处理后使用HPLC进行分析。
发酵时间优化:在现有优化基础上,延长菌体发酵时间至120 h,生产1,6-己二胺。然后分别于72、96、120 h取样,样品衍生化处理后使用HPLC进行分析。
1.2.6 检测方法
使用酶标仪通过分光光度法检测羧酸还原酶辅因子NADPH在340 nm处吸光度值的降低来测定羧酸还原酶活力。羧酸还原酶活力的测定在包含Tris-HCl缓冲液(100 mmol/L,pH 7.5)、1 mmol/L NADPH、2.5 mmol/L ATP、10 mmol/L MgCl2、底物(10 mmol/L 6-氨基己酸)以及10 μg纯化羧酸还原酶的反应混合物(0.2 mL)中进行。单位酶活定义为1 U/g=1 μmol NADPH/(min·g蛋白)。
1,6-己二胺样品处理及检测方法参照文献[20]进行。
2 结果与分析
2.1 己二胺合成羧酸还原酶的筛选
如图1-a所示,在1,6-己二胺合成途径中,羧酸还原酶作为第一步反应酶可以将6-氨基己酸中的羧酸基团还原为醛基生成中间产物6-氨基己醛,其对6-氨基己酸的活性高低,对后续转氨反应影响较大。因此,根据文献报道[12, 17-19],选择了羧酸还原酶MAB CAR、MAB CAR L342E、NI CAR、MAV CAR和MSM CAR来优化1,6-己二胺人工合成途径中的羧酸还原效率。对经过表达纯化后的羧酸还原酶进行了酶活力测定,如图1-b所示,4种羧酸还原酶对6-氨基己酸的催化活性较低,其中野生型MAB CAR对6-氨基己酸的单位酶活力仅为20 U/g,而MAB CAR L342E突变体对6-氨基己酸的活性有显著提高,单位酶活力达到139 U/g,相比野生型提高了5.95倍,因此选择MAB CAR L342E突变体进行后续研究。
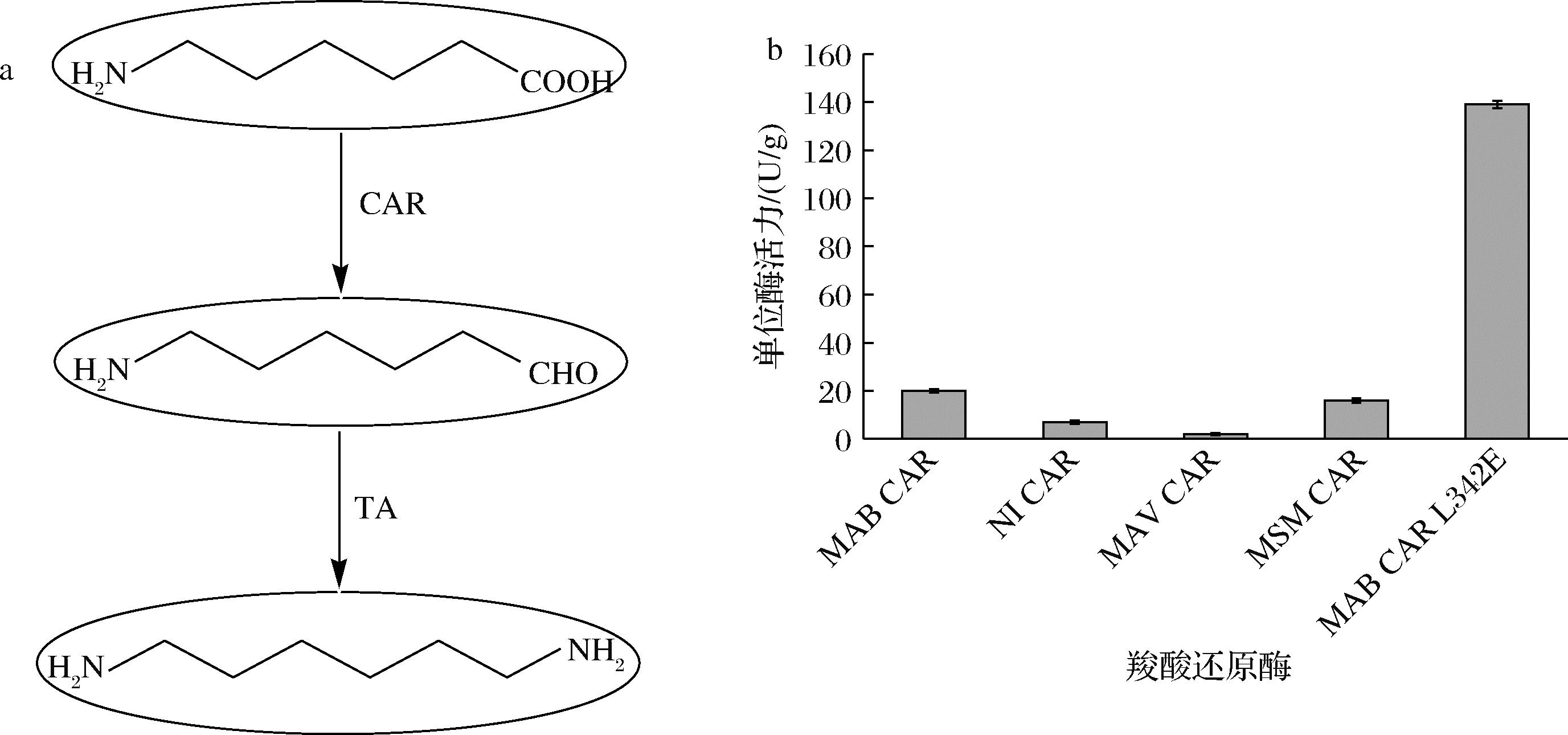
a-从6-氨基己酸出发合成1,6-己二胺;b-羧酸还原酶同工酶活力
图1 1,6-己二胺合成途径和羧酸还原酶活力测定
Fig.1 1,6-Hexanediamine synthesis pathway and enzyme activity determination of carboxylic acid reductase
2.2 己二胺合成单转氨酶筛选
在1,6-己二胺的人工合成途径中,转氨酶将6-氨基己醛转化为1,6-己二胺,对全细胞生物合成途径起着至关重要的作用。为了提高1,6-己二胺的产量,首先对1,6-己二胺人工合成途径中的转氨酶进行了优化。根据催化底物相似性,从生物酶数据库中筛选了8种转氨酶,包括PatA、SPTA、GabT、HATA、CVTA、VFTA、STTA和PDTA。将羧酸还原酶MAB CAR L342E分别和8种转氨酶结合,构建了8株单转氨酶菌株(DAH1~DAH8),进行摇瓶发酵,发现DAH2和DAH4能够合成1,6-己二胺,结果表明转氨酶SPTA和HATA具有将中间产物6-氨基己醛转化1,6-己二胺的能力(图2)。其中菌株DAH4的1,6-己二胺产量最高,达到了3.01 mg/L,是菌株DAH2的3.58倍。因此,选择性能较好的单转氨酶菌株DAH4作为研究的对象。
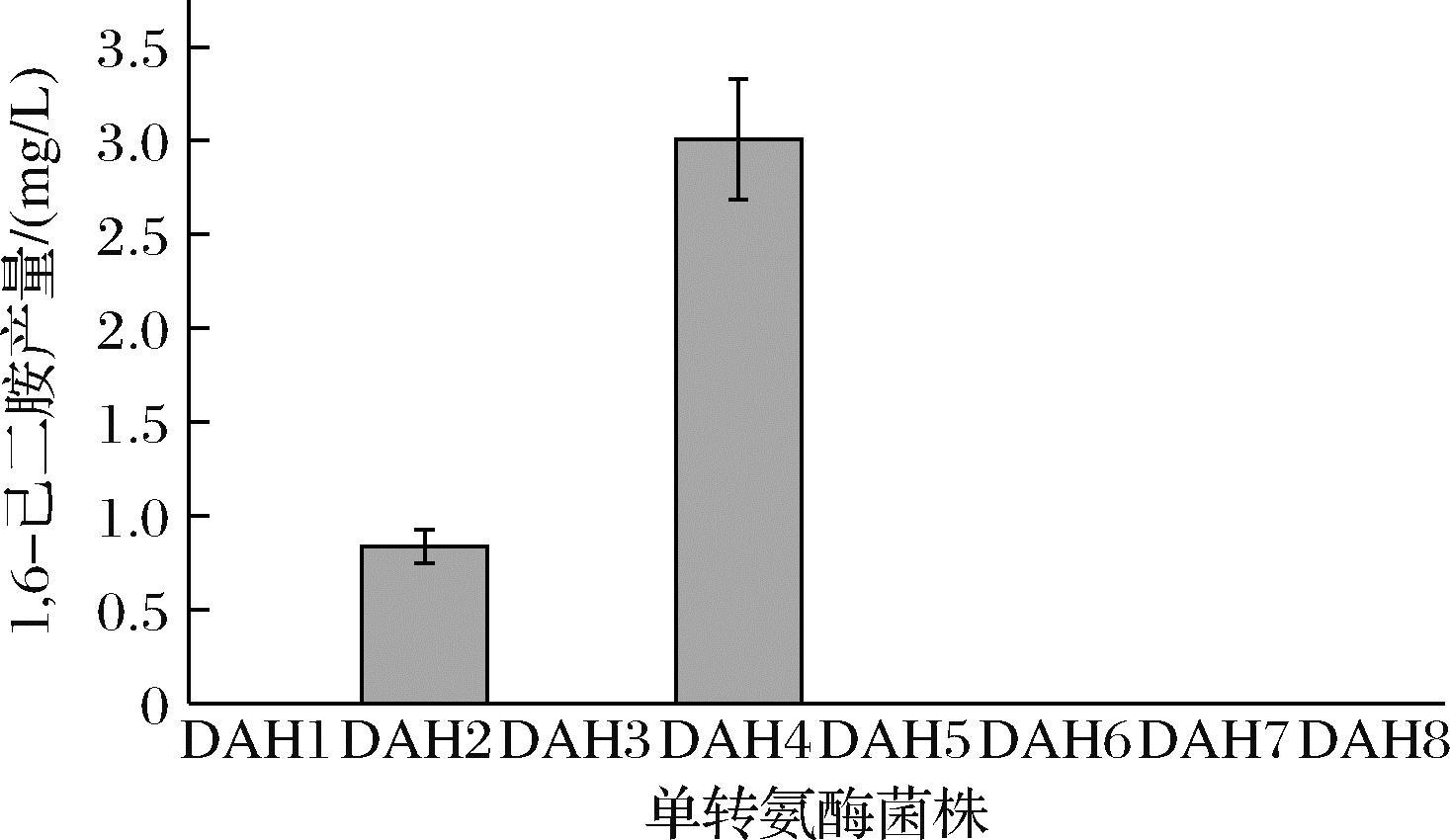
图2 己二胺合成单转氨酶筛选
Fig.2 Screening of single transaminase for hexanediamine synthesis
2.3 己二胺合成双转氨酶筛选
根据文献报道,WANG等[21]发现使用低拷贝质粒表达双转氨酶具有更好的催化效果,为了进一步增强转氨作用,将8种转氨酶两两结合,构建了28株双转氨酶菌株(DAH9~DAH36)。将构建的28株双转氨酶菌株进行摇瓶发酵实验,通过测定1,6-己二胺的产量,发现菌株DAH11、DAH13、DAH14、DAH15、DAH24、DAH25、DAH26、DAH29、DAH30、DAH31、DAH32和DAH33表现出一定的1,6-己二胺合成能力(图3)。在这些菌株中,菌株DAH13的1,6-己二胺产量最高,达到了5.80 mg/L,确定了最适合的双转氨酶组合为PatA和VFTA。在此基础上,将patA和VFTA放在同一个低拷贝质粒pACYA Duet中进行表达,构建了菌株DAH37,己二胺产量达到8.50 mg/L(图3),是菌株DAH13产量的1.47倍。因此,选择性能较好的双转氨酶菌株DAH37作为研究对象。
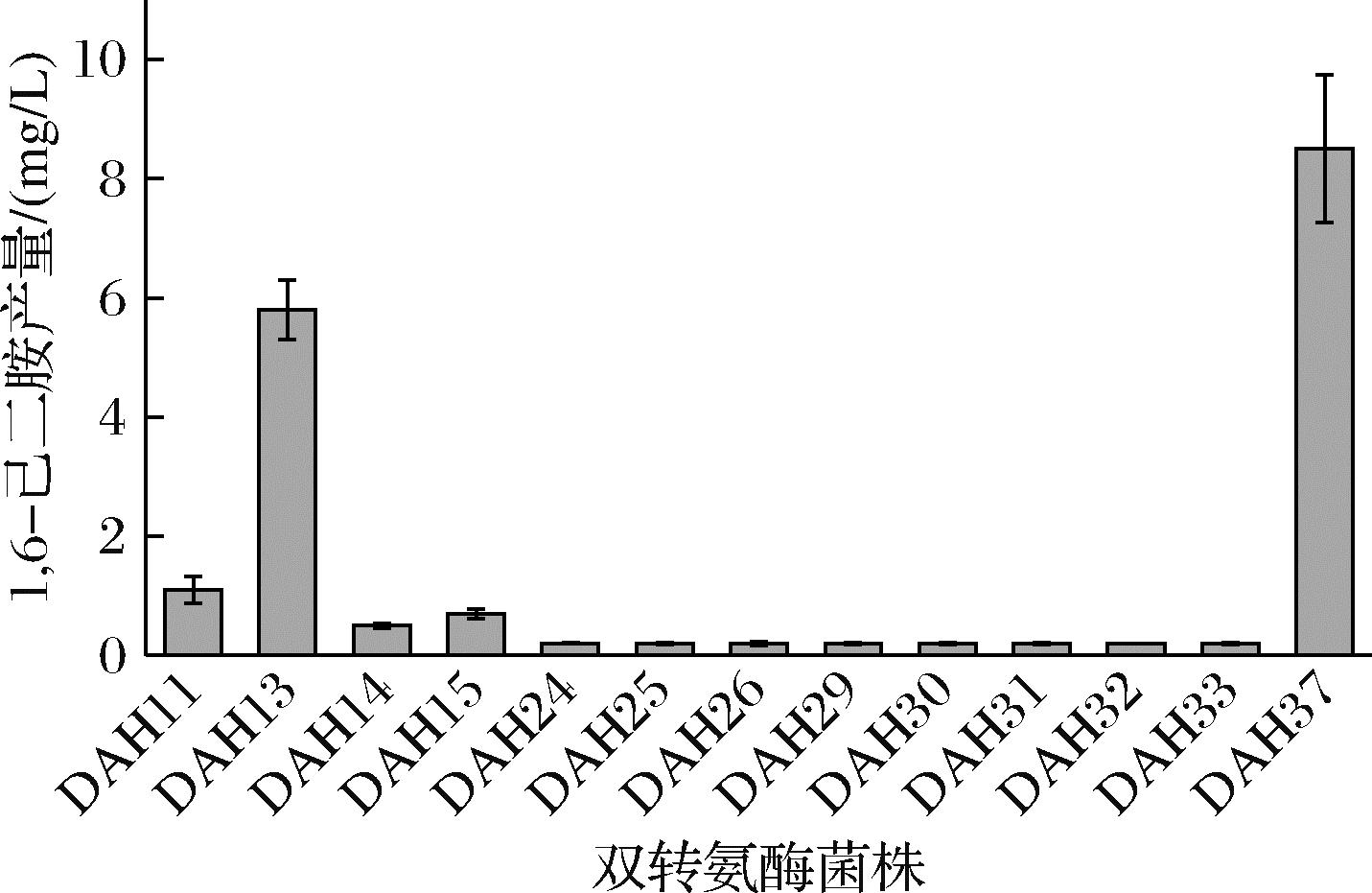
图3 己二胺合成双转氨酶筛选
Fig.3 Screening of double transaminase for hexanediamine synthesis
2.4 工程菌株己二胺合成发酵强化
2.4.1 底物浓度对己二胺合成的影响
底物是生物合成中的初始原料,过少不能满足生物合成的消耗,过量则会抑制微生物的生长和发育,进而对产物的合成产生影响。因此,需要研究最适合1,6-己二胺合成的初始底物浓度。根据图4的结果,当底物6-氨基己酸质量浓度为8 g/L时,菌株DAH4和DAH37的1,6-己二胺的产量达到最高值,随着6-氨基己酸浓度的进一步增加,二者的1,6-己二胺产量呈下降趋势。其中菌株DAH4在72 h的1,6-己二胺产量达到28.44 mg/L,相比之下提高了8.45倍。菌株DAH37在72 h的1,6-己二胺产量达到20.85 mg/L,相比之下提高了1.45倍。因此,确定其最佳初始底物质量浓度为8 g/L。

a-菌株DAH4在不同底物浓度下的1,6-己二胺产量; b-菌株DAH37在不同底物浓度下的1,6-己二胺产量
图4 底物浓度对1,6-己二胺产量的影响
Fig.4 Effects of substrate concentration on the production of 1,6-hexanediamine
2.4.2 初始糖浓度对己二胺合成的影响
葡萄糖作为一种快速碳源,容易被菌体吸收和利用,通常添加在发酵培养基中以促进菌体的生长和目的产物的合成。然而,葡萄糖过量供给可能引发“葡萄糖效应”,对菌体的生长产生负面影响,并可能导致大量杂酸的产生,从而抑制目的产物的合成[22]。因此,需要研究最适合1,6-己二胺合成的初始葡萄糖浓度。如图5所示,在初始糖质量浓度为2 g/L时,菌株DAH4和DAH37的1,6-己二胺的产量达到最高值,随着初始糖浓度的进一步增加,1,6-己二胺产量显著下降。其中菌株DAH4在72 h的1,6-己二胺产量达到40.76 mg/L,提高了0.43倍。菌株DAH37在72 h的1,6-己二胺产量达到44.13 mg/L,提高了1.12倍。上述结果表明初始糖浓度对发酵产量有着显著影响,并确定了1,6-己二胺发酵的最佳初始糖质量浓度为2 g/L。
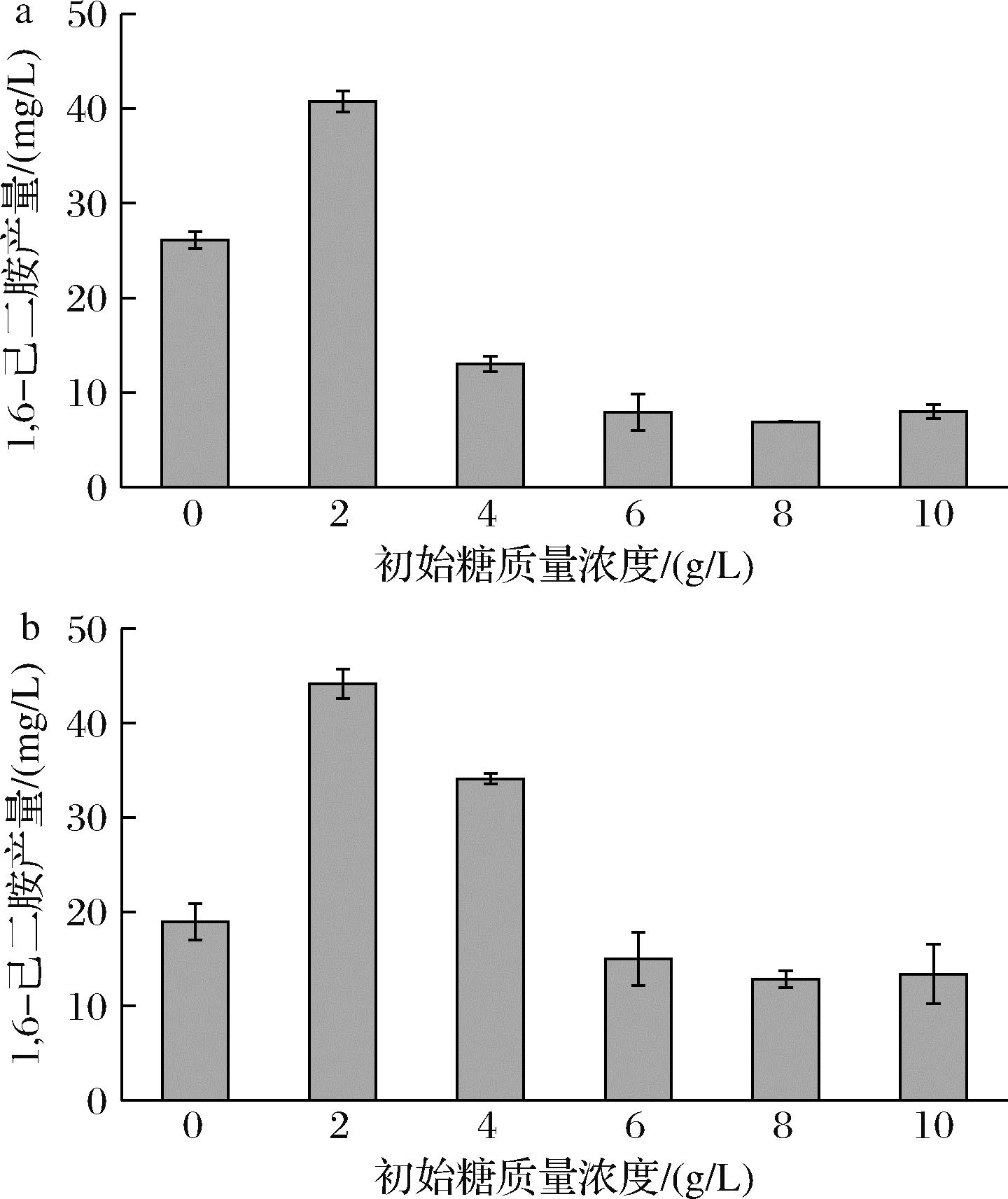
a-菌株DAH4在不同初始糖浓度下的1,6-己二胺产量; b-菌株DAH37在不同初始糖浓度下的1,6-己二胺产量
图5 初始糖浓度对1,6-己二胺产量的影响
Fig.5 Effects of initial sugar concentration on the production of 1,6-hexanediamine
2.4.3 诱导时间对己二胺产量的影响
异源蛋白表达的启动对宿主细胞的正常代谢会带来负担,对菌体浓度、蛋白表达和质粒稳定性都会产生负面影响,过早诱导不利于菌体生长,过晚诱导导致菌体老化并且产酶能力减弱,因此蛋白质的表达需要使菌体处于适当的生长水平[23]。从图6中可以观察到,菌株DAH4和DAH37的1,6-己二胺产量随着诱导时间的延后先增加后降低。在菌株DAH4中,1.5 h诱导(OD600值约为0.3~0.4)1,6-己二胺产量达到44.52 mg/L,提高了0.09倍。而在菌株DAH37中,3.5 h诱导(OD600值约为1.8)1,6-己二胺产量达到57.33 mg/L,提高了0.30倍。因此,确定了菌株DAH4和DAH37在摇瓶中发酵1,6-己二胺的最佳诱导时间分别为1.5 h和3.5 h。
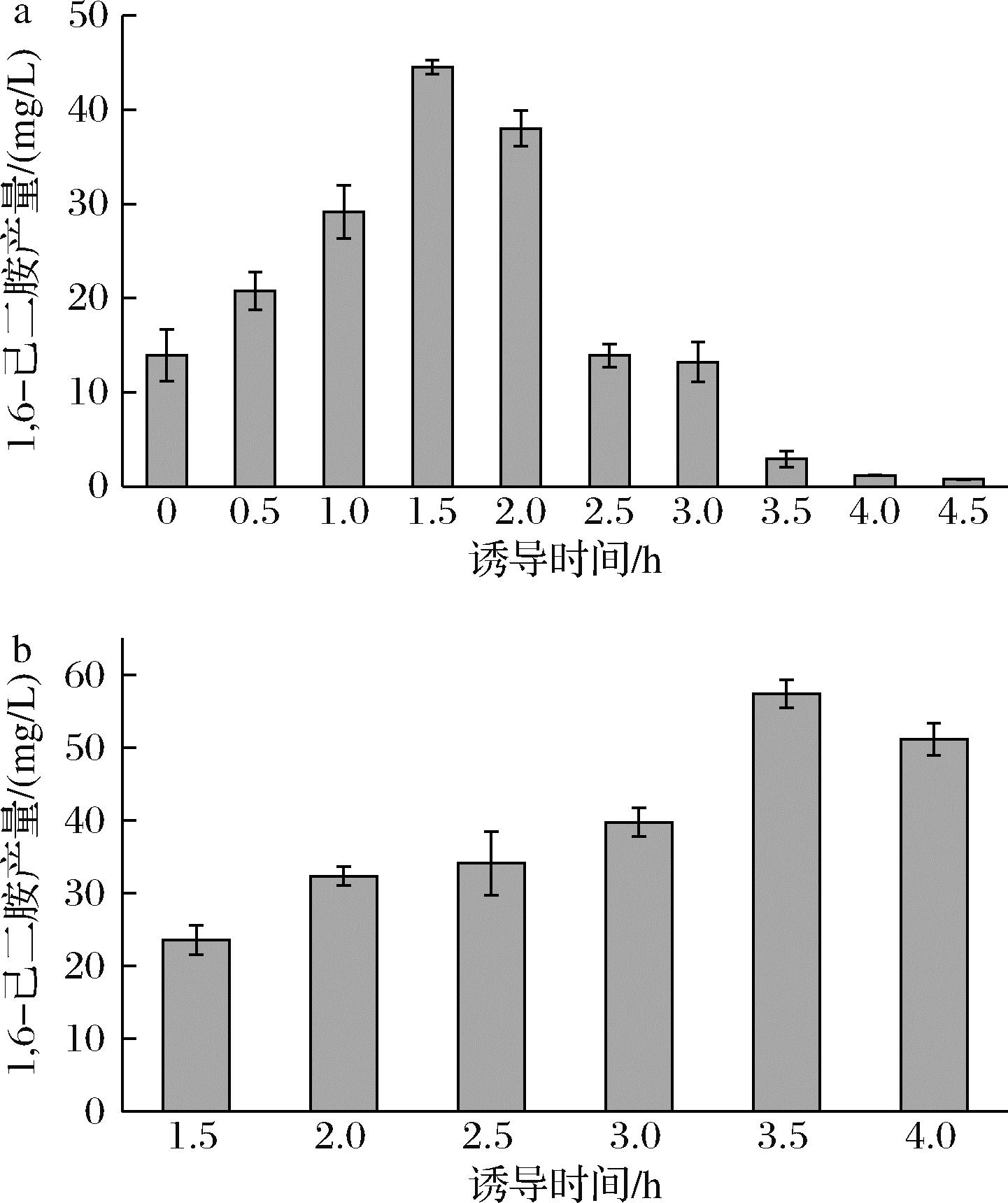
a-菌株DAH4在不同诱导时间下的1,6-己二胺产量; b-菌株DAH37在不同诱导时间下的1,6-己二胺产量
图6 诱导时间对1,6-己二胺产量的影响
Fig.6 Effects of induction time on the production of 1,6-hexanediamine
2.4.4 发酵时间对己二胺产量的影响
不同发酵时间对1,6-己二胺产量的影响如图7所示。随着摇瓶发酵时间的增加,1,6-己二胺的产量持续增加,在96 h达到最高值,并且在120 h基本保持不变。在菌株DAH4中,96 h的1,6-己二胺产量达到64.33 mg/L,提高了0.44倍。而在菌株DAH37中,96 h的1,6-己二胺产量达到153.93 mg/L,提高了1.68倍。因此,确定了1,6-己二胺的最佳发酵时间为96 h。
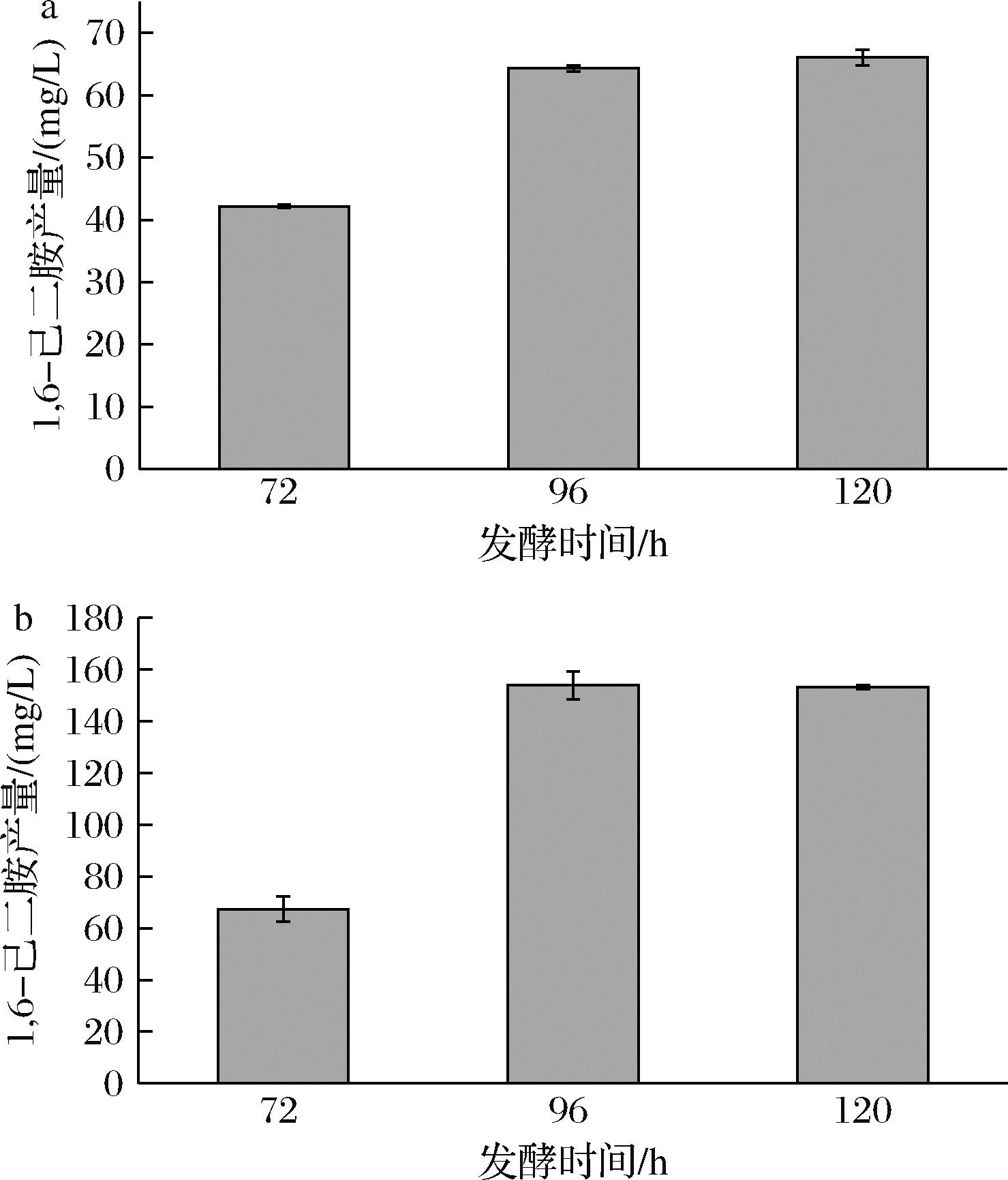
a-菌株DAH4在不同发酵时间下的1,6-己二胺产量; b-菌株DAH37在不同发酵时间下的1,6-己二胺产量
图7 发酵时间对1,6-己二胺产量的影响
Fig.7 Effects of fermentation time on the production of 1,6-hexanediamine
3 结论与讨论
本研究基于6-氨基己酸的底物特异性,开展元件与途径的适配组装,首先获得了催化性能显著增强的羧酸还原酶突变体MAB CAR L342E,单位酶活力达到139 U/g;其次,通过单转氨酶和双转氨酶的组合筛选方法,获得了两株高产1,6-己二胺的大肠杆菌菌株DAH4和DAH37。进一步开展发酵强化,确定了最佳的发酵条件,即6-氨基己酸的添加量为8 g/L,初始糖质量浓度为2 g/L,发酵时间为96 h。对于菌株DAH4和DAH37,最佳的诱导时间分别为1.5 h和3.5 h。在最佳条件下,1,6-己二胺的产量分别达到了64.33 mg/L和153.93 mg/L。这些结果为后续生物法生产1,6-己二胺及其他二元胺提供了有益的参考和借鉴。
[1] 谢锐, 徐保明, 陈坤.己二胺合成工艺的研究进展[J].应用化工, 2022, 51(3):873-877;883.XIE R, XU B M, CHEN K.Research progress on the synthesis of hexamethylenediamine[J].Applied Chemical Industry, 2022, 51(3):873-877;883.
[2] 琚裕波, 童明全, 潘蓉, 等.己二腈合成工艺路线研究进展[J].河南化工, 2017, 34(1):12-15.JU Y B, TONG M Q, PAN R, et al.Research progress on synthesis of adiponitrile synthesis process[J].Henan Chemical Industry, 2017, 34(1):12-15.
[3] PARVATE S, MAHANWAR P.Insights into the preparation of water-based acrylic interior decorative paint:Tuning binder’s properties by self-crosslinking of allyl acetoacetate-hexamethylenediamine[J].Progress in Organic Coatings, 2019, 126:142-149.
[4] 王明胜, 梅华.己二腈加氢制备己二胺催化剂的研究进展[J].合成纤维工业, 2012, 35(1):54-58.WANG M S, MEI H.Research progress in catalysts for adiponitrile hydrogenation to hexanediamine[J].China Synthetic Fiber Industry, 2012, 35(1):54-58.
[5] 陈聚良, 张华森, 刘国际.己二腈催化加氢的动力学研究[J].郑州大学学报(工学版), 2012, 33(4):103-107.CHEN J L, ZHANG H S, LIU G J.Study on the dynamics of catalytic hydrogenation of adiponitrile[J].Journal of Zhengzhou University (Engineering Science), 2012, 33(4):103-107.
[6] 俞磊, 王俊, 曹洪恩, 等.丙烯腈催化二聚反应的研究进展[J].有机化学, 2014, 34(10):1986-1991.YU L, WANG J, CAO H E, et al.A review on catalyzed dimerization of acrylonitrile[J].Chinese Journal of Organic Chemistry, 2014, 34(10):1986-1991.
[7] TOLMAN C A, MCKINNEY R J, SEIDEL W C, et al.Homogeneous nickel-catalyzed olefin hydrocyanation[J].Advances in Catalysis, 1985, 33:1-46.
[8] 冯赛平, 程党国, 陈丰秋, 等.己二酸氨化制己二腈的宏观动力学[J].化工学报, 2015, 66(8):3057-3063.FENG S P, CHENG D G, CHEN F Q, et al.Apparent kinetics of adipic acid ammoniation to adiponitrile[J].CIESC Journal, 2015, 66(8):3057-3063.
[9] 赵国忠. 己二腈生产技术进展及展望[J].化工设计, 2022, 32(4):10-13;50;1.ZHAO G Z.Progressand prospect of adiponitrile production technology[J].Chemical Engineering Design, 2022, 32(4):10-13;50;1
[10] 王超. 己二腈生产工艺及现状[J].化工管理, 2020(4):178-179.WANG C.Production technology and present situation of adiponitrile[J].Chemical Enterprise Management, 2020(4):178-179.
[11] 屠庆华. 己二腈行业现状及发展趋势分析[J].化学工业, 2020, 38(1):44-51.TU Q H.Current situation and development trend of adiponitrile industry[J].Chemical Industry, 2020, 38(1):44-51.
[12] FEDORCHUK T P, KHUSNUTDINOVA A N, EVDOKIMOVA E, et al.One-pot biocatalytic transformation of adipic acid to 6-aminocaproic acid and 1, 6-hexamethylenediamine using carboxylic acid reductases and transaminases[J].Journal of the American Chemical Society, 2020, 142(2):1038-1048.
[13] DROS A B, LARUE O, REIMOND A, et al.Hexamethylenediamine (HMDA) from fossil- vs.bio-based routes:An economic and life cycle assessment comparative study[J].Green Chemistry, 2015, 17(10):4760-4772.
[14] ZHANG Z W, FANG L, WANG F, et al.Transforming inert cycloalkanes into α, ω-diamines by designed enzymatic cascade catalysis[J].Angewandte Chemie (International Ed), 2023, 62(16):e202215935.
[15] 石焜, 郁惠蕾, 许建和.羧酸还原酶的研究进展[J].微生物学通报, 2020, 47(7):2255-2265.SHI K, YU H L, XU J H.Recent advances in carboxylic acid reductases[J].Microbiology China, 2020, 47(7):2255-2265.
[16] TURK S C H J, KLOOSTERMAN W P, NINABER D K, et al.Metabolic engineering toward sustainable production of nylon-6[J].ACS Synthetic Biology, 2016, 5(1):65-73.
[17] STOLTERFOHT H, SCHWENDENWEIN D, SENSEN C W, et al.Four distinct types of E.C.1.2.1.30 enzymes can catalyze the reduction of carboxylic acids to aldehydes[J].Journal of Biotechnology, 2017, 257:222-232.
[18] KRAMER L, LE X, RODRIGUEZ M, et al.Engineering carboxylic acid reductase (CAR) through a whole-cell growth-coupled NADPH recycling strategy[J].ACS Synthetic Biology, 2020, 9(7):1632-1637.
[19] KHUSNUTDINOVA A N, FLICK R, POPOVIC A, et al.Exploring bacterial carboxylate reductases for the reduction of bifunctional carboxylic acids[J].Biotechnology Journal, 2017, 12(11):1-12.
[20] 黄荻萱, 李国辉, 毛银, 等.生物发酵产丁二胺的定量测定[J].食品与发酵工业, 2020, 46(12):231-236.HUANG D X, LI G H, MAO Y, et al.A quantitative method for microbial-based putrescine determination[J].Food and Fermentation Industries, 2020, 46(12):231-236.
[21] WANG L, LI G H, LI A T, et al.Directed synthesis of biobased 1, 6-diaminohexane from adipic acid by rational regulation of a functional enzyme cascade in Escherichia coli[J].ACS Sustainable Chemistry &Engineering, 2023, 11(15):6011-6020.
[22] ZHANG Y, DAI X F, JIN H N, et al.The effect of optimized carbon source on the synthesis and composition of exopolysaccharides produced by Lactobacillus paracasei[J].Journal of Dairy Science, 2021, 104(4):4023-4032.
[23] 胡耀辉, 王丹, 朴春红, 等.重组麦芽糖转葡萄糖基酶工程菌发酵条件的优化[J].食品科学, 2011, 32(19):141-146.HU Y H, WANG D, PIAO C H, et al.Optimization of fermentation conditions for genetically engineered recombinant bacterium with amylomaltase gene[J].Food Science, 2011, 32(19):141-146.