右旋糖酐即葡聚糖,分子式为(C6H10O5)n[1],通常由来源于肠明状明串珠菌的右旋糖酐蔗糖酶以蔗糖为底物,合成以α-1,6糖苷键为主链(50%以上),以α-1,3糖苷键为支链,偶尔也存在以α-1,2糖苷键和α-1,4糖苷键为支链的一种微生物多糖[1-2]。除此之外,也有来源于魏氏菌属、乳酸杆菌属和链球菌的右旋糖酐蔗糖酶合成右旋糖酐[2]。同时,由于右旋糖酐的聚合度不同,其分子质量也有很大差异,不同的分子质量右旋糖酐有不同的应用价值,主要应用于食品和医药行业[3-4]。重均分子质量(weight average molecular mass, MW)>1 MDa的右旋糖酐可以用于色谱柱填充剂[1]。MW在1~2 MDa的右旋糖酐可以用作食品添加剂,改善包括发酵乳制品和烘焙食品等的质地特性[5]。MW在40~100 kDa的右旋糖酐可以作为医疗行业中的血液体积膨胀剂,用于临床失血的紧急治疗[3]。右旋糖酐40和右旋糖酐70可用作血浆代用品[6]。而低分子质量的右旋糖酐(<2 000 Da)已经被证实是一种潜在的益生元[5]。
右旋糖酐蔗糖酶是属于GH70家族中的一种葡萄糖基转移酶[7]。野生右旋糖酐蔗糖酶催化得到的右旋糖酐产物普遍存在分子质量高、黏度大的问题,产物不易分离纯化。为了控制右旋糖酐的产物分子质量,往往需要化学法、物理法或者生物法对高分子质量的右旋糖酐进一步降解[3,6,8-9]。酸解法是降解高分子质量右旋糖酐的一种传统化学方法,虽然酸解法的降解速度快,但是通过酸解法得到的右旋糖酐产物中存在大量氯化物和产物不均一的问题[2,4,8,10-11]。超声法是降解高分子质量右旋糖酐的一种物理方法,该方法虽然操作简单,但是存在耗能大的缺点,不适合用于右旋糖酐大规模生产[12]。而利用右旋糖酐酶降解高分子质量右旋糖酐,可以绿色环保且高效的获得右旋糖酐产物[6,9-10,12-13]。
右旋糖酐酶可以特异性催化右旋糖酐中的α(1,6)糖苷键的水解[1,14-15]。右旋糖酐酶包括外切右旋糖酐酶和内切右旋糖酐酶[1,13]。外切右旋糖酐酶是作用于右旋糖酐的还原端或非还原端,水解底物以释放葡萄糖、异麦芽糖或异麦芽三糖[1,13,16]。而内切右旋糖酐酶则作用于右旋糖酐的内部糖苷键,从而产生不同分子质量的右旋糖酐、低聚异麦芽糖(聚合度2~10)、潘糖和葡萄糖[4,14]。
目前,已有关于将右旋糖酐蔗糖酶和右旋糖酐酶进行融合,构建融合酶以直接生产获得低分子质量右旋糖酐的报道。KIM等[17]将这两种酶进行融合,通过控制蔗糖浓度调控右旋糖酐分子质量,成功生产得到低分子质量右旋糖酐,且融合酶的产量比同等活性的双酶法的混合物高30倍。张宇馨[14]通过对右旋糖酐蔗糖酶和右旋糖酐酶之间添加不同长度的连接肽构建融合酶,成功构建了一种人工双功能酶,可以将蔗糖直接转化为低分子质量右旋糖酐(13 050 Da),并通过研究融合酶的温度动态成功调节融合酶的两级催化效率,提高了低分子质量均相右旋糖酐的产率(产率为62%)。可见,通过对不同来源的右旋糖酐蔗糖酶和右旋糖酐进行融合,可以成功生产低分子质量的右旋糖酐,而关于对两种酶的融合生产高分子质量右旋糖酐的研究甚少。
因此,本文将来源于肠膜状明串珠菌0326的右旋糖酐蔗糖酶和来源于短杆菌的右旋糖酐酶BMdex通过连接肽进行连接,成功在大肠杆菌中得到表达,得到具有双酶活性的融合酶,并进行酶学性质研究,成功制备得到重均分子质量为2 MDa左右的右旋糖酐,产率可以达到32.6%。
1 材料与方法
1.1 材料
1.1.1 菌株和载体
带有右旋糖酐蔗糖酶编码基因P473S的重组质粒和带有右旋糖酐酶编码基因BMdex的质粒均为本实验室保存。克隆载体 pET-28a(+)、Trans1-T1和E.coli BL21(DE3)感受态细胞为实验室保藏。
1.1.2 试剂和试剂盒
目的基因克隆所用质粒小提试剂盒,北京全式金生物科技有限公司;酵母浸粉、胰蛋白胨,Oxoid公司;NaCl、Na2HPO4、KH2PO4、NH4Cl、KNO3、MgSO4、丙三醇、蔗糖、葡萄糖、乙酸钙、冰醋酸、咪唑、三羟甲基氨基甲烷、3,5-二硝基水杨酸、无水乙醇,国药集团化学试剂有限公司;卡那霉素、IPTG,生工生物工程(上海)有限公司。所有化学试剂均为分析纯。
1.1.3 主要培养基
LB液体培养基(g/L):5.0酵母浸粉、10.0胰蛋白胨、10.0 NaCl。
LB固体培养基:在LB液体培养基添加成分的基础上,添加20.0 g/L琼脂粉。
发酵培养基:12.0 mg/mL的MgSO4;25%(质量分数)的葡萄糖溶液;50%(质量分数)的甘油;M9盐包含171.05 mg/mL Na2HPO4·12H2O、30 mg/mL KH2PO4和10 mg/mL NH4Cl;母液包含11.7 mg/mL的胰蛋白胨和11.7 mg/mL的KNO3,172 mL分装。向母液中添加MgSO4溶液200 μL,甘油2 mL,葡萄糖4 mL,以及M9盐20 mL,构成发酵培养基。
1.1.4 实验设备与仪器
恒温摇床、生化培养箱,上海智诚分析仪器;高速冷冻离心机,美国Beckman公司;小型低温离心机,德国SIGMA;超净工作台,力康精密科技(上海)有限公司;PCR仪,杭州博日科技有限公司;凝胶成像系统、稳压稳流电泳仪、DNA电泳槽,天能公司;立式圆形压力蒸汽灭菌器,张家港市化菱医疗设备有限公司;移液器(各种规格),德国Eppendorf公司;微波炉,广东美的电器股份有限公司。
1.2 实验方法
1.2.1 融合前后酶的软件模拟
通过同源建模的方法构建融合前后酶的三维结构模型。融合前后酶的3D模型通过Discovery Studio 2019创建。
1.2.2 获取右旋糖酐蔗糖酶和右旋糖酐酶融合基因
以带有右旋糖酐蔗糖酶编码基因P473S的质粒为模板,以F1和R1为引物进行PCR扩增,获得含有右旋糖酐蔗糖酶P473S基因与部分刚性连接肽基因的载体片段;以质粒右旋糖酐酶BMdex为模板,以F2和R2为引物进行PCR扩增,得到右旋糖酐酶BMdex基因与部分刚性连接肽基因片段。PCR反应程序为:95 ℃保温5 min;95 ℃保温30 s,55 ℃退火30 s,72 ℃延伸3 min,30个循环;72 ℃保温10 min。引物序列见表1,其中F1和F2以及R1和R2之间含有15~25 bp的同源序列以便于后续通过重叠延伸PCR进行右旋糖酐蔗糖酶和右旋糖酐酶基因的融合(融合酶中间通过刚性连接肽连接[(EAAAK)5])。
表1 构建右旋糖酐蔗糖酶-右旋糖酐酶融合基因的引物序列
Table 1 Construction of primer sequences for the dextransucrase-dextranase fusion gene
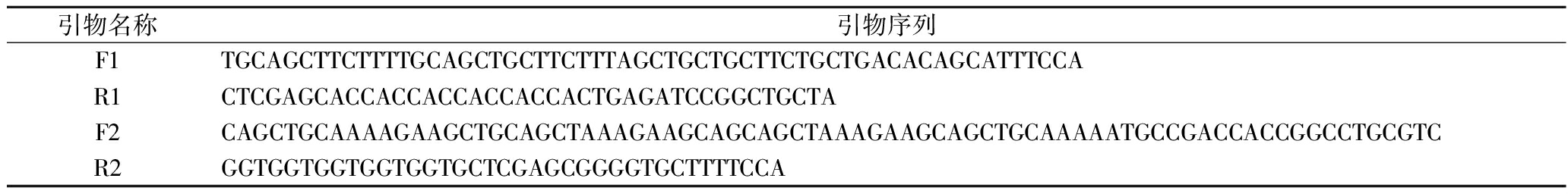
引物名称引物序列F1TGCAGCTTCTTTTGCAGCTGCTTCTTTAGCTGCTGCTTCTGCTGACACAGCATTTCCAR1CTCGAGCACCACCACCACCACCACTGAGATCCGGCTGCTAF2CAGCTGCAAAAGAAGCTGCAGCTAAAGAAGCAGCAGCTAAAGAAGCAGCTGCAAAAATGCCGACCACCGGCCTGCGTCR2GGTGGTGGTGGTGGTGCTCGAGCGGGGTGCTTTTCCA
反应结束后,取5 μL的PCR扩增产物用质量分数0.08%的琼脂糖凝胶电泳对其进行检测,条带大小正确的基因片段备用。对上述PCR扩增产物进行DNA纯化:参照EasyPure® PCR Purification Kit和EasyPure® Quick Gel Extraction Kit说明书进行纯化。对纯化后的DNA进行浓度测量:使用NanoDrop进行DNA浓度测定。采用无缝克隆的方法对右旋糖酐蔗糖酶和右旋糖酐酶基因进行融合:参照pEASY®-Basic Seamless Cloning and Assembly Kit说明书进行。将无缝克隆产物转化入克隆感受态:参照Trans1-T1 Phage Resistant化学感受态细胞说明书转化。转化后进行单克隆阳性验证,方法:菌液PCR、重组质粒提取与测序验证。
1.3 融合表达质粒的构建、转化
对测序正确的克隆进行质粒提取,获得重组载体P473S-Linker[(EAAAK)5]-BMdex,取5 μL将其转化入50 μL大肠杆菌感受态细胞中,冰浴30 min,42 ℃热激45 s,2 min后加入450 μL的LB液体培养基,置于37 ℃、220 r/min摇床培养1 h,涂布于含有卡那霉素的LB固体平板,37 ℃恒温培养箱倒置过夜培养。
1.4 重组酶的诱导表达
将成功构建的阳性重组融合质粒转化到E.coli BL21(DE3)感受态细胞中,将转化后的大肠杆菌涂布在含有卡那抗性的固体LB培养基上,用接种环挑取单菌落,转接到50 mL新鲜的液体LB培养基(含卡那抗性50 μg/mL)中,置于37 ℃、250 r/min摇床中,过夜培养16~18 h。按照质量分数1%的接种量将菌液转接到发酵培养基(即转接2 mL菌液到200 mL发酵培养基)中,将发酵培养基置于37 ℃、250 r/min的摇床中,培养4~6 h。取出发酵液,待温度降至室温,向其中加入500 μL的IPTG(0.025 g/mL)诱导大肠杆菌产酶,将培养基置于15 ℃,250 r/min的摇床中,过夜诱导16 h,产酶。在4 ℃,6 000 r/min的条件下离心、收集菌沉。向200 mL发酵液得到的菌沉加入20 mL的pH 5.4的10 mmol/L乙酸-乙酸钙缓冲溶液,振荡摇匀。将混匀的菌液置于0 ℃冰浴,超声破碎25 min。将破碎后的酶液进行离心,条件为:15 min、6 000 r/min,保留上清液(即粗酶液),于4 ℃冰箱保藏。
1.5 酶活力的测定
采用DNS法来测定右旋糖酐酶和右旋糖酐蔗糖酶的酶活力。
右旋糖酐蔗糖酶反应体系:200 μL适当稀释的酶液、2.8 mL质量分数10%的蔗糖溶液,10 mmol/L pH 5.5的乙酸钙缓冲溶液,25 ℃水浴1 h后,取500 μL反应液,加入375 μL的DNS溶液,沸水浴中煮沸5 min后,加入5 mL水,在520 nm下测定吸光值[2,14]。
酶活力定义为:上述条件下,每分钟产生1 μmol还原糖所需的酶量为1个单位(U)。
右旋糖酐酶反应体系:100 μL适当稀释的酶液、400 μL质量分数3%的T70溶液,10 mmol/L、pH 5.5的乙酸钙缓冲溶液,25 ℃水浴1 h后,加入375 μL的DNS溶液,沸水浴中煮沸5 min后,加入5 mL水,在540 nm下测定吸光值[4,14,16]。上述酶活力测定实验均独立重复3次。
1.6 酶学性质分析
1.6.1 最适温度及热稳定性测定
将酶进行适当稀释,在25~55 ℃温度条件下,pH 5.4,进行酶活力测定。以最高酶活力为100%,计算相对酶活力。在25、35、45、55 ℃下孵育60 min,考察酶的热稳定性。上述酶活力测定实验均独立重复3次。
1.6.2 最适pH及pH稳定性测定
将酶进行适当稀释,分别在右旋糖酐酶和右旋糖酐蔗糖酶的最适温度下测定不同pH值(5.0~10.0)条件下的酶活力。将酶用不同pH的乙酸-乙酸钙缓冲液进行稀释,在4 ℃下孵育1 h,在最适条件下测定剩余酶活力。以初始酶活力为100%,计算相对酶活力,考察酶的pH稳定性。上述酶活力测定实验均独立重复3次。
1.6.3 动力学常数测定
为测定融合酶的催化效率,分别以蔗糖和T70为底物,测定了融合酶中右旋糖酐蔗糖酶和右旋糖酐酶的动力学常数(Michaelis-Menten动力学常数,Km, Vmax),并计算了动力学参数(催化常数,kcat,以及与速度相关的方程的效率,kcat/Km)[14]。分别以0.2~1.0 mg/mL的蔗糖和5~10 mg/mL的T70为底物,在pH 5.4、30 ℃条件下测定右旋糖酐蔗糖酶活力,在pH 9.0、50 ℃条件下测定右旋糖酐酶活力,反应时间均为5 min,酶活力测定同上述酶测定。除另有说明,在相同条件下,通过Origin 2021程序使用Michaelis-Menten动力学方程进行计算。
1.7 右旋糖酐的酶法制备
将0.1 g/mL的蔗糖底物溶于乙酸-乙酸钙缓冲溶液中,加入终浓度5 U/mL(以融合酶中的右旋糖酐蔗糖酶酶活力添加)的融合酶,以融合酶中右旋糖酐蔗糖酶适宜的温度和pH为基准,在160 r/min条件下,反应24 h,沸水浴5 min,终止反应,离心除去蛋白,透析(500 kDa透析袋)24 h,干燥得到右旋糖酐产品。
游离酶反应中,游离的右旋糖酐蔗糖酶与右旋糖酐酶酶活力添加量同上述融合酶反应液中添加的融合酶酶活力一致。反应条件与反应后处理均同上述1.7节融合酶的一致。
1.8 右旋糖酐分子质量标定
产品使用HPLC在CXDH-3000工作站上进行分析。使用G6000 PWXL,G-DNA-PW(300 mm×7.8 mm)色谱柱对产物进行分离。流动相:水;流速0.6 mL/min;柱温40 ℃。用标准葡聚糖(200 000、2 518 000、3 450 000、6 100 000)测定产品分子质量。
将融合酶与游离酶的右旋糖酐产品进行HPLC检测,通过右旋糖酐标准曲线,对产物右旋糖酐分子质量进行标定,确定产物分子质量大小。
1.9 数据处理
实验均设立3组平行,利用Origin 2021软件绘制图表及处理数据。
2 结果与分析
2.1 融合酶的软件模拟
连接肽是融合酶组成中必不可少的重要元件。本文在来源于肠膜状明串珠菌0326的右旋糖酐蔗糖酶(图1-a)和来源于短杆菌的右旋糖酐酶BMdex(图1-c)之间添加刚性连接肽[(EAAAK)5](图1-b)进行融合酶的连接。这种刚性连接肽[(EAAAK)5]的引入会形成稳定的α螺旋结构,这种螺旋构象稳定的原因是片段内存在Glu-Lys+盐桥结构,形成了相对稳定的二级结构,使右旋糖酐蔗糖酶与右旋糖酐酶之间存在相对稳定的距离,在一定程度上降低了两种酶分子相互攻击的可能性,使得融合酶整体的构象较为稳定(图2)。
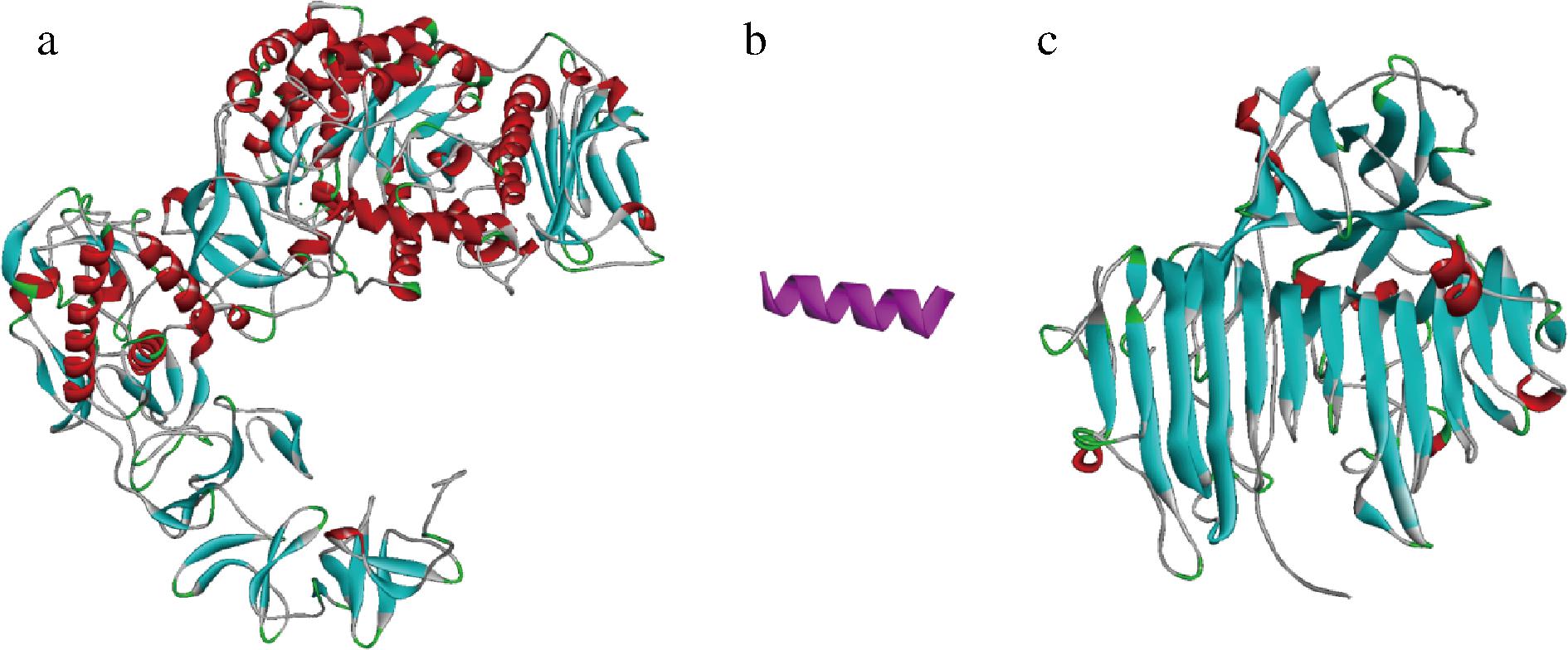
a-右旋糖酐蔗糖酶P473S;b-刚性连接肽; c-右旋糖酐酶BMdex的三维结构模拟图
图1 右旋糖酐蔗糖酶P473S、刚性连接肽、右旋糖酐酶 BMdex的三维结构模拟图
Fig.1 3D structural simulation diagrams of dextransucrase P473S, rigid connecting peptide and dextranase BMdex
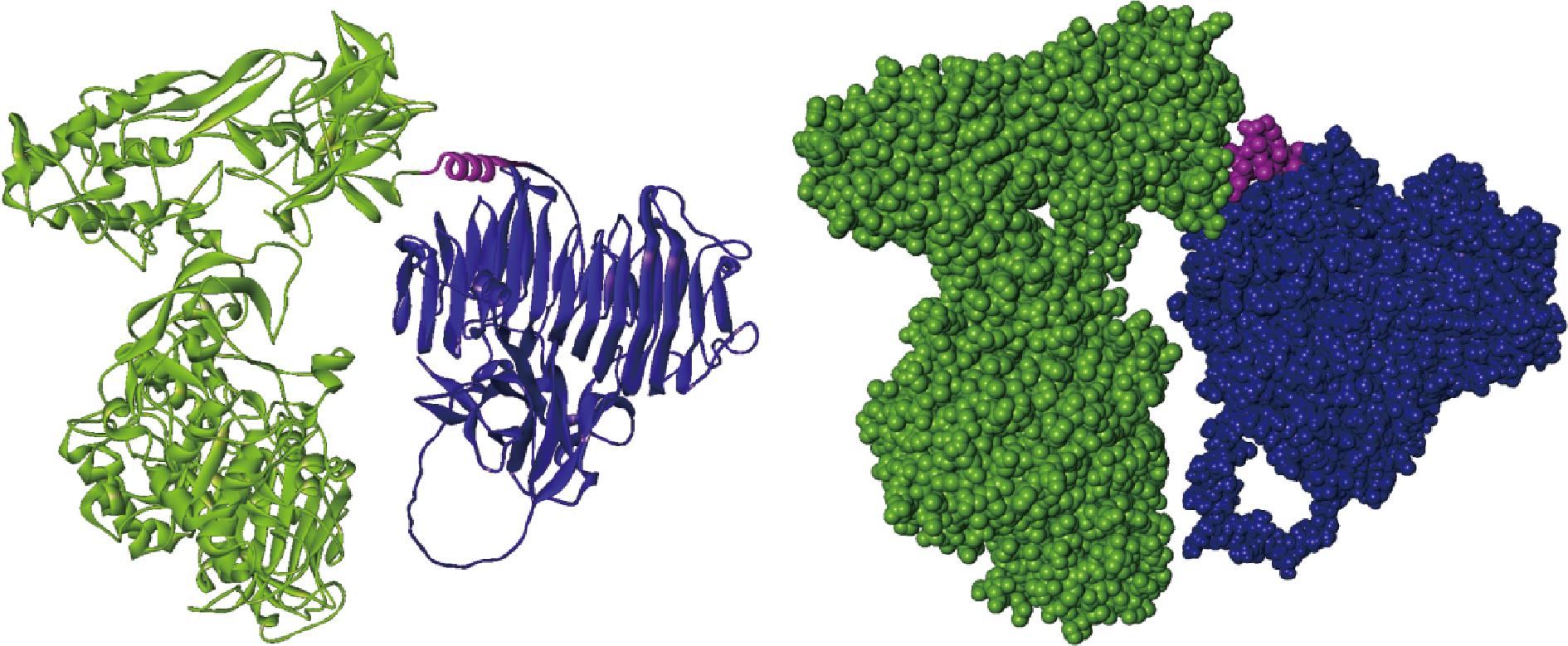
图2 融合酶的三维结构模拟图
Fig.2 3D structural simulation diagrams of the fusion enzyme
通过同源建模的方法构建得到融合前酶的三维结构模型(图1)以及融合后酶的三维结构模型(图2)。
2.2 重组质粒的构建与融合蛋白的表达
从菌液中提取质粒,获得含有右旋糖酐蔗糖酶P473S基因的质粒和右旋糖酐酶BMdex的质粒。通过PCR获得含有右旋糖酐蔗糖酶P473S和部分连接肽的载体片段(10 000 bp左右)以及右旋糖酐酶BMdex和部分连接肽的基因片段(2 000 bp),结果如图3所示,采用无缝克隆方法,将无缝克隆产物转化到Trans1-T1感受态,测序成功后(图4),转化到大肠杆菌中进行表达产酶,可以成功获得具有两种酶活力的融合酶。
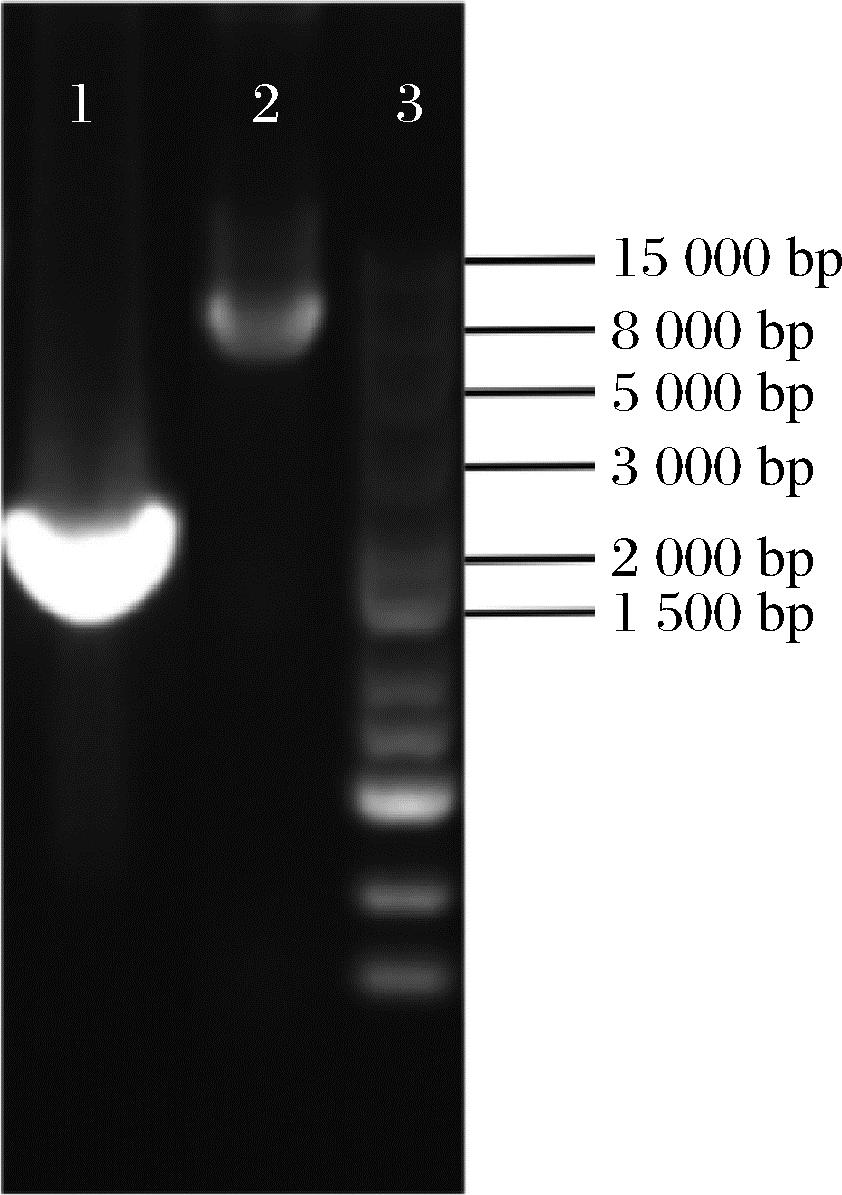
1-右旋糖酐酶BMdex基因片段;2-右旋糖酐蔗糖酶 P473S基因片段;3-Maker
图3 目的基因PCR扩增结果
Fig.3 Results of PCR amplification of target gene
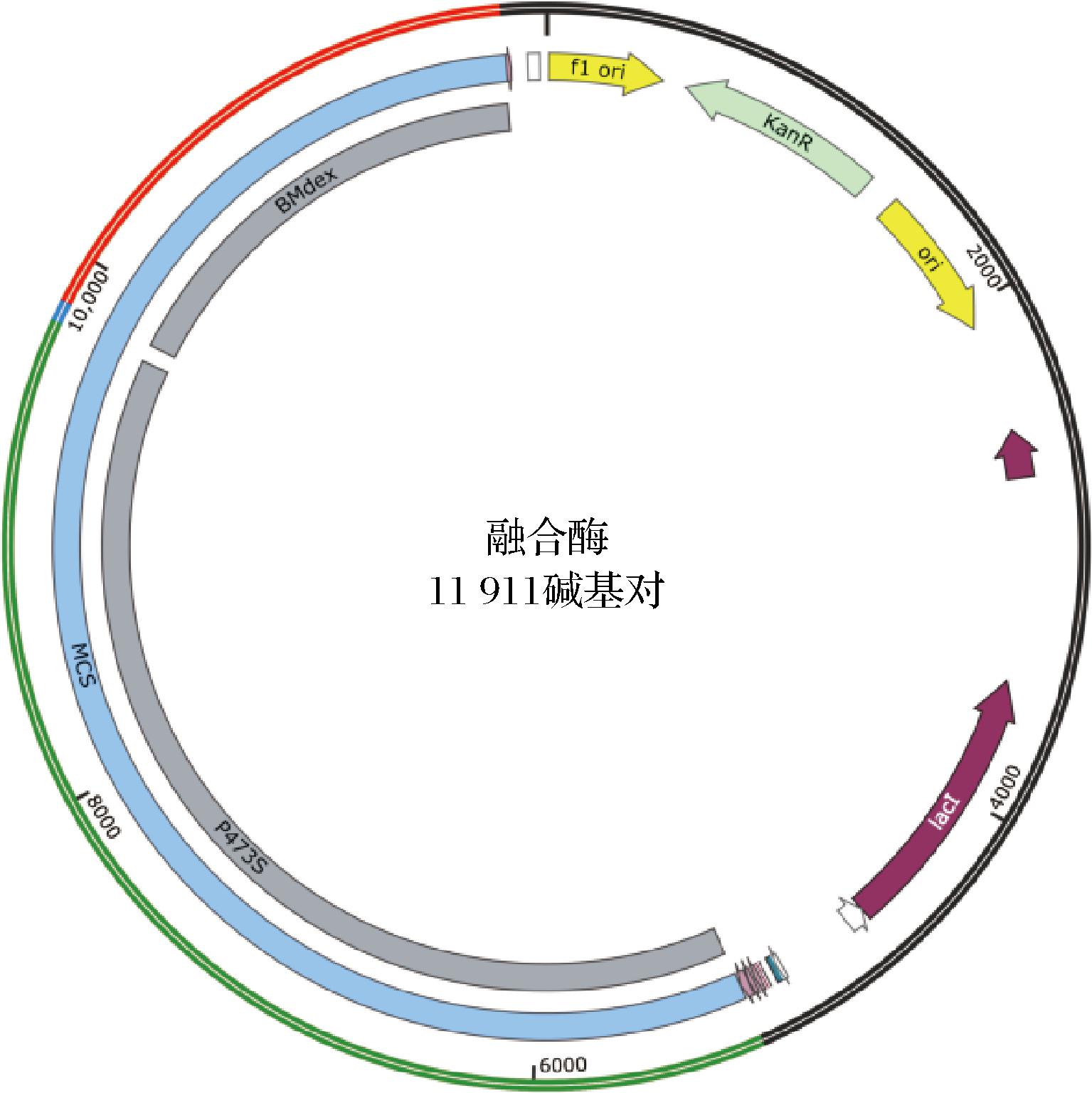
图4 融合酶的质粒示意图
Fig.4 Schematic diagram of plasmid for fusion enzyme
2.3 融合酶的酶学性质
2.3.1 融合酶的最适pH及pH稳定性
融合酶中的右旋糖酐蔗糖酶的最适pH值为5.5(图5-a),与游离酶相比最适pH并未发生变化;在pH 5.0~7.0时,融合酶中的右旋糖酐蔗糖酶的剩余酶活力基本一致,均能剩余40%左右的酶活力(图5-a)。融合酶中的右旋糖酐酶的最适pH值是9.0(图5-b),在pH 5.5~10.0能仍保有50%以上的酶活力。与游离的右旋糖酐酶相比,右旋糖酐酶的最适pH也未发生改变。

a-融合酶右旋糖酐蔗糖酶与游离右旋糖酐蔗糖酶最适pH;b-融合酶右旋糖酐酶与游离右旋糖酐酶最适pH; c-融合酶右旋糖酐蔗糖酶与游离右旋糖酐蔗糖酶pH稳定性;d-融合酶右旋糖酐酶与游离右旋糖酐酶pH稳定性
图5 融合前后右旋糖酐蔗糖酶和右旋糖酐酶最适pH及pH稳定性
Fig.5 Optimum pH and pH stability of free dextransucrase and free dextranase and fusion enzymes
与游离的右旋糖酐蔗糖酶相比,其在pH 7.0条件下,pH稳定性由原来剩余5%以下的酶活力提升到40%以上的剩余酶活力(图5-c)。融合酶提高了右旋糖酐蔗糖酶在pH 7.0的稳定性。这可能是由于融合酶中引入了刚性连接肽与右旋糖酐酶导致的。因为刚性连接肽[(EAAAK)5]的引入会形成稳定的α螺旋结构,使得右旋糖酐蔗糖酶与右旋糖酐酶之间保有相对固定的距离,在一定程度上降低了两种酶分子相互攻击的可能性,使融合酶整体的构象较为稳定。此外,因为游离的右旋糖酐酶在pH 5.0~10.0内本身就很稳定,在孵育1 h之后,酶活仍基本保持不变。且融合后的右旋糖酐酶的稳定性与游离的右旋糖酐酶相比基本也没有发生变化。因此在右旋糖酐蔗糖酶的C端与右旋糖酐酶的N端之间插入刚性连接肽构建得到融合酶,融合酶中的右旋糖酐蔗糖酶在pH 7.0的稳定性得以提高(图5-d),且融合后酶分子的构象也较为稳定(图2)。
2.3.2 融合酶的最适温度及温度稳定性
融合酶中右旋糖酐蔗糖酶最适温度是30 ℃(图6-a),且在25 ℃时有70%以上的酶活力,在35 ℃时保有50%左右的酶活力,后续随着温度升高,酶活力大幅降低。当温度达到55 ℃时,酶活力基本为零。与游离酶相比最适温度并未发生变化,但游离酶在25~35 ℃下均能保有80%以上的酶活力,优于融合酶。
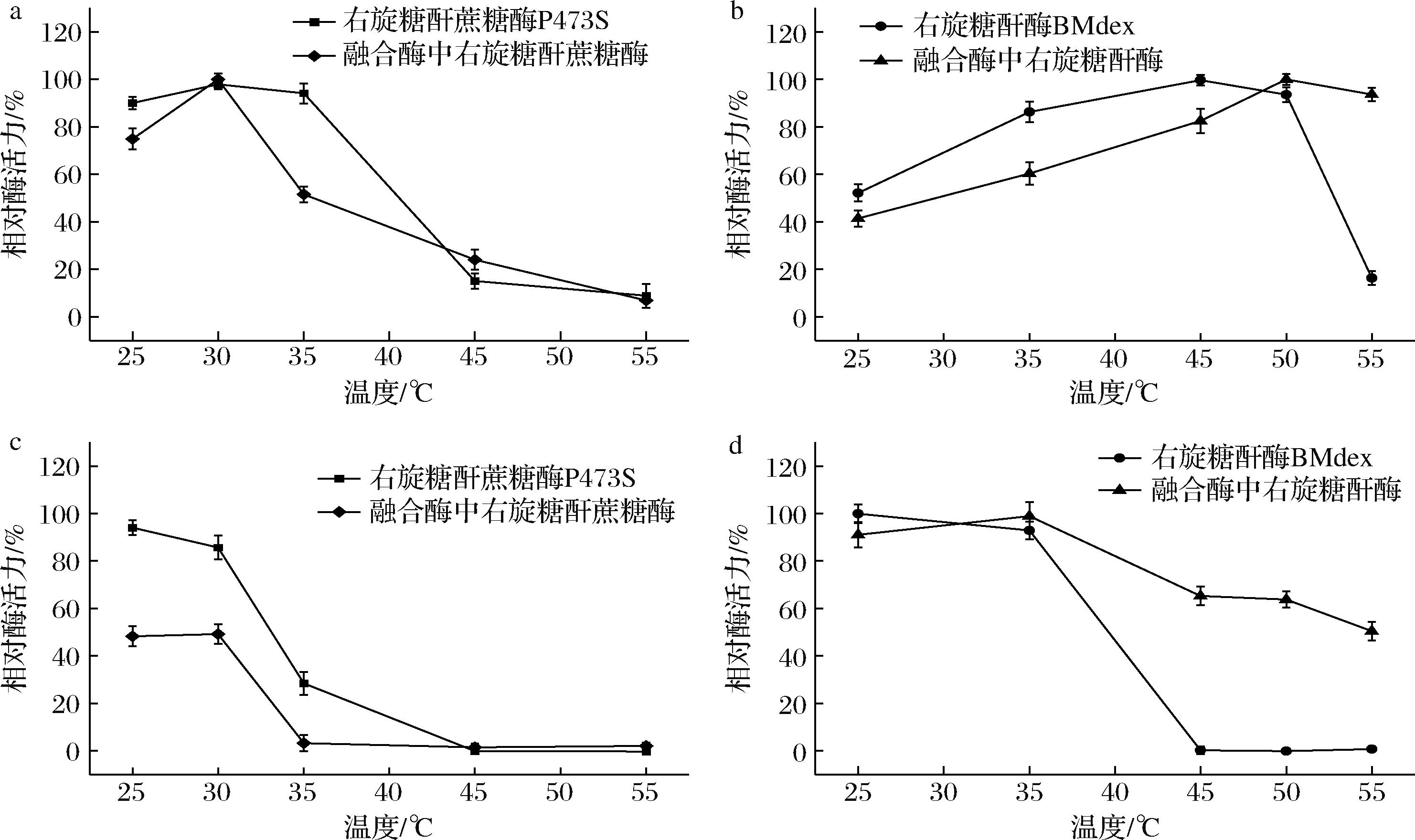
a-融合酶右旋糖酐蔗糖酶与游离右旋糖酐蔗糖酶最适温度;b-融合酶右旋糖酐酶与游离右旋糖酐酶最适温度; c-融合酶右旋糖酐蔗糖酶与游离右旋糖酐蔗糖酶温度稳定性;d-融合酶右旋糖酐酶与游离右旋糖酐酶温度稳定性
图6 融合前后右旋糖酐蔗糖酶和右旋糖酐酶最适温度及温度稳定性
Fig.6 Optimum temperature and temperature stability of free dextransucrase and dextranase and fusion enzyme
融合酶中的右旋糖酐蔗糖酶在25~30 ℃时,酶活力较稳定,孵育1 h后,酶活力仍剩余为原始酶活的50%以上(图6-c)。在温度达到35 ℃以上时,融合酶中的右旋糖酐蔗糖酶稳定性较差,孵育1 h后,酶活力几乎完全丧失。相比之下,游离酶的温度稳定性较好,在25 ℃下孵育1 h时,酶活力基本不变;在30 ℃时,剩余酶活力80%以上;在35 ℃时,酶活力仍保有30%。这表明融合蛋白酶中右旋糖酐酶的存在对右旋糖酐蔗糖酶的温度稳定性有负面影响。
融合酶中右旋糖酐酶的最适温度是50 ℃(图6-b),与游离酶相比提高了5 ℃。在45~55 ℃时,融合酶中右旋糖酐酶保有80%以上的酶活力,当温度低于35 ℃时,仅能发挥原始酶不到60%的活力。
在不同温度下孵育1 h,检测了游离酶和融合酶的热稳定性(图6-d)。在25~35 ℃时,融合酶中右旋糖酐酶和游离酶均非常稳定,孵育1 h后酶活力仍可以维持在90%以上;在45~55 ℃时,融合酶中的右旋糖酐酶酶活力可以维持在50%以上,而游离酶在该温度范围孵育1 h,几乎完全丧失酶活力,这表明右旋糖酐蔗糖酶的添加,使得右旋糖酐酶的稳定性得以提升。
2.3.3 融合酶的动力学参数测定
融合酶右旋糖酐蔗糖酶的Km高于游离酶(表2),说明融合后右旋糖酐蔗糖酶对蔗糖的亲和力比游离酶的亲和力低;融合酶右旋糖酐蔗糖酶的kcat/Km也低于游离酶(表2)。这表明,蛋白融合后,右旋糖酐酶的存在影响了右旋糖酐蔗糖酶对底物的亲和力和催化效率。
表2 右旋糖酐蔗糖酶和右旋糖酐酶融合前后的动力学参数
Table 2 Kinetic parameters of free dextrosesucrase and dextrose and fusion enzymes
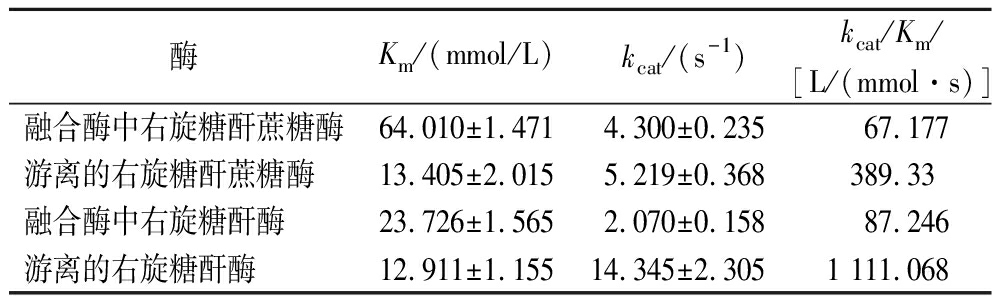
酶Km/(mmol/L)kcat/(s-1)kcat/Km/[L/(mmol·s)]融合酶中右旋糖酐蔗糖酶64.010±1.4714.300±0.235 67.177游离的右旋糖酐蔗糖酶13.405±2.0155.219±0.368389.33融合酶中右旋糖酐酶23.726±1.5652.070±0.15887.246游离的右旋糖酐酶12.911±1.15514.345±2.3051 111.068
融合酶右旋糖酐酶的Km高于游离酶(表2),说明融合后右旋糖酐酶的亲和力略低于游离酶的亲和力;融合酶右旋糖酐酶的kcat/Km远低于游离酶(表2)。这表明,蛋白融合后,右旋糖酐蔗糖酶的存在也影响了右旋糖酐酶对底物的亲和力和催化效率。这可能是融合后两种酶之间存在的空间位阻导致的。
2.4 右旋糖酐产物分析
由右旋糖酐标品Mw及相应出峰时间(Ve)拟合得到lgMw与Ve对应的线性方程式:lgMw=-0.098 4Ve+7.740 8,R2=0.996 9。
在25 ℃,pH 5.5条件下,按照上述1.7节进行实验。分别对游离酶与融合酶生产的的右旋糖酐产物进行HPLC检测(图7)。D值是表征右旋糖酐均一性的重要指标。当D=1时,为均一分子质量的右旋糖酐。D的数值比1越大说明分子质量分布越宽,右旋糖酐的分散性程度越大。通过表3可知,融合酶生产的右旋糖酐产物较为均一,D值为1.13,重均分子质量在2 MDa左右;而游离酶的分布指数大于融合酶的,说明其右旋糖酐产物的分散程度更大,产物重均分子质量在2.2~7.7 MDa。融合酶中刚性连接肽的引入形成了稳定的α-螺旋,可能会参与“底物通道”[14]的形成,两种酶之间存在顺序级联关系,当底物蔗糖出现时,融合酶中的右旋糖酐蔗糖酶首先发挥作用,催化α-1,2糖苷键的断裂,聚合蔗糖中的葡萄糖生成右旋糖酐。与此同时,右旋糖酐通过底物通道及时被右旋糖酐酶的催化活性部位所捕捉,右旋糖酐酶开始发挥水解作用,断裂右旋糖酐中的α-1,6糖苷键,最终生成分子质量为2 MDa的右旋糖酐产物。这是融合酶产生2 MDa均一右旋糖酐产物的原因。同时也是催化效率优于游离酶的原因。
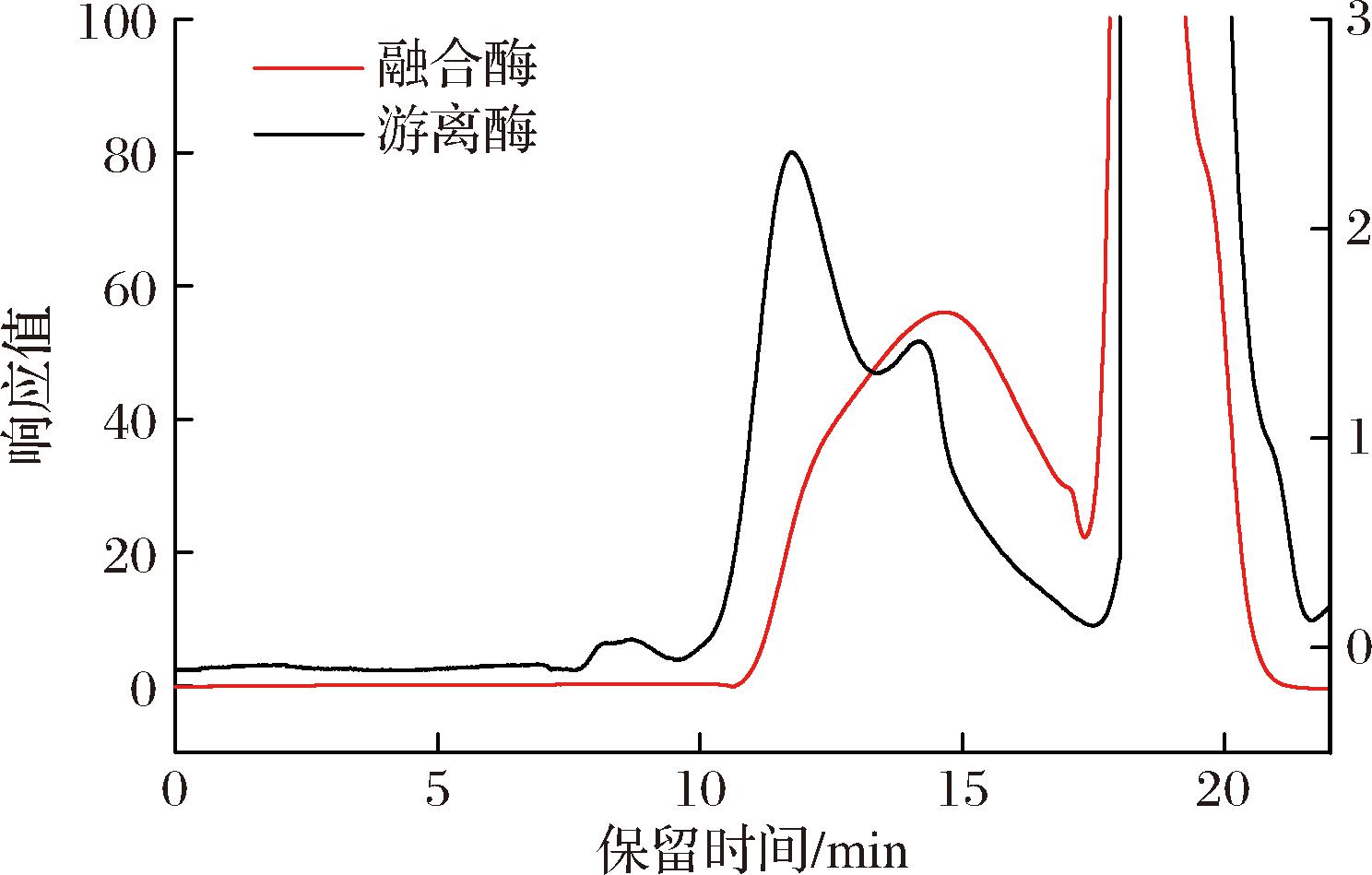
图7 融合酶与游离酶的催化产物HPLC图
Fig.7 HPLC plots of the catalytic products of the fusion enzyme and the free enzyme
表3 融合酶与游离酶的产物比较
Table 3 Comparison of the products of the fusion enzyme and the free enzyme
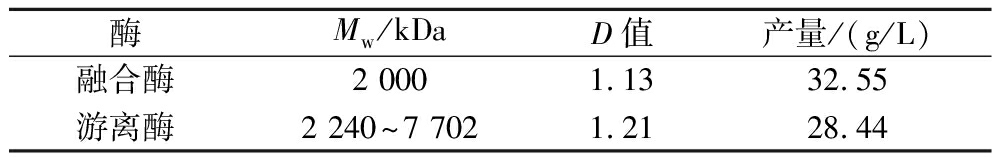
酶Mw/kDaD值产量/(g/L)融合酶2 0001.1332.55游离酶2 240~7 7021.2128.44
因此,通过构建融合酶,一步酶法合成右旋糖酐,无论是在产物的均一性上,还是产率上均有所提高。融合酶生产右旋糖酐T2000,产率可以达到32.6%。
3 结论与讨论
通过对来源于肠膜状明串珠菌0326的右旋糖酐蔗糖酶和来源于短杆菌的右旋糖酐酶BMdex基因之间添加刚性连接肽,成功实现了双酶的融合表达,获得了具有右旋糖酐蔗糖酶和右旋糖酐酶双酶活性的融合蛋白。研究结果显示,融合酶中右旋糖酐蔗糖酶的最适pH值是5.5、最适温度是30 ℃,在25~30 ℃内比较稳定;融合酶中右旋糖酐酶的最适pH值是9.0、最适温度是50 ℃。融合酶中引入的右旋糖酐酶在pH 5.0~10.0条件下本身就很稳定,孵育1 h后,酶活力基本保持不变,融合后右旋糖酐酶的稳定性基本没有发生变化,从而对融合酶中右旋糖酐蔗糖酶在pH 7.0时的稳定性产生了正面影响。同时,融合酶中右旋糖酐蔗糖酶的添加也提高了融合酶中右旋糖酐酶在45~55 ℃的温度稳定性。这两种酶之间存在顺序级联关系,融合酶中通过引入刚性连接肽,可能形成了底物通道,底物通过“连续性机制”被催化合成右旋糖酐产物,经过分离纯化后可以得到纯度较高且重均分子质量在2 MDa左右的均一右旋糖酐,产率可以达到32.6%。该基础研究为工业化一步酶法生产2 MDa左右分子质量的右旋糖酐提供了依据。
[1] CHEN Z W, CHEN J J, NI D W, et al.Microbial dextran-hydrolyzing enzyme:Properties, structural features, and versatile applications[J].Food Chemistry, 2024, 437:137951.
[2] NAESSENS M, CERDOBBEL A, SOETAERT W, et al.Leuconostoc dextransucrase and dextran:Production, properties and applications[J].Journal of Chemical Technology &Biotechnology, 2005, 80(8):845-860.
[3] 梁明征. 生物合成右旋糖酐及分子量调控[D].广西:广西民族大学, 2012.LIANG M Z.Biosynthesis dextran and molecular weight control by the biological[D].Guangxi:Guangxi University for Nationalities, 2012.
[4] 王雪娇, 覃琴, 李媚, 等.右旋糖酐酶调控右旋糖酐分子质量研究进展[J].食品科技, 2020, 45(6):310-315.WANG X J, QIN Q, LI M, et al.Research progress of dextranase regulating dextran molecular weight[J].Food Science and Technology, 2020, 45(6):310-315.
[5] BEJAR W, GABRIEL V, AMARI M, et al.Characterization of glucansucrase and dextran from Weissella sp.TN610 with potential as safe food additives[J].International Journal of Biological Macromolecules, 2013, 52:125-132.
[6] 相萍萍. 生物法调控右旋糖酐分子量的研究进展[J].食品安全导刊, 2023(28):159-161.XIANG P P.Progress in biological regulation of dextran molecular weight[J].China Food Safety Magazine, 2023(28):159-161.
[7] MOULIS C, JOUCLA G, HARRISON D, et al.Understanding the polymerization mechanism of glycoside-hydrolase family 70 glucansucrases[J].Journal of Biological Chemistry, 2006, 281(42):31254-31267.
[8] 李廿, 曾平, 唐梅, 等.生物合成中低分子量右旋糖酐的初步研究[J].广西民族大学学报(自然科学版), 2014, 20(2):80-83.LI N, ZENG P, TANG M, et al.Preliminary study on the biosynthesis of low molecular weight dextran[J].Journal of Guangxi University for Nationalities (Natural Science Edition), 2014, 20(2):80-83.
[9] 黄双霞, 相萍萍, 齐鹏翔, 等.酶法合成右旋糖酐过程规律的研究[J].中国调味品, 2018, 43(7):43-49.HUANG S X, XIANG P P, QI P X, et al.Study on the process law of enzymatic synthesis of dextran[J].China Condiment, 2018, 43(7):43-49
[10] 黄瑞杰, 李媚, 廖安平, 等.酸解法与酶解法调控右旋糖酐分子质量的比较[J].食品科学, 2020, 41(6):43-50.HUANG R J, LI M, LIAO A P, et al.Comparison of acid hydrolysis and enzymatic hydrolysis of dextran[J].Food Science, 2020, 41(6):43-50.
[11] IQBAL S, MARCHETTI R, AMAN A, et al.Enzymatic and acidic degradation of high molecular weight dextran into low molecular weight and its characterizations using novel diffusion-ordered NMR spectroscopy[J].International Journal of Biological Macromolecules, 2017, 103:744-750.
[12] 于玥, 陈华磊, 李素霞, 等.葡聚糖超声降解的反应动力学研究[J].应用化工, 2017, 46(3):473-476;480.YU Y, CHEN H L, LI S X, et al.Study on the reaction kinetic model of dextran polymers during ultrasonic degradation[J].Applied Chemical Industry, 2017, 46(3):473-476;480.
[13] MENG X F, PIJNING T, DOBRUCHOWSKA J M, et al.Characterization of the functional roles of amino acid residues in acceptor-binding subsite +1 in the active site of the glucansucrase GTF180 from Lactobacillus reuteri 180[J].Journal of Biological Chemistry, 2015, 290(50):30131-30141.
[14] 张宇馨. 基于低分子量右旋糖酐生物合成的右旋糖酐蔗糖酶的融合改造及其分子机制研究[D].合肥:合肥工业大学, 2022.ZHANG Y X.Fusion modification of dextran sucrase based on low molecular weight dextran biosynthesis and its molecular mechanism[D].Hefei:Hefei University of Technology, 2022.
[15] D AZ-MONTES E.Dextran:Sources, structures, and properties[J].Polysaccharides, 2021, 2(3):554-565.
AZ-MONTES E.Dextran:Sources, structures, and properties[J].Polysaccharides, 2021, 2(3):554-565.
[16] NGUYEN T T H, LEE D G, APU M A I, et al.The bifidogenic effects and dental plaque deformation of non-digestible isomaltooligosaccharides synthesized by dextransucrase and alternansucrase[J].Enzyme and Microbial Technology, 2022, 153:109955.
[17] KIM Y M, SEO M Y, KANG H K, et al.Construction of a fusion enzyme of dextransucrase and dextranase:Application for one-step synthesis of isomalto-oligosaccharides[J].Enzyme and Microbial Technology, 2009, 44(3):159-164.