泻剂结肠是长期服用类似番泻叶、大黄等蒽醌类刺激性泻药所致的一种慢传输型便秘[1],与普通便秘最大的区别在于其组织病理学上表现出严重的肠神经和肠道屏障损伤[2],尤其是肠神经胶质细胞(enteric glail cells, EGCs)的数量减少以及功能障碍、肠神经元退行性变化,以及肠道黏膜结构的破坏,炎症水平的上升和肠道菌群的显著改变[3]。
肠动力受肠神经的控制,而2020年发表在Nature上的文章揭示了肠神经主要受到肠道菌群的控制[4]。基于此,则建立了肠道菌群-肠神经-肠动力三者间的关系。发表在Journal of Clinical Investigation上的研究发现[5],EGCs(肠神经的重要组成部分)敲除鼠,表现出严重的肠道炎症及肠动力的减弱,这提示了肠神经-肠免疫-肠动力间的相关性。综合上述研究猜测:通过改变肠道菌群-肠神经-肠免疫互作可调节肠动力。
应用益生菌调控胃肠道健康已得到研究者的广泛认可。益生菌主要是通过改善肠腔环境,调节宿主肠道免疫等方式发挥作用[6]。例如乳酸菌通过与上皮细胞相互作用并调节细胞因子水平来影响宿主免疫反应[7],乳酸菌还能够抑制炎症性NF-κB信号通路的激活、降低诱导型一氧化氮合酶水平并减弱对便秘的促炎反应[8]。团队前期研究发现,益生菌,特别是副干酪乳酪杆菌CCFM1164在缓解泻剂结肠的同时,修复了肠神经,主要表现为显著提高了EGCs的数量[9]。这提示了副干酪乳酪杆菌CCFM1164或是通过调节肠道菌群及其代谢产物,从而调控肠神经-肠免疫互作去发挥对泻剂结肠的缓解作用。基于此,本研究拟从肠道菌群-肠神经-肠免疫的角度探究副干酪乳酪杆菌CCFM1164缓解泻剂结肠的可能作用途径,研究结果将为包含泻剂结肠在内的慢传输型便秘的治疗方向以及副干酪乳酪杆菌缓解泻剂结肠的研究提供理论基础。
1 材料与方法
1.1 材料和仪器
1.1.1 材料与试剂
实验菌株,本实验所用菌株CCFM1164(Lacticaseibacillus paracasei)来源于江南大学生物技术中心菌种保藏库。
番泻叶提取物,西安旭煌生物技术有限公司;琥珀酸普芦卡必利,江苏豪森药业集团有限公司;活性炭粉、PCR扩增引物以及合成序列,生工生物工程(上海)股份有限公司;伊文思蓝,美国Sigma-Aldrich公司;阿拉伯树胶粉、乙酸、丙酸、丁酸,国药集团化学试剂公司;小鼠胶质细胞源性神经营养因子(glial cell line-derived neurotrophic factor,GDNF)、小鼠脑源性神经营养因子(brain-derived neurotrophic factor,BDNF)、小鼠5羟色胺(5-hydroxytryptamine,5-HT)、小鼠乙酰胆碱(acetylcholine,ACh)、小鼠神经元型一氧化氮合酶(neuronsal nitric oxide synthase,nNOS)和小鼠血管活性肠肽(vasoactive intestinal peptide,VIP)ELISA试剂盒,南京森贝伽生物科技有限公司;白细胞介素-1β(interleukin-1β,IL-1β),R&D Systems(中国);白细胞介素-22(interleukin 22,IL-22)ELISA试剂盒,南京福麦斯生物技术有限公司;反转录试剂盒、HiScript III RTSuperMix for qPCR试剂盒,南京诺唯赞生物科技有限公司;粪便DNA快速提取试剂盒,美国MP公司。
1.1.2 仪器与设备
Multiscan Go多功能酶标仪、RC BIOS 10落地式离心机,美国Thermo公司;真空冷冻干燥机,美国LABCONCO公司;GC-MS、Milli-Q水净化系统,密理博(中国)有限公司;CFX 384 qPCR仪器,伯乐公司;Pannoramic MIDI数字切片扫描仪,匈牙利3DHistech;MiSeq PE300高通量测序平台,美国Illumina公司。
1.2 实验方法
1.2.1 菌种活化培养
取-80 ℃冷冻保藏的菌液,用一次性接种环蘸取少量菌液在MRS固体培养基上划线分离,37 ℃恒温培养48 h,挑取单菌落接种于液体MRS培养基中,37 ℃培养24 h,以2%接种量传代2次进行活化并扩大培养18 h,以转速8 000 r/min,4 ℃下离心10 min收集菌泥,无菌生理盐水洗涤2次后用10%脱脂乳重悬至5×109 CFU/mL,分装于保菌管-80 ℃冻存。
1.2.2 动物实验设计
于北京维通利华公司购入8周龄的SPF级雄性C57BL/6J小鼠24只,动物伦理审查编号:JN.No20220615c1201125[217]。饲养环境温度(23±2) ℃,相对湿度(50±10)%,光照和黑夜各12 h更替。给予1周的环境适应时间后,随机分为4组,分别为:空白组(NC)、模型组(CC)、阳性药物普芦卡必利组(PRU)、副干酪乳酪杆菌CCFM1164组(CCFM1164)(已公开于专利CN112877260A),每组6只小鼠,每天早上9点开始灌胃,每次0.2 mL。菌悬液的灌胃剂量为5×109 CFU/mL,普芦卡必利的剂量为0.384 mg/mL,实验动物设计方案见图1。
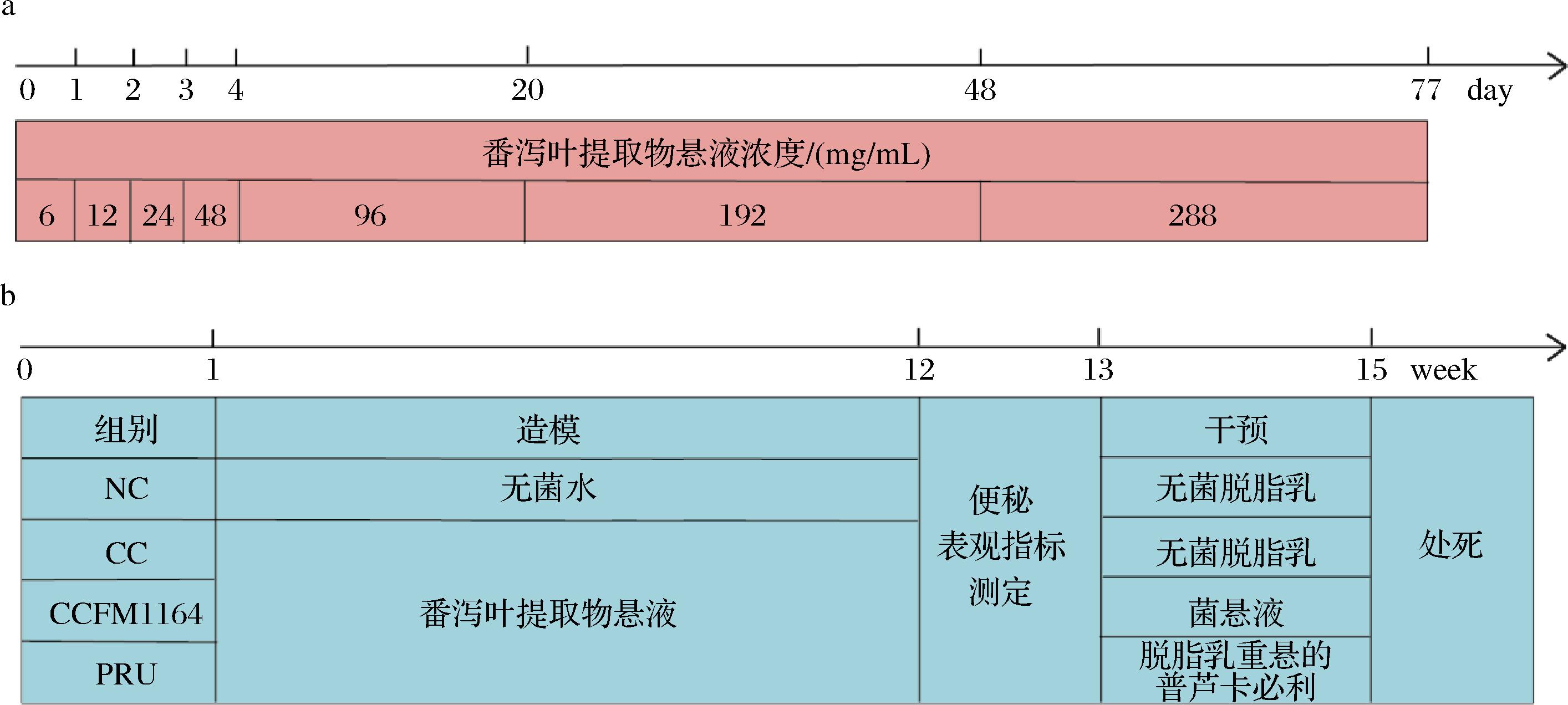
a-小鼠造模步骤;b-动物实验方案
图1 动物实验设计方案
Fig.1 Design for animal experiments
1.2.3 泻剂结肠小鼠便秘相关指标测定
单独收集每只小鼠的粪便样本,分别测量其冻干前后的粪便湿重和干重,粪便含水量的计算如公式(1)所示:
粪便含水量![]()
(1)
每只小鼠灌胃0.2 mL伊文思蓝半液体溶液[3](2.5%伊文思蓝和1%甲基纤维素),并记录每只小鼠排首粒蓝便时间和5 h内排蓝便粒数。
在处死小鼠之前向每只小鼠灌胃0.2 mL墨汁,30 min后处死解剖,剪取上端自幽门下端至盲肠,测量小肠全长为“小肠总长度”,从幽门位置到墨汁前端位置为“墨汁推进长度”,小肠推进率的计算如公式(2)所示:
小肠推进率![]()
(2)
1.2.4 小鼠结肠组织神经营养因子含量、神经递质分泌、炎症因子水平测定
使用对应ELISA试剂盒小鼠结肠组织中GDNF、BDNF、5-HT、ACh、VIP、nNOS、IL-22、IL-1β的蛋白含量,详细步骤见于相关试剂盒说明书。
1.2.5 小鼠结肠组织S100β、GFAP、5-HT4基因表达水平检测
采用实时荧光定量聚合酶链反应(fluorescence real time quantitative polymerase chain reaction,RT-qPCR)来测定S100β、GFAP、5-HT4基因的表达量。使用Trizol法提取结肠总RNA后将小鼠结肠总RNA反转录为cDNA。生工生物工程(上海)股份有限公司合成各引物序列。小鼠S100β、GFAP、5-HT4基因和内参基因GAPDH基因引物如表1所示。
表1 引物序列
Table 1 Primers sequence
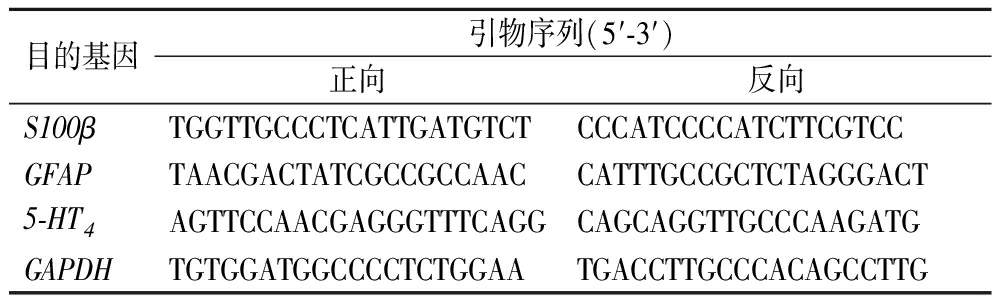
目的基因引物序列(5′-3′)正向反向S100βTGGTTGCCCTCATTGATGTCTCCCATCCCCATCTTCGTCCGFAPTAACGACTATCGCCGCCAACCATTTGCCGCTCTAGGGACT5-HT4AGTTCCAACGAGGGTTTCAGGCAGCAGGTTGCCCAAGATGGAPDHTGTGGATGGCCCCTCTGGAATGACCTTGCCCACAGCCTTG
根据试剂盒说明书制备RT-qPCR体系,在qPCR仪中对小鼠结肠各基因的转录水平进行检测。
1.2.6 粪便短链脂肪酸(short chain fatty acids, SCFAs)测定
小鼠粪便冻干后参照毛丙永[10]的方法进行处理后,使用GC-MS测定粪便中的SCFAs含量。使用软件Xcalibur分析结果。
1.2.7 肠道菌群16S rRNA测序分析
使用试剂盒从粪便样本中提取微生物基因组DNA。采用通用引物(341F和806R)进行V3~V4区特异性扩增。按照TIABgel Mini纯化试剂盒的说明书纯化PCR产物,Qubit dsDNA检测试剂盒对DNA进行定量和混样。在MiSeq PE300平台上使用MiSeq试剂盒对纯化扩增子进行测序。使用QIIME2平台进行原始数据处理和生物信息学分析。微生物群落的β多样性和门水平相对丰度利用在线网站(https://www.ChiPlot.online/)进行可视化分析。采用线性判别分析效应值(LDA effect size,LEfSe)计算微生物类群的差异丰度,并利用在线网站(https://www.bioincloud.tech/)绘制分类分支树。
1.3 统计与分析
数值表示为“平均值±标准差”(mean ± SD),采用Prism 9.5进行统计分析和图形绘制。空白组与模型组采用t-test进行比较,模型组与干预组采用one-way ANOVA分析。#代表空白组与模型组之间有显著差异。显著性标准设为P<0.05;显著性等级以符号数目区分,其中#P<0.05,##P<0.01,###P<0.001,####P<0.0001。*代表干预组与模型组之间有显著差异。显著性标准设为P<0.05;显著性等级以符号数目区分,其中*P<0.05,**P<0.01,***P<0.001,****P<0.000 1。
2 结果与分析
2.1 副干酪乳酪杆菌CCFM1164可缓解泻剂结肠
由图2可知,泻剂结肠小鼠排首粒黑便时间明显增加(即全肠道转运时间延长)、小肠推进率无明显变化、粪便含水量显著下降(P<0.01),表明泻剂结肠小鼠的肠道转运障碍主要发生在结肠。这些结果与以往的研究一致[11],表明泻剂结肠小鼠模型构建成功。
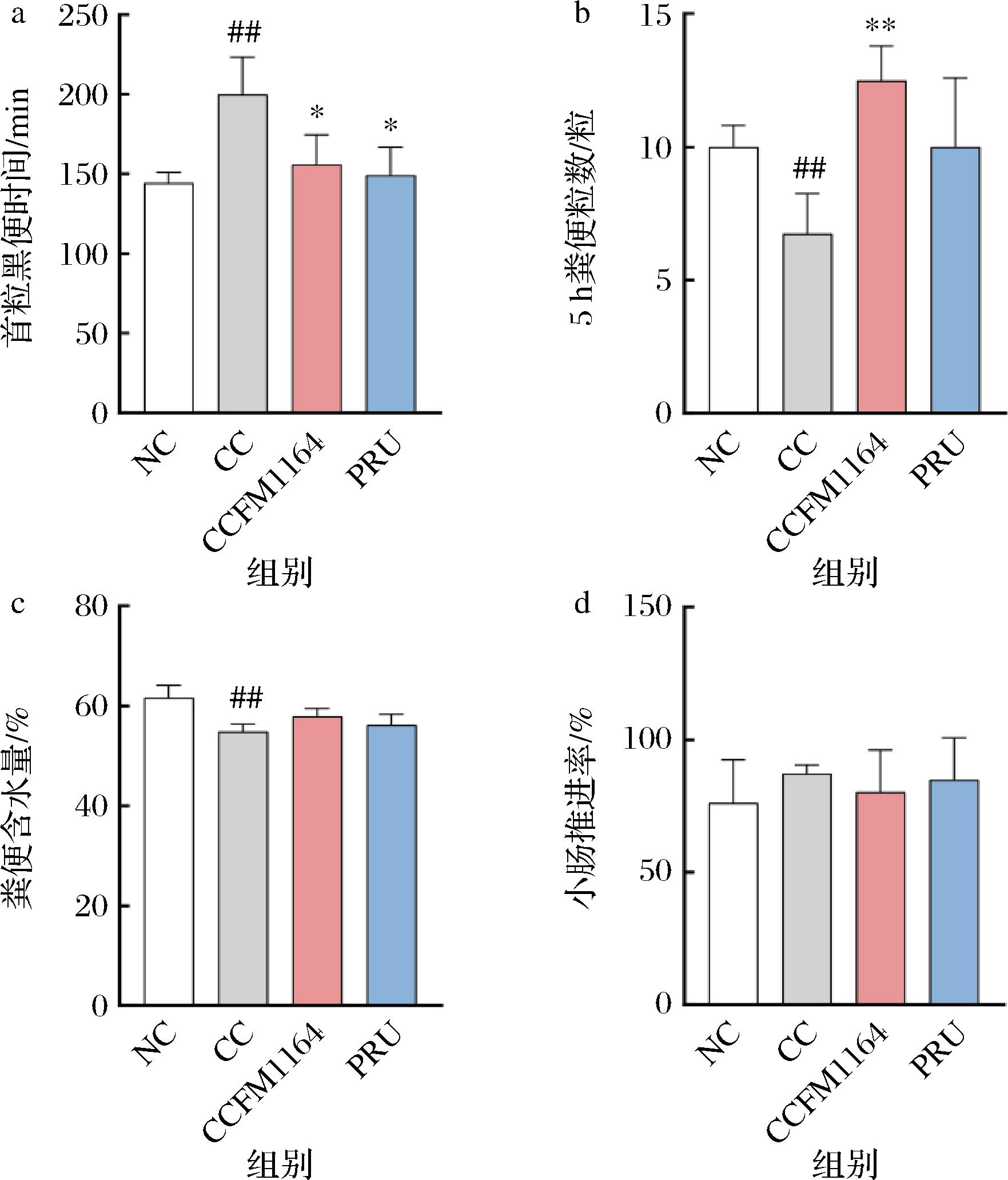
a-首粒黑便时间;b-5 h粪便粒数;c-粪便含水量;d-小肠推进率
图2 副干酪乳酪杆菌CCFM1164对便秘相关指标的影响
Fig.2 Effects of Lactobacillus paracasei CCFM1164 on constipation-related indicators
注:*表示P<0.05,**表示P<0.01,***表示P<0.001,****表示 P<0.0001(干预组与模型组比较);#表示P<0.05,##表示P<0.01, ###表示P<0.001,####表示P<0.0001(模型组与 空白组比较)(下同)。
相较于模型组,副干酪乳酪杆菌CCFM1164干预可将泻剂结肠小鼠的排首粒黑便时间明显缩短(P<0.05)、5 h粪便粒数较模型组也显著提高(P<0.01)(图2-a、图2-b),并且在5 h粪便粒数这一指标上效果优于阳性药物普芦卡必利。说明副干酪乳酪杆菌CCFM1164可以缓解泻剂结肠小鼠的便秘症状。
2.2 副干酪乳酪杆菌CCFM1164缓解泻剂结肠的作用研究
2.2.1 副干酪乳酪杆菌CCFM1164修复泻剂结肠小鼠受损的肠神经系统
胃肠道的运动、分泌和吸收等功能受到肠神经系统的严格调控以达到最优效能[12]。其中,EGCs是肠神经系统的重要组成部分,具有支持、营养和保护肠神经元,维持肠道稳态的作用,正常生理状态下EGCs可以分泌保护性神经营养因子如GDNF、BDNF等进而促进肠神经的发育,EGCs和肠神经元之间也存在活跃的信号机制,能够调控胃肠道反射、调节肠动力。生理性肠神经元-神经胶质信号传导涉及胆碱能信号传导,并且有数据指出,结肠中的EGCs优先被兴奋性传递激活,对抑制性神经元不反应或处于抑制性状态[13-14]。
因此,本文对泻剂结肠小鼠结肠组织中EGCs特征标志物(S100β和GFAP)mRNA表达水平,GDNF、BDNF两种神经营养因子的蛋白含量以及5-HT、ACh、NO、VIP的蛋白含量进行了检测。其中NO化学性质活泼,在体内很容易被氧化,因此这里通过检测nNOS来表征NO水平的变化情况。由图3可知,CC组小鼠S100β和GFAP表达量、GDNF水平相比于NC组显著下降(P<0.01),提示泻剂结肠小鼠存在肠神经系统受损。副干酪乳酪杆菌CCFM1164干预后,EGCs标志蛋白基因S100β和GFAP表达水平较模型组分别有所提高(图3-a、图3-b)、GDNF水平显著提高(图3-c)(P<0.01)。泻剂结肠小鼠BDNF水平确有下降,CCFM1164干预后BDNF水平有所回升,且各组之间上升幅度的趋势与GDNF一致(图3-d),此趋势侧面反映了长期的番泻叶提取物处理确实损害了小鼠结肠部位的EGCs,造成了EGCs的功能障碍,但总的来说益生菌干预之后BDNF的含量变化并无统计学意义。此外,泻剂结肠小鼠结肠组织中5-HT、ACh含量相比于NC组明显减少,副干酪乳酪杆菌CCFM1164干预后ACh含量有所上升(图3-e)(P<0.05),而5-HT含量无显著变化(图3-f)。模型组结肠中nNOS含量极显著上调,而VIP含量虽然有上升趋势,但无显著性变化。益生菌干预后对nNOS含量有下调的趋势,但无显著性变化,而对于VIP含量的调节,各组均没有效果(图3-g、图3-h)。

a-S100β相对表达量;b-GFAP相对表达量;c-GDNF含量;d-BDNF含量;e-Ach浓度;f-5-HT浓度;g-nNOS浓度; h-VIP浓度;i-5-HT4相对表达量
图3 副干酪乳酪杆菌CCFM1164对肠神经系统的影响
Fig.3 Effects of Lactobacillus paracasei CCFM1164 on the enteric nervous system
因此推测是GDNF这一神经营养因子在EGCs修复肠神经时起到了关键作用,而ACh的增加是激活EGCs促进其分泌GDNF的主要原因。
2.2.2 副干酪乳酪杆菌CCFM1164对泻剂结肠小鼠肠道生物屏障的影响
当下,肠道微生物群被认为是有助于调节宿主健康的关键性要素之一,肠道菌群与多种肠道疾病密切相关[15]。对小鼠粪便肠道菌群进行16S rRNA测序和分析,以探究副干酪乳酪杆菌CCFM1164对泻剂结肠小鼠肠道菌群多样性及丰富度的影响。与NC组相比,泻剂结肠小鼠的Chao1指数和Shannon指数显著降低(图4-a、图4-b)(P<0.001),表明长期番泻叶处理会导致微生物群α多样性降低,CCFM1164增强了泻剂结肠小鼠的这两个指标(P<0.01、P<0.001)。在PCoA中观察到NC、CC和CCFM1164明显的分离(图4-c),表明泻剂结肠小鼠的菌群组成发生了显著变化,CCFM1164的干预调节了肠道微生物群组成。计算了肠道菌群在门水平上的相对丰度,结果如图4-c所示,CC组的厚壁菌门(Firmicutes)/拟杆菌门(Bacteroidetes)(F/B)比率低于NC组,CCFM1164处理逆转了泻剂结肠小鼠中F/B的失调。
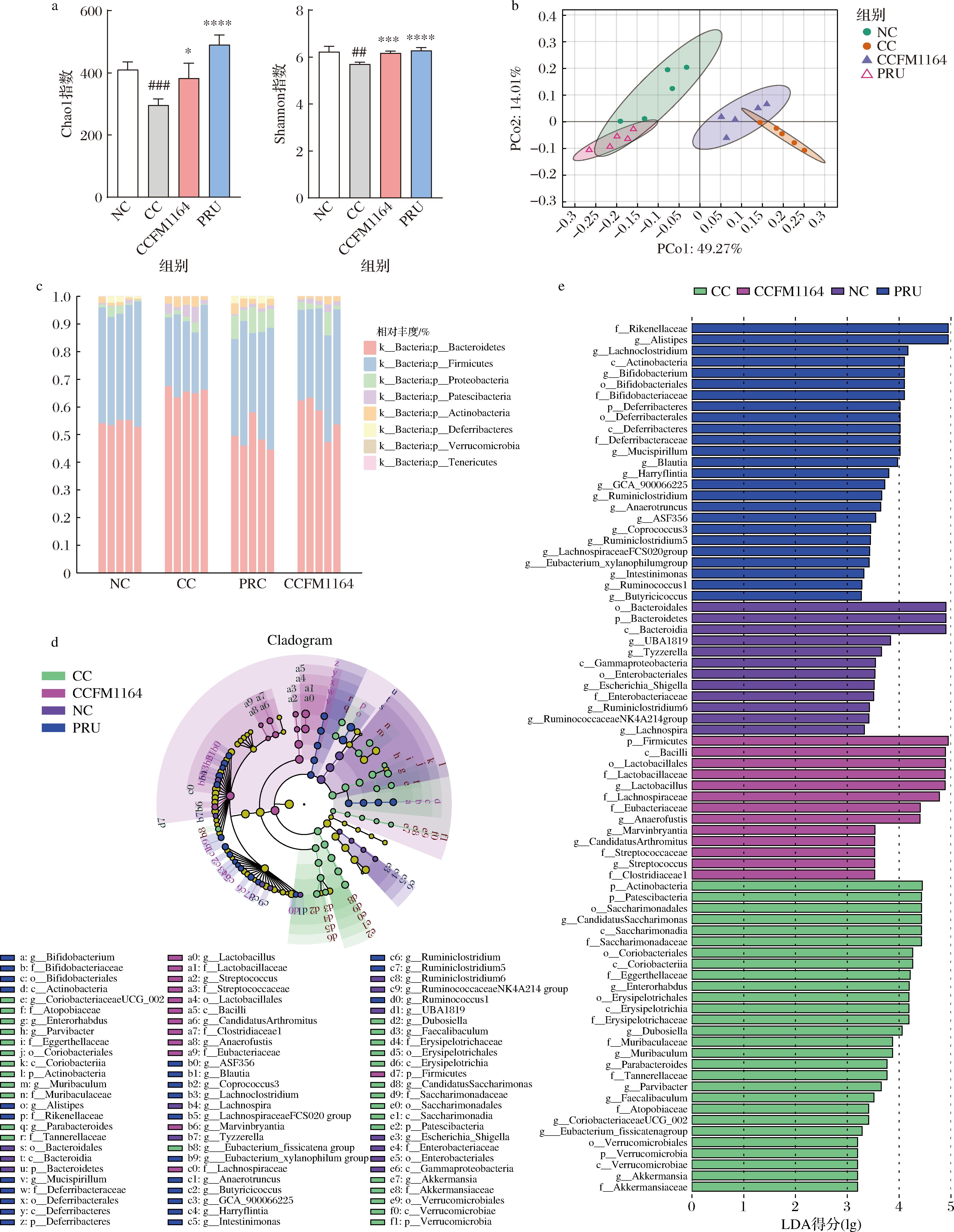
a-肠道菌群α多样性;b-肠道菌群β多样性;c-门水平相对丰度;d-LEfSe分析;e-基于LDA的分布直方图(LDA得分>3.0)
图4 副干酪乳酪杆菌CCFM1164对肠道生物屏障的影响
Fig.4 Effects of Lactobacillus paracasei CCFM1164 on the intestinal biological barrier
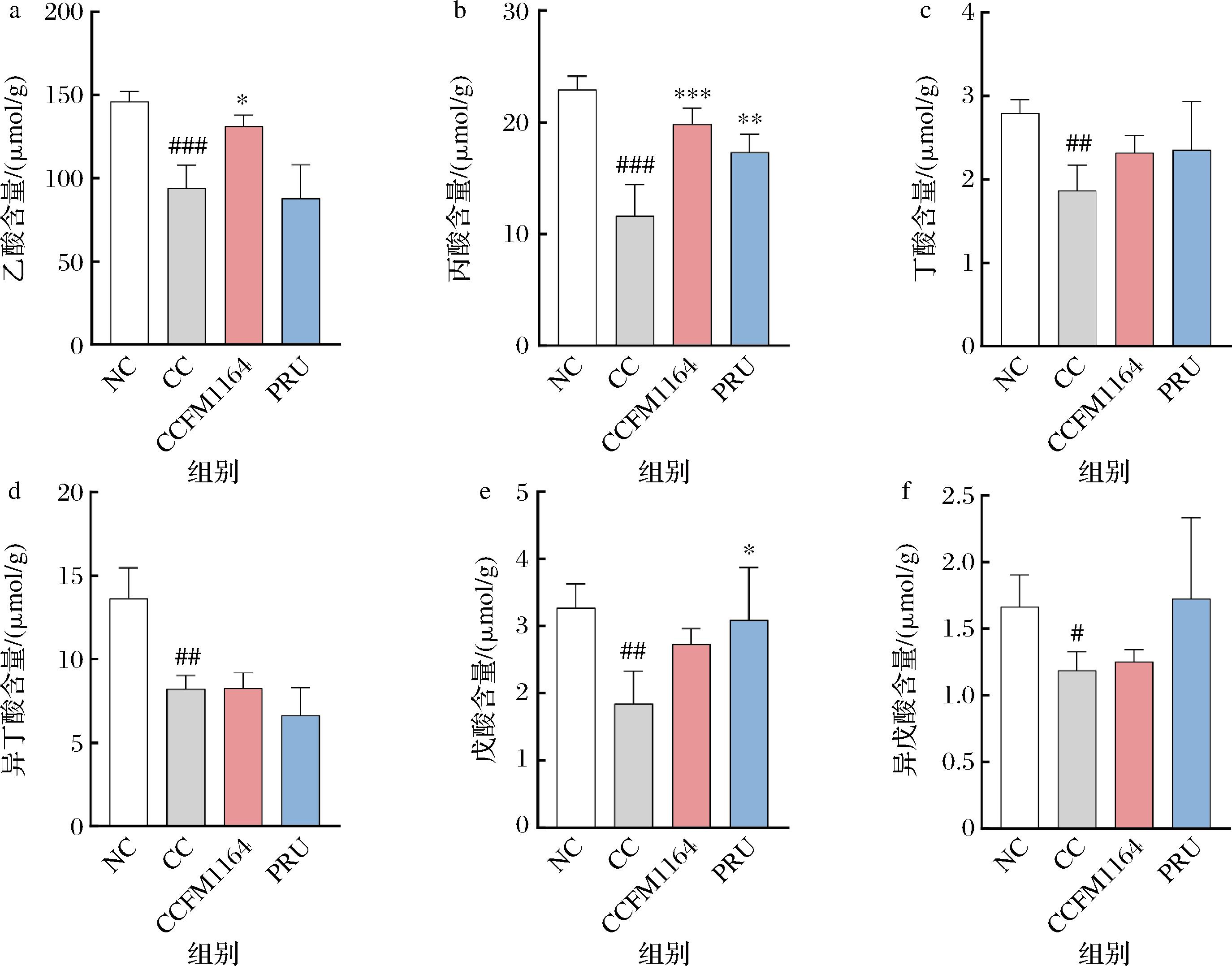
a-乙酸含量;b-丙酸含量;c-丁酸含量;d-异丁酸含量;e-戊酸含量;f-异戊酸含量
图5 副干酪乳酪杆菌CCFM1164对肠道化学屏障的影响
Fig.5 Effects of Lactobacillus paracasei CCFM1164 on the intestinal chemical barrier
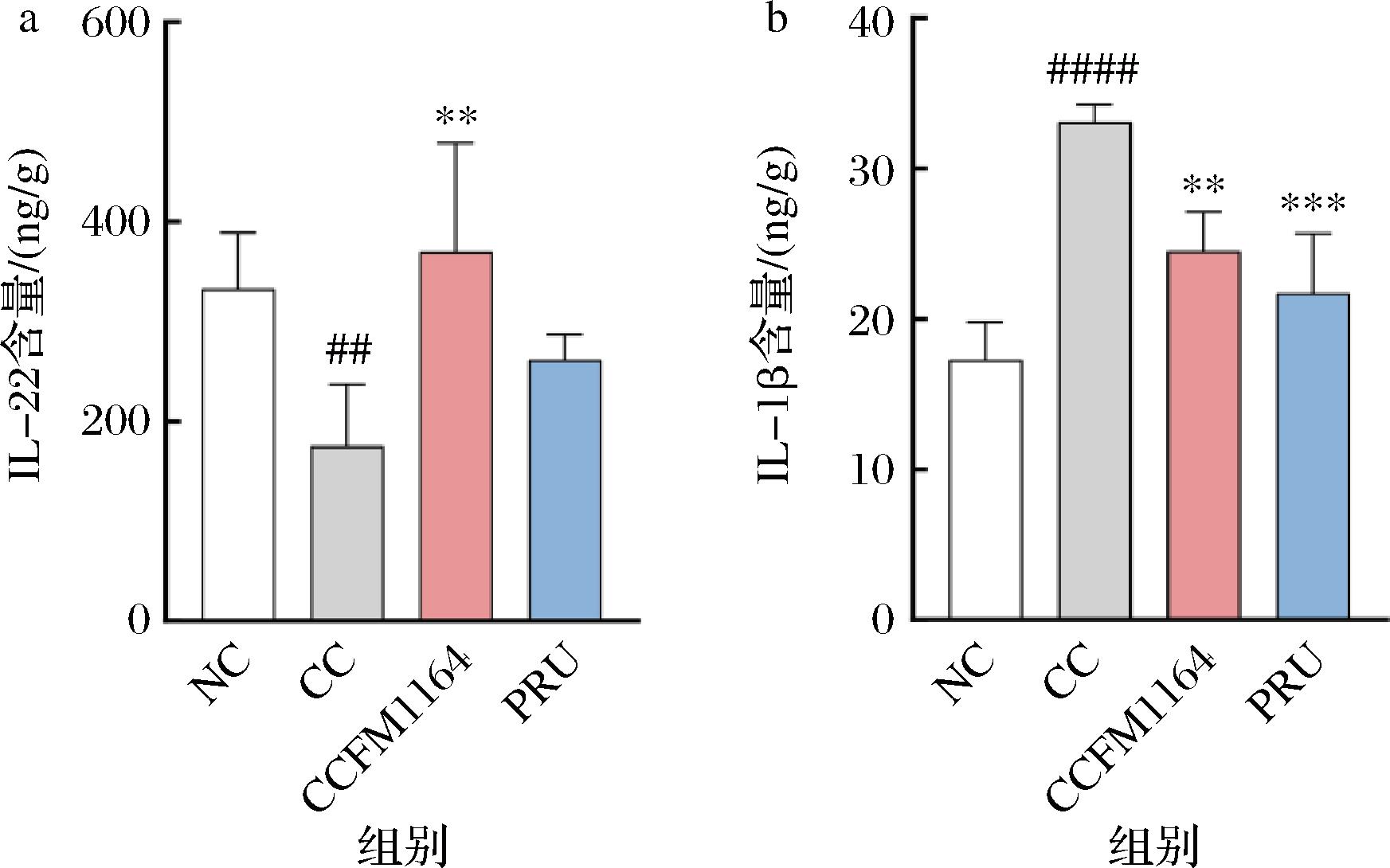
a-IL-22含量;b-IL-1β含量
图6 副干酪乳酪杆菌CCFM1164对肠道免疫屏障的影响
Fig.6 Effects of Lactobacillus paracasei CCFM1164 on the intestinal immune barrier
LEfSe分析(LDA>3)确定了各组之间的显著差异物种。结果如图4-d和图4-e所示。NC组的特征菌群毛螺菌科(Lachnospira)、瘤胃球菌属(Ruminiclostridum)6、瘤胃球菌属(Ruminococcaceae)NK4A214 group等,其中Lachnospira是肠道核心菌属,属于厚壁菌门毛螺菌属,该菌属存在于大多数健康人的肠道里,与多种碳水化合物的代谢相关[16]。Ruminiclostridum也能够降解纤维素产生SCFAs[17]。CC组的特征菌群有红蝽菌科(Coriobacteriaceae)UCG 002、Enterorhabdus、Candidatus Saccharimonas等,其中Coriobacteriaceae UCG-002属于红蝽菌科,产生苯酚和对甲酚,这两种物质都具有细胞毒性并降低肠屏障功能[18],Candidatus Saccharimonas是条件致病菌,被报道与IL-1β等促炎因子呈显著正相关。CCFM1164组特征菌群是乳杆菌属(Lactobacillus)、Anaerofustis、Marvinbryantia等,其中Lactobacillus可通过发酵碳水化合物产生SCFAs[19],Marvinbryantia的增多也能引起SCFAs的增加[20]。SCFAs与多种代谢性疾病和慢性炎症呈负相关,具有抗炎特性,促进肠道黏膜的修复[21]。
肠道菌群产生的SCFAs与结肠内稳态和免疫功能有着广泛的联系[22]。因此副干酪乳酪杆菌CCFM1164处理小鼠肠道中产生SCFAs细菌的增加可能是其调节肠道稳态的重要因素。
2.2.3 副干酪乳酪杆菌CCFM1164对泻剂结肠小鼠肠道化学屏障的影响
肠道微生物会影响肠道内多种代谢物进而调节肠道动力[6]。检测粪便中SCFAs含量以探究副干酪乳酪杆菌CCFM1164对泻剂结肠的缓解是否与SCFAs的变化有关。相较于对照组来说,模型组小鼠粪便中乙酸、丙酸、丁酸、异丁酸、戊酸、异戊酸含量均显著降低,表明长期番泻叶处理导致泻剂结肠小鼠粪便中短链脂肪酸含量显著下降。副干酪乳酪杆菌CCFM1164干预后,乙酸和丙酸含量都显著升高(P<0.05、P<0.001),并且效果要优于普芦卡必利(图5-a~图5-f)。
2.2.4 副干酪乳酪杆菌CCFM1164对泻剂结肠小鼠肠道免疫屏障的影响
肠道炎症也会影响肠道运动,细胞因子IL-1β是炎症反应的关键介质,可能会加剧慢性疾病和急性组织损伤期间的损害,IL-22的释放可以调节肠道炎症[23]。本文检测了IL-1β、IL-22两种细胞因子的蛋白含量来探究肠道炎症水平。结果如图6所示,CC组与NC组相比,IL-1β水平显著升高(P<0.000 1)、而IL-22显著下降(P<0.05),表明番泻叶长期处理后小鼠存在肠道炎症。应用副干酪乳酪杆菌CCFM1164干预后,显著降低了机体的炎症水平,改善了肠道免疫屏障。
2.2.5 副干酪乳酪杆菌CCFM1164对泻剂结肠小鼠肠道机械屏障的影响
肠道菌群、神经和免疫系统的许多相互作用起源于肠道黏膜[24]。H&E染色可用于评估结肠组织的损伤情况。观察图7小鼠结肠组织的病理切片,模型组小鼠的结肠部位显示出更严重的组织病理学损伤,模型组小鼠结肠组织的黏液层变薄,隐窝结构缩短,杯状细胞减少,并且存在炎症浸润的现象(图7-b)。但是灌胃副干酪乳酪杆菌CCFM1164后,小鼠结肠组织中的黏液层变厚,杯状细胞的界限更加清晰明了,同时平滑肌结构也较为完整(图7-c)。以上结果表明副干酪乳酪杆菌CCFM1164修复了泻剂结肠小鼠受损的肠道机械屏障。

a-NC组H&E染色;b-CC组H&E染色;c-CCFM1164组H&E染色;d-PRU组H&E染色;e-组织病理学评分
图7 CCFM1164对肠道机械屏障的影响
Fig.7 Effects of Lactobacillus paracasei CCFM1164 on the intestinal mechanical barrier
3 结论
本研究表明副干酪乳酪杆菌CCFM1164可缓解泻剂结肠,且其缓解作用可能是通过改变肠道菌群,显著提高产SCFAs菌的相对丰度,从而提高小鼠肠道内SCFAs水平,促进结肠中兴奋性神经递质ACh的分泌,从而刺激EGCs分泌GDNF,修复小鼠肠神经的损伤,降低肠道炎症,修复肠道机械屏障损伤,从而缓解疾病。本文对于副干酪乳酪杆菌CCFM1164缓解泻剂结肠可能途径的探究为后续对于副干酪乳酪杆菌缓解泻剂结肠关键物质的确定和作用机制的解析提供了良好的理论基础和研究方向。
[1] WU J S, LIU B H, TONG W D, et al.Opioid receptors and associated regulator of G protein signaling are involved in the cathartic colon of rats[J].Experimental and Therapeutic Medicine, 2015, 9(4):1229-1234.
[2] 李鑫萍, 王琳琳, 赵建新, 等.两歧双歧杆菌FGSYC45M3缓解泻剂结肠及其作用机制分析[J].食品与发酵工业, 2021, 47(22):42-48.LI X P, WANG L L, ZHAO J X, et al.Analysis of the effects on cathartic colon alleviation by Bifidobacterium bifidum FGSYC45M3 and its mechanism[J].Food and Fermentation Industries, 2021, 47(22):42-48.
[3] TANG N, YU Q Q, MEI C X, et al.Bifidobacterium bifidum CCFM1163 alleviated cathartic colon by regulating the intestinal barrier and restoring enteric nerves[J].Nutrients, 2023, 15(5):1146.
[4] OBATA Y, CASTA O
O  , BOEING S, et al.Neuronal programming by microbiota regulates intestinal physiology[J].Nature, 2020, 578(7794):284-289.
, BOEING S, et al.Neuronal programming by microbiota regulates intestinal physiology[J].Nature, 2020, 578(7794):284-289.
[5] SHARKEY K A.Emerging roles for enteric Glia in gastrointestinal disorders[J].The Journal of Clinical Investigation, 2015, 125(3):918-925.
[6] BERGMAN K R, LIU S X L, TIAN R L, et al. Bifidobacteria stabilize claudins at tight junctions and prevent intestinal barrier dysfunction in mouse necrotizing enterocolitis[J]. The American Journal of Pathology, 2013, 182(5): 1595-1606.
[7] WANG L L, CHAI M, WANG J L, et al.Bifidobacterium longum relieves constipation by regulating the intestinal barrier of mice[J].Food &Function, 2022, 13(9):5037-5049.
[8] ZHOU X, CHEN Y F, MA X, et al.Efficacy of Bacillus coagulans BC01 on loperamide hydrochloride-induced constipation model in Kunming mice[J].Frontiers in Nutrition, 2022, 9:964257.
[9] 李鑫萍. 乳酸菌对泻剂结肠的缓解作用探究[D].无锡:江南大学, 2021.LI X P.The study of alleviation effects on cathartic colon by lactic acid bacteria[D].Wuxi:Jiangnan University, 2021
[10] 毛丙永. 功能性低聚糖对肠道细菌的影响及机制[D].无锡:江南大学, 2015.MAO B Y.Effects of functional oligosaccharides on the gut bacteria and the mechanism[D].Wuxi:Jiangnan University, 2015.
[11] 张燕, 李红岩.泻剂引起结肠壁形态学改变的临床意义[J].中国临床解剖学杂志, 2004, 22(4):405-407;416.ZHANG Y, LI H Y.The clinical significance of rhubarb causing the morphological changes in colon wall[J].Chinese Journal of Clinical Anatomy, 2004, 22(4):405-407;416.
[12] KOVLER M L, GONZALEZ SALAZAR A J, FULTON W B, et al.Toll-like receptor 4-mediated enteric Glia loss is critical for the development of necrotizing enterocolitis[J].Science Translational Medicine, 2021, 13(612):eabg3459.
[13] SEGUELLA L, GULBRANSEN B D.Enteric glial biology, intercellular signalling and roles in gastrointestinal disease[J].Nature Reviews.Gastroenterology &Hepatology, 2021, 18(8):571-587.
[14] SORET R, SCHNEIDER S, BERNAS G, et al.Glial cell-derived neurotrophic factor induces enteric neurogenesis and improves colon structure and function in mouse models of hirschsprung disease[J].Gastroenterology, 2020, 159(5):1824-1838.
[15] DE VOS W M, TILG H, VAN HUL M, et al.Gut microbiome and health:Mechanistic insights[J].Gut, 2022, 71(5):1020-1032.
[16] VACCA M, CELANO G, CALABRESE F M, et al.The controversial role of human gut Lachnospiraceae[J].Microorganisms, 2020, 8(4):573.
[17] WU W, ZHOU J W, XUAN R R, et al.Dietary κ-carrageenan facilitates gut microbiota-mediated intestinal inflammation[J].Carbohydrate Polymers, 2022, 277:118830.
[18] YU Z T, LI D G, SUN H X.Herba Origani alleviated DSS-induced ulcerative colitis in mice through remolding gut microbiota to regulate bile acid and short-chain fatty acid metabolisms[J].Biomedicine &Pharmacotherapy, 2023, 161:114409.
[19] YU J S, YOUN G S, CHOI J, et al.Lactobacillus lactis and Pediococcus pentosaceus-driven reprogramming of gut microbiome and metabolome ameliorates the progression of non-alcoholic fatty liver disease[J].Clinical and Translational Medicine, 2021, 11(12):e634.
[20] WANG Z X, SHAO D, WU S, et al.Heat stress-induced intestinal barrier damage and dimethylglycine alleviates via improving the metabolism function of microbiota gut brain axis[J].Ecotoxicology and Environmental Safety, 2022, 244:114053.
[21] YAN C, HUANG S H, DING H F, et al.Adverse effect of oxidized cholesterol exposure on colitis is mediated by modulation of gut microbiota[J].Journal of Hazardous Materials, 2023, 459:132057.
[22] VAN DER HEE B, WELLS J M.Microbial regulation of host physiology by short-chain fatty acids[J].Trends in Microbiology, 2021, 29(8):700-712.
[23] IBIZA S, GARC A-CASSANI B, RIBEIRO H, et al.Glial-cell-derived neuroregulators control type 3 innate lymphoid cells and gut defence[J].Nature, 2016, 535(7612):440-443.
A-CASSANI B, RIBEIRO H, et al.Glial-cell-derived neuroregulators control type 3 innate lymphoid cells and gut defence[J].Nature, 2016, 535(7612):440-443.
[24] MACPHERSON A J, PACHNIS V, PRINZ M.Boundaries and integration between microbiota, the nervous system, and immunity[J].Immunity, 2023, 56(8):1712-1726.