动物肠道健康在养殖业中至关重要,幼龄动物易遭受外界因素诱发炎性肠病(inflammatory bowel disease,IBD),导致体温升高、食欲不振,严重者因腹泻脱水而死亡[1]。抗生素可用于治疗肠道炎症,但由于抗生素的过度使用,导致动物性食品中抗生素残留物、耐药菌产生,严重威胁人类健康,因此养殖业推出“禁抗”令,在此背景下,寻找能够减少炎症反应,改善肠道黏膜屏障、促进肠道黏膜修复、维持肠道微生态平衡的“绿色”生物饲料添加剂至关重要。
植物乳杆菌可以有效减轻动物结肠炎症状并表现出菌株特异性[2-3],LI等[4]研究发现低剂量的鼠李糖乳杆菌(Lactobacillus rhamnosus)可以缓解断奶仔猪急性炎症和腹泻;但高剂量L. rhamnosus减少了回肠食糜中乳杆菌属(Lactobacillius)和拟杆菌属(Bacteroides)的相对丰度,肠道 pH 值升高,容易诱发断奶仔猪腹泻,造成不良影响。因此,需要精确地探究植物乳杆菌对不同动物的最适剂量,而且在实际操作中乳酸菌的大规模制备面临成本高、推广难以及剂量不定等问题,限制了其规模化应用。
研究发现,发酵豆粕(fermented soybean meal, FSBM)在幼龄动物胃肠发育调控方面有“替抗”潜力[5],豆粕经过微生物发酵后适口性改良,抗营养因子含量显著减少,有机酸含量提高,大量增殖的有益菌和发酵产生的消化酶能把豆粕中的大分子蛋白质转化为活性小肽、游离氨基酸、脂肪酸等营养物质,显著减轻了幼龄动物消化压力[6-7]。ZHU等[8]研究发现,在断奶仔猪饲料中添加FSBM能够提高平均日增重,降低腹泻发病率,显著提高血清中免疫球蛋白含量;鲁春玲等[9]研究发现,在饲料中添加FSBM能提高肉鸡生长性能、血清超氧化物歧化酶活性;CATAL N等[10]研究发现,FSBM可促进鱼类肠道乳酸菌生长和黏蛋白产生。上述研究表明,在养殖过程中,FSBM 可以提高动物生长性能和肠胃发育,降低腹泻率,具有成本低、流通性强、易推广等优势。然而,目前关于 FSBM 对动物肠道屏障的保护作用、抗炎作用及益生机理的相关研究较为缺乏。
N等[10]研究发现,FSBM可促进鱼类肠道乳酸菌生长和黏蛋白产生。上述研究表明,在养殖过程中,FSBM 可以提高动物生长性能和肠胃发育,降低腹泻率,具有成本低、流通性强、易推广等优势。然而,目前关于 FSBM 对动物肠道屏障的保护作用、抗炎作用及益生机理的相关研究较为缺乏。
本实验室前期筛选获得了一株植物乳杆菌DY6[11-12],拥有较强的耐酸、耐胆盐、产酸和抑菌等特点,用其发酵豆粕能够显著提高豆粕中有机酸、小肽、总酸含量[13],现已建成年产10万t FSBM生产线。本研究探讨植物乳杆菌DY6FSBM对结肠炎小鼠的防治效果,探究其抑菌、抗炎和修复黏膜的作用,为养殖业预防和缓解动物结肠炎提供理论参考。
1 材料与方法
1.1 实验材料
1.1.1 实验动物与菌种
实验动物:SPF级BALB/c雄性小鼠,体重18~20 g,6~8周龄,购买于斯贝福生物技术有限公司,所有动物实验均按照《实验动物饲养与使用准则》(许可证号:SYXK 2021-0056)进行,并经江南大学动物伦理委员会批准(许可证号:JN.No20221130b0200110[472])。
实验菌株:植物乳杆菌DY-6,本实验室保存。
1.1.2 试剂与药品
参照文献配制[11] MRS 液体培养基,所需试剂和药品购自国药化学试剂有限公司。葡聚糖硫酸钠(dextran sodium sulfate,DSS)分子质量为35 000~40 000 Da,美国MP公司;美沙拉嗪,上海爱的发制药有限公司;隐血检测试剂盒,上海源叶生物有限公司;白细胞介素-6(interleukin-6,IL-6)ELISA检测试剂盒、肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)ELISA检测试剂盒,上海酶联生物有限公司。豆粕,益海嘉里有限公司。
1.1.3 仪器与设备
1260 Infinity Ⅱ高效液相色谱,美国安捷伦有限公司;ST-16R高速冷冻离心机,赛默飞世尔科技(中国)有限公司;SCIENTZ-10ND/C冷冻干燥机,宁波新芝生物科技股份有限公司;CFX Opus 96实时荧光定量PCR仪,美国Bio-Rad公司;XSP-63A光学显微镜,日本Nikon;DHP-9162恒温培养箱,上海医疗器械研究所;QWZY-C3组合式摇床,上海跃进医疗器械厂;LS-B50L型立式圆形压力蒸气灭菌器,上海医用核子仪器厂。
1.1.4 实验菌株和饲料的制备
在无菌条件下,挑取冻存的植物乳杆菌DY6划线于MRS固体培养基上,在37 ℃恒温培养箱中培养1~2 d直到长出单菌落。无菌条件下挑取单菌落,接种于含有50 mL MRS液体培养基的三角瓶中,37 ℃、250 r/min培养12 h,继续传代培养2~3代,得到植物乳杆菌DY6的种子液。
冻干菌粉制备:将种子液在4 ℃,10 000 r/min离心10 min收集菌泥,用PBS清洗3次。将菌泥称重后按照 1∶0.5(g∶mL)的比例加入灭菌生理盐水,加入质量分数10%的脱脂乳放入-80 ℃冰箱6 h,快速转移到冷冻干燥机进行冻干24~48 h。使用前将冻干菌粉重悬于PBS缓冲液,调整浓度为7.5×109 CFU/mL,每只灌胃0.2 mL,即1.5×109 CFU/(只·d)。
DY6FSBM制备:将风干的豆粕、DY6种子液(质量分数为3%~5%)、蛋白酶(>1 800 U/g)、水(质量分数为50%)、糖蜜(质量分数为3%)和酵母粉(质量分数为3%),混合均匀后置于无菌自封袋中,置于37 ℃培养箱中厌氧发酵48 h后55 ℃进行烘干[13]。将普通基础饲料中的普通豆粕替换为DY6 FSBM(此后称为DY6饲料),订制于江苏省协同医药生物工程有限责任公司。
动物实验造模所需DSS水:称取3 g DSS粉末充分溶解于100 mL小鼠饮用水中配制成30 g/L的DSS水,DSS溶液新鲜配制、隔天更换。美沙拉嗪(mesalazine,MSLZ)药剂:按照实验动物与人体表面积比等效剂量换算比率,小鼠美沙拉嗪给药剂量为 10.4 mg/(只·d)。
1.2 实验方法
选用BALB/c雄性小鼠46只,适应性喂养1周后开始试验,实验流程如图1所示。将小鼠随机分组,空白组(8只)、模型组(30只)和DY6饲料预防组(8只),第1天开始给DY6饲料预防组饲喂DY6饲料直至实验结束。造模结束后(第9天),每组随机取3只小鼠进行取血和解剖,随后选取20只造模型组造模效果较好的模型组小鼠随机分为4组:模型组, DY6饲料治疗组,DY6治疗组和MSLZ治疗组,每组5只进行后续治疗期实验(10~16 d)。具体分组和饲养方案见表1和表2。第16天对各组剩余全部小鼠进行取血和解剖取材。
表1 造模期小鼠分组及饲养方案
Table 1 Mice grouping and feeding program
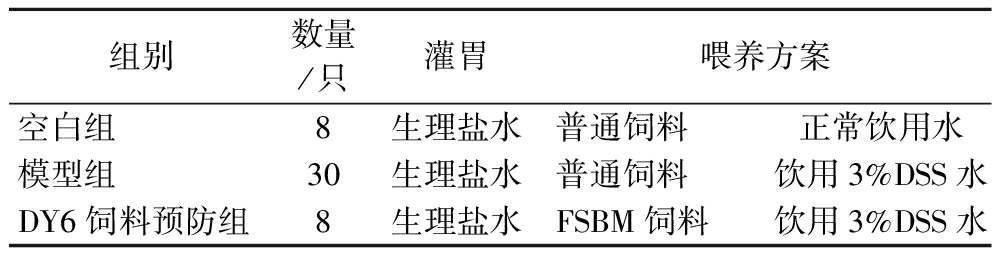
组别数量/只灌胃喂养方案空白组8生理盐水普通饲料正常饮用水模型组30生理盐水普通饲料饮用3%DSS水DY6饲料预防组8生理盐水FSBM饲料饮用3%DSS水
表2 治疗期小鼠分组及饲养方案
Table 2 Mice grouping and feeding program

组别只数灌胃方案喂养方案空白组5生理盐水普通饲料正常饮用水模型组5生理盐水普通饲料正常饮用水DY6饲料预防组5生理盐水FSBM饲料正常饮用水DY6饲料治疗组5生理盐水FSBM饲料正常饮用水DY6治疗组5DY6菌悬液普通饲料正常饮用水MSLZ治疗组5MSLZ普通饲料正常饮用水
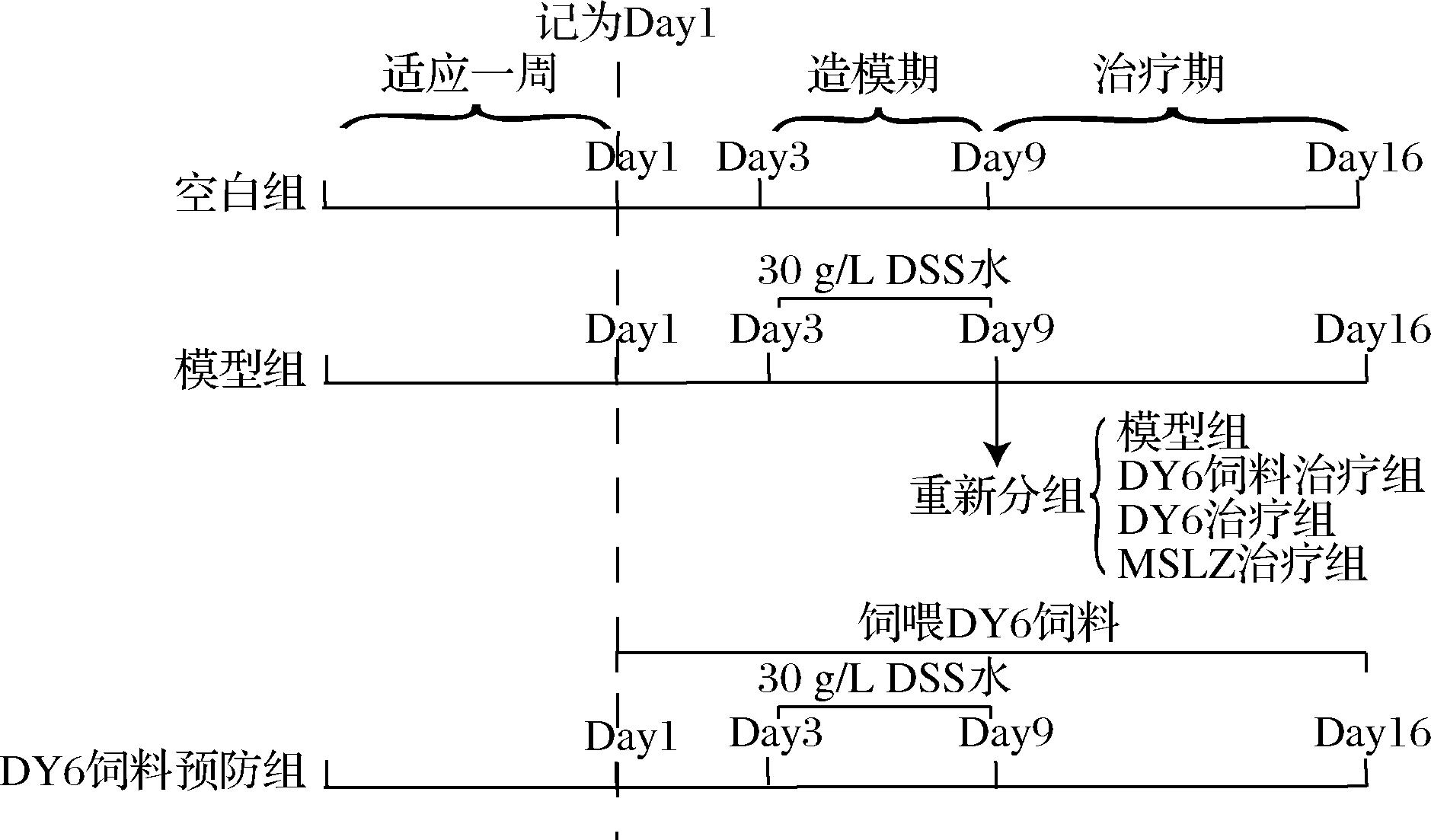
图1 实验流程图
Fig.1 Experimental protocols
1.2.1 取材
实验期间每天测量小鼠体重、收集并观察粪便,计算小鼠疾病活动指数(disease activity index, DAI)评分,评分准则如表3所示。于第9天每组随机选取3只、第16天每组剩余小鼠进行摘眼球取血,脱颈处死小鼠后解剖,取脏器和肠道进行观察称重对比,取结肠内容物按1∶9(g∶mL)加入灭菌生理盐水,将剩余结肠组织放入-80 ℃冰箱保存。
表3 疾病活动指数评分标准
Table 3 Mice grouping and feeding program

分数体重下降百分率/%粪便性状粪便隐血情况00正常阴性(-)11~526~10稀便阳性(+)311~154>15水样便强阳性(+++)
1.2.2 小鼠肠道组织学观察
解剖后将小鼠结肠组织迅速取出,取距离结肠末端1 cm位置的肠段约1 cm,放入固定液(4%多聚甲醛)中固定,送塞维尔生物科技有限公司进行后续包埋和苏木精-伊红(hematoxylin-eosin,H&E)染色。
1.2.3 小鼠血清中IL-6测定
最后一次给药24 h后,每只小鼠进行摘眼球取血500~600 μL,室温静置2 h, 4 ℃,5 000 r/min离心15 min,取上清液置于-80 ℃保存。按照试剂盒方法进行测定。
1.2.4 小鼠肠组织中TNF-α含量的测定
将冻存在-80 ℃的结肠组织取出,剪一段进行称重,按0.1∶2(g∶mL)的比例加入PBS缓冲液,充分研磨使其呈匀浆状,按照试剂盒方法进行实验。
1.2.5 小鼠结肠组织通透性的测定
取适量小鼠结肠组织样本加入Trizol中,使用匀浆机匀浆,参照康为试剂盒进行RNA的提取、逆转录合成cDNA和荧光定量PCR,严格按照说明书进行实验,引物序列详见表4。利用totallab V2.01软件对RT-PCR结果进行检测,计算不同样本中闭合蛋白(occludin)目的基因的相对含量,并进行比较。
表4 引物序列
Table 4 Primer sequences

引物引物序列(5′-3′)occludin正向:CACACTTGCTTGGGACAGAG反向:TAGCCATAGCCTCCATAGCCβ-action正向:GGGAAATCGTGCGTGACATTA反向:TTGCCGATAGTGATGACCTGA
1.2.6 数据统计学处理
数据表示为“平均值±标准差”,采用软件 SPSS 27 进行显著性差异分析,采用单因素方差分析(ANOVA),采用Prism软件绘制图形。
2 结果与分析
2.1 发酵饲料对小鼠饮食量的影响
各组小鼠饮食情况如图2所示,空白组小鼠在整个实验期间日均进食量保持在4~6 g之间。1~2 d,DY6饲料预防组小鼠在未经任何干预时日均进食量比空白组高了0.70 g,造模期间(3~9 d),模型组小鼠饮食量明显下降,DY6饲料预防组的饮食量比模型组约高28%;治疗期间(图2-b)DY6饲料相关组小鼠进食量比其他实验组高。说明相较于普通饲料,小鼠更愿意摄入DY6饲料,这可能是由于DY6FSBM中富含有机酸如乳酸和柠檬酸等,使饲料具有酸香味,提高了适口性,进而提升动物食欲。
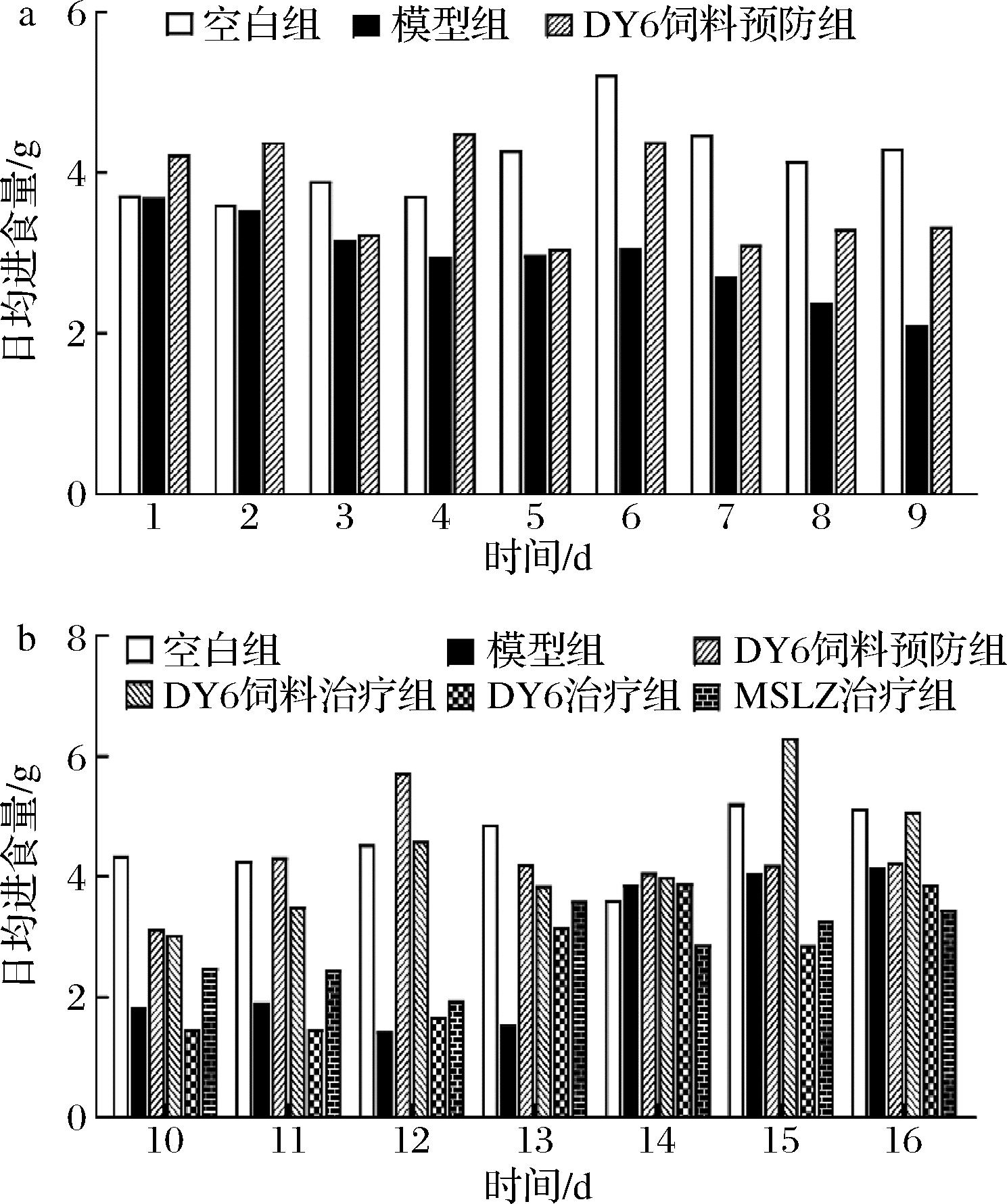
a-1~9 d各组小鼠饮食量; b-10~16 d各组小鼠饮食量
图2 实验期间各组小鼠饮食量
Fig.2 Dietary intake of each group of mice during the experiment
2.2 发酵饲料对小鼠存活率的影响
小鼠存活率能够较直观反映小鼠结肠炎的严重程度和防治效果(图3)。造模期间无小鼠死亡,各实验组小鼠在造模结束后临床症状并未立即好转,小鼠出现发抖、蜷缩和体重严重下降等情况后死亡。各组小鼠存活情况如下:空白组、DY6饲料预防组、DY6治疗组各存活5只(在治疗期未有小鼠死亡),DY6饲料治疗组存活4只,模型组、MSLZ治疗组存活3只。表明 DY6饲料和菌液都能够提高结肠炎小鼠存活率,且防治效果优于MSLZ治疗组,存活率与饲喂DY6饲料时间长短有关。吴思琪[14]的研究也表明,DSS诱导溃疡性结肠炎模型会导致大鼠出现死亡,而植物乳杆菌灌胃可以提高大鼠的存活率。
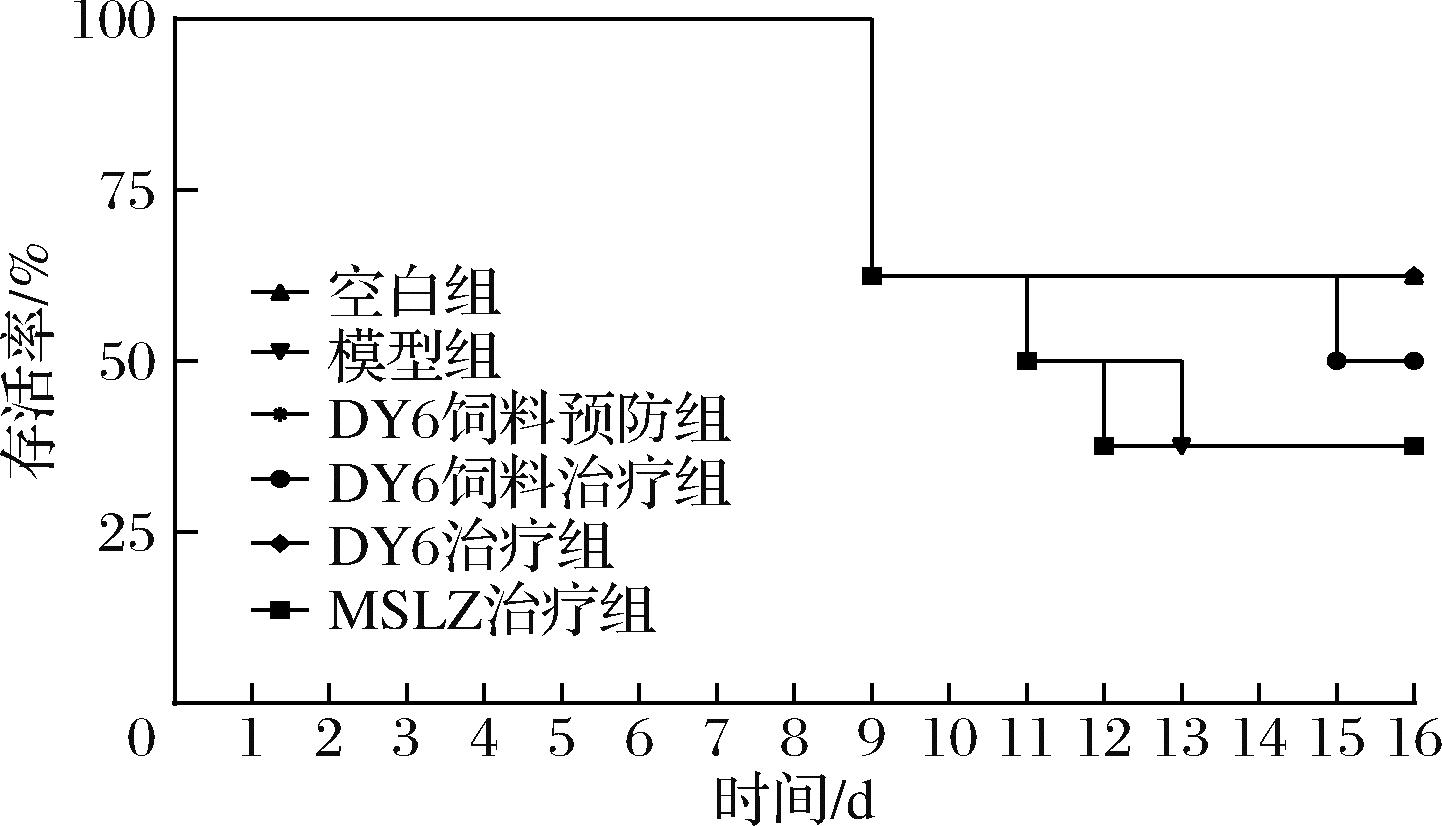
图3 各组小鼠存活率
Fig.3 Survival rate of mice in each group
DY6饲料对提高小鼠进食量和降低死亡率有明显作用,其原因可能是发酵饲料比普通饲料营养价值高,DY6FSBM中富含有机酸和小肽等物质[13],一方面因适口性提升使得动物采食量增加,另一方面小肽更容易被肠道吸收,减少了消化负担[6],此外饲料中大量的乳酸可直接参与机体新陈代谢,是三羧酸循环的燃料,同时还有抑菌作用,能够维持肠道菌群平衡,降低腹泻,促进钙磷的吸收[15],另外苹果酸能够促进氨基酸的吸收[16],使得小鼠更快恢复健康。
2.3 FSBM对小鼠体重变化和DAI评分的影响
小鼠体重变化情况如图4-a所示,空白组小鼠体重增长稳定。造模期模型组和预防组小鼠体重下降明显,直到第16天模型组小鼠体重仍没有明显恢复,这可能是由于结肠炎导致小鼠食欲不振;随治疗的进行各治疗组小鼠体重都有明显提高,而MSLZ治疗组小鼠体重恢复效果欠佳,仅高于模型组;DY6饲料预防组小鼠体重增长率在整个试验期间都高于其他实验组。表明提前摄入DY6饲料能够预防和缓解结肠炎引起的体重下降,结肠炎发生后摄入DY6饲料也能产生较好的治疗效果,而且与单独使用DY6效果相当,都明显优于MSLZ治疗效果。
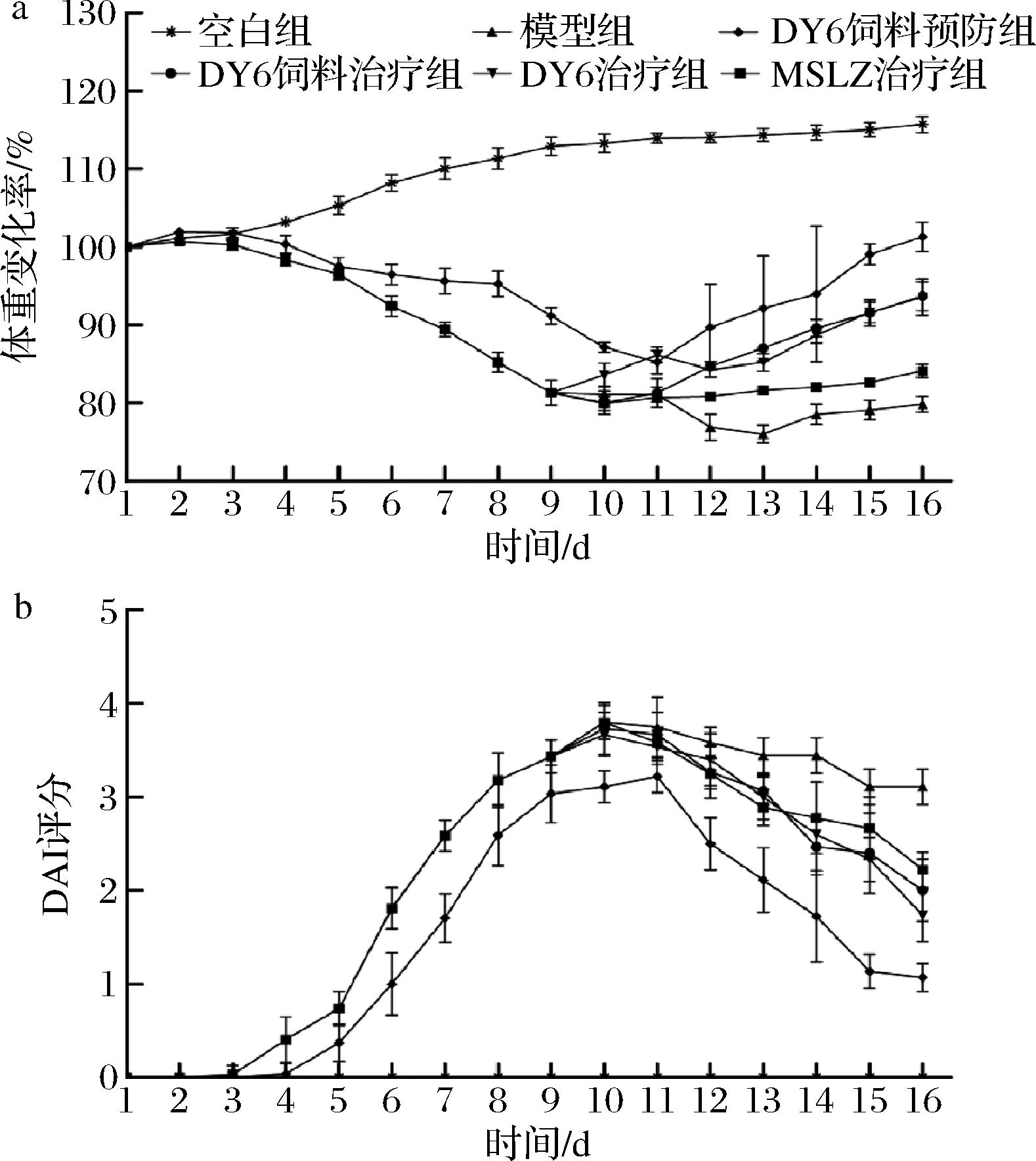
a-小鼠体重变化率;b-DAI评分
图4 实验期间小鼠一般状态记录
Fig.4 Records of the general state of the mice during the experiment
小鼠DAI是一种评估结肠炎疾病情况的基础指标,分值越高,结肠炎越严重。由图4-b所示,空白组小鼠DAI评分稳定在0~0.03分;第4天开始,所有造模小鼠粪便出现隐血情况,且逐渐加重,直到第9天模型组小鼠全部肉眼便血,此时DAI评分达到3.43分;治疗期各组DAI评分下降,而直到第16天模型组评分仍高达3.11分,DY6饲料治疗组和DY6治疗组降低为2.00分和1.73分,MSLZ治疗组评分仍较高为2.22分。DY6饲料预防组DAI评分始终低于其他组,在第9天评分仅为3.03,第16天已降低为1.06分,说明长期饲喂DY6饲料对结肠炎有明显的预防作用。这一结果好于先前的一些研究[17],副干酪乳酪杆菌R3在降低DAI值方面与MSLZ差异不明显,这表明DY6饲料和DY6具有良好的缓解结肠炎的益生特性且优于之前的一些菌株。
2.4 小鼠肠道组织观察
通过观察小鼠结肠H&E染色切片可以评估小鼠结肠病理损伤情况。由图5所示,空白组小鼠结肠黏膜结构完整,腺体排列整齐,黏膜正常,无炎性细胞浸润;第9天,模型组小鼠的结肠受损严重,肌层组织水肿,腺体排列紊乱,隐窝结构被完全破坏,黏膜坏死,大量炎性细胞浸润,DY6饲料预防组小鼠结肠组织也出现损伤情况,但好于模型组;第16天模型组仍有大量炎细胞浸润,且黏膜层受损,而DY6饲料预防组、DY6治疗组和MSLZ治疗组均有明显改善,但仍有少量炎细胞浸润。
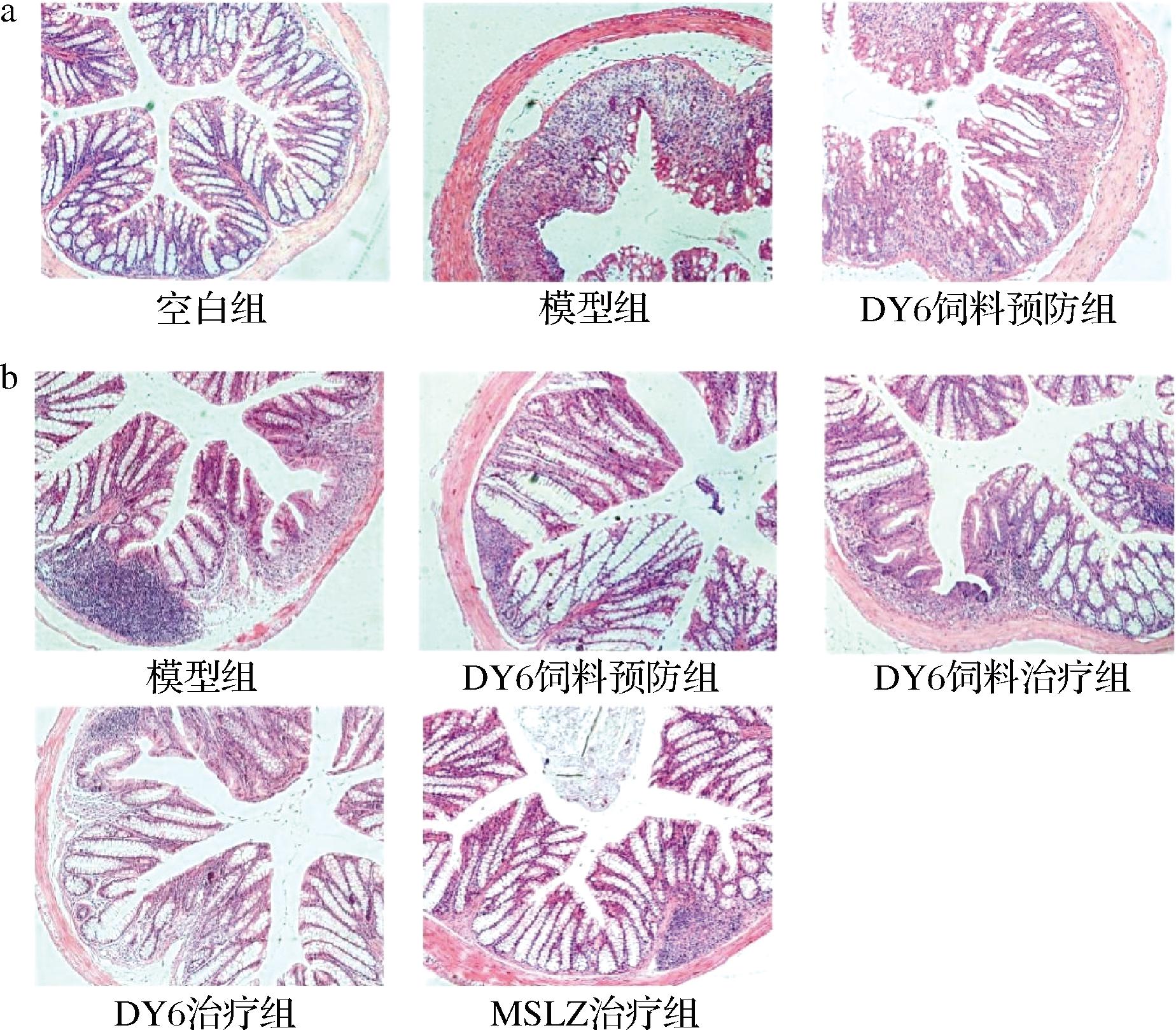
a-造模结束;b-治疗结束
图5 造模结束和治疗结束各组小鼠结肠组织H&E切片
Fig.5 H&E sections of colonic tissues of mice in each group at the end of modeling and at the end of treatment
肠黏膜每3 d进行一次自我更新,主要能量物质是以谷氨酸、谷氨酰胺为代表的氨基酸,或是以丁酸为代表的短链脂肪酸为主[18]。DY6饲料中的大量小肽进入肠道后被分解为游离氨基酸,一部分转运到肠外,一部分被肠道截留合成肠黏膜蛋白质和多肽等含氮物质[19];另外,其含有的丁酸是结肠的首要能源物质[18],能够提供肠黏膜上皮细胞所需的能量,保护黏膜和隐窝,维持肠上皮的完整性,这与向大育[20]饲喂断奶仔猪的研究一致。由此可见,在饲料中添加含有丰富小肽、氨基酸和有机酸的DY6FSBM对维持肠黏膜形态保护肠道健康具有重要的作用。
2.5 小鼠体内炎症因子水平
促炎性细胞因子的异常表达会引起肠道炎症及组织损伤,本研究检测了最具代表性的促炎因子IL-6和TNF-α[21]。
IL-6 主要通过 STAT3 信号通路发挥重要作用[22]。通过ELISA试剂盒检测血清中炎症因子IL-6的含量,如图6-a所示,第9天模型组和DY6饲料预防组小鼠血清中IL-6水平明显高于空白组(P<0.001),说明结肠炎的发病与IL-6含量上升有关。第16天,模型组小鼠IL-6水平虽有所降低但仍显著高于空白组(P<0.05),其余各组较模型组显著下降(P<0.05),DY6饲料相关组与其他治疗组IL-6水平相当,与空白组相比无显著差异,表明DY6饲料能够有效抑制STAT3 信号通路降低小鼠体内的IL-6水平。
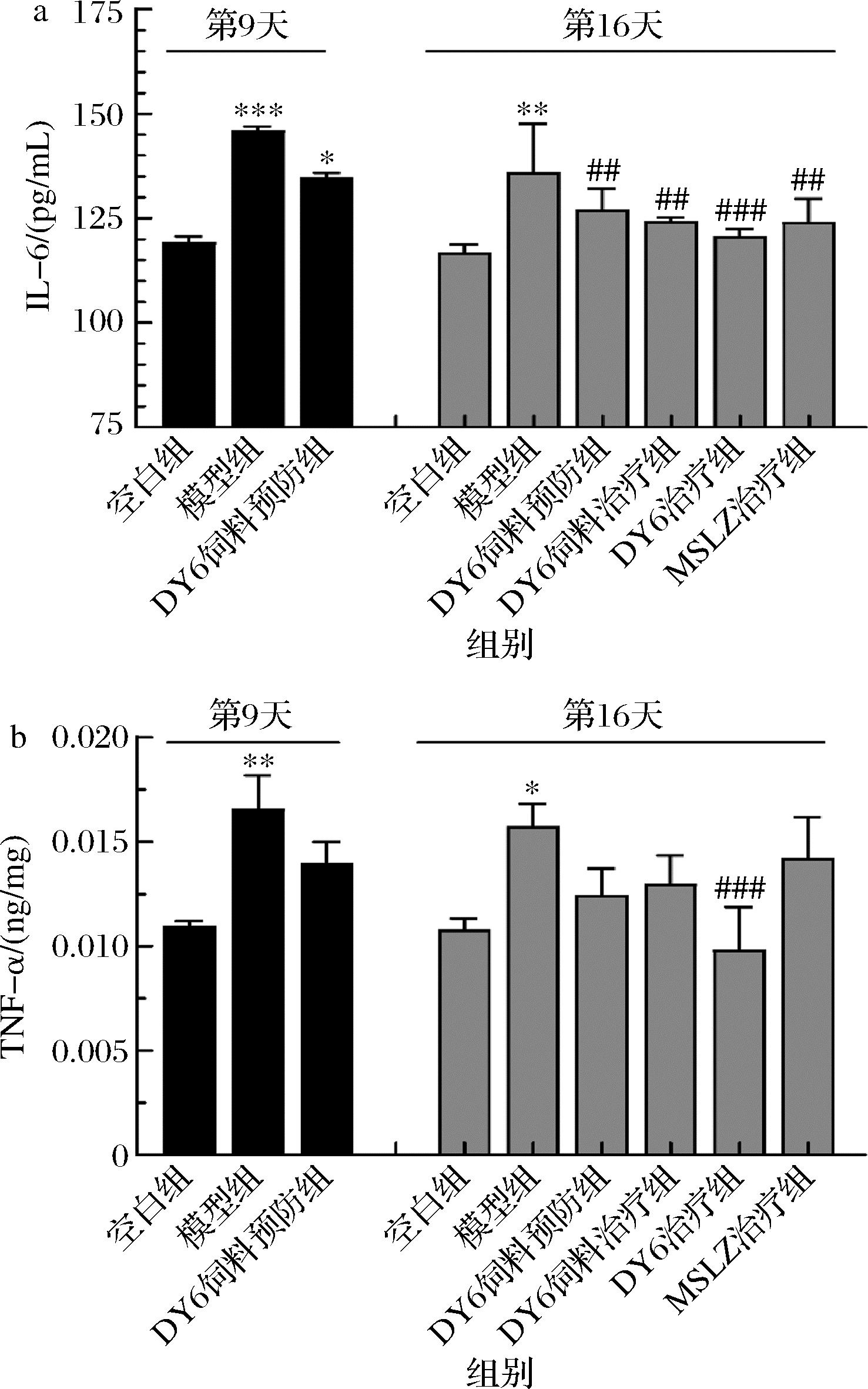
a-IL-6含量;b-TNF-α含量
图6 各组小鼠体内炎症因子变化情况
Fig.6 Changes in inflammatory factors in mice in each group
注:与空白组相比,*表示P<0.05,**表示P<0.01, ***表示P<0.001;与第9天模型组相比,#表示P<0.05, ##表示P<0.01,###表示P<0.001(下同)。
当发生结肠炎时,机体的免疫细胞通过TLR4/NF-КB等信号通路激活[23],释放促炎因子TNF-α。通过ELISA试剂盒检测小鼠肠道组织中炎症因子TNF-α的含量,结果如图6-b所示,第9天模型组小鼠结肠组织中TNF-α含量显著提升(P<0.01),DY6饲料预防组虽提高但低于模型组且与空白组无显著差异(P>0.05)。第16天,模型组小鼠TNF-α含量仍显著高于空白组正常水平(P<0.05),DY6饲料相关组和DY6治疗组有所降低,且低于阳性对照MSLZ组中的TNF-α水平,这一结果好于侯保秋等[24]得出的低中高剂量的副高酪乳杆菌对降低DSS引起的溃疡性结肠炎小鼠体内TNF-α与MSLZ相当,甚至较差于MSLZ的研究结果,说明DY6饲料在缓解结肠炎引起的TNF-α上升效果好于之前研究中的一些菌株。
推测DY6FSBM的作用与调节 DSS 诱导结肠炎中炎症因子水平有关, DY6FSBM中含有的有机酸、氨基酸和肽能够调节细胞信号和炎性基因表达,达到抗炎作用[25-26]。在以往的一些研究中也发现,益生功能的乳酸菌与发酵物具有抗氧化、抗炎症等功效,并证实对结肠炎有一定的改善作用[27]。
2.6 小鼠结肠组织的通透性
肠道通透性的增加是结肠炎发生的重要标志,其屏障功能由肠上皮紧密连接蛋白(tight junctions,TJs)调节,在调节细胞膜通透性和维持上皮完整性方面发挥关键作用,occludin蛋白是TJs的结构基础和重要功能元件[28]。
通过qRT-PCR测小鼠紧密连接蛋白的表达量,如图7所示,第9天模型组和预防组occludin的表达显著降低(P<0.001)。第16天模型组occludin表达水平仍显著低于空白组(P<0.001),其余组occludin表达得到著提高(P<0.01),DY6饲料预防组高于DY6饲料治疗组和MSLZ治疗组。这表明DY6饲料对肠道完整性起到有效的保护作用,长期饲喂DY6饲料能够更好地缓解小鼠结肠中紧密连接蛋白表达量降低的情况。这可能是由于DY6FSBM中含有大量的有机酸、游离氨基酸和小肽,其中丁酸可为结肠提供能量来源,氨基酸可作为合成含氮物质的底物,乙酸能促进肠黏膜紧密连接蛋白等相关蛋白的表达,降低肠道通透性[15, 19]。结合DY6耐酸耐胆盐能力强等特点,其在提升occludin表达水平方面表现更好,可能是由于其进入肠道并定植,分泌的有机酸等代谢产物多于DY6饲料中的含量。综上,DY6FSBM能够改善肠道黏膜损伤,通过维持小鼠肠道机械屏障的完整性预防和治疗结肠炎,这可能是该菌发酵饲料治疗结肠炎的重要作用机制之一。
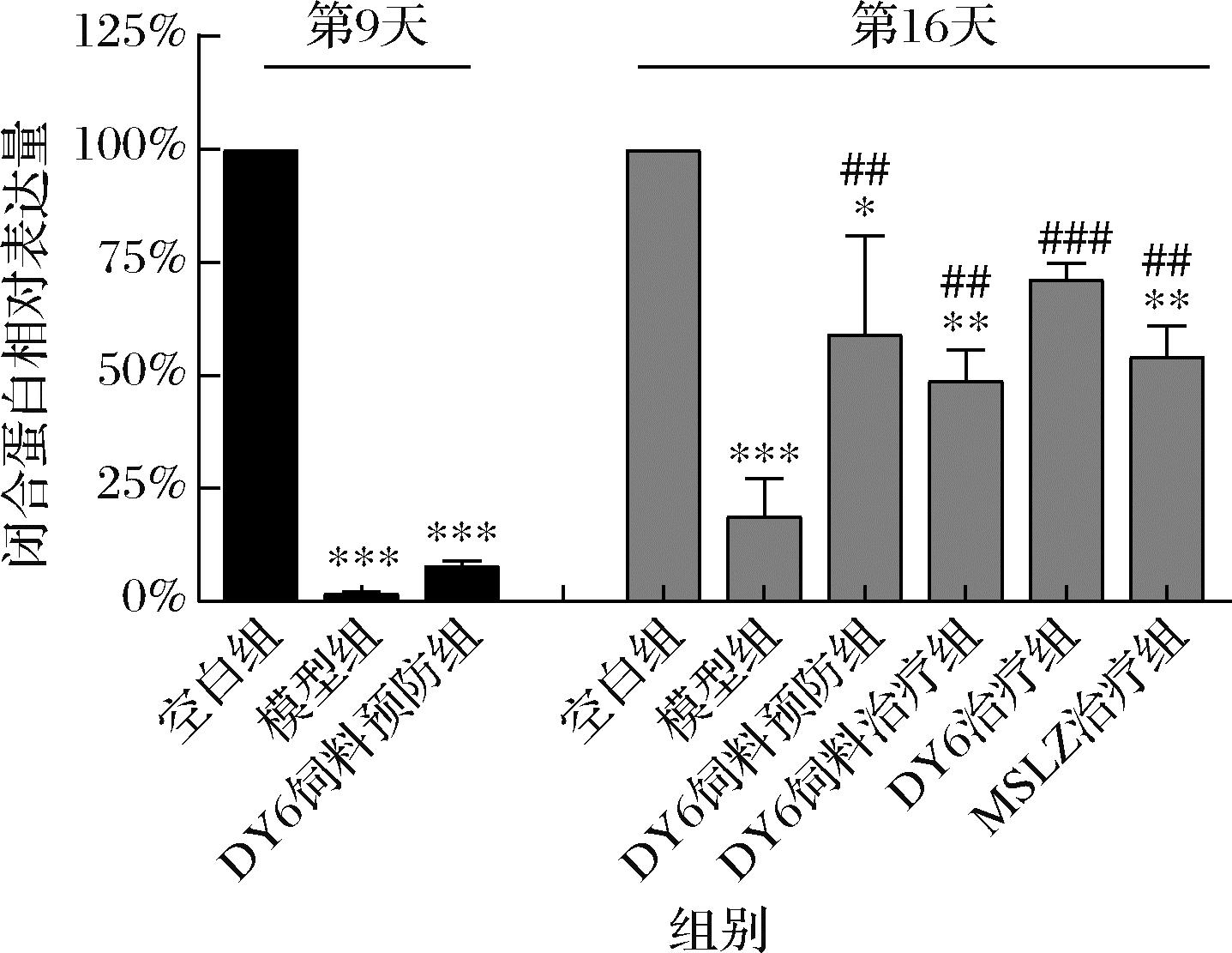
图7 小鼠结肠组织中occludin蛋白表达量
Fig.7 Occludin protein expression in mouse colon tissue
3 结论
肠道炎症病因复杂,极易反复,引起动物肠黏膜受损和肠道屏障功能破坏,严重影响动物健康及养殖业的经济效益。随着禁抗、限抗政策法规颁布,开发出天然、绿色无公害的肠道炎症防控药物或添加剂迫在眉睫。本研究表明,由于DY6FSBM中有机酸、游离氨基酸和小肽等营养物质含量高,在饲料中添加DY6FSBM明显缓解了DSS诱导的结肠炎小鼠症状,且在有些方面防治效果好于美沙拉嗪药物治疗,该饲料适口性得到改善,动物食欲增加,显著降低小鼠DAI评分和结肠组织病变情况,能够通过抑制STAT3和TLR4/NF-КB信号通路减轻体内炎症反应,使小鼠体内的促炎因子IL-6和TNF-α的含量降低,进一步研究发现DY6FSBM还能够显著提高小鼠肠道组织中重要的紧密连接蛋白的表达量,有助于保护肠道黏膜完整性,降低肠道黏膜通透性。DY6饲料预防比DY6饲料治疗效果好,表明长期饲喂DY6饲料更能发挥其抑菌、抗炎、修复黏膜功能。DY6饲料干预与DY6菌液干预效果相当,表明DY6饲料可以代替DY6制剂添加到饲料中。综上,本研究拓宽了植物乳杆菌DY6的应用形式,为DY6FSBM提供新的应用方向,为养殖业中防治炎性肠病提供理论依据,有望研发能够有效防治炎症性疾病的“替抗”饲料产品。
[1] 吴莲云. 壳寡糖对动物实验性炎性肠病防治作用的研究[D].湛江:广东海洋大学, 2020.WU L Y.Study on the prevention and treatment of chitooligosaccharide on animal experimental inflammatory bowel disease[D].Zhanjiang:GuangDong Ocean University, 2020.
[2] SUN M Y, LIU Y J, SONG Y L, et al.The ameliorative effect of Lactobacillus plantarum-12 on DSS-induced murine colitis[J].Food &Function, 2020, 11(6):5205-5222.
[3] YU P, KE C X, GUO J X, et al.Lactobacillus plantarum L15 alleviates colitis by inhibiting LPS-mediated NF-κB activation and ameliorates DSS-induced gut microbiota dysbiosis[J].Frontiers in Immunology, 2020, 11:575173.
[4] LI X Q, ZHU Y H, ZHANG H F, et al.Risks associated with high-dose Lactobacillus rhamnosus in an Escherichia coli model of piglet diarrhoea:Intestinal microbiota and immune imbalances[J].PLoS One, 2012, 7(7):e40666.
[5] 王文文. 发酵豆粕对断奶仔猪肠道屏障的保护作用及机理研究[D].呼和浩特:内蒙古农业大学, 2023.WANG W W.Protective effect and mechanism of fermented soybean meal on gut barrier in weaned piglets[D].Hohhot:Inner MongoliaAgricultural University, 2023.
[6] 余俊达. 一株短小芽孢杆菌用于豆粕固态发酵及防治细菌性腹泻的初步研究[D].长沙:湖南农业大学, 2020.YU J D.Preliminary study on a strain of Bacillus pumilus used for solid fermentation of soybean meal and prevention of bacterial diarrhea[D].Changsha:Hunan Agricultural University, 2020.
[7] 陶红艳, 徐欣维, 汪明金, 等.乳酸菌益生特性及其应用的研究进展[J].安徽农学通报, 2021, 27(21):45-48.TAO H Y, XU X W, WANG M J, et al.Research progress on probiotic characteristics and application of lactic acid bacteria[J].Anhui Agricultural Science Bulletin, 2021, 27(21):45-48.
[8] ZHU J J, GAO M X, ZHANG R L, et al.Effects of soybean meal fermented by L.plantarum, B.subtilis and S.cerevisieae on growth, immune function and intestinal morphology in weaned piglets[J].Microbial Cell Factories, 2017, 16(1):191.
[9] 鲁春灵, 李军国, 蒋万春, 等.湿态发酵豆粕对肉鸡生长性能、抗氧化能力和肠道健康的影响[J].动物营养学报, 2021, 33(7):4162-4174.LU C L, LI J G, JIANG W C, et al.Effects of wet fermented soybean meal on growth performance, antioxidant capability and intestine healthy of broilers[J].Chinese Journal of Animal Nutrition, 2021, 33(7):4162-4174
[10] CATAL N N, VILLASANTE A, WACYK J, et al.Fermented soybean meal increases lactic acid bacteria in gut microbiota of atlantic salmon (Salmo salar)[J].Probiotics and Antimicrobial Proteins, 2018, 10(3):566-576.
N N, VILLASANTE A, WACYK J, et al.Fermented soybean meal increases lactic acid bacteria in gut microbiota of atlantic salmon (Salmo salar)[J].Probiotics and Antimicrobial Proteins, 2018, 10(3):566-576.
[11] 刘颖颖, 卢艳波, 杨小雁, 等.植物乳杆菌DY6的生理特性及代谢机制分析[J].食品与发酵工业, 2022, 48(18):11-19.LIU Y Y, LU Y B, YANG X Y, et al.Physiological characteristics of Lactobacillus plantarum DY6 and its metabolic mechanisms analysis[J].Food and Fermentation Industries, 2022, 48(18):11-19.
[12] 陆春波, 毛银, 李国辉, 等.植物乳杆菌DY6主要抑菌代谢物的分析和鉴定[J].微生物学通报, 2019, 46(9):2258-2271.LU C B, MAO Y, LI G H, et al.Analysis and identification of main antibacterial metabolites secreted by Lactobacillus plantarum DY6[J].Microbiology China, 2019, 46(9):2258-2271.
[13] 毛银, 陆春波, 李国辉, 等.菌酶协同发酵豆粕工艺的优化[J].食品与发酵工业, 2019, 45(14):108-114.MAO Y, LU C B, LI G H, et al.Optimized fermentation process of soybean meal by bacteria with enzymes[J].Food and Fermentation Industries, 2019, 45(14):108-114.
[14] 吴思琪. 植物乳杆菌Zhang-LL对DSS诱导大鼠慢性溃疡性结肠炎预防效果评价[D].北京:北京农学院, 2018.WU S Q.Effect on DSS-induced chronic ulcerative colitis in rats of Lactobacillus Plantarum Zhang-LL[D].Beijing:Beijing University of Agriculture, 2018.
[15] 侯楠楠, 王梅, 王倩, 等.乳酸菌固态发酵豆粕产酸性能分析[J].中国酿造, 2022, 41(9):124-129.HOU N N, WANG M, WANG Q, et al.Acid production from soybean meal by solid-state fermentation with lactic acid bacteria[J].China Brewing, 2022, 41(9):124-129.
[16] 梁静, 张文举, 王博.L-苹果酸的生理功能及其在反刍动物生产应用中的研究进展[J].中国畜牧兽医, 2016, 43(7):1916-1921.LIANG J, ZHANG W J, WANG B.Research progress on the physiological function of L-malic acid and its application in ruminant production[J].China Animal Husbandry &Veterinary Medicine, 2016, 43(7):1916-1921.
[17] 杨紫嫣. 副干酪乳杆菌对DSS诱导小鼠结肠炎免疫调节作用的研究[D].湛江:广东医科大学, 2020.YANG Z Y.Immunomodulatory effect of Lactobacillus paracasei on DSS-induced colitis in mice[D].Zhanjiang:Guangdong Medical University, 2020.
[18] 薛永强, 张辉华, 王达, 等.短链脂肪酸对肠道健康的调控机制及在动物生产中的应用[J].饲料工业, 2020, 41(19):18-22.XUE Y Q, ZHANG H H, WANG D, et al.Regulation mechanism of short-chain fatty acids on intestinal health and their application in animal production[J].Feed Industry, 2020, 41(19):18-22.
[19] CHEN M D, LIU Y Y, XIONG S B, et al.Dietary L-tryptophan alleviated LPS-induced intestinal barrier injury by regulating tight junctions in a Caco-2 cell monolayer model[J].Food &Function, 2019, 10(5):2390-2398.
[20] 向大育. 发酵豆粕对断奶仔猪肠道形态及消化酶活性的影响[J].中国饲料, 2019(17):48-50;54.XIANG D Y.Effect of fermented soybean meal on intestinal morphology and digestive enzyme activity of weaned piglets[J].China Feed, 2019(17):48-50;54.
[21] XU C H, LIU J H, GAO J W, et al.Combined soluble fiber-mediated intestinal microbiota improve insulin sensitivity of obese mice[J].Nutrients, 2020, 12(2):351.
[22] LI Y, DE HAAR C, CHEN M, et al.Disease-related expression of the IL6/STAT3/SOCS3 signalling pathway in ulcerative colitis and ulcerative colitis-related carcinogenesis[J].GUT, 2010, 59(2):227-235.
[23] XIA Y J, CHEN Y, WANG G Q, et al. Lactobacillus plantarum AR113 alleviates DSS-induced colitis by regulating the TLR4/MyD88/NF-κB pathway and gut microbiota composition[J].Journal of Functional Foods, 2020, 67:103854.
[24] 侯保秋, 董怡文, 刘方.一株分离自牦牛乳中的副干酪乳杆菌ZZ102对溃疡性结肠炎的缓解作用研究[J].中国乳品工业, 2023, 51(10):21-25.HOU B Q, DONG Y W, LIU F.Alleviative effect on ulcerative colitis of Lactobacillus paracasei ZZ102 isolated from yak milk[J].China Dairy Industry, 2023, 51(10):21-25.
[25] RAVINDRAN R, LOEBBERMANN J, NAKAYA H I, et al.The amino acid sensor GCN2 controls gut inflammation by inhibiting inflammasome activation[J].Nature, 2016, 531(7595):523-527.
[26] LAN J, DOU X J, LI J W, et al.L-Arginine ameliorates lipopolysaccharide-induced intestinal inflammation through Inhibiting the TLR4/NF-κB and MAPK pathways and stimulating β-defensin expression in vivo and in vitro[J].Journal of Agricultural and Food Chemistry, 2020, 68(9):2648-2663.
[27] 左云洋, 胡萍, 许浩翔, 等.副干酪乳杆菌SR10-1发酵刺梨汁对葡聚糖硫酸钠诱导小鼠溃疡性结肠炎的缓解作用[J].食品科学, 2023, 44(15):121-128.ZUO Y Y, HU P, XU H X, et al.Relieving effect of Rosa roxburghii tratt.Juice fermented by Lactobacillus paracasei SR10-1 on dextran sulfate sodium-Induced ulcerative colitis in mice[J].Food Science, 2023, 44(15):121-128.
[28] SRIVASTAVA A K, VENKATA B S, SWEAT Y Y, et al.Serine 408 phosphorylation is a molecular switch that regulates structure and function of the occludin a-helical bundle[J].Proceedings of the National Academy of Sciences of the United States of America, 2022, 119(34):e2204618119.