随着经济水平提高,奶茶、蛋糕为代表的高脂高糖食物,在我国居民饮食结构中出现越加频繁。高脂高糖饮食不仅加重肝脏糖脂代谢负担,还会对肠道健康产生诸多不利因素[1-2]。肠道菌群是机体重要的微生态系统,按功能分为益生菌或致病菌,正常机体内肠道菌群形成的天然屏障可以抵御病菌[3]。肠道菌群失调(表现为:有害菌丰度>有益菌丰度)[4]会引起机体代谢紊乱,对摄入的物质出现病理性的消化与吸收。研究表明高脂高糖的饮食会损伤肠道屏障功能,并造成以肥胖为主要特征的代谢综合征,而机体肥胖会导致肠道菌群失调[5]。
叶绿素是一种广泛存在于食用植物中的脂溶性色素,由一个卟啉环(镁原子居于卟啉环中间)和一条植醇的链组成,高等植物的叶绿素主要是叶绿素a和叶绿素b。研究表明植物中的叶绿素,经过复杂代谢形成的叶绿素衍生物到达肠道后,可以通过调节肠道菌群缓解肥胖[6]。叶绿素还能促进肠道菌群产生短链脂肪酸进而参与调控机体代谢水平,而短链脂肪酸还能对机体的免疫、大脑活动产生有益影响[7]。不仅如此,LI等[8]使用从菠菜提取的叶绿素混合物(主要是叶绿素a和叶绿素b)喂养高脂饲料饲育的C57BL/6 J小鼠后发现,叶绿素能够影响肠道菌群结构并降低炎症因子水平来减缓肥胖。SEMAAN等[9]发现,植物中叶绿素可以通过影响细胞脂质摄取来缓解肥胖。然而目前对叶绿素改善肠道菌群的研究,采用的多是叶绿素粗提物,里面除了有不同种类的叶绿素还含有一些类胡萝卜素、多酚、类黄酮等。此外,LI等[10]通过体外消化系统模拟叶绿素消化发现,叶绿素在肠道中存在的形式主要是以脱镁叶绿素及其衍生物存在。CHEN等[11]使用体外消化进一步发现,脱镁叶绿素消化后的终产物是以132-羟基-脱镁叶绿素,151-羟基-内酯脱镁叶绿素及脱镁叶绿酸(脱镁叶绿素失去植醇链后的产物)存在,并且叶绿素a比叶绿素b更容易在消化中发生脱镁化。然而,脱镁叶绿素对高脂饮食诱导的肠道菌群结构及代谢调节作用目前尚未完全阐明,相关作用还需要深入探究。
为进一步探究脱镁叶绿素对高脂饮食诱导的肠道菌群调节作用,本研究我们以高脂饮食诱导的小鼠粪便为材料,添加纯化后脱镁叶绿素a和脱镁叶绿酸a进行体外发酵。使用16S rRNA微生物组学技术和超高效液相色谱/四极杆飞行时间质谱,研究脱镁叶绿素对于高脂饮食诱导的肠道菌群结构及菌群代谢产物的影响,更进一步揭示叶绿素对高脂饮食诱导的肠道菌群调节作用。
1 材料与方法
1.1 材料与试剂
紫菜(干坛紫菜,产地福建霞浦),重庆市北碚区永辉超市;盐酸、二甲基亚砜、丙酮、石油醚(30~60 ℃)、石油醚(60~90 ℃)、乙醇、甲醇、NaCl、吡啶、2-甲基苯肼盐酸盐(2-methylphenylhydrazine hydrochloride,NPH-HCl)、1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐(1-ethyl-3-(3-dimethylaminopropyl)carbodiimide hydrochloride,EDC-HCl)、KH2PO4、K2HPO4、MgSO4、CaCl2、HCl、NaOH,川东化工公司;Na2SO4、NaH2PO4、Na2HPO4,科龙化工公司,以上试剂均为分析纯;乙酸铵、丙酮、甲醇均为色谱纯,Sigma-Aldrich贸易有限公司;所需标准品:乙酸(99.8%)、丙酸(99.8%)、丁酸(99.5%)、戊酸(99.8%),坛墨质检科技股份有限公司;培养基成分:蛋白胨水,酵母提取物、碳酸氢钠、L-半胱氨酸-盐酸、胆盐、吐温80(Tween-80)、维生素K、氯化血红素、刃天青,源叶生物科技有限公司;PBS,Bio-sharp公司。
1.2 仪器与设备
Agilent 1290超高效液相色谱仪,美国Agilent公司;Impact II四极杆飞行时间质谱仪(Bruker Compass DataAnalysis 5.1数据处理软件),德国Bruker公司;Vortex-2涡旋混匀仪,上海沪析实业有限公司;RE-52AA旋转蒸发器,上海亚荣生化仪器厂;DW-HL398超低温冷冻储存箱,中科美菱低温科技股份有限公司;UV-5200紫外可见光分光光度计,上海元析仪器有限公司;KQ5200DE型数控超声波清洗器,昆山市超声仪器有限公司;Mini Spin高速微型离心机,德国Eppendorf公司;LAI-3DT型厌氧培养箱,上海龙跃仪器设备有限公司。
1.3 实验方法
1.3.1 提取分离脱镁叶绿素a和脱镁叶绿酸a
按照LI等[12]方法制备富含脱镁叶绿素a和脱镁叶绿酸a的紫菜提取物。称取干紫菜10 g,碾碎成粉末,加20 mL纯水浸泡紫菜0.5 h。随后加入4倍体积的丙酮,用中速滤纸进行过滤。加入0.5 mL的盐酸(0.1 mol/L)摇晃,再加入过量NaCl固体,少量NaHCO3粉末中和盐酸。随后进行分液萃取,将上清液通过无水Na2SO4过滤,35 ℃减压旋转蒸发至干。
通过采用课题组已经建立的分离方法[12],将脱镁叶绿素粗提物均匀点样在1 mm厚的滤纸板上,进行石油醚洗脱的薄层层析(石油醚∶乙醇∶甲醇=60∶20∶1)。层析后产生的棕色条带为脱镁叶绿素a,灰色条带为脱镁叶绿酸a。将层析得到的脱镁叶绿素条带裁下用丙酮溶解后,得到相应的脱镁叶绿素-丙酮溶液,放置于-20 ℃冰箱中保存至使用。
1.3.2 动物实验
20只雄性C57BL/6 J小鼠(6周龄),取10只进行高脂饮食诱导,剩余的正常喂养(动物实验伦理编号,IACUC-20221102-03)。喂养条件为:[相对湿度55%~65%;室温(25±1) ℃],在12 h黑暗/12 h光照循环条件下喂养,采用实验室标准的饮食和供水。适应性喂养1周后,诱导组换高脂饲料喂养,饲料配方(质量分数):38% 基础饲料+28% 猪油+10.8% 全脂奶粉+5.6% 蔗糖+11.5% 酪蛋白+2% 混合矿物质+1.9% 微晶纤维素+1.8%磷酸氢钙+0.4% 钙粉。两组连续喂养10周,期间小鼠可以自由进食饮水。
1.3.3 高脂饮食诱导的小鼠粪便体外发酵
本实验2个实验组和1个对照组,分别是添加脱镁叶绿素a的高脂饮食实验组、添加脱镁叶绿酸a的高脂饮食实验组、不添加脱镁叶绿素的高脂饮食空白对照组,所有组均设置6个平行。
1.3.3.1 培养基与高脂饮食诱导的肠道菌群悬液的制备
用于发酵的基础培养基按照以下配制[13]:蛋白胨水0.9 g,酵母提取物0.9 g,NaCl 0.045 g,K2HPO4 0.018 g,KH2PO4 0.018 g,MgSO4·7H2O 0.004 5 g,CaCl2·6H2O 0.004 5 g,NaHCO3 0.9 g,L-半胱氨酸-盐酸0.225 g,胆盐0.225 g,Tween-80 0.9 mL,维生素K 4.5 μL,氯化血红素0.022 5 g,刃天青0.025%(以上物质均按照1 L计算)。配制完成后,滴加NaOH调节pH值至7.0后进行灭菌处理以待使用。
新鲜粪便采集自喂养完成后的C57BL/6J小鼠,参照LI等[6]方法制备粪便混悬液。将粪便样品用无菌PBS(10 mmol/L,pH 6.8)稀释10倍,500 r/min离心5 min,去除较大的粪便颗粒,得到10%的粪便混悬液。
1.3.3.2 脱镁叶绿素的体外发酵
按照VIERA等[14]测定新鲜小鼠粪便中叶绿素浓度,根据《中国居民膳食指南》建议体重70 kg成年人1天至少摄入300 g蔬菜[6],按照所摄入叶绿素含量,换算后得到体外发酵叶绿素的质量浓度为0.025 mg/mL。将脱镁叶绿素-丙酮溶液,在35 ℃减压旋转蒸发至干,分别准确称取2.5 mg脱镁叶绿素a和脱镁叶绿酸a,溶于1 mL二甲基亚砜(dimethyl sulfoxide,DMSO)中,加入9 mL无菌纯水,再经0.45 μm有机膜过滤得到0.25 mg/mL的脱镁叶绿素的10% DMSO溶液(体积分数,下同),按照培养基∶菌液∶脱镁叶绿素溶液=6∶3∶1,配制10 mL发酵液。不含脱镁叶绿素的空白组加入等体积的10% DMSO溶液以代替脱镁叶绿素。所有样品均在37 ℃的厌氧室(10% CO2、10% H2和80% N2)中发酵48 h,并在0、12、24、48 h分别收集上清液及沉淀保存于-80 ℃待用。每次收集后的剩余样品,重新充氮后继续厌氧发酵。
1.3.4 脱镁叶绿素的定性定量测定
参考AGARRY等[15]方法采用超高效液相-二极管阵列检测器(ultra high performance liquid phase diode array detector,UPLC-DAD)测定脱镁叶绿素的浓度,检测条件设置为:分析柱Poroshell 120 C18柱(2.1 mm×100 mm,1.9 μm),保护柱使用相同材质。进样条件按照实验室已建立的检测方法进行设置:流速为0.2 mL/min,液体流动相A为V(甲醇)∶V(水)=8∶2,B相为V(甲醇)∶V(丙酮)=1∶1,两种流动相中均加入5 mmol/L乙酸铵。采用梯度洗脱程序:0~15 min,25% B~100% B;15~20 min,100% B;20~25 min,25% B。DAD检测器记录19~800 nm的检测峰,记录在410 nm下的色谱图,结合峰形,保留时间,吸光性质定性脱镁叶绿素,利用实验室所建立的基于叶绿素标准品所作标准曲线进行定量测定。
1.3.5 高脂饮食诱导的肠道菌群测序分析
发酵完成后的样品中肠道微生物总DNA提取以及高通量测序,委托上海美吉生物医药科技有限公司进行。相关菌群的DNA按照试剂盒说明书进行提取,使用PCR扩增细菌16S rRNA基因的V3和V4区。回收PCR产物后使用2%琼脂糖凝胶电泳检测,最终扩增产物在Illumina公司的PE250平台进行测序,使用QIIME2软件进行分析。
1.3.6 短链脂肪酸含量的测定
样品处理:从样品中吸取50 μL发酵液,加入100 μL乙腈进行超声波处理(5 ℃, 40 KHz, 30 min)。随后,在4 ℃下以13 500×g离心15 min。上清液中加入20 μL NPH-HCl (0.2 mmol/L,含有6%吡啶)和20 μL EDC-HCL(0.12 mmol/L,含6%吡啶)溶液,40 ℃反应30 min,再用50%乙腈-水溶液稀释至750 μL进行检测。使用超高效液相色谱-质谱联用技术对样品中的短链脂肪酸进行测定,方法参照MENG等[16]进行。仪器参数及规格如下:Agilent 1290液相色谱联用四级杆飞行时间串联质谱仪,Poroshell 120 C18(2.1 mm×100 mm,1.9 μm)液相色谱柱,柱温40 ℃,进样量为2 μL。流动相A(0.1% 甲酸-水溶液),流动相B(0.1% 甲酸-乙腈)。4种短链脂肪酸标准曲线如公式(1)~公式(4)所示:
乙酸:y=0.000 001 035x-1.775 469 537(R2=0.998 816)
(1)
丙酸:y=0.000 003 481 9x+0.134 940 833(R2=0999 498)
(2)
丁酸:y=0.000 001 358 41x+0.176 774 359(R2=0.999 608)
(3)
戊酸:y=0.000 001 463 71x+0.056 999 162(R2=0.999 924)
(4)
1.3.7 非靶向代谢组检测
非靶向代谢组方法参考CHAN等[17]研究,采用超高效液相色谱-质谱联用技术进行检测。样品处理:吸取0.6 mL发酵液到已灭菌的微型离心管并立即冷冻离心(10 000 r/min,4 ℃,5 min),吸取上清液0.2 mL加入0.8 mL V(乙腈)∶V(甲醇)=1∶1于新离心管内,进行冷冻离心(10 000 r/min,4 ℃,5 min),取上清液200 μL进行样品制备。检测条件:色谱柱采用Poroshell 120 C18(2.1 mm×100 mm,1.9 μm),柱温30 ℃,进样量5 μL,时间30 min,ESI正、负离子模式进行质谱采集。ESI正离子模式下流动相A(0.1% 甲酸-水),流动相B(乙腈);ESI负离子模式下流动相A(0.1% 甲酸-水-5 mmol/L乙酸铵),流动相B(乙腈)。
1.3.8 数据分析
所有实验组均为6个平行,实验数据使用SPSS 23.0.0进行显著性分析。组间比较采用单因素方差分析(ANOVA),P<0.05为存在显著差异,用Graph pad Prism 9.1进行作图。微生物组学部分的原始数据进行分类操作单元的划分(ASV水平),肠道菌群丰度及微生物种类差异分析通过美吉生物云平台(https://www.majorbio.com/)分析。超高效液相色谱-质谱联用技术非靶向检测发酵48 h后粪菌液,原始数据放入Bruker Data Analysis 5.1软件进行校正后,profile.文件转为MzXML格式放入Wizard MZmine 3进行降噪、基线校正、归一化、去同位素等处理。KEGG(https://www.genome.jp/kegg/)在线注释后的数据导出为excel文件,表格数据根据样本组别进行分列整理。非靶向代谢组学相关分析使用基迪奥在线生信云处理平台(https://www.omicshare.com/tools/)。
2 结果与分析
2.1 发酵前肠道微生物结构组成
高脂饮食诱导后的空白组和正常饮食组小鼠粪便肠道微生物组成如图1-a~图1-b所示,在门水平占据主要丰度的是厚壁菌门(Firmicutes)、拟杆菌门(Bacteroidota)、疣微菌门(Verrucomicrobiota)、放线菌门(Actinobacteriota)以及变形菌门(Proteobacteria),属水平上丰度排名前五的是Allobaculum、Faecalibaculum、乳杆菌属(Lactobacillus)、Muribaculaceae和阿克曼菌属(Akkermansia),两组样品的肠道微生物菌种和丰度差异明显,高脂饮食诱导的肠道菌群结果与同行所发现一致[8]。
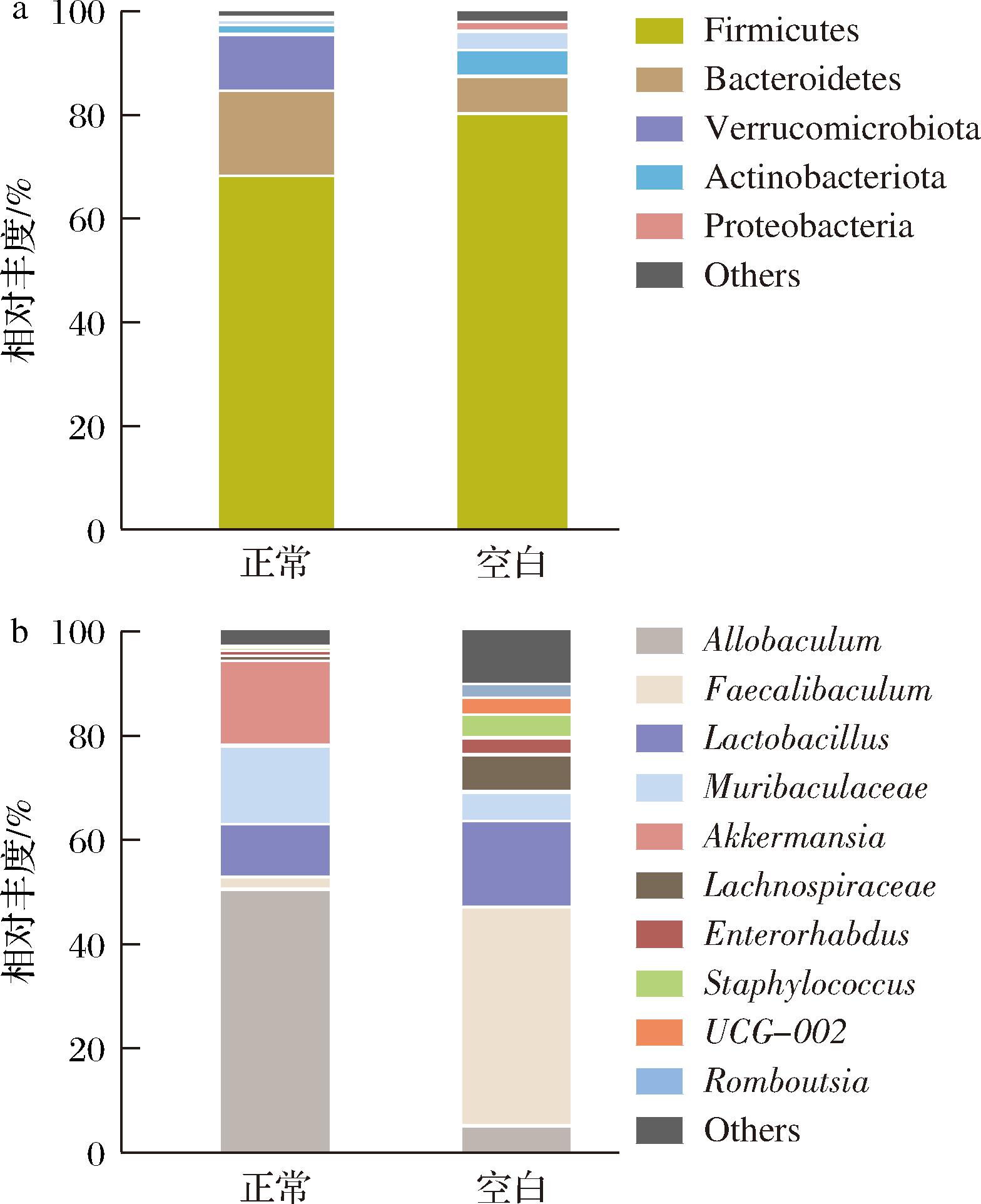
a-门水平;b-属水平
图1 发酵前肠道微生物群落组成
Fig.1 Microflora community composition before fermentation
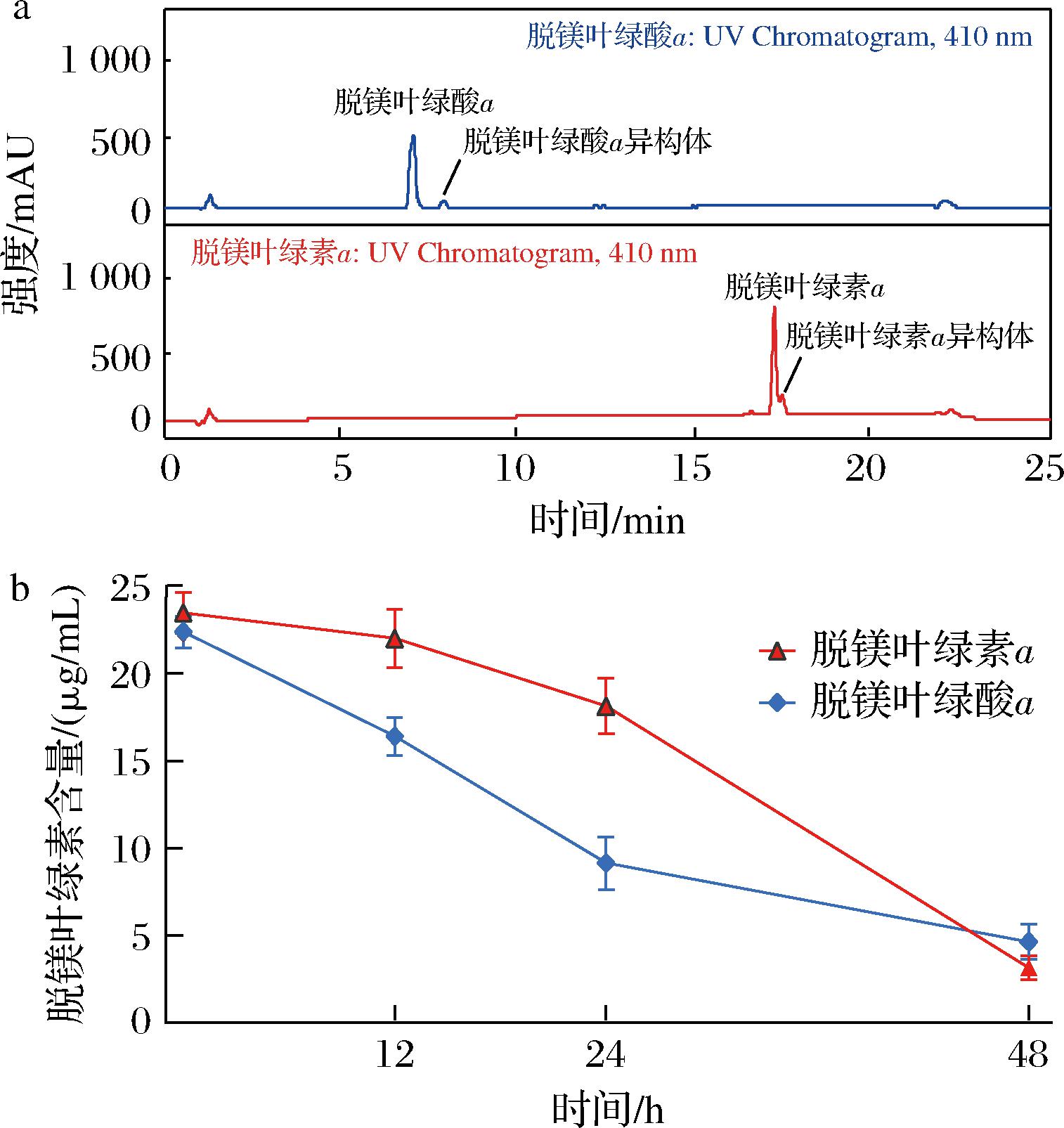
a-发酵前脱镁叶绿素液相色谱;b-发酵过程中 脱镁叶绿素含量
图2 脱镁叶绿素纯度及体外发酵过程中含量
Fig.2 Purity of pheophytins and changes in its concentration during in vitro fermentation process
2.2 发酵前脱镁叶绿素纯度及体外发酵过程中含量的变化
脱镁叶绿素a和脱镁叶绿酸a的纯度如图2-a所示,脱镁叶绿素a纯度约97%,脱镁叶绿酸a纯度约为95%。如图2-b所示,在整个发酵过程中脱镁叶绿素a和脱镁叶绿酸a组的含量均呈现下降趋势。在发酵24 h后,脱镁叶绿素a组含量从24 μg/mL下降到18 μg/mL,而在最后的24 h内含量极为显著的下降到3 μg/mL(P<0.001);而在脱镁叶绿酸a组中含量从最初的22 μg/mL极为显著的下降到9 μg/mL(P<0.001),随后在24~48 h显著下降到5 μg/mL(P<0.05)。发酵过程中,在最初的24 h内脱镁叶绿素a的含量变化并不明显,在24~48 h内却急剧下降;与之不同,发酵中脱镁叶绿酸a含量在0~24 h剧烈下降(含量<50%),随后下降的趋势减缓。
这表明高脂粪菌对脱镁叶绿素a和脱镁叶绿酸a的利用速度不同。脱镁叶绿酸a相比脱镁叶绿素a分子质量更小,极性更大。而分子的极性、离子化程度和分子大小对代谢利用有很大影响[18]。这也被研究者用人结直肠腺癌细胞Caco-2证实,脱镁叶绿素a和脱镁叶绿酸a在肠道上皮细胞吸收中,脱镁叶绿酸a的细胞转运速度远快于脱镁叶绿素a[19]。
2.3 脱镁叶绿素体外发酵对高脂饮食诱导的肠道菌群影响
2.3.1 Alpha多样性和Beta多样性评价
Alpha多样性常被用于评价菌群的丰富度和均匀度,本文采用Chao1指数和Shannon指数在ASV水平上进行分析。发酵48 h后结果如图3-a~图3-b所展示。与空白组相比,脱镁叶绿素a组和脱镁叶绿酸a组没有差异,表明脱镁叶绿素对高脂饮食诱导的小鼠肠道菌群物种丰富度和均匀度影响不显著。
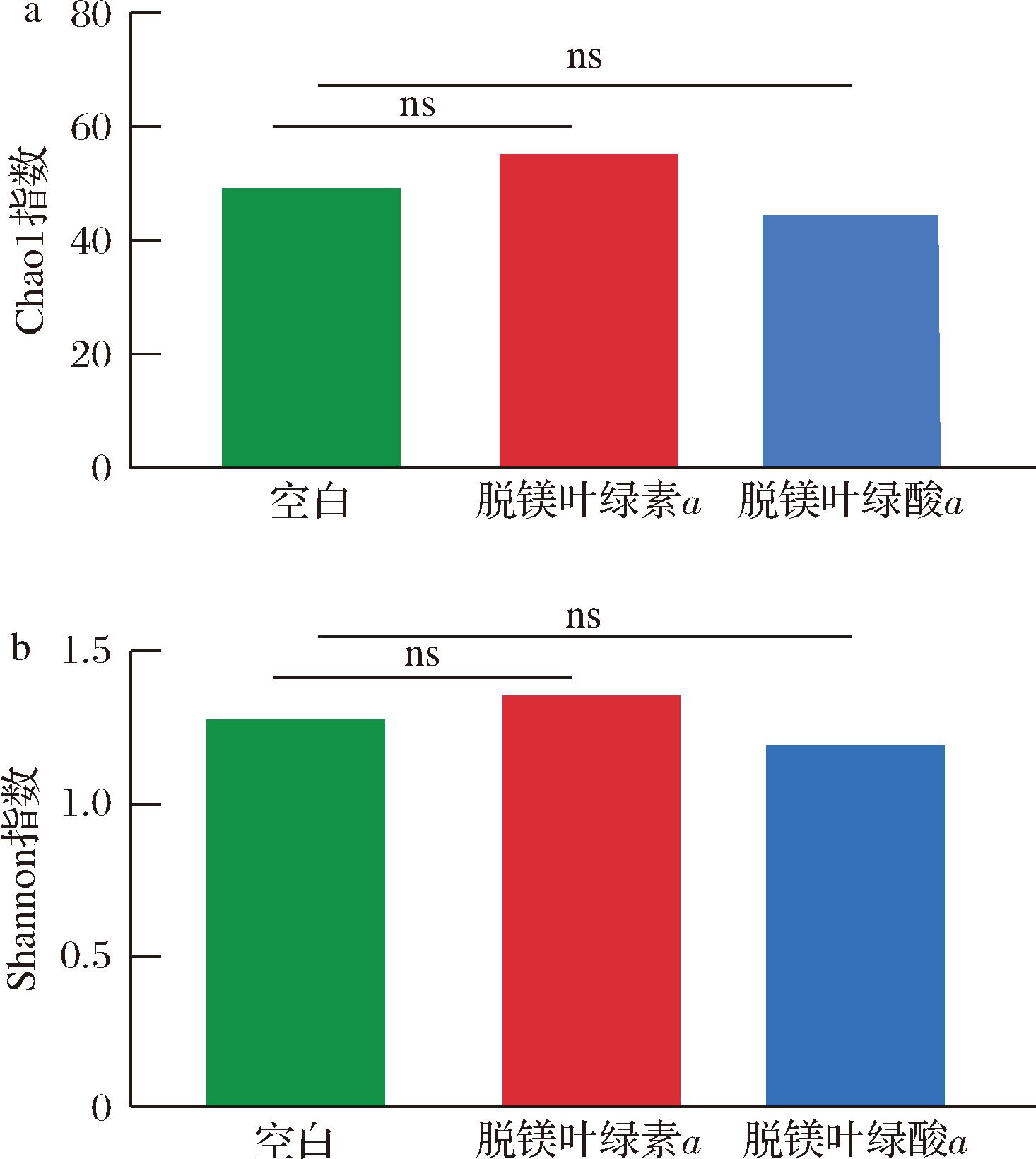
a-Chao1指数;b-Shannon指数
图3 体外发酵48 h后Alpha多样性分析
Fig.3 Alpha diversity analysis after 48 hours in vitro fermentation
注:ns:无差异。
随后使用Beta多样性在ASV水平上分析,对发酵48 h后样本群落组成进行主坐标分析(principal co-ordinates analysis,PCoA)。结果表明,3组样品之间存在统计学差异性,同组样品间有明显的聚类,PC1坐标可以解释最大约70%的数据变化,3组样品组间有明显的分开(图4-a)。使用NMDS(non-metric multidimensional scaling sorting)来评估不同组之间的相似性(图4-b)。在NMDS中,脱镁叶绿酸a组相距空白组较远,脱镁叶绿素a介于两组样品之间。PCoA和NMDS的结果表明,在添加脱镁叶绿素a和脱镁叶绿酸a处理后,同组样品能聚集,组间能分开。表明脱镁叶绿素a和脱镁叶绿酸a均能对高脂饮食诱导的肠道菌群结构产生差异化影响。ANOSIM检验后,PCoA模型R2=0.403,P=0.012,NMDS模型R2=0.325,P=0.029参数表明,两种模型分析的组内差异具有统计学意义。
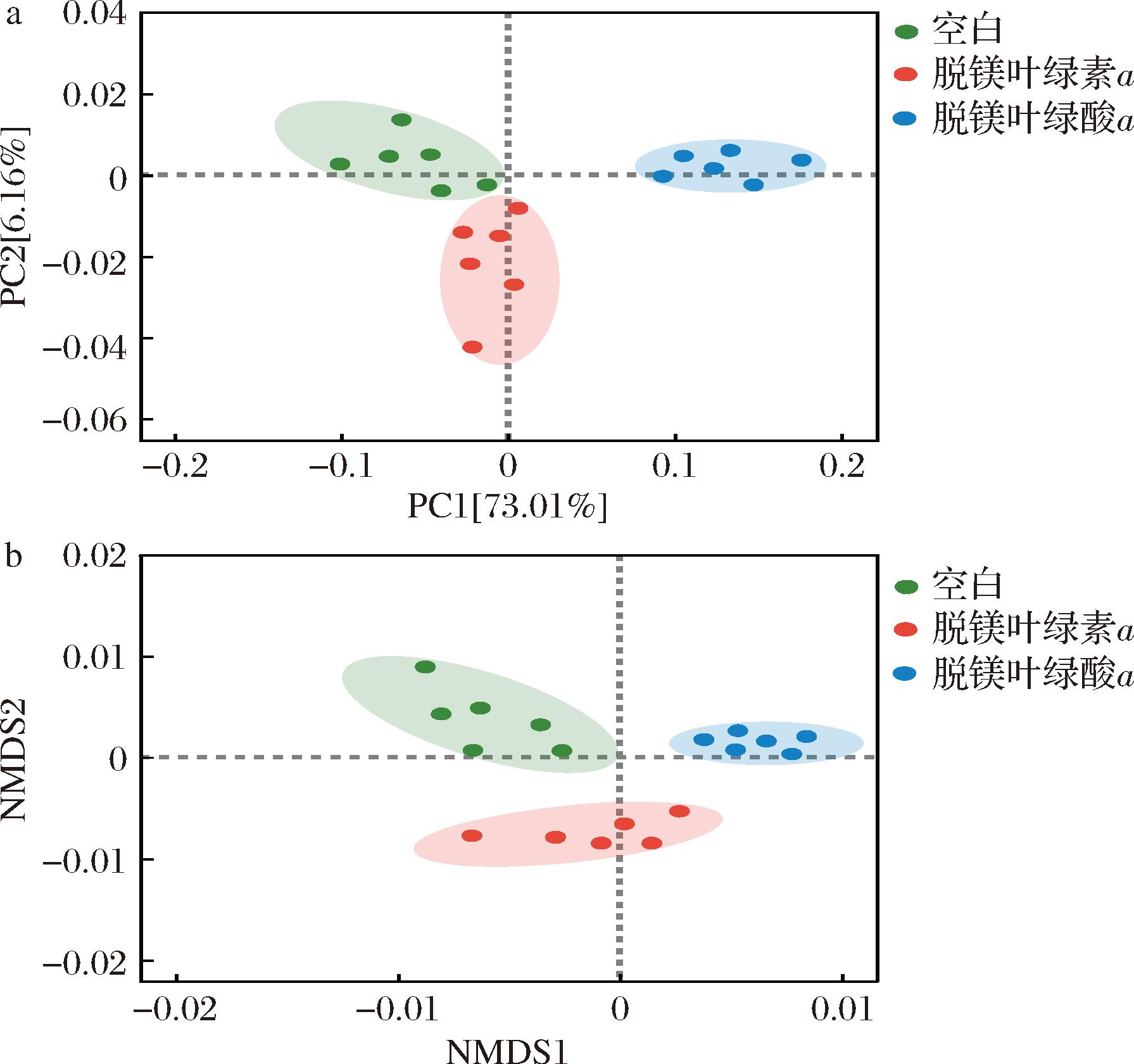
a-PCoA;b-NMDS分析
图4 体外发酵48 h后Beta多样性分析
Fig.4 Beta diversity analysis after 48 hours in vitro fermentation
2.3.2 脱镁叶绿素对高脂饮食诱导的肠道菌群物种组成的影响
在门水平和属水平上评估添加脱镁叶绿素发酵后的菌群调节作用。如图5-a所示,与最初的菌落丰度相比,发酵48 h后门水平上的菌种丰度出现明显变化。从结果上来说,脱镁叶绿酸a组发酵后的丰度变化比脱镁叶绿素a组更明显。发酵48 h后,在门水平上占据99%丰度的菌群是变形菌门(Proteobacteria)和厚壁菌门(Firmicutes)。与空白组相比,脱镁叶绿素a和脱镁叶绿酸a处理组均降低了变形菌门(Proteobacteria)丰度,提高了厚壁菌门(Firmicutes)丰度。Proteobacteria包括许多病原菌,它们的丰度降低通常代表了有益菌群的增长[8]。属水平的丰度如图5-b所示,发酵48 h后属水平上主要是埃希氏-志贺菌属(Escherichia-Shigella),不动杆菌属(Acinetobacter),Aerococcus,假单胞菌属(Pseudomonas)和肠球菌属(Enterococcus)。在属水平上脱镁叶绿素处理组与空白组相比,埃希氏-志贺菌属(Escherichia-Shigella)的丰度均被显著抑制(P<0.05),不动杆菌属(Acinetobacter)的丰度虽有所升高但无显著性差异(P>0.05)。埃希氏-志贺菌属(Escherichia-Shigella)是一类导致典型细菌性痢疾的病原菌,脱镁叶绿素组中埃希氏-志贺菌属丰度下降,推测高脂饮食诱导的肠道菌群和脱镁叶绿素互作产物对其有一定的抑制作用。
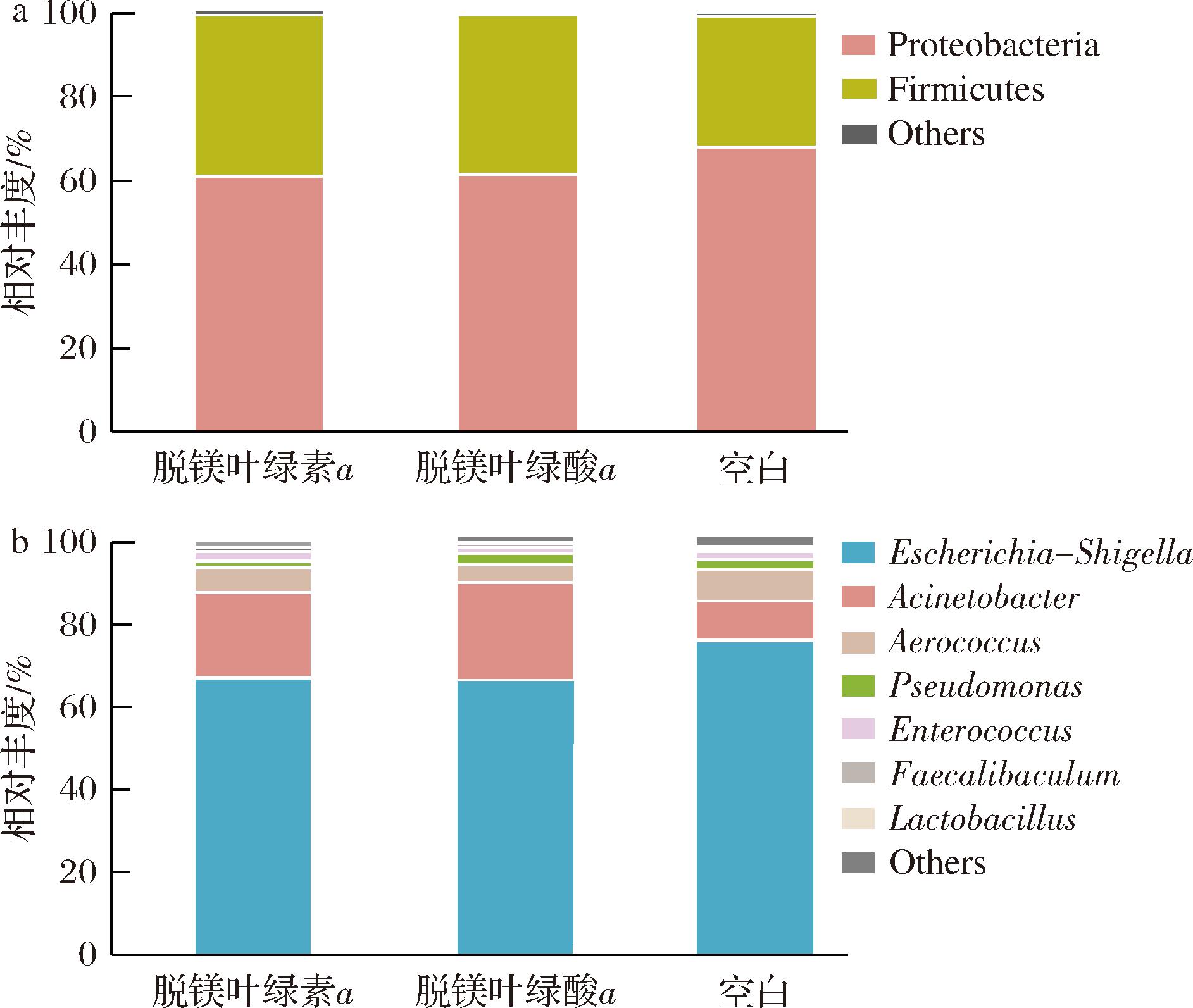
a-门水平丰度;b-属水平丰度
图5 体外发酵48 h后肠道微生物群落组成变化
Fig.5 The composition of the microflora changed after 48 hours of in vitro fermentation
2.4 添加脱镁叶绿素发酵后对高脂饮食诱导的肠道菌群代谢影响
2.4.1 发酵过程中短链脂肪酸含量变化
短链脂肪酸是重要的肠道菌群代谢物。如图6-a~图6-e所示,在发酵的24 h内,脱镁叶绿素a组和脱镁叶绿酸a组发酵后产生的短链脂肪酸含量均显著高于空白组(P<0.05)。在整个发酵过程中,3组样品的短链脂肪酸含量先升高后下降,可能的原因是因为脱镁叶绿素无法直接提供微生物代谢所需能量,当培养基中碳水化合物消耗殆尽时,乙酸、丙酸也可以为微生物代谢提供能量,所以在发酵的24~48 h总短链脂肪酸含量下降[20-21]。
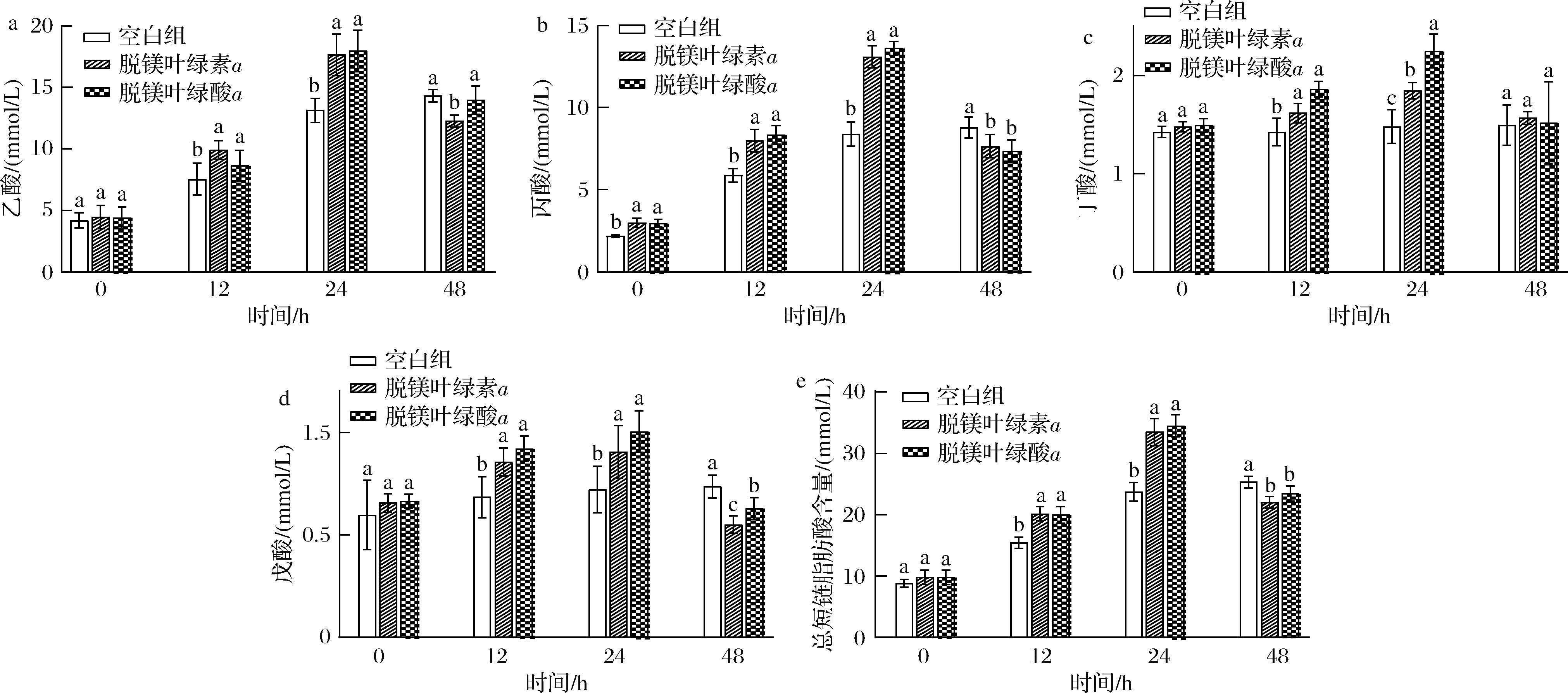
a-乙酸含量;b-丙酸含量;c-丁酸含量;d-戊酸含量;e-总短链脂肪酸含量
图6 体外发酵48 h后短链脂肪酸含量
Fig.6 Short chain fatty acid contents after 48 hours of in vitro fermentation

a-脱镁叶绿素a和空白组的非靶向代谢组学OPLSDA;b-脱镁叶绿酸a和空白组的非靶向代谢组学OPLSDA; c-脱镁叶绿素a的代谢差异物和微生物的Spearman相关性;d-脱镁叶绿酸a的代谢差异物和微生物的Spearman相关性
图7 非靶向代谢组学结果
Fig.7 Results of untargeted metabolomics
注:*表示P<0.05;**表示P<0.01。
2.4.2 非靶向代谢组学分析高脂饮食诱导的肠道菌群代谢产物
采用超高效液相色谱-质谱联用技术非靶向检测发酵48 h后粪菌液,对原始数据进行处理。通过OPLSDA(orthogonal partial least squares-discriminant analysis)两两比较分析(脱镁叶绿素a和空白组;脱镁叶绿酸a和空白组),结果如图7-a~图7-b所示。按照VIP>1.5,P≤0.05的条件,筛选出脱镁叶绿素a组和脱镁叶绿酸a组中与微生物额外作用产生的差异代谢物。再对高脂饮食诱导的肠道菌群和差异代谢物进行Spearman相关性分析,相关系数用r表示,r在-1~1之间,r绝对值越大,相关性越强。结果如图7-c~图7-d所示,在脱镁叶绿素a组中与代谢产物密切关联的是肠球菌属(Enterococcus)和费克蓝姆菌属(Facklamia);脱镁叶绿酸a中则是Aerococcus和Enterorhabdus。脱镁叶绿素a组共筛选出20种物质,其中14种酯类化合物,3种胆汁酸盐。脱镁叶绿酸a组筛选出了共33种物质,其中有20种酯类化合物,4种氨基衍生物,3种胆汁酸盐。此外,还存在强相关的抗生素类物质。istamycin AO是对革兰氏阳性和阴性菌均有很强抑制作用的抗生素[22],夫西地酸对各种革兰氏阳性球菌有明显的抑菌作用[23],而庆大霉素C1对革兰氏阴性菌有明显抑制作用[24]。这些类抗生素也可能是埃希氏-志贺菌属(Escherichia-Shigella)丰度受到抑制的原因。
3 结论
本研究通过对高脂饮食诱导的肠道菌群添加脱镁叶绿素a和脱镁叶绿酸a,进行体外发酵实验,进一步探究脱镁叶绿素对高脂饮食诱导的肠道菌群调节作用。基于16S rRNA的微生物组学结果表明,脱镁叶绿素在门水平上降低变形菌门(Proteobacteria)丰度,升高厚壁菌门(Firmicutes)丰度;属水平上显著抑制致病菌(P<0.05)埃希氏-志贺菌属(Escherichia-Shigella)丰度。基于液质联用技术靶向测定短链脂肪酸结果表明,添加脱镁叶绿素后能促进高脂饮食诱导的粪菌生成短链脂肪酸,尤其是乙酸、丙酸、丁酸。最后,非靶向代谢组结果表明,埃希氏-志贺菌属(Escherichia-Shigella)受到抑制,可能是因为脱镁叶绿素与高脂饮食诱导的粪菌的相互作用后产生的抗菌物质(istamycin AO、夫西地酸、庆大霉素C1)。现有结果表明,脱镁叶绿素对高脂饮食诱导的小鼠肠道菌群及其代谢存在调节作用,对机体健康具有潜在有益影响。但体外发酵结果并不能完全反映脱镁叶绿素与高脂饮食诱导的肠道菌群互相作用,相应机制和潜在健康效应还需深入研究。
[1] BRAY G A, KIM K K, WILDING J P H, et al.Obesity:A chronic relapsing progressive disease process.A position statement of the World Obesity Federation[J].Obesity Reviews, 2017, 18(7):715-723.
[2] 胡俐泉,屠琳玥,赵悦伶,等.西湖龙井茶对高脂高果糖饮食小鼠肠道菌群的调节作用[J].浙江大学学报(农业与生命科学版),2024,50(3):481-494.HU L Q, TU L Y, ZHAO Y L, et al. Regulatory effects of Xihu Longjing on the intestinal flora of mice fed on the high-fat and high-fructose diet[J]. Journal of Zhejiang University (Agriculture and Life Sciences), 2024,50(3):481-494.
[3] BELKAID Y, HAND T W.Role of the microbiota in immunity and inflammation[J].Cell, 2014, 157(1):121-141.
[4] DE VOS W M, TILG H, VAN HUL M, et al.Gut microbiome and health:Mechanistic insights[J].Gut, 2022, 71(5):1020-1032.
[5] FAN Y, PEDERSEN O.Gut microbiota in human metabolic health and disease[J].Nature Reviews.Microbiology, 2021, 19(1):55-71.
[6] LI Y Y, LU F, WANG X, et al.Biological transformation of chlorophyll-rich spinach (Spinacia oleracea L.) extracts under in vitro gastrointestinal digestion and colonic fermentation[J].Food Research International, 2021, 139:109941.
[7] MARTIN-GALLAUSIAUX C, MARINELLI L, BLOTTI RE H M, et al.SCFA:Mechanisms and functional importance in the gut[J].Proceedings of the Nutrition Society, 2021, 80(1):37-49.
RE H M, et al.SCFA:Mechanisms and functional importance in the gut[J].Proceedings of the Nutrition Society, 2021, 80(1):37-49.
[8] LI Y Y, CUI Y, LU F, et al.Beneficial effects of a chlorophyll-rich spinach extract supplementation on prevention of obesity and modulation of gut microbiota in high-fat diet-fed mice[J].Journal of Functional Foods, 2019, 60:103436.
[9] SEMAAN D G, IGOLI J O, YOUNG L, et al.In vitro anti-diabetic effect of flavonoids and pheophytins from Allophylus cominia Sw.on the glucose uptake assays by HepG2, L6, 3T3-L1 and fat accumulation in 3T3-L1 adipocytes[J].Journal of Ethnopharmacology, 2018, 216:8-17
[10] LI Y Y, CAO J R, ZHENG H L, et al.Transformation pathways and metabolic activity of free chlorophyll compounds from chloroplast thylakoid membrane under in vitro gastrointestinal digestion and colonic fermentation in early life[J].Food Bioscience, 2021, 42:101196.
[11] CHEN K W, ROCA M.In vitro digestion of chlorophyll pigments from edible seaweeds[J].Journal of Functional Foods, 2018, 40:400-407.
[12] LI Y C, AGARRY I E, DING D S, et al.Screening of dephytinization reaction of chlorophyll pigments with Citrus acetone powder by UPLC-DAD-MS[J].Journal of Food Science, 2023, 88(1):147-160.
[13] FENG J C, WANG J, BU T T, et al.Structural, in vitro digestion, and fermentation characteristics of Lotus leaf flavonoids[J].Food Chemistry, 2023, 406:135007.
[14] VIERA I, CHEN K W, R OS J J, et al.First-pass metabolism of chlorophylls in mice[J].Molecular Nutrition &Food Research, 2018, 62(17):e1800562.
OS J J, et al.First-pass metabolism of chlorophylls in mice[J].Molecular Nutrition &Food Research, 2018, 62(17):e1800562.
[15] AGARRY I E, DING D S, LI Y C, et al.In vitro bioaccessibility evaluation of chlorophyll pigments in single and binary carriers[J].Food Chemistry, 2023, 415:135757.
[16] MENG X J, PANG H H, SUN F, et al.Simultaneous 3-nitrophenylhydrazine derivatization strategy of carbonyl, carboxyl and phosphoryl submetabolome for LC-MS/MS-based targeted metabolomics with improved sensitivity and coverage[J].Analytical Chemistry, 2021, 93(29):10075-10083.
[17] CHAN Y T, HUANG J T, WONG H C, et al.Metabolic fate of black raspberry polyphenols in association with gut microbiota of different origins in vitro[J].Food Chemistry, 2023, 404:134644.
[18] FERNANDES A S, NASCIMENTO T C, PINHEIRO P N, et al.Insights on the intestinal absorption of chlorophyll series from microalgae[J].Food Research International, 2021, 140:110031.
[19] GANDUL-ROJAS B, GALLARDO-GUERRERO L, ISABEL M NGUEZ-MOSQUERA M.Influence of the chlorophyll pigment structure on its transfer from an oily food matrix to intestinal epithelium cells[J].Journal of Agricultural and Food Chemistry, 2009, 57(12):5306-5314.
NGUEZ-MOSQUERA M.Influence of the chlorophyll pigment structure on its transfer from an oily food matrix to intestinal epithelium cells[J].Journal of Agricultural and Food Chemistry, 2009, 57(12):5306-5314.
[20] CHEN L, WANG Y X, LIU J X, et al.Structural characteristics and in vitro fermentation patterns of polysaccharides from Boletus mushrooms[J].Food &Function, 2023, 14(17):7912-7923.
[21] FU X, CAO C L, REN B B, et al.Structural characterization and in vitro fermentation of a novel polysaccharide from Sargassum thunbergii and its impact on gut microbiota[J].Carbohydrate Polymers, 2018, 183:230-239.
[22] KUDO F, EGUCHI T.Biosynthetic genes for aminoglycoside antibiotics[J].Journal of Antibiotics, 2009, 62(9):471-481.
[23] 张雷, 蔡芸, 王睿.米诺环素与夫西地酸对98株耐甲氧西林金黄色葡萄球菌的联合药敏研究[J].中国临床药理学杂志, 2011, 27(8):587-589.ZHANG L, CAI Y, WANG R.Antibacterial activity of minocycline in combination with fusidic acid against 98 strains of methicillin-residtant Staphylococcus aureus in vitro[J].The Chinese Journal of Clinical Pharmacology, 2011, 27(8):587-589.
[24] 李帆, 张伟, 丁文渊.庆大霉素等抗菌药物在大肠杆菌培养基中的抑菌效果[J].宜春学院学报, 2018, 40(12):62-64;75.LI F, ZHANG W, DING W Y.Antibacterial effect of gentamycin and other antibiotics in agar medium for Escherichia coli[J].Journal of Yichun University, 2018, 40(12):62-64;75.