二十世纪初,路易斯·巴斯德发现某些微小生物作用可导致食物发酵[1]。俄国科学家梅契尼可夫发现,摄入更多的发酵乳制品可使人群更健康,更长寿,这种现象在长期摄入发酵乳制品的保加利亚地区更加显著[2]。益生菌的定义在2013年得以规范,其是指以足够的量施用可以给宿主带来健康益处的活性微生物[3]。
细菌可以通过不同的机制与肠道细胞相互作用,从而短期或者长期的存在于肠道中。益生菌黏附在肠道上皮细胞后,可以通过分泌生物活性因子调节细胞的各项生理功能,而对于细胞免疫功能的调节便是益生菌对于生物体的重要作用之一,有研究表明,益生菌与通过调节Toll样受体信号通路从而增强先天免疫力并调节病原体诱导的验证效应[4]。分离自中国健康的婴儿肠道的鼠李糖乳酪杆菌MP108,通过体内外多重筛选,在2021年4月份发布的《可用于婴幼儿食品的菌种名单》[5]中,鼠李糖乳酪杆菌MP108正式被列入可用于婴幼儿食品的菌株名录,是我国第一株由国人自主研发并可用于婴幼儿的菌株。
低聚糖可以通过促进生长和黏附等方式协助益生菌定殖肠道,低聚果糖(fructooligosaccharide,FOS)和低聚半乳糖(galactooligosaccharide,GOS)[6]研究较多,这些低聚糖可以优先被双歧杆菌代谢,因为双歧杆菌具有分解代谢的相关功能的酶,FOS与GOS间的化学键容易被双歧杆菌属中存在的β-果糖苷酶和β-半乳糖苷酶打断从而降解[7]。目前,母乳低聚糖开始进入实用阶段。本文主要通过动物模型探究母乳低聚糖2′-岩藻糖基乳糖(2′-focusllactos,2′-FL)与鼠李糖乳酪杆菌MP108在免疫调节方面的协同作用。
1 材料与方法
1.1 材料与试剂
FOS、GOS(纯度>95%),量子高科(中国)生物股份有限公司;2′-FL(纯度>95%),德国BASF公司;环磷酰胺,北京索莱宝生物工程公司;左旋咪唑,广州益特宝动物药业有限公司;肿瘤坏死因子(tumor necrosis factor-α,TNF-α)、白细胞介素-2(interleukin-2,IL-2)、白细胞介素-10(interleukin-10,IL-10)检测试剂盒,上海华蓝化学制品有限公司;免疫球蛋白M、G(IgM、IgG)检测试剂盒,北京索莱宝生物工程研究所;葡萄糖、蛋白胨、无水乙酸钠、MgSO4·7H2O、MnSO4·7H20、K2HPO4·7H2O、柠檬酸二铵,酵母膏、吐温-80,国药集团化学试剂有限公司;牛肉膏、琼脂粉,生工生物工程股份有限公司。
MRS培养基(g/L):葡萄糖 20,蛋白胨 10,无水乙酸钠 5,MgSO4·7H2O 0.2,MnSO4·7H20 0.05,K2HPO4·7H2O 2,柠檬酸二铵 2,酵母膏 5,牛肉膏 10,吐温-80 1 mL,固体培养基额外添加琼脂粉 2%。
1.2 仪器与设备
BXP-16恒温培养箱,上海力辰邦仪器科技有限公司;JF-SX-500型全自动灭菌锅,日本TOMY公司;SW-CJ-1FD型超净工作台,苏州净化设备有限公司;HERACELL二氧化碳培养箱,美国Thermo公司。
1.3 实验方法
1.3.1 菌株的培养
将鼠李糖乳酪杆菌MP108以3%的接种量接种在37 ℃的MRS肉汤培养基中培养18 h,在MRS固体平板中分离纯化3次后,备用。
1.3.2 菌株的培养
低聚糖溶液的制备:低聚糖总质量浓度均为15.3 g/L,其中复配低聚糖中各低聚糖的质量比为FOS∶GOS∶2′-FL=10∶1∶1。
菌悬液的制备:将实验菌株在MRS液体培养基中活化3代,于6 000 r/min离心10 min收集菌体,并用灭菌生理盐水清洗菌体两次,用PBS或低聚糖溶液调整菌数为1.0×109 CFU/ mL。
1.3.3 动物分组及处理
本实验使用SPF级Wistar大鼠为雄性,周龄4~5周[济南朋悦实验动物繁殖有限公司,许可证号:SCXK(鲁)20190003],动物伦理由扬州大学实验动物伦理委员会审查,编号:202302103。
将Wistar大鼠适应性饲养1周后,随机分为8组,每组10只,实验开始前,选择40 mg/kg BW的环磷酰胺腹腔注射3 d的方式构建免疫低下大鼠的模型。结束后连续干预4周,所有样品均按0.1 mL/(10 g·d)剂量灌胃(各样品按照1.3.2节准备),每天定时补充饮水和饲料,灌胃完成后对动物进行观察,及时记录动物的状态,一周更换两次垫料。具体分组及干预情况见表1。
表1 动物实验分组情况及干预情况
Table 1 Grouping of animal experiments and intervention
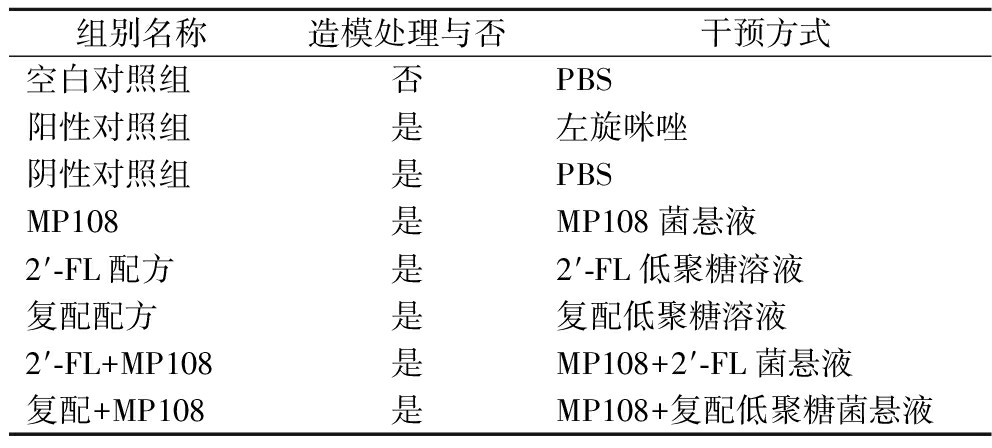
组别名称造模处理与否干预方式空白对照组否PBS阳性对照组是左旋咪唑阴性对照组是PBSMP108是MP108菌悬液2′-FL配方是2′-FL低聚糖溶液复配配方是复配低聚糖溶液2′-FL+MP108是MP108+2′-FL菌悬液复配+MP108是MP108+复配低聚糖菌悬液
1.3.4 免疫器官指数测定
在干预4周后,将大鼠断粮24 h后称重,取眼球血后颈椎脱臼后处死。摘取胸腺和脾脏,将周围组织剥离干净后清洗,使用滤纸吸干后称重,按照公式(1)计算器官指数:
器官指数![]()
(1)
1.3.5 血清制备及相关指标的测定
采大鼠眼球血,使用无菌管收集大鼠血液样品,室温血液自然凝固15 min,4 ℃离心(2 000 r/min,20 min),收集血清。使用ELISA试剂盒检测血清中的IL-2、IL-10和TNF-α等免疫因子和免疫球蛋白。
1.4 数据分析
所有数据进行平行测定3次,结果使用Excel、SPSS和Origin进行统计学分析并作图。对数据进行显著性分析,采用不同字母表示显著性差异(P<0.05)。
2 结果与分析
2.1 免疫低下大鼠的体重变化
机体体重的变化是免疫力低下最直观的外在表现。从造模成功后开始计算天数,整个干预期间大鼠体重增长情况如图1所示,空白对照组的体重增量呈现出较为稳定的趋势,而干预组的增长速度较缓慢。在第3~6天时,阴性对照组出现了体重降低的情况。所有干预组的体重整体上都呈现出上升的趋势,最终体重的增长量均在80~100 g左右,其中复配低聚糖组的体重增量相对最小。各干预组的生长均慢于对照组(前15 d),表明建模有效。干预前6 d,2′-FL表现出最好的保护效果,其体重与空白组的差距最小。对于环磷酰胺导致的免疫低下带来体重变化的效应,在许多其他研究中均有涉及,这些研究带来的趋势并不一致,这与环磷酰胺的造模方式或者实验动物的品系有关,例如,LYU等[8]的研究中,将环磷酰胺分别在实验的第1、2、3、10天注射入SD大鼠体内,体重在第10天注射完毕至结束时出现了较为明显的下降。在ALJUTAILY等[9]的研究中,使用Wistar大鼠对草药与骆驼奶的免疫调节功能进行了评价,体重均有增长,但是增长速率和最终体重不一致。
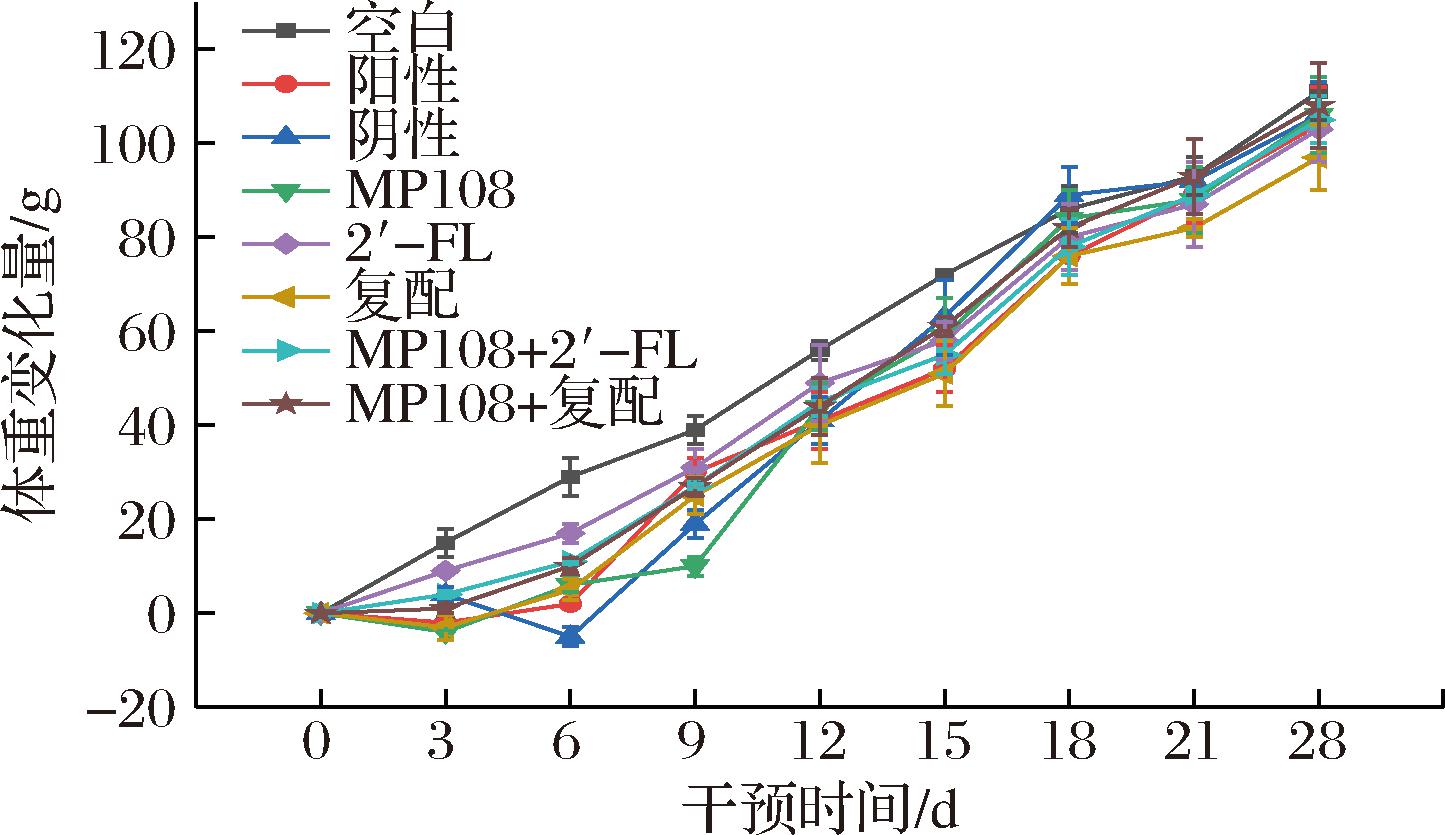
图1 各组大鼠体重变化
Fig.1 Body weight of rats in each group
2.2 免疫低下大鼠的器官指数变化
作为体内最大的免疫器官,脾脏的重量与免疫系统的健康度有直接联系,一般情况下如果脾脏的重量下降,免疫力会受损。胸腺则是人体免疫系统的中枢器官,各类免疫细胞的增殖分化在胸腺内完成。如图2所示,可以发现所有经过环磷酰胺处理的组别均出现了脾脏指数下降的现象。空白对照组的脾脏指数显著高于其他组(P<0.05)。在干预组中,单独使用鼠李糖乳酪杆菌MP108的脾脏指数与作为阳性对照的药物的无显著性差异(P>0.05),且显著高于其他组(P<0.05)。而只使用低聚糖进行干预的复配低聚糖组和2′-FL组对于脾脏指数的恢复情况则较差,整体数值水平与阴性对照组类似。
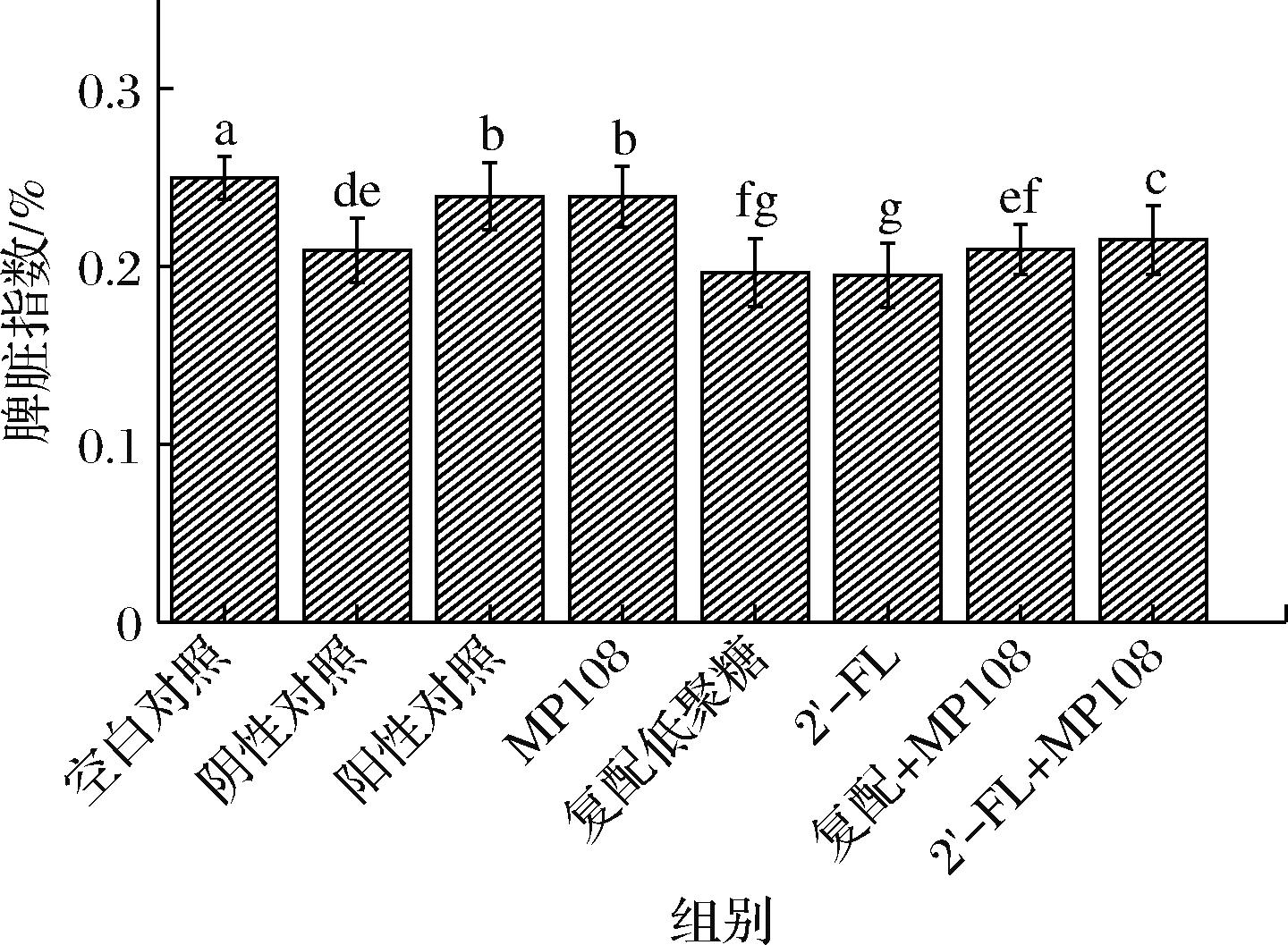
图2 各组大鼠脾脏指数
Fig.2 Spleen index of rats in each group
注:不同字母表示有显著性差异(P<0.05) (下同)。
如图3所示,阴性对照组的胸腺指数显著低于空白对照组,这表明环磷酰胺导致胸腺萎缩,从而导致了胸腺指数的下降。在干预组中,2′-FL组和2′-FL+MP108组的胸腺指数与空白对照组无显著性差异(P>0.05)。这表明这两组具有提高胸腺指数的能力。
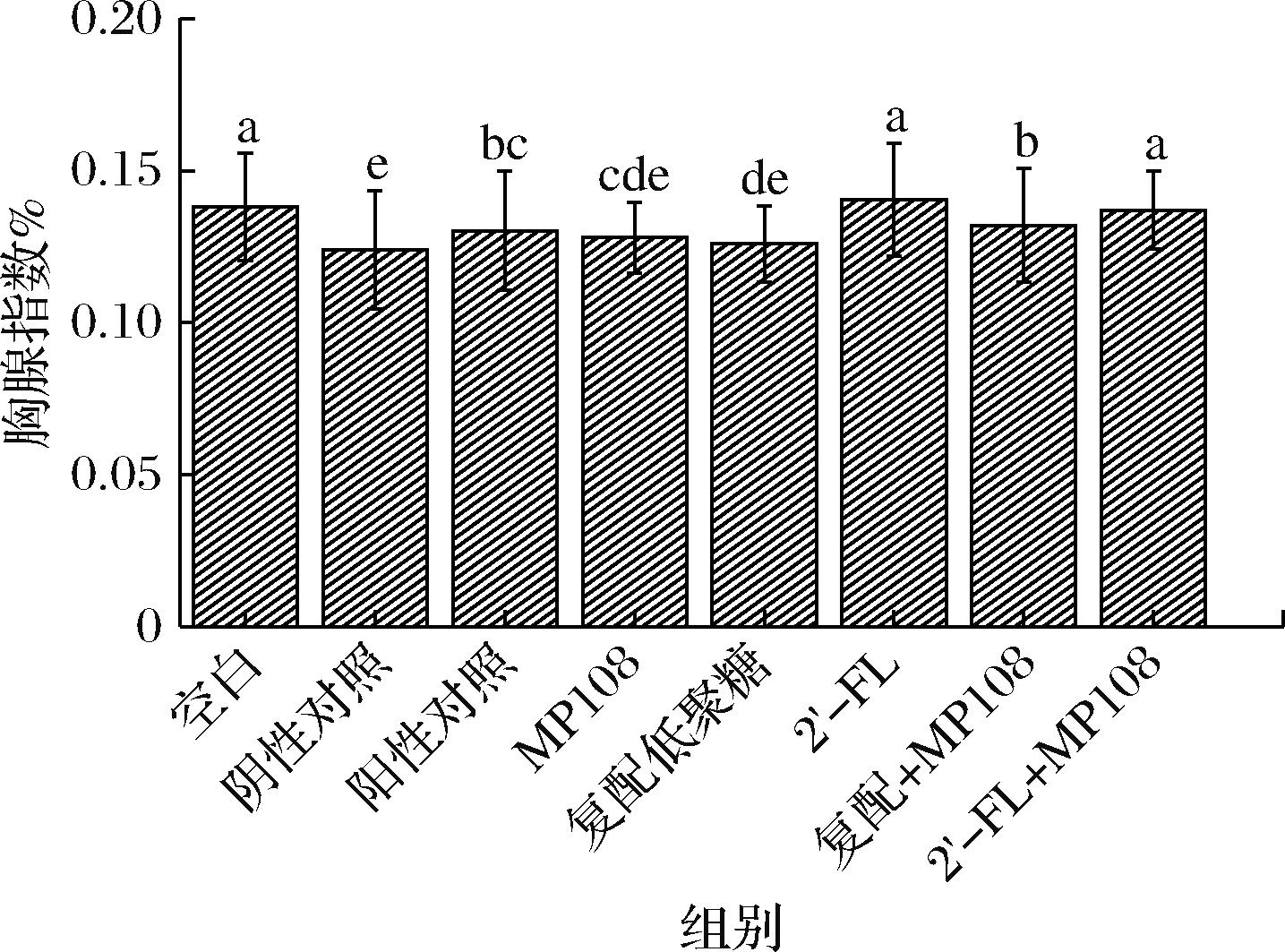
图3 各组大鼠胸腺指数
Fig.3 Thymic index of rats in each group
上述结果表明,使用低聚糖和鼠李糖乳酪杆菌MP108均可以恢复由于环磷酰胺造成的免疫器官萎缩,对于脾脏指数而言,鼠李糖乳酪杆菌MP108的效果更好。对于胸腺指数而言,2′-FL效果更好。宋翔等[10]的研究中,发现使用乳酸菌干预后的小鼠的胸腺指数有所上升,但是脾脏指数变化不明显。MA等[11]的研究表明,免疫低下可以诱导免疫器官的萎缩,使用益生菌干预后,胸腺指数显著升高,随着益生菌浓度的提高,这种现象越明显。但是脾脏指数则无显著性差异。MENG等[12]研究表明,高剂量的益生菌干预均可以有效改善由于环磷酰胺造成的胸腺指数和脾脏指数下降。各类研究出现不一致的情况可能与动物品系、造模方式等因素相关。
2.3 免疫低下大鼠的血清主要免疫指标的变化
2.3.1 细胞因子分泌量的变化
TNF是一类由免疫细胞产生的细胞因子,具有抑制肿瘤细胞活性,调节机体免疫功能,抗感染等作用[13]。TNF主要由活化的巨噬细胞、自然杀伤细胞和T淋巴细胞产生。TNF-α的生物学活性占TNF总活性的70%~95%,因此,常通过检测TNF-α来评价整体的TNF活性水平。
根据图4发现,阴性对照组的TNF-α分泌量明显上升,而使用药物干预的阳性对造组的TNF-α分泌量则出现了下降,且在数值上与空白对照组无明显差异(P>0.05)。各干预组中,单独使用菌体干预的MP108组对于TNF-α的分泌量与阴性对照组无显著性差异(P>0.05)。而2′-FL组、复配+MP108组和2′-FL+MP108组则与阳性对照组无显著性差异(P>0.05),这表明这些干预组均可以使TNF-α的分泌量恢复至与阳性对照组相似的水平。上述实验结果表明,低聚糖对于TNF-α的分泌具有调节效果。
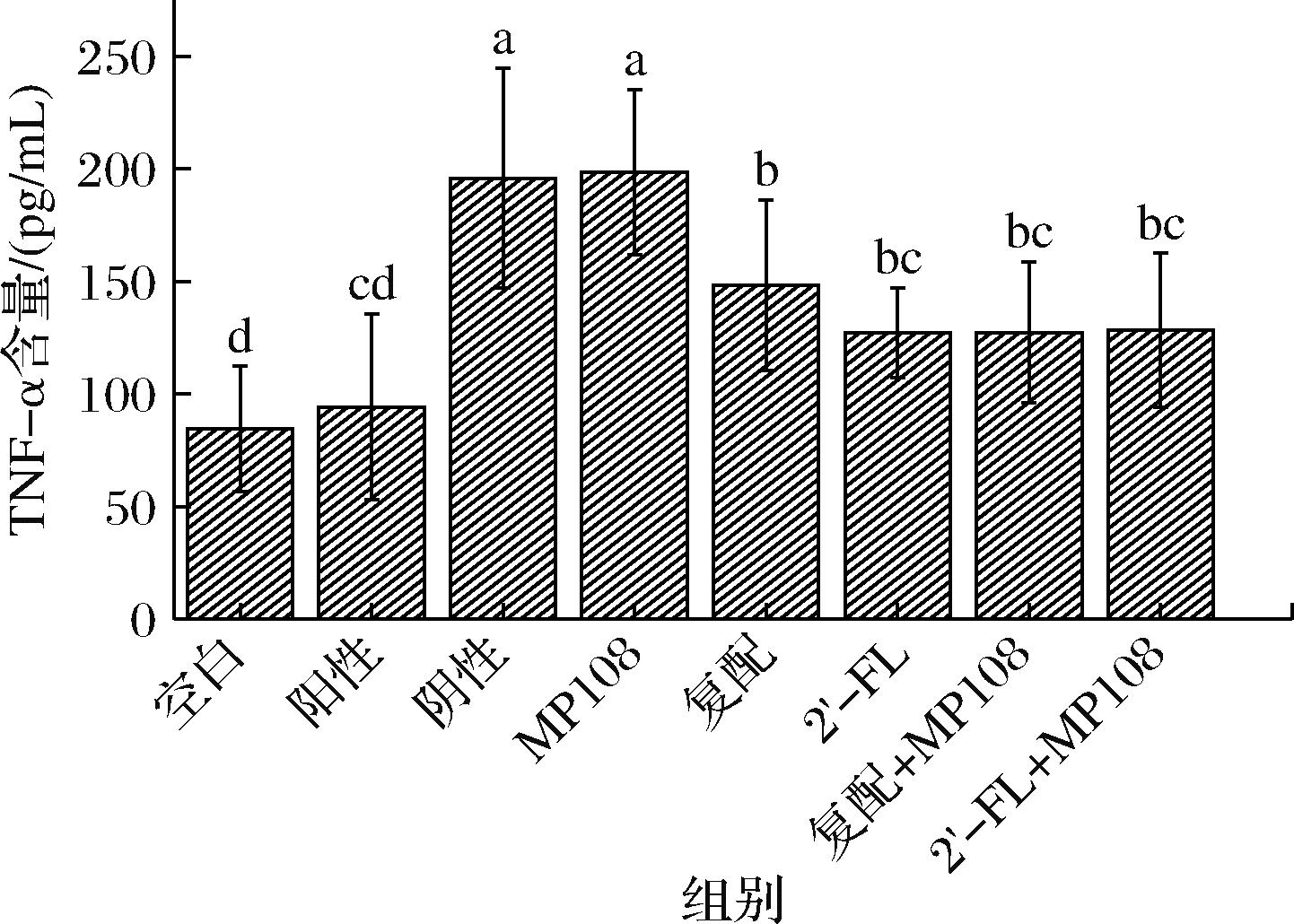
图4 各组别大鼠TNF-α分泌量
Fig.4 TNF-α secretion of rats in each group
IL-2是一种多细胞来源的,具有多向作用的细胞因子,对机体的免疫应答和抗病毒感染等功能具有重要作用[14]。由图5所示,阴性对照组对比空白对照组,IL-2的分泌量明显提高。而阳性对照组则显示药物可以降低IL-2的分泌水平。在实验组中,MP108组无法降低IL-2的分泌量,其分泌量与阴性对照组无显著差异(P>0.05)。而其他组均可以将IL-2的分泌量降低至于阳性对照组相似的水平。这表明MP108的存在与否对于IL-2的分泌量并无影响,低聚糖是影响IL-2分泌量的主要因素。
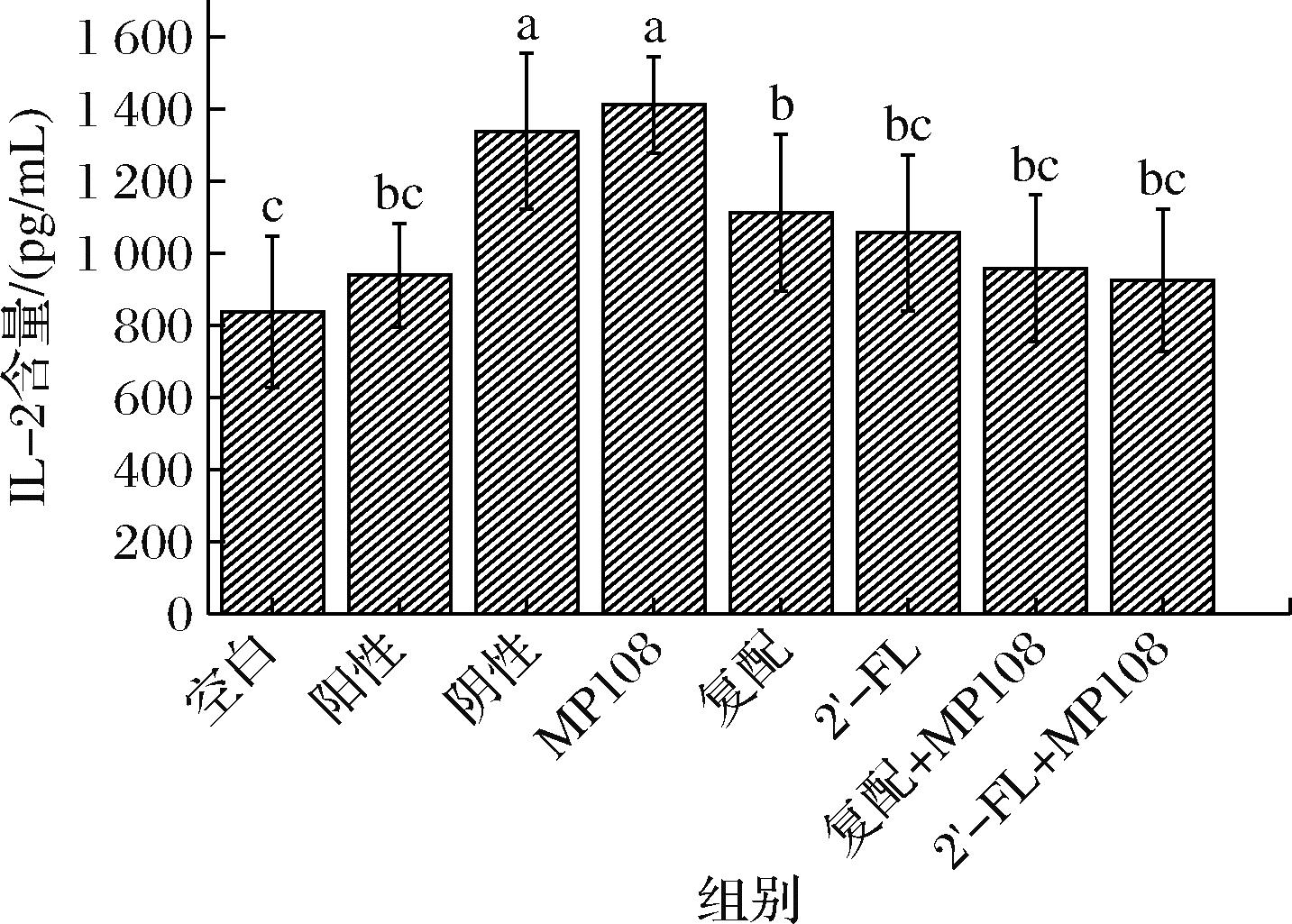
图5 各组别大鼠IL-2分泌量
Fig.5 IL-2 secretion of rats in each group
IL-10是一种常见的,多细胞源的细胞因子,参与免疫反应和炎症反应,是一种较为公认的炎症和免疫抑制因子[15]。由图6可知,空白组、阳性对照组和阴性对照组在IL-10分泌量的数值上无显著性差异(P>0.05),这表明环磷酰胺造模对于本次试验的大鼠并没有改变IL-10分泌量的能力。但是所有干预组相对于空白对照组都出现了IL-10分泌量提高的现象。其中2′-FL组、复配+MP108组和2′-FL+MP108组的提高数值最大,显著高于3个对照组(P<0.05)。
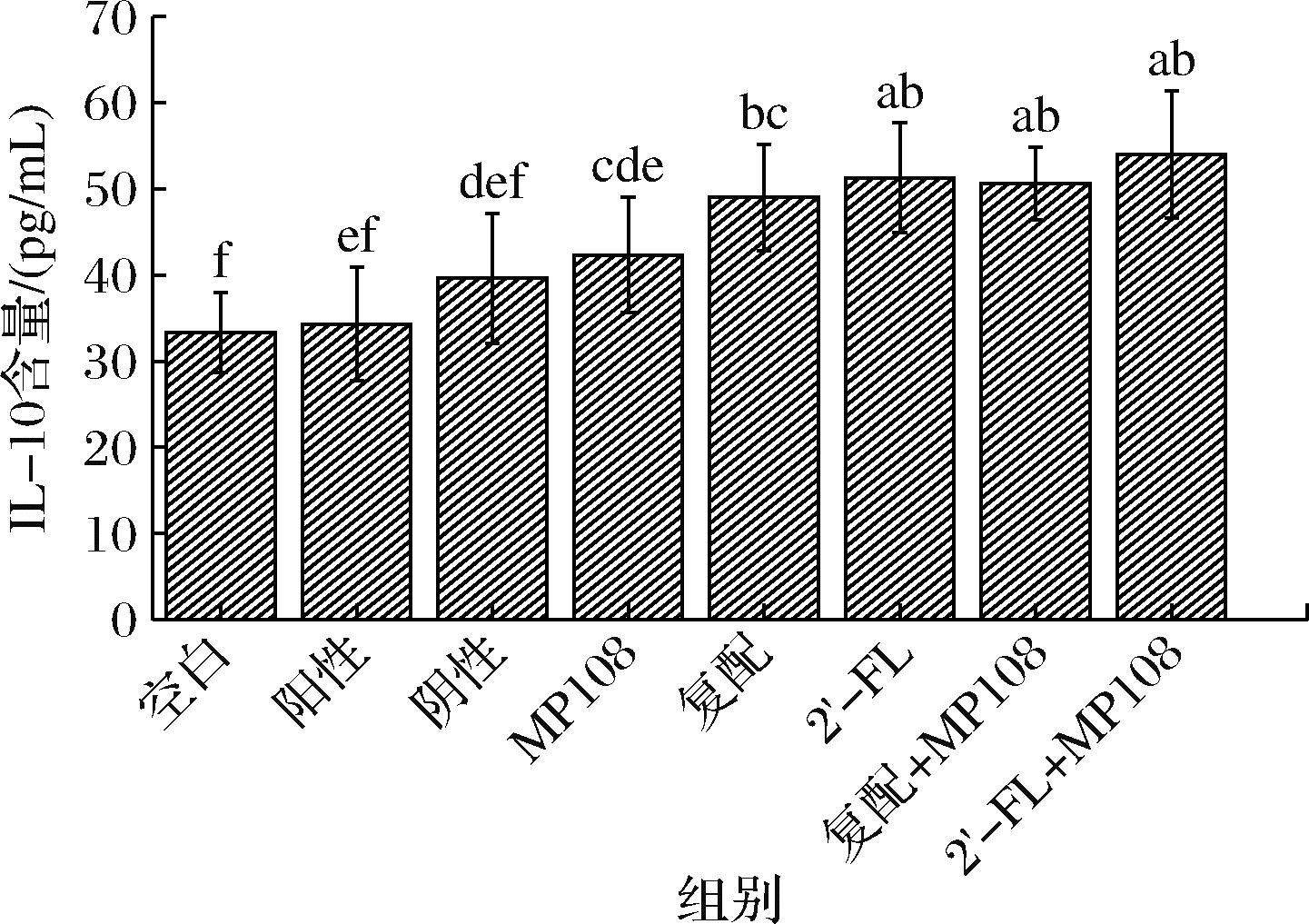
图6 各组别大鼠IL-10分泌量
Fig.6 IL-10 secretion of rats in each group
ZHANG等[16]研究发现,使用沙棘果肉油干预免疫低下小鼠,细胞因子IL-2、IL-4、IL-12和TNF-α都呈现出下降的结果。而XIE等[17]的研究则显示,使用铁皮石槲叶多糖干预的免疫低下小鼠的促炎因子(IL-6、TNF-α等)增加量降低,而抗炎因子IL-10的分泌量提高。KURATA等[18]研究表明,植物乳杆菌的胞外囊泡可以产生对宿主有益的物质,这些物质可以刺激宿主的细胞分泌细胞因子IL-1β、IL-6、IL-10和INF-γ等细胞因子。这与本研究的结果类似,这表明细胞因子会随着大鼠免疫低下症状的缓解而发生变化。
鼠李糖乳酪杆菌MP108和低聚糖对IL-2和TNF-α的调节效果类似,其中2′-FL的调节效果最显著;而MP108和复合低聚糖的调节作用存在协同效果。鼠李糖乳酪杆菌MP108和低聚糖对IL-10均存在上调效果,同样2′-FL的调节效果最显著,而MP108和复合低聚糖的调节作用存在协同效果。
2.3.2 免疫球蛋白分泌情况
IgG是血清和细胞外液中含量最高的免疫球蛋白,在体内分布广泛,是机体抗感染的主力军。可透过胎盘屏障,在新生儿免疫感染的过程中扮演重要角色[19]。由图7可知,空白对照组、阳性对照组和阴性对照组的IgG含量并无显著性差异(P>0.05)。这表明环磷酰胺造模对于IgG含量并无影响。而在干预组中,MP108组和复配+MP108组的IgG含量显著高于空白对照组(P<0.05),这表明这两种干预方式可以提高血清内IgG含量。这说明在存在低聚糖的情况下,MP108可以更好地调节IgG的分泌情况。而单独使用2′-FL对于IgG的分泌并无显著影响(P>0.05)。
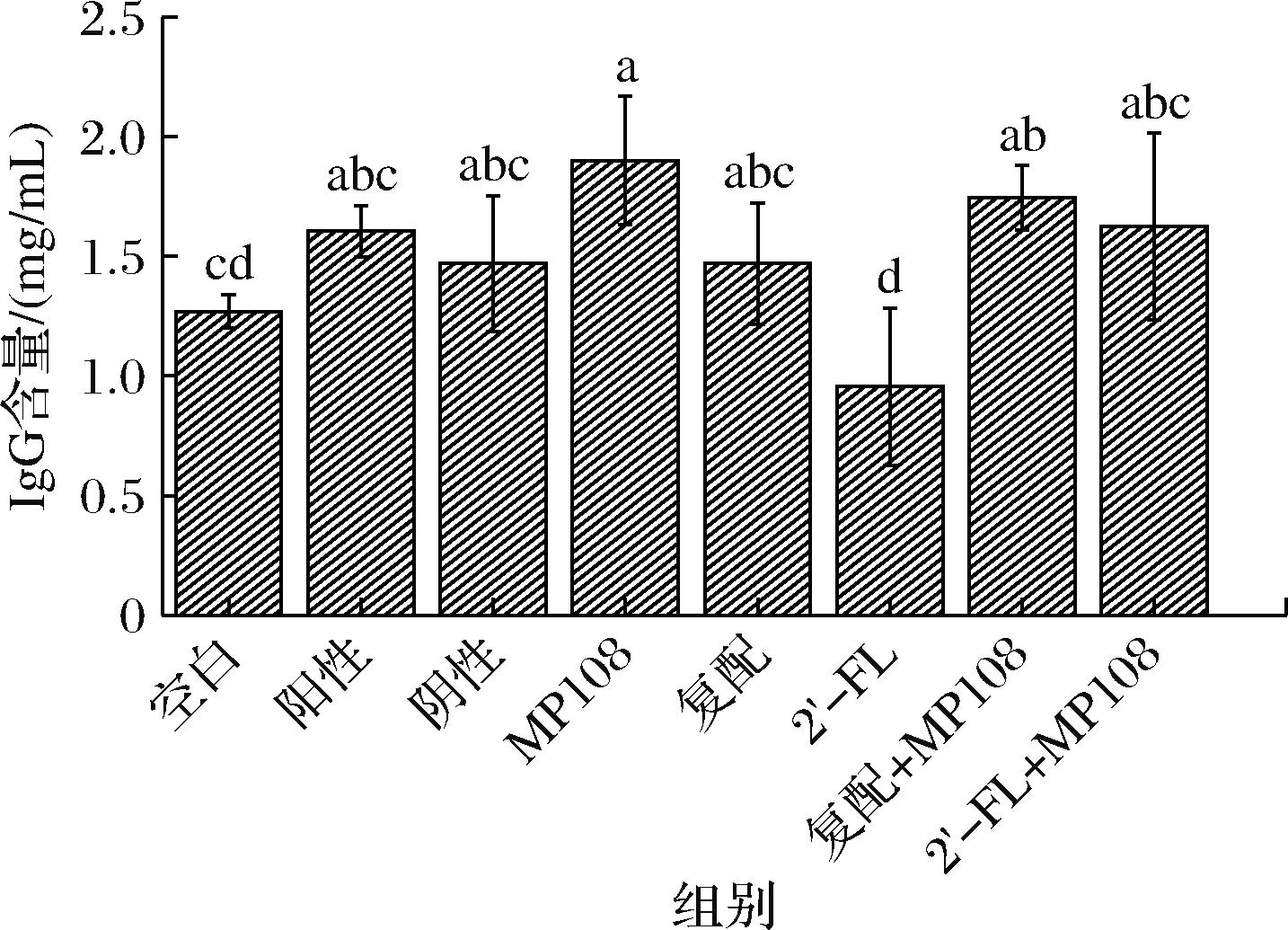
图7 大鼠血清中IgG含量
Fig.7 IgG content in rat serum
IgM是分子质量最大的免疫球蛋白,主要存在于血液中,是个体在发育过程中最早分泌的免疫球蛋白。同时IgM也是体液免疫应答中最早出现的抗体,是机体感染诊断的早期标志性指标[20]。由图8的实验结果显示,所有组别的IgM含量均无显著性差异(P>0.05)。这表明造模与干预均无法影响IgM的含量。
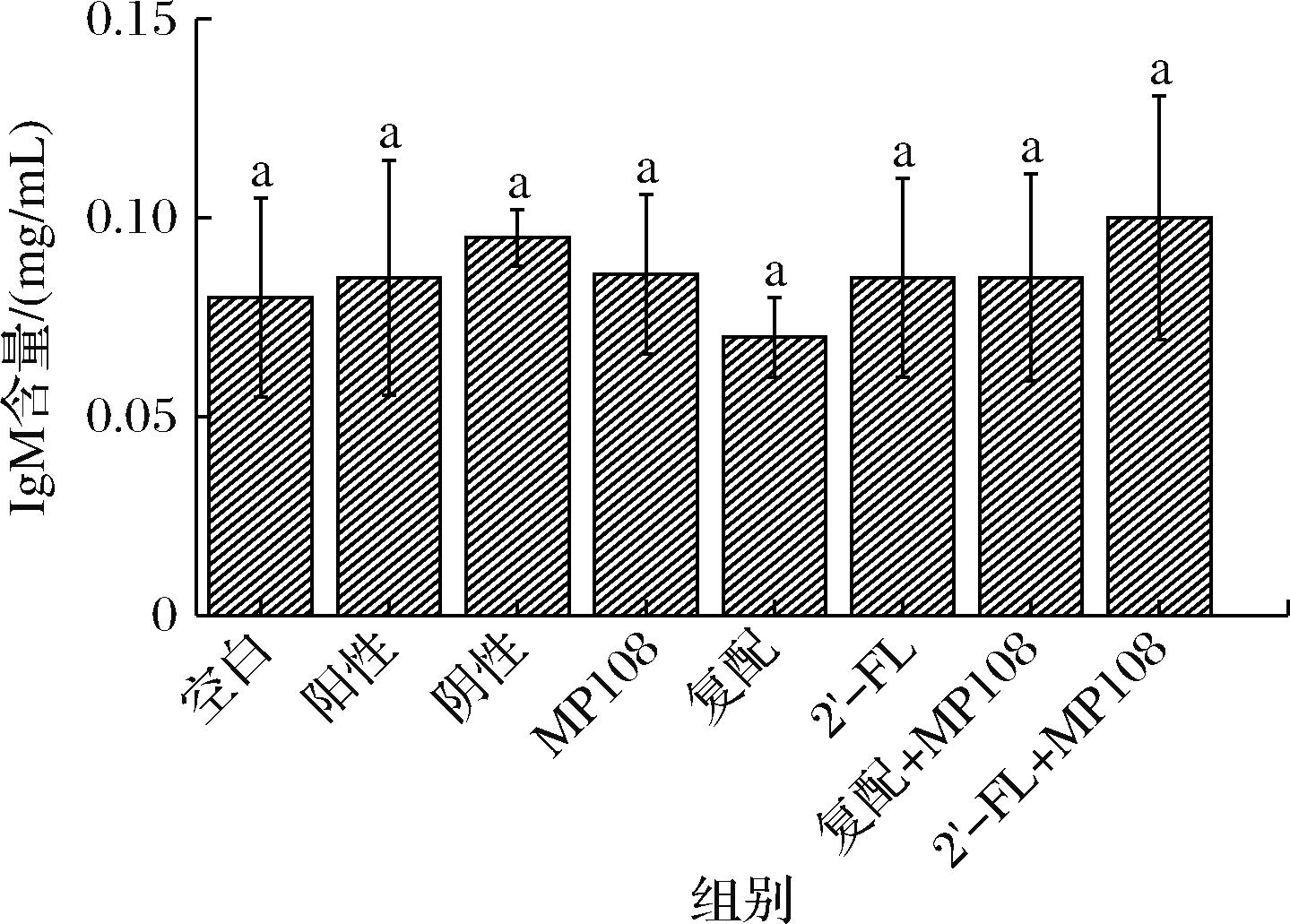
图8 大鼠血清中IgM含量
Fig.8 IgM content in rat serum
免疫球蛋白含量也是反应免疫系统功能的一个重要的指标,许多关于免疫调节的文章都关注过免疫球蛋白的含量。例如SONG等[21]的研究中,发现植物乳杆菌干预后的免疫低下小鼠的IgA、IgG和IgM含量都有提升,同样的现象也出现在WEN等[22]的研究中。这样的结果并没有在本文的研究中观测到,这种现象的出现可能与本研究选择的造模方式有关,SONG等[21]选择的是在实验结束前注射环磷酰胺,检测益生菌对于环磷酰胺造成的损伤的保护作用;而WEN等[22]的造模方式则是在第10天和第30天分别给予环磷酰胺,这可能是因为造模方式的不同导致了研究结果的不同。
3 结论与讨论
在体重变化情况上,所有组的最终体重的增长量均在80~100 g左右,其中只有复配低聚糖组的变化量较小。对于脾脏指数而言,单独使用鼠李糖乳酪杆菌MP108的脾脏指数恢复的较好,只使用低聚糖进行干预的复配低聚糖组和2′-FL组对于脾脏指数的恢复情况则较差。而所有组别的胸腺指数中,2′-FL组和2′-FL+MP108组的胸腺指数可以恢复至与空白对照组相似的水平。研究表明,益生菌对于免疫系统除了直接作用外,也存在着间接改善的途径,例如通过调整肠道菌群改善营养代谢从而间接作用到机体的器官等途径[23]。对于细胞因子而言,2′-FL组、复配+MP108组和2′-FL+MP108组均可以使TNF-α的分泌量恢复至与阳性对照组相似的水平,而除MP108组外的其他组均可以将IL-2的分泌量降低至与阳性对照组相似的水平。所有干预组相对于空白对照组都出现了IL-10分泌量提高的现象,其中2′-FL组、复配+MP108组和2′-FL+MP108组的提高数值最大。益生菌对于免疫因子的调节存在显著的菌株特异性,这种调节一般是间接的,益生菌代谢的产物通过作用于肠道细胞,从而间接改善免疫因子的分泌,而低聚糖可以被益生菌吸收利用,从而产生短链脂肪酸等代谢产物,这些代谢产物是可以调节细胞代谢的生物活性因子,这可能是低聚糖和益生菌对于免疫系统调节的潜在机制[24]。
综上所述,对于各表征指标而言,使用低聚糖和鼠李糖乳酪杆菌MP108进行干预后,可以提高免疫低下大鼠的各项指标的恢复效果。低聚糖在恢复胸腺指数、细胞因子分泌量上具有较好的效果。而鼠李糖乳酪杆菌MP108对脾脏指数的恢复效果较好。在两者共同使用时,脾脏指数,胸腺指数以及各细胞因子的分泌量均呈现了较好的恢复效果,这表明在调节由于环磷酰胺造成的免疫低下的大鼠模型时,复配使用低聚糖和鼠李糖乳酪杆菌MP108具有更好的综合效果。益生菌对于免疫系统调节的作用的机制,一般可以归纳为胞外多糖、酶、细胞碎片和短链脂肪酸等代谢产物的作用。而低聚糖的存在可以影响胞外多糖和短链脂肪酸的分泌,而这可能是益生菌和低聚糖协同作用的机制之一[25]。另外,由于低聚糖的存在,也可以间接促进肠道内的原生菌群的结构趋向有益的方向,这也会使得免疫系统间接受益[26]。
[1] GASBARRINI, GIOVANNI M D, et al.Probiotics history[J].Journal of Clinical Gastroenterology, 2016, 50:116-119.
[2] MCFARLAND L V.From yaks to yogurt:The history, development, and current use of probiotics[J].Clinical Infectious Diseases, 2015, 60(Suppl 2):S85-S90.
[3] OZEN M, DINLEYICI E C.The history of probiotics:The untold story[J].Beneficial Microbes, 2015, 6(2):159-165.
[4] VANDERPOOL C, YAN F, POLK D B.Mechanisms of probiotic action:Implications for therapeutic applications in inflammatory bowel diseases[J].Inflammatory Bowel Diseases, 2008, 14(11):1585-1596.
[5] 解读《关于β-1,3/α-1,3-葡聚糖等6种“三新食品”的公告》(2021年第5号)[J].中国食品卫生杂志, 2021, 33(3):350-368.Interpretation of the announcement on six kinds of “Three New Foods” including β-1,3/α-1,3-glucan (No.5 of 2021)[J].Chinese Journal of Food Hygiene, 2021, 33(3):350-368.
[6] RASTALL R A, GIBSON G R.Recent developments in prebiotics to selectively impact beneficial microbes and promote intestinal health[J].Current Opinion in Biotechnology, 2015, 32:42-46.
[7] RASTALL R A.Functional oligosaccharides:Application and manufacture[J].Annual Review of Food Science and Technology, 2010, 1:305-339.
[8] LYU L X, MU D G, DU Y L, et al.Mechanism of the immunomodulatory effect of the combination of live Bifidobacterium, Lactobacillus, Enterococcus, and Bacillus on immunocompromised rats[J].Frontiers in Immunology, 2021, 12:694344.
[9] ALJUTAILY T.Evaluating the nutritional and immune potentiating characteristics of unfermented and fermented turmeric camel milk in cyclophosphamide-induced immunosuppression in rats[J].Antioxidants, 2022, 11(4):792
[10] 宋翔, 侯玉凤, 陈晓雯.1株具有免疫增强功能的乳酸菌筛选及其免疫效果评价[J].畜牧与兽医, 2022, 54(1):49-54.SONG X, HOU Y F, CHEN X W.Screening of a strain of lactic acid bacterium with immune enhancing function and evaluation on its immune effect[J].Animal Husbandry &Veterinary Medicine, 2022, 54(1):49-54.
[11] MA W W, LI W W, YU S, et al.Immunomodulatory effects of complex probiotics on the immuno-suppressed mice induced by cyclophosphamide[J].Frontiers in Microbiology, 2023, 14:1055197.
[12] MENG Y Y, LI B L, JIN D, et al.Immunomodulatory activity of Lactobacillus plantarum KLDS1.0318 in cyclophosphamide-treated mice[J].Food &Nutrition Research, 2018, 62:62.
[13] IDRISS H T, NAISMITH J H.TNF alpha and the TNF receptor superfamily:Structure-function relationship(s)[J].Microscopy Research and Technique, 2000, 50(3):184-195.
[14] ABBAS A K, TROTTA E, SIMEONOV D R, et al.Revisiting IL-2:Biology and therapeutic prospects[J].Science Immunology, 2018, 3(25):eaat1482.
[15] SARAIVA M, O’GARRA A.The regulation of IL-10 production by immune cells[J].Nature Reviews.Immunology, 2010, 10(3):170-181.
[16] ZHANG J, ZHOU H C, HE S B, et al.The immunoenhancement effects of sea buckthorn pulp oil in cyclophosphamide-induced immunosuppressed mice[J].Food &Function, 2021, 12(17):7954-7963.
[17] XIE H L, FANG J Y, FARAG M A, et al.Dendrobium officinale leaf polysaccharides regulation of immune response and gut microbiota composition in cyclophosphamide-treated mice[J].Food Chemistry:X, 2022, 13:100235.
[18] KURATA A, KIYOHARA S, IMAI T, et al.Characterization of extracellular vesicles from Lactiplantibacillus plantarum[J].Scientific Reports, 2022, 12(1):13330.
[19] WAHN V, VON BERNUTH H.IgG subclass deficiencies in children:Facts and fiction[J].Pediatric Allergy and Immunology.2017, 28(6):521-524.
[20] KHWAJA J, D’SA S, MINNEMA M C, et al.IgM monoclonal gammopathies of clinical significance:Diagnosis and management[J].Haematologica, 2022, 107(9):2037-2050.
[21] SONG Y L, SUN M Y, MA F L, et al.Lactiplantibacillus plantarum DLPT4 protects against cyclophosphamide-induced immunosuppression in mice by regulating immune response and intestinal flora[J].Probiotics and Antimicrobial Proteins, 2024, 16(2):321-333.
[22] WEN J, MA L, XU Y J, et al.Effects of probiotic Litchi juice on immunomodulatory function and gut microbiota in mice[J].Food Research International, 2020, 137:109433.
[23] YAN F, POLK D B.Probiotics and immune health[J].Current Opinion in Gastroenterology, 2011, 27(6):496-501.
[24] KANG H J, IM S H.Probiotics as an immune modulator[J].Journal of Nutritional Science and Vitaminology, 2015, 61 Suppl:S103-S105.
[25] ![]() J, MARZEC A, RUSZCZY
J, MARZEC A, RUSZCZY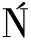 SKI M, et al.Postbiotics-a step beyond pre- and probiotics[J].Nutrients, 2020, 12(8):2189.
SKI M, et al.Postbiotics-a step beyond pre- and probiotics[J].Nutrients, 2020, 12(8):2189.
[26] MARKOWIAK P,  LIZ·EWSKA K.Effects of probiotics, prebiotics, and synbiotics on human health[J].Nutrients, 2017, 9(9):1021.
LIZ·EWSKA K.Effects of probiotics, prebiotics, and synbiotics on human health[J].Nutrients, 2017, 9(9):1021.