随着肥胖人口的迅速增加,肥胖已成为一个全球性问题,它通常被认为是各种疾病的危险因素,如糖尿病和心血管疾病[1]。肥胖症的形成,很大程度上是由不健康的饮食习惯和生活方式引起的,特别是长期过量摄入高脂膳食。胰脂肪酶(pancreatic lipase,PL)是脂肪消化吸收过程的关键酶,抑制胰脂肪酶的活性可以减少人体对脂肪的吸收[2],因此,通过抑制胰脂肪酶活性来降低脂肪的消化和吸收,是抑制肥胖的有效方法。然而,目前临床常用的减肥降脂药物如奥利司他、利拉鲁肽、他汀类药物等对人体具有一定的副作用,包括胃肠道不良反应、油性粪便、粪便急迫和油性斑点等[3],因而限制了其广泛应用。因此,开发天然高效、无毒副作用的新型胰脂肪酶抑制剂已成为近年来的研究热点之一。
目前,常见天然来源的胰脂肪酶抑制剂包括黄酮类、皂苷类、萜类、生物碱等活性物质[4]。花色苷是一种类黄酮物质,广泛分布于深色谷物、浆果及蔬菜中,可赋予其红、蓝、紫等色调[5]。研究发现,花色苷具有抗氧化、抗炎症、降血糖及降血脂[6-7]等多种功能。然而,花色苷的稳定性较差,其应用容易受到一些物理或化学因素的限制,例如pH、氧气、温度和金属离子等[8]。随着对海洋生物资源研究的不断深入,海洋生物活性肽因其良好的天然活性、安全性以及高效性而受到广泛关注[9]。研究表明,牡蛎肽具有降血糖、免疫调节、降血脂及抗疲劳[10-12]等多种生物活性功能,但因其消化稳定性差的问题,极大地限制了活性肽的活性发挥。近些年,文献研究报道黄酮类物质与蛋白质的相互作用具有提高二者稳定性、促进其活性发挥的优势[13-15]。因此,将牡蛎肽与花色苷协同组装成复合物具有保护二者活性结构、协同增强胰脂肪酶抑制活性的潜力。但目前对于牡蛎肽和花色苷协同抑制胰脂肪酶活性及探究二者相互作用的研究鲜有报道。
本研究以牡蛎肽-花色苷复合物为研究对象,探讨不同比例下牡蛎肽和花色苷的协同复合物对脂肪酶活性的影响,并探索牡蛎肽和花色苷之间的相互作用,从互作角度解析牡蛎肽和花色苷抑制胰脂肪酶的增效作用。研究结果可为阐明牡蛎肽和花色苷协同降脂作用机制及相关减肥降脂功能食品的开发利用提供理论依据和科学指导。
1 材料与方法
1.1 材料与试剂
试验用新鲜牡蛎肉,广东省湛江市水产品批发市场;桑葚花色苷,陕西沐凡生物科技有限公司;碱性蛋白酶(≥200 000 U/g),北京索莱宝科技有限公司;胰脂肪酶(猪胰,35 U/mg)、奥利司他和对硝基棕榈酸苯酯(p-nitrophenyl palmitate, p-NPP),上海麦克林生化科技有限公司;Tris三(羟甲基)氨基甲烷,北京索莱宝科技有限公司;KBr,上海易恩化学技术有限公司;盐酸、NaOH及其他试剂均为分析纯。
1.2 仪器与设备
FA2004B电子天平,上海高致精密仪器有限公司;LGJ-18冷冻干燥机,北京松源华兴科技发展公司;MT4-FE28-METER pH计,梅特勒-托利多仪器有限公司;Sorvall LYNX 6000高速落地离心机、Varioskan LUX全自动酶标仪,美国Thermo公司;SHJ-6AB磁力搅拌水浴锅,常州金坛良友仪器公司;LC-JSY-3恒温金属浴,上海力辰仪器科技有限公司;Cary 60紫外可见-分光光度计,安捷伦科技有限公司;RF-5301PC荧光分光光度计,日本岛津公司;Bruker Tensor 27傅里叶红外光谱仪,德国Bruker公司。
1.3 方法
1.3.1 牡蛎肽的制备
参考柏昌旺等[16]的方法并稍作修改,新鲜牡蛎开壳取肉并洗净,按料液比1∶3(g∶mL)加水匀浆,调节pH值至9。8 000 r/min均质2 min,加入2%(质量分数)碱性蛋白酶后于50 ℃水浴酶解3 h,沸水浴灭酶10 min。快速冷却至室温,4 ℃,8 000 r/min离心15 min,收集上清液并冷冻干燥。
1.3.2 牡蛎肽和花色苷协同复合物的制备
分别用超纯水配制质量浓度为3.2 mg/mL的牡蛎肽、花色苷溶液,并稀释至合适浓度,分别吸取样品溶液至2 mL离心管,使混合溶液中牡蛎肽∶花色苷=4∶1、2∶1、1∶1、1∶2、1∶4(浓度比),充分振荡混匀后,于25 ℃、1 000 r/min下反应2 h获得牡蛎肽-花色苷复合物。
1.3.3 牡蛎肽和桑葚花色苷的胰脂肪酶抑制活性测定
参考GUTIÉRREZ-GRIJALVA等[17]的方法,将提取出的牡蛎肽和桑葚花色苷按梯度浓度溶于超纯水中,配制成一系列浓度梯度的样品溶液,取100 μL样品溶液和100 μL脂肪酶溶液(0.35 U/mL)于2 mL离心管中混匀,补充Tris-HCl缓冲溶液(pH=8.0)至350 μL,于37 ℃下水浴10 min,再加入50 μL 1 mg/mL 的p-NPP底物于37 ℃下水浴20 min。最后取200 μL反应后的溶液于96孔板中,在405 nm处测定吸光度值,并根据公式(1)计算抑制率。实验设置样品组、样品空白组、对照组和空白组。
胰脂肪酶抑制率![]()
(1)
式中:A1,样品组吸光度;A2,样品空白组吸光度;B1,对照组吸光度;B2,空白组吸光度。
1.3.4 牡蛎肽协同花色苷抑制胰脂肪酶活性的增效作用分析
1.3.4.1 牡蛎肽和花色苷抑制胰脂肪酶的协同浓度区域筛选
参考蒋美龄等[10]的方法并稍作修改,设计牡蛎肽与花色苷的样品剂量协同矩阵,根据矩阵对应的样品浓度进行脂肪酶抑制活性测定,利用Synergy Finder软件的最高单药(highest single agent,HSA)和零相互作用效力(zero interaction potency,ZIP)协同评分模型分析两者在不同浓度下的协同抑制胰脂肪酶能力。HSA模型表示预期的联合效应等于单个药物的更高效应,任何高于单个药物处理的额外效应都表示为HSA的协同作用;ZIP模型通过比较单个药物及其组合之间剂量-反应曲线的效力(在一定剂量水平下的作用)的变化来捕获药物相互作用关系[18]。采用HSA模型和ZIP模型计算得到Synergy score(δ),δ>10、δ<-10及-10<δ<10分别表示药物组合具有协同、拮抗和加和作用[19]。
1.3.4.2 牡蛎肽和花色苷抑制胰脂肪酶的协同比例优化
根据Synergy Finder筛选出来协同度最高的区域,利用Compusyn软件进一步探究此区域下不同浓度比例牡蛎肽-花色苷复合物(4∶1、2∶1、1∶1、1∶2、1∶4)的协同效果。根据Chou和Talalay提出的中效原理确定联合指数(combination index,CI),通过CI值定量判断复合物单组分间的相互作用强度以及性质。CI<1被认为是协同作用,CI=1被认为是加和作用,CI>1被认为是拮抗作用;CI值越低,表明组合的协同潜力越强[20]。
1.3.5 牡蛎肽、花色苷及其协同复合物的酶抑制动力学研究
设定p-NPP的质量浓度为1 mg/mL,以不添加和添加抑制剂牡蛎肽(0、0.8、2 mg/mL)、花色苷(0、1.6、3.2 mg/mL)及复合物(0、2、2.4 mg/mL)为实验条件,测定不同酶浓度下(0.05、0.15、0.25、0.35、0.45 U/mL)的吸光值,以酶浓度为横坐标,反应速率(V)为横坐标,绘制曲线判断抑制剂对胰脂肪酶的可逆作用。
设定胰脂肪酶溶液浓度为0.35 U/mL,以不添加和添加抑制剂牡蛎肽(0、0.6、1 mg/mL)、花色苷(0、0.8、2 mg/mL)以及复合物(0、1.2、2 mg/mL)为实验条件,测定不同p-NPP浓度下(0.6、0.8、1、1.2、1.4 mg/mL)的吸光值,以底物浓度的倒数(1/S)为横坐标,反应速率的倒数(1/V)为纵坐标,绘制Lineweaver-Burk曲线,并根据Lineweaver-Burk方程判断抑制剂对胰脂肪酶的抑制类型。
1.3.6 牡蛎肽和花色苷的相互作用研究
1.3.6.1 紫外-可见吸收光谱分析
固定浓度的牡蛎肽(1 mg/mL)分别与不同浓度的花色苷(0.1~1 mg/mL)复合来制备样品,使用紫外可见分光光度计测量牡蛎肽与复合物的紫外-可见吸收光谱,波长范围为190~600 nm。
1.3.6.2 傅里叶变换红外光谱(Fourier transform infrared spectroscopy, FT-IR)分析
精确称取1 mg真空冷冻干燥后的牡蛎肽、花色苷以及复合物样品,与100 mg KBr混合后研磨压片,采用KBr压片法测定红外光谱,扫描波长4 000~400 cm-1,扫描次数32次。
1.3.6.3 荧光光谱分析
内源荧光光谱:通过将固定质量浓度的牡蛎肽(1 mg/mL)分别与不同质量浓度的花色苷(0.04~0.6 mg/mL)复合来制备样品,设置样品的发射信号采集范围为300~500 nm,激发波长为280 nm,激发和发射狭缝宽度均为5.0 nm。
同步荧光光谱:样品浓度保持不变,Δλ分别设置为15、60 nm时,记录发射波长为280~400 nm的荧光光谱。
1.4 数据处理
所得数据均用“平均值±标准差”表示,运用Excel和SPSS 27.0软件进行数据处理和方差分析(One-way ANOVA),差异显著性采用Duncan分析并进行多重比较,P<0.05表示差异显著且具有统计学意义。使用Origin Pro 2021软件处理和生成图像。
2 结果与分析
2.1 牡蛎肽和桑葚花色苷对胰脂肪酶的抑制活性
胰脂肪酶在脂代谢中起关键作用,人体摄入膳食脂肪后,必须经脂肪酶水解后才能吸收,因此,抑制胰脂肪酶活性可进一步抑制人体对脂肪的吸收利用[2]。由图1-a可知,牡蛎肽对胰脂肪酶具有显著的抑制能力,随着浓度的增加,牡蛎肽对胰脂肪酶的抑制率也随之升高,呈现剂量浓度效应,其IC50值为(1.35±0.02) mg/mL。由图1-b可知,随着浓度的增加,桑葚花色苷对胰脂肪酶的抑制率也随之增强,其IC50值为(3.54±0.06) mg/mL。韩鹏薇等[21]采用酶解法制备的克氏原螯虾壳蛋白水解物对胰脂肪酶具有较好的抑制能力,其IC50值(4.71±1.12) mg/mL。陈浩南等[22]制备的高良姜水提物对胰脂肪酶具有一定的抑制效果,其IC50值为543.51 mg/mL。与上述研究相比,本研究制备的牡蛎肽以及桑葚花色苷对胰脂肪酶的抑制活性更强,说明其在减肥降脂作用方面具有良好的应用前景。
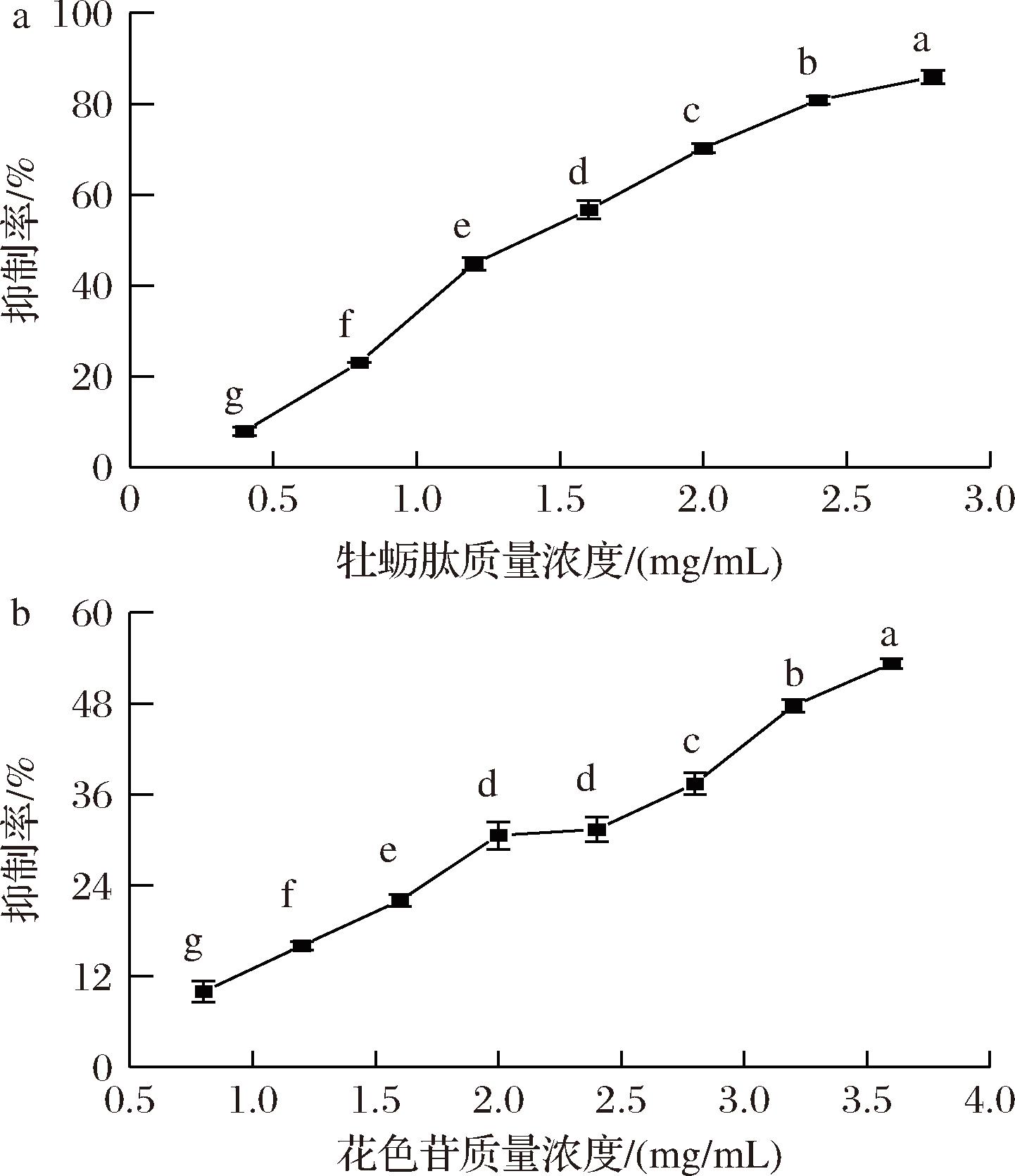
a-牡蛎肽;b-桑葚花色苷
图1 牡蛎肽和桑葚花色苷对胰脂肪酶的抑制能力
Fig.1 The inhibitory abilities of oyster peptides and mulberry anthocyanins against pancreatic lipase
注:不同小写字母表示差异显著(P<0.05)。
2.2 牡蛎肽协同花色苷抑制胰脂肪酶的活性增效作用
2.2.1 牡蛎肽和花色苷抑制胰脂肪酶的协同浓度区域筛选
本研究同时采用HSA和ZIP两种协同计算模型评价牡蛎肽和花色苷抑制胰脂肪酶的协同作用,并对其协同浓度范围进行筛选。由图2可知,当牡蛎肽和花色苷复合后,其ZIP模型整体协同得分(δ)为7.899,HSA模型整体协同得分(δ)为11.412,说明二者复合后存在一定的协同作用。其中,牡蛎肽和花色苷质量浓度在0.8~3.2 mg/mL时,ZIP协同评分(δ)为11.208(δ>10),HSA协同评分为(δ)为17.781(δ>10),此时二者达到强协同效果。综上,ZIP模型和HSA模型均显示出牡蛎肽和花色苷对胰脂肪酶具有协同抑制作用,且质量浓度为0.8~3.2 mg/mL时,牡蛎肽和花色苷对胰脂肪酶具有显著的协同抑制增效作用。

a-ZIP模型整体协同得分;b-ZIP模型最佳协同区域协同得分; c-HSA模型整体协同得分;d-HSA模型最佳协同区域协同得分
图2 牡蛎肽和花色苷对胰脂肪酶的协同抑制作用评分图
Fig.2 The score chart of the synergistic inhibitory effect of oyster peptides and anthocyanins against pancreatic lipase
2.2.2 不同比例下牡蛎肽和花色苷协同复合物对胰脂肪酶的抑制能力
由图3可知,不同浓度比例的牡蛎肽和花色苷(4∶1、2∶1、1∶1、1∶2、1∶4)协同复合物对胰脂肪酶均具有良好的抑制能力,且随着浓度的增加,其抑制率也逐渐增强,呈剂量依赖性。不同浓度比例的牡蛎肽和花色苷对胰脂肪酶的抑制能力强弱顺序为4∶1[IC50=(1.80±0.02) mg/mL]>2∶1[IC50=(2.00±0.06) mg/mL]>1∶1[IC50=(2.11±0.03) mg/mL]>1∶2[IC50=(2.56±0.04) mg/mL]>1∶4[IC50=(2.69±0.08) mg/mL],其中牡蛎肽∶花色苷=4∶1(浓度比)时对胰脂肪酶的抑制能力最强。尽管不同比例下复合物的IC50值没有高于单独的牡蛎肽(1.35 mg/mL),但均显著强于单独的花色苷(3.54 mg/mL)(P<0.05)。通过进一步对比分析单独的牡蛎肽和花色苷,与不同比例下牡蛎肽和花色苷协同复合物发挥胰脂肪酶抑制活性时肽和花色苷的用量发现,当胰脂肪酶抑制率相同时,协同复合物中牡蛎肽和花色苷的用量显著低于发挥相同胰脂肪酶抑制效果的单独牡蛎肽和花色苷:当牡蛎肽和花色苷比例为4∶1、2∶1、1∶1、1∶2、1∶4时的协同复合物达到半数抑制浓度时,花色苷在复合物中的用量分别为0.36、0.67、1.06、1.71、2.15 mg/mL,与单独使用花色苷用量相比有显著下降(P<0.05),分别减少了89.83%、81.07%、70.06%、51.69%、39.27%;当浓度比例为1∶1、1∶2、1∶4的复合物达到半数抑制浓度时,牡蛎肽在复合物中的用量分别为1.06、0.85、0.54 mg/mL,与单独使用牡蛎肽用量相比有显著下降(P<0.05),分别减少了21.48%、37.04%、60.00%。蒋美龄等[10]研究发现,牡蛎肽-花色苷复合物体外胃肠模拟消化后对DPP-Ⅳ酶、α-淀粉酶的抑制率与牡蛎肽相比有显著提高,复合物间形成了较稳定的体系,可对抗复杂的模拟消化环境,保护了牡蛎肽和花色苷的降糖活性。以上结果说明牡蛎肽与花色苷协同复合后,二者的稳定性可能得到了显著增强,导致其活性保留率得到提升。苏小洁等[23]研究发现合成肽(FPVGR, FR-5)与花色苷组装成复合物后,复合物的IC50值虽高于单独的花色苷,但合成肽FR-5可通过非共价作用力与花色苷发生相互作用,提高花色苷抵抗不良环境因子的能力,通过增强花色苷稳定性提高了其活性保留率。综上,复合物(1∶1、1∶2、1∶4)中牡蛎肽与花色苷的用量与单独使用相比均有显著下降(P<0.05),具有达到减少用量,提高稳定性,起到活性增效作用的潜力。
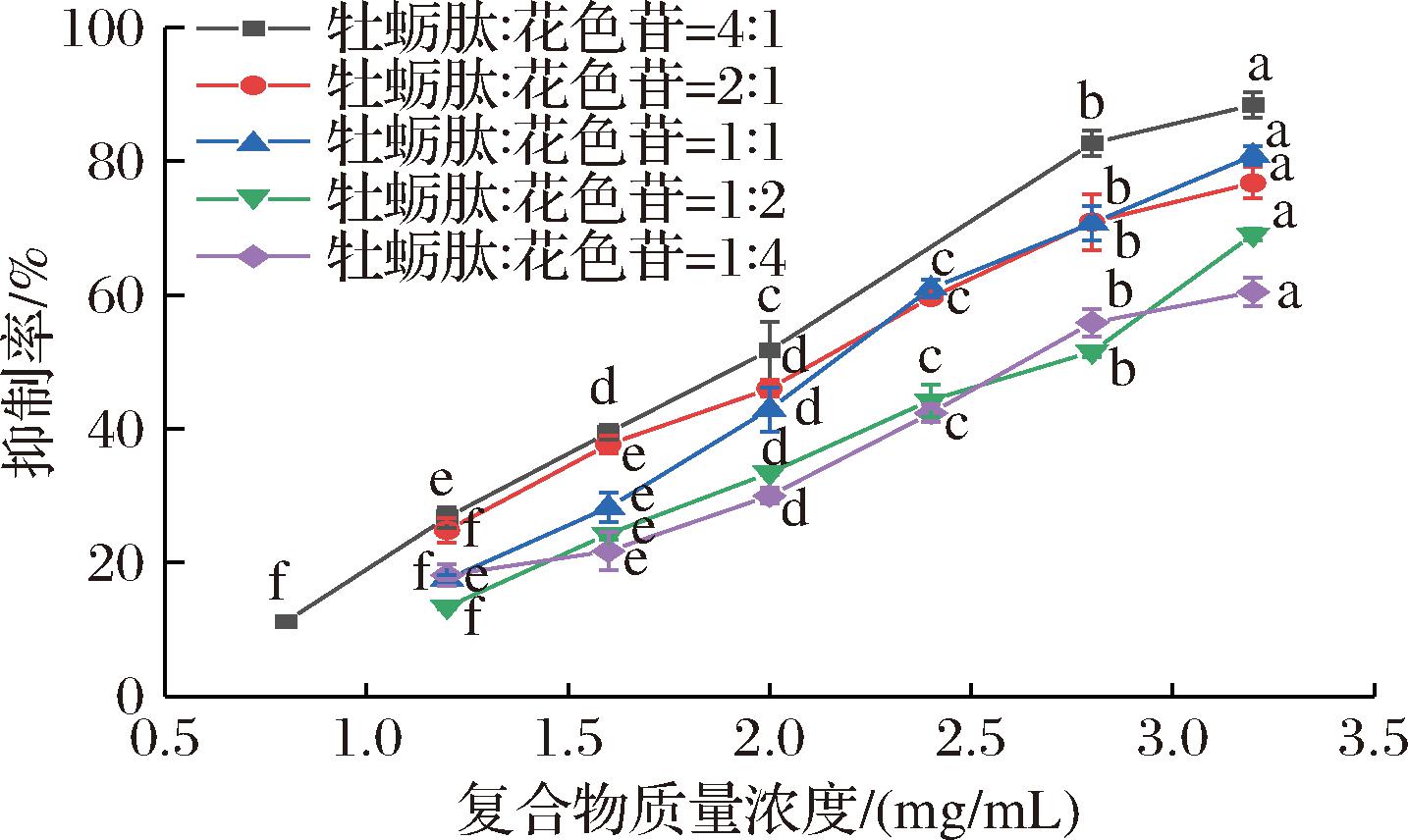
图3 不同浓度比例牡蛎肽-花色苷协同复合物 对胰脂肪酶的抑制能力
Fig.3 The inhibitory effect of oyster peptide-anthocyanin synergistic complexes against pancreatic lipase at different concentration ratios
注:图中小写字母表示同一浓度比例复合物中不同 浓度间的显著性分析(P<0.05)。
2.2.3 不同比例牡蛎肽和花色苷协同抑制胰脂肪酶CI与剂量减少指数(dose-reduction index,DRI)分析
DRI是用来衡量两种或多种活性物质在相同作用水平下协同使用时比单独使用时每种物质剂量减少多少倍的指数,DRI越大意味着相同治疗效果下剂量减少越多;而CI则是用来评价物质之间的协同作用,CI值越小,意味着两者之间的协同作用越强[23]。由图4可知,不同浓度比例下牡蛎肽和花色苷协同复合物的CI均随着浓度的增加而逐渐减小,且不同浓度比例的复合物(4∶1、2∶1、1∶1、1∶2、1∶4)分别在抑制效果(Fa)≥0.75、Fa≥0.97、Fa≥0.65、Fa≥0.7、Fa≥0.55时,对应的CI小于1,表明此时不同浓度比例的牡蛎肽和花色苷均具有一定的协同作用。结合DRI图分析,当牡蛎肽∶花色苷=1∶1、1∶2、1∶4时,牡蛎肽和花色苷的DRI均大于1,且随Fa的增大而增大,说明在这些比例下联合使用可以减少牡蛎肽和花色苷的使用剂量。同时由表1可知,当牡蛎肽:花色苷=1∶1,其Fa=50/75/90/95时,对应的CI值为1.085 47、0.888 44、0.733 93、0.647 52,明显低于其他比例,说明相较于其他比例而言,此比例下牡蛎肽和花色苷对胰脂肪酶的协同抑制效果最强。综上,不同比例(4∶1、2∶1、1∶1、1∶2、1∶4)的牡蛎肽和花色苷均有一定的协同增效作用,其中牡蛎肽∶花色苷=1∶1时,其协同增效作用最强。同时由以上结果推测,牡蛎肽与花色苷协同时二者之间的相互作用可能受到其复合比例影响,复合比例会影响肽与花色苷的结合位点,进而影响牡蛎肽-花色苷复合物的结构和性质,导致其对胰脂肪酶的抑制能力不同[13,15]。有研究也报道过类似结果,黄淋[24]测定核桃蛋白肽(FQ)、绿原酸(chlorogenic acid, CA)以及不同摩尔比FQ和CA组合下的乙酰胆碱酯酶(acetylcholinesterase, AChE)抑制活性,结果显示当FQ与CA的摩尔比为4∶1时,其对AChE的抑制表现出最强协同作用,说明复合物之间的比例会影响其抑制活性。
表1 不同浓度比例牡蛎肽-花色苷协同复合物的CI值
Table 1 CI values of oyster peptide-anthocyanin synergistic complexes at different concentration ratios
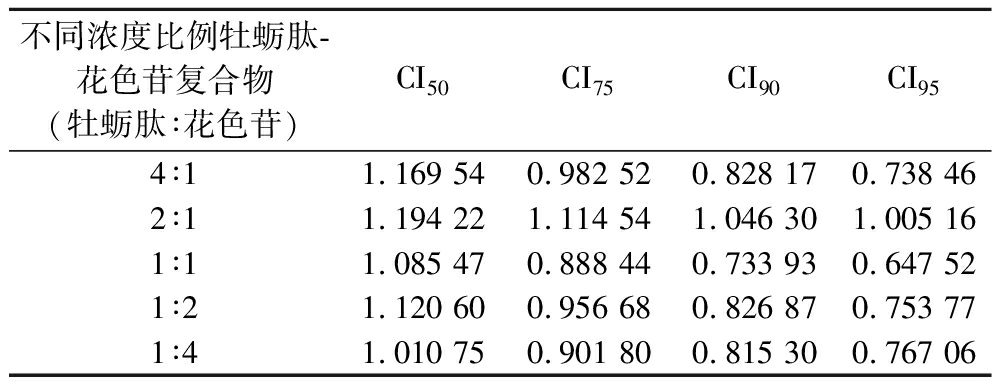
不同浓度比例牡蛎肽-花色苷复合物(牡蛎肽∶花色苷)CI50CI75CI90CI954∶11.169 540.982 520.828 170.738 462∶11.194 221.114 541.046 301.005 161∶11.085 470.888 440.733 930.647 521∶21.120 600.956 680.826 870.753 771∶41.010 750.901 800.815 300.767 06

A1-牡蛎肽∶花色苷=4∶1联合指数图;A2-牡蛎肽∶花色苷=2∶1联合指数图;A3-牡蛎肽∶花色苷=1∶1联合指数图;A4-牡蛎肽∶花色苷=1∶2联合指数图;A5-牡蛎肽∶花色苷=1∶4联合指数图;B1-牡蛎肽∶花色苷=4∶1剂量减少指数图;B2-牡蛎肽∶花色苷=2∶1剂量减少指数图; B3-牡蛎肽∶花色苷=1∶1剂量减少指数图;B4-牡蛎肽∶花色苷=1∶2剂量减少指数图;B5-牡蛎肽∶花色苷=1∶4剂量减少指数图
图4 牡蛎肽和花色苷协同复合物的CI图与DRI图
Fig.4 The CI and DRI of oyster peptide-anthocyanin synergistic complexes
2.3 牡蛎肽、花色苷及其协同复合物的酶抑制动力学分析
酶抑制类型可根据抑制剂与酶结合位点的结合方式分成可逆性和不可逆性两种。由图5可知,不同浓度的抑制剂样品:牡蛎肽、花色苷及其协同复合物的直线均近似过原点,且随着浓度的增加,其斜率逐渐减小,说明牡蛎肽、花色苷及其复合物对胰脂肪酶的抑制类型均为可逆性抑制[18]。通过Lineweaver-Burk双倒数曲线图可判断抑制剂对酶的抑制类型,由图6可知,牡蛎肽、花色苷及其复合物的双倒数曲线表现出良好的线性关系,如图6-a所示,随着牡蛎肽浓度的增加,最大反应速率(Vm)减小,米氏常数(Km)增大,双倒数曲线交于第二象限上一点,说明牡蛎肽对胰脂肪酶的抑制类型为非竞争性和竞争性混合型抑制,即牡蛎肽既能通过竞争性抑制作用与胰脂肪酶结合,也能通过非竞争性抑制作用与胰脂肪酶-底物复合物结合[25]。同时由表2可知,牡蛎肽对胰脂肪酶的抑制常数(Ki:0.458 2 mg/mL)<对胰脂肪酶-底物复合物的抑制常数(Kis:7.804 9 mg/mL),说明牡蛎肽对胰脂肪酶的结合比对酶-底物复合物的结合更紧密,即混合型抑制中竞争性抑制占主导作用[26]。由图6-b可知,随着花色苷浓度的增加,Vm减小,Km增大,双倒数曲线交于第二象限上一点,说明花色苷对胰脂肪酶的抑制类型同样为非竞争性和竞争性混合型抑制,即花色苷既能与胰脂肪酶结合也能与胰脂肪酶-底物复合体结合;同时,花色苷的Ki和Kis分别为1.211 4 mg/mL和7.143 6 mg/mL,Ki<Kis,说明花色苷对胰脂肪酶的结合比对酶-底物复合物的结合更紧密,混合型抑制中竞争性抑制占主导作用。其他天然黄酮类物质也有类似的现象,例如黑果腺肋花楸果提取物[25]、红江橙果皮黄酮提取物[27]等,说明黄酮类物质易通过范德华力、氢键、疏水力等非共价键与蛋白酶的活性催化位点结合,同时也可以结合到其他酶活性部位以外的催化位点,发挥抑制作用。由图6-c可知,随着牡蛎肽-花色苷复合物浓度的增加,Km增大,Vm不变,双倒数曲线相交于Y轴上一点,说明复合物对于脂肪酶属于竞争性抑制。WANG等[28]也发现了类似的结果,矢车菊素-3-O-葡萄糖苷(cyanidin-3-O-glucoside, C3G)和儿茶素抑制胰脂肪酶的机理分别为竞争性抑制和非竞争性抑制,当C3G和儿茶素协同复合后对胰脂肪酶的抑制机理为混合型。综上,牡蛎肽和花色苷协同后改变了二者对胰脂肪酶的抑制类型,说明二者复合后,与胰脂肪酶的作用位点发生了变化,复合物更易进入胰脂肪酶的疏水空腔,通过氢键或疏水作用与酶的催化位点结合,阻碍底物和酶之间的结合来抑制胰脂肪酶的催化活性[20]。
表2 牡蛎肽、花色苷及其协同复合物对胰脂肪酶的 抑制动力学参数
Table 2 Kinetic parameters of pancreatic lipase inhibition by oyster peptides, anthocyanins and their synergistic complexes

样品质量浓度/(mg/mL)Km/(mg/mL) Vmax/min-1Ki/(mg/mL)Kis/(mg/mL)牡蛎肽00.235 40.237 40.60.578 20.214 410.695 90.211 10.458 27.804 9花色苷00.226 50.238 40.80.397 90.203 120.506 10.184 31.211 47.143 6复合物00.247 80.246 31.20.815 70.247 621.045 40.246 4//
注:Km,米氏常数;Vmax,最大反应速率;Ki,胰脂肪酶抑制常数;Kis,胰脂肪酶-底物复合物抑制常数;/代表无需计算。
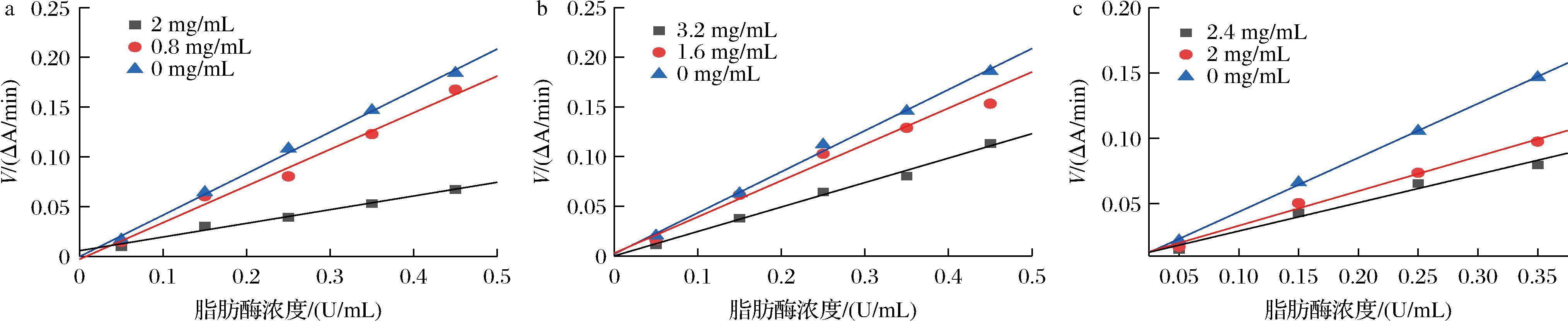
a-牡蛎肽抑制类型曲线;b-花色苷抑制类型曲线;c-复合物抑制类型曲线
图5 牡蛎肽、花色苷及其协同复合物对胰脂肪酶的抑制作用类型
Fig.5 Inhibition types of oyster peptides, anthocyanins and their synergistic complexes against pancreatic lipase

a-牡蛎肽的Lineweaver-Burk曲线;b-花色苷的Lineweaver-Burk曲线;c-复合物的Lineweaver-Burk曲线
图6 牡蛎肽、花色苷及其协同复合物对胰脂肪酶抑制作用的Lineweaver-Burk曲线
Fig.6 Lineweaver-Burk curves of oyster peptides, anthocyanins and their synergistic complexes against pancreatic lipase
2.4 牡蛎肽和花色苷的相互作用分析
基于以上结果,为了进一步探究牡蛎肽和花色苷协同复合后其对胰脂肪酶的抑制能力和酶抑制类型发生变化的原因,利用多光谱学方法研究了牡蛎肽和花色苷的相互作用。
2.4.1 紫外-可见吸收光谱分析
由于特定氨基酸的侧链基团能够吸收一定波长范围的紫外光,因此紫外光谱扫描广泛应用于多肽结构分析及蛋白质或活性肽与多酚或黄酮间的相互作用,具体可表现为紫外光谱峰值的蓝移或红移、信号的增强或减弱[13]。图7-a为牡蛎肽与花色苷复合之后的紫外吸收谱图,牡蛎肽在200 nm和280 nm附近出现吸收峰,且随着协同花色苷浓度的增加,其最大吸收峰逐渐增强,说明牡蛎肽与花色苷之间发生了相互作用,其共轭体系的形成使得π→π电子对能级跃迁,从而导致其紫外吸收强度的增强,同时最大吸收峰的位置发生了一定程度的红移,表明在协同花色苷后,牡蛎肽的芳香族氨基酸微环境发生变化,酪氨酸和色氨酸残基暴露,疏水性降低,极性增加[29],这进一步证实牡蛎肽和花色苷发生了相互作用。CHENG等[14]也报道了类似的结果,结果显示β-乳球蛋白(β-lactoglobulin, β-Lg)与矢车菊素-3-O-葡萄糖苷协同复合后β-Lg的吸收峰强度增加,并且其最大峰位置从214 nm轻微偏移至216 nm,说明β-Lg内芳香族氨基酸残基的疏水性微环境发生了转变。综上,当牡蛎肽协同花色苷后,二者发生了相互作用,牡蛎肽最大吸收峰位置以及强度均受到了影响,导致肽构象和芳香族氨基酸残基的微环境发生改变。
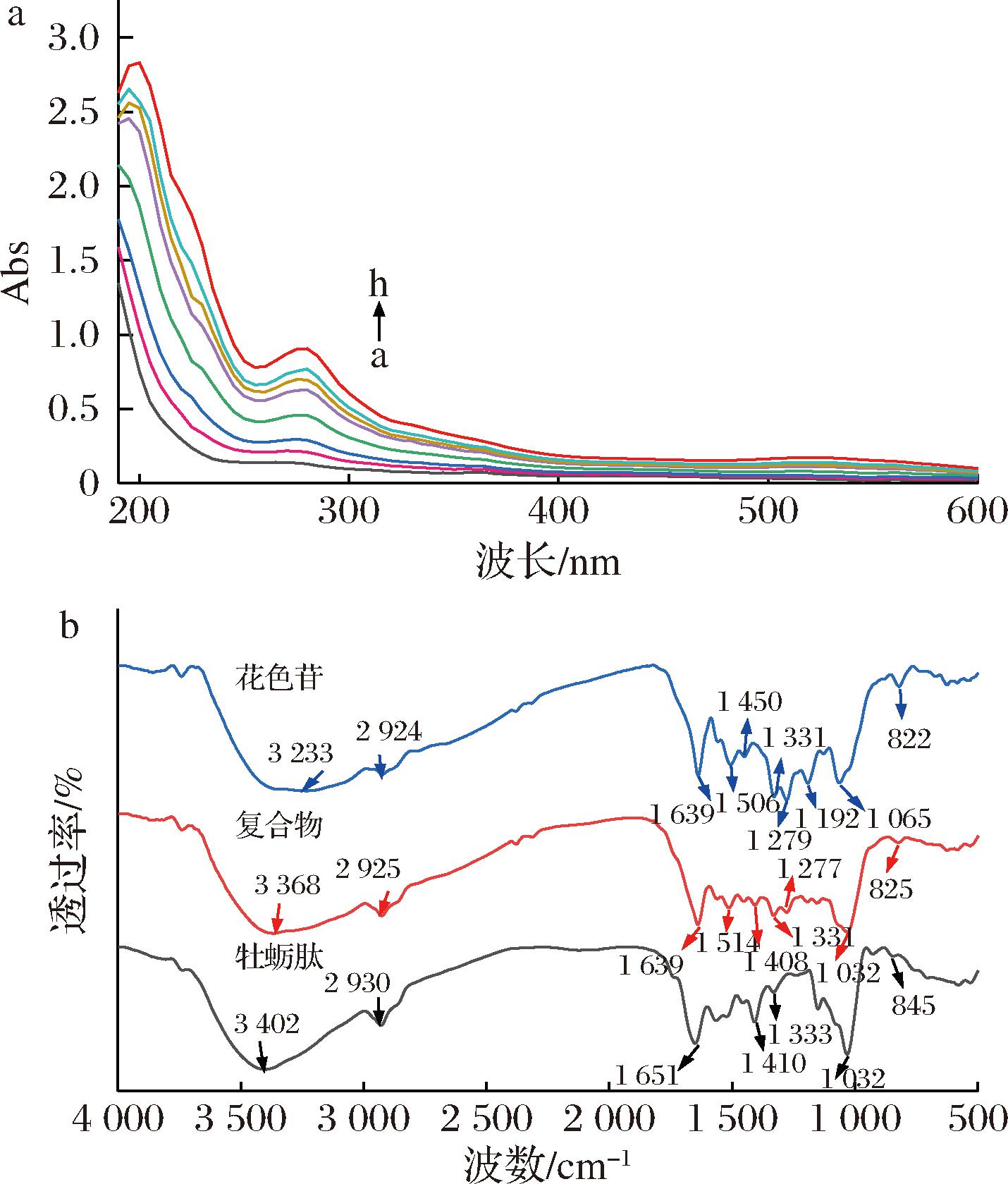
a-紫外吸收谱图;b-红外光谱图
图7 牡蛎肽与花色苷协同复合后的紫外吸收谱图和 牡蛎肽、花色苷及其协同复合物的FTIR
Fig.7 UV absorption spectra of oyster peptides interacted with anthocyanins and FTIR of oyster peptides, anthocyanins and their synergistic complexes
注:a→h表示花色苷质量浓度分别为0、0.1、0.2、0.4、0.6、 0.7、0.8、1 mg/mL。
2.4.2 FT-IR分析
FT-IR广泛应用于分析蛋白质或活性肽二级结构变化,通过FT-IR可深入了解蛋白质或活性肽与不同配体的相互作用[13]。在3 450~3 300 cm-1产生的吸收峰称为酰胺A带,主要反映了N—H的拉伸振动和O—H伸缩振动,在1 600~1 700 cm-1的区域产生吸收峰称为酰胺I带,主要反映C![]() O伸缩;<1 548 cm-1产生的吸收峰称为酰胺Ⅱ带,主要反映了C—N拉伸和N—H弯曲[30]。花色苷的红外光谱主要反映其结构中的苯环、含氧杂环、糖和羟基、甲氧基四部分。由图7-b可知,花色苷在3 233 cm-1附近处有强而宽的吸收峰,推测是由于花色苷结构中的芳香环与糖基上的多羟基产生的伸缩振动,花色苷分子间的羟基以氢键相连,使该处的吸收峰波形变宽;2 924 cm-1附近处的吸收峰是由于其甲氧基中C—H的伸缩振动;1 639 cm-1处的吸收峰,推测是花色苷分子结构中的羰基(C
O伸缩;<1 548 cm-1产生的吸收峰称为酰胺Ⅱ带,主要反映了C—N拉伸和N—H弯曲[30]。花色苷的红外光谱主要反映其结构中的苯环、含氧杂环、糖和羟基、甲氧基四部分。由图7-b可知,花色苷在3 233 cm-1附近处有强而宽的吸收峰,推测是由于花色苷结构中的芳香环与糖基上的多羟基产生的伸缩振动,花色苷分子间的羟基以氢键相连,使该处的吸收峰波形变宽;2 924 cm-1附近处的吸收峰是由于其甲氧基中C—H的伸缩振动;1 639 cm-1处的吸收峰,推测是花色苷分子结构中的羰基(C![]() O)伸缩振动导致;1 506 cm-1、1 450 cm-1处的特征振动吸收峰反映了花色苷结构中苯环的基本骨架,推测是花色苷苯并吡喃的芳环和含氧杂环的骨架振动所致;1 331 cm-1、1 279 cm-1、1 192 cm-1 附近处的吸收峰对应于碳环中碳氧键(C—O—C)的伸缩振动[7]。牡蛎肽中,3 402 cm-1主要为O—H和N—H伸缩特征峰,2 930 cm-1附近处的吸收峰是由于甲氧基中C—H的伸缩振动,1 651 cm-1处的吸收峰,是由牡蛎肽结构中的羰基(C
O)伸缩振动导致;1 506 cm-1、1 450 cm-1处的特征振动吸收峰反映了花色苷结构中苯环的基本骨架,推测是花色苷苯并吡喃的芳环和含氧杂环的骨架振动所致;1 331 cm-1、1 279 cm-1、1 192 cm-1 附近处的吸收峰对应于碳环中碳氧键(C—O—C)的伸缩振动[7]。牡蛎肽中,3 402 cm-1主要为O—H和N—H伸缩特征峰,2 930 cm-1附近处的吸收峰是由于甲氧基中C—H的伸缩振动,1 651 cm-1处的吸收峰,是由牡蛎肽结构中的羰基(C![]() O)伸缩振动导致;1 410 cm-1处的吸收峰,是C—N和N—H键拉伸振动造成的;1 032 cm-1处的吸收峰对应为—C—O—的拉伸振动。
O)伸缩振动导致;1 410 cm-1处的吸收峰,是C—N和N—H键拉伸振动造成的;1 032 cm-1处的吸收峰对应为—C—O—的拉伸振动。
与单独的牡蛎肽相比,牡蛎肽和花色苷的协同复合物在酰胺A带的吸收峰发生了蓝移(从3 402 cm-1移动到3 368 cm-1),说明牡蛎肽和花色苷之间可能通过氢键结合和疏水作用发生了相互作用。酰胺Ⅰ带(1 600~1 700 cm-1)与多肽主链上的C![]() O伸缩振动或与COO—偶连的氢键有关,酰胺Ⅱ带主要负责N—H键的弯曲与C—N拉伸振动,复合物的酰胺Ⅰ带与酰胺Ⅱ带相较于单独的肽发生了一定的振动偏移,复合物的特征峰向低波数方向移动,牡蛎肽与花色苷复合后酰胺Ⅰ带的峰从1 651 cm-1蓝移到1 639 cm-1,表明与花色苷协同后,牡蛎肽的二级结构发生了改变,这很可能是由于牡蛎肽通过静电及疏水作用与花色苷发生相互作用导致的[30]。
O伸缩振动或与COO—偶连的氢键有关,酰胺Ⅱ带主要负责N—H键的弯曲与C—N拉伸振动,复合物的酰胺Ⅰ带与酰胺Ⅱ带相较于单独的肽发生了一定的振动偏移,复合物的特征峰向低波数方向移动,牡蛎肽与花色苷复合后酰胺Ⅰ带的峰从1 651 cm-1蓝移到1 639 cm-1,表明与花色苷协同后,牡蛎肽的二级结构发生了改变,这很可能是由于牡蛎肽通过静电及疏水作用与花色苷发生相互作用导致的[30]。
综上,牡蛎肽和花色苷协同后,二者通过C![]() O、C—N和N—H基团发生氢键和疏水相互作用,导致牡蛎肽羰基氢键网络结构重排,这有助于提高牡蛎肽-花色苷复合物的稳定性。
O、C—N和N—H基团发生氢键和疏水相互作用,导致牡蛎肽羰基氢键网络结构重排,这有助于提高牡蛎肽-花色苷复合物的稳定性。
2.4.3 荧光光谱分析
蛋白质或活性肽中的色氨酸(Trp)、酪氨酸(Tyr)残基可以发射荧光,所以常用荧光猝灭来反映蛋白质或活性肽与其他小分子物质之间的相互作用[13]。由图8-a可知,在添加了不同浓度的花色苷后,牡蛎肽的荧光强度显著降低。当花色苷浓度为0.6 mg/mL时,牡蛎肽荧光强度从648.566 a.u.下降至335.452 a.u,表明花色苷的添加可以使牡蛎肽的内源荧光被猝灭,且随着花色苷浓度的增加,猝灭程度增强。当花色苷浓度为0.6 mg/mL时,荧光猝灭率可达到48.28%。这可能是因为花色苷的芳香环与牡蛎肽的疏水氨基酸残基(酪氨酸、色氨酸残基)相结合,降低了氨基酸残基周围微环境的疏水性[14]。在添加了不同浓度的花色苷后,最大吸收峰出现了明显的红移(由351 nm移动到378 nm),这说明更多的Trp和Tyr残基暴露于溶液中,使这两种氨基酸周围环境的亲水性增强,疏水性减弱,极性增强,该结果与上述的紫外吸收光谱相一致。ZHANG等[31]也发现了类似的结果,在豆粕水解产物(soybean meal hydrolysate, SMH)中添加原花青素(procyanidin, PC)、表没食子儿茶素没食子酸酯(epigallocatechin gallate, EGCG)、没食子酸(gallic acid, GA)和咖啡酸(caffeic acid, CA)会使其荧光强度降低,且SMH-EGCG、SMH-GA和SMH-CA复合物相对于相应的SMH发生了红移,并且与多酚复合后可显著提高SMH的抗氧化活性,特别是其清除ABTS阳离子自由基和DPPH自由基的能力。

a-荧光光谱;b-△λ=15 nm时的同步荧光光谱;c-△λ=60 nm时的同步荧光光谱
图8 牡蛎肽与花色苷相互作用的荧光光谱和同步荧光光谱
Fig.8 Fluorescence spectra and synchronous fluorescence spectra of oyster peptides interacted with anthocyanins
注:a→g表示花色苷浓度分别为0、0.4×10-1、0.8×10-1、0.1、0.2、0.4、0.6 mg/mL。
为进一步确定花色苷的协同复合对牡蛎肽构象的影响,采用同步荧光光谱法探究牡蛎肽构象的变化,可从微观上了解其色氨酸和酪氨酸周围微环境的变化。当激发光波长和发射光波长的差值(Δλ)为15 nm时,同步荧光可反映酪氨酸残基的特性;当Δλ为60 nm时,同步荧光主要反映色氨酸残基的特性[30]。由图8-b、8-c可知,随着花色苷浓度的增加,牡蛎肽的荧光强度均逐渐降低,其中Δλ=15 nm时酪氨酸最大发射波长发生轻微红移(由295 nm移动到297 nm);而Δλ=60 nm时色氨酸最大发射波长的位置明显红移(由292 nm移动到305 nm),这说明花色苷的协同使牡蛎肽的酪氨酸和色氨酸残基周围微环境的疏水性降低,极性增加[31]。此外,当Δλ=15 nm时,随着花色苷浓度增加,牡蛎肽的荧光强度从290.963 a.u持续猝灭到8.215 a.u,当花色苷质量浓度为0.6 mg/mL时,荧光猝灭率为97.18%;当Δλ=60 nm时,牡蛎肽的荧光强度从229.987持续猝灭到47.358,当花色苷质量浓度为0.6 mg/mL时,荧光猝灭率为79.41%。可见Tyr和Trp残基附近的极性发生变化,疏水性减弱,并且花色苷对牡蛎肽Tyr残基(Δλ=15 nm)的猝灭作用比对Trp残基(Δλ=60 nm)的猝灭作用更强,这可能是因为牡蛎肽与花色苷的互作位点更接近Tyr残基[29]。综上,花色苷与牡蛎肽协同后,二者通过发生相互作用导致牡蛎肽的构象发生变化,使其氨基酸微环境极性增大,疏水性减弱。
3 结论
本文首先探究了牡蛎肽和花色苷的胰脂肪酶抑制活性,采用Synergy Finder和Chou-Talalay中效原理分析牡蛎肽协同花色苷抑制胰脂肪酶的活性增效作用,利用酶抑制动力学研究其抑制类型,并运用多光谱学研究牡蛎肽与花色苷的相互作用。结果显示,牡蛎肽、花色苷及不同比例的牡蛎肽和花色苷协同复合物对胰脂肪酶均具有显著的抑制作用,当复合物比例为牡蛎肽∶花色苷=1∶1时,二者协同作用最强,且酶抑制动力学研究表明牡蛎肽、花色苷及其复合物主要通过混合型抑制和竞争性抑制方式发挥酶抑制作用。多光谱学研究结果表明,牡蛎肽和花色苷主要通过氢键和疏水作用发生相互作用,致使酪氨酸(Tyr)和色氨酸(Trp)残基附近的极性发生变化,疏水性减弱,肽构象发生变化,羰基氢键网络结构重排,提高了牡蛎肽-花色苷协同复合物的结构稳定性,起到协同增效作用。本研究为牡蛎肽和花色苷协同增效研究奠定了基础,同时为牡蛎肽、花色苷及其复合物的降脂产品开发提供了数据参考。
[1] SHI Q Y, WANG Y, HAO Q K, et al.Pharmacotherapy for adults with overweight and obesity:A systematic review and network meta-analysis of randomised controlled trials[J].The Lancet, 2024, 403(10434):e21-e31.
[2] LIU T T, LIU X T, CHEN Q X, et al.Lipase inhibitors for obesity:A review[J].Biomedicine &Pharmacotherapy, 2020, 128:110314.
[3] KIM S, KIM J H, SEOK S H, et al.Anti-obesity effect with reduced adverse effect of the co-administration of mini-tablets containing orlistat and mini-tablets containing xanthan gum:In vitro and in vivo evaluation[J].International Journal of Pharmaceutics, 2020, 591:119998.
[4] RAJAN L, PALANISWAMY D, MOHANKUMAR S K.Targeting obesity with plant-derived pancreatic lipase inhibitors:A comprehensive review[J].Pharmacological Research, 2020, 155:104681.
[5] LAFOUNTAIN A M, YUAN Y W.Repressors of anthocyanin biosynthesis[J].New Phytologist, 2021, 231(3):933-949.
[6] HERRERA-BALANDRANO D D, CHAI Z, HUTABARAT R P, et al.Hypoglycemic and hypolipidemic effects of blueberry anthocyanins by AMPK activation:In vitro and in vivo studies[J].Redox Biology, 2021, 46:102100.
[7] 袁婷婷. 彩色马铃薯花色苷提取物降脂作用研究[D].重庆:西南大学, 2023.YUAN T T.Study on lipid-lowering effect of anthocyanin extract from colored potato[D].Chongqing:Southwest University, 2023.
[8] YAO L, XU J, ZHANG L W, et al.Nanoencapsulation of anthocyanin by an amphiphilic peptide for stability enhancement[J].Food Hydrocolloids, 2021, 118:106741.
[9] ZHU D Y, YUAN Z, WU D, et al.The dual-function of bioactive peptides derived from oyster (Crassostrea gigas) proteins hydrolysates[J].Food Science and Human Wellness, 2023, 12(5):1609-1617
[10] 蒋美龄, 陈忠琴, 秦小明, 等.牡蛎降糖肽的结构表征及其协同花色苷的活性增效作用[J].大连海洋大学学报, 2023, 38(3):455-463.JIANG M L, CHEN Z Q, QIN X M, et al.Structural characterization and the synergistic effects with anthocyanin of oyster hypoglycemic peptides[J].Journal of Dalian Ocean University, 2023, 38(3):455-463.
[11] 章超桦. 牡蛎营养特性及功能活性研究进展[J].大连海洋大学学报, 2022, 37(5):719-731.ZHANG C H.Research progress on nutritional characteristics and bioactivities of oysters:A review[J].Journal of Dalian Ocean University, 2022, 37(5):719-731.
[12] CHEN H, DONG X T, ZHOU M Y, et al.Modulation of lipid metabolism by oyster peptides in mice with high-fat diet-induced obesity[J].Food Bioscience, 2024, 58:103529.
[13] 苟彦君, 胡孝君, 林德贤, 等.胶原蛋白与多酚相互作用机理研究及应用进展[J].食品与发酵工业, 2024, 50(14):357-363.GOU Y J, HU X J, LIN D X, et al.Study on mechanism of interaction between collagen and polyphenols and progress[J].Food and Fermentation Industries, 2024, 50(14):357-363.
[14] CHENG J, LIU J H, PRASANNA G, et al.Spectrofluorimetric and molecular docking studies on the interaction of cyanidin-3-O-glucoside with whey protein, β-lactoglobulin[J].International Journal of Biological Macromolecules, 2017, 105:965-972.
[15] SU S W, WAN Y L, GUO S T, et al.Effect of peptide-phenolic interaction on the antioxidant capacity of walnut protein hydrolysates[J].International Journal of Food Science &Technology, 2018, 53(2):508-515.
[16] 柏昌旺, 章超桦, 林海生, 等.响应面法优化制备牡蛎短肽工艺[J].广东海洋大学学报, 2019, 39(6):85-92.BAI C W, ZHANG C H, LIN H S, et al.Optimization of preparation process of oyster oligopeptides by response surface methodology[J].Journal of Guangdong Ocean University, 2019, 39(6):85-92.
[17] GUTIÉRREZ-GRIJALVA E P, ANTUNES-RICARDO M, ACOSTA-ESTRADA B A, et al.Cellular antioxidant activity and in vitro inhibition of α-glucosidase, α-amylase and pancreatic lipase of oregano polyphenols under simulated gastrointestinal digestion[J].Food Research International, 2019, 116:676-686.
[18] MA C Y, ZHOU X C, YU H R, et al.Virtual screening and multi-synergism of inhibitory compounds against pancreatic lipase[J].Food Bioscience, 2024, 57:103601.
[19] 王云富, 崔彩芳, 孙兆岳, 等.基于SynergyFinder探究花旗松素和葛根素的协同抗氧化能力[J].食品与发酵工业, 2024, 50(15):132-141.WANG Y F, CUI C F, SUN Z Y, et al.Synergistic antioxidant capacity of taxifolin and puerarin based on SynergyFinder[J].Food and Fermentation Industries, 2024, 50(15):132-141.
[20] LI X X, PU Y J, JIANG H T, et al.Inhibitory effect of procyanidin B2 and tannin acid on cholesterol esterase and their synergistic effect with orlistat[J].Food Science and Human Wellness, 2024, 13(1):360-369.
[21] 韩鹏薇, 易彤, 李虹辉, 等.虾壳源蛋白水解物降糖降脂活性评价及肽序分析[J].食品与机械, 2024, 40(4):148-157.HAN P W, YI T, LI H H, et al.Study on hypoglycemic and lipid-lowering activity of shrimp shell-derived enzymatic hydrolysate and peptide sequence function analysis[J].Food &Machinery, 2024, 40(4):148-157.
[22] 陈浩南, 李姣, 王婉愉, 等.高良姜水提物的体外抗氧化和胰脂肪酶、α-葡萄糖苷酶抑制功能研究[J].中国调味品, 2019, 44(4):43-47;51.CHEN H N, LI J, WANG W Y, et al.Antioxidant activities and inhibitory effects against pancreatic lipase and α-glucosidase of galangal aqueous extracts in vitro[J].China Condiment, 2019, 44(4):43-47;51.
[23] 苏小洁, 陈忠琴, 曹文红, 等.牡蛎DPP-Ⅳ抑制肽的结构特征及其协同花色苷的活性增效作用研究[J].食品与发酵工业, 2024, 50(15):87-96.SU X J, CHEN Z Q, CAO W H, et al.Structural characterization and synergistic inhibition of DPP-Ⅳ activity of oyster peptides and anthocyanins[J].Food and Fermentation Industries, 2024, 50(15):87-96.
[24] 黄淋. 核桃多肽及多酚对乙酰胆碱酯酶抑制作用研究[D].广州:华南理工大学, 2022.HUANG L.Inhibitory effect of walnut peptides and polyphenols on acetylcholinesterase[D].Guangzhou:South China University of Technology, 2022.
[25] SOSNOWSKA D, PODSDEK A, REDZYNIA M, et al.Inhibitory effect of black chokeberry fruit polyphenols on pancreatic lipase-Searching for most active inhibitors[J].Journal of Functional Foods, 2018, 49:196-204.
[26] 倪丹, 蒋新元, 唐玉莲, 等.鞣花酸抑制酪氨酸酶的动力学、荧光光谱分析及分子对接[J].食品科学, 2024, 45(2):104-112.NI D, JIANG X Y, TANG Y L, et al.Kinetic, fluorescence spectroscopy and molecular docking studies of tyrosinase inhibition by ellagic acid[J].Food Science, 2024, 45(2):104-112.
[27] 林海生, 饶梦微, 秦小明, 等.红江橙果皮黄酮提取物对α-葡萄糖苷酶和胰脂肪酶的抑制作用[J].现代食品科技, 2023, 39(10):89-96.LIN H S, RAO M W, QIN X M, et al.Inhibitory effects of total flavonoids extracted from the peel of Citrus sinensis Osbeck’Hongjiang’on α-glucosidase and pancreatic lipase activities[J].Modern Food Science and Technology, 2023, 39(10):89-96.
[28] WANG Y Y, CHEN L H, LIU H M, et al.Characterization of the synergistic inhibitory effect of cyanidin-3-O-glucoside and catechin on pancreatic lipase[J].Food Chemistry, 2023, 404:134672.
[29] 翟晓宇,董文江,于鑫欣,等.不同pH值环境下β-乳球蛋白与咖啡中3种主要多酚之间的相互作用[J].食品科学,2024, 45(19): 26-40.ZHAI X Y, DONG W J, YU X X, et al. The Interaction between β-lactoglobulin and three main polyphenols in coffee under different pH environments[J]. Food Science,2024, 45(19): 26-40.
[30] HE Z Y, XU M Z, ZENG M M, et al.Interactions of milk α- and β-casein with malvidin-3-O-glucoside and their effects on the stability of grape skin anthocyanin extracts[J].Food Chemistry, 2016, 199:314-322.
[31] ZHANG X Y, XU Z, ZHANG S, et al.Improving the biological activity and emulsification ability of soybean meal hydrolysate via non-covalent interactions with polyphenols[J].LWT, 2023, 182:114869.