丁二胺又名1,4-二氨基丁烷或腐胺(putrescine),其在工业上最主要的应用是生产尼龙46,后者因其高耐热性、耐磨性、耐冲击性以及耐燃性的优点被广泛应用于电子电器元件、轴承以及汽车引擎的制造[1-2]。目前,丁二胺的化学合成主要是通过丙烯腈与氢氰酸反应得到丁二腈后加氢来制备[3]。然而氢氰酸剧毒,所需设备要求较高,导致丁二胺合成技术壁垒高。
在微生物的体内存在鸟氨酸脱羧和精氨酸脱羧两种丁二胺合成途径[4],前者以鸟氨酸为前体,在鸟氨酸脱羧酶的催化作用下,可以一步合成丁二胺,后者以L-精氨酸为前体,通过精氨酸脱羧酶(AdiA和SpeA)和胍丁胺酶(SpeB)两步催化产生丁二胺。以鸟氨酸合成途径为基础,QIAN等[5]敲除大肠杆菌中鸟氨酸氨基甲酰转移酶基因(argI)并过表达鸟氨酸合成基因(argE-C),以此来增加前体鸟氨酸的积累;并通过过表达了鸟氨酸脱羧酶基因(speC),删除全局转录调控因子RpoS,最终补料分批发酵丁二胺产量达到了24.2 g/L。WENDISCH团队在谷氨酸棒杆菌中敲除argF(编码鸟氨酸转氨甲酰酶)和argR(编码L-精氨酸阻遏物)基因以增加鸟氨酸的浓度,最终丁二胺产量达到19 g/L,产率为0.16 g/(g葡萄糖)[6]。刘建忠团队敲除了谷氨酸棒杆菌中的谷氨酰胺丁二胺氧化酶基因puo、葡萄糖脱氢酶基因butA以及丁二胺乙酰化基因snaA,结合适应性进化,丁二胺最高产量达到12.44 g/L,产率为0.29 g/(g葡萄糖)[7]。以精氨酸途径为基础,THONGBHUBATE等[8]在大肠杆菌中通过解除L-精氨酸的反馈抑制,并对启动子等进行优化,丁二胺的最高产量达到1.74 g/L。LI等[9]在大肠杆菌中过表达精氨酸脱羧酶SpeA和胍丁胺酶 SpeB的表达基因,并结合发酵控制,48 h丁二胺产量达到了26.21 g/L。虽然上述方法都成功实现了丁二胺的生物合成,但都存在代谢路径复杂、产量和生产效率均较低的问题。
近年来,氨基酸的生物法合成工艺日渐成熟,以L-精氨酸等为前体直接催化合成丁二胺具有显著优势。HUI等[10]通过构建不同质粒平衡大肠杆菌中精氨酸脱羧酶和胍丁胺酶的表达,获得了最佳菌株pACYCDute-speB-speA,在最优条件下利用全细胞体系进行催化,获得了1.72 g/L的丁二胺。随树珍[11]以鸟氨酸为前体,通过敲除大肠杆菌BL21中的鸟氨酸氨甲酰基转移酶基因argI,构建工程菌株PUT-A,最终通过全细胞催化的方式获得了0.64 g/L丁二胺。YANG等[12]通过冷处理防止了副产物对酶促反应的反馈抑制,利用L-精氨酸进行全细胞催化,大肠杆菌中丁二胺产量达到17.1 g/L。
目前,催化法生产丁二胺虽取得一定成果,但在全细胞催化过程中仍存在底物添加量较低,物质传输较为困难等问题。因此,本研究以L-精氨酸为底物,利用透性化细胞处理来提升物质的传输效率,并结合工程菌株培养和催化过程强化来提升丁二胺的合成能力,最终为丁二胺的生物法合成提供参考和借鉴。
1 材料与方法
1.1 材料和试剂
1.1.1 菌株和质粒
质粒pET-speAB-adiA(736E)[13]、菌株BL21(ΔEGAP)来自实验室保藏。
1.1.2 试剂和仪器
本实验中使用的NaCl、葡萄糖、甘油、乙醚、乙腈、盐酸、NaOH、NaHCO3、丙酮等化学试剂均为分析纯,上海国药集团化学试剂有限公司;1,7-庚二胺、气相色谱,梯希爱(上海)化成工业发展有限公司;丹磺酰氯、高效液相色谱,上海阿拉丁生化科技股份有限公司;氨苄青霉素(ampicillin, Amp),上海生工生物工程公司;胰蛋白胨、酵母提取物,英国oxoid公司。
HGPN-Ⅱ-50 恒温培养箱,上海恒越医疗器械有限公司;nexus GX2 PCR仪、ST 16R Eppendorf高速离心机,德国Eppendorf公司;UV2450紫外可见光分光光度计,日本Shimadzu公司;LS-B50L型立式圆形压力蒸气灭菌器,上海医用核子仪器厂;HYL-C3恒温摇床,上海跃进医疗器械厂。
1.1.3 培养基和缓冲液
LB培养基(g/L):蛋白胨10,酵母提取物5,NaCl 10;LB固体培养基按2%(质量分数)添加琼脂粉,根据需要加入相应浓度抗生素。灭菌条件为121 ℃, 20 min。
磷酸盐缓冲液(g/L):KH2PO4 0.27,Na2HPO4 1.42,NaCl 8,KCl 0.2。
1.2 实验方法
1.2.1 工程菌株构建
将保存于-20 ℃ pET-speAB-adiA(736E)质粒取出,转入BL21(ΔEGAP)感受态中,涂于含Anp抗性的平板,记为工程菌株PUT-736E,置于37 ℃恒温培养箱过夜培养,挑取单菌落接入含氨苄青霉素的10 mL LB培养基中,将其置于37 ℃恒温摇床中过夜培养,按2%接种量接种于50 mL的含氨苄青霉素LB培养基中,在37 ℃恒温摇床中250 r/min培养3 h后,加入1 mmol/L的异丙基-β-D-硫代半乳糖苷(isopropyl-beta-D-thiogalactopyranoside,IPTG)进行诱导,同时加入底物L-精氨酸,再将其置于30 ℃恒温摇床中250 r/min培养,每隔12 h取样检测丁二胺产量。
1.2.2 工程菌株透性化细胞催化合成丁二胺
按1.2.1节方法培养菌体12 h,将诱导后的发酵液在冷冻离心机中以4 ℃、5 000 r/min的条件离心10 min,离心后弃去上清液,将剩余菌体用含30%乙醇,pH 7的PBS重悬。再次于冷冻离心机中4 ℃、5 000 r/min离心10 min,弃去上清液。使用不含乙醇,pH 7的PBS清洗菌体3次,再次离心(4 ℃,5 000 r/min)后,用PBS将菌体重悬。催化过程于50 mL离心管中进行,反应体系:100 g/L L-精氨酸、4 mmol/L MgSO4、4 mmol/L MnSO4、1 mmol/L PLP、0.4 mmol/L二硫苏糖醇(dithiothreitol,DTT)、0.4 mmol/L IPTG、1 mmol/L Anp、OD600值为30的菌体,最后用PBS(pH 7.0)将体系补充至10 mL。整个反应在30 ℃、250 r/min恒温摇床中进行,每隔12 h取样,进行丁二胺检测。
1.2.3 HPLC法检测丁二胺
将发酵液于12 000 r/min离心5~10 min,取上清液稀释一定倍数至300 μL,加入300 μL饱和NaHCO3,3 μL 100 mg/L的1,7-庚二胺作为内标。用15 g/L NaOH溶液调pH值至9.4。加5 mg/mL丹磺酰氯-丙酮溶液600 μL后,在60 ℃条件下避光水浴30 min进行衍生化反应。衍生化结束后,加150 μL饱和NaCl溶液终止反应。先用2 mL无水乙醚萃取,取上清液,再将下层液体用1 mL无水乙醚萃取,取上清液。45 ℃水浴在通风橱中将乙醚吹干。随后用300 μL乙腈超声波溶解,过0.22 μm有机相膜后进行检测。检测参数如下:柱温30 ℃,紫外检测波长254 nm,进样体积10 μL,流动相A为超纯水,流动相B为乙腈,梯度洗脱方案:0~4 min流动相B从55%升至70%;然后保持70%的比例2 min;6~11 min流动相B从70%升至95%;然后保持95%的比例1 min;12~13 min,流动相B从95%降至55%;最后维持55%的比例2 min,流速设定为0.7 mL/min。
1.2.4 工程菌株透性化细胞催化条件优化
不同方法处理细胞:将培养的种子液以2%的接种量接种到50 mL的培养基中,于37 ℃恒温摇床中250 r/min培养菌体3 h后,加入IPTG进行诱导,30 ℃ 250 r/min继续培养12 h。分别用乙醇、十六烷基三甲基溴化铵(hexadecyl trimethyl ammonium bromide,CTAB)、吐温-80处理细胞,细胞处理完成后,在终质量浓度100 g/L L-精氨酸、4 mmol/L MgSO4、4 mmol/L MnSO4、1 mmol/L PLP、0.4 mmol/L DDT、OD60030条件下,进行催化。HPLC检测丁二胺产量,以确定最佳细胞处理方法。
乙醇处理细胞比例优化:将培养的种子液以2%的接种量接种到50 mL的培养基中,于37 ℃恒温摇床中250 r/min培养菌体3 h后,加入IPTG进行诱导,30 ℃ 250 r/min继续培养12 h。设置10%、20%、30%、40%、50%的乙醇体积分数进行透性化细胞处理,细胞处理完成后,在终质量浓度100 g/L L-精氨酸、4 mmol/L MgSO4、4 mmol/L MnSO4、1 mmol/L PLP、0.4 mmol/L DDT、OD600值为30条件下,进行催化。HPLC检测丁二胺产量,以确定最佳乙醇处理比例。
诱导剂添加时间优化:将培养的种子液以2%的接种量接种到50 mL的培养基中,于37 ℃恒温摇床中250 r/min培养菌体2、2.5、3、3.5、4 h后,分别加入IPTG进行诱导,30 ℃恒温摇床中250 r/min继续培养12 h。用体积分数为30%乙醇处理细胞后,在终质量浓度100 g/L L-精氨酸、4 mmol/L MgSO4、4 mmol/L MnSO4、1 mmol/L PLP、0.4 mmol/L DDT、OD600值为30条件下,进行催化。HPLC检测丁二胺产量,以确定最佳诱导剂添加时间。
菌体培养时间优化:将培养的种子液以2%的接种量接种到50 mL的培养基中,于37 ℃恒温摇床中250 r/min培养3.5 h后,加入IPTG进行诱导。30 ℃恒温摇床中250 r/min继续分别培养10、12、24、36、48 h。用体积分数为30%乙醇处理细胞后,在终质量浓度100 g/L L-精氨酸、4 mmol/L MgSO4、4 mmol/L MnSO4、1 mmol/L PLP、0.4 mmol/L DDT、OD600值为30条件下,进行催化。HPLC检测丁二胺产量,以确定最佳菌体培养时间。
菌体添加量优化:将培养的种子液以2%的接种量接种到50 mL的培养基中,于37 ℃恒温摇床中250 r/min培养3.5 h后,加入IPTG进行诱导。30 ℃恒温摇床中250 r/min继续培养12 h。用体积分数为30%乙醇处理细胞,在终质量浓度100 g/L L-精氨酸、4 mmol/L MgSO4、4 mmol/L MnSO4、1 mmol/L PLP、0.4 mmol/L DDT条件下,控制OD600值分别为10、20、30、40、50、60进行催化。HPLC检测丁二胺产量,以确定最佳菌体添加量。
Mg2+浓度优化:将培养的种子液以2%的接种量接种到50 mL的培养基中,于37 ℃恒温摇床中250 r/min培养3.5 h后,加入IPTG进行诱导。30 ℃恒温摇床中250 r/min继续培养12 h。用体积分数30%乙醇处理细胞,在终质量浓度100 g/L L-精氨酸、4 mmol/L MnSO4、1 mmol/L PLP、0.4 mmol/L DDT、OD600值为50条件下,控制Mg2+浓度分别为2、4、6、8、10 mmol/L进行催化。HPLC检测丁二胺产量,以确定最佳Mg2+浓度。
Mn2+浓度优化:将培养的种子液以2%的接种量接种到50 mL的培养基中,于37 ℃恒温摇床中250 r/min培养3.5 h后,加入IPTG进行诱导。30 ℃恒温摇床中250 r/min继续培养12 h。用体积分数30%乙醇处理细胞,在终质量浓度100 g/L L-精氨酸、4 mmol/L MgSO4、1 mmol/L PLP、0.4 mmol/L DDT、OD600值为50条件下,控制Mn2+浓度分别为4、8、12、16、20 mmol/L进行催化。HPLC检测丁二胺产量,以确定最佳Mn2+浓度。
底物添加量优化:将培养的种子液以2%的接种量接种到50 mL的培养基中,于37 ℃恒温摇床中250 r/min培养3.5 h后,加入IPTG进行诱导。30 ℃恒温摇床中250 r/min继续培养12 h。用体积分数30%乙醇处理细胞,在终浓度4 mmol/L MgSO4、12 mmol/L MnSO4、1 mmol/L PLP、0.4 mmol/L DDT、OD600值为50条件下,控制L-精氨酸浓度分别为80、100、120、140、160、180 g/L进行催化。HPLC检测丁二胺产量,以确定最佳底物添加量。
1.2.5 统计学分析
使用SPSS 26软件进行数据处理和分析。
2 结果与分析
2.1 丁二胺合成工程菌株构建
L-精氨酸在大肠杆菌内可通过两步转化为丁二胺。首先,L-精氨酸在精氨酸脱羧酶SpeA和AdiA的作用下转化为胍基丁胺,而后经胍丁胺酶SpeB催化生成丁二胺(图1)。将质粒pET-speAB-adiA(736E)转入大肠杆菌感受态中,构建工程菌株PUT-736E,开展丁二胺的催化合成研究。结果如图2所示,前12 h丁二胺合成较少,其原因可能是前期菌体量较少使得丁二胺合成效率较低;36 h时丁二胺产量最高达到8.92 g/L,但其摩尔转化率仅为24%,这可能是由于大肠杆菌细胞膜和细胞壁所起天然保护作用使得底物和产物进出细胞较为困难。因此,需要改变细胞膜的通透性以强化物质的运输效率。
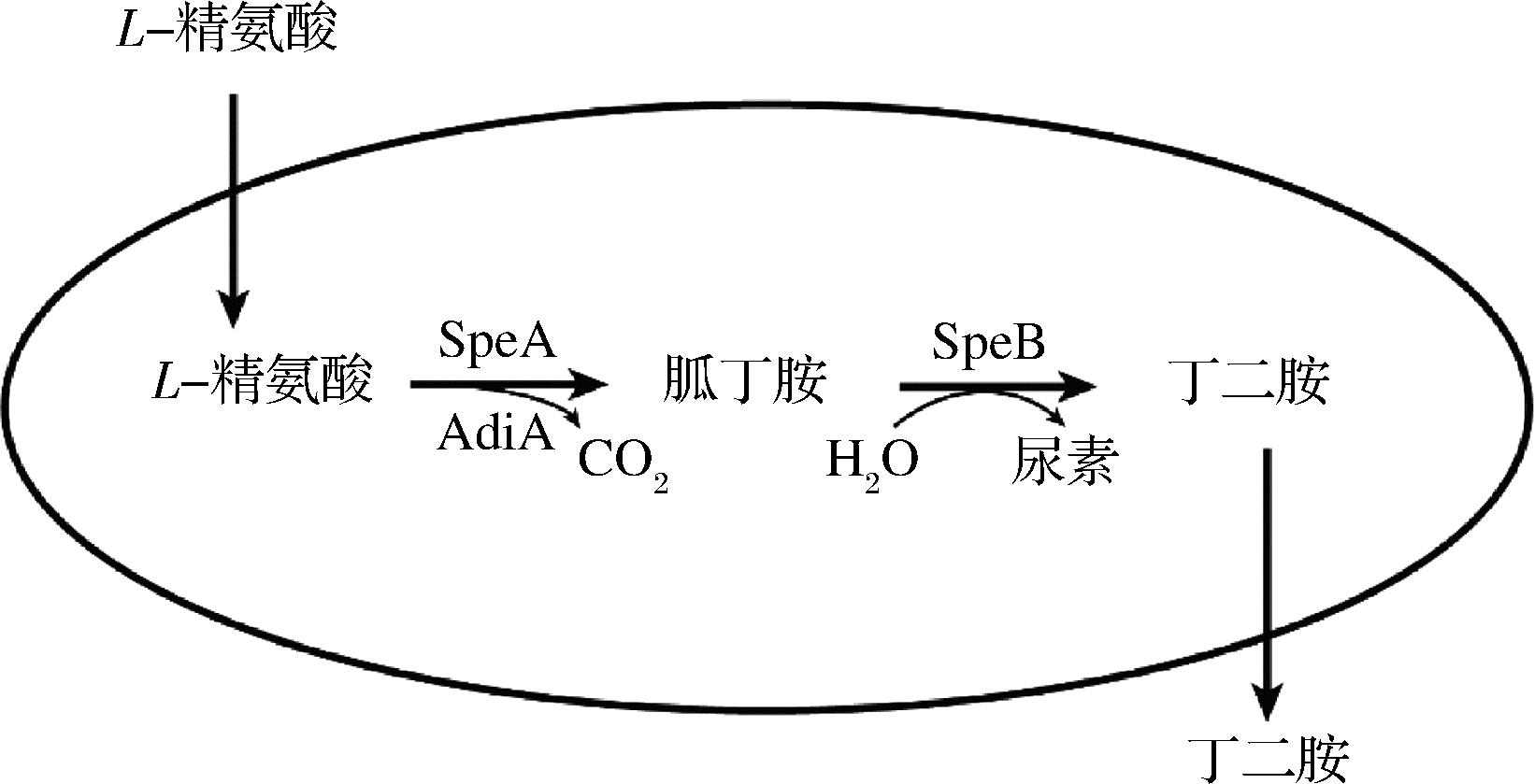
图1 精氨酸合成丁二胺路线图
Fig.1 Roadmap for the synthesis of putrescine from arginine
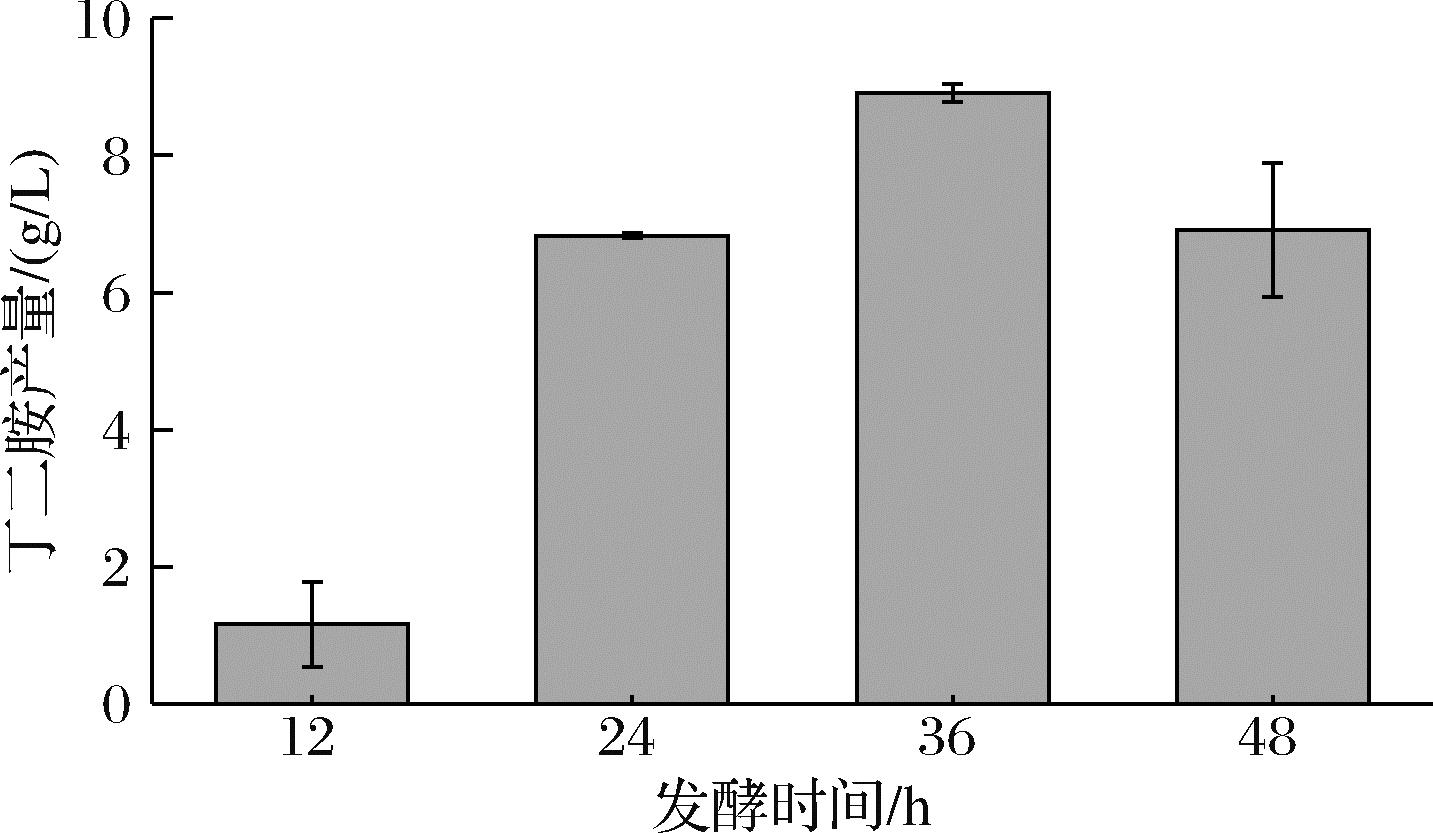
图2 工程菌株PUT-736E催化合成丁二胺
Fig.2 Putrescine produced by engineered strain PUT-736E
2.2 透性化工程细胞提高丁二胺合成能力
2.2.1 不同透性化试剂处理细胞对丁二胺合成的影响
细胞壁、细胞膜不仅可以使营养物质进入细胞,同时也能防止外界有毒有害物质的侵入[14-15],但在全细胞催化过程中,细胞壁、细胞膜的这些特性会对物质的快速运输产生阻碍。CTAB、吐温-80是常见的表面活性剂,其可以自发插入细胞膜,降低边缘张力,使细胞膜不稳定破裂;而乙醇可以与细胞膜产生静电作用,破坏亲疏水平衡[16],从而最终改变细胞膜的通透性,使底物更易进入。使用三者处理细胞(图3),相较于对照,工程菌株的催化能力均有一定提升,效果最好的是乙醇处理细胞,丁二胺产量达到14.92 g/L,相较于对照提高了50%。使用乙醇进行透性化处理可部分溶解大肠杆菌的细胞结构,这样既能增强底物与酶的接触,也能促进产物的释放[17]。因此,选择用乙醇处理细胞为最适透性化处理方法。
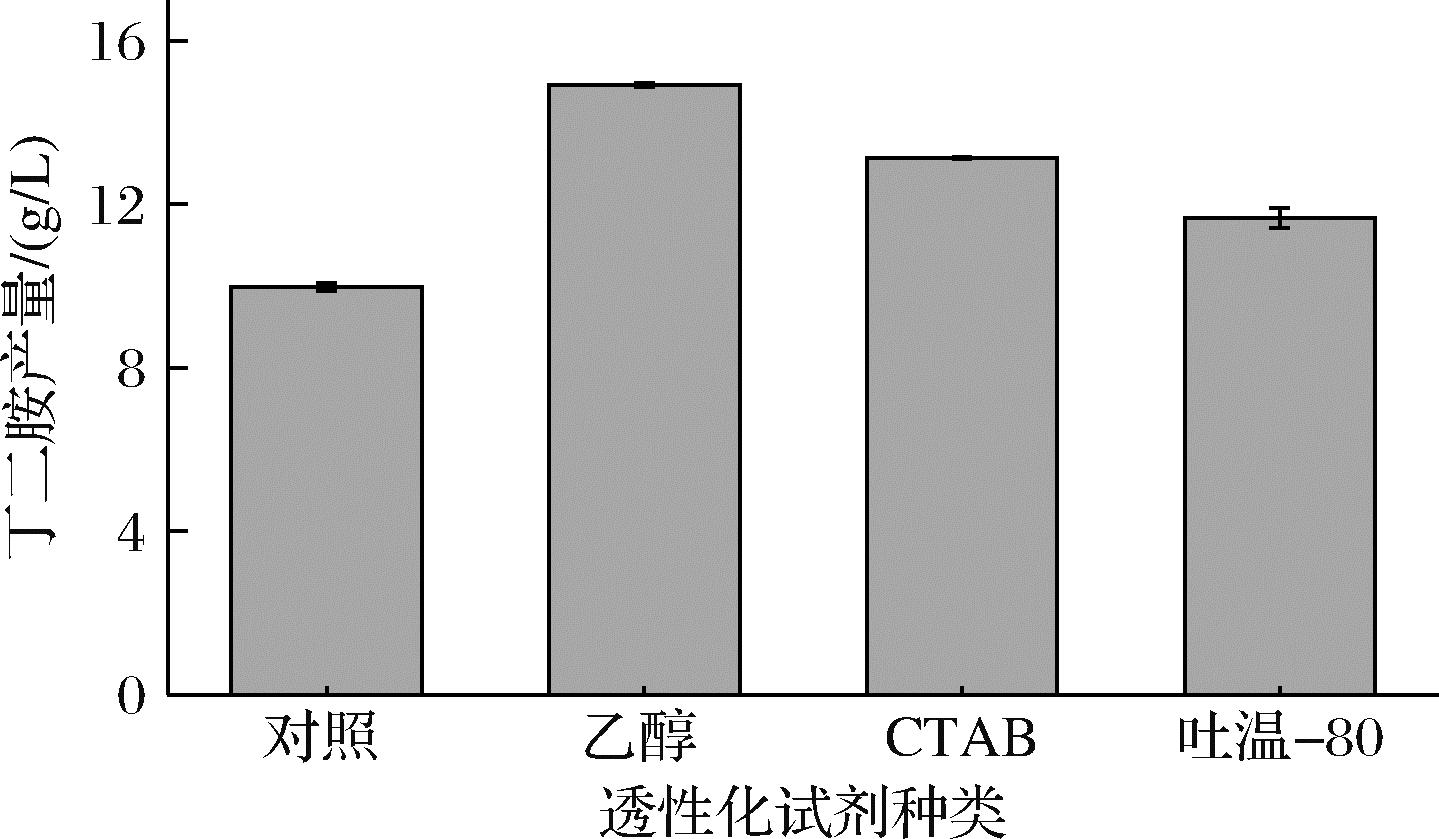
图3 不同透性化试剂处理对丁二胺合成影响
Fig.3 Effect of different permeabilizing reagent treatments on the synthesis of putrescine
2.2.2 不同乙醇比例处理细胞对丁二胺合成的影响
有机溶剂乙醇使用量对细胞活性和催化效果影响较大,较低的乙醇比例可能对细胞膜通透性的改变不足,底物进入细胞较为困难,较高则可能对膜蛋白结构改变过大,导致菌体受损死亡,因此,需要找寻一个合适的乙醇用量。如图4所示,随着乙醇使用比例的提高,细胞催化L-精氨酸合成丁二胺能力也逐渐增强,表明随乙醇使用量的增加,细胞膜通透性改善显著,从而促进底物L-精氨酸进入,但当乙醇比例大于30%时,丁二胺催化能力出现明显下降,这可能是由于乙醇作为一种常用的消毒剂,其较高的浓度可能对细胞产生毒害作用,导致部分细胞失活,使得其催化能力明显降低,这与刘宇轩[17]透性化处理细胞生产戊二胺时得到的结论相符。因此,丁二胺合成的最适乙醇处理比例为30%。

图4 不同乙醇比例处理细胞对丁二胺合成影响
Fig.4 Effect of pretreatment with different ethanol ratios on the synthesis of putrescine
2.3 菌体生长对透性化细胞催化合成丁二胺的影响
2.3.1 诱导剂添加时间对透性化细胞催化合成丁二胺的影响
不同的培养时间对菌体进行诱导酶的表达效果各不相同,过早诱导可能会由于菌体量较低导致蛋白表达量较少,而较晚诱导又可能由于菌体生长产生了较多代谢产物而导致其蛋白表达能力减弱。在不同时间添加诱导剂经一段时间培养后,对其进行丁二胺的催化合成,结果如图5所示,在2~3.5 h内,随着诱导时间的增加,丁二胺的产量也明显提高,在3.5 h达到最高值19.87 g/L,表明随着诱导时间的延后,精氨酸脱羧酶等的表达效果也随之增强,菌体催化L-精氨酸合成丁二胺的能力也随之提高。但当诱导时间超过3.5 h 后,丁二胺产量出现下降,这可能是由于较晚的诱导,导致菌体产生较多的副产物导致关键酶表达减弱。因此,选择最佳的诱导时间3.5 h进行后续研究。
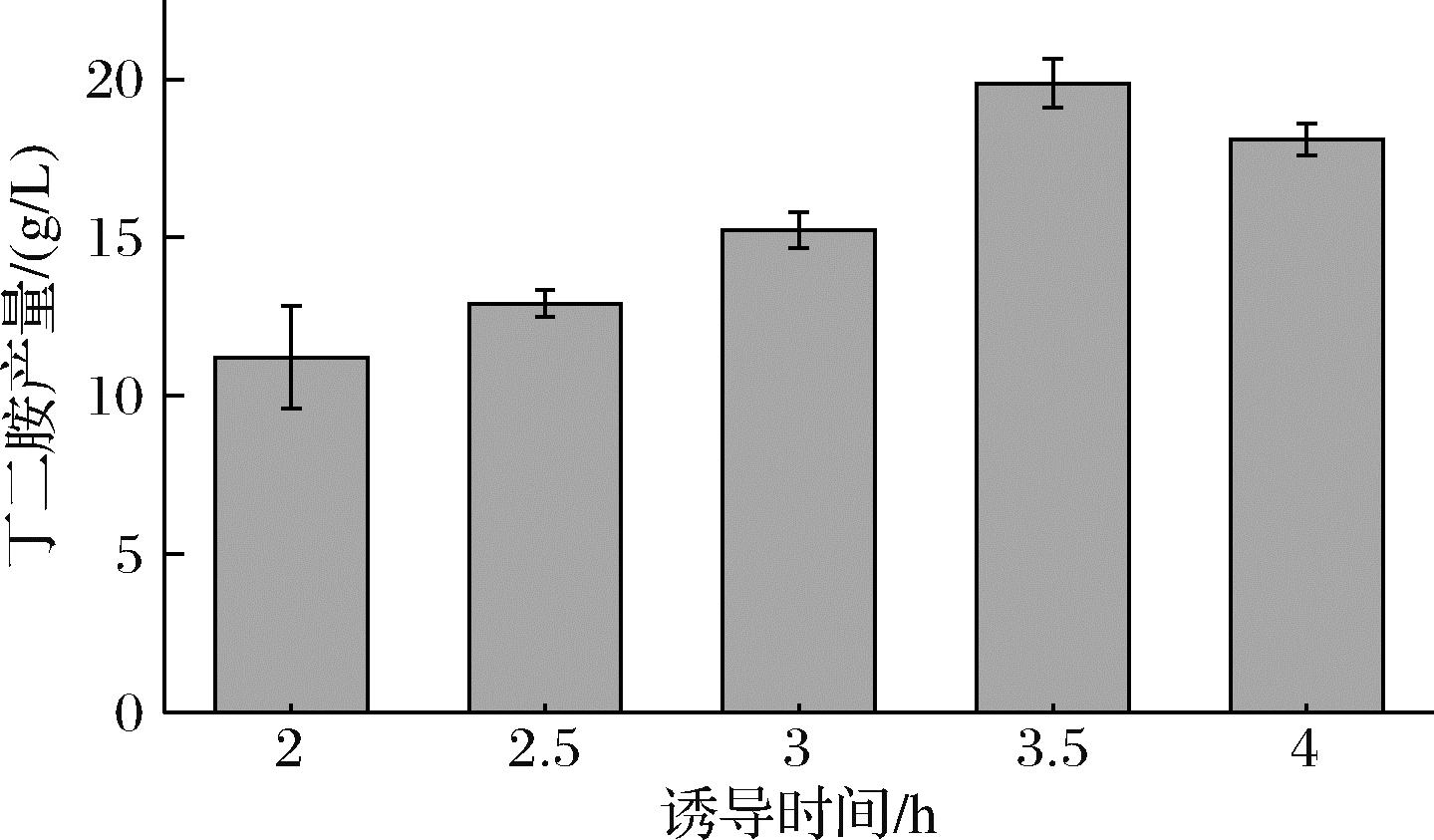
图5 不同诱导时间对丁二胺合成影响
Fig.5 Effect of different induction times on the synthesis of putrescine
2.3.2 菌体培养时间对透性化细胞催化合成丁二胺的影响
菌体培养时间是透性化细胞催化的重要影响因素,菌体培养时间较短可能使得菌体蛋白表达不充分,从而影响催化效率,而菌体培养时间较长,则又可能导致细胞处于衰老状态,酶的催化活性也相应降低。利用不同培养时间的菌体进行催化,结果如图6所示,随着菌体培养时间的延长,细胞催化精氨酸合成丁二胺的能力也逐渐增强,当菌体培养时间为12 h时,丁二胺的产量最高达到25.82 g/L,随后继续增加菌体培养时间,丁二胺产量开始下降。王越等[18]利用全细胞催化合成α-酮戊二酸,随着菌体培养时间增加,α-酮戊二酸的产量随之增加,但当菌体培养时间超过12 h时,α-酮戊二酸的产量也出现明显降低,这与本研究得到的结论一致。因此,丁二胺催化合成的最佳菌体培养时间为12 h。
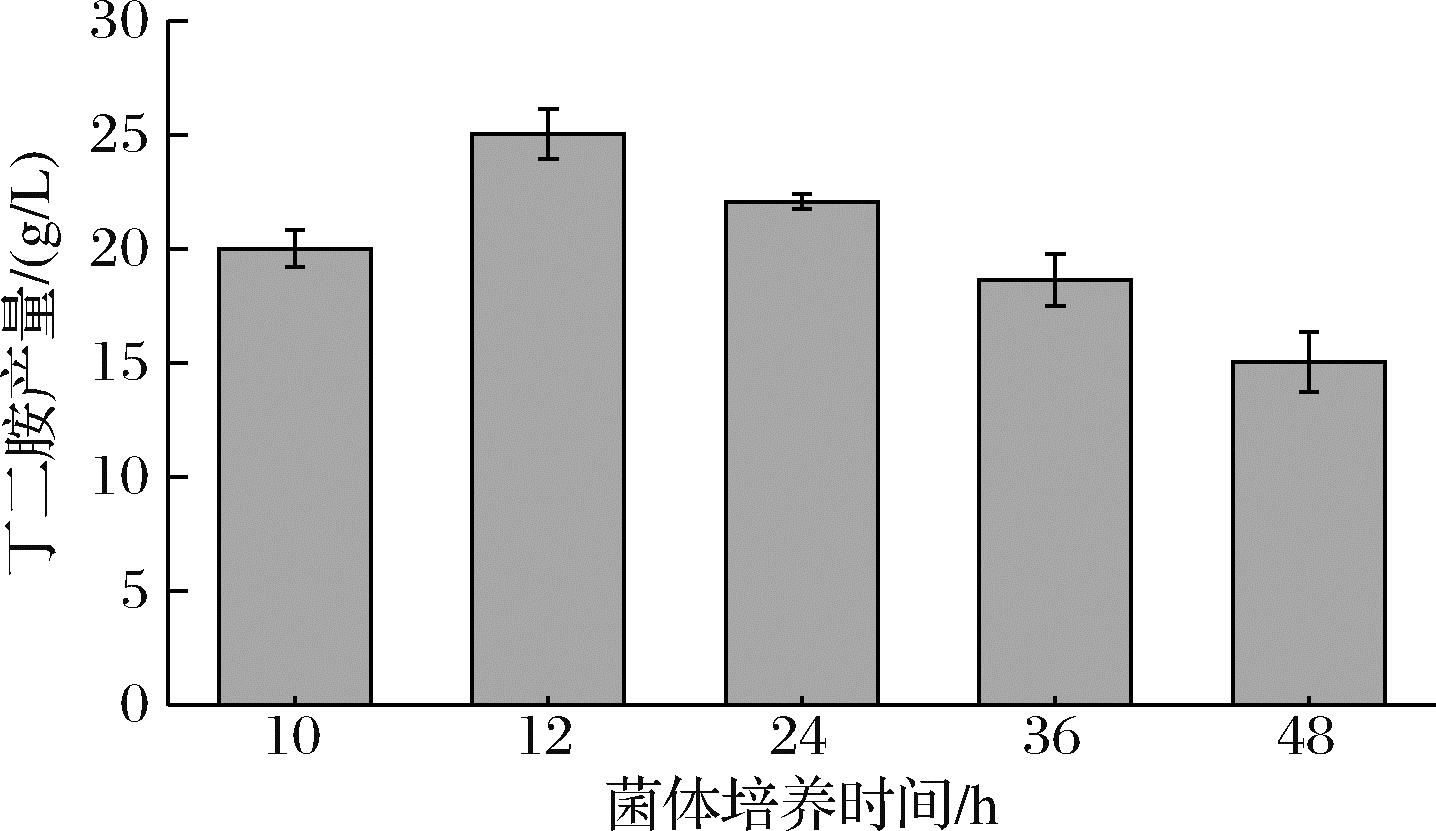
图6 不同菌体培养时间对丁二胺合成影响
Fig.6 Effect of different incubation times of bacteria on the synthesis of putrescine
2.4 透性化细胞丁二胺合成过程强化
2.4.1 不同菌体量对丁二胺合成的影响
菌体量在一定程度上反应了催化体系中酶的含量,出于催化效率以及经济的考虑,将菌体量控制在适宜的浓度对于催化反应来说至关重要。使用不同的菌体量进行催化,结果如图7所示,随着催化体系中菌体量的提高,丁二胺产量也随之一起增长,这可能是由于菌体量的提高增加了体系中酶的含量,从而提升了催化效率。当催化体系中菌体OD600值为50时,丁二胺的产量达到29.77 g/L,继续增加菌体浓度虽然丁二胺产量仍有一定的提高,但其提升幅度较小。因此,出于经济成本的考虑,催化体系选择OD600值为50作为最适催化菌体添加量。
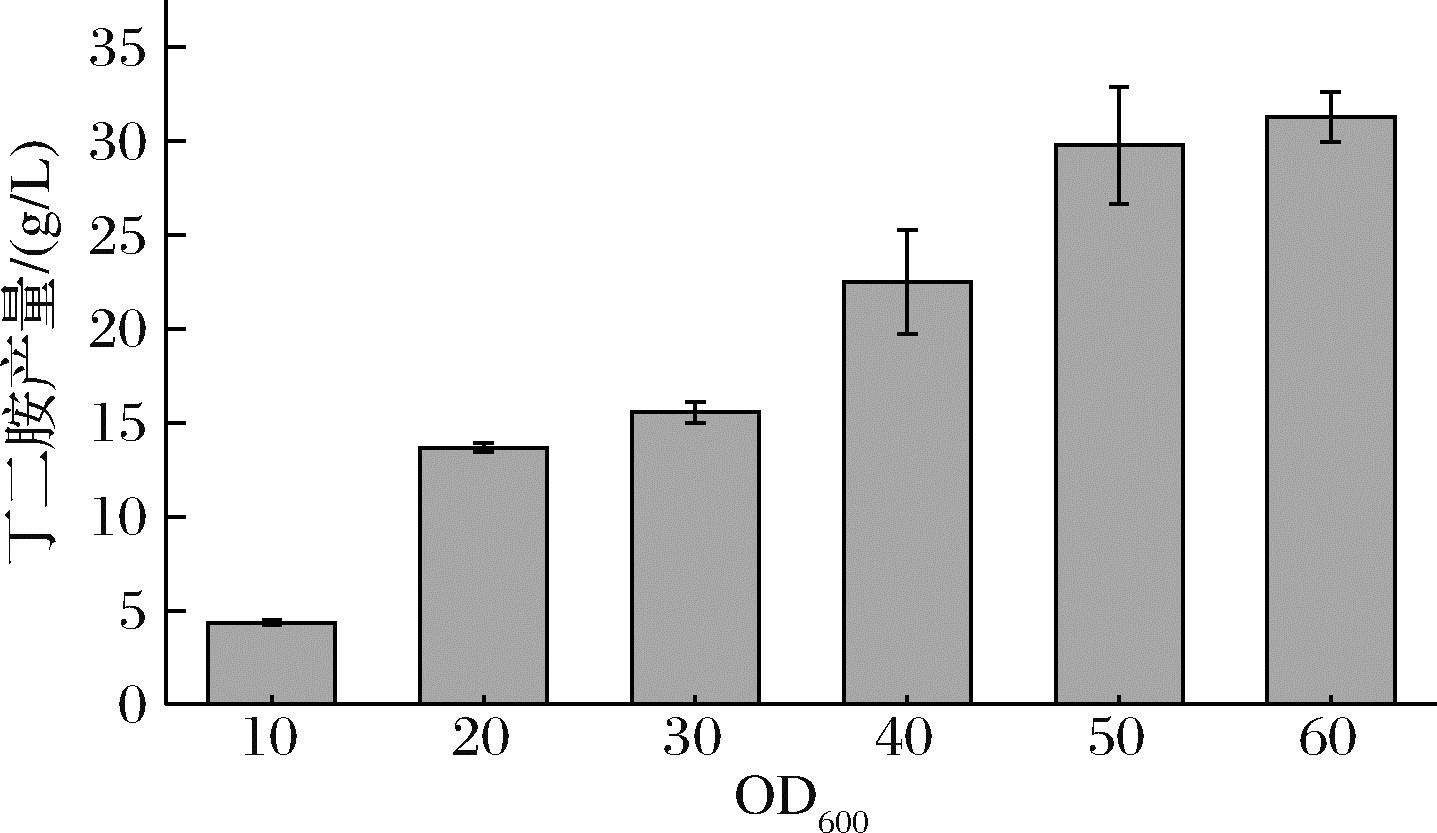
图7 不同菌体量对丁二胺合成影响
Fig.7 Effect of different amounts of bacteria on the synthesis of putrescine
2.4.2 不同金属离子浓度对丁二胺合成的影响
SUZUKI等[19]的研究表明,Mg2+可以促进精氨酸脱羧酶对L-精氨酸的利用。在催化过程中加入不同浓度的Mg2+,结果如图8-a所示,随着Mg2+浓度的增加,丁二胺的产量也随之提高,当Mg2+浓度达到4 mmol/L时,丁二胺产量达到最高值43.40 g/L。因此,Mg2+的最适添加浓度为4 mmol/L。Mn2+是胍丁胺酶SpeB催化中间产物胍基丁胺合成丁二胺时的辅因子[20]。因此,添加适当浓度的Mn2+对于丁二胺的合成起一定的促进作用。加入不同浓度的Mn2+进行催化,结果如图8-b所示,随着Mn2+加入浓度的提高,丁二胺的产量也随之增加,当加入12 mmol/L的Mn2+时,丁二胺的产量达到最高值43.63 g/L。因此, Mn2+的最适添加浓度为12 mmol/L。
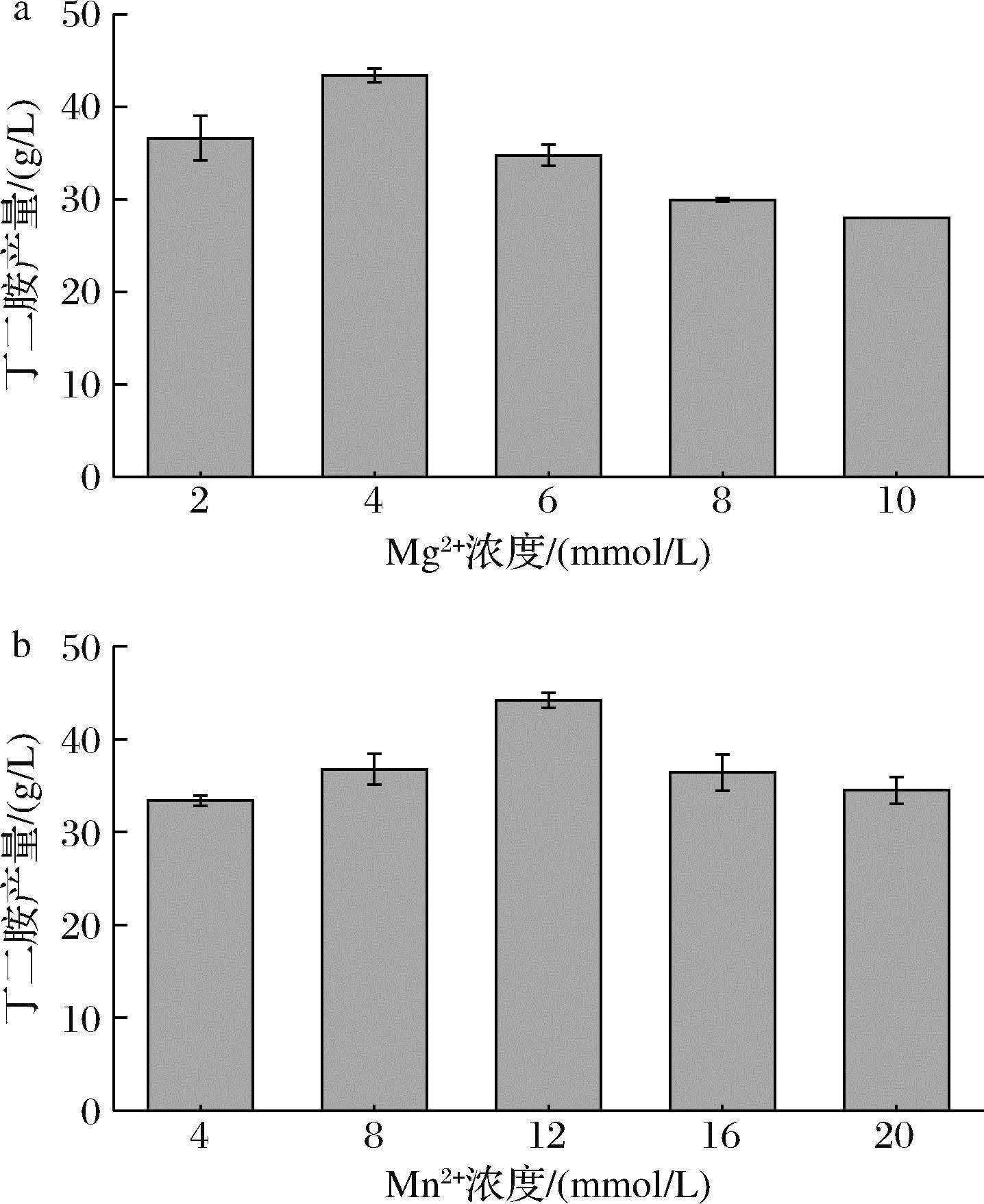
a-不同浓度Mg2+对丁二胺合成影响; b-不同浓度Mn2+对丁二胺合成影响
图8 不同浓度金属离子对丁二胺合成影响
Fig.8 Effect of different concentrations of metal ions on the synthesis of putrescine
2.4.3 底物添加量对丁二胺合成的影响
底物浓度是影响催化反应的一个重要参数,适当的底物浓度可以促进酶促反应的进行,但过高的底物浓度可能会对反应产生抑制。在丁二胺催化过程中加入不同浓度的L-精氨酸,结果如图9所示,随着底物浓度的提高,丁二胺产量也逐渐升高,当加入L-精氨酸质量浓度为160 g/L时丁二胺产量达到最高值88.67 g/L。但当底物质量浓度超过160 g/L时,其产量开始下降,这可能是由于高浓度的底物以及产物可能抑制了酶促反应的进行。此时对发酵液中残余的L-精氨酸进行检测,发现其实际消耗量仅为118 g/L,经计算丁二胺的摩尔转化率达到0.81 mol/mol,生产效率为2.46 g/(L·h)。因此,精氨酸的最适底物添加浓度为160 g/L。
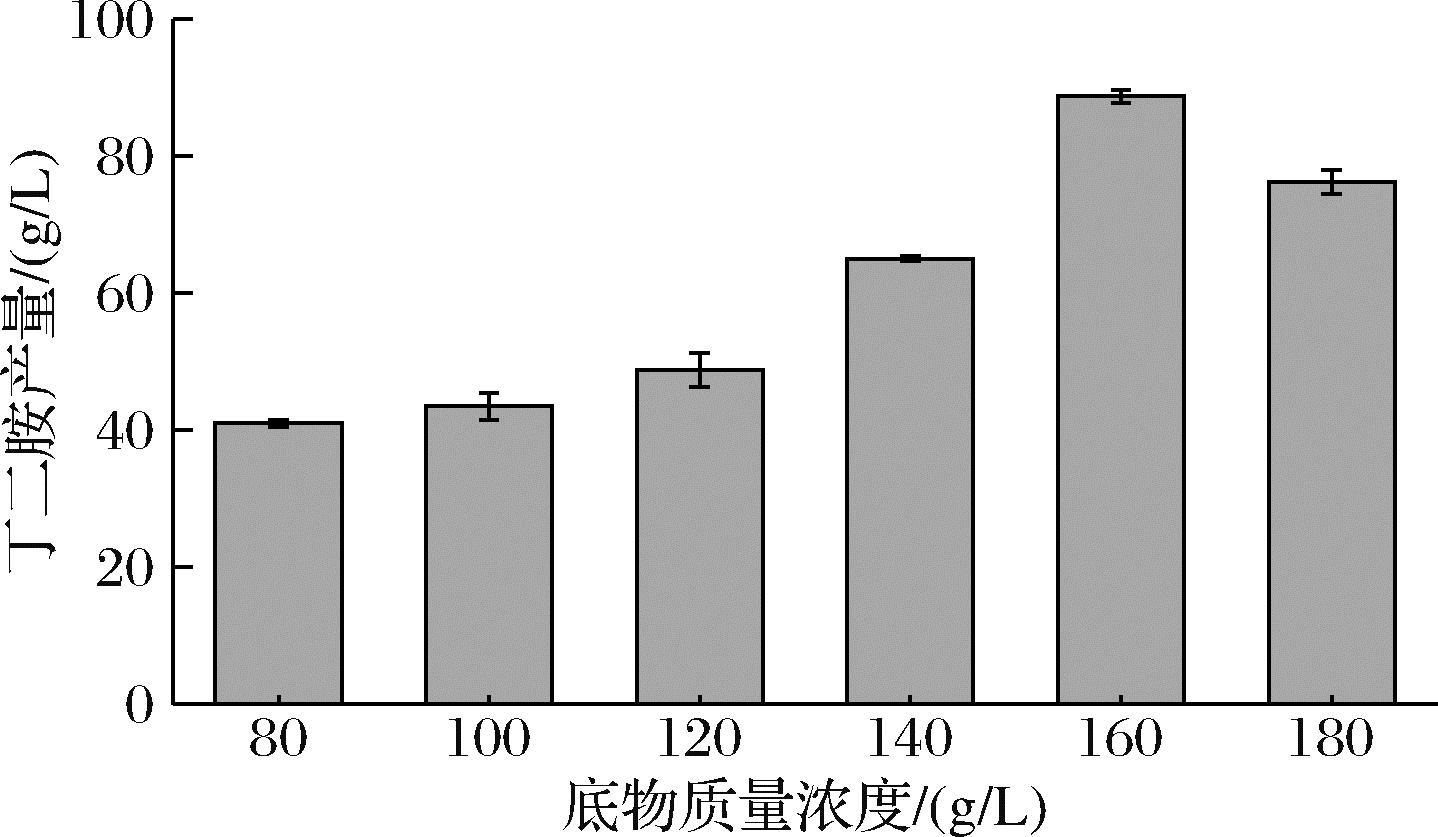
图9 不同底物浓度对丁二胺合成影响
Fig.9 Effect of different substrate concentrations on the synthesis of putrescine
3 结论与讨论
本研究通过透性化处理工程菌株以改变细胞膜通透性,并结合菌体培养和过程强化确定了全细胞催化的最适反应条件:30%乙醇处理,诱导时间3.5 h,菌体培养时间12 h,菌体量OD600值为50,Mg2+ 4 mmol/L,Mn2+ 12 mmol/L,L-精氨酸160 g/L。最终丁二胺产量达到已有报道的最高水平88.67 g/L,产物生产效率为2.46 g/(L·h),摩尔转化率0.81 mol/mol。与传统方法相比,本研究显著提升了丁二胺的合成能力。后续可针对精氨酸脱羧酶进行理性改造,并开展放大催化研究,以进一步提高其工业化应用能力。
[1] YAMANOBE T, KURIHARA Y, UEHARA H, et al.Structure and characterization of nylon 46[J].Journal of Molecular Structure, 2007, 829(1-3):80-87.
[2] 吴全德, 郝源增.新型尼龙46工程塑料的性能及应用[J].工程塑料应用, 2000, 28(11):31-33.WU Q D, HAO Y Z.Property and application of new engineering plastics nylon 46[J].Engineering Plastics Application, 2000, 28(11):31-33.
[3] 赵晓. 高分子量聚己二酰丁二胺的合成工艺及性能研究[D].郑州:郑州大学, 2014.ZHAO X.Study on synthesis technology and properties of high molecular weight poly(tetramethylene adipamide)[D].Zhengzhou:Zhengzhou University, 2014.
[4] CHAE T U, AHN J H, KO Y S, et al.Metabolic engineering for the production of dicarboxylic acids and diamines[J].Metabolic Engineering, 2020, 58:2-16.
[5] QIAN Z G, XIA X X, LEE S Y.Metabolic engineering of Escherichia coli for the production of putrescine:A four carbon diamine[J].Biotechnology and Bioengineering, 2009, 104(4):651-662.
[6] NGUYEN A Q D, SCHNEIDER J, REDDY G K, et al.Fermentative production of the diamine putrescine:System metabolic engineering of Corynebacterium glutamicum[J].Metabolites, 2015, 5(2):211-231.
[7] LI Z, SHEN Y P, JIANG X L, et al.Metabolic evolution and a comparative omics analysis of Corynebacterium glutamicum for putrescine production[J].Journal of Industrial Microbiology &Biotechnology, 2018, 45(2):123-139.
[8] THONGBHUBATE K, IRIE K, SAKAI Y M, et al.Improvement of putrescine production through the arginine decarboxylase pathway in Escherichia coli K-12[J].AMB Express, 2021, 11(1):168.
[9] LI G H, HUANG D X, WANG L, et al.Highly efficient whole-cell biosynthesis of putrescine by recombinant Escherichia coli[J].Biochemical Engineering Journal, 2021, 166:107859
[10] HUI H J, BAI Y J, FAN T P, et al.Biosynthesis of putrescine from L-arginine using engineered Escherichia coli whole cells[J].Catalysts, 2020, 10(9):947.
[11] 随树珍. 生物转化法合成1,4-丁二胺大肠杆菌工程菌的构建[D].天津:天津科技大学, 2016.SUI S Z.Construction of recombinant Escherichia coli for production of 1,4-blutyldiamine via biotransformation[D].Tianjin:Tianjin University of Science & Technology, 2016.
[12] YANG S C, TING W W, NG I S.Effective whole cell biotransformation of arginine to a four-carbon diamine putrescine using engineered Escherichia coli[J].Biochemical Engineering Journal, 2022, 185:108502.
[13] 王莉. 大肠杆菌生物法合成二元胺的机理研究[D].无锡:江南大学, 2023.WANG L.Biosynthesis of diamines in Escherichia coli[D].Wuxi:Jiangnan University, 2023.
[14] DE CARVALHO C C C R.Enzymatic and whole cell catalysis:Finding new strategies for old processes[J].Biotechnology Advances, 2011, 29(1):75-83.
[15] CHEN R R.Permeability issues in whole-cell bioprocesses and cellular membrane engineering[J].Applied Microbiology and Biotechnology, 2007, 74(4):730-738.
[16] 王艺颖, 董钰漫, 尹伟, 等.全细胞生物催化过程强化的研究进展[J].化学通报, 2020, 83(10):875-882.WANG Y Y, DONG Y M, YIN W, et al.Progress in the process intensification of whole-cell biocatalysis[J].Chemistry, 2020, 83(10):875-882.
[17] 刘宇轩. 基于赖氨酸脱羧酶的高纯度戊二胺的合成工艺开发[D].天津:天津大学, 2020.LIU Y X.Development of a process for the production of high-purified cadaverine based on lysine decarboxylase[D].Tianjin:Tianjin University, 2020.
[18] 王越, 李江华, 堵国成, 等.L-氨基酸脱氨酶的分子改造及其用于全细胞催化法生产α-酮戊二酸条件的优化[J].中国生物工程杂志, 2019, 39(3):56-64.WANG Y, LI J H, DU G C, et al.Molecular modification of L-amino acid deaminase and optimization of α-ketoglutaric acid production by whole-cell biocatalysis[J].China Biotechnology, 2019, 39(3):56-64.
[19] SUZUKI H, THONGBHUBATE K, MURAOKA M, et al.Agmatine production by Escherichia coli cells expressing SpeA on the extracellular surface[J].Enzyme and Microbial Technology, 2023, 162:110139.
[20] MATURANA P, ORELLANA M S, HERRERA S M, et al.Crystal structure of Escherichia coli agmatinase:Catalytic mechanism and residues relevant for substrate specificity[J].International Journal of Molecular Sciences, 2021, 22(9):4769.