漆酶,属于多酚氧化酶,能够以氧分子作为最终电子受体,以此来催化酚类、芳香类、苯胺类以及抗坏血酸等化合物[1]。漆酶的分子结构包含4种铜离子,通常分为3种类型:1型(T1)、2型(T2)和两种3型(T3)铜离子。1型铜蛋白为电子传递蛋白,2型铜蛋白一般处于配位不饱和状态,所以能够结合底物分子,进行催化反应。3型铜蛋白较为特殊,其活性中心包含两个铜离子,并且两个铜离子之间存在很强的相互作用[2]。铜是机体蛋白质和酶的重要组分[3],也是组装含铜蛋白所必需的,微量补充铜可以增强漆酶活性。一般情况下,微生物对铜离子的需求极低,以游离状态存在的铜离子浓度过高,会对微生物产生极强的毒性[4]。而漆酶是为数不多,被鉴定为拥有铜耐受性的蛋白[5-7]。针对这一特性进行研究,能够探索细菌漆酶表达量的最优条件。
当前众多研究表明分子改造技术与铜离子激发可以提高漆酶表达量与酶活性。DAI等[8]采用易错PCR技术获得lac2-9,优化后的突变酶lac2-9的表达量较未优化前提高了(22±2)%;WANG等[9]通过定点突变,构建芽孢杆菌漆酶突变体D501G,漆酶表达量略有提高;ZHENG等[10]发现细菌Proteus hauseri ZMd44可在硫酸铜诱导下产生McoA-漆酶,漆酶表达量随着铜浓度的少量提升有所提高;MURUGESAN等[11]发现芽孢杆菌属PK4在所测试的诱导剂中,0.1 mmol/L的硫酸铜使漆酶表达量最大化,有效提高了漆酶的表达量;MALHOTRA等[12]发现培养过程中添加0.1 mmol/L CuSO4使γ-变形菌JB的漆酶表达量增加13倍。但迄今为止,以枯草芽孢杆菌漆酶基因在大肠杆菌中进行异源表达为基础,探究重组菌漆酶表达量受铜离子浓度影响的研究还相对较少。
通过控制铜离子添加量,探究重组CotA漆酶及突变细菌漆酶I421A、T466A、K464A表达菌株菌体浓度与漆酶表达量的变化。探究铜离子添加量对菌株生长和漆酶表达量的影响。通过分析突变细菌漆酶分子结构的不同,解析不同内部结构的细菌漆酶表达量受铜离子添加量的影响。期望进一步优化铜离子浓度对重组细菌漆酶及突变细菌漆酶表达量的诱导条件,为细菌漆酶的工业应用提供帮助。
1 材料与方法
1.1 材料
1.1.1 菌株
重组CotA漆酶表达菌株;突变CotA漆酶I421A、T466A、K464A、C492A表达菌株(均保藏于安徽科技学院生命与健康科学学院实验室);大肠杆菌BL21(DE3)。
1.1.2 试剂
CuSO4(分析纯)、十二烷基硫酸钠(Sodium dodecyl sulfate,SDS,化学纯),国药集团化学试剂有限公司;1.5 mol/L Tris-HCl(pH 8.8)、甘氨酸、考马斯亮蓝-250,上海源叶生物科技有限公司;LB培养基,上海生工生物工程股份有限公司;氨基甲烷缓冲液(Tris),上海麦克林生化科技股份有限公司;过硫酸铵(分析纯)、溴酚蓝(分析纯),默克公司;β-巯基乙醇(分析纯),北京生物试剂公司;N-N-N′-N-四甲基乙二胺(N,N,N′,N′-tetramethylethylenediamine,TEMED,分析纯),上海碧云天生物技术股份有限公司。
1.1.3 仪器与设备
XS-ZD1小型组合式全温振荡培养箱,象尚昱科(上海)实验仪器有限公司;KS-650DN超声波细胞粉碎机,昆山洁力美超声仪器有限公司;UV-2600紫外可见分光光度计,岛津仪器(苏州)有限公司;AKTA purifier UPC10×蛋白快速纯化系统,GE医疗集团;Eco-Mini垂直电泳转印系统,德国耶拿分析仪器股份公司。
1.2 方法
1.2.1 CotA漆酶
来自枯草芽孢杆菌的cotA漆酶基因(来自GenBank数据库),GeneID:936 023。
1.2.2 菌株培养
重组CotA漆酶,突变漆酶I421A、T466A、K464A、C492A低温保存菌株接种于LB液体培养基,添加硫酸卡那霉素(100 mg/mL),添加量为培养基体积的1‰,振荡培养。活化菌液转接于LB液体培养基,添加硫酸卡那霉素(100 mg/mL),添加量为培养基体积的1‰,振荡培养。菌体浓度在OD600下达到0.6停止培养,添加1 mol/L IPTG,添加量为培养基体积的1‰,添加1 mol/L CuSO4溶液,添加量为培养基体积的1‰,振荡培养。
1.2.3 诱导条件优化
1.2.3.1 诱导时间
诱导36 h,间隔6 h取少量菌液。诱导24~36 h,每2 h使用ABTS检测培养基是否存在酶活反应。
1.2.3.2 铜离子添加量
诱导步骤添加不同量的CuSO4溶液,铜离子终浓度分别为:0.25、0.5、1、1.5、2 mmol/L。
1.2.4 漆酶表达量测定与验证
1.2.4.1 菌株的漆酶表达量
定量菌株:重组CotA漆酶表达菌株,突变CotA漆酶I421A,T466A,K464A表达菌株用于实验的菌体质量一致,即1 g菌体。
定量菌液:重组CotA漆酶表达菌株,突变CotA漆酶I421A、T466A、K464A表达菌株用于实验的菌液体积一致,即50 mL菌液。
1.2.4.2 漆酶纯化
破碎液使用高速离心机去杂,过孔径0.22 μm过滤薄膜。样品预处理:100 mL样品中添加0.17 mL 1 mol/L Tris-Hcl溶液,0.438 3 g NaCl,4.2 mL 500 mmol/L咪唑溶液。使用HisTrap FF crude 5 mL预装柱,配合AKTA purifier层析系统进行蛋白纯化。上样缓冲液:25 mmol/L咪唑溶液,洗脱液:500 mmol/L咪唑溶液。脱盐使用amicon ultra超滤管(50 000 MWCO),1×PBS缓冲液置换咪唑溶液。
以ABTS作为反应物,在紫外分光光度计动力学模式,420 nm波长下检测漆酶活性。酶活力计算如公式(1)所示:
酶活力![]()
(1)
式中:A2,漆酶与ABTS反应过程中最接近0.2的数值;A1,漆酶与ABTS反应过程中最接近0.15的数值。
1.2.4.3 SDS-PAGE
使用SDS-PAGE蛋白凝胶电泳对纯化效果及蛋白含量进行验证。PCR管中加入4 μL SDS-PAGE加样缓冲液(5×)与16 μL待测蛋白酶液,高温加热使蛋白变性。分离胶浓度为12%(体积分数),浓缩胶浓度为5%(体积分数),染色使用考马斯亮蓝R-250染色液,脱色使用考马斯亮蓝染色脱色液。
1.2.5 漆酶的三维结构模拟
1.2.5.1 建模所需的材料与网站
供试材料CotA细菌漆酶cDNA序列(1 542 bp,NCBI登录号为NC-000 964.3),氨基酸序列 (513AA)。
1.2.5.2 CotA细菌漆酶突变体的三维结构模拟
通过蛋白质序列网络对CotA细菌漆酶的氨基酸序列进行结构分析,利用PyMOL软件进行三维结构建模。将CotA细菌漆酶的氨基酸序列提交到蛋白质序列网络,进行结构预测,与已有文献报道的CotA漆酶结构进行比较。通过PyMOL软件,以单模板法构建CotA细菌漆酶的三维结构模型,进行结构分析。
2 结果与分析
2.1 诱导条件优化
由图1可知,菌株在诱导的30~36 h菌体浓度开始下降或无明显增长,而添加铜离子浓度为2 mmol/L时,菌体浓度的下降提前至24 h。可能是铜离子虽然具有促进漆酶合成作用,但对菌株的生长也有抑制作用[13-14]。添加铜离子浓度越高抑制作用可能越强,过高铜离子浓度可能会形成毒性作用[15-16]。
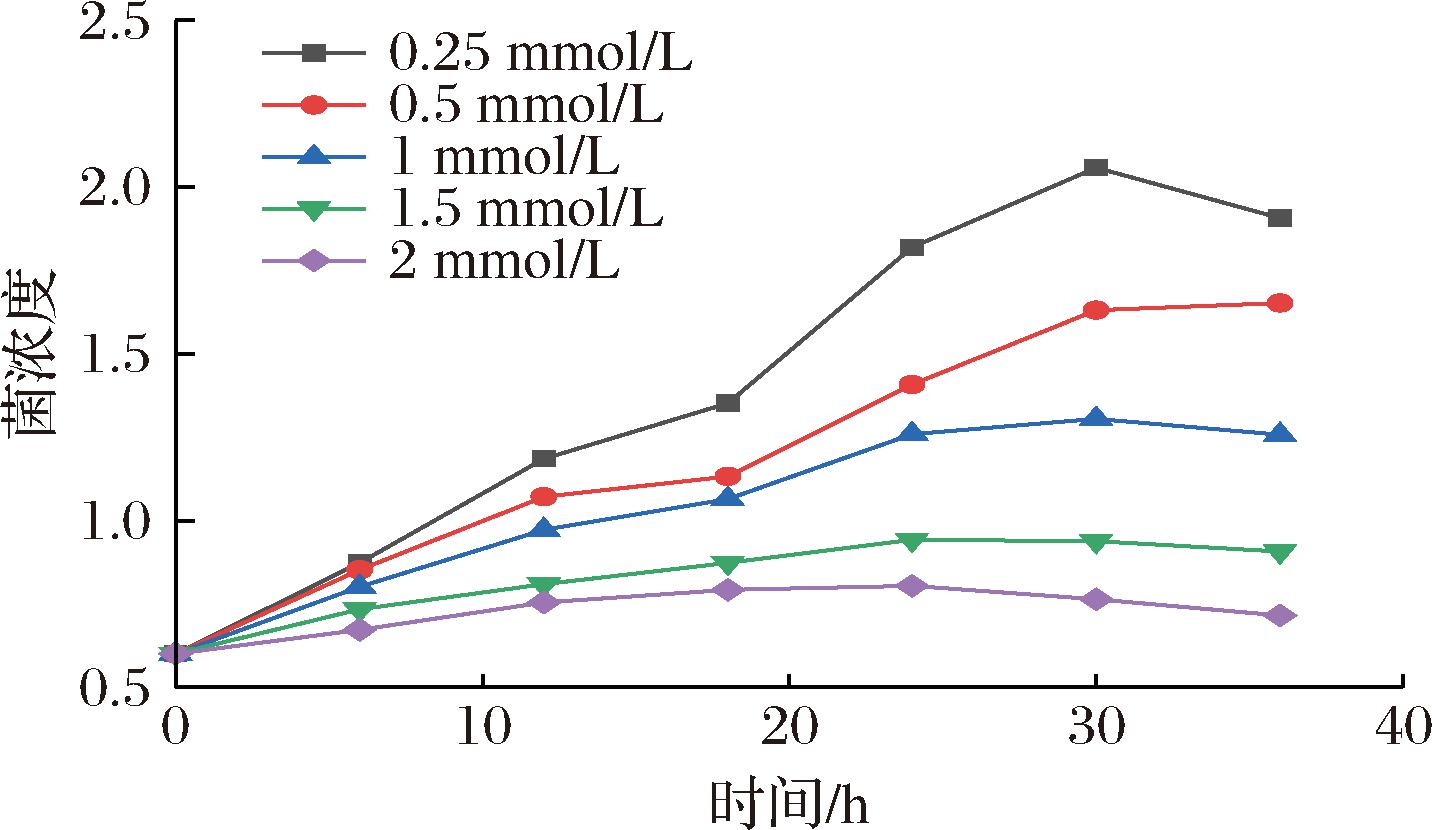
图1 不同铜离子浓度下重组CotA漆酶表达菌株菌体浓度变化
Fig.1 Changes in cell density of the recombinant CotA laccase- expressing strain under different copper ion concentrations
菌株的细胞膜拥有保护和物质转运的能力,且漆酶菌株似乎具有一定的铜离子耐受性[17]。可能是在诱导初期,菌株正常生长。诱导中期,菌株进入生长平稳期和衰退期。诱导后期,菌株出现死亡并开始破裂。诱导的第30 h,液体培养基中检测出的酶活反应似乎一定程度上证明了这个推测。综合上述现象,可能是随着诱导时间延长,漆酶形成过程中所需的游离态Cu2+趋于饱和,剩余Cu2+仍在菌株内逐渐累积,最终导致菌株死亡破裂。而诱导初期加入的铜离子越多,菌株死亡时间也相应提前。该推测与FOWLER等[18]的研究结果相似。因此菌株的诱导时间选择菌浓度较高,且培养基中无酶活反应的28 h较好。
2.2 不同铜离子添加量下表达菌株的漆酶活力
2.2.1 定量菌株的漆酶活力
由图2和图3可知,重组CotA漆酶表达菌株在添加铜离子浓度为1 mmol/L时破碎液漆酶活性较高,达到2 207 U/mL,相较于添加铜离子浓度为0.25 mmol/L时的241 U/mL提高约8.2倍;突变细菌漆酶I421A表达菌株在添加铜离子浓度为1.5 mmol/L时破碎液漆酶活性较高,达到631 U/mL,相较于添加铜离子浓度为0.25 mmol/L时的52 U/mL提高11.1倍;突变细菌漆酶T466A表达菌株在添加铜离子浓度为1.5 mmol/L时破碎液漆酶活性较高,达到852 U/mL,相较于添加铜离子浓度为0.25 mmol/L时的114 U/mL提高约6.5倍;突变细菌漆酶K464A表达菌株在添加铜离子浓度为1 mmol/L时破碎液漆酶活性较高,达到295 U/mL,相较于添加铜离子浓度为0.25 mmol/L时的16 U/mL提高约17.0倍。由此推测,重组CotA漆酶表达菌株,突变漆酶I421A、T466A、K464A表达菌株,在0.25 mmol/L低铜离子浓度下,单个表达菌株的漆酶表达量均低于1 mmol/L 或1.5 mmol/L铜离子浓度下,单个表达菌株的漆酶表达量。
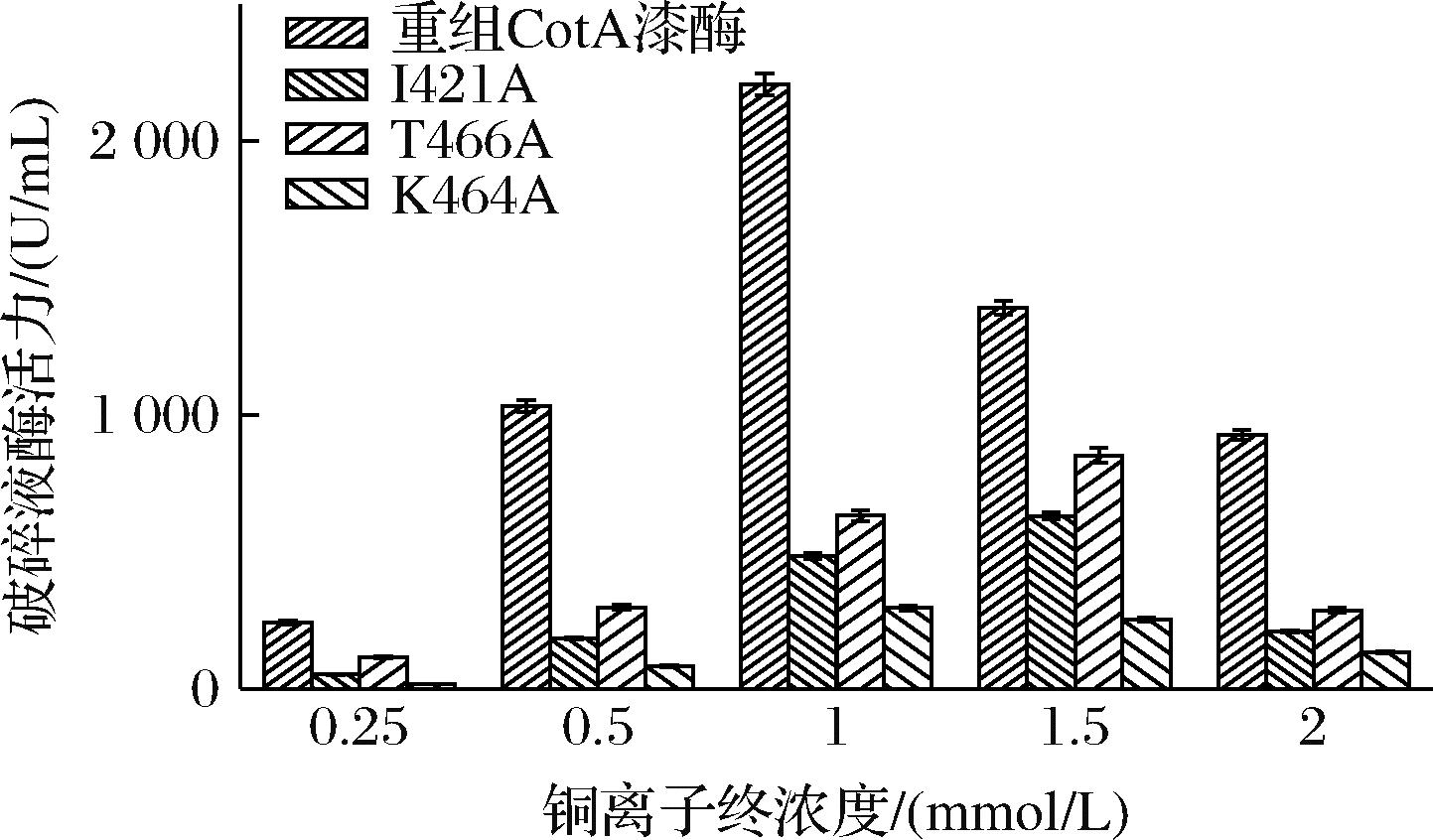
图2 不同铜离子浓度对定量菌株破碎液漆酶活性的影响
Fig.2 Effects of different copper ion concentrations on laccase activity in cell lysates of the mutant strains
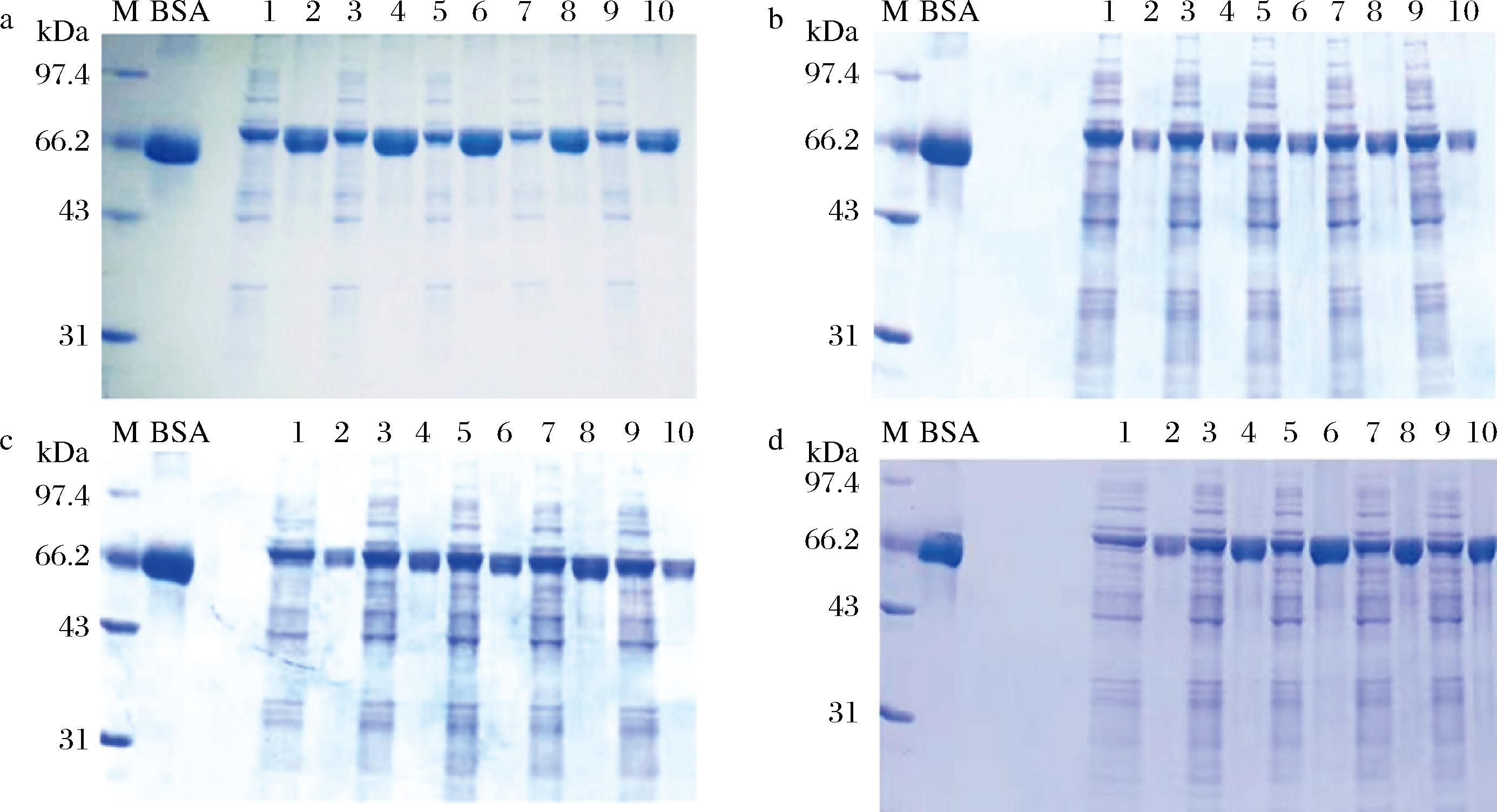
a-重组CotA漆酶;b-突变细菌漆酶I421A;c-突变细菌漆酶T466A;d-突变细菌漆酶K464A
图3 四种表达菌株破碎液及纯化漆酶SDS-PAGE图谱
Fig.3 SDS-PAGE analysis of cell lysates and purified laccase from four expressing strains
注:M-Marker(14.4~97.4 kDa);BSA牛血清蛋白(66.43 kDa)1-添加0.25 mmol/L铜离子破碎液;2-添加0.25 mmol/L铜离子漆酶;3-添加0.5 mmol/L铜离子破碎液;4-添加0.5 mmol/L铜离子漆酶;5-添加1 mmol/L铜离子破碎液;6-添加1 mmol/L铜离子漆酶;7-添加1.5 mmol/L铜离子破碎液;8-添加1.5 mmol/L铜离子漆酶;9-添加2 mmol/L铜离子破碎液;10-添加2 mmol/L铜离子漆酶(下同)。
2.2.2 定量菌液的漆酶活力
由图4可知,重组CotA漆酶表达菌株在添加铜离子浓度为0.5 mmol/L时菌体浓度较高,达到1.533,相较于添加铜离子浓度为2.0 mmol/L时的1.043提高约47%;突变细菌漆酶I421A表达菌株在添加铜离子浓度为0.5 mmol/L时菌体浓度较高,达到1.527,相较于添加铜离子浓度为2 mmol/L时的1.207提高约26%;突变细菌漆酶T466A表达菌株在添加铜离子浓度为0.25 mmol/L时菌体浓度较高,达到1.694,相较于添加铜离子浓度为2 mmol/L时的1.203提高约41%;突变细菌漆酶K464A表达菌株在添加铜离子浓度为0.25 mmol/L时菌体浓度较高,达到1.620,相较于添加铜离子浓度为2 mmol/L时的0.610提高约166%。重组CotA漆酶表达菌株,突变漆酶I421A、T466A、K464A表达菌株均在2 mmol/L铜离子浓度下菌浓度较低。进一步证明,较高的铜离子浓度对表达菌株的生长有着抑制作用。
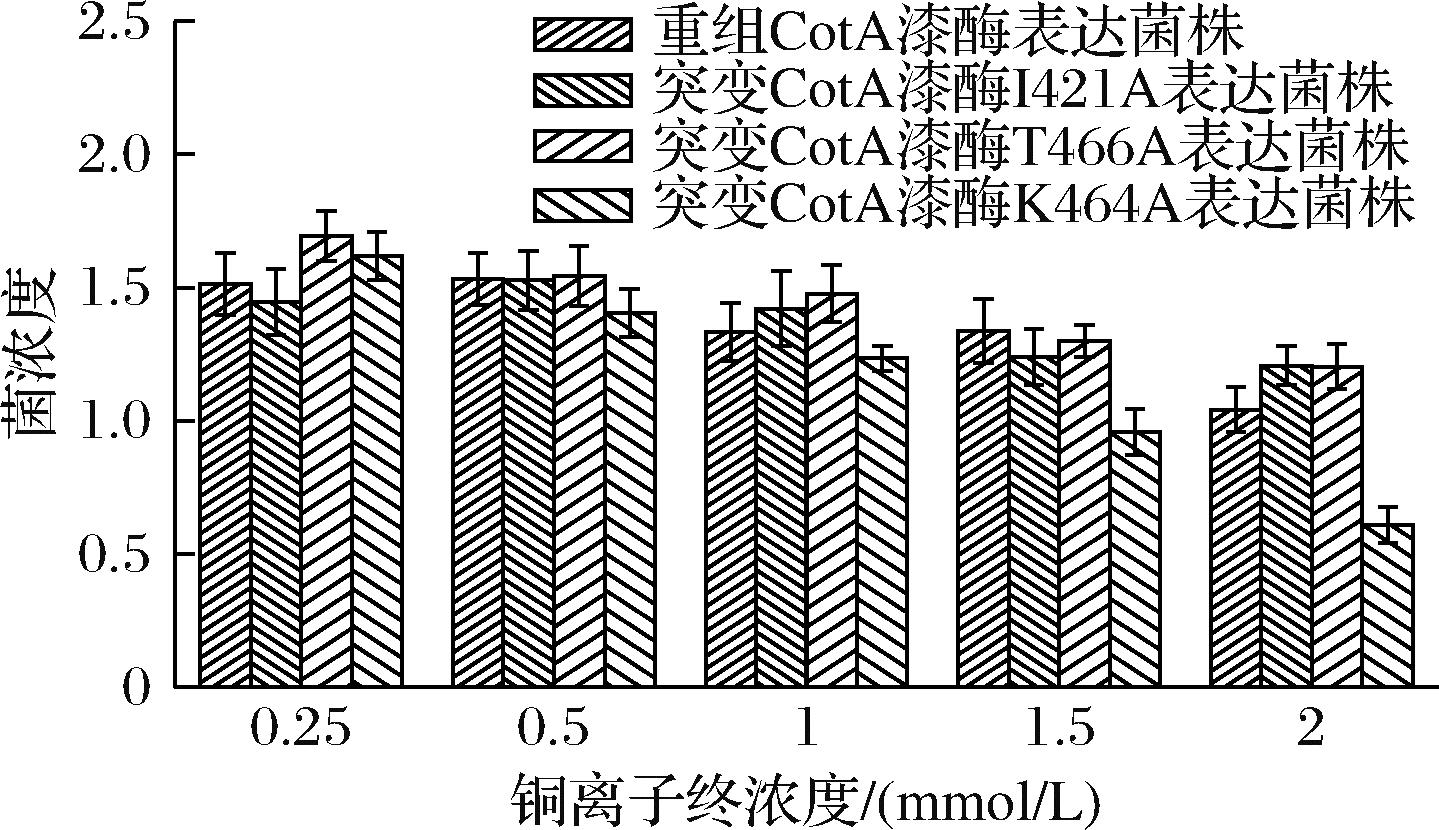
图4 添加不同铜离子浓度对表达菌株的生长影响
Fig.4 Impact of different copper ion concentrations on the growth of the expressing strains
由图5和图6可知,重组CotA漆酶表达菌株在添加铜离子浓度为1 mmol/L时破碎液漆酶活性较高,达到910 U/mL,相较于添加铜离子浓度为0.25 mmol/L时的135 U/mL提高约5.7倍;突变细菌漆酶I421A表达菌株在添加铜离子浓度为1 mmol/L时破碎液漆酶活性较高,达到245 U/mL,相较于添加铜离子浓度为0.25 mmol/L时的27 U/mL提高8.0倍;突变细菌漆酶T466A表达菌株在添加铜离子浓度为1.5 mmol/L时破碎液漆酶活性较高,达到336 U/mL,相较于添加铜离子浓度为0.25 mmol/L时的73 U/mL提高约3.6倍;突变细菌漆酶K464A表达菌株在添加铜离子浓度为1 mmol/L时破碎液漆酶活性较高,达到107 U/mL,相较于添加铜离子浓度为0.25 mmol/L时的11 U/mL提高约8.7倍。
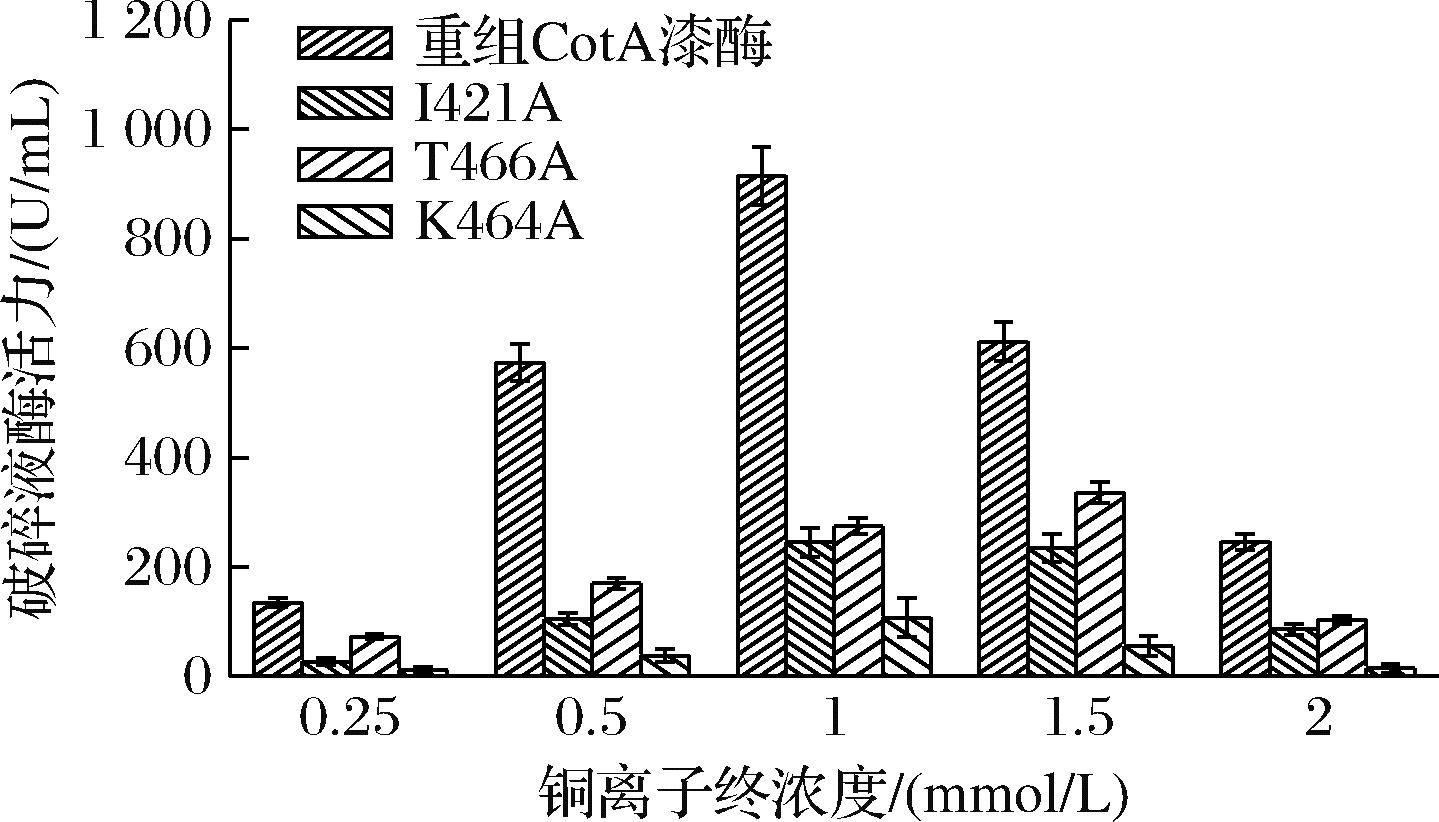
图5 添加不同铜离子浓度对定量菌液漆酶表达量的影响
Fig.5 Effects of different copper ion concentrations on laccase expression levels in quantified cell cultures
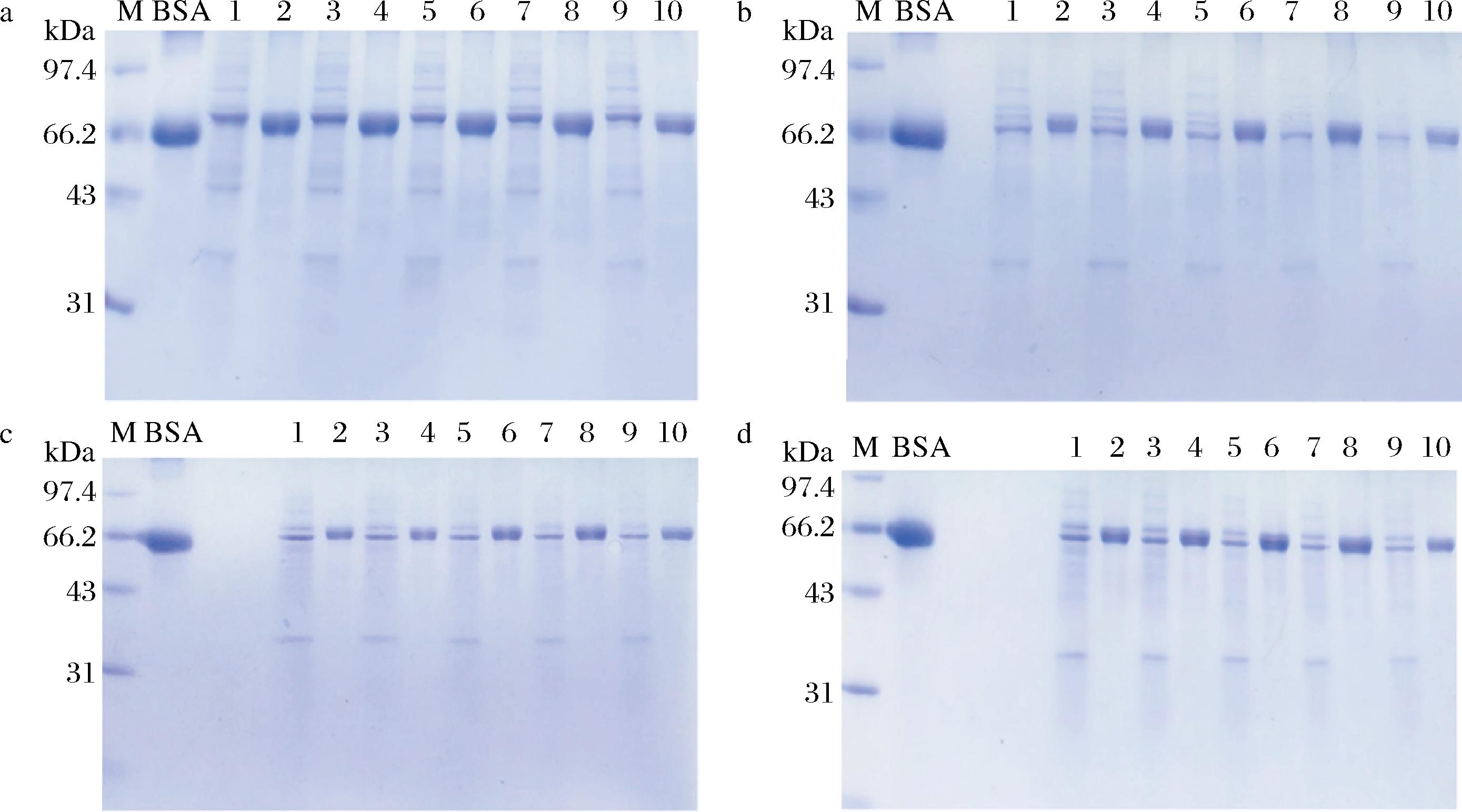
a-重组CotA漆酶;b-突变细菌漆酶I421A;c-突变细菌漆酶T466A;d-突变细菌漆酶K464A
图6 四种表达菌株破碎液及纯化漆酶SDS-PAGE图谱
Fig.6 SDS-PAGE analysis of cell lysates and purified laccase from four expressing strains
值得注意的是,突变细菌漆酶I421A表达菌株在定量菌株情况下,破碎液漆酶活性在铜离子浓度为1.5 mmol/L时较好。而在定量菌液情况下,可能由于1 mmol/L铜离子浓度对表达菌株的生长抑制低于1.5 mmol/L铜离子浓度,使突变细菌漆酶I421A表达菌株在1 mmol/L铜离子浓度下1.422的菌浓度,相较于1.5 mmol/L铜离子浓度下1.239的菌浓度高出15%。最终导致突变细菌漆酶I421A表达菌株在添加铜离子浓度为1 mmol/L时破碎液漆酶活性较高。故而,在进行铜离子添加量优化时,需根据不同的实验需求,考虑不同的影响因素。
2.3 CotA细菌漆酶突变体三维结构模拟分析
I421,T466,K464三个位点在CotA细菌漆酶结构中所在位置如图7所示。
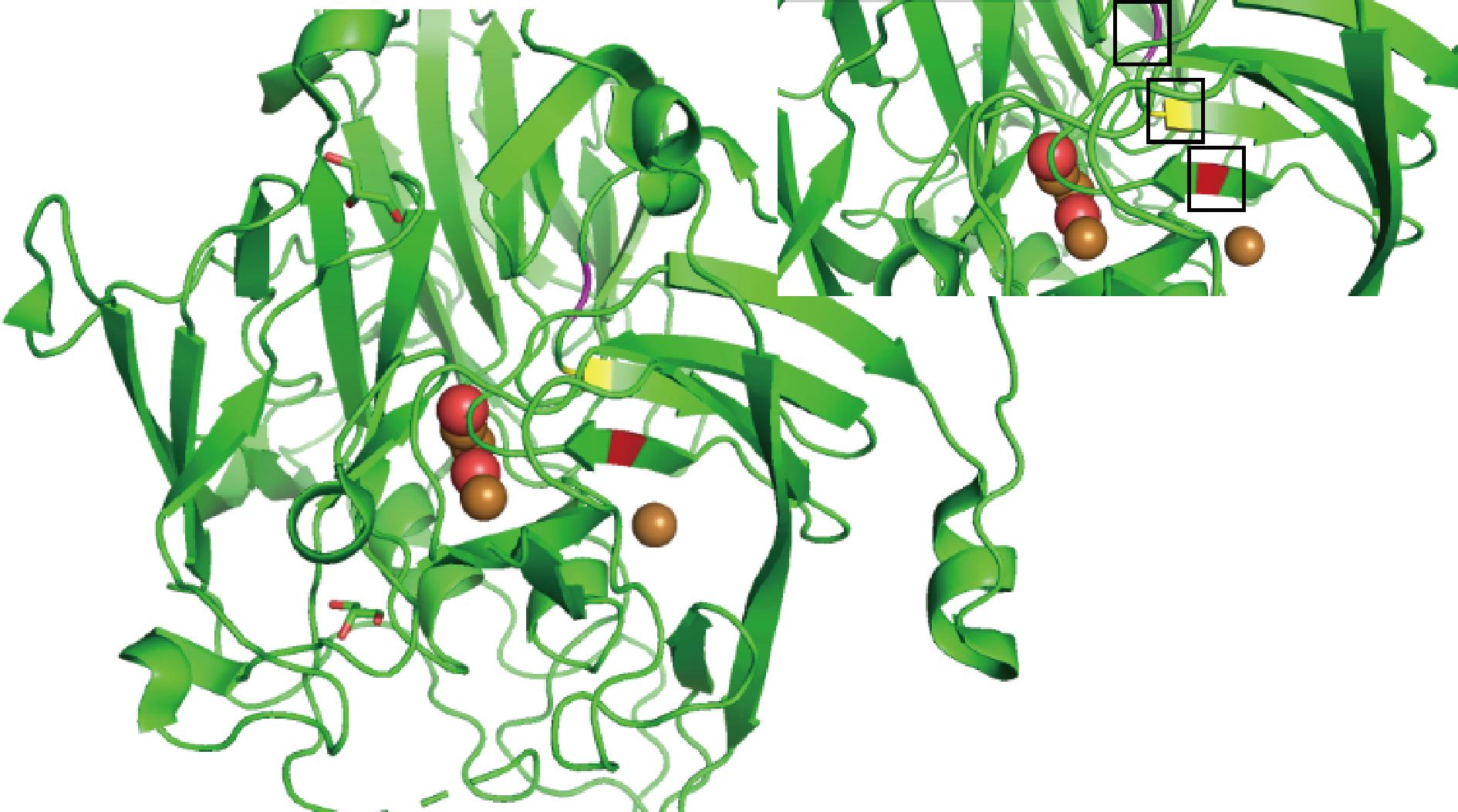
图7 PyMOL建模显示漆酶三维结构突变位点
Fig.7 PyMOL modeling showing mutation sites in the three-dimensional structure of laccase
注:红色,I421;黄色,T466;紫色,K464。
2.3.1 突变细菌漆酶I421
图8为I421位点突变前后结构示意图,421位点上的异亮氨酸(Ile)位于漆酶口袋结构反应中心通道首端,当突变为丙氨酸后,侧链变短,中心通道首端由窄变宽,导致T1铜位置附近结构发生变化,可能影响酶的折叠效率。突变细菌漆酶I421表达量降低,但影响程度小于突变细菌漆酶T466A。此结果与KOSCHORRECK等[19]在通过随机和定点诱变提高漆酶的功能性表达相似。
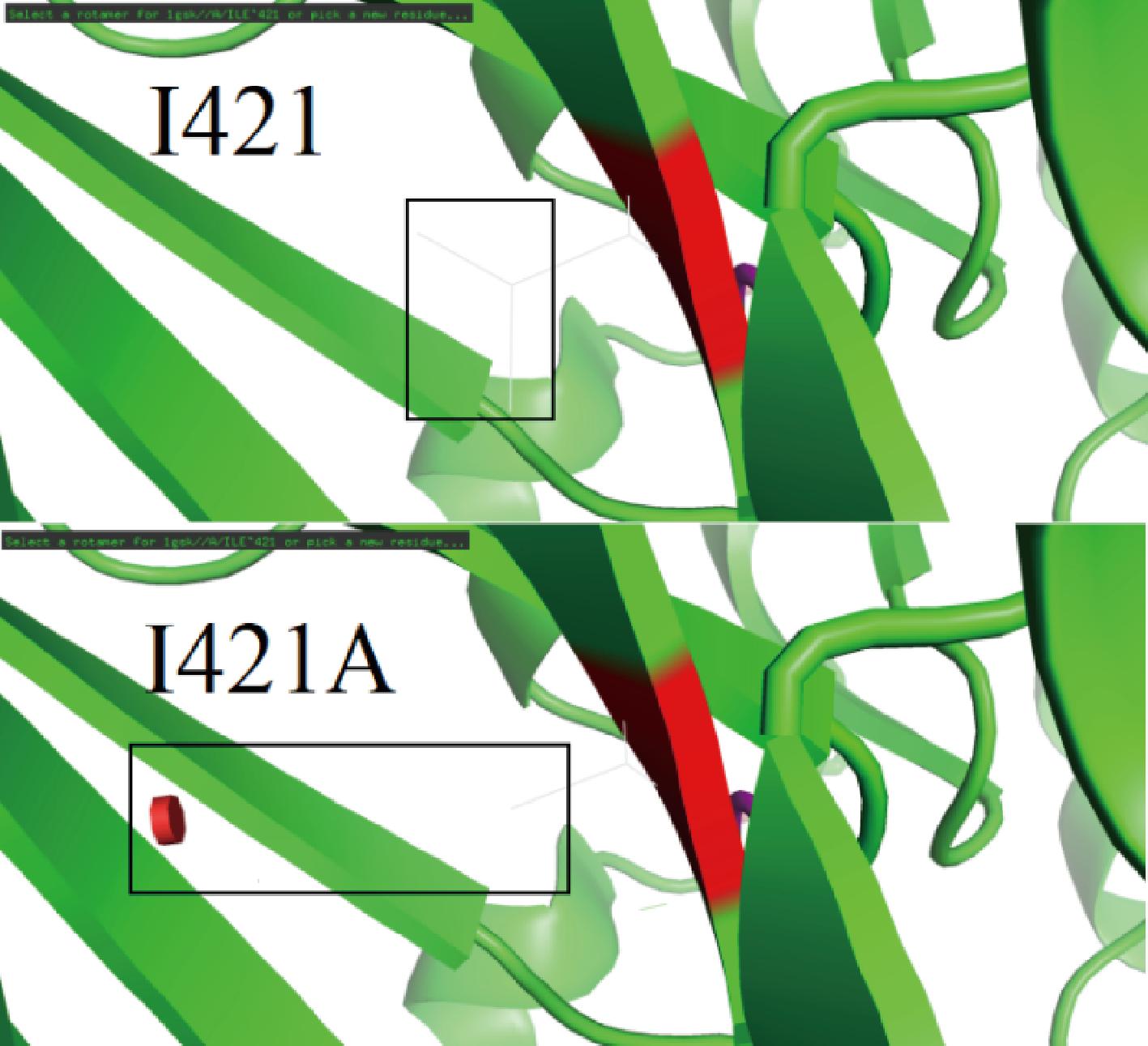
图8 突变体I421A突变前后三级结构模拟对比图
Fig.8 Comparison of the simulated tertiary structures of the I421A mutant before and after mutation
2.3.2 突变细菌漆酶T466
图9为T466位点突变前后结构示意图,466位点的苏氨酸位于漆酶口袋结构中心通道三簇铜反应中心的T2铜离子附近,由于T466位点离T1铜的距离比I421远,故而酶的有效折叠可能比与突变体I421低,导致漆酶表达量为3种突变细菌漆酶中最低的。
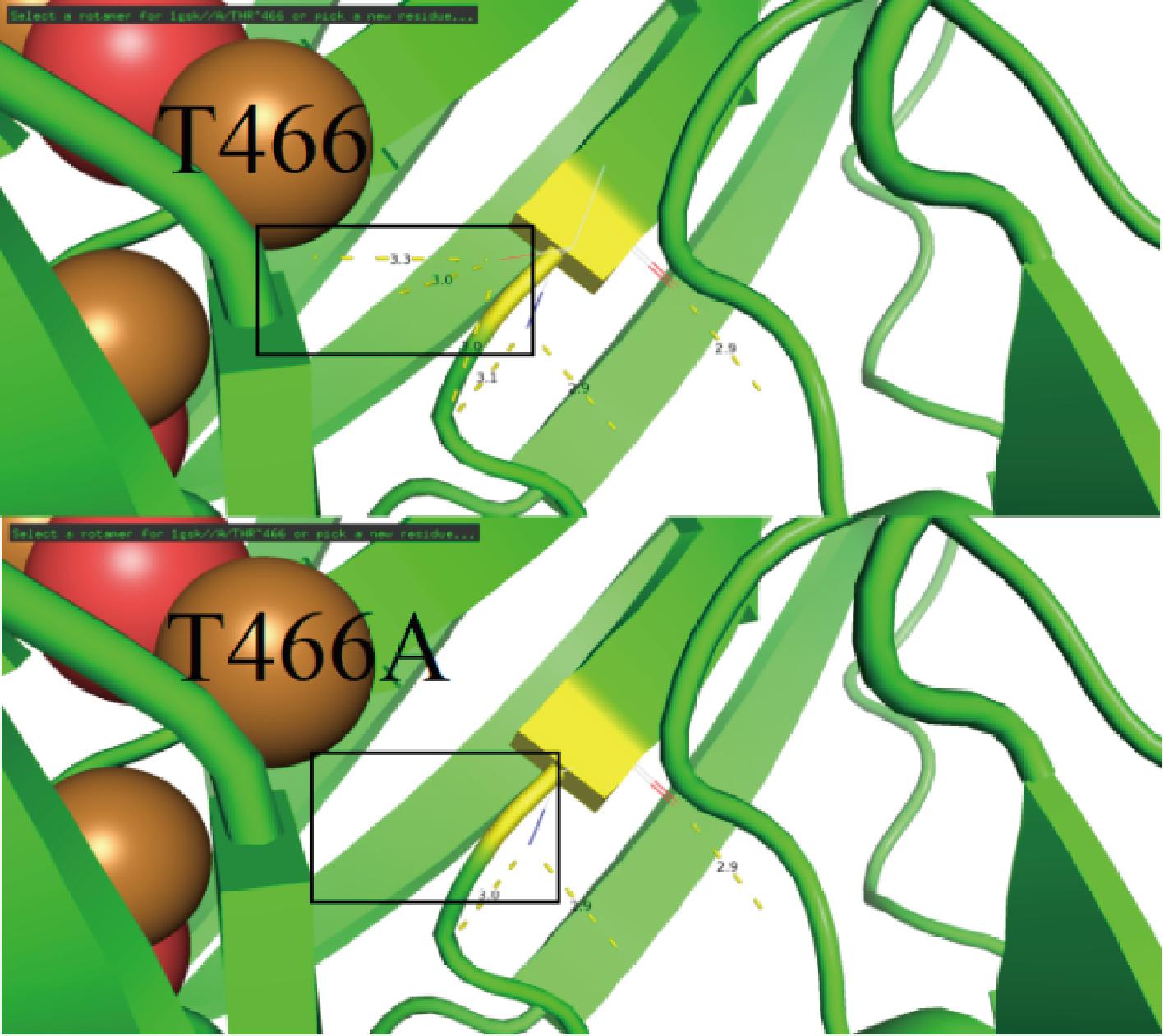
图9 突变体T466A突变后三级结构模拟对比图
Fig.9 Comparison of the simulated tertiary structures of the T466A mutant before and after mutation
2.3.3 突变细菌漆酶K464
图10为K464位点突变前后结构示意图,位于464位点漆酶反应口袋结构末端的赖氨酸(Lys)被替换为丙氨酸后,漆酶口袋结构反应中心通道末端背向通道处原本被挤压的亚基脱离挤压状态,导致了通道末端结构的变化,而通道末端具有还原或运输水分子的功能,原本亲水的赖氨酸变为疏水的丙氨酸后,蛋白质与水分子之间形成的疏水作用力有利于蛋白质的折叠。且赖氨酸的464位点在漆酶反应口袋结构末端,距离T1铜较远,对酶的折叠效率影响可能较低,故而突变体K464A表达量为3个突变细菌漆酶中最高。
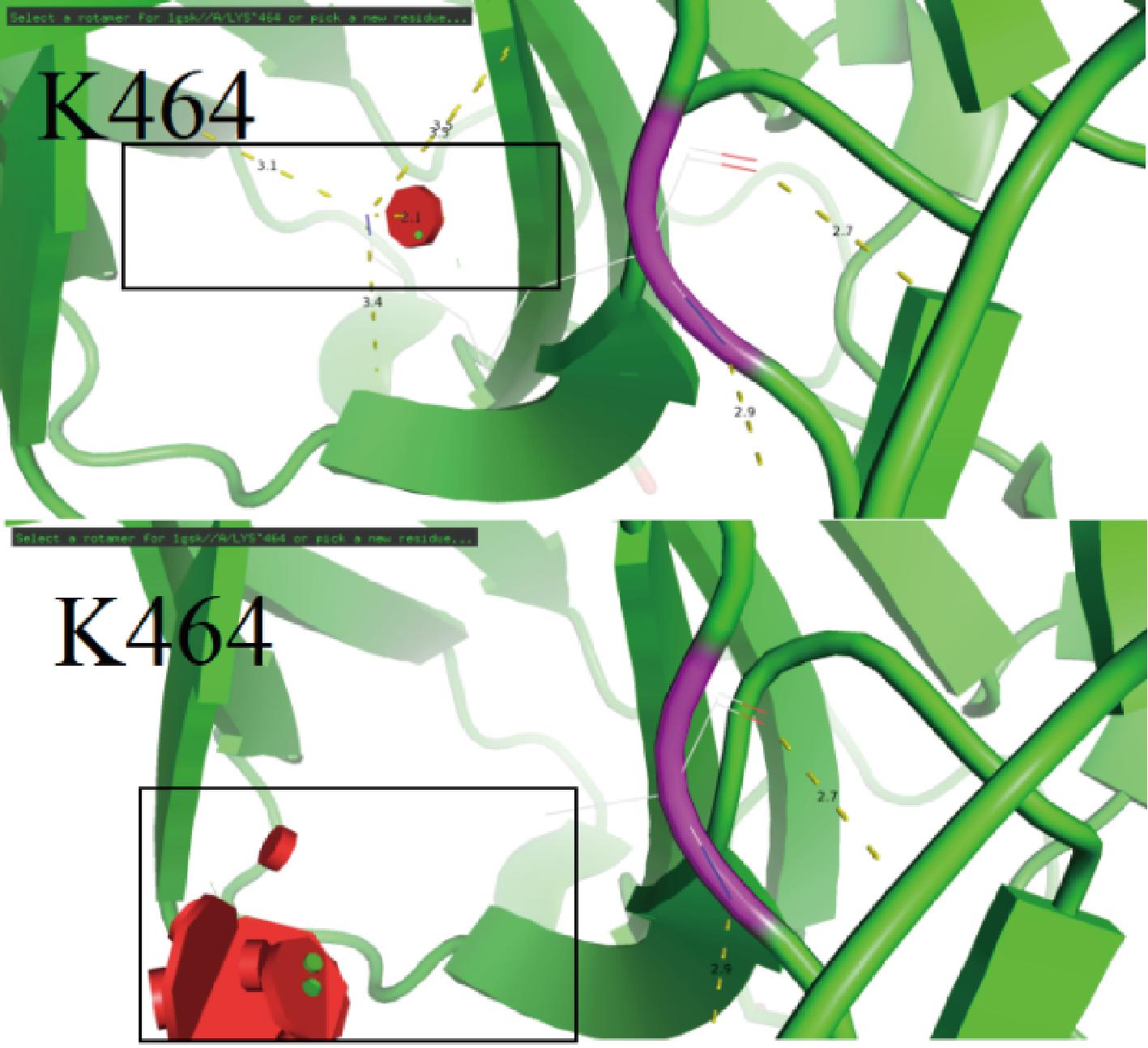
图10 突变体K464A突变后三级结构模拟对比图
Fig.10 Comparison of the simulated tertiary structures of the K464A mutant before and after mutation
2.4 突变细菌漆酶C492
突变细菌漆酶C492是将漆酶中的半胱氨酸替换成丙氨酸。漆酶是通过捕捉到底物中电子进行氧化。保守区域的改变,原理上对离子通道的功能有重大影响。故而,突变细菌漆酶C492应无法氧化底物。然而,纯化的突变细菌漆酶C492,在ABTS中却表现出明显变色。使用紫外分光光度计进行酶活力检测,酶活力最高达到了6 U/mL。似乎丙氨酸代替半胱氨酸,仍然执行了部分作用,存在氧化底物的可能。
由图11可知,突变细菌漆酶C492在1.5 mmol/L铜离子浓度下,表达量最高。
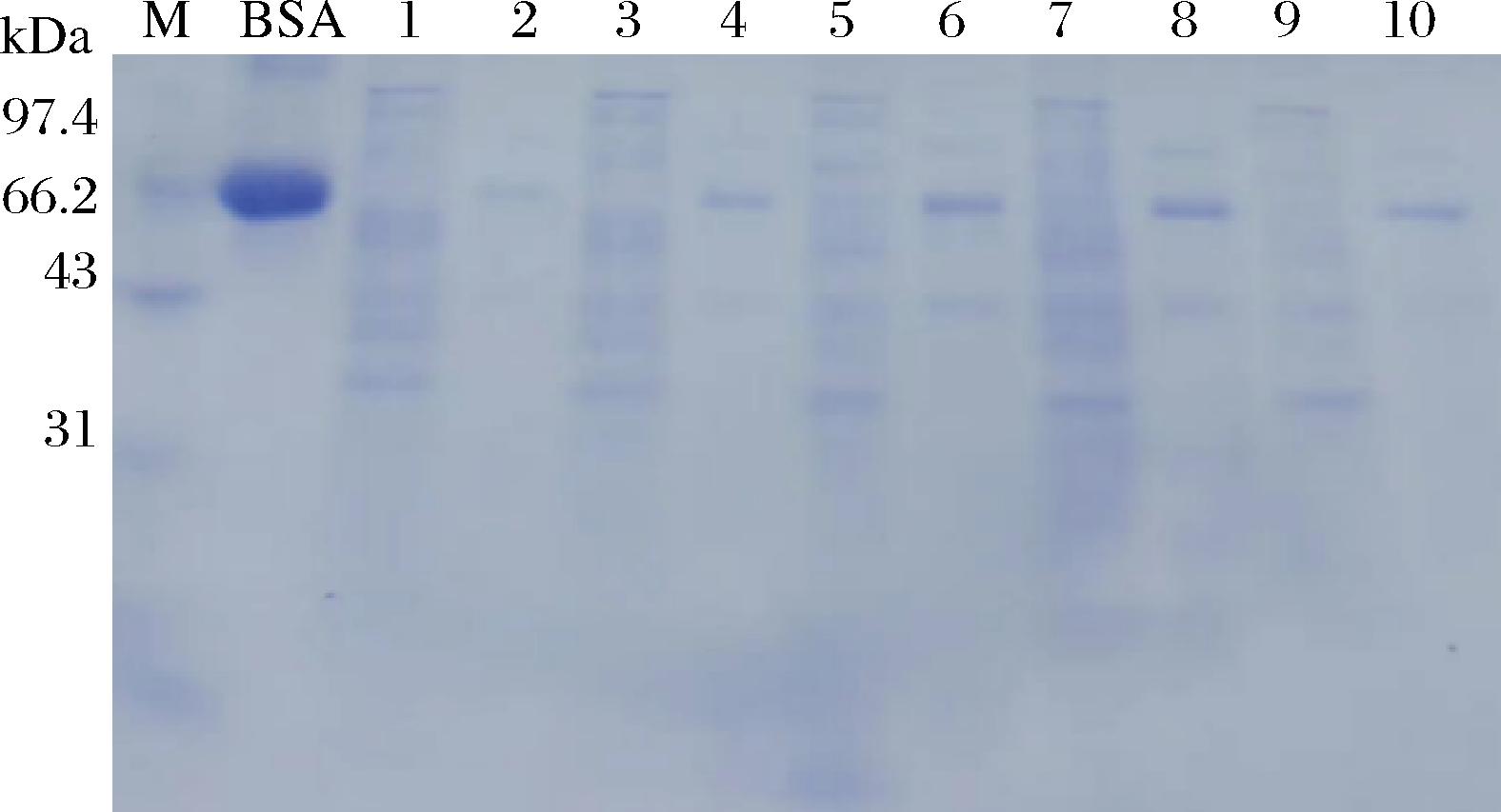
图11 不同铜离子浓度下突变细菌漆酶C492A表达量电泳图
Fig.11 SDS-PAGE of mutant bacterial laccase C492A expression levels under different copper ion concentrations
3 讨论
近年来,以漆酶作为表征的含铜蛋白质结构-功能关系的模型系统越来越受到关注,使其在脱木质素、植物纤维衍生等领域的生物技术方面表现出的应用潜力巨大[20]。而Cu2+是多酚氧化酶的重要组分[21],以硫酸铜作诱导剂,能够为漆酶表达菌株形成漆酶提供帮助。本文通过探究定体积、定量、诱导时间等多个因素,解析不同分子内部空间的细菌漆酶表达量受添加铜离子的影响。一定程度上证明铜离子浓度是改善细菌漆酶产量低下问题的重要途径。
铜离子添加量仅是影响漆酶表达量的因素之一,能够影响漆酶表达量的方法还有很多,如将不同来源的漆酶基因在大肠杆菌中进行异源表达。ECE等[22]利用分子手段使来源于链霉菌的漆酶在大肠杆菌中高效表达,使漆酶的产量提高达到104 mg/L。GUNNE等[23]利用分子手段使来源于地衣芽孢杆菌的漆酶在大肠杆菌中高效表达。KAUR等[24]在M162培养基中补充高达0.1%的葡萄糖增加了漆酶的产量。YU[25]在最优发酵培养基条件下,变色栓菌的实际发酵酶活为850.05 U/L,与未添加诱导剂的优化发酵培养基中的发酵漆酶活力66.56 U/L相比,漆酶产量提高了12.77倍。这些研究在不同程度上提高了漆酶的表达量。以上有关培养基组成条件优化的文献更是可以作为参考,使本文中的漆酶表达量可能得到进一步的提高。
[1] CLAUS H.Laccases:Structure, reactions, distribution[J].Micron, 2004, 35(1-2):93-96.
[2] PIONTEK K, ANTORINI M, CHOINOWSKI T.Crystal structure of a laccase from the fungus Trametes versicolor at 1.90-a resolution containing a full complement of coppers[J].Journal of Biological Chemistry, 2002, 277(40):37663-37669.
[3] 陈洪惠. 通过循环排列研究Ⅰ型铜蛋白结构与功能的关系[D].天津:天津科技大学,2019.CHEN H H.Probing the structure-function relationship of type Ⅰ copper protein by circular permutation[D].Tianjin:Tianjin University of Science &Technology,2019.
[4] OWUSU-FORDJOUR M.铜离子诱导和超声强化促进变色栓菌产漆酶及其在果汁澄清中的应用[D].镇江:江苏大学,2023.OWUSU-FORDJOUR M.Improved Laccase production from Trametes versicolor by Copper Ion Induction and ultrasound intensification and its application in juice clarificatio[D].Zhenjiang:Jiangsu University,2023.
[5] DU W, SUN C, LIANG J, et al.Improvement of laccase production and its characterization by mutagenesis[J].Journal of Food Biochemistry, 2015, 39(1):101-108.
[6] 孙仁彤. 细菌漆酶的定向进化研究[D].长春:吉林大学, 2023.SUN R T.Study on directed evolution of bacterial laccase[D].Changchun:Jilin University, 2023.
[7] XIE Y N,WANG R,LI Z,et al.Semi-rational engineering of microbial laccase Lac15 for enhanced activity[J].Acta Microbiologica Sinica,2022,62(4):1501-1512.
[8] DAI S, YAO Q, YU G, et al.Biochemical characterization of a novel bacterial laccase and improvement of its efficiency by directed evolution on dye degradation[J].Frontiers in Microbiology, 2021, 12:633004.
[9] WANG J Y, LU L, FENG F J.Improving the indigo carmine decolorization ability of a Bacillus amyloliquefaciens laccase by site-directed mutagenesis[J].Catalysts, 2017, 7(9):275
[10] ZHENG X S, NG I S, YE C M, et al.Copper ion-stimulated McoA-laccase production and enzyme characterization in Proteus hauseri ZMd44[J].Journal of Bioscience and Bioengineering, 2013, 115(4):388-393.
[11] MURUGESAN R, VEMBU B.Production of extracellular laccase from the newly isolated Bacillus sp.PK4[J].African Journal of Biotechnology, 2016, 15(34):1813-1826.
[12] MALHOTRA K, SHARMA P, CAPALASH N.Copper and dyes enhance laccase production in γ-proteobacterium JB[J].Biotechnology Letters, 2004, 26(13):1047-1050.
[13] DECEMBRINO D, GIRHARD M, URLACHER V B.Use of copper as a trigger for the in vivo activity of E.coli laccase CueO:A simple tool for biosynthetic purposes[J].Chembiochem, 2021, 22(8):1470-1479.
[14] BUDDHIKA U V A, SAVOCCHIA S, STEEL C C.Copper induces transcription of BcLCC2 laccase gene in phytopathogenic fungus, Botrytis cinerea[J].Mycology, 2020, 12(1):48-57.
[15] ZENG J, ZHU Q H, WU Y C, et al.Oxidation of polycyclic aromatic hydrocarbons using Bacillus subtilis CotA with high laccase activity and copper independence[J].Chemosphere, 2016, 148:1-7.
[16] 卢娇娇. 铜(Cu2+)对糙皮侧耳生长发育的影响研究[D].郑州:河南农业大学, 2015.LU J J.Effects of copper (Cu2+) on the growth and development of Pleurotus ostreatus[D].Zhengzhou:Henan Agricultural University, 2015.
[17] MUTANDA I, ZAHOOR, SETHUPATHY S, et al.Optimization of heterologous production of Bacillus ligniniphilus L1 laccase in Escherichia coli through statistical design of experiments[J].Microbiological Research, 2023, 274:127416.
[18] FOWLER L, ENGQVIST H, ÖHMAN-M GI C.Effect of copper ion concentration on bacteria and cells[J].Materials, 2019, 12(22):3798.
GI C.Effect of copper ion concentration on bacteria and cells[J].Materials, 2019, 12(22):3798.
[19] KOSCHORRECK K, SCHMID R D, URLACHER V B.Improving the functional expression of a Bacillus licheniformis laccase by random and site-directed mutagenesis[J].BMC Biotechnology, 2009, 9:12.
[20] MARTINS L O, SOARES C M, PEREIRA M M, et al.Molecular and biochemical characterization of a highly stable bacterial laccase that occurs as a structural component of the Bacillus subtilis endospore coat[J].Journal of Biological Chemistry, 2002, 277(21):18849-18859.
[21] HULLO M F, MOSZER I, DANCHIN A, et al.CotA of Bacillus subtilis is a copper-dependent laccase[J].Journal of Bacteriology, 2001, 183(18):5426-5430.
[22] ECE S L, LAMBERTZ C, FISCHER R, et al.Heterologous expression of a Streptomyces cyaneus laccase for biomass modification applications[J].AMB Express, 2017, 7(1):86.
[23] GUNNE M, AL-SULTANI D, URLACHER V B.Enhancement of copper content and specific activity of CotA laccase from Bacillus licheniformis by coexpression with CopZ copper chaperone in E.coli[J].Journal of Biotechnology, 2013, 168(3):252-255.
[24] KAUR K, SINGH G, GUPTA V, et al.Impact of phosphate and other medium components on physiological regulation of bacterial laccase production[J].Biotechnology Progress, 2017, 33(2):541-548.
[25] 余卓. 蓝铜胜肽诱导变色栓菌液态发酵产漆酶及其机制的研究[D].镇江:江苏大学, 2021.YU Z.Study on laccase production by Trametes versicolor induced by blue copper peptide and its mechanism[D].Zhenjiang:Jiangsu University, 2021.