随着人类社会对蛋白质的需求日益增大,蛋白质资源紧缺已然成为当今的一个世界性难题,在人口基数大的我国尤为突出[1]。通过“开源节流”,提高现有蛋白质资源的利用效率以及积极寻找新的蛋白资源是缓解蛋白短缺的主要发展路径[2-4]。近年来,以资源型昆虫为媒介的生物蛋白合成技术受到广泛关注。一些昆虫物种能够利用有机废弃物生长繁殖,不仅具有较高的生物转化效率而且可以实现高密度的工业化养殖,其中以黑水虻等腐生性昆虫最具代表性。
黑水虻是一种原产于美洲的双翅目水虻科昆虫,广泛分布于世界热带和温带地区。与其他全变态节肢动物相似,黑水虻生命周期包括卵、幼虫、蛹和成虫4个阶段。黑水虻摄食广泛,餐厨垃圾、畜禽粪便和剩余污泥等有机固体废弃物均可以作为其生长底物[5-6]。此外,黑水虻属于变态发育昆虫,幼虫阶段摄食量大,在转化有机废弃物过程中还能抑制病原菌生长。最为关键的是,黑水虻成虫期短,产卵后迅速死亡,不会进入人居空间,因此具有非常好的生态安全性。幼虫生物量(虫蛹)富含蛋白质、脂肪、维生素和矿物质,且氨基酸组分丰富,是一种优质的动物蛋白饲料来源。转化后的残留物(虫沙)还可以用作有机肥料[7-8]。因此,黑水虻生物转化技术被认为是一种极具应用前景的有机废弃物处理技术。
餐厨垃圾是城镇有机固体废弃物的主要组成部分,具有产生量大、有机质含量丰富、可生物利用性高等特点,非常适用于黑水虻等腐生性昆虫的资源化处理[9-10]。由于餐厨垃圾富含淀粉、蛋白质和纤维素等大分子有机质,需要在肠道中经过微生物转化才能被虫体吸收和利用,因此如何有效提升黑水虻的吸收和转化效能值得进一步研究。益生菌是指能够赋予宿主健康益处的活性微生物,是目前研究最为热门的一类饲料添加剂。研究认为,益生菌经摄食后进入宿主体内,通过改善宿主肠道微生物菌群功能,能够增强宿主机体的健康水平、免疫能力以及其他生理特性。此外,益生菌预发酵原料还可以改善其可消化性和风味口感,进而有利于提高宿主的摄食倾向和吸收转化。但是益生菌对黑水虻转化有机废弃物有何影响目前仍然缺乏研究。有鉴于此,本论文采用益生菌对餐厨垃圾进行预发酵,通过在有机质降解、虫体生长以及虫体蛋白抗氧化活性等层面的比较研究,分析益生菌对黑水虻转化餐厨垃圾合成蛋白的作用效能。
1 材料与方法
1.1 实验材料
餐厨垃圾来源于江苏无锡某餐厨垃圾处理企业,经制浆+提油+除杂+三相分离后产生的有机固渣作为亮斑扁角水虻幼虫的饲养原料。主要成分如表1所示:总固体(total soild,TS)含量约占湿重的26.8%;挥发性固体(volatile solids,VS)、粗蛋白和总糖分别约占总固体的91.8%、33.2%和30.7%。原料置于-20 ℃下保存待用。
表1 餐厨垃圾原料主要组分
Table 1 Main components of kitchen waste
参数TS/%(VS/TS)/%(粗蛋白/TS)/%(总糖/TS)/%餐厨垃圾原料26.8±1.291.8±1.533.2±1.630.7±1.3
嗜酸乳杆菌、枯草芽孢杆菌和产朊假丝酵母3种益生菌已在饲料添加剂中普遍应用,是目前公认安全的益生菌,生物转化方法不仅环保安全,而且可能带来额外的营养价值[11-12]。本实验使用的嗜酸乳杆菌ATCC832、枯草芽孢杆菌YQ-XJ-2和产朊假丝酵母AS2.281购自于北京生物保藏中心。通过益生菌分解利用餐厨垃圾中的有机质完成自身生长繁殖,同时产生大量蛋白酶、淀粉酶和纤维素酶类等,将其中大分子营养物质(蛋白质、淀粉和纤维素等)降解成易被肠道消化的小分子物质。黑水虻虫卵购买自丰裕生物科技有限公司。以麦麸作为虫卵孵化基质,初始含水率调节至75%。然后将虫卵加入麦麸中,并放置于恒温恒湿培养箱中避光孵化。孵化湿度和温度分别控制在75%~80%和25~30 ℃。幼虫孵出后继续培养,控制虫龄为3~4日龄。最后用10目筛网将接种幼虫从麦麸中分离出来,并称重计数。
1.2 餐厨垃圾益生菌预发酵
餐厨垃圾预发酵均在2 L开放式发酵罐中进行,分为4个实验组,包括:对照组(不接种)、单菌组(嗜酸乳杆菌)、双菌组(枯草芽孢杆菌+产朊假丝酵母)和三菌组(嗜酸乳杆菌+枯草芽孢杆菌+产朊假丝酵母)。益生菌由试管斜面转接至液体培养基活化两次,其中嗜酸乳杆菌和枯草芽孢杆菌活化培养采用LB培养基,产朊假丝酵母活化培养采用YPD培养基。每个实验组的反应体系中装入1 000 g餐厨垃圾(湿重),单菌组嗜酸乳杆菌接种量为6.0%;双菌组两菌接种量分别3.0%;三菌组接种量分别为2.0%。预发酵温度和搅拌转速分别控制在36.5 ℃和60.0 rpm;发酵时间均为40 h,每隔8 h取样分析。每个实验组做3个平行样。
1.3 黑水虻饲养
首先将预发酵后的物料平铺在黑水虻饲养盒中,物料厚度控制在10~15 cm。然后将3~4日龄幼虫接种至饲养物料中,接种量约为1 000只/kg物料。黑水虻饲养于人工气候培养箱中,湿度和温度分别设置在80%和30 ℃。当幼虫大约一半出现预蛹时结束饲养过程,并采用8目筛网分离出虫体和虫粪。收集后的虫体经超声洗涤后烘干至恒重,测定虫体干重和粗蛋白含量。每个实验组做3个平行样。
餐厨垃圾减量率、产虫率和粗蛋白产率计算如公式(1)、(2)、(3)所示:
(1)
(2)
E=P×R
(3)
式中:M,餐厨垃圾减量率,%;P,产虫率,g/g-TS;E,粗蛋白产率,g/g-TS;M0,添加的餐厨垃圾量(以TS计),g;M1,剩余有机质的数量(以TS计),g;H,收获的黑水虻幼虫干重,g;R,收获黑水虻幼虫的粗蛋白量占虫体干重的比例,%。
1.4 虫体蛋白体外抗氧化活性测定
(a)虫体蛋白制备
首先将幼虫在60 ℃下烘干至恒重,然后研磨成粉并装入脱脂滤纸袋,采用全自动索氏提取器充分去除油脂。脱脂虫粉60 ℃下烘干后,与20 g/L NaOH溶液混合(1∶20,g∶mL);在53 ℃水浴下搅拌1 h,离心20 min(6 000 r/min)获得的上清液即为黑水虻虫体蛋白粗提液。将粗提液调节至不同酸性pH,4 ℃下静置2 h,通过测定上清液蛋白质浓度减少量确定等电点以沉淀回收虫体蛋白。蛋白质粗提液经等电点沉淀后,离心去除上清液,沉淀通过冷冻干燥最终获得虫体蛋白。将上述制备得到的虫体蛋白配制成不同浓度的蛋白溶液,以维生素C和卵清蛋白(ovalbumin,OVA)为对照,测定其抗氧化活性。
(b)总还原力测定
采用铁氰化钾法测定虫体蛋白总还原力[13]。反应体系包括0.2 mol/L磷酸缓冲液(pH 6.6)、1%(质量分数)K3[Fe(CN)5]和样品溶液各1 mL。在50 ℃下水浴保持20 min后,加入10%(质量分数)三氯乙酸溶液(1 mL)以终止反应。离心取上清液2 mL,再加入2 mL蒸馏水和400 μL 0.1%(质量分数)FeCl3溶液,混合均匀后在波长700 nm处测定吸光度。以去离子水代替K3[Fe(CN)5]溶液作为对照,吸光度的高低反映了样品的还原能力强弱。
(c)超氧阴离子自由基清除率测定
采用邻苯三酚自氧化法测定黑水虻虫体蛋白对超氧阴离子自由基的清除率[13-14]。取1 mL样品溶液,并加入3 mL含有0.1 mmol/L EDTA-2 Na的Tris-HCl缓冲溶液(0.05 mol/L,pH 8.2),25 ℃下水浴加热25 min。向混合液中加入50 μL邻苯三酚溶液(50 mmol/L),继续25 ℃水浴保持4 min。最后加入1 mL HCl溶液终止反应(1 mol/L),测定波长325 nm处的吸光度,样品对超氧阴离子自由基的清除率的计算如公式(4)所示:
(4)
式中:Q,样品超氧阴离子自由基清除率,%;AX,样品溶液的吸光度;A0,样品对照组吸光度(用0.01 mol/L HCl溶液代替邻苯三酚溶液);A1,空白对照组吸光度(以去离子水代替样品溶液)。
(d)羟自由基清除率测定
采用Fenton法测定羟自由基清除率[15]。反应体系包括:样品溶液、硫酸亚铁溶液(0.009 mol/L)、水杨酸-乙醇溶液和0.01%(质量分数)H2O2溶液各1 mL。37 ℃水浴保持30 min后,离心取上清液在波长510 nm处测定吸光度,羟自由基清除率的计算如公式(5)所示:
(5)
式中:W,样品羟自由基清除率,%;BX,样品溶液的吸光度;B0,样品对照组吸光度(以蒸馏水代替H2O2溶液);B1,空白对照组吸光度(以去离子水代替样品溶液)。
(e)DPPH自由基清除活性测定
分别取1 mL样品溶液、2 mL DPPH乙醇溶液(0.1 mmol/L,溶剂为95%(质量分数)C2H5OH),混匀。在25 ℃和避光条件下反应30 min后,离心取上清液在波长517 nm处测定吸光度[16],DPPH自由基清除活性的计算如公式(6)所示:
(6)
式中:P,样品DPPH自由基清除率,%;CX,样品溶液的吸光度;C0,样品对照组吸光度(以95%C2H5OH代替DPPH溶液);C1,空白对照组吸光度(以去离子水代替样品溶液)
(f)ABTS阳离子自由基清除活性的测定
将过硫酸钾(5.2 mmol/L)和ABTS溶液(14.8 mmol/L)按照体积比1∶1混合,25 ℃下避光反应24 h。然后用甲醇溶液进行稀释,使得混合液在734 nm处的吸光度达到1.1左右。取1 mL样品溶液和3 mL稀释后的混合液,25 ℃下水浴保持10 min。离心取上清液在735 nm波长处测定吸光度[17],ABTS阳离子自由基清除活性的计算如公式(7)所示:
(7)
式中:H,样品ABTS阳离子自由基清除率(%);DX,样品溶液的吸光度;D0,样品对照组吸光度(以甲醇溶液代替稀释后的ABTS溶液);D1,空白对照组吸光度(以去离子水代替样品溶液)。
(g)亚铁离子螯合能力的测定
准备1 mL样品溶液和3 mL蒸馏水,加入0.2 mL的Ferrozine溶液(5 mmol/L)和50 μL的硫酸亚铁溶液(2 mmol/L)。25 ℃下水浴保持10 min,离心取上清液在562 nm处测定吸光度[17],计算亚铁离子螯合率的计算如公式(8)所示:
(8)
式中:M,样品金属离子螯合能力,%;EX,样品溶液的吸光度;E0,样品对照组吸光度(用去离子水代替FeSO4溶液);E1,空白对照组吸光度(以去离子水代替样品溶液)
1.5 指标测定方法
样品总固体和挥发性固体含量采用烘干法测定(HJ 613—2011)。粗蛋白含量采用凯氏定氮法测定(GB/T 6432—2018),粗脂肪含量采用索氏抽提法测定(GB/T 6433—2006),可溶性蛋白含量采用Folin-酚法测定[18]。
1.6 数据分析
每组试验至少3次平行,所有数据均表示为平均值±标准偏差。采用Origin8.0进行数据处理和图形绘制。虫体蛋白羟基自由基清除活性、金属离子螯合能力均通过IC50进行比较和评价(IC50即达到各个指标因变量50%时所需要的样品浓度)[19]。P<0.05定义为差异显著。
2 结果与讨论
2.1 餐厨固渣可溶性蛋白变化
通过采用3种不同的微生物组合对餐厨固渣进行预发酵,以可溶性蛋白浓度为指标评价餐厨固渣的水解效果,在水解效果最佳时投加黑水虻幼虫,提高餐厨固渣黑水虻生物转化利用率,促进黑水虻幼虫生长代谢速率。如图1所示,在预发酵过程中,3个实验组的可溶性蛋白含量均呈现先升高再平稳的过程。40 h时,双菌组和三菌组的可溶性蛋白含量均达到最大值,分别为173.1 mg/g和224.02 mg/g,比原料中可溶性蛋白含量分别提高了3.91倍和5.06倍。而添加嗜酸乳杆菌的单菌组在48 h时达到了最大值,可溶性蛋白含量为130.39 mg/g,比原料中可溶性蛋白高出2.52倍。实验表明,餐厨固渣接种嗜酸乳杆菌、枯草芽孢杆菌和产朊假丝酵母后,通过预发酵可达到更好的水解效果。由于嗜酸乳杆菌的添加创造了较低的pH环境,可抑制发酵过程中杂菌的生长,从而营造有利于枯草芽孢杆菌和产朊假丝酵母的生长条件。枯草芽孢杆菌自身合成的酶促进餐厨固渣中大分子物质转化为单糖等小分子物质,提高了可溶性蛋白的含量。同时,产朊假丝酵母本身属于菌体蛋白,又充分利用了餐厨固渣中的还原糖进行生长繁殖,提高了发酵液中的蛋白浓度。因此,进行黑水虻生物转化实验中,分别在可溶性蛋白含量最高值进行投加,即40 h时将黑水虻投加至双菌组和三菌组,48 h时投加至单菌组。
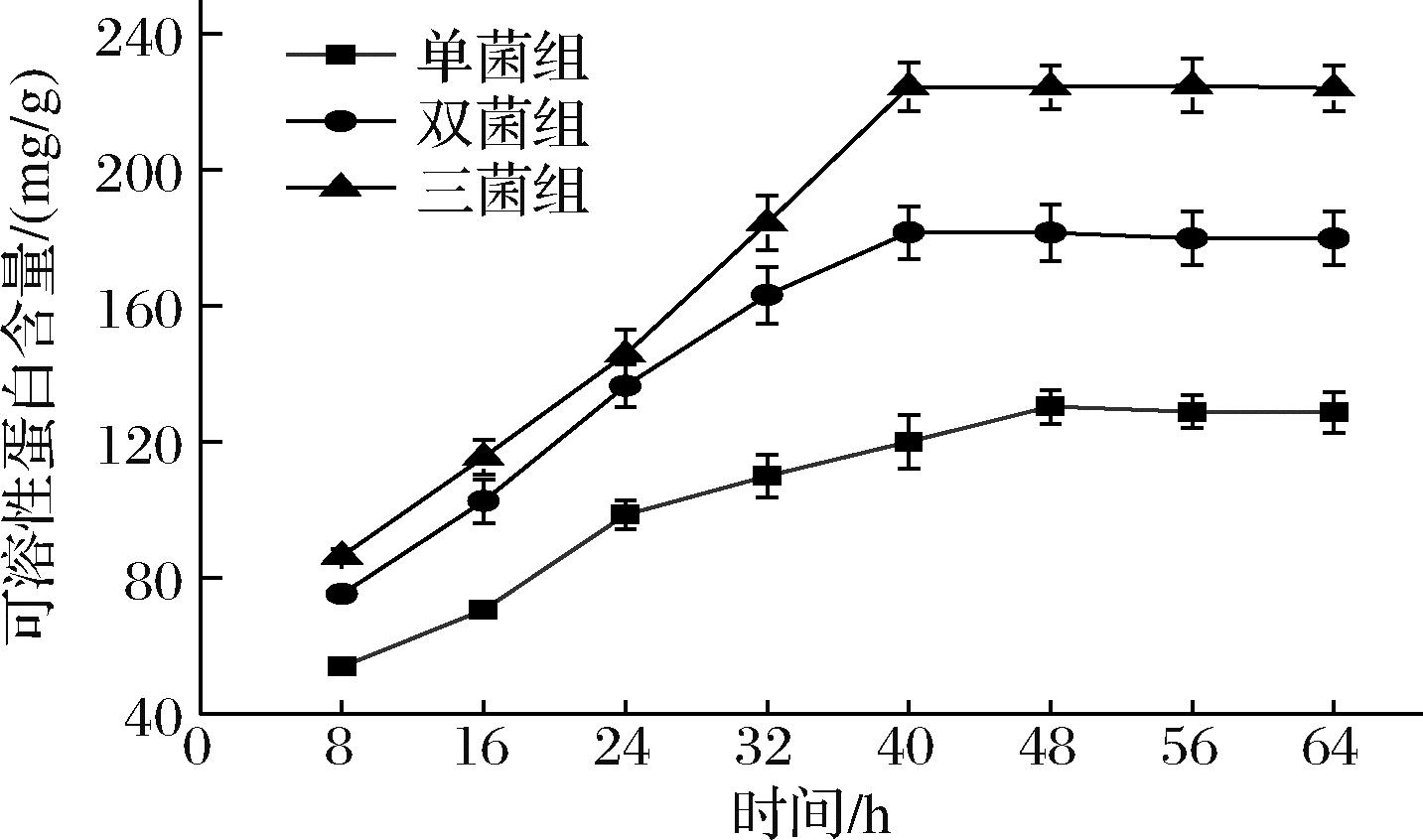
图1 餐厨固渣预发酵过程中可溶性蛋白变化
Fig.1 Changes of soluble protein during kitchen waste pre-fermentation process
2.2 餐厨固渣生物转化率及虫体蛋白产率变化
通过预处理后的餐厨固渣,在黑水虻生物转化过程中,餐厨固渣的减量率和虫体生物质含量呈现出了明显的区别(如图2所示)。经过嗜酸乳杆菌、枯草芽孢杆菌和产朊假丝酵母预处理后的三菌组,餐厨固渣剩余物仅为25.9%,减量率达到了74.1%,比对照组提高了1.2倍。与对照组、单菌组和双菌组对比,代谢量分别提高了70.9%、29.9%和11.1%,虫体生物质含量提高了74.7%、76.5%、47.2%。结果表明,通过嗜酸乳杆菌、枯草芽孢杆菌和产朊假丝酵母预处理后餐厨固渣的生物转化率明显提高。为进一步明晰经过微生物预处理后虫体蛋白产率的变化,针对各实验组中的幼虫组分进行分析。如表2所示,三菌组中黑水虻幼虫的虫体蛋白产率达到了(0.16±0.002) g/g-TScomsumed,比对照组提高了1倍。说明采用嗜酸乳杆菌、枯草芽孢杆菌和产朊假丝酵母预处理后的餐厨固渣,明显促进了黑水虻对餐厨固渣的吸收和转化,提高了虫体蛋白的合成。与对照组相比,经过益生菌预处理后,餐厨垃圾中的大分子物质(蛋白质、糖类)降解为分子质量较低的小分子物质,易被黑水虻幼虫吸收利用。三菌组丰富了发酵体系中微生物的种类,分泌的酶系较全,使得餐厨垃圾中大分子物质降解相对完全[20]。
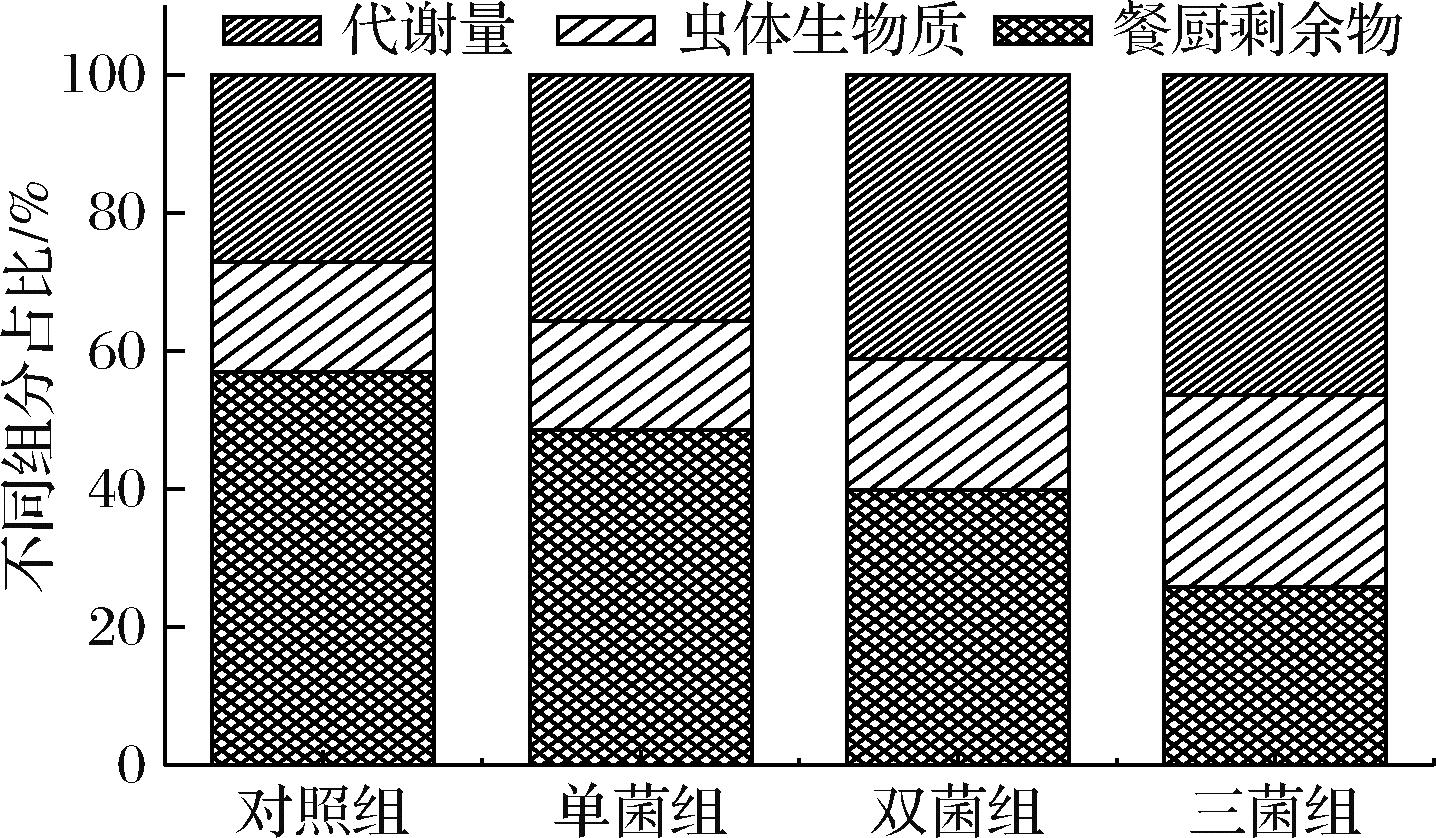
图2 不同处理组餐厨垃圾干物质减量变化
Fig.2 Changes of dry matter reduction of kitchen waste in different treatment groups
表2 不同处理组黑水虻虫体组分
Table 2 Components of the insect body in different treatment groups
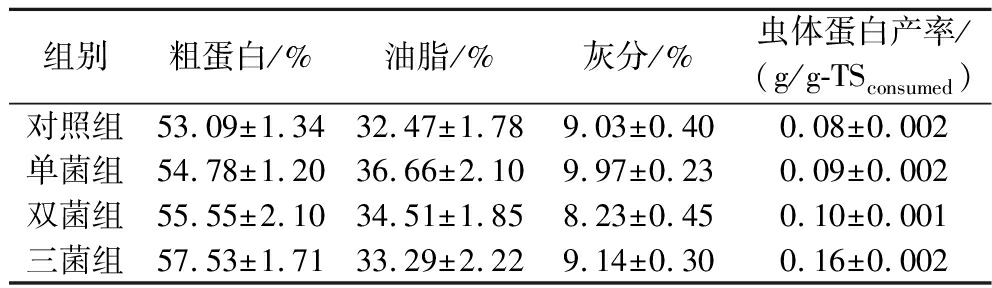
组别粗蛋白/%油脂/%灰分/%虫体蛋白产率/(g/g-TSconsumed)对照组53.09±1.3432.47±1.789.03±0.400.08±0.002单菌组54.78±1.2036.66±2.109.97±0.230.09±0.002双菌组55.55±2.1034.51±1.858.23±0.450.10±0.001三菌组57.53±1.7133.29±2.229.14±0.300.16±0.002
2.3 黑水虻虫体蛋白等电点测定
等电点是蛋白质的特殊性质,在等电点时蛋白质分子以双极离子存在,总净电荷为零,颗粒无电荷间的排斥作用,易凝聚成大颗粒[20-22]。因此在等电点时,蛋白质最不稳定,溶解度最小,易于沉淀析出。为使黑水虻虫体蛋白的沉淀效率达到最佳,实验过程中将餐厨固渣孵化出的黑水虻幼虫烘干、脱脂后制成蛋白粗提取液,通过调节蛋白提取液的pH对等电点的范围进行筛选。选取对照组和三菌组的黑水虻蛋白提取液为实验对象,采用0.5 mol/L的HCl溶液调节pH,分别调节pH值为2.5、3.0、3.5、4.0、4.5、5.0和5.5(如图3-a所示)。结果表明,当pH值为5时,两个实验组的虫体蛋白沉淀率达到最高,分别为85.34%和89.95%。为进一步确定pH值的准确性,分别调节pH值为4.8、4.9、5.0、5.1、5.2和5.3(如图3-b所示),对照组和三菌组均在pH值为4.9时达到最高值,因此确定4.9为黑水虻虫体蛋白等电点,在pH值为4.9时分子颗粒更易凝聚而产生蛋白沉淀,黑水虻虫体蛋白粗提取液经等电点沉淀后,离心去除上清液,通过冷冻干燥最终可获得虫体蛋白纯度较高。
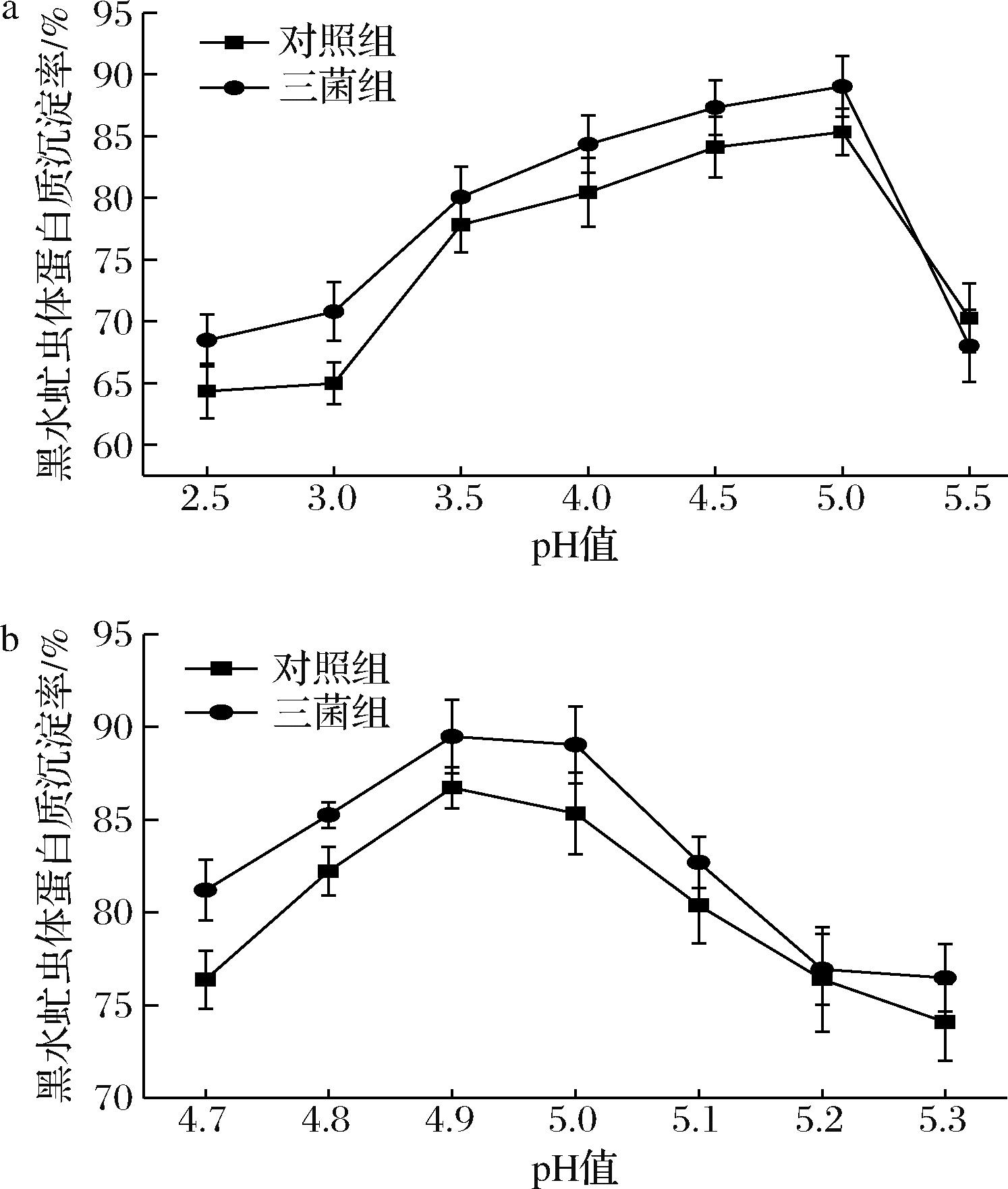
a-pH值在2.5~5.5范围内虫体蛋白等电点测定; b-pH值在4.8~5.3范围内虫体蛋白等电点测定
图3 黑水虻虫体蛋白等电点测定
Fig.3 Isoelectric point determination of insect protein
2.4 黑水虻虫体蛋白总还原力分析
总还原力是评价蛋白样品抗氧化能力的基础指标之一,总还原力的强弱反映了抗氧化性的高低。黄超等[23]以黑水虻幼虫为原料研究了4种溶解性蛋白的理化性质,4种蛋白具有一定的总还原力,且还原力的大小与抗氧化活性呈正相关。为验证虫体蛋白的抗氧化活性,实验中选取了对照组、三菌组、OVA组和维生素C组进行总还原力的测定(如图4所示)。两个实验组、OVA组以及维生素C组均表现出一定的还原能力,与其浓度呈正相关。维生素C组总还原力显著高于实验组和OVA组,三菌组显著高于对照组。对4个样品进行不同次数的拟合,当A700=1时,对照组所需质量浓度为5.26 mg/mL,三菌组为4.43 mg/mL,维生素C组为0.072 mg/mL,OVA组为7.02 mg/mL。维生素C的总还原力最强,OVA最弱。经过益生菌预处理后虫体蛋白总还原力是对照组的1.14倍。总还原力越强,蛋白的抗氧化活性就越强,实验结果表明益生菌预处理可有效提高虫体蛋白的抗氧化活性。具有较高总还原力的蛋白样品能够有效地清除自由基,减少氧化反应的发生,从而保护细胞免受氧化损伤。维生素C作为阳性对照,显示出最强的抗氧化活性。因维生素C是公认的强效抗氧化剂,常被用作评估其他抗氧化物质效力的参考标准[24]。
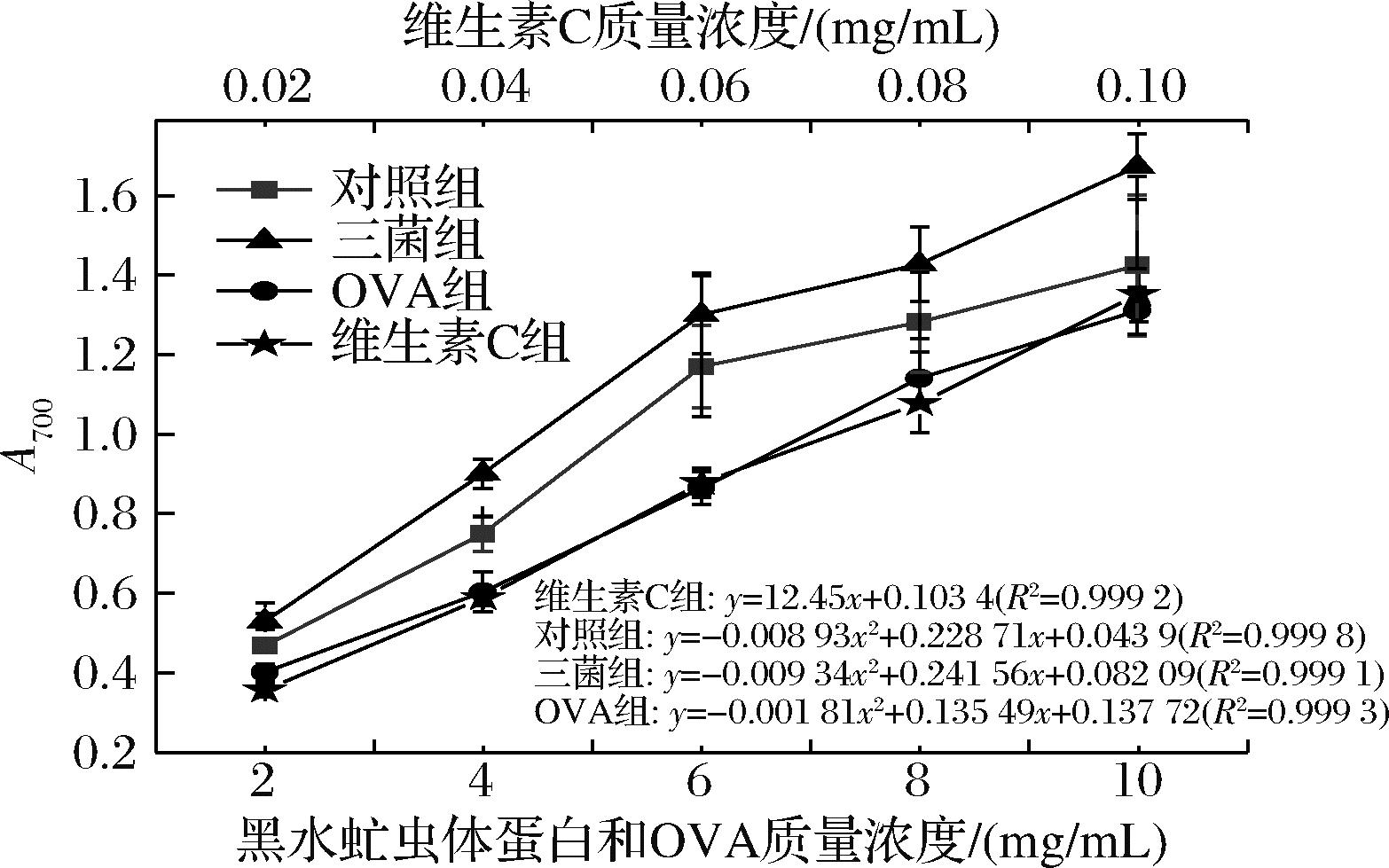
图4 黑水虻虫体蛋白总还原力测定
Fig.4 Total reducing power determination of insect protein
2.5 黑水虻虫体蛋白超氧阴离子自由基清除活性分析
超氧阴离子自由基是一种高度活跃的氧化性物质,可损害细胞膜、DNA和其他生物分子,导致细胞损伤和氧化应激。如图5所示,对照组和三菌组超氧阴离子自由基清除率具有显著差异(P<0.05)。4个样品都对超氧阴离子自由基有一定的清除能力,维生素C组随着质量浓度的增加,超氧阴离子自由基的清除率随之增强。OVA组和两个黑水虻蛋白样品随着质量浓度的增加清除率也增强,当浓度超过2 mg/mL后,清除率转为缓慢上升,在质量浓度达到8 mg/mL后,清除率基本保持不变。因此,在所测的4个样品中,维生素C最强,OVA最弱,黑水虻虫体蛋白超氧阴离子清除活性居中,其中三菌组大于对照组。超氧阴离子自由基广泛存在于生物体内,自身具有很大毒性并能够衍生出许多具有细胞毒性的自由基,如黄嘌呤氧化酶、过氧化物酶等[24]。实验结果表明,经过益生菌预处理可有效提高虫体蛋白超氧阴离子自由基清除活性,能够清除由特定体系产生的超氧阴离子自由基,从而减少自由基的氧化作用。
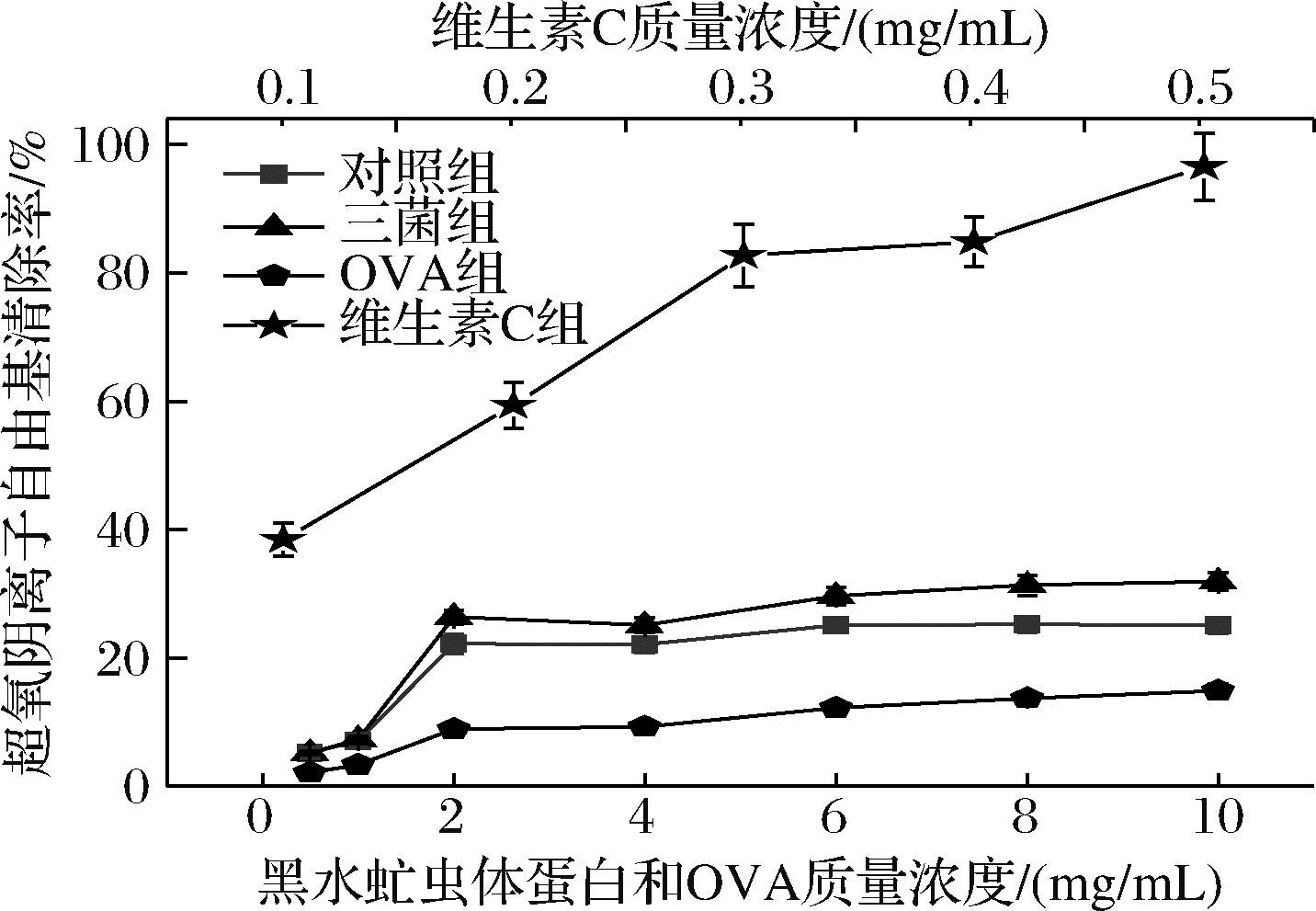
图5 为黑水虻虫体蛋白超氧阴离子自由基清除活性测定
Fig.5 Superoxide anion radical scavenging activity determination of insect protein
2.6 黑水虻虫体蛋白羟自由基清除活性分析
羟自由基可以直接攻击碳水化合物分子上的碳氢键,使分子结构发生变化。在生物体内可引发脂质过氧化、DNA损伤和蛋白质氧化等反应,被认为是许多疾病发生和发展的重要因素。实验中分析了虫体蛋白羟基自由基的清除活性,对照组和实验组羟基自由基的清除活性均与虫体蛋白浓度成正比(如图6所示)。三菌组与对照组羟基自由基清除率有显著差异(P<0.05),分别对4个样品进行不同次数的拟合可以得出清除羟自由基的IC50:对照组为3.08 mg/mL,微生物处理组为2.65 mg/mL,OVA组为12.07 mg/mL以及维生素C组为0.28 mg/mL。所测的样品中,维生素C的羟基自由基清除活性最高。三菌组羟基自由基的清除能力次之,是对照组的1.16倍,OVA组最差。因此,嗜酸乳杆菌、枯草芽孢杆菌和产朊假丝酵母预处理组虫体蛋白样品具有良好的羟自由基清除能力,且这种活性与蛋白质浓度呈正相关。这一发现与之前关于虫体蛋白抗氧化能力的研究结果相一致[23],虽与已知的抗氧化剂维生素C对比仍有较大差距,但仍高于OVA对照组。相对于合成抗氧化剂,黑水虻虫体蛋白作为天然来源可能具有更好的生物相容性和安全性,进一步证实了黑水虻虫体蛋白作为天然抗氧化剂的潜力。
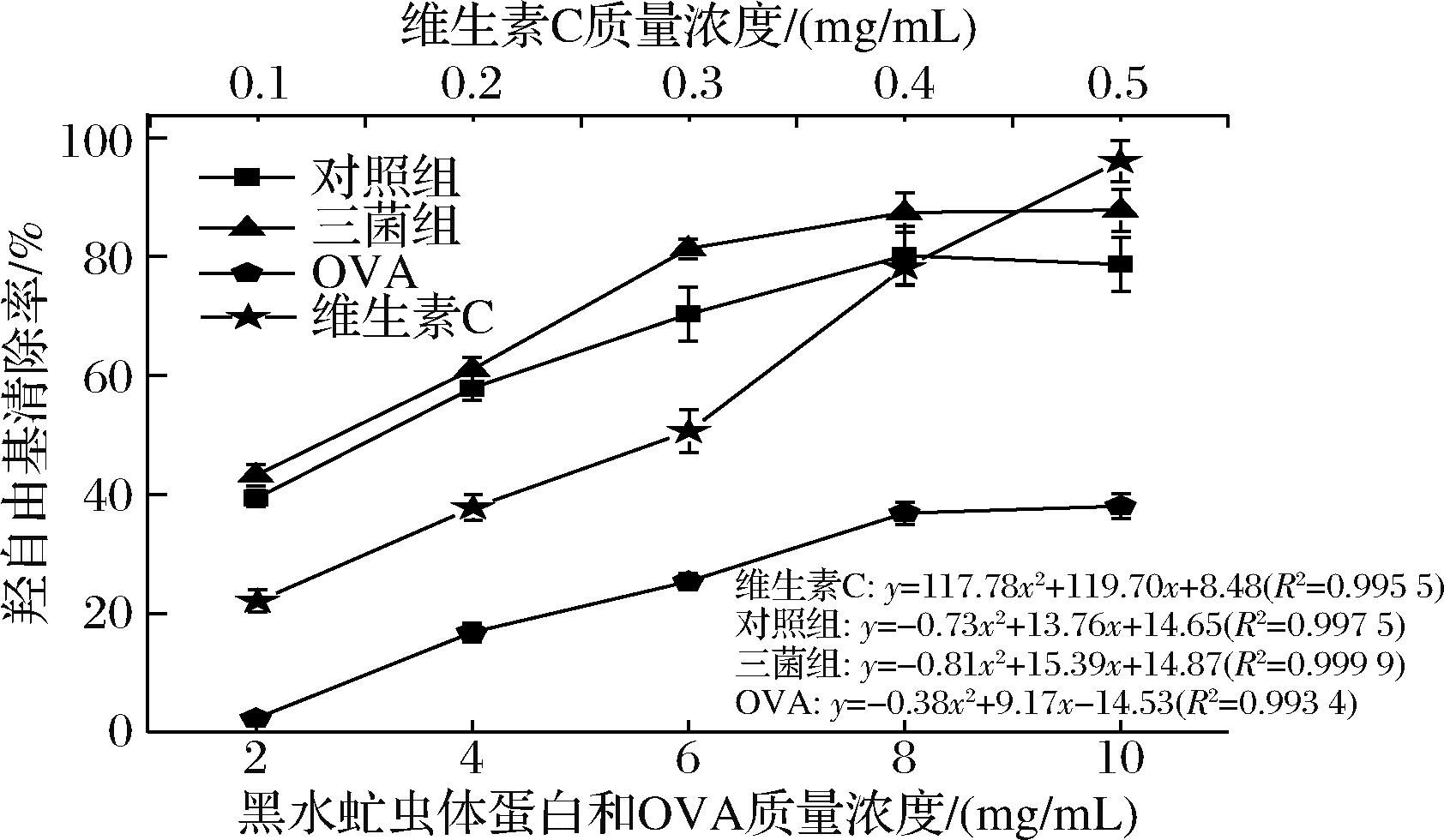
图6 黑水虻虫体蛋白羟自由基清除活性测定
Fig.6 Hydroxyl radical scavenging activity determination of insect protein
2.7 黑水虻虫体蛋白DPPH自由基清除活性分析
DPPH自由基是一种广泛用于评估抗氧化活性的化学试剂,通过测定抗氧化物质对DPPH自由基的清除率,间接反应其对自由基的抑制作用,即抗氧化能力的强弱。实验中分析了DPPH自由基清除活性,对照组和实验组DPPH自由基清除活性均与虫体蛋白浓度成正比(如图7所示)。三菌组显著高于对照组(P<0.05),对照组、三菌组、OVA组和维生素C组的IC50分别为4.58、3.03、7.29和0.29 mg/mL。所测的样品中,三菌组DPPH自由基清除活性是对照组的1.51倍,维生素C组的最高。通过嗜酸乳杆菌、枯草芽孢杆菌和产朊假丝酵母预处理,虫体蛋白样品具有良好的DPPH自由基清除活性。这种增强效果可能源于微生物发酵过程中产生的代谢物或者对虫体蛋白结构的修饰,从而提高了其清除自由基的能力。
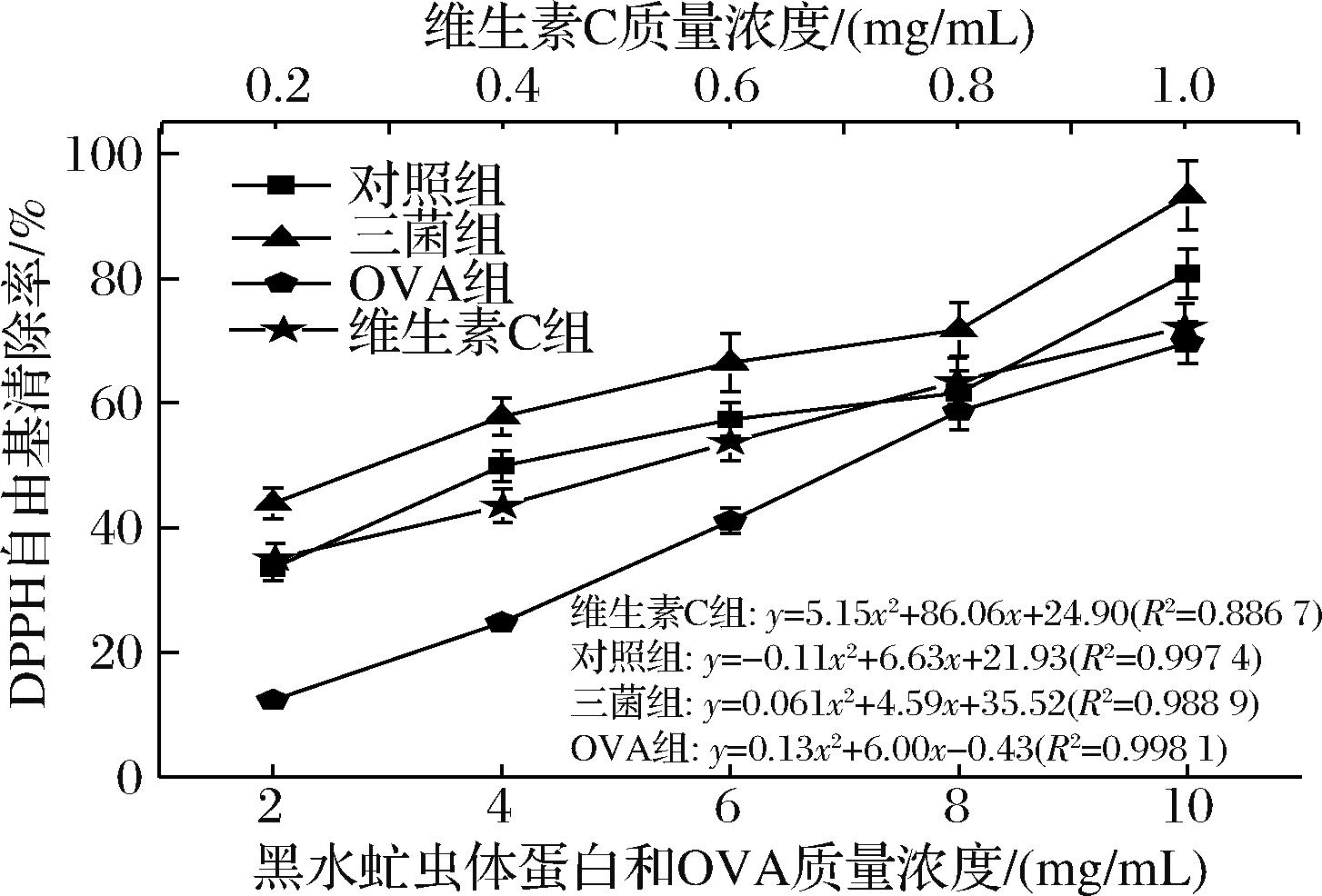
图7 黑水虻虫体蛋白DPPH自由基清除活性测定
Fig.7 DPPH free radical scavenging activity determination of insect protein
然而,OVA组的IC50值高于对照组和三菌组,表明卵清蛋白可能不具备显著的抗氧化活性,或在本实验条件下其抗氧化效果较弱。这一结果与先前的研究一致,如XU等[24]报道的卵清蛋白在DPPH自由基清除实验中表现出较低的活性。
2.8 黑水虻虫体蛋白ABTS阳离子自由基清除活性分析
ABTS阳离子自由基清除活性是衡量样品作为潜在抗氧化剂效力的一个关键指标。如图8所示,ABTS阳离子自由基清除率均与蛋白质浓度成正比,维生素C组的ABTS阳离子自由基清除率显著高于其他处理组(P<0.05)。对照组和三菌组ABTS阳离子自由基清除率差异不显著(P>0.05)。对照组、三菌组、OVA组和维生素C组的IC50分别为0.31、0.25、0.6和0.018 mg/mL。三菌组是对照组的1.24倍。通过嗜酸乳杆菌、枯草芽孢杆菌和产朊假丝酵母预处理后,三菌组黑水虻虫体蛋白ABTS阳离子自由基清除活性有了明显提升,其清除能力介于OVA和维生素C之间,具有良好的ABTS阳离子自由基清除活性。结果进一步表明,微生物预处理能够显著提高黑水虻虫体蛋白的抗氧化能力。而OVA组的ABTS阳离子自由基清除活性低于三菌组和对照组,其IC50值为0.6 mg/mL。表明OVA的抗氧化能力相对较弱,可能与其蛋白质结构和组成有关[23]。
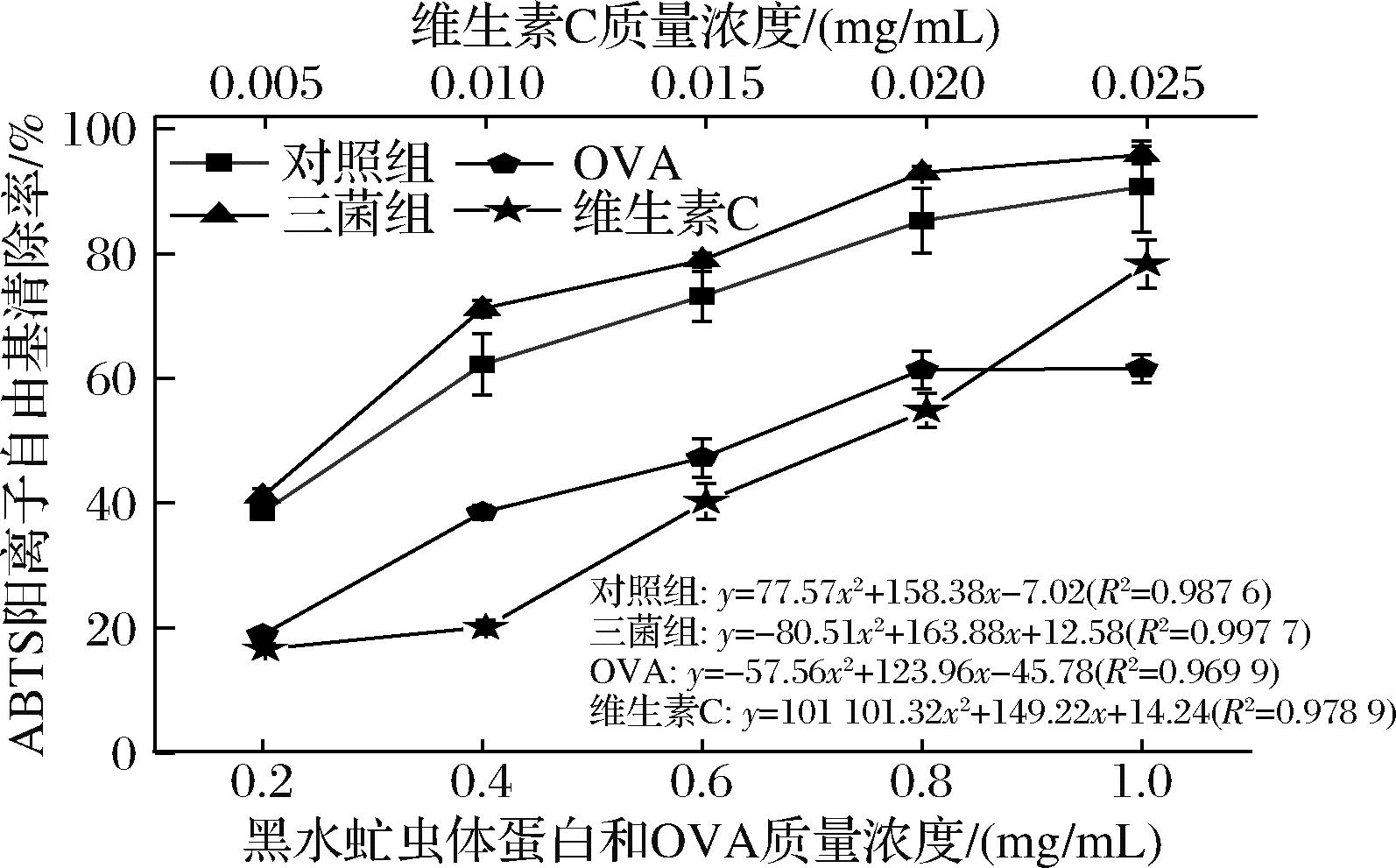
图8 黑水虻虫体蛋白ABTS阳离子自由基清除活性测定
Fig.8 ABTS cationic radical scavenging activity determination of insect protein
2.9 黑水虻虫体蛋白金属离子螯合能力
虫体蛋白通常含有多个氨基酸残基,如组氨酸、天冬氨酸和谷氨酸等,这些残基可以通过配位键、静电引力等方式与金属离子形成稳定的配合物,从而表现出良好的金属离子螯合活性,发挥抗氧化和保护细胞的作用。实验中分析了EDTA、对照组和三菌组虫体蛋白的金属离子螯合能力。如图9所示,亚铁离子螯合能力分别与EDTA和虫体蛋白浓度呈现出良好的正相关性,表明螯合作用是一个浓度依赖的过程,增加螯合剂的浓度可以提高其螯合效率。分别对其进行方程拟合,EDTA、对照组和三菌组的亚铁离子螯合率IC50分别为0.011、1.08和0.89 mg/mL。EDTA作为专业的螯合剂,表现出最强的亚铁离子螯合能力,其次是经过微生物处理的三菌组虫体蛋白,而未经处理的对照组虫体蛋白螯合能力最弱。经过嗜酸乳杆菌、枯草芽孢杆菌和产朊假丝酵母处理后亚铁离子螯合能力是对照组1.21倍,证实了微生物预处理能够有效提高虫体蛋白的螯合能力。
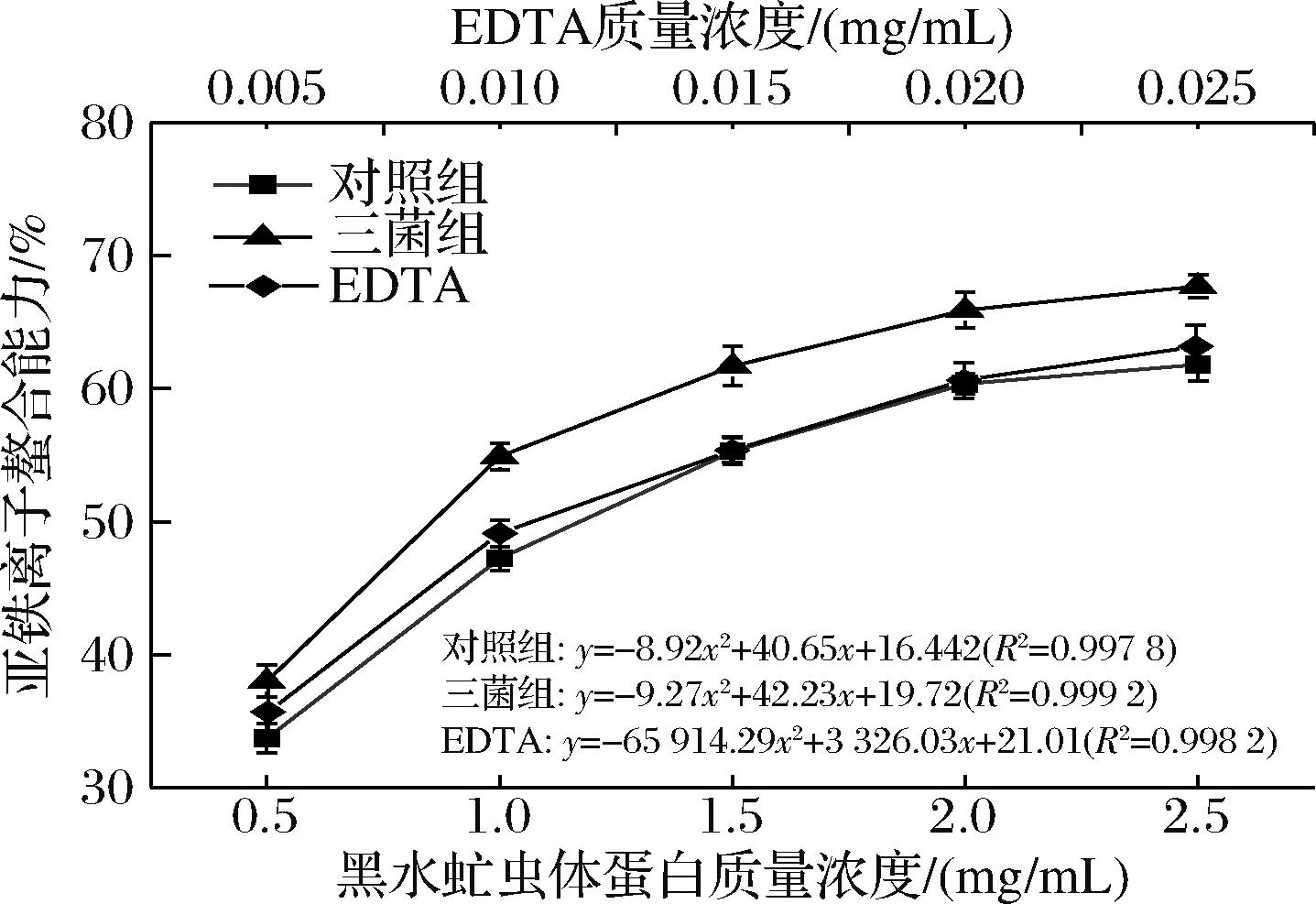
图9 黑水虻虫体蛋白金属离子螯合能力测定
Fig.9 Metal ion chelating ability determination of insect protein
3 结论
本研究采用不同组合益生菌对餐厨垃圾进行预发酵,获得黑水虻虫体蛋白并配制成不同浓度蛋白溶液。通过测定虫体蛋白的体外抗氧化活性,总还原力、羟自由基清除活性、DPPH自由基清除活性、ABTS阳离子自由基清除活性以及金属离子螯合能力,并以维生素C、OVA和EDTA作为阳性对照,对黑水虻虫体蛋白的体外抗氧化活性进行综合评价。结果表明,益生菌的预处理可以更好的强化餐厨垃圾中有机质的分解利用,促进黑水虻虫体的生长繁殖。虫体蛋白具有更加良好的体外抗氧化活性,适合作为天然抗氧化剂或用于抗氧化功能蛋白食品的研究,为餐厨垃圾的进一步研究和资源化利用提供依据。
[1] MAKKAR H P S, TRAN G, HEUZÉ V, et al.State-of-the-art on use of insects as animal feed[J].Animal Feed Science and Technology, 2014, 197:1-33.
[2] 谢亚萍. 太空诱变混菌固态发酵苹果渣生产单细胞蛋白的研究[D].兰州:甘肃农业大学, 2011.XIE Y P.Study on the production of single cell protein by solid-state fermentation of apple pomace with space mutation and mixed bacteria[D].Lanzhou:Gansu Agricultural University, 2011.
[3] VAN H A.Potential of insects as food and feed in assuring food security[J].Annual Review of Entomology, 2013, 58:563-583.
[4] SURENDRA K C, TOMBERLIN J K, VAN HUIS A, et al.Rethinking organic wastes bioconversion:Evaluating the potential of the black soldier fly (Hermetia illucens (L.)) (Diptera:Stratiomyidae) (BSF)[J].Waste Management, 2020, 117:58-80.
[5] ZHENG L Y, LI Q, ZHANG J B, et al.Double the biodiesel yield:Rearing black soldier fly larvae, Hermetia illucens, on solid residual fraction of restaurant waste after grease extraction for biodiesel production[J].Renewable Energy, 2012, 41:75-79.
[6] XIAO X P, MAZZA L, YU Y Q, et al.Efficient co-conversion process of chicken manure into protein feed and organic fertilizer by Hermetia illucens L.(Diptera:Stratiomyidae) larvae and functional bacteria[J].Journal of Environmental Management, 2018, 217:668-676.
[7] ZHOU Y, ENGLER N, NELLES M.Symbiotic relationship between hydrothermal carbonization technology and anaerobic digestion for food waste in China[J].Bioresource Technology, 2018, 260:404-412.
[8] BIASATO I, RENNA M, GAI F, et al.Partially defatted black soldier fly larva meal inclusion in piglet diets:Effects on the growth performance, nutrient digestibility, blood profile, gut morphology and histological features[J].Journal of Animal Science and Biotechnology, 2019, 10:12.
[9] 路延, 张鸣谦, 杨骁婧, 等.餐厨垃圾的黑水虻处理中含钙矿物及微生物对油脂转化效率的影响[J].环境科学学报, 2021, 41(12):4973-4985.LU Y, ZHANG M Q, YANG X J, et al.Effects of calcium mineral and microbial inoculum on the lipid conversion efficiency during food waste treatment by black soldier fly larvae[J].Acta Scientiae Circumstantiae, 2021, 41(12):4973-4985
[10] 王凯军, 王婧瑶, 左剑恶, 等.我国餐厨垃圾厌氧处理技术现状分析及建议[J].环境工程学报, 2020, 14(7):1735-1742.WANG K J, WANG J Y, ZUO J E, et al.Analysis and suggestion of current food waste anaerobic digestion technology in China[J].Chinese Journal of Environmental Engineering, 2020, 14(7):1735-1742.
[11] 杨丹丹, 潘冬梅, 刘圣鹏, 等.餐厨垃圾乳酸菌发酵生产生物饲料的研究[J].中国农学通报, 2016, 32(26):1-5.YANG D D, PAN D M, LIU S P, et al.Biological feed fermented from kitchen garbage with Lactobacillus[J].Chinese Agricultural Science Bulletin, 2016, 32(26):1-5.
[12] 蔡静, 张紊玮, 贠建民, 等.餐厨垃圾微生物发酵生产蛋白饲料的工艺优化[J].中国酿造, 2015, 34(2):114-119.CAI J, ZHANG W W, YUN J M, et al.Optimization of microbial fermentation process to produce protein feed from kitchen waste[J].China Brewing, 2015, 34(2):114-119.
[13] 郭倩. 大麦虫蛋白质的分离纯化及其抗氧化性研究[D].杨凌:西北农林科技大学, 2011.GUO Q.Isolation, purification and antioxidant activity of protein from barley worm[D].Yangling:Northwest A &F University, 2011.
[14] 赖冬花, 傅红, 杨琳, 等.菠菜色素蛋白复合物的抗氧化性研究[J].食品研究与开发, 2013, 34(3):116-120.LAI D H, FU H, YANG L, et al.Research on antioxidant activity of spinach pigment protein complexes[J].Food Research and Development, 2013, 34(3):116-120.
[15] 陈根洪. 藤茶总多酚的提取及其抗氧化活性研究[J].食品科学, 2011, 32(6):127-130.CHEN G H.Extraction and antioxidant activity of total polyphenols from Ampelopsis grossedendata[J].Food Science, 2011, 32(6):127-130.
[16] 崔莉, 刘春泉, 李大婧, 等.发酵莴苣茎叶功能活性研究[J].核农学报, 2011, 25(3):523-528.CUI L, LIU C Q, LI D J, et al.Functional activities of fermented lettuce stem and leaf[J].Journal of Nuclear Agricultural Sciences, 2011, 25(3):523-528.
[17] INTARASIRISAWAT R, BENJAKUL S, VISESSANGUAN W, et al.Antioxidative and functional properties of protein hydrolysate from defatted skipjack (Katsuwonous Pelamis) roe[J].Food Chemistry, 2012, 135(4):3039-3048.
[18] 罗群. 考马斯亮蓝法快速测定菜籽粕中可溶性蛋白质的含量[J].成都大学学报(自然科学版), 2014, 33(2):125-126;129.LUO Q.Rapid determination of soluble protein content in rapeseed meal by coomassie brilliant blue method[J].Journal of Chengdu University (Natural Science Edition), 2014, 33(2):125-126;129.
[19] 刘洪对, 于丽娜, 高俊安, 等.五种花生抗氧化肽体外抗氧化活性比较[J].核农学报, 2013, 27(8):1162-1167;1172.LIU H D, YU L N,GAO Jun’an, et al.Antioxidant activity comparison of five kinds of peanut(Arachin conarachin L.) antioxidant peptides in vitro[J].Journal of Nuclear Agricultural Sciences, 2013, 27(8):1162-1167;1172.
[20] 王熙涛, 张玉苍, 何连芳.餐厨废弃物发酵生产微生物饲料的资源化研究[J].环境工程, 2010, 28(S1):222-225;276.WANG X T, ZHANG Y C, HE L F.Study on resource utilization of microbial feed produced by fermentation of kitchen waste[J].Environmental Engineering, 2010, 28(S1):222-225;276.
[21] 唐宇琦, 叶松涛, 刘嘉, 等.分子伴侣作用下的蛋白质稳定与进化[J].合成生物学, 2022, 3(3):445-464.TANG Y Q, YE S T, LIU J, et al.Molecular chaperones promote protein stability and evolution[J].Synthetic Biology Journal, 2022, 3(3):445-464.
[22] 阮青云, 黄莘, 孟子钧, 等.蛋白质稳定性计算设计与定向进化前沿工具[J].合成生物学, 2023, 4(1):5-29.RUAN Q Y, HUANG X, MENG Z J, et al.Computational design and directed evolution strategies for optimizing protein stability[J].Synthetic Biology Journal, 2023, 4(1):5-29.
[23] 黄超, 秦磊磊, 沈侨, 等.黑水虻幼虫蛋白质分级提取及理化性质研究[J].化学与生物工程, 2019, 36(1):26-30.HUANG C, QIN L L, SHEN Q, et al.Sequential extraction and physicochemical properties of black soldier fly(Hermetia illucens L.)larvae protein[J].Chemistry &Bioengineering, 2019, 36(1):26-30.
[24] XU Z L, PAN S J, LI G, et al.Albumin conjugating amino acid schiff-base metal complexes for scavenging superoxide anion radical[J].Journal of Inorganic and Organometallic Polymers and Materials, 2015, 25(6):1313-1319.