纳豆(natto)是由纳豆芽孢杆菌(Bacillus subtilis natto)发酵而成的一种食品,富含氨基酸、有机酸、寡糖等多种易被人体吸收的成分,具有抗肿瘤、降血压、防止骨质疏松、调整肠功能等保健作用[1]。同时,纳豆在发酵过程中会产生大量的纳豆激酶(nattokinase),是一种对人体有益的碱性蛋白酶,它在胃肠道中可以保持稳定活性,具有较好的溶解血栓效果,因此食用纳豆能够预防血栓栓塞性疾病[2]。
目前,对纳豆发酵条件的优化通常以纳豆激酶活性为判断依据,通过接种量、发酵时间、发酵温度等参数的研究,筛选合适的纳豆发酵条件,但由于纳豆发酵过程中发酵菌株不同,纳豆激酶活性也具有较大差异。田莉等[3]利用高产纳豆激酶的工程菌,通过响应面优化法优化了该菌株液态发酵的最佳发酵培养条件,使液态发酵下的纳豆激酶活性达到2 186.17 IU/mL。在液态发酵时,菌株的纳豆激酶活性随接种量增加呈先增加后降低趋势,接种量在3%时纳豆激酶活性最高,并在6%~9%接种量呈大幅下降趋势。王晶等[4]在对纳豆固态发酵研究中采用对甲苯磺酰-L-精氨酸甲酯法测定纳豆激酶活性,利用正交优化法优化纳豆发酵条件。使用甘油作为碳源,纳豆接种量为6%,在此发酵条件生产的纳豆颜色、口感、黏度与拉丝效果都较好。此外,固态发酵时纳豆激酶活性随接种量的增加呈先降低再增加的趋势。赵廉谦[5]以豆腐渣为底物发酵纳豆,进行Plackett Burman等实验,采用福林酚法与纤维蛋白平板法检测纳豆激酶活性发现,随着发酵时间的增加,酶活性开始缓慢下降,36 h时达到最高峰,到44 h时菌体会发生自溶。李恋龙等[6]以纳豆激酶酶活力为主要指标,以感官评定为辅助,通过正交试验优化纳豆发酵条件,研究发现,纳豆激酶活性在发酵18~26 h呈上升趋势,其中22~26 h纳豆激酶活性显著上升,随后纳豆激酶酶活性会快速下降。KAPOOR等[7]通过将不同种黄豆作为底物,以同种纳豆芽孢杆菌接种,结果表明,纳豆发酵过程中底物的选择对纳豆激酶活性影响不大。此外,有学者以不同底料发酵纳豆并优化条件后,发现纳豆激酶活性随温度升高呈先升高后降低的趋势,但在30~40 ℃发酵温度下纳豆激酶活性有较大差异,最高达到1 473.37 U/mL[8-11]。
1992年,NAKAMURA等[12]通过鸟枪法克隆了纳豆芽孢杆菌中编码纳豆激酶的aprN基因,总长度为1 473 bp。该基因编码381个氨基酸,前29个氨基酸残基组成信号肽序列,分子质量约为28 kDa[13]。葛芸等[14]通过构建aprN基因失活菌株,用纤维蛋白平板法未检测到溶栓活性,揭示了纳豆激酶是纳豆芽孢杆菌中唯一具有纤溶活性的酶。目前,aprN基因已经在植物、乳酸菌、大肠杆菌、毕赤酵母和动物细胞等进行了异源表达研究[15-19]。
纳豆发酵过程中产生的氨气是影响纳豆风味的主要因素之一,与产生氨气相关的基因有rocG、gudB和ure,其中rocG和gudB基因编码谷氨酸脱氢酶(glutamate dehydrogenase, GDH),ure基因编码尿素酶(urease)[20]。KADA等[21]在商品纳豆发酵剂中筛出一株枯草芽孢杆菌,并构建枯草芽孢杆菌rocG、gudB二者均失活的突变体,结果表明双重失活株发酵氨生产水平低于原始菌株的50%,这表明谷氨酸的脱氨是纳豆发酵过程中产生氨的主要反应。此外,在对GDH的研究中发现,通常情况下gudB基因不具有生物活性,但若当rocG基因失活,gudB基因会自发进行9 bp重复序列的缺失突变形成gudB1基因,从而产生有活性的GDH[22]。
aprN与rocG基因纳豆激酶活性与氨气产生量的生物学特性相关,但在不同发酵条件下两基因的定量表达及其与纳豆激酶活性、与氨气产生量的关系暂未见报道。本研究以本课题组筛出的一株纳豆芽孢杆菌为供试菌株,以接种量、发酵时间、发酵温度为参数,通过正交试验研究纳豆的发酵条件,同时采用实时荧光定量PCR方法,探究该菌株在发酵过程中aprN基因与纳豆激酶活性、rocG基因与氨气产量的关系,从而筛选出高酶活、产氨较少的纳豆发酵条件,为纳豆生产工艺提供参考依据。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株与主要试剂
本试验所用的菌株为实验室筛出的1株纳豆芽孢杆菌(GI:2626074044),发酵所用的小粒大豆由黑龙江省农科院提供。
细菌RNA提取试剂盒、反转录试剂盒,天根生化科技(北京)有限公司;PCRmix,北京聚合美生物科技有限公司;SYBR qPCR Mix,深圳市华晨阳有限公司。
1.1.2 试验设备
GR60高温高压灭菌锅,厦门致微仪器有限公司;Eppendorf concentrator Plus真空干燥设备、5427R离心机,德国艾本德股份公司;DK-8D水浴锅,广州合众生物科技有限公司;ETC811 PCR仪,东胜兴业科学仪器有限公司;Nanodrop 2000微量分光光度计,赛默飞世尔科技(中国)有限公司;Mix-28+涡旋振荡器,杭州米欧仪器有限公司;Sartorius电子天平、CFX96 Optics Module荧光定量PCR仪、DH124D培养箱,天津市泰斯特仪器有限公司;HZQ-C空气浴摇床,哈尔滨市东联电子技术开发有限公司;BH-90氨气检测仪,保时安电子科技有限公司。
1.1.3 尿激酶标准曲线制备
将100 000 U尿激酶冻干粉溶解于10 mL生理盐水,获得10 000 U/mL的尿激酶溶液,进一步稀释依次得到200~2 000 U/mL(梯度差为200 IU/mL)的尿激酶溶液,通过纤维蛋白平板法绘制尿激酶标准曲线,标准曲线见图1。
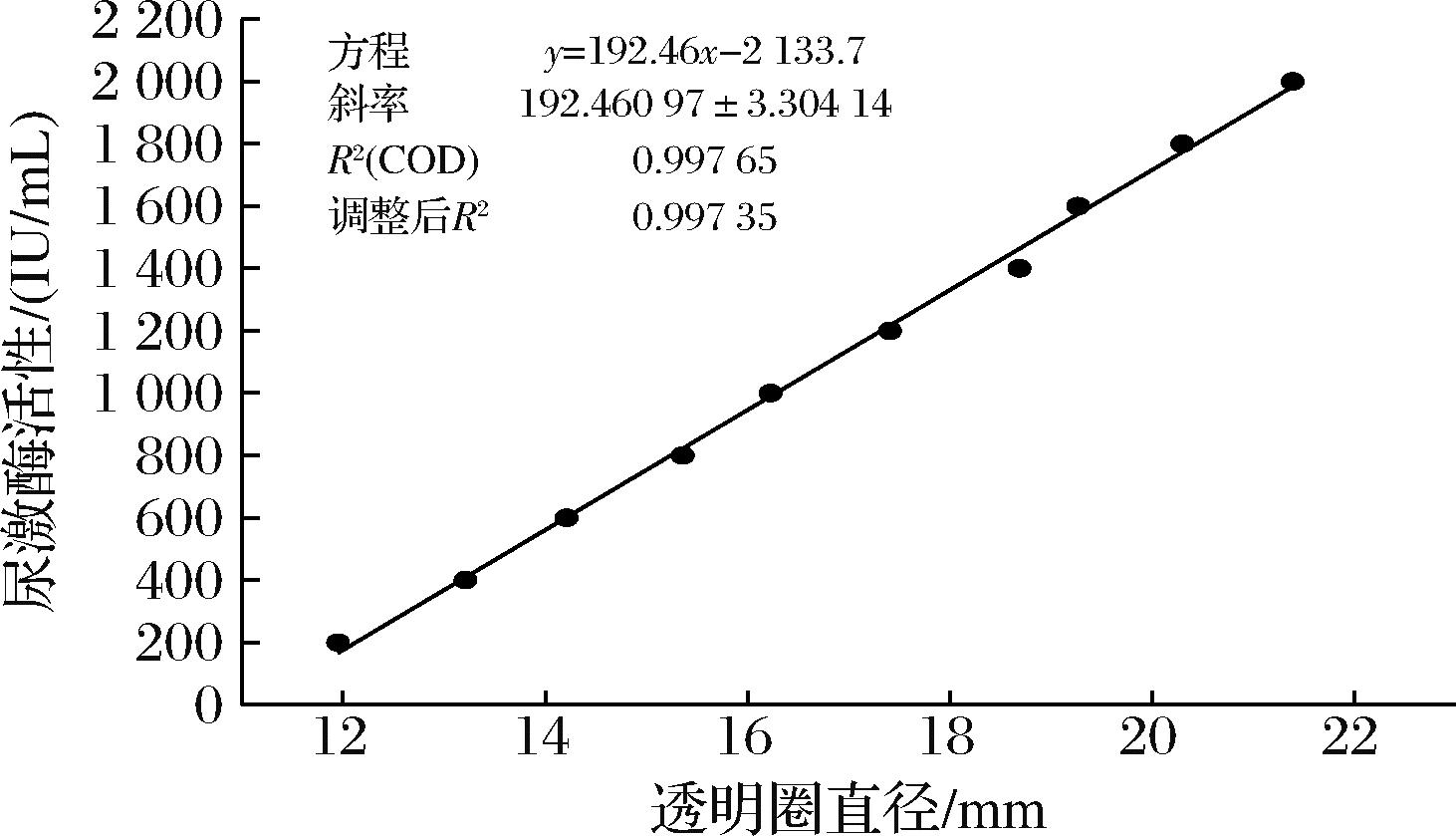
图1 尿激酶标准曲线
Fig.1 Preparation of urokinase standard curve
1.2 试验方法
1.2.1 纳豆芽孢杆菌菌液制备
将本试验室保存的纳豆芽孢杆菌在LB固体培养基上活化,挑取单菌落至装有100 mL液体LB培养基的三角瓶中,在37 ℃、180 r/min条件下培养至对数生长期(OD600值为0.8)。
1.2.2 纳豆芽孢杆菌发酵纳豆
称取200 g大豆,加入3倍体积的水浸泡12 h,清洗并沥干水分后放入高压灭菌锅中122 ℃、20 min蒸熟,加入制备好的纳豆芽孢杆菌菌液,搅拌均匀并分装到小盒中,于培养箱内发酵后在4 ℃后熟24 h。
1.2.3 纳豆发酵过程的单因素试验
以发酵时间(12、18、24、30 h)、菌液接种量(2%、3%、4%、5%,体积分数,下同)和发酵温度(25、29、33、37 ℃)为主要影响因素,进行纳豆发酵条件的单因素试验。
1.2.4 纳豆发酵过程的正交试验
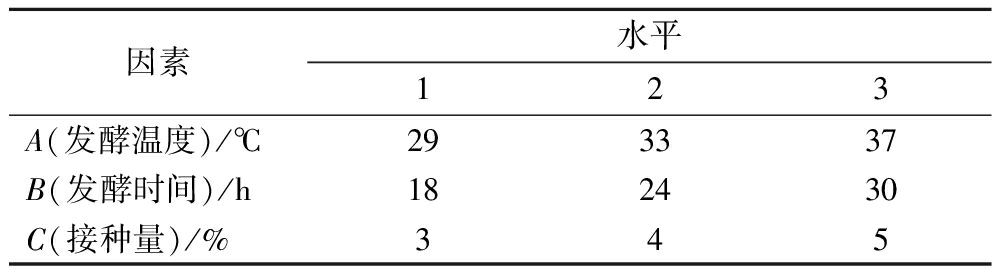
根据单因素试验结果,采用L9(34)正交表对纳豆发酵条件进行正交试验,以发酵温度、发酵时间、接种量为3因素,每个因素设3个水平,具体如表1所示。
表1 正交试验因素水平表
Table 1 Orthogonal test factor level table
因素水平123A(发酵温度)/℃293337B(发酵时间)/h182430C(接种量)/%345
1.2.5 纤维蛋白平板法测定纳豆激酶活性
将0.15 g纤维蛋白原溶解于150 mL PBS缓冲液中(1 mg/mL),将2 g琼脂糖放入200 mL PBS缓冲液中并加热溶解,将这2种溶液放在45 ℃恒温水浴锅中保温备用。取15 mL纤维蛋白-PBS缓冲液(1 mg/mL)、20 mL琼脂糖-PBS缓冲液和100 U/mL的凝血酶1 mL放入三角瓶中,混匀后迅速倒入培养皿中,冷却后制成纤维蛋白平板。用胶头滴管在纤维蛋白平板上打孔,向孔内加入10 μL尿激酶标准液或纳豆粗酶液,37 ℃培养18 h后用游标卡尺测量溶解圈直径。
1.2.6 纳豆粗酶液制备
将灭菌后的研钵与生理盐水置于4 ℃冰箱预冷,称取发酵好的纳豆2 g放入研钵中,加入2 mL生理盐水充分研磨,放入4 ℃冷藏20 min后加入4 mL生理盐水,混匀后装入离心管,7 000 r/min离心10 min,上清液即为纳豆粗酶液。
1.2.7 纳豆发酵过程中氨气值检测
利用氨气检测仪对纳豆发酵过程中产生的氨气量进行实时检测。
1.2.8 纳豆中纳豆芽孢杆菌RNA的提取与cDNA制备
用灭菌的玻璃棒搅拌纳豆,然后加入10 mL生理盐水与少许玻璃珠,振荡2 min,吸取悬浊液并离心收集菌体,利用细菌RNA提取试剂盒提取纳豆芽孢杆菌的RNA,并利用细菌反转录试剂盒制备cDNA。
1.2.9 纳豆芽孢杆菌aprN与rocG基因表达的定量分析
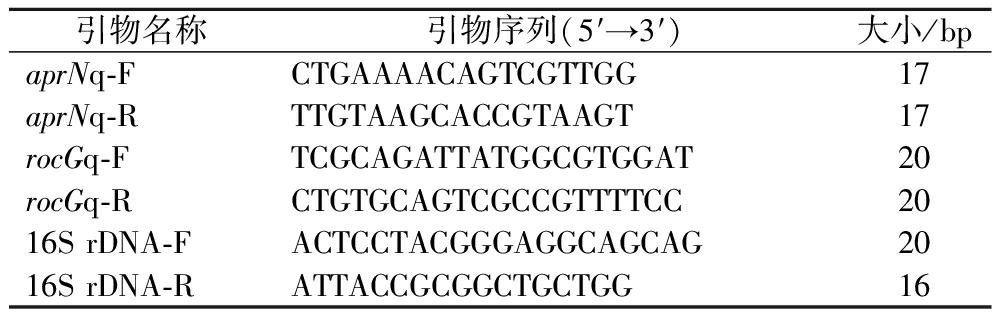
以1.2.8节制备的纳豆芽孢杆菌cDNA为模板,利用NCBI根据Genbank基因序列设计相应荧光定量引物进行qRT-PCR,以16 s rRNA为内参基因,引物信息见表2。qRT-PCR扩增体系为25 μL,具体组分及浓度见表3,qRT-PCR程序设定:95 ℃ 10 min;(95 ℃ 15 s,50 ℃ 30 s,72 ℃ 15 s)×40个循环。以29 ℃发酵条件组作为数据对照组,使用2-ΔΔct法分析数据。
表2 引物序列
Table 2 Primer sequence
引物名称引物序列(5′→3′)大小/bpaprNq-FCTGAAAACAGTCGTTGG17aprNq-RTTGTAAGCACCGTAAGT17rocGq-FTCGCAGATTATGGCGTGGAT20rocGq-RCTGTGCAGTCGCCGTTTTCC2016S rDNA-FACTCCTACGGGAGGCAGCAG2016S rDNA-RATTACCGCGGCTGCTGG16
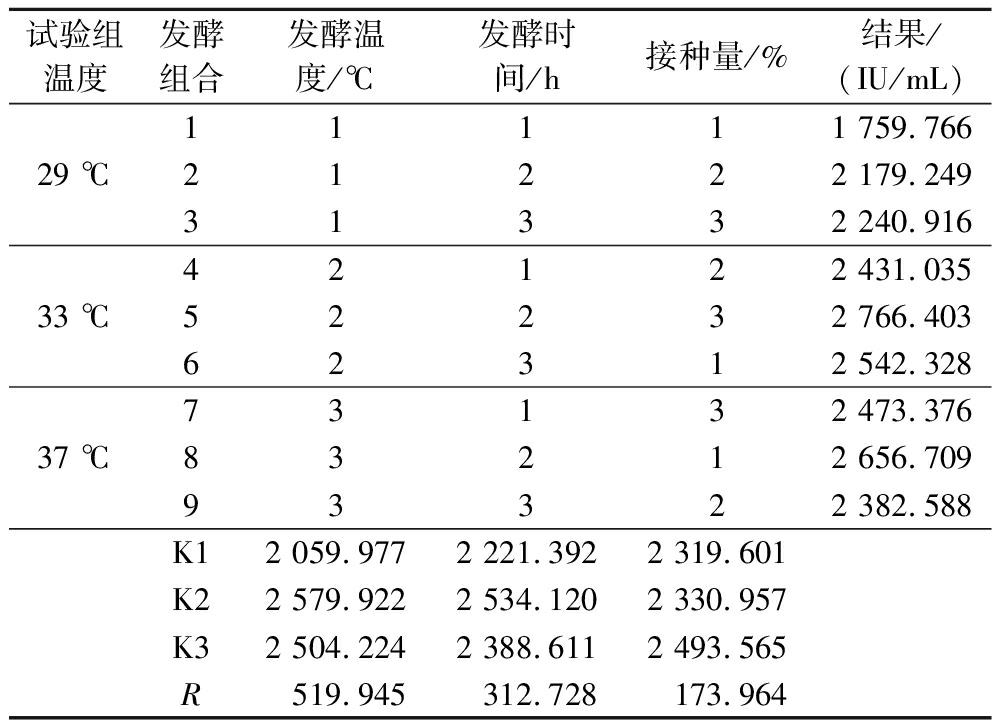
表3 正交试验结果
Table 3 Orthogonal test results
试验组温度发酵组合发酵温度/℃ 发酵时间/h接种量/%结果/(IU/mL)29 ℃11111 759.76621222 179.24931332 240.91633 ℃42122 431.03552232 766.40362312 542.32837 ℃73132 473.37683212 656.70993322 382.588K12 059.9772 221.3922 319.601K22 579.9222 534.1202 330.957K32 504.2242 388.6112 493.565R519.945312.728173.964
注:29 ℃试验组(1、2、3);33 ℃试验组(4、5、6);37 ℃试验组(7、8、9)(下同)。
2 结果与分析
2.1 纳豆发酵条件的单因素试验结果
2.1.1 不同发酵时间对纳豆激酶活性的影响
在本研究中分别测定了纳豆发酵12、18、24、30、36 h纳豆激酶的活性并与尿激酶标准曲线(图1)比对活力大小,结果表明纳豆发酵12~18 h期间纳豆激酶活性大幅度增加,如图2所示,在发酵24 h时,纳豆激酶活性达到最高2 478.2 IU/mL;发酵36 h时,发酵时间较长,且纳豆激酶活性较低。因此在后续纳豆发酵条件正交试验时可选择18、24、30 h作为纳豆发酵时间的3个水平。
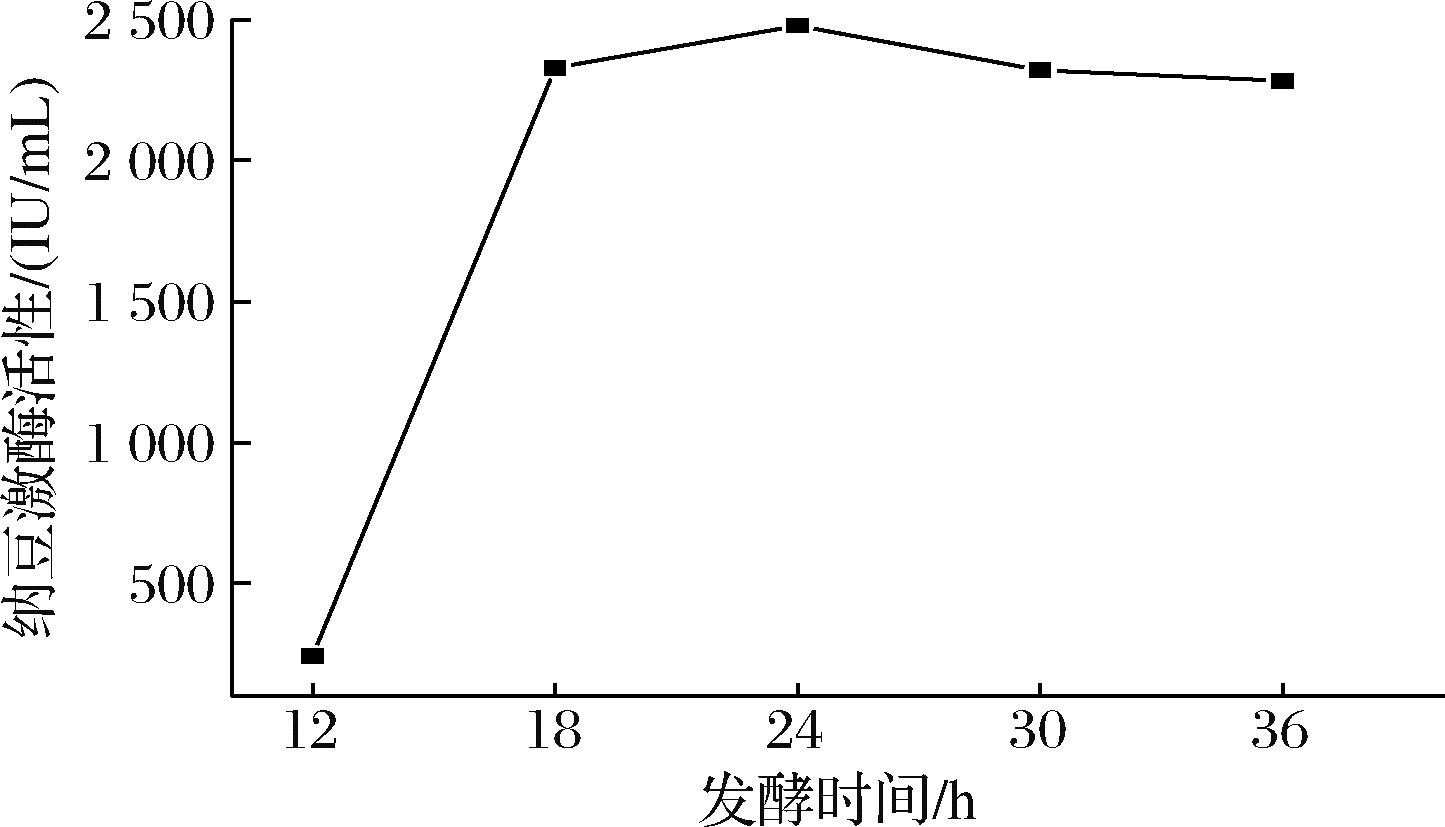
图2 发酵时间对纳豆激酶活性的影响
Fig.2 Effect of fermentation times on nattokinase activity
2.1.2 不同接种量对纳豆激酶活性的影响
试验结果显示,纳豆发酵过程中纳豆芽孢杆菌菌液(OD600=0.8)的接种量(2%、3%、4%、5%、6%)对纳豆激酶活性影响显著。随着纳豆芽孢杆菌菌液接种量由2%增加到5%,纳豆激酶活性持续增加,如图3所示,在接种量5%时纳豆激酶活性达到最高2 380.449 IU/mL。纳豆芽孢杆菌菌液接种量为6%时,纳豆激酶活性急剧降低。因此,可以选择3%、4%、5%纳豆芽孢杆菌菌液接种量作为正交试验的3个水平。
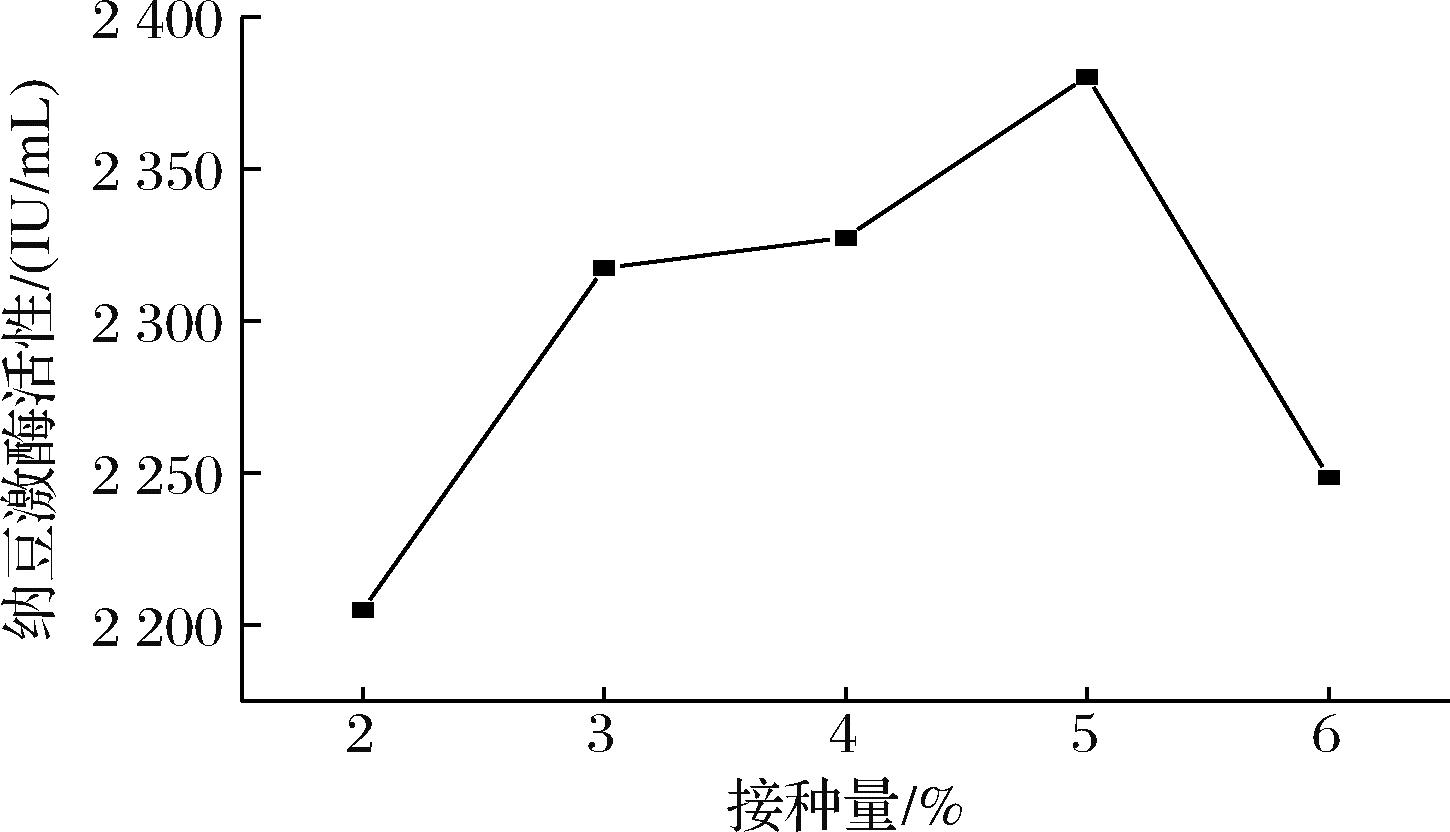
图3 接种量对纳豆激酶活性的影响
Fig.3 Effect of inoculation quantity on nattokinase activity
2.1.3 不同温度对纳豆激酶活性的影响与分析
在以温度为单一变量的发酵条件下,测定纳豆激酶活性。试验结果显示,随着发酵温度从25 ℃升高到33 ℃,纳豆激酶活性持续上升,如图4所示,在发酵温度33 ℃时纳豆激酶活性达到峰值2 247.65 IU/mL。发酵温度高于33 ℃后,纳豆激酶活性则降低。然而发酵过程中发现温度达到40 ℃时,纳豆形状干瘪、口感较硬,因此在后续的正交试验中选择29、33、37 ℃为发酵温度的3个水平。
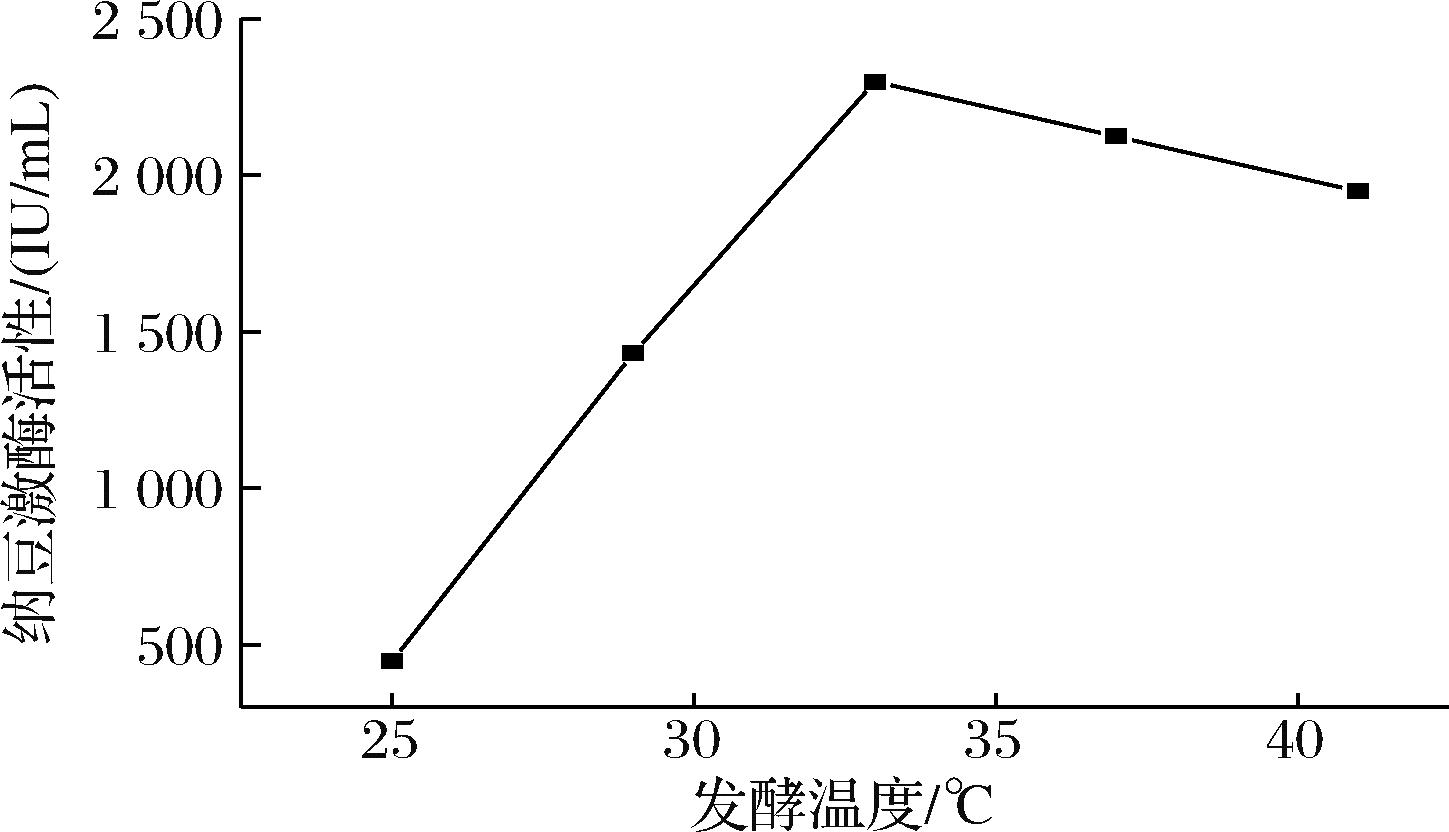
图4 发酵温度对纳豆激酶活性的影响
Fig.4 Effect of fermentation temperatures on nattokinase activity
2.2 纳豆发酵条件的正交试验结果
根据正交试验表进行纳豆发酵,采用纤维蛋白平板法测定纳豆激酶活性,筛选纳豆最佳的发酵条件。试验结果如表3所示,该表中极差数据表明,纳豆发酵因素影响力由大到小的顺序为:发酵温度>发酵时间>接种量,根据正交试验结果表中平均值表示最优发酵温度为33 ℃、最优发酵时间为24 h、最优接种量为5%。
2.3 纳豆发酵过程中氨气值检测
利用氨气检测仪检测纳豆发酵过程中的氨气值,按照正交试验表进行检测,以不同发酵温度分为3组绘制结果折线图,每组以发酵18 h为对照。结果如图5所示,37 ℃下发酵组合的纳豆氨气产生的量高于29、33 ℃发酵组合。对不同温度各个时间段氨气的积累量统计,见表4所示,由表可知29、33 ℃发酵组合氨气积累速度先快后慢,37 ℃发酵组合氨气积累速度先慢后快。2个结果表明随着发酵温度升高,氨气产生的量增加。
表4 不同温度各个时间段氨气积累量
Table 4 Ammonia accumulation at different temperatures in different time periods

温度/℃时间段/h氨气积累量/(mg/m3)2918~240.062 3 24~300.041 0 3318~240.197 624~300.084 43718~240.513 824~300.757 7
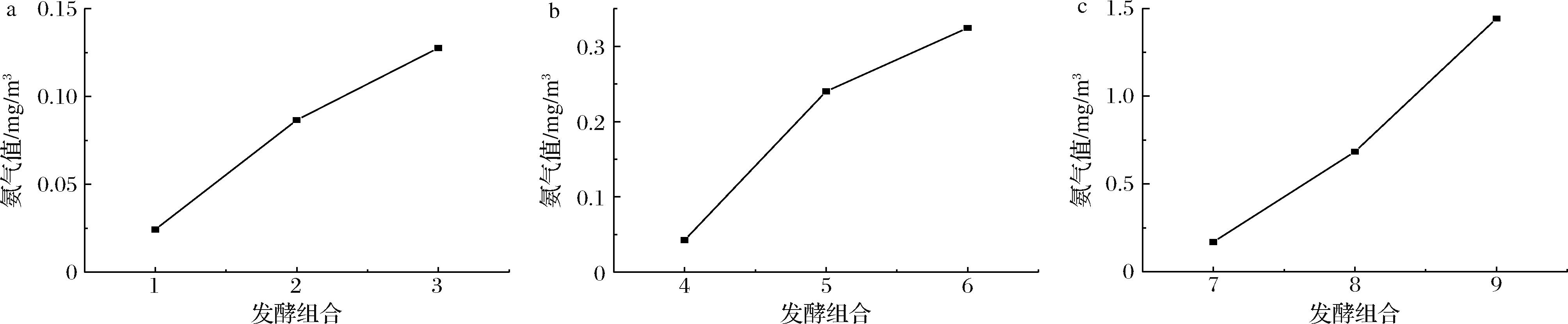
a-29 ℃试验组;b-33 ℃试验组;c-37 ℃试验组
图5 纳豆发酵的氨气值测定
Fig.5 Determination of ammonia value in natto fermentation
2.4 纳豆芽孢杆菌aprN与rocG基因表达的定量分析
为检测不同发酵条件下的纳豆激酶基因aprN与产氨基因rocG的表达模式,根据正交试验表的发酵组合进行试验,通过qRT-PCR分析不同发酵条件下2个基因的相对表达量,将表3中的发酵组合分为3个温度试验组,以每组18 h作为对照,利用2-ΔΔCT法对基因进行表达量分析、prismch软件进行Bonferroni的多重比较检验分析结果见图6和图7。结果表明在所有试验组中发酵组合5(33 ℃、24 h、5%)的aprN基因表达量最高,rocG表达量最低。29 ℃试验组中发酵组合2、3的aprN基因表达显著下调,33 ℃试验组中组合5中aprN基因表达显著上调,为该试验组对照组的2倍。37 ℃试验组中组合9显著下调。29 ℃试验组中组合2的rocG基因表达量最高,为该试验对照组的2倍,33 ℃试验组中基因表达量低于其他实验组,其中组合5仅为对照组的40%。以上结果表明该菌株较适合在33 ℃条件下发酵,且33 ℃、24 h、5%这一纳豆发酵条件下的aprN与rocG基因表达量较符合理想发酵条件下的aprN与rocG基因表达量。
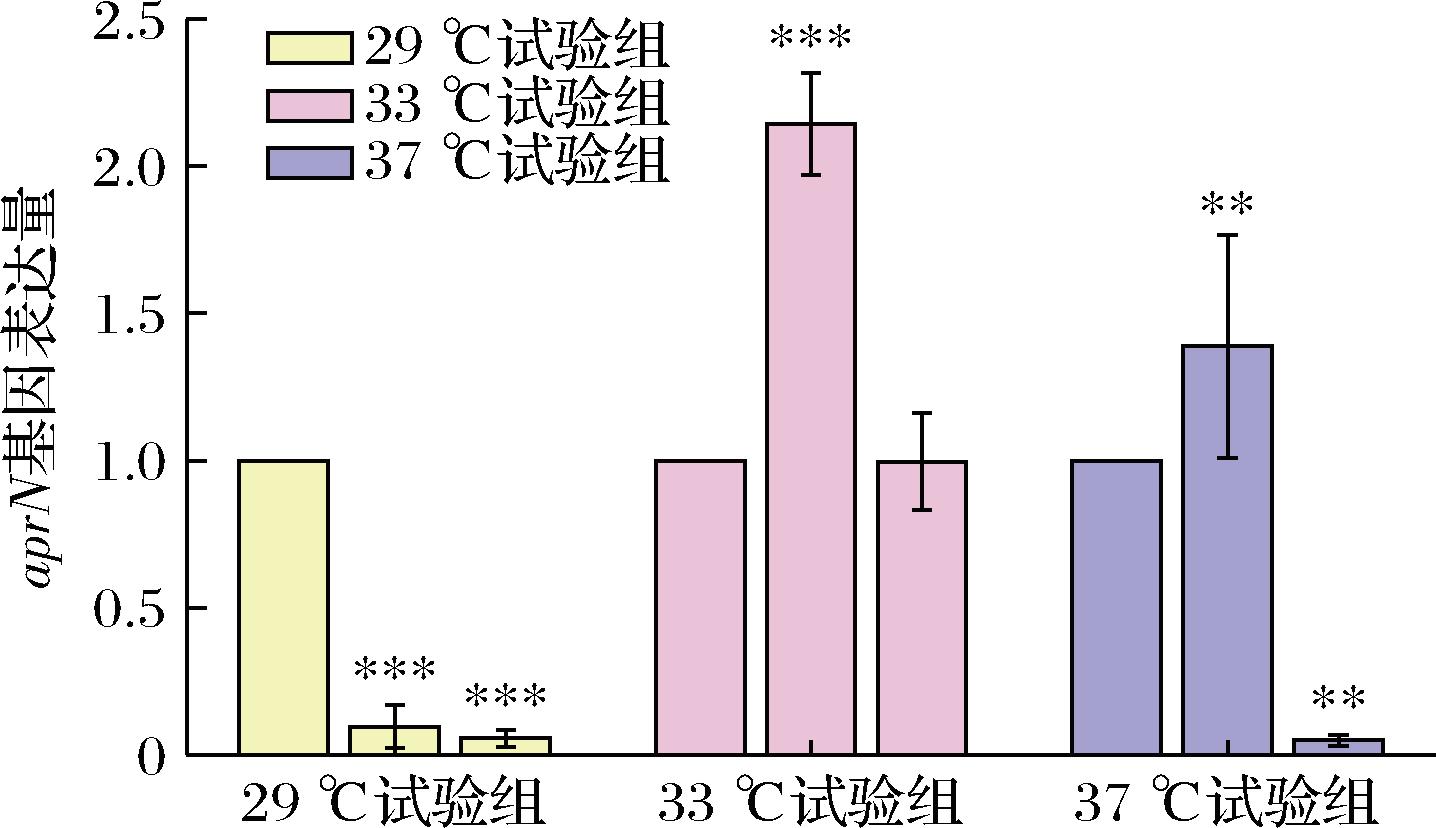
图6 aprN基因在不同发酵条件下相对表达量
Fig.6 Analysis of relative expression levels of aprN gene under different fermentation conditions
注:***表示P<0.001,**表示P<0.01,*表示P<0.05(下同)。
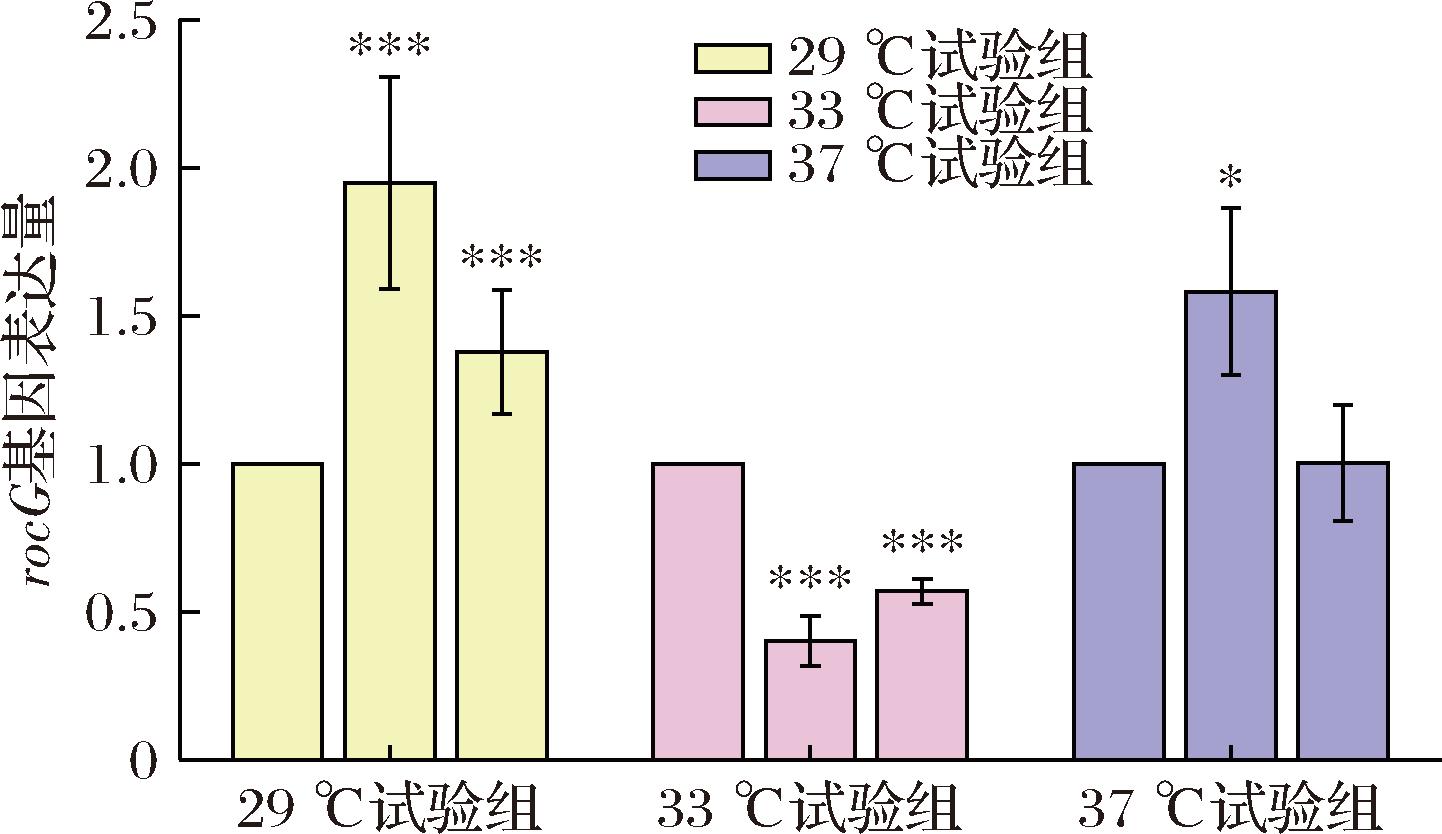
图7 rocG基因在不同发酵条件下相对表达量
Fig.7 Analysis of relative expression levels of rocG gene under different fermentation conditions
3 结论
纳豆作为保健食品,其纳豆激酶的活性是判断纳豆品质的重要指标,通过优化发酵条件提升纳豆激酶的活性是改善纳豆品质的重要途径。常用的纳豆发酵条件的优化方法有单因素试验和正交试验,其主要的发酵影响因素包括发酵温度、发酵时间、接种量、发酵基质及发酵菌种等。在纳豆发酵的相关研究中,张海粟等[23]利用响应面法优化条件、Folin-酚法测定纳豆激酶活性,制备了口感较好的箭筈豌豆纳豆。当接种量超过2%的情况下,纳豆激酶活性缓慢降低,这可能是因为菌体生长速度快、菌体间营养成分竞争大,导致底物初级代谢快,从而导致纳豆激酶活性降低[24]。同时YANG等[25]通过混合菌种发酵制备纳豆的研究也表明了接种量初始浓度较低的发酵速度慢,不易于积累发酵产物;初始浓度较高的新陈代谢较快,细胞要消耗大部分营养物质生长,产生大量发酵废物,导致纳豆品质降低。在本研究前期发现,2%~6%接种量之间,纳豆激酶活性先增加再降低,在5%达到峰值2 380.449 U/mL。因此随着初始接种量增加,菌体数目增加,纳豆发酵较为完全,纳豆激酶活性随之增加,而接种量过大时细胞数目过多,增长速度过快,消耗了大豆内营养成分进而抑制纳豆激酶活性。姜晓阳等[26]利用混合菌株固态发酵花生粕,以纳豆激酶的活力和γ-氨基丁酸的含量为指标进行正交试验,表明纳豆激酶活性随发酵温度呈现先上升后下降的趋势,在34 ℃时达到峰值,与本研究达到峰值的温度相近,这可能是两株菌最适生长温度较相似。纳豆发酵过程中前期温度升高,菌体繁代速率加快、菌体浓度升高、发酵速度加快,纳豆激酶活性随之增长,达到最适温度后纳豆激酶出现活性降低的趋势,表明超过最适生长温度,抑制发酵过程,同时抑制了纳豆激酶活性。在温度较高的发酵条件下,底物豆子体积出现明显变化,37 ℃时豆子体积稍有减小,但仍绵软,在41 ℃时豆子已经干瘪、发硬并且颜色加深,这与罗仓学等[27]的研究相似。此外,本研究发现发酵时间对纳豆激酶活性影响不显著,18~30 h发酵阶段纳豆激酶趋势平和,30 h过后纳豆激酶活性呈下降趋势,表明菌活力降低、数目过多消耗营养物质进而导致纳豆激酶活性降低。纳豆发酵产生的纳豆激酶是溶解血栓的最主要的成分,但因纳豆风味原因难以被广泛接受,因此在保证纳豆激酶品质的同时降低氨味具有较大的意义。本研究通过氨气检测仪对纳豆发酵的氨气值进行检测,发现在发酵前24 h阶段氨气积累较快,但超过24 h氨气积累较慢氨气积累速度减慢,并且氨气积累量与积累速度随发酵温度增加而增加。WU等[28]通过研究低场核磁共振和磁共振成像技术监测纳豆发酵过程,发现由于发酵过程中氨的产生导致28 h后纳豆pH增加。结合该研究,纳豆发酵过程中产生的氨气可以被纳豆吸收一部分,所以超过24 h以后纳豆氨气积累的较慢。本研究以单因素试验、正交试验结合分子遗传学手段探讨纳豆芽孢杆菌发酵纳豆的最佳发酵条件。结果表明,33 ℃、24 h、接种5%的发酵条件下,aprN基因相对表达量较高,rocG基因相对表达量低,符合理想发酵条件的要求,并科学地验证了正交试验的发酵结果。在此条件下,纳豆激酶活性为2 766.403 U/mL,氨气值为0.316 ppm,虽然在此条件下纳豆发酵产生的氨气并不是最低的,但该条件下的纳豆激酶活性最高且aprN基因表达量为所有发酵条件下表达最高,rocG基因表达量为所有发酵条件下表达最低,因此该条件为一个理想且科学的发酵条件。综上所述,基于本研究所采用的纳豆发酵条件正交试验及纳豆芽孢杆菌aprN与rocG基因表达的定量分析,确定纳豆最佳的发酵条件为发酵温度33 ℃、发酵时间24 h及接种量5%,该条件下发酵的纳豆中纳豆激酶活性达到2 766.403 U/mL,而且产生的氨气量较低,能够同时满足纳豆品质与风味的需求。
[1] WANG Y X, WANG J, ZHANG X, et al.Genomic and transcriptomic analysis of Bacillus subtilis JNFE1126 with higher nattokinase production through ultraviolet combined 60 Co-γ ray mutagenesis[J].LWT, 2021, 147:111652.
[2] 姚明静, 杨杨, 范婧, 等.纳豆激酶的微生物生产及其生理功能的研究进展[J].食品工业科技, 2022, 43(14):435-444.YAO M J, YANG Y, FAN J, et al.Advance on nattokinase microbial production and physiological function[J].Science and Technology of Food Industry, 2022, 43(14):435-444.
[3] 田莉, 卢轶男, 朱建, 等. 产纳豆激酶的枯草芽孢杆菌基因工程菌发酵条件的响应面优化[J].武汉工程大学学报, 2018, 40(6): 619-626.TIAN L, LU Y N, ZHU J, et al. Optimization of fermentation conditions for nattokinase production by genetically engineered Bacillus subtilis using response surface methodology[J]. Journal of Wuhan Institute of Technology, 2018, 40(6): 619-626.
[4] 王晶, 刘鹏莉.高活性纳豆固态发酵工艺优化及纳豆口含片制备[J].食品工业, 2021, 42(10):44-48.WANG J, LIU P L.Optimization of solid-state fermentation technology of high activity natto and preparation of natto lozenges[J].The Food Industry, 2021, 42(10):44-48.
[5] 赵廉谦. 豆腐渣纳豆菌发酵工艺及其产品功能分析[D].太谷:山西农业大学, 2021.ZHAO L Q.Fermentation technology of Bacillus natto from bean curd residue and functional analysis of its products[D].Taigu:Shanxi Agricultural University, 2021.
[6] 李恋龙, 高云霞, 杜亚飞.风味纳豆的制备工艺研究[J].生物化工, 2022, 8(1):122-127.LI L L, GAO Y X, DU Y F.Study on the craftsmanship of flavor natto[J].Biological Chemical Engineering, 2022, 8(1):122-127.
[7] KAPOOR R, KHOWAL S, PANDA B P, et al.Comparative genomic analyses of Bacillus subtilis strains to study the biochemical and molecular attributes of nattokinases[J].Biotechnology Letters, 2022, 44(3):485-502.
[8] 张杰, 杨希娟, 党斌, 等.蚕豆纳豆发酵工艺优化及其酶学性质[J].食品工业科技, 2019, 40(6):205-210.ZHANG J, YANG X J, DANG B, et al.Optimization of fermentation process of natto by broad bean and its enzymatic properties[J].Science and Technology of Food Industry, 2019, 40(6):205-210.
[9] 用慧敏, 唐君钰, 丁靖苇, 等.花生蛋白纳豆菌发酵工艺条件的研究[J].安徽农业科学, 2017, 45(35):70-74.YONG H M, TANG J Y, DING J W, et al.Study on fermentation conditions of peanut protein of Bacillus natto[J].Journal of Anhui Agricultural Sciences, 2017, 45(35):70-74
[10] 于江淼, 王家林, 张海粟.黑纳豆固态发酵工艺优化的研究[J].中国调味品, 2020, 45(3):101-106.YU J M, WANG J L, ZHANG H S.Study on optimization of solid-state fermentation technology of black natto[J].China Condiment, 2020, 45(3):101-106.
[11] 耿晓然. 纳豆菌种选育及新型风味纳豆食品的开发[D].保定:河北农业大学, 2019.GENG X R.Screening of natto strain and the developing of a new flavor natto food[D].Baoding:Hebei Agricultural University, 2019.
[12] NAKAMURA T, YAMAGATA Y, ICHISHIMA E.Nucleotide sequence of the subtilisin NAT gene, aprN, of Bacillus subtilis (natto)[J].Bioscience, Biotechnology, and Biochemistry, 1992, 56(11):1869-1871.
[13] GUNKA K, THOLEN S, GERWIG J, et al.A high-frequency mutation in Bacillus subtilis:Requirements for the decryptification of the gudB glutamate dehydrogenase gene[J].Journal of Bacteriology, 2012, 194(5):1036-1044.
[14] 葛芸, 汤斌, 李松.纳豆芽孢杆菌产纳豆激酶发酵工艺控制及纤溶酶分析[J].食品与发酵工业, 2019, 45(16):176-180;186.GE Y, TANG B, LI S.Optimization of nattokinase fermentation by Bacillus natto and its fibrinolytic activity[J].Food and Fermentation Industries, 2019, 45(16):176-180;186.
[15] 韩岚, 鞠林芳, 牛一丁, 等.纳豆激酶基因的优化设计、合成及其在烟草叶片中的瞬时表达[J].中国生物工程杂志, 2015, 35(9):14-20.HAN L, JU L F, NIU Y D, et al.Optimization, synthesis and transient expression of nattokinase gene in tobacco(Nicotiana tabacum L.) leaves[J].China Biotechnology, 2015, 35(9):14-20.
[16] 董慧. 基于thyA基因的乳酸乳球菌表达系统的构建及纳豆激酶基因的克隆[D].保定:河北农业大学, 2013.DONG H.Construction of Lactoccus lactis expression systenm based on thyA gene and cloning of nattokinase gene[D].Baoding:Hebei Agricultural University, 2013.
[17] 李佳增. 纳豆激酶毕赤酵母X33高效表达双启动子系统构建及发酵条件优化[D].沈阳:辽宁大学, 2021.LI J Z.Construction and optimization of fermentation conditions of a dual-promoter subsystem for high expression of nattokinase in Pichia pastoris X33[D].Shenyang:Liaoning University, 2021
[18] 朱立成. 纳豆激酶和hGM-CSF在家蚕杆状病毒表达系统中表达纯化及活性研究[D].杭州:浙江大学, 2005.ZHU L C.Study on production of nattokinase and hGM-CSF in silkworm baculovirusexpression system using BmNPV and its biological activity analysis[D].Hangzhou:Zhejiang University, 2005.
[19] 于晓淼, 赵允章, 王锋超, 等.通过定点突变提高纳豆激酶纤溶活性和热稳定性[J].微生物学杂志, 2023, 43(2):21-27.YU X M, ZHAO Y Z, WANG F C, et al.Enhancing fibrinolytic activity and thermal stability of nattokinase by site-directed mutagenesis[J].Journal of Microbiology, 2023, 43(2):21-27.
[20] BELITSKY B R, SONENSHEIN A L.Role and regulation of Bacillus subtilis glutamate dehydrogenase genes[J].Journal of Bacteriology, 1998, 180(23):6298-6305.
[21] KADA S, YABUSAKI M, KAGA T, et al.Identification of two major ammonia-releasing reactions involved in secondary natto fermentation[J].Bioscience, Biotechnology, and Biochemistry, 2008, 72(7):1869-1876.
[22] CHEN K Y, GAO C C, HAN X M, et al.Co-fermentation of lentils using lactic acid bacteria and Bacillus subtilis natto increases functional and antioxidant components[J].Journal of Food Science, 2021,86(2):475-483.
[23] 张海粟, 王家林.箭筈豌豆纳豆的发酵工艺[J].青岛科技大学学报(自然科学版), 2021, 42(6):52-58.ZHANG H S, WANG J L.Fermentation process of common vetch natto[J].Journal of Qingdao University of Science and Technology (Natural Science Edition), 2021, 42(6):52-58.
[24] HU Y J, GE C R, YUAN W, et al.Characterization of fermented black soybean natto inoculated with Bacillus natto during fermentation[J].Journal of the Science of Food and Agriculture, 2010, 90(7):1194-1202.
[25] YANG Y, LAN G Q, TIAN X Y, et al.Effect of fermentation parameters on natto and its thrombolytic property[J].Foods, 2021, 10(11):2547.
[26] 姜晓阳, 胡迎芬, 郑靖义, 等.混菌固态发酵花生粕的工艺优化[J].食品工业科技, 2019, 40(22):120-124.JIANG X Y, HU Y F, ZHENG J Y, et al.Optimization of solid-state fermentation of peanut meal by mixed bacteria[J].Science and Technology of Food Industry, 2019, 40(22):120-124.
[27] 罗仓学, 刘晓宇, 张雯.响应面法优化鹰嘴豆发酵纳豆工艺[J].中国调味品, 2019, 44(2):51-55.LUO C X, LIU X Y, ZHANG W.Optimization of fermentation process of chickpea by response surface methodology[J].China Condiment, 2019, 44(2):51-55.
[28] WU J, LI Y R, GAO X S.Monitoring a typical fermentation process of natto by low-field nuclear magnetic resonance (LF-NMR) and magnetic resonance imaging (MRI) techniques[J].Analytical Methods, 2016, 8(39):7135-7140.