众所周知,肠道微生物群对健康至关重要[1]。为了维持肠道微生物群的平衡,人们越来越注重摄入有益微生物,尤其是乳酸菌[2]。乳杆菌属(Lactobacillus)和双歧杆菌属(Bifidobacterium)等乳酸菌是人体胃肠道中的常见菌群,被归类为益生菌。有研究表明,乳酸菌具有免疫调节的作用[3]。因此,通过摄入益生性乳酸菌来改善肠道环境,被认为是一种有效的免疫调节方法[4]。
嗜酸乳杆菌 L-55是从健康婴儿的粪便中分离出来的益生性乳酸菌,也是用于乳制品发酵的启动菌株[2]。已有研究表明,L-55菌株具有很高的附着性,尤其是对人体肠上皮细胞Caco-2的附着性[5]。此外,动物实验结果显示,L-55菌株不仅能够缓解过敏性鼻炎和特应性皮肤炎症状,还能抑制IgE抗体的产生[2,5]。研究还发现,L-55菌株对缓解花粉症症状具有显著效果[6],并且对家禽病毒性疾病具有疫苗增强剂的作用[7-8]。另外,研究表明[9],L-55菌株通过影响免疫细胞的数量和活性,发挥抗病毒的作用。
植物性雌激素是一类具有雌激素特性的植物来源化合物,主要包括异黄酮和木脂素两种化合物,它们广泛存在于人类饮食中,在大豆、葛根等豆科植物中含量较为丰富[10]。大豆富含的异黄酮类物质具有丰富的生物活性,包括降低心血管疾病风险、减少乳腺癌、结肠癌的发病率,以及改善骨骼健康等多种保健作用,因此备受关注[11]。大豆异黄酮是大豆在其生长过程中形成的一类次生代谢产物。自首次从大豆中分离出大豆异黄酮以来,已经鉴定出了12种不同结构的大豆异黄酮[12]。这些异黄酮可分为糖苷型和苷元型,其中糖苷型是异黄酮与糖类形成的配糖体,而苷元型则是游离的异黄酮[11]。游离型苷元包括大豆苷元(daidzein)、染料木黄酮(genistein)和黄豆黄素(glycitein),而结合型糖苷则包括大豆黄素苷(daidzin)、染料木素苷(genistin)、黄豆黄素苷(glycitin)等[11]。苷元型异黄酮更容易被吸收,除了在发酵食品中,大豆和大豆食品中几乎不以游离的形式存在,95%以上以配糖体的形式存在[12]。由于其与哺乳动物雌激素的化学结构相似,大豆异黄酮能够与雌激素受体结合,在特定的实验条件下表现出雌激素样的作用,因此被称为植物雌激素[13]。大豆中含有的异黄酮在肠道细菌的作用下,可以从糖苷型转换为苷元型[14]。肠道细菌代谢大豆苷元的代谢途径如图1所示[15]。大豆异黄酮的最初代谢产物是雌马酚(equol),研究表明,雌马酚是一种对人体非常有益的化合物,然而,能够将大豆苷元转化为雌马酚的个体较少[14],仅有30%到50%的成人能够产生雌马酚[16]。肠道细菌代谢染料木黄酮的代谢途径如图2所示[15]。5-羟基-雌马酚(5-hydroxy-equol,5-OH-EQ)也与雌马酚作用相似,具有雌激素样作用。
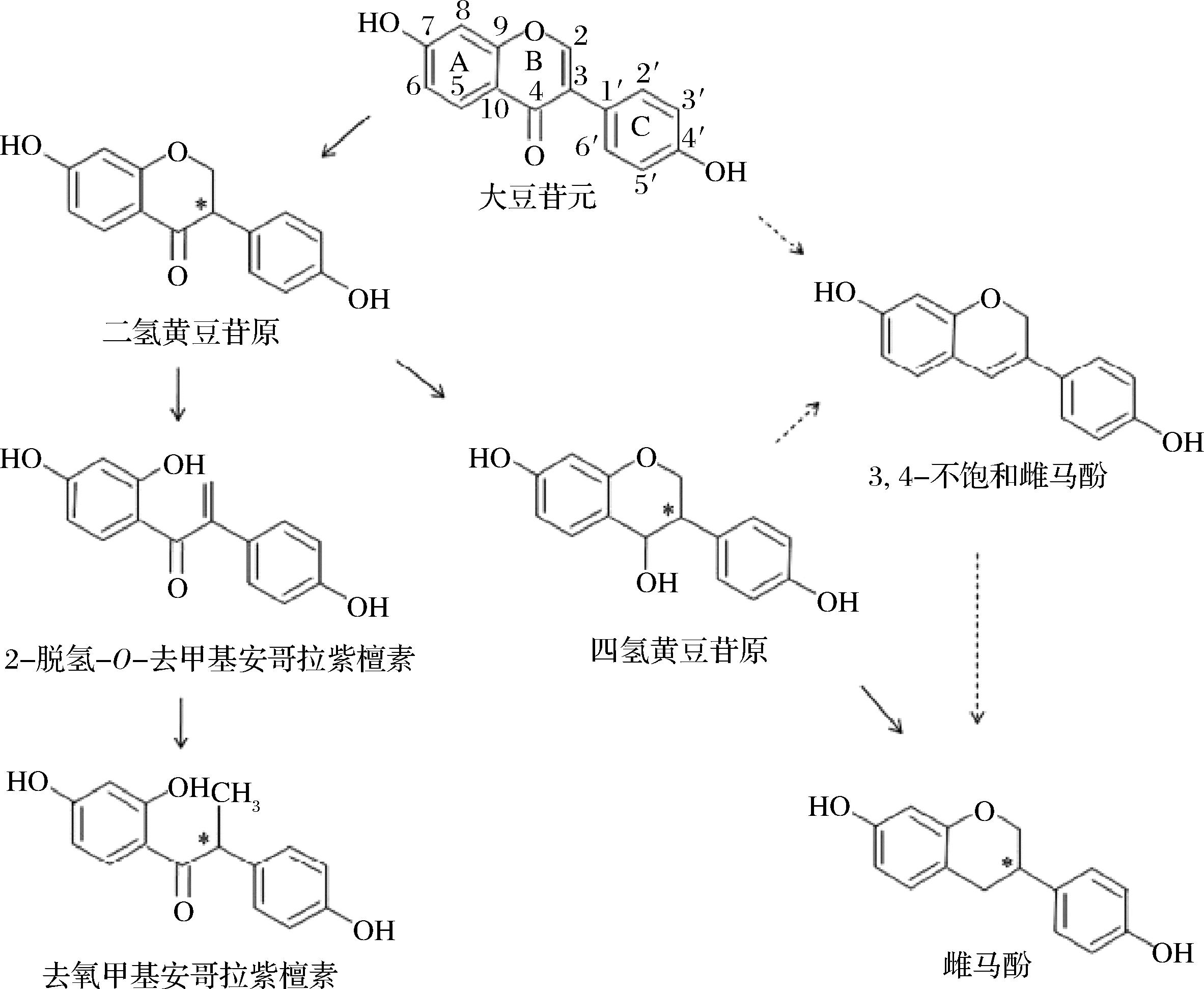
图1 肠道细菌对大豆苷元的代谢
Fig.1 The intestinal bacteria-mediated metabolism of daidzein
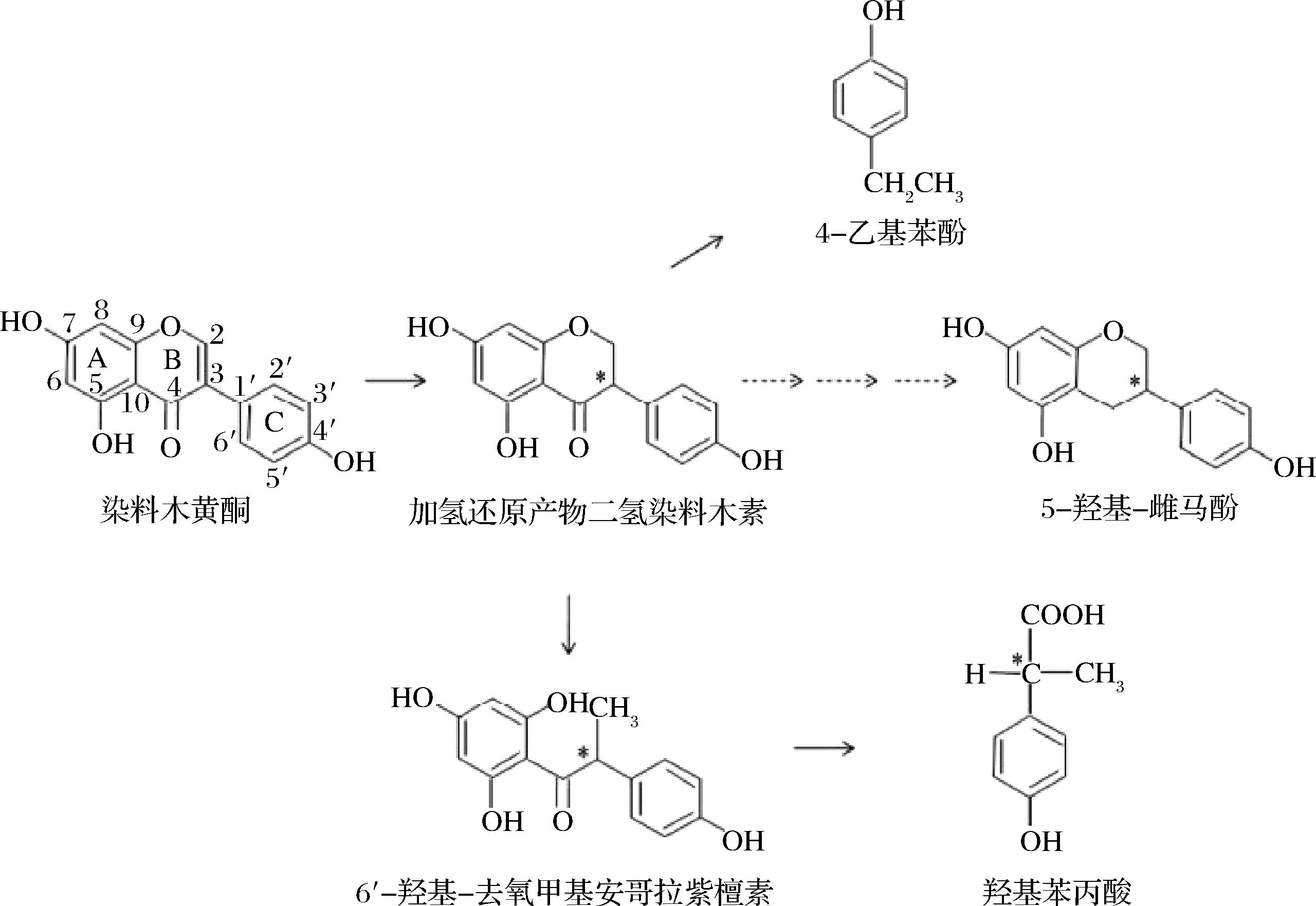
图2 肠道细菌对染料木黄酮的代谢
Fig.2 The intestinal bacteria-mediated metabolism of genistein
研究表明,参与异黄酮来源的大豆黄素苷转化为大豆苷元以及染料木素苷转化为染料木黄酮的酶均为β-葡萄糖苷酶[17]。DZNR、DHDR、DDRC和THDR是参与大豆苷元合成雌马酚的基因[18-19]。通过以前的研究,已获得了能够产生雌马酚的细菌Adlercreutzia equolifaciens DSM 19450T的完整基因组序列以及相关产生雌马酚的基因(图3)[20]。本研究关注L-55菌株中是否存在相关基因。
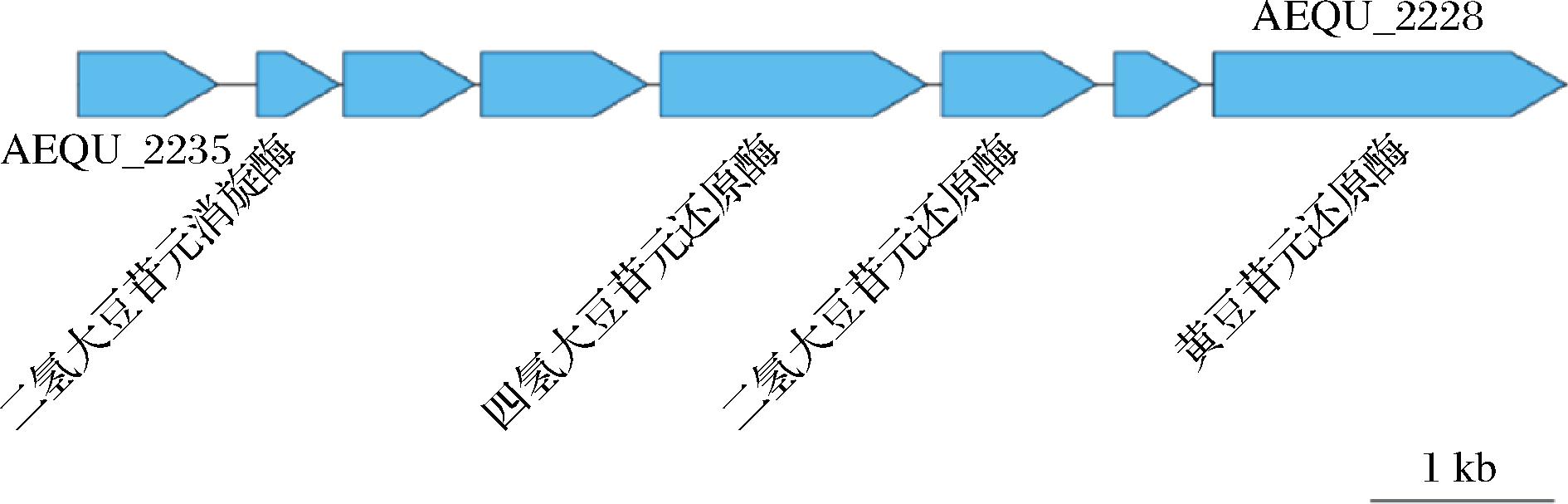
图3 人肠道细菌 Adlercreutzia equolifaciens 菌株中 将异黄酮转化为苷元型和雌马酚的相关基因群
Fig.3 Human intestinal bacterium Adlercreutzia equolifaciens converts isoflavones into aglycotype and equol related gene groups
以牛奶为原料的酸奶和益生菌饮料被视为优质的功能性食品。乳糖不耐受通常是消费牛奶产品的人们所面临的主要限制问题。乳糖不耐症指乳糖吸收不良患者在摄入乳糖后出现腹痛、腹胀、腹泻等症状。这种吸收不良是由于小肠无法消化或吸收乳糖引起的[21]。因此,对于乳糖不耐症患者而言,酸奶是一种有益的选择[22]。普通酸奶是由生牛乳经加热处理或浓缩后,在唾液链球菌嗜热亚种菌株(Streptococcus salivarius subsp. thermophilus)和德氏乳杆菌保加利亚亚种菌株(Lactobacillus delbrueckii subsp.bulgaricus)的共同作用下进行发酵制成的[23]。相比牛奶,酸奶的保质期更长,并且富含多种对肠道有益的微生物[24],并且对糖尿病等有益[25]。基于酸奶的概念,豆乳酸奶被研制而成,豆乳酸奶以豆乳为原料,是一种植物性发酵食品。由于以植物性素材制成,植物基酸奶不含胆固醇和乳糖,因此得到了不喜欢牛乳制品或对其过敏的人的关注[26]。本研究旨在探究不含完全乳糖的酸奶。
此外,异黄酮还具有其他生理学效果[27],如抑制酪氨酸激酶、抗血管新生、激活自然杀伤细胞、以及抗氧化等作用。在绝经后的女性中,随着雌激素分泌的减少,骨量减少、高胆固醇血症和动脉硬化发病率上升、骨质疏松风险增加等问题变得突出。此外,进入更年期后,由于荷尔蒙平衡紊乱,会出现上火、出汗、关节痛、心悸等症状,由于在雌激素水平低时异黄酮具有雌激素作用,因此对上述症状具有一定疗效[28-29]。另一方面,在雌激素水平高时,异黄酮也具有抗雌激素作用,可以预防乳腺癌[13]。因此检测豆乳中的异黄酮含量可以确定其雌激素效果。
由于豆乳具有很多益处,豆乳等大豆制品富含大豆蛋白[30]和异黄酮等功能性成分,市场上出现了许多与豆乳相关的食品,因此其成为功能性食品的热门原料。豆乳作为传统食品,常被用作豆腐的原料,其是从大豆中提取水溶性物质得到的产品。如今,豆乳作为一种健康饮料备受关注[31],许多西方国家的乳制品消费量正在下降,而植物性奶类的销量在增加[32]。植物性牛奶现在占牛奶行业总数的15%[33],还是低于牛奶的占比,因此,本研究着眼于探究与豆乳相关的食品,以发挥其更多的健康作用。豆乳中含有的异黄酮在微生物发酵过程中会发生结构变化。豆乳酸奶是通过脱糖的苷元型异黄酮进行发酵而产生的,这样就可以有效地摄取异黄酮的营养成分。豆乳酸奶中的大豆异黄酮能够提供普通酸奶所不含的植物性雌激素。相比普通酸奶,豆乳酸奶热量更低,蛋白质吸收更充分,备受以健康为中心人群的青睐。因此,研究与豆乳酸奶相关的微生物被认为对人类健康的研究具有重要意义。本研究侧重于有雌激素样活性的大豆苷元和染料木黄酮,探讨L-55菌株对大豆异黄酮向雌激素样物质转化的影响。嗜酸乳杆菌 L-55在维持健康方面发挥着多种重要作用,但其许多功能尚未被充分挖掘。因此,本研究旨在深入研究L-55菌株的功能。研究将L-55菌株添加到豆乳中进行发酵,并测定了豆乳酸奶中的大豆异黄酮含量,同时将其与市面上常见的唾液链球菌嗜热亚种菌株和德氏乳杆菌保加利亚亚种菌株发酵的豆乳酸奶进行了异黄酮含量比较。探讨了嗜酸乳杆菌 L-55菌株对豆乳发酵的影响。
1 材料与方法
1.1 材料与试剂
1.1.1 使用菌株
本实验使用了来自本实验室保存的酸奶发酵常用菌株:市售酸奶的唾液链球菌嗜热亚种菌株和德氏乳杆菌保加利亚亚种菌株,以及本实验室保存的嗜酸乳杆菌 L-55菌株。
1.1.2 试剂
MRS培养基,英国OXOID公司;磷酸盐缓冲液,美国Thermo Fisher Scientific公司;豆乳粉,日本九州乳業公司;二甲基亚砜(dimethyl sulfoxide, DMSO)、大豆苷元、染料木黄酮、雌马酚、5-羟基-雌马酚标准品,美国Sigma-Aldrich公司;所有有机溶剂均为分析纯。
1.2 仪器与设备
LC-2030高效液相色谱仪,日本岛津公司;细菌培养箱,美国Thermo Fisher Scientific公司;Aquelix 5超纯水机,美国默克密理博公司。
1.3 菌株培养
本实验使用的MRS培养基是一种典型的乳酸菌(Lactobacillus属)的选择性培养基,在许多研究中被采用。
制备过程如下:首先,在锥形瓶中加入1 L蒸馏水和52 g MRS培养基粉末混合,然后在灭菌前使用10%盐酸(质量分数,下同)调节pH值。接下来,将混合液置于高压蒸汽灭菌锅中,在121 ℃下灭菌15 min。灭菌后,将MRS液体培养基分装到试管中。然后,使用接种环从冷冻管中接种嗜酸乳杆菌 L-55至培养基中。随后,将含有L-55菌株的MRS液体培养基置于37 ℃下静置培养16 h。之后,使用磷酸盐缓冲液洗涤悬浮的菌体,以备后续的发酵培养。
1.4 嗜酸乳杆菌 L-55菌株的发酵条件
将200 mL豆乳中接种5%的嗜酸乳杆菌 L-55菌株,平均分入6个培养瓶中,不同温度下培养24 h,测定其pH值变化量及菌种活率。在确定培养温度后,将20 mL豆乳中接种5%的嗜酸乳杆菌 L-55菌株,培养48 h,每2 h检测菌种活率及pH值,以确定嗜酸乳杆菌 L-55菌株的最佳发酵条件。
1.5 豆乳酸奶的发酵
在烧杯中将80 g豆乳粉用1 L超纯水溶解,然后将配制好的豆乳在90 ℃下煮沸15 min灭菌。接着,将菌株加入到豆乳中进行发酵。分别将来自市售酸奶的唾液链球菌嗜热亚种菌株、德氏乳杆菌保加利亚亚种菌株以及嗜酸乳杆菌L-55菌株加入到加热杀菌后的豆乳中。将混合物置于37 ℃下培养24小时,以配制豆乳酸奶。
1.6 异黄酮含量的测定
培养24 h后,通过HPLC测定豆乳酸奶和未发酵豆乳中的各类异黄酮含量。异黄酮的定量方法如下:
首先,制备植物雌激素的原液,包括大豆苷元、染料木黄酮、雌马酚、5-羟基-雌马酚。将标准粉末溶解在5.0 mL DMSO中,并加入96%(体积分数,下同)乙醇制成10 mmol/L溶液。然后,使用96%乙醇对各原液进行稀释,获得不同浓度值的标准液,用于制作校准曲线。例如,大豆苷元的标准液包括0.5、0.25和0.16 mmol/L,染料木黄酮的标准液包括0.50、0.25和0.12 mmol/L。
HPLC分析使用Adsorbosphere C18柱直接连接到P PolarAdvantage II(4.6 mm×150 mm,3 μm)。分析样品的注入量为100 μL。溶出液是使用水和乙腈的混合物(A为乙腈,B为蒸馏水)作为流动相,流速为0.80 mL/min,进行40 min的分析。具体操作如下:在溶出液中添加20%的A,在16 min后维持稳定,然后在16~30 min内逐渐将溶出液中A的浓度提高至70%,并在稳定5 min后维持,直到分析结束,最后恢复至20% A的浓度。分析对象通过二极管阵列检测器检测,使用260 nm的波长来检测大豆苷元和染料木黄酮,205 nm检测雌马酚和5-羟基-雌马酚。计算待测样品和标准品物的峰面积或峰高比值,以及它们的浓度比值。利用这些比值和已知浓度,可以计算出待测样品的浓度。并将得到的大豆苷元、染料木黄酮、雌马酚、5-羟基-雌马酚总含量统计记录。苷元型异黄酮含量(mg/100 mL)=大豆苷元含量+染料木黄酮含量+雌马酚含量+5-羟基-雌马酚含量。
1.7 统计分析
使用CHROMELEON软件和Excel 2023进行数据采集和处理,使用Prism进行作图。并记录每次实验中测定的异黄酮含量数值数据,将其整理在表格中。随后,使用柱状图对数据进行可视化展示。并对其基因组进行分析,确定其相关基因。
2 结果与分析
2.1 嗜酸乳杆菌 L-55菌株在豆乳中的发酵条件选择
将接种了嗜酸乳杆菌 L-55菌株的豆乳分别置于28、31、34、37、40、42 ℃条件下培养24 h,测量其活率及豆乳pH值的变化,了解嗜酸乳杆菌的生长过程,pH变化值越大说明其酸度下降越多,发酵效果越好。结果如图4所示,37 ℃培养的嗜酸乳杆菌的活率最高,豆乳pH值变化最大。在温度过高或者过低的情况下均会影响菌株的生长。因此选择37 ℃作为较优培养条件。
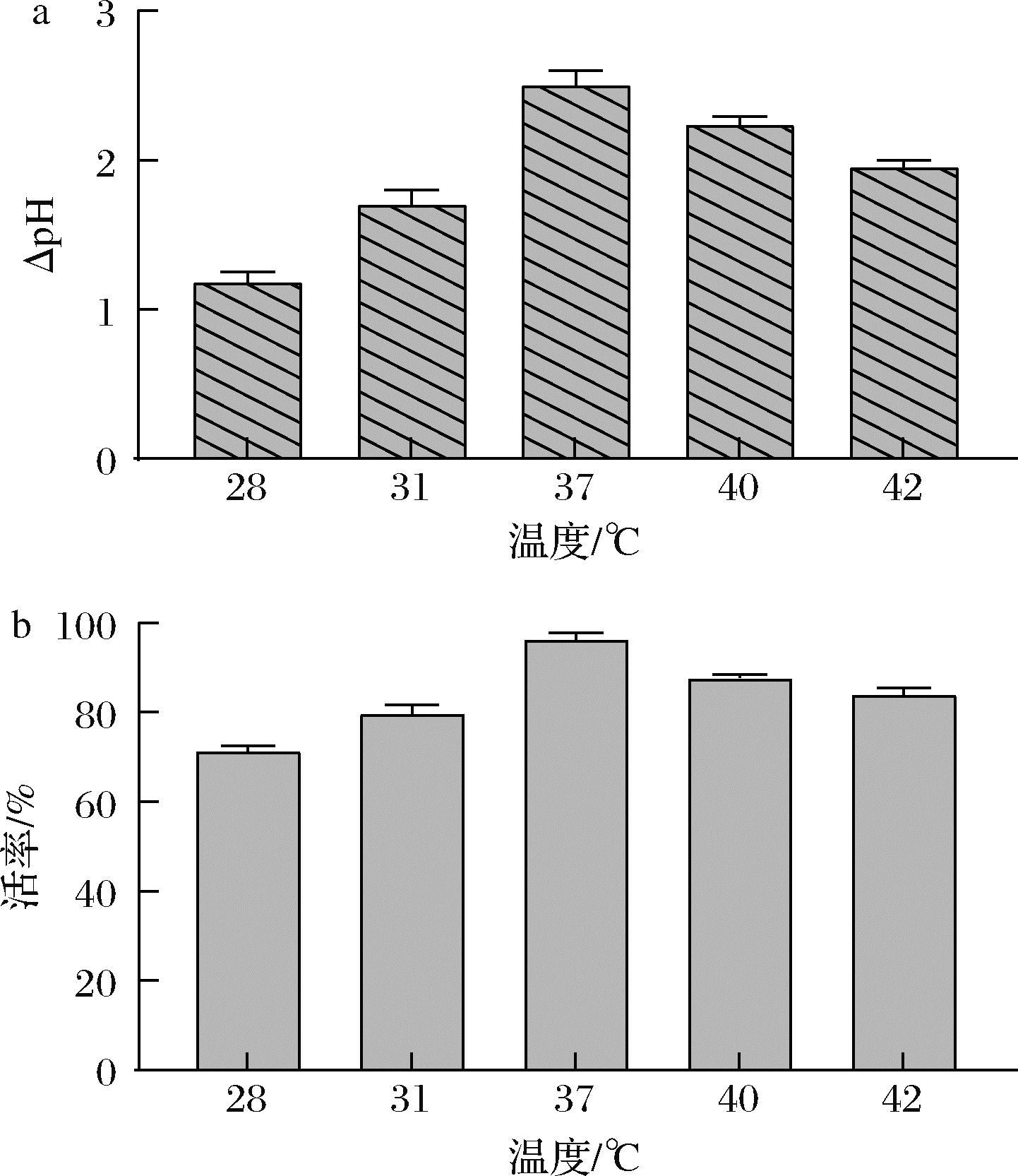
a-pH值;b-活率
图4 不同培养温度对嗜酸乳杆菌 L-55菌株的影响
Fig.4 Effects of different culture temperatures on Lactobacillus acidophilus L-55
将嗜酸乳杆菌 L-55菌株接种于豆乳中在37 ℃下培养48 h,每隔2 h测定菌种活率及pH值。如图5所示,培养时间在0~24 h期间,L-55菌株的活率随着培养时间的延长逐渐上升,pH值逐渐下降,在24 h后,pH值稳定在4.0左右,菌种活率稳定在98%左右基本保持不变,代表菌种生长进入稳定状态,因此选择24 h作为培养时间。
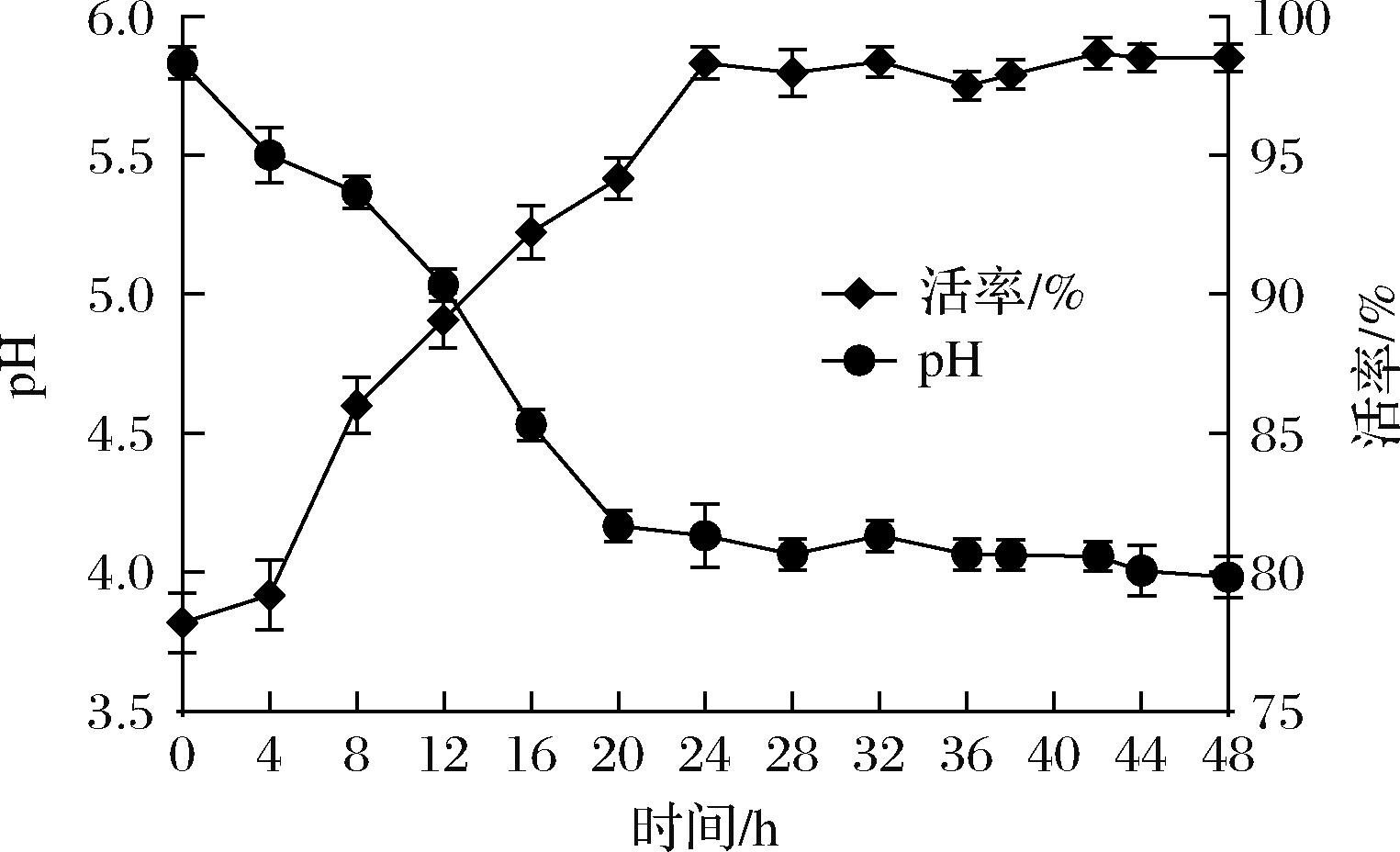
图5 不同培养时间对嗜酸乳杆菌 L-55菌株的影响
Fig.5 Effects of different culture time on Lactobacillus acidophilus L-55
以上分析可知,嗜酸乳杆菌L-55菌株在豆乳中的最适发酵条件为37 ℃、发酵24 h,并将此作为豆乳的发酵条件。
2.2 豆乳酸奶中的异黄酮含量
2.2.1 豆乳酸奶中大豆苷元的含量
如图6可知,未发酵豆乳中只检测到少量大豆苷元。在使用唾液链球菌嗜热亚种菌株和德氏乳杆菌保加利亚亚种菌株制备的豆乳酸奶中也只检测到少量大豆苷元的存在。然而,在接种了嗜酸乳杆菌L-55菌株的豆乳酸奶中检测到了0.74 mg/100 mL的大豆苷元存在,显著高于其他两种菌株产生的大豆苷元(P<0.05)。
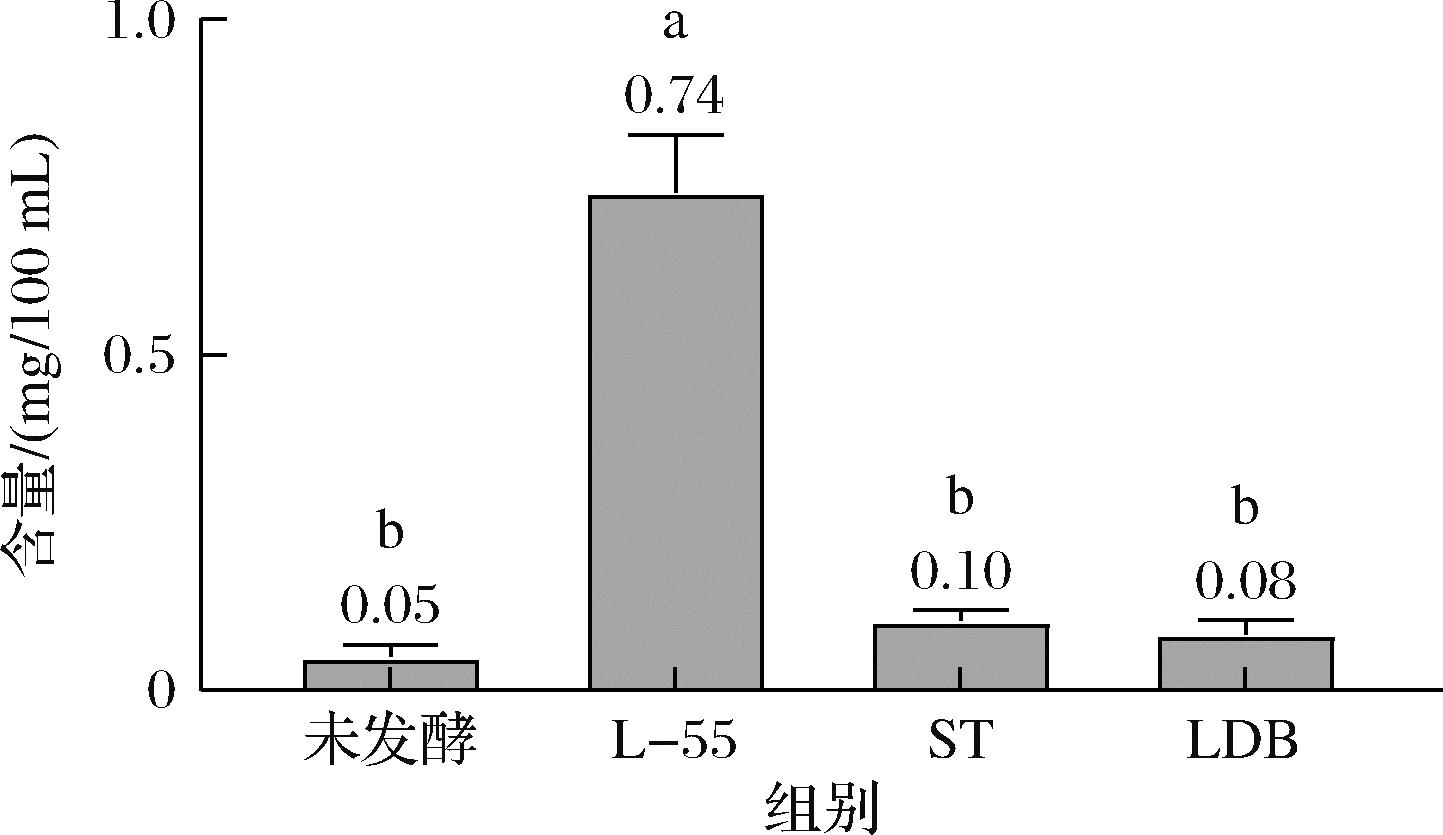
图6 HPLC测定的大豆苷元含量柱状图
Fig.6 Histogram of daidzein content determined by HPLC
注:ST:Streptococcus salivarius subsp.thermophilus;LDB:Lactobacillus delbrueckii subsp.bulgaricus;L-55:Lactobacillus acidophilus L-55; 小写字母不同表示不同数据具有显著性差异(P<0.05),下同。
2.2.2 豆乳酸奶中染料木黄酮的含量
如图7所示,未发酵豆乳中只检测到少量染料木黄酮。同样地,在使用唾液链球菌嗜热亚种菌株和德氏乳杆菌保加利亚亚种菌株制备的豆乳酸奶中也只检测到少量染料木黄酮的存在。然而,在接种了嗜酸乳杆菌L-55菌株的豆乳酸奶中检测到了2.35 mg/100 mL的染料木黄酮。
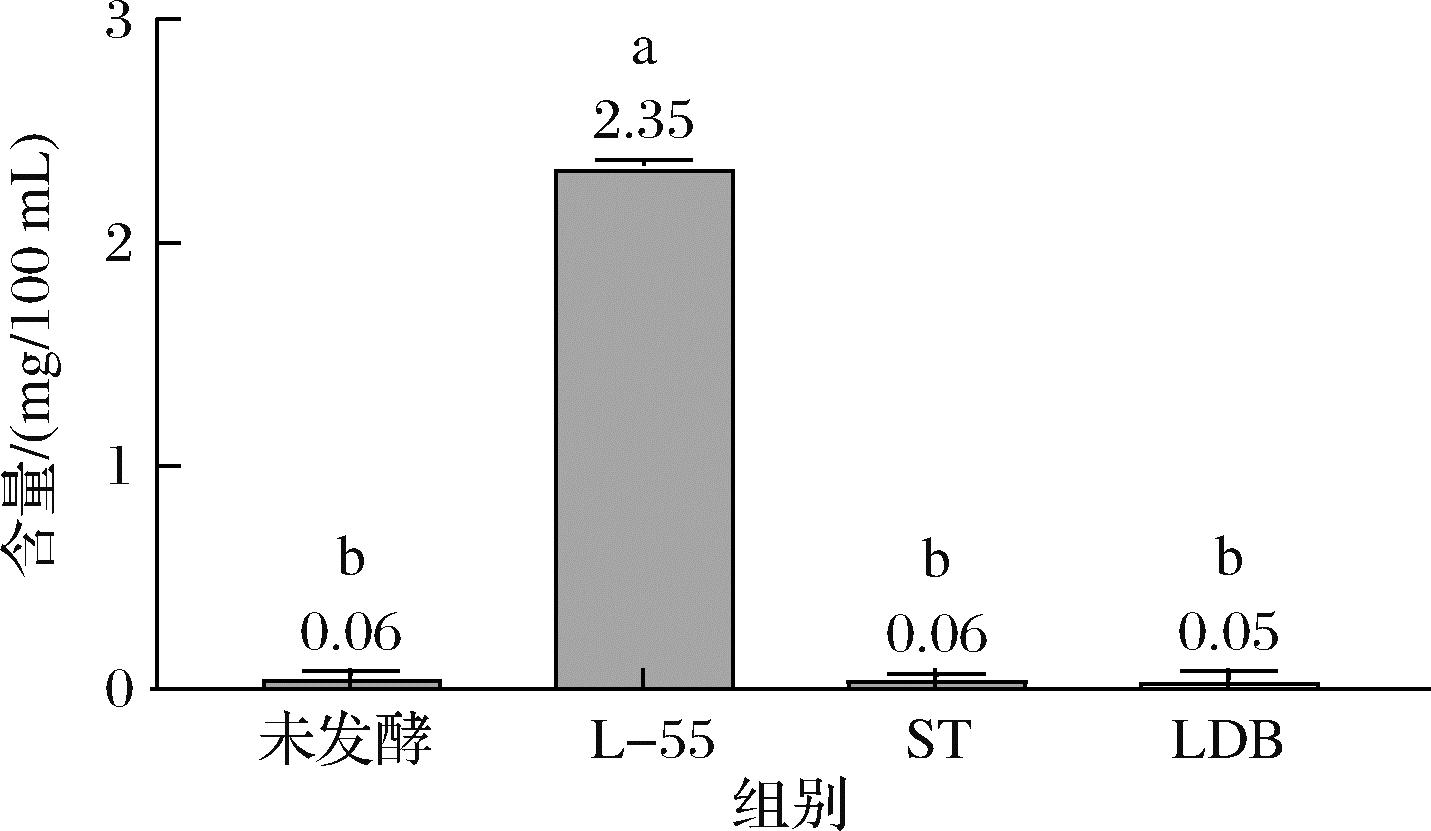
图7 HPLC测定的染料木黄酮含量柱状图
Fig.7 Histogram of genistein content determined by HPLC
2.2.3 豆乳酸奶中雌马酚和5-羟基-雌马酚的含量
如图8所示,未发酵豆乳中检测到的雌马酚和5-羟基-雌马酚很少量。同样地,在使用唾液链球菌嗜热亚种菌株和德氏乳杆菌保加利亚亚种菌株制备的豆乳酸奶中和接种了L-55菌株的豆乳酸奶中均未检测到大量的雌马酚和5-羟基-雌马酚的存在。这证明L-55菌株并不能将异黄酮转化为雌马酚和5-羟基-雌马酚,这表明雌马酚和5-羟基雌马酚不是L-55菌株发酵豆乳酸奶中苷元型异黄酮的主要存在形式。
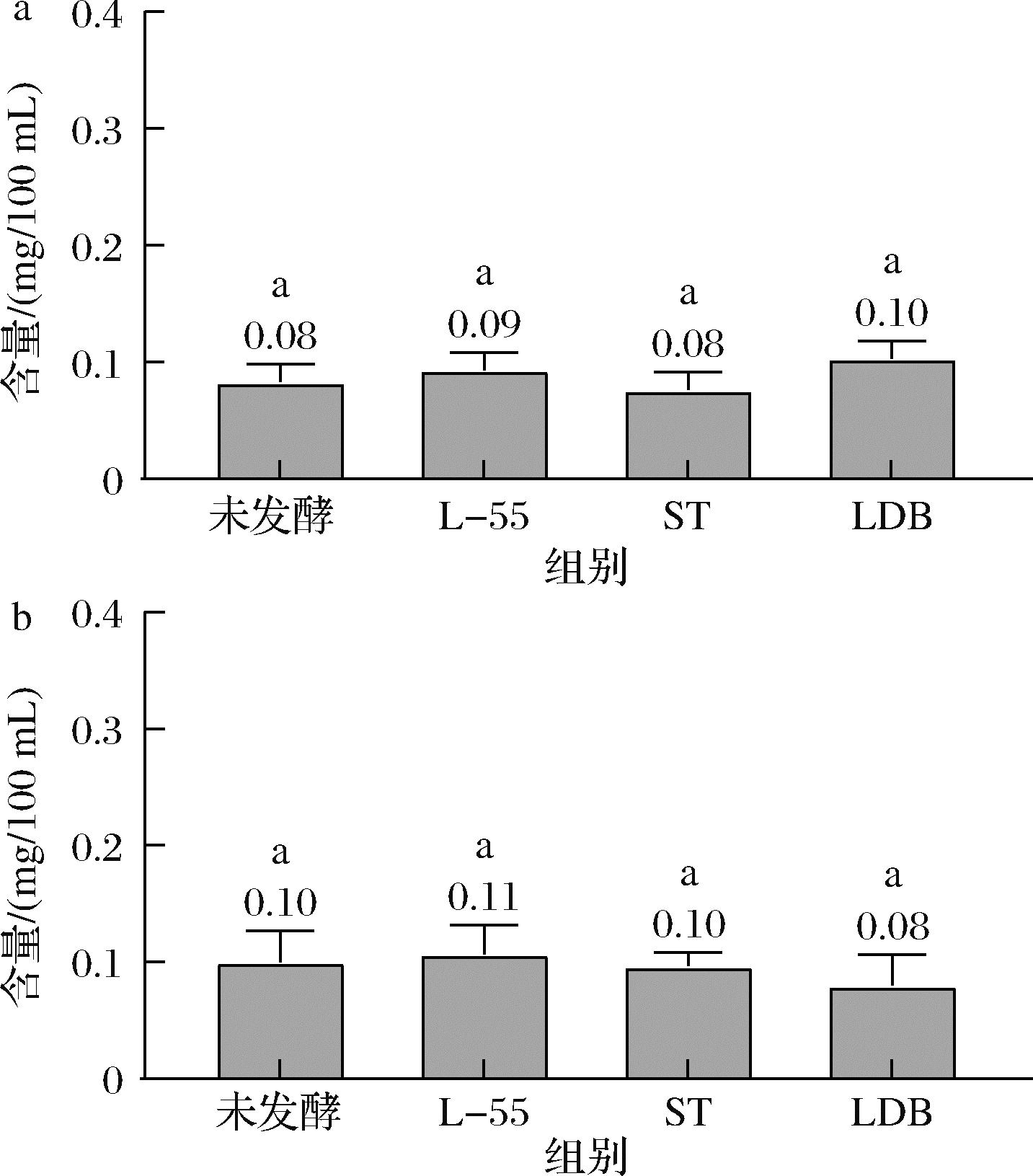
a-雌马酚含量;b-5-羟基-雌马酚含量
图8 HPLC测定的雌马酚和5-羟基-雌马酚含量柱状图
Fig.8 Histogram of equol and 5-OH-EQ content determined by HPLC
2.2.4 豆乳酸奶中苷元型异黄酮的含量
如图9所示,在接种了L-55菌株的豆乳酸奶中,检测到了大量的苷元型异黄酮,总含量为3.29 mg/100 mL,显著高于未发酵豆乳(P<0.05);接种其他两个菌株的豆乳酸奶中的苷元型异黄酮含量与未发酵豆乳无显著差异(P>0.05),均显著低于L-55菌株(P<0.05)。由此可见,L-55株具有将大豆异黄酮转化为苷元型异黄酮的功能,且在L-55菌株作用下产生的雌激素样物质主要是大豆苷元和染料木黄酮,其中染料木黄酮的含量显著高于大豆苷元含量(P<0.05)。由此可见,大豆苷元和染料木黄酮是豆乳酸奶中苷元型异黄酮的主要存在形式。
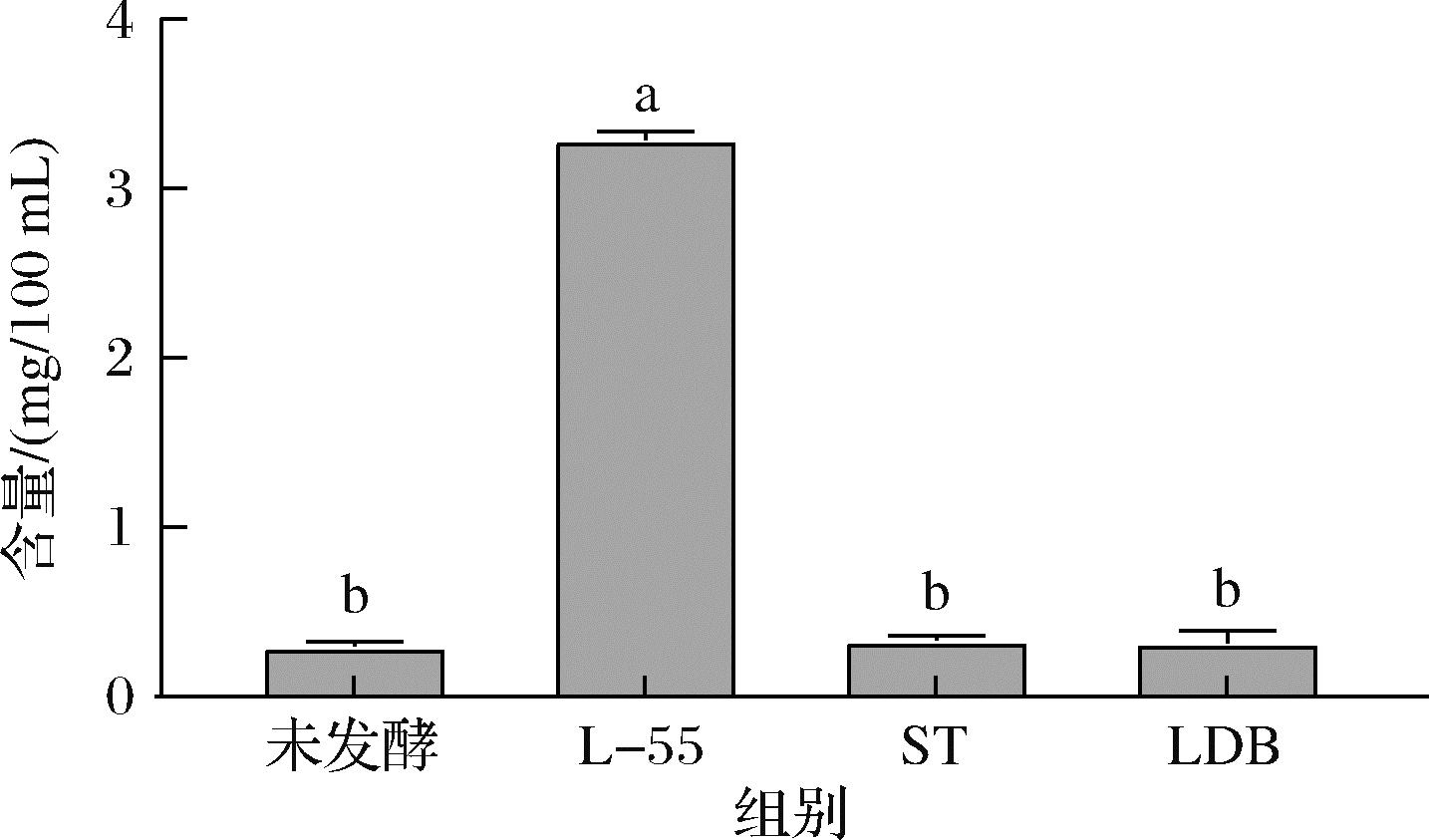
图9 HPLC测定的苷元型异黄酮含量柱状图
Fig.9 Histogram of isoflavone aglycone content determined by HPLC
2.3 嗜酸乳杆菌L-55的基因组信息
如表1所示,本研究分析了本实验室现有的嗜酸乳杆菌 L-55的基因组信息,并对比了另3个完整的嗜酸乳杆菌菌株的基因组信息[34]。通过基因组信息可以得知,L-55菌株与嗜酸乳杆菌菌种的另3种菌株相似。这4个菌株的序列对比结果如图10所示,嗜酸乳杆菌 NCFM与嗜酸乳杆菌 L-55的相似度高达99%,另2个菌株也在93%。为了分析乳杆菌菌种的亲缘关系,通过NCBI选取了同源性较高的22种乳杆菌构建了系统发育树,结果如图11所示,L-55菌株与另3种菌株亲缘相近,功能相似。
表1 嗜酸乳杆菌 L-55的基因组信息和有完整长度 报告的3个嗜酸乳杆菌菌株的基因的比较
Table 1 Comparison of genomic information for Lactobacillus acidophilus L-55 and genes for three strains of Lactobacillus acidophilus with full-length reports
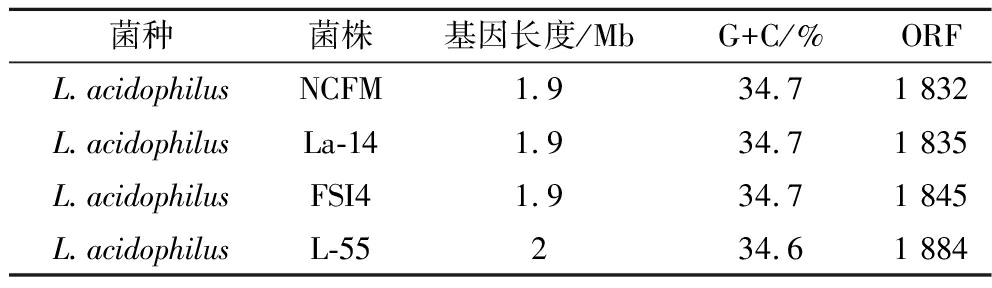
菌种菌株基因长度/MbG+C/%ORFL.acidophilusNCFM1.934.71 832L.acidophilusLa-141.934.71 835L.acidophilusFSI41.934.71 845L.acidophilusL-55234.61 884

图10 嗜酸乳杆菌 L-55与其他嗜酸乳杆菌序列对比
Fig.10 Sequence comparison between Lactobacillus acidophilus L-555 and other Lactobacillus acidophilus
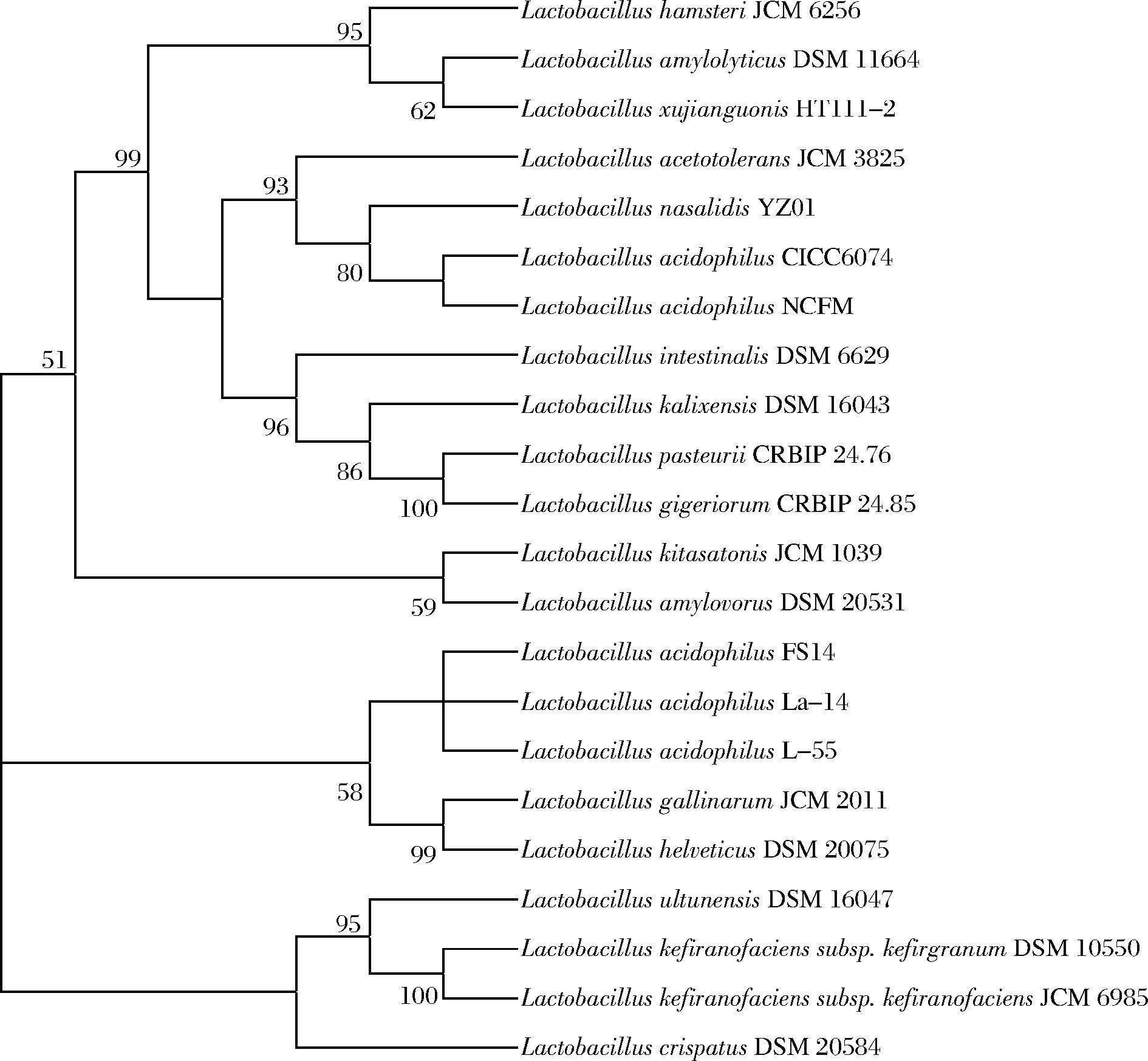
图11 乳杆菌系统进化树
Fig.11 Phylogenetic tree of Lactobacillus
2.4 嗜酸乳杆菌L-55菌株转化为雌激素样物质的相关基因群
根据之前的研究发现,DZNR、DHDR、DDRC和THDR是参与从大豆苷元合成雌马酚的相关基因[19-20]。而从大豆黄素苷合成大豆苷元、从染料木素苷合成染料木黄酮的相关基因编码的酶均为β-葡萄糖苷酶[19]。
通过分析已有的L-55菌株的基因组序列,使用blast进行序列比对,搜索了与将糖苷型异黄酮转化为大豆苷元、染料木黄酮、雌马酚和5-羟基-雌马酚相关的基因。选取开放阅读框并进行了比较,以确认是否存在这些相关基因。比较结果显示,在L-55菌株的基因组中,检索到具有从大豆黄素苷合成大豆苷元、从染料木素苷合成染料木黄酮的β-葡萄糖苷酶的相关基因,但不存在将糖苷型异黄酮转化为雌马酚和5-羟基-雌马酚的相关基因,这一结果与在该菌株发酵的豆乳酸奶中含有大量的大豆苷元和染料木黄酮含量和未检测到大量雌马酚和5-羟基-雌马酚的结果一致。因此,经嗜酸乳杆菌 L-55菌株发酵的豆乳可以得到具有雌激素作用的大豆苷元、染料木黄酮得到证实,发酵后的豆乳比未发酵的具有更高的营养价值。同样的,利用唾液链球菌嗜热亚种菌株、德氏乳杆菌保加利亚亚种菌株的基因组信息(图12、13),通过blast进行序列比对,发现这2种菌株中均不存在将糖苷型转化为与大豆苷元、染料木黄酮、雌马酚和5-羟基-雌马酚的相关基因,这与未在这2种菌株发酵的豆乳中检测到大量苷元型异黄酮的结果一致。

图12 德氏乳杆菌保加利亚亚种菌株的基因组信息
Fig.12 Genomic information of Lactobacillus delbrueckii subsp.bulgaricus
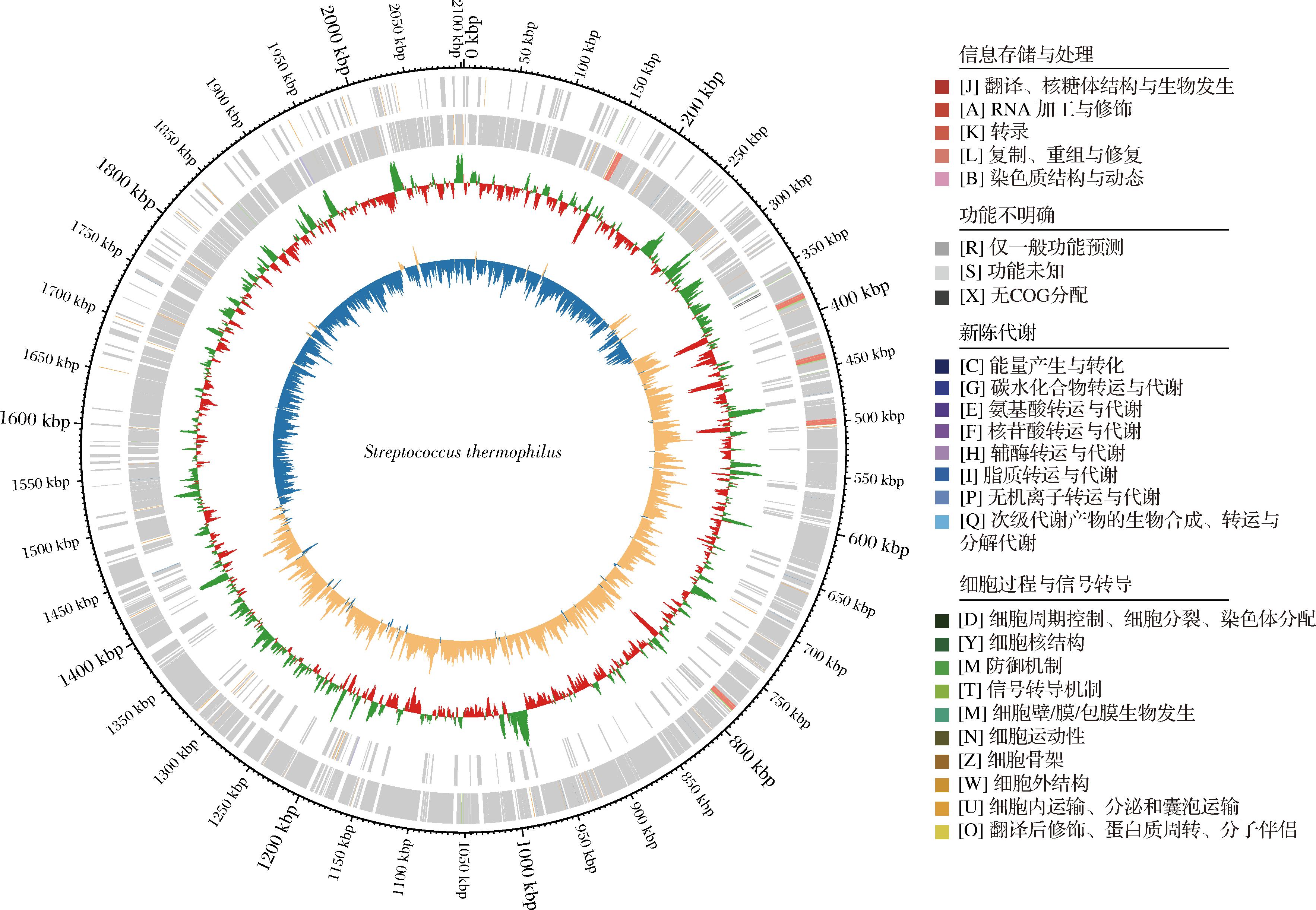
图13 唾液链球菌嗜热亚种菌株的基因组信息
Fig.13 Genomic information of Streptococcus salivarius subsp. thermophilus
3 结论
通过这项研究,发现在37 ℃,24 h的条件下,在L-55菌株发酵的豆乳酸奶中未大量检测到同样具有雌激素作用的雌马酚和5-羟基-雌马酚,这与在L-55菌株基因组中未发现其相关基因的结果一致。同时由于缺乏这些基因,L-55菌株发酵的豆乳酸奶中积累了具有雌激素样作用的染料木黄酮和大豆苷元。因此,与普通市售牛乳酸奶相比,经过L-55菌株发酵的豆乳酸奶中含有更多雌激素样物质。由此认为L-55菌株具有将糖苷型大豆异黄酮转化为雌激素样物质的潜力,也说明与普通牛乳酸奶相比豆乳酸奶能够提供更丰富的营养物质。与豆乳酸奶相关的新发现的产生也为未来的研究提供了期待,进一步提高雌激素样物质的含量以及豆乳相关健康食品的开发将成为后续研究的重点。
[1] RASTALL R A.Bacteria in the gut:Friends and foes and how to alter the balance[J].The Journal of Nutrition, 2004, 134(8):2022S-2026S.
[2] SUNADA Y, NAKAMURA S, KAMEI C.Effect of Lactobacillus acidophilus strain L-55 on the development of atopic dermatitis-like skin lesions in NC/Nga mice[J].International Immunopharmacology, 2008, 8(13-14):1761-1766.[LinkOut]
[3] MEYDANI S N, HA W K.Immunologic effects of yogurt[J].The American Journal of Clinical Nutrition, 2000, 71(4):861-872.
[4] RUIZ RODR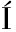 GUEZ L G, MOHAMED F, BLECKWEDEL J, et al.Diversity and functional properties of lactic acid bacteria isolated from wild fruits and flowers present in northern Argentina[J].Frontiers in Microbiology, 2019, 10:1091.
GUEZ L G, MOHAMED F, BLECKWEDEL J, et al.Diversity and functional properties of lactic acid bacteria isolated from wild fruits and flowers present in northern Argentina[J].Frontiers in Microbiology, 2019, 10:1091.
[5] SUNADA Y, NAKAMURA S, KAMEI C.Effects of Lactobacillus acidophilus strain L-55 on experimental allergic rhinitis in BALB/c mice[J].Biological &Pharmaceutical Bulletin, 2007, 30(11):2163-2166.
[6] KIMURA G, AKAGI H, OKADA C, et al.Clinical effects of Lactobacillus acidophilus strain L-55-contained yogurt on symptoms of Japanese cedar pollen allergy[J].Arerugi =[Allergy], 2012, 61(5):628-641.
[7] HO D T, HATABU T, SUNADA Y, et al.Oral administration of the probiotic bacterium Lactobacillus acidophilus strain L-55 modulates the immunological parameters of the laying hen inoculated with a Newcastle disease virus-based live attenuated vaccine[J].Bioscience of Microbiota, Food and Health, 2020, 39(3):117-122.
[8] PHAM H H S, FUJII Y, ARAKAWA K, et al.Differential effects of orally administered Lactobacillus acidophilus L-55 on the gene expression of cytokines and master immune switches in the ileum and spleen of laying hen with an attenuated Newcastle disease virus vaccine[J].Bioscience of Microbiota, Food and Health, 2022, 41(1):12-19.
[9] SUNADA Y.Effects of Lactobacillus acidophilus strain L-55 on viral infection[J].Milk Science, 2013, 62(3):139-142.
[10] KAUFMAN P B, DUKE J A, BRIELMANN H, et al.A comparative survey of leguminous plants as sources of the isoflavones, genistein and daidzein:Implications for human nutrition and health[J].Journal of Alternative and Complementary Medicine, 1997, 3(1):7-12.
[11] MURPHY P A, BARUA K, HAUCK C C.Solvent extraction selection in the determination of isoflavones in soy foods[J].Journal of Chromatography B, 2002, 777(1-2):129-138.
[12] WANG H, MURPHY P A.Isoflavone content in commercial soybean foods[J].Journal of Agricultural and Food Chemistry, 1994, 42(8):1666-1673.
[13] OSENI T, PATEL R, PYLE J, et al.Selective estrogen receptor modulators and phytoestrogens[J].Planta Medica, 2008, 74(13):1656-1665.
[14] SETCHELL K D R, BROWN N M, LYDEKING-OLSEN E.The clinical importance of the metabolite equol—a clue to the effectiveness of soy and its isoflavones[J].The Journal of Nutrition, 2002, 132(12):3577-3584.
[15] 赵晓佳, 李易聪, 王秀伶.大豆异黄酮微生物转化研究进展[J].微生物学报, 2020, 60(2):211-226.ZHAO X J, LI Y C, WANG X L.Progress in microbial conversion of soy isoflavones[J].Acta Microbiologica Sinica, 2020, 60(2):211-226.
[16] RUIZ DE LA BASTIDA A, PEIROTÉN  , LANGA S, et al.Heterologous production of equol by lactic acid bacteria strains in culture medium and food[J].International Journal of Food Microbiology, 2021, 360:109328.
, LANGA S, et al.Heterologous production of equol by lactic acid bacteria strains in culture medium and food[J].International Journal of Food Microbiology, 2021, 360:109328.
[17] PEI X, ZHAO J Q, CAI P L, et al.Heterologous expression of a GH3 β-glucosidase from Neurospora crassa in Pichia pastoris with high purity and its application in the hydrolysis of soybean isoflavone glycosides[J].Protein Expression and Purification, 2016, 119:75-84.
[18] WANG X L, HUR H G, LEE J H, et al.Enantioselective synthesis of S-equol from dihydrodaidzein by a newly isolated anaerobic human intestinal bacterium[J].Applied and Environmental Microbiology, 2005, 71(1):214-219.
[19] SHIMADA Y, TAKAHASHI M, MIYAZAWA N, et al.Identification of a novel dihydrodaidzein racemase essential for biosynthesis of equol from daidzein in Lactococcus sp.strain 20-92[J].Applied and Environmental Microbiology, 2012, 78(14):4902-4907.
[20] TOH H, OSHIMA K, SUZUKI T, et al.Complete genome sequence of the equol-producing bacterium Adlercreutzia equolifaciens DSM 19450T[J].Genome Announcements, 2013, 1(5):e00742-13.
[21] MISSELWITZ B, BUTTER M, VERBEKE K, et al.Update on lactose malabsorption and intolerance:Pathogenesis, diagnosis and clinical management[J].Gut, 2019, 68(11):2080-2091.
[22] HIDALGO-FUENTES B, DE JES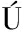 S-JOSÉ E, CABRERA-HIDALGO A J, et al.Plant-based fermented beverages:Nutritional composition, sensory properties, and health benefits[J].Foods, 2024, 13(6):844.
S-JOSÉ E, CABRERA-HIDALGO A J, et al.Plant-based fermented beverages:Nutritional composition, sensory properties, and health benefits[J].Foods, 2024, 13(6):844.
[23] SAVAIANO D A, HUTKINS R W.Yogurt, cultured fermented milk, and health:A systematic review[J].Nutrition Reviews, 2021, 79(5):599-614.
[24] 陈玉胜, 陈全战.一种功能性酸奶的研制及其抗氧化活性[J].江苏农业科学, 2020, 48(14):221-226.CHEN Y S, CHEN Q Z.Development of a functional yogurt and its antioxidant activity[J].Jiangsu Agricultural Sciences, 2020, 48(14):221-226.
[25] AYDAR E F, TUTUNCU S, OZCELIK B.Plant-based milk substitutes:Bioactive compounds, conventional and novel processes, bioavailability studies, and health effects[J].Journal of Functional Foods, 2020, 70:103975.
[26] DHAKAL D, YOUNAS T, BHUSAL R P, et al.Design rules of plant-based yoghurt-mimic:Formulation, functionality, sensory profile and nutritional value[J].Food Hydrocolloids, 2023, 142:108786.
[27] KANO M, TAKAYANAGI T, HARADA K, et al.Bioavailability of isoflavones after ingestion of soy beverages in healthy adults 1[J].The Journal of Nutrition, 2006, 136(9):2291-2296.
[28] GUO Y Y, ZHAO L C, FANG X, et al.Isolation and identification of a human intestinal bacterium capable of daidzein conversion[J].FEMS Microbiology Letters, 2021, 368(8):fnab046.
[29] PENG Q W, LI Y Y, SHANG J, et al.Effects of genistein on common kidney diseases[J].Nutrients, 2022, 14(18):3768.
[30] BOECK T, SAHIN A W, ZANNINI E, et al.Nutritional properties and health aspects of pulses and their use in plant-based yogurt alternatives[J].Comprehensive Reviews in Food Science and Food Safety, 2021, 20(4):3858-3880.
[31] SILVA A R A, SILVA M M N, RIBEIRO B D.Health issues and technological aspects of plant-based alternative milk[J].Food Research International, 2020, 131:108972.
[32] ISLAM N, SHAFIEE M, VATANPARAST H.Trends in the consumption of conventional dairy milk and plant-based beverages and their contribution to nutrient intake among Canadians[J].Journal of Human Nutrition and Dietetics, 2021, 34(6):1022-1034.
[33] HARPER A R, DOBSON R C J, MORRIS V K, et al.Fermentation of plant-based dairy alternatives by lactic acid bacteria[J].Microbial Biotechnology, 2022, 15(5):1404-1421.
[34] FUJII Y, TOH H, MATSUBARA T, et al.Draft genome sequence of probiotic Lactobacillus acidophilus strain L-55 isolated from a healthy human gut[J].Genome Announcements, 2016, 4(6):e01357-16.