近年来,生物质基膜作为“绿色包装”材料替代难以降解的塑料包装材料成为食品包装领域的研究热点[1]。羧甲基壳聚糖(carboxymethyl chitosan, CMC)来源广泛、价格低廉,主要由水产加工副产物制备而成,具有无毒、生物相容性好和成膜稳定性高等优点,是制备生物质基膜的良好原料[2]。然而,CMC膜耐水性较差[水溶性(water solubility, WS)和溶胀率(swelling ratio, SR)高],限制了其在高水分食品和高湿环境中的应用[3]。
改善生物质基膜耐水性的方法主要有物理法、化学法、复合法等,其中化学法包括交联剂法、酶法和美拉德反应(maillard reaction, MR)法等[4]。MR是氨基化合物(胺、氨基酸、肽和蛋白质)和羰基化合物(糖类)发生的反应,不仅可以提高食品的风味性,同时MR产物还具有较强的抗氧化和抗菌活性,可应用于食品安全控制和功能食品开发等[5-6]。研究表明,MR可改善生物大分子的理化性能,在生物大分子改性方面具有较大的应用潜力[7-8]。由于CMC分子中含有氨基,理论上可与还原糖中的羰基发生MR,从而对CMC膜进行改性。
MR通常分为初期、中期和末期3个阶段(图1),产物复杂多样,影响因素较多,反应温度、初始pH值、还原糖浓度等对MR过程影响极大;此外,随着MR反应程度的加深,产物的颜色加深、分子流动性下降,进而影响膜的性能[9-10]。因此探究MR条件对CMC膜耐水性的影响是CMC膜改性的重要环节。

图1 CMC与木糖的MR简意图
Fig.1 The schematic diagram of MR between CMC and xylose
目前,基于小分子还原糖改善CMC膜性能的系统性研究鲜见报道。本文以MR为改性手段,以耐水性为主要指标,分析MR条件对CMC改性膜耐水性的影响;通过对不同MR程度CMC改性膜性能与结构的表征,解析MR程度与CMC改性膜性能的关系。本研究将为CMC改性膜在高水分含量食品包装上的应用提供技术支撑。
1 材料与方法
1.1 主要试剂
CMC、葡萄糖、乳糖、麦芽糖、半乳糖、木糖、果糖、D-阿拉伯糖,北京索莱宝科技有限公司;甘油、NaOH、HCl、乙醇、磷酸盐缓冲液、铁氰化钾、三氯乙酸、氯化铁,国药集团化学试剂有限公司;1,1-二苯基-2-三硝基苯肼(DPPH),美国Sigma-Aldrich公司;LB营养琼脂培养基,青岛海博生物技术有限公司;大肠杆菌(ATCC25922),中国工业微生物菌种保藏中心。
1.2 主要仪器
PB-21台式精密酸度计、BT 125D电子天平,赛多利斯科学仪器(北京)有限公司;YS6002台式色彩雾度仪,深圳市三恩时科技有限公司;GZX-9140MBE鼓风干燥箱、YXQ-LS-75立式压力蒸汽灭菌器、BSC-150恒温恒湿箱,上海博讯实业有限公司医疗设备厂;ZQ-990LA电动拉力试验机,东莞市智取精密仪器有限公司;QYC 211恒温振荡培养箱,上海福玛实验设备有限公司;SW-CJ-2F洁净工作台,苏净集团安泰公司;SYA-7045 JY测厚规,德清盛泰芯电子科技有限公司;MiniFlex 600 X-射线衍射(X-ray diffraction, XRD)仪,日本Rigaku公司;Iraffinity-1s傅里叶红外光谱(Fourier transform infrared spectroscopy, FTIR)仪,日本Shimadzu公司;Sigma 300扫描电子显微镜(scanning electron microscope, SEM),德国ZEISS公司。
1.3 实验方法
1.3.1 CMC膜的制备
取4.0 g CMC溶于100 mL蒸馏水中,加入1 mL甘油,用NaOH溶液(7.5 mol/L)和HCl溶液(2 mol/L)调节溶液pH值至10.0,室温下搅拌30 min,静置30 min,得CMC成膜液。取20 mL成膜液倒入10 cm×10 cm的模具中,25 ℃干燥成膜48 h,揭膜后置于25 ℃和相对湿度50%的恒温恒湿箱中平衡24 h,制得CMC膜,保存于4 ℃冰箱中待测。
1.3.2 CMC改性膜的制备
按照1.3.1的方法,CMC成膜液中加入设定量的还原糖,调节膜液初始pH值,揭膜后置于鼓风干燥箱中,在设定温度下反应一段时间,反应结束后于25 ℃和相对湿度50%的恒温恒湿箱中平衡24 h,制得CMC改性膜,保存于4 ℃冰箱中待测。
CMC改性膜的MR反应条件设置如下:(a)还原糖种类包括葡萄糖、乳糖、麦芽糖、半乳糖、木糖、果糖和D-阿拉伯糖,固定CMC/还原糖质量比8∶1、膜液初始pH值10.0、加热温度60 ℃、加热时间1 h;(b)CMC/木糖质量比为1∶0、32∶1、16∶1、8∶1、4∶1、2∶1和1∶1,固定膜液初始pH值10.0、加热温度60 ℃、加热时间1 h;(c)膜液初始pH值为8.0、9.0、10.0、11.0和12.0,固定CMC/木糖质量比4∶1、加热温度60 ℃、加热时间1 h;(d)固定CMC/木糖质量比4∶1、膜液初始pH值10.0,加热温度为50、60、70和80 ℃,加热时间为0、1、2、3、6、9、15和24 h。
1.4 测定指标
1.4.1 WS
参照KCHAOU等[7]的方法,取质量约为0.1 g的样品,置于称量瓶中,105 ℃烘箱中烘至恒定质量(m1,g),将膜置于30 mL蒸馏水中,25 ℃静置24 h后取出,105 ℃烘箱中烘至恒定质量(m2,g),WS的计算如公式(1)所示:
(1)
1.4.2 SR
参照RUI等[8]的方法,取质量约为0.1 g的样品,称重(m3,g),置于30 mL蒸馏水中,25 ℃静置24 h后取出,滤纸吸去表面水分,称重(m4,g),SR的计算如公式(2)所示:
(2)
1.4.3 色差及透光性
采用台式色彩雾度仪测定膜的颜色,并扫描400~700 nm范围内的吸光值图谱。
1.4.4 机械性能
采用电动拉力试验机测试膜的拉伸强度(tensile strength, TS)和断裂伸长率(elongation at break, EAB)。裁取20 mm×80 mm的膜,设定初始夹距为40 mm,拉伸速度为50 mm/min。测试前使用测厚规测定膜随机5个位置的厚度。TS、EAB的计算如公式(3)和公式(4)所示:
(3)
式中:F,膜断裂时承受的最大张力,N;A,试验前膜的横截面积,mm2。
(4)
式中:L0,膜测试前的长度,mm;L,膜断裂时的长度,mm。
1.4.5 抗氧化活性
参照KCHAOU等[7]的方法测定膜的DPPH自由基清除率和还原力。DPPH自由基清除率:10 mg膜浸入500 μL蒸馏水中,加入375 μL乙醇和125 μL DPPH溶液(0.02%,溶于乙醇),25 ℃避光放置24 h,测517 nm处吸光值。DPPH自由基清除率的计算如公式(5)所示:
DPPH自由基清除率![]()
(5)
式中:AC,无膜DPPH液吸光度;AB,加膜不加DPPH液吸光度;AS,加膜加DPPH液吸光度。
还原力:10 mg膜浸入0.5 mL蒸馏水、1.25 mL磷酸盐缓冲液(0.2 mol/L,pH 6.6)和1.25 mL铁氰化钾(1%,质量分数)混合溶液中,50 ℃反应3 h,加入0.5 mL三氯乙酸溶液(10%,质量分数),10 000×g离心10 min,取1.25 mL上清液与1.25 mL蒸馏水、0.25 mL氯化铁(0.1%,质量分数)混合,25 ℃反应10 min,测700 nm处吸光值。
1.4.6 抗菌活性
参考陈晓涵等[11]的方法,截取直径10 mm的圆形膜,在超净工作台中两面各经紫外线照射30 min。取100 μL大肠杆菌溶液(106 CFU/mL)涂于LB营养琼脂平板,将膜贴于平板上,37 ℃培养24 h,测量抑菌圈的直径(mm)。
1.4.7 SEM
采用SEM观察4 000放大倍数下的膜表面和截面形貌, 截面采用液氮脆断并进行喷金处理。
1.4.8 FTIR
膜样品经干燥处理后加入KBr,研磨混匀,压片,以KBr作为空白对照,采用FTIR仪在波数范围4 000~600 cm-1内扫描32次。
1.4.9 XRD
采用XRD仪分析样品,扫描衍射角范围为5°~60°,扫描速率为2 °/min。
1.5 统计分析
结果以“平均值±标准偏差”的形式表示;采用SPSS 19.0软件进行单因素方差分析(ANOVA)和Tukey显著性检验,以P<0.05为具有统计学意义上的显著差异。
2 结果与讨论
2.1 MR反应条件对CMC改性膜耐水性的影响
2.1.1 还原糖种类
如图2所示,添加不同还原糖后,CMC改性膜在420 nm处的吸光值(A420)均有不同程度的增加,表明不同还原糖与CMC之间皆发生了MR。CMC膜的WS为100%,除乳糖外,添加还原糖后改性膜WS显著下降(P<0.05),其中添加木糖后改性膜的WS最低;CMC膜的SR为160.8%,添加还原糖后改性膜SR均显著下降(P<0.05)。推测可能的原因是添加还原糖后,CMC的氨基与还原糖的羰基在加热的条件下发生MR,一方面CMC与还原糖结合后形成更为致密的立体网状结构,另一方面CMC与还原糖发生MR生成水不溶性物质,最终导致膜的WS降低[12]。研究表明,MR中不同还原糖的反应活性不同,木糖和阿拉伯糖等五碳糖的碳链更短,反应活性更强[13]。基于与CMC的反应活性,本研究选择木糖作为CMC膜MR改性的还原糖进行后续研究。
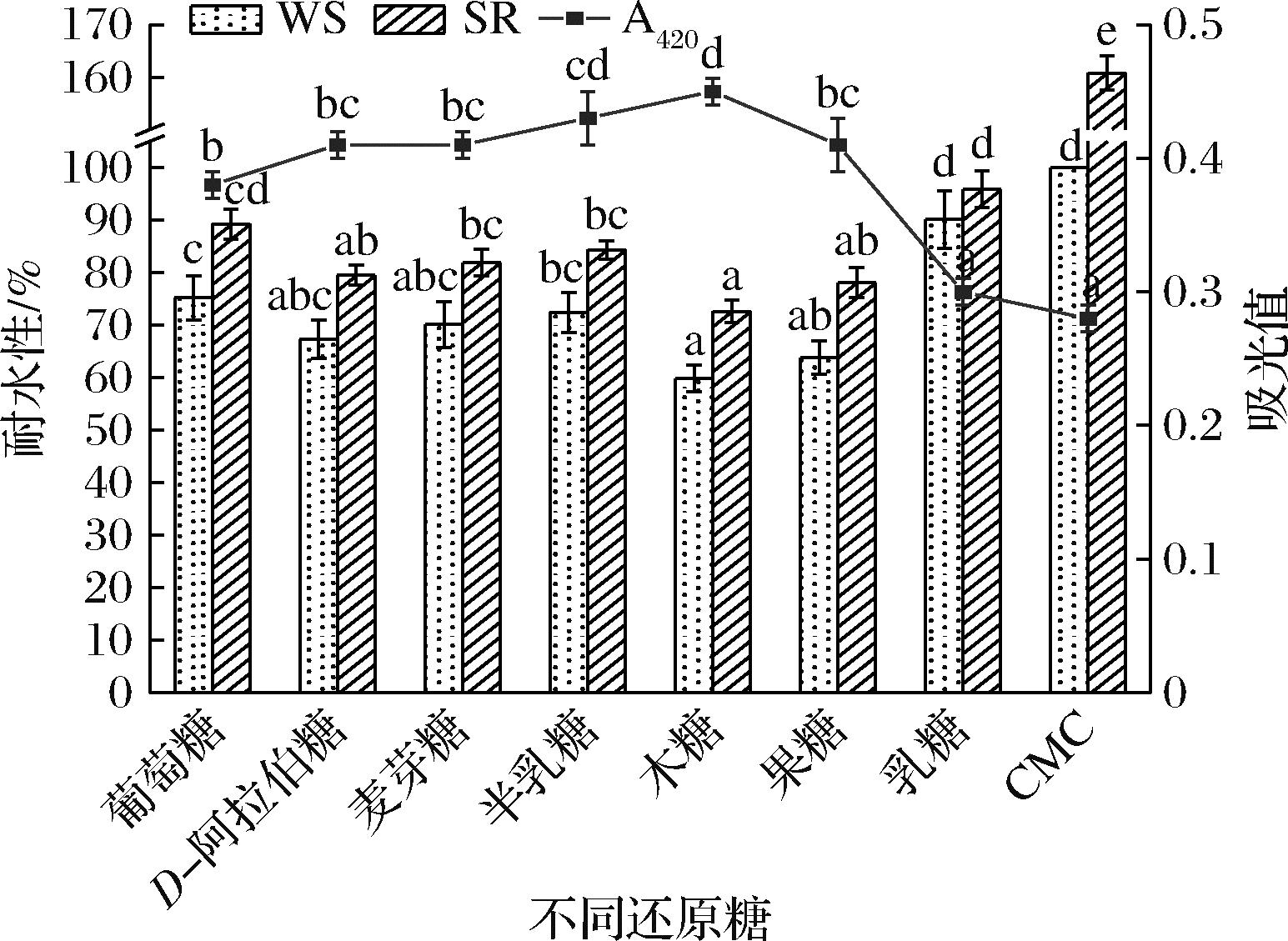
图2 还原糖种类对 CMC改性膜耐水性和A420的影响
Fig.2 Effects of reducing sugar types on water resistance properties and A420 of modified CMC films
注:同一指标不同小写字母表示差异显著(P<0.05)(下同)。
2.1.2 CMC/木糖比例和膜液初始pH值
如图3-a所示,随着木糖占比的增加,CMC改性膜的A420增大,表明MR程度随木糖占比升高而加深。改性膜WS和SR随木糖占比增加呈先下降后上升的趋势,当CMC/木糖比例为4∶1时,改性膜WS最低。当CMC/木糖比例在1∶0~4∶1范围内,随着木糖占比的增加,更多的WS CMC与木糖反应,CMC分子之间交联度增大,膜结构更为致密,WS和SR降低;当木糖占比过高(CMC/木糖比例<4∶1),反应体系中木糖相对过剩,木糖本身WS强,且过量的木糖可能破坏膜结构的紧密程度,进而导致膜的WS和SR升高[14]。

a-CMC/木糖比例;b-膜液初始pH值
图3 CMC/木糖比例和膜液初始pH值对CMC改性膜 耐水性和A420的影响
Fig.3 Effects of xylose ratio and initial pH on water resistance properties and A420 of modified CMC films
图3-b为改性膜耐水性和A420随膜液初始pH值的变化情况,随着初始pH值的升高,A420增大,MR反应程度加深,然而膜的WS和SR无明显变化。研究表明,MR在碱性条件下较易发生,随着反应起始pH值的升高,MR反应程度加深,与本研究结果一致;然而在强碱性条件下,可能增加CMC分子之间静电排斥作用,因破坏膜致密性而使膜的WS和SR升高[15],综合效应导致膜液初始pH值对膜的耐水性无显著影响。
2.1.3 反应温度与反应时间
如图4所示,随着反应温度的升高和反应时间的延长,A420呈上升趋势,表明改性膜的MR程度随反应温度的升高和反应时间的延长而加深,这与AFFES等[16]的研究结果一致,反应温度和反应时间对MR程度影响显著。当反应时间达到9 h(70 ℃和80 ℃)或15 h(50 ℃和60 ℃)后,延长反应时间对改性膜的A420无显著影响。
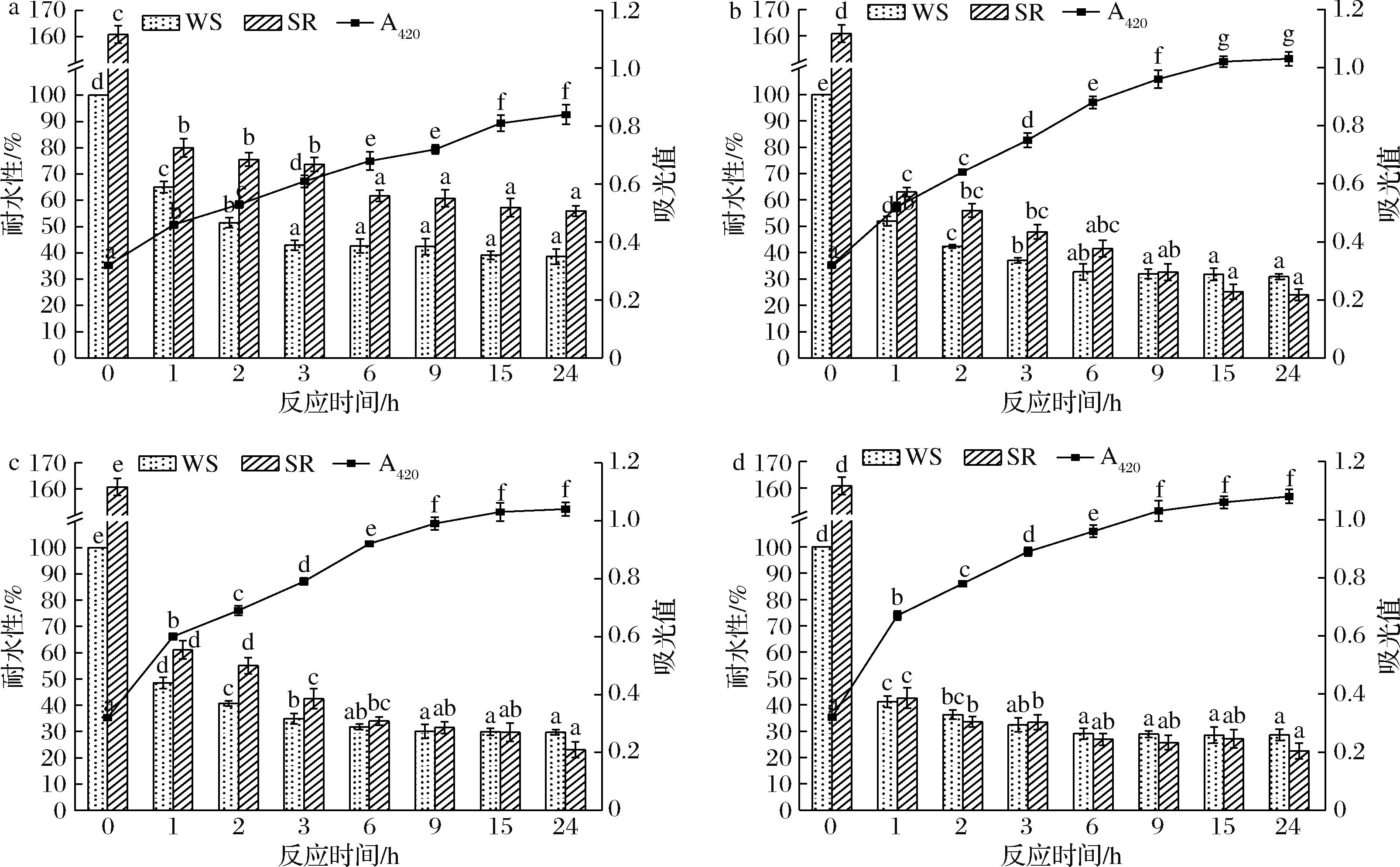
a-50 ℃;b-60 ℃;c-70 ℃;d-80 ℃
图4 反应温度和反应时间对CMC改性膜耐水性和A420的影响
Fig.4 Changes in water resistance properties and A420 of modified CMC films with different reaction temperatures over time
在反应时间6 h内,随着反应温度的升高和反应时间的延长,改性膜的WS和SR下降(图4)。当延长反应时间至一定阶段(6 h后),此时随着反应的进行,MR进入中级或最终阶段,CMC与木糖的交联结构变化不大,导致改性膜的耐水性随反应时间的变化较小;而由于MR程度随反应温度升高而明显加深,不溶性MR产物随反应温度升高而增多,导致改性膜的WS和SR在反应6 h后随反应温度的升高而进一步下降。此外,60、70、80 ℃下反应24 h后,改性膜的WS分别降至30.9%、29.7%和28.6%,SR分别降至24.0%、23.1%和22.5%,由此可知,在60~80 ℃范围内,可以通过控制反应时间得到WS和SR相似的改性膜。
综上,当MR体系组成固定时,随着反应温度的升高和反应时间的延长,CMC改性膜的A420升高、耐水性增强,通过调节MR程度,可调节改性膜的耐水性。
2.2 MR反应程度对CMC改性膜特性的影响
2.2.1 颜色和透光率
由表1可知,随着MR程度的加深,CMC改性膜50-1、60-3和70-9的颜色加深,MR又称为非酶褐变反应,随着反应的进行会产生褐色物质,生成物的颜色变化可表征MR程度,与A420结果一致。CHENG等研究表明[17],豌豆蛋白/普鲁兰多糖膜中MR在前6 h内为初级反应阶段,膜的颜色变化不明显,膜的水溶性略有下降,反应6 h后体系中水不溶性褐色物质增多,膜颜色加深、水溶性下降显著,与本研究结果相似。
表1 MR反应程度对CMC改性膜理化性质的影响
Table 1 Effect of Maillard reaction degree on physicochemical properties of modified CMC films
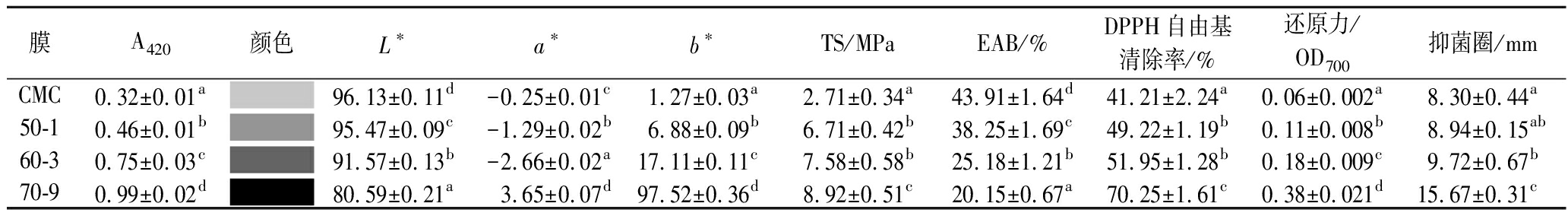
膜A420颜色L∗a∗b∗TS/MPaEAB/%DPPH自由基清除率/%还原力/OD700抑菌圈/mmCMC0.32±0.01a96.13±0.11d-0.25±0.01c1.27±0.03a2.71±0.34a43.91±1.64d41.21±2.24a0.06±0.002a8.30±0.44a50-10.46±0.01b95.47±0.09c-1.29±0.02b6.88±0.09b6.71±0.42b38.25±1.69c49.22±1.19b0.11±0.008b8.94±0.15ab60-30.75±0.03c91.57±0.13b-2.66±0.02a17.11±0.11c7.58±0.58b25.18±1.21b51.95±1.28b0.18±0.009c9.72±0.67b70-90.99±0.02d80.59±0.21a3.65±0.07d97.52±0.36d8.92±0.51c20.15±0.67a70.25±1.61c0.38±0.021d15.67±0.31c
注:50-1为50 ℃反应1 h;60-3为60 ℃反应3 h;70-9为70 ℃反应9 h。
此外,CMC改性膜亮度(L*)降低(表1),a*值和b*值分别向红色和黄色区域增加,与膜呈现的颜色一致(棕黄色)。MR过程中产生类黑素,随着MR程度的加深,类黑素生产增多导致膜的颜色变深变暗[18]。随着MR程度的加深,CMC改性膜的透光率下降(图5),对光的阻隔性提高。
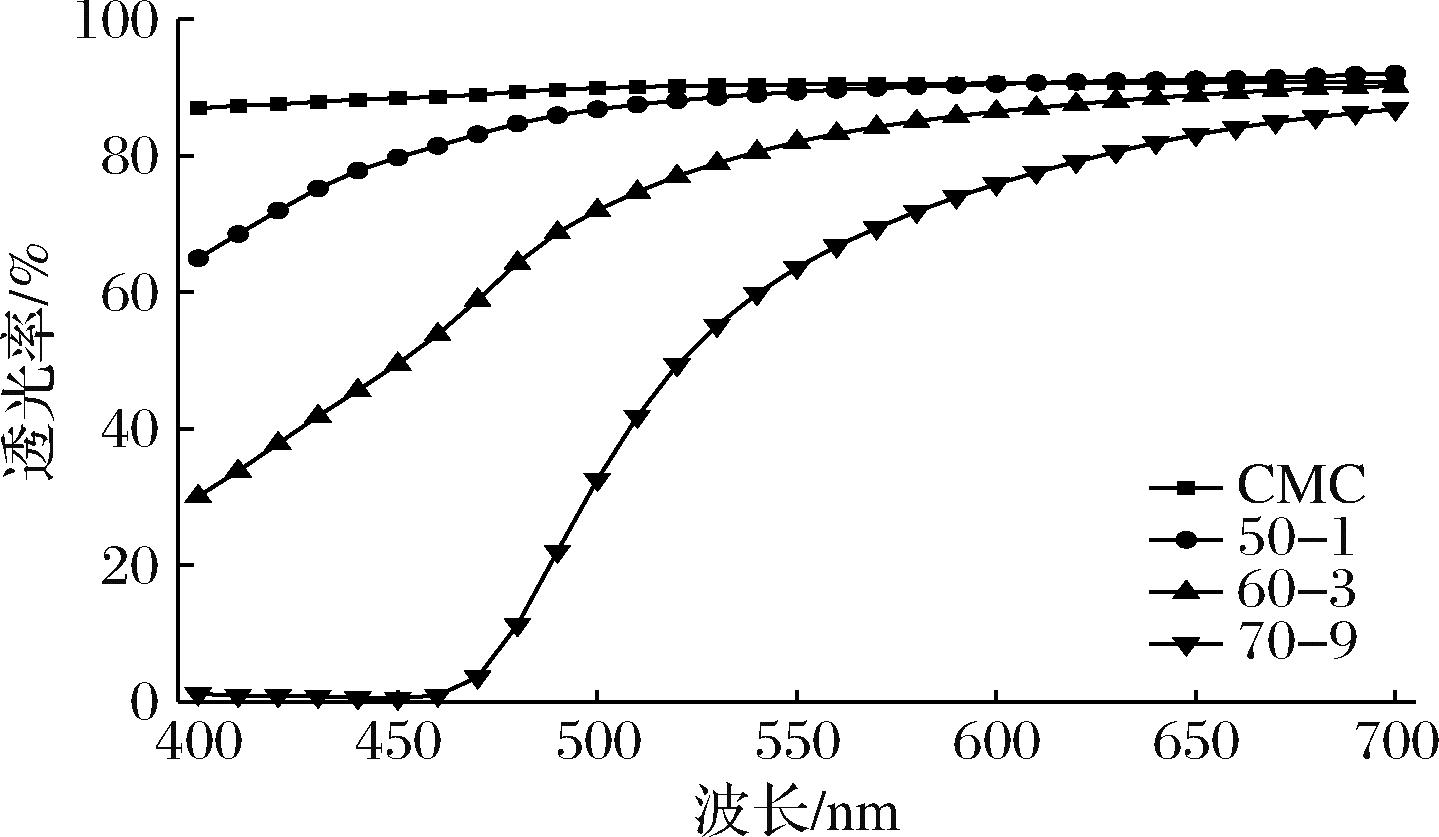
图5 MR反应程度对CMC改性膜透光率的影响
Fig.5 Effects of Maillard reaction degree on the transparency of modified CMC films
2.2.2 机械性能
TS和EAB是评价包装膜机械性能的重要指标。由表1可知,随着MR程度的加深,CMC改性膜的TS升高、EAB降低,可能的原因是MR程度越深,木糖和CMC分子间相互作用加强,分子网络结构更加致密,从而TS升高;而分子间相互作用加强使得分子流动性变差,从而导致EAB下降[16]。
2.2.3 抗氧化和抗菌活性
由表1可知,MR显著提高了CMC改性膜的抗氧化和抗菌活性,随着MR程度的加深,CMC改性膜的抗氧化和抗菌活性呈现升高的趋势,膜的自由基清除率由41.21%提高到70.25%,还原力由0.06提高到0.38,对大肠杆菌的抑菌圈直径由8.30 mm提高到15.67 mm。研究表明,MR产物具有较强的抗菌和抗氧化活性[19],在MR改性明胶膜中观察到了相似的结果[20],较高的抗氧化和抗菌活性有利于膜作为活性包装材料,保护食品免受氧化和微生物侵染。
2.3 CMC改性膜的结构表征
2.3.1 SEM
图6展示了膜的表面和截面微观结构,CMC膜表面平整光滑、无明显颗粒和裂纹,截面整体结构均匀致密,表明CMC具有良好的成膜性[21]。随着MR程度的加深,CMC改性膜表面有轻微凸起,截面更加致密,这是因为MR过程中木糖与CMC分子间相互作用加强,形成更为稳固的网格结构。郄梓含等[22]在乳清分离蛋白MR改性膜中观察到相似结果。

图6 膜的表面和截面SEM
Fig.6 SEM of surface and cross section of films
2.3.2 FTIR
如图7所示,CMC膜在3 280 cm-1处较宽的吸收峰是酰胺A带特征峰,主要为氨基和羟基的伸缩振动,随着MR程度的加深,CMC改性膜50-1、60-3和70-9的吸收峰向低波数移动,分别为3 278、3 276、3 274 cm-1处,表明膜中分子间或分子内相互作用增强;CMC膜在2 921 cm-1和2 877 cm-1处的特征峰归属于C—H的对称伸缩振动和反对称伸缩振动,在1 589 cm-1 和1 405 cm-1处的特征峰分别对应于COO—的反对称振动和对称振动[23],改性膜中此处特征吸收峰未发生明显变化。MR产生Amadori重排产物,生成席夫碱,席夫碱的特征吸收峰约在1 640 cm-1处,然而随着MR程度的加深,改性膜中无新峰出现,可能的原因是MR改性后虽然有席夫碱等物质的生成但是不足以体现在光谱之中。BHAT等[24]在明胶薄膜加入核糖后,其红外光谱也并未发生明显变化。
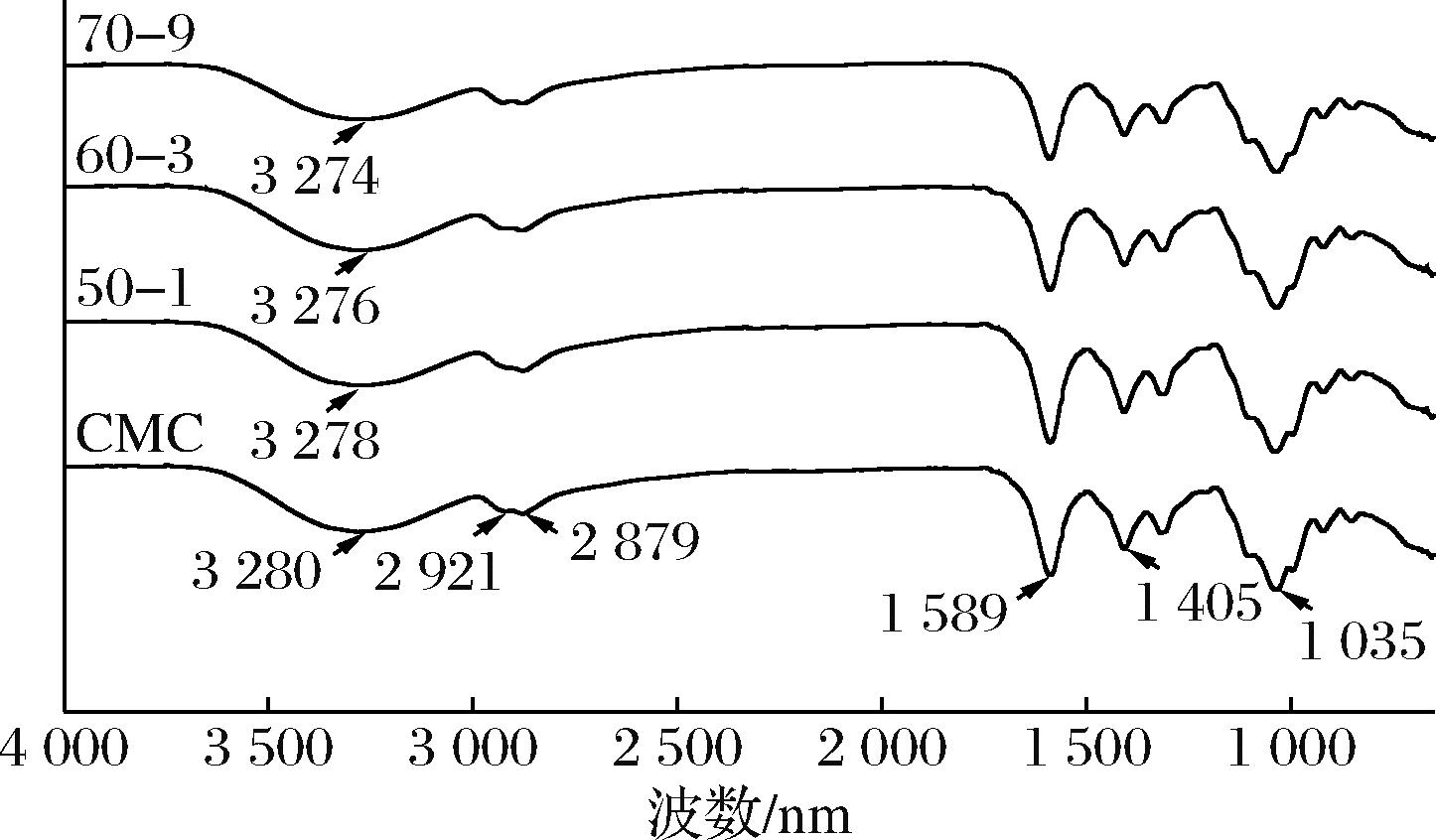
图7 膜的FTIR光谱
Fig.7 FTIR spectroscopy of films
2.3.3 XRD
如图8所示,CMC膜和CMC改性膜皆在2θ为20 °附近存在一个很宽的衍射峰,表明膜是无定形结构。随着MR程度的加深,改性膜在2θ为20°附近的特征衍射峰位置向右略微偏移,2θ由CMC的20.2°偏移至70-9的20.8°,表明CMC与木糖之间发生了反应,此外,随着MR程度的加深,改性膜的衍射峰变宽、峰强度降低,表明CMC与木糖之间相互作用增强,进而导致改性膜的结晶度下降。
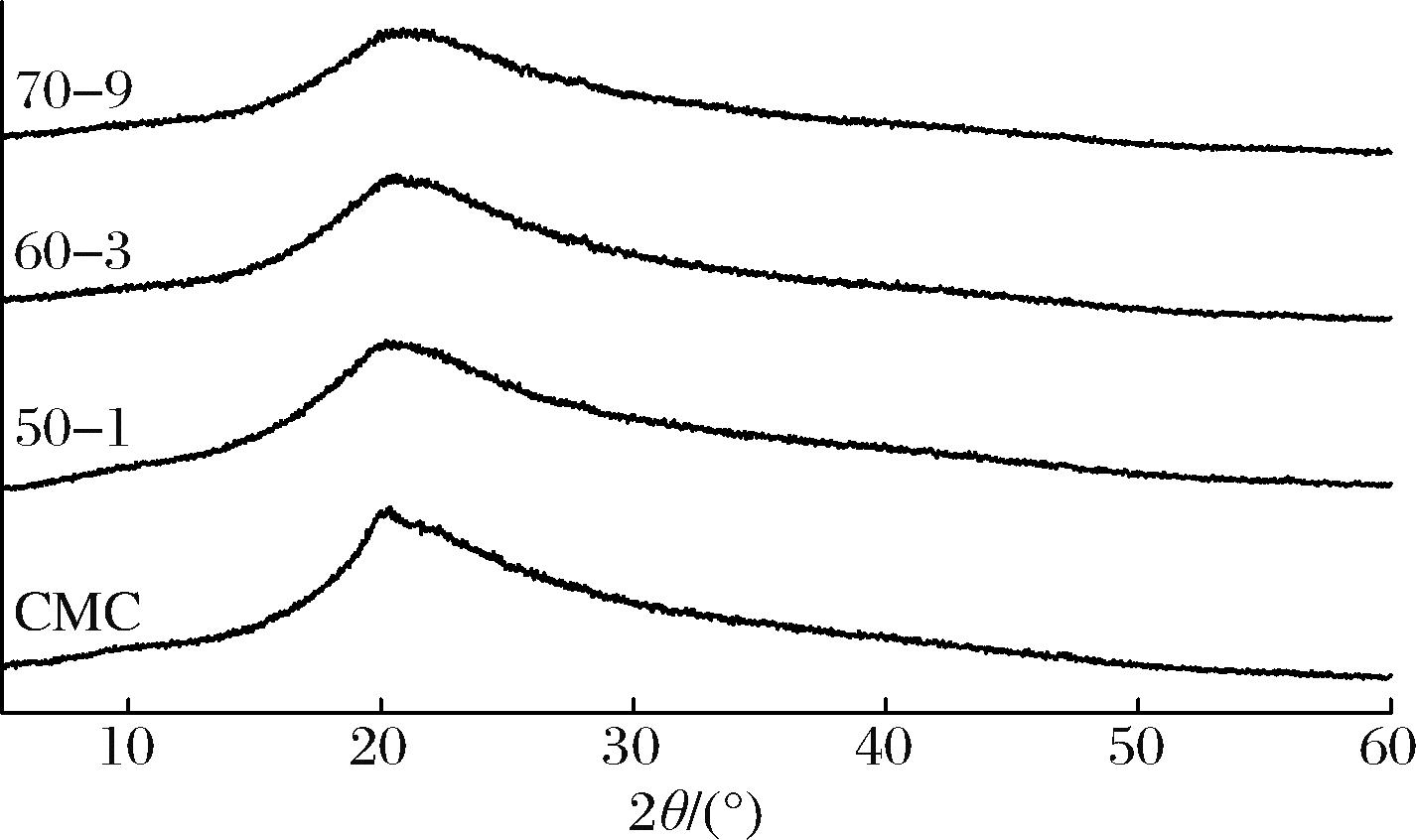
图8 膜的XRD图谱
Fig.8 XRD spectroscopy of films
3 结论
本研究解析了还原糖种类、CMC/木糖比例、膜液初始pH值、反应温度和反应时间对改性膜耐水性和A420的影响,探究了MR程度与CMC改性膜性能之间的关系。结果表明,在CMC/木糖比例4∶1膜液初始pH值10.0的条件下,随着反应温度的升高和反应时间的延长,CMC改性膜的A420升高、耐水性增强,通过调节MR程度,可调节改性膜的耐水性。此外,随着MR程度的加深,CMC改性膜的颜色加深、亮度降低,拉伸强度、抗氧化和抗菌活性升高,透光率和断裂伸长率下降,膜的结构更为致密、分子间或分子内相互作用增强、结晶度降低。本研究对CMC基膜在高水分含量食品中的应用具有一定的指导意义,为生物质基膜的改性研究提供方法参考。
[1] 王牌, 杨少玲, 戚勃, 等.基于共混和层层自组装方法协同交联剂对琼胶/海藻酸钠复合膜性能的影响[J].食品与发酵工业, 2024, 50(1):89-97.WANG P, YANG S L, QI B, et al.Effect of synergistic crosslinking agent based on blending and layer-by-layer assembly method on properties of agar/sodium alginate composite film[J].Food and Fermentation Industries, 2024, 50(1):89-97.
[2] TAUBNER T, MAROUNEK M, SYNYTSYA A.Preparation and characterization of hydrophobic and hydrophilic amidated derivatives of carboxymethyl chitosan and carboxymethyl β-glucan[J].International Journal of Biological Macromolecules, 2020, 163:1433-1443.
[3] NADIRA P P, ABDUL MUJEEB V M, RAHMAN P M, et al.Effects of cashew leaf extract on physicochemical, antioxidant, and antimicrobial properties of N, O-Carboxymethyl chitosan films[J].Carbohydrate Polymer Technologies and Applications, 2022, 3:100191.
[4] PENG L, WANG H X, DAI H J, et al.Preparation and characterization of gelatin films by transglutaminase cross-linking combined with ethanol precipitation or Hofmeister effect[J].Food Hydrocolloids, 2021, 113:106421.
[5] KAN X H, CHEN G J, ZHOU W T, et al.Application of protein-polysaccharide Maillard conjugates as emulsifiers:Source, preparation and functional properties[J].Food Research International, 2021, 150(Pt A):110740.
[6] JIANG Z H, HUANGFU Y P, JIANG L, et al.Structure and functional properties of whey protein conjugated with carboxymethyl cellulose through Maillard reaction[J].LWT, 2023, 174:114406.
[7] KCHAOU H, BENBETTAIEB N, JRIDI M, et al.Influence of Maillard reaction and temperature on functional, structure and bioactive properties of fish gelatin films[J].Food Hydrocolloids, 2019, 97:105196.
[8] RUI L Y, XIE M H, HU B, et al.A comparative study on chitosan/gelatin composite films with conjugated or incorporated Gallic acid[J].Carbohydrate Polymers, 2017, 173:473-481.
[9] KCHAOU H, BENBETTAÏEB N, JRIDI M, et al.Enhancement of structural, functional and antioxidant properties of fish gelatin films using Maillard reactions[J].Food Hydrocolloids, 2018, 83:326-339
[10] KE C X, LI L.Influence mechanism of polysaccharides induced Maillard reaction on plant proteins structure and functional properties:A review[J].Carbohydrate Polymers, 2023, 302:120430.
[11] 陈晓涵, 庞杰, 吴春华.魔芋葡甘聚糖/壳聚糖复合抗菌食品包装膜的制备及其特性[J].食品科学, 2021, 42(7):232-239.CHEN X H, PANG J, WU C H.Fabrication and characterization of antimicrobial food packaging materials composed of konjac glucomannan, chitosan and fulvic acid[J].Food Science, 2021, 42(7):232-239.
[12] STEVENSON M, LONG J, SEYFODDIN A, et al.Characterization of ribose-induced crosslinking extension in gelatin films[J].Food Hydrocolloids, 2020, 99:105324.
[13] GULL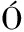 N B, MONTENEGRO M I, RUIZ-MATUTE A I, et al.Synthesis, optimization and structural characterization of a chitosan-glucose derivative obtained by the Maillard reaction[J].Carbohydrate Polymers, 2016, 137:382-389.
N B, MONTENEGRO M I, RUIZ-MATUTE A I, et al.Synthesis, optimization and structural characterization of a chitosan-glucose derivative obtained by the Maillard reaction[J].Carbohydrate Polymers, 2016, 137:382-389.
[14] GHANBARZADEH B, MUSAVI M, OROMIEHIE A R, et al.Effect of plasticizing sugars on water vapor permeability, surface energy and microstructure properties of zein films[J].LWT-Food Science and Technology, 2007, 40(7):1191-1197.
[15] JIANG J, CHEN J, XIONG Y L.Structural and emulsifying properties of soy protein isolate subjected to acid and alkaline pH-shifting processes[J].Journal of Agricultural and Food Chemistry, 2009, 57(16):7576-7583.
[16] AFFES S, MAALEJ H, LI S M, et al.Effect of glucose substitution by low-molecular weight chitosan-derivatives on functional, structural and antioxidant properties of Maillard reaction-crosslinked chitosan-based films[J].Food Chemistry, 2022, 366:130530.
[17] CHENG J J, WANG J, LI Z Z, et al.Improving the mechanical and water-resistance properties of pea protein-based edible film via wet-heating Maillard reaction:Insights into the simultaneous effect of heating and Maillard reaction[J].Food Packaging and Shelf Life, 2023, 35:101024.
[18] AFFES S, NASRI R, LI S M, et al.Effect of glucose-induced Maillard reaction on physical, structural and antioxidant properties of chitosan derivatives-based films[J].Carbohydrate Polymers, 2021, 255:117341.
[19] 满涛, 熊晓辉, 王亚楠, 等.玉米蛋白美拉德反应产物膜对冷鲜牛肉的保鲜效果[J].现代食品科技, 2023, 39(4):154-162.MAN T, XIONG X H, WANG Y N, et al.Effect of zein in Maillard reaction product films on the preservation of chilled fresh beef[J].Modern Food Science and Technology, 2023, 39(4):154-162.
[20] HAMDI M, NASRI R, BEN AZAZA Y, et al.Conception of novel blue crab chitosan films crosslinked with different saccharides via the Maillard reaction with improved functional and biological properties[J].Carbohydrate Polymers, 2020, 241:116303.
[21] KOSHY R R, REGHUNADHAN A, MARY S K, et al.pH indicator films fabricated from soy protein isolate modified with chitin nanowhisker and Clitoria ternatea flower extract[J].Current Research in Food Science, 2022, 5:743-751.
[22] 郄梓含, 雷桥, 高文婧, 等.美拉德交联对乳清分离蛋白-酪蛋白酸钠-普鲁兰多糖薄膜阻隔性及抗氧化性的改性研究[J].食品与发酵工业, 2020, 46(14):70-76.QIE Z H, LEI Q, GAO W J, et al.Modification of Maillard crosslinking on barrier and antioxidant properties of WPI-Na Cas-pullulan based edible films[J].Food and Fermentation Industries, 2020, 46(14):70-76.
[23] ZHOU W, HE Y X, LIU F, et al.Carboxymethyl chitosan-pullulan edible films enriched with galangal essential oil:Characterization and application in mango preservation[J].Carbohydrate Polymers, 2021, 256:117579.
[24] BHAT R, KARIM A A.Towards producing novel fish gelatin films by combination treatments of ultraviolet radiation and sugars (ribose and lactose) as cross-linking agents[J].Journal of Food Science and Technology, 2014, 51(7):1326-1333.
 lm;Maillard reaction;water resistance property;mechanical property;modification
lm;Maillard reaction;water resistance property;mechanical property;modification