γ-氨基丁酸(γ-aminobutyric acid,GABA)是一种具有提高免疫能力、调节血压、延缓智力退化、改善大脑功能的非蛋白质氨基酸,主要存在于植物的种子、根茎和组织液以及哺乳动物的神经组织中[1-2]。在植物体内,GABA的合成途径主要关键酶是谷氨酸脱羧酶(glutamate decarboxylase,GAD)、二胺氧化酶(diamine oxidase,DAO)和多胺氧化酶(polyamine oxidase,PAO),其代谢途径主要有两条,首先是GABA支路,指L-谷氨酸在GAD的催化作用下脱羧生成GABA,随后在GABA转氨酶(GABA transaminase,GABA-T)以及琥珀酸半醛脱氢酶(succinic semialdehyde dehydrogenase,SSADH)催化下生成琥珀酸进入三羧酸循环;其次是多胺降解途径,腐胺、亚精胺和精胺分别在DAO和PAO的催化作用下生成4-氨基丁醛,最后经氨基醛脱氢酶(aminoaldehyde dehydrogenase,AMADH)催化生成GABA[3]。
目前,市面上的GABA产品主要以糙米[4]、大豆[5]、荞麦[6]等为原料,但含量较低,并不能满足人体的日常需求。芸豆含有丰富的蛋白质、碳水化合物和多种对人体有益的生物活性物质,是维生素和矿物质的良好来源,具有降血脂、抗肿瘤、预防糖尿病等作用,但在食品应用方面,芸豆开发利用率较低,深加工食品类型较少[7]。目前已有研究[8]发现,盐胁迫协同抗坏血酸处理萌发芸豆会促进GABA富集,但有关发芽芸豆在环境胁迫和外源因子协同处理下富集GABA的机理研究较少。
本研究以发芽芸豆为原料,进行谷氨酸钠(monosodium glutamate,MSG)协同低温冻融处理,对处理前后发芽芸豆GABA相关酶活性进行测定,并通过非靶向代谢组学分析MSG协同低温冻融对发芽芸豆代谢物质以及代谢通路的影响,探究MSG协同低温冻融促进发芽芸豆富集GABA的作用机理。
1 材料与方法
1.1 材料与仪器
芸豆,中国黑龙江省种植品种(红花芸豆);GABA标准品(纯度≥99.9%),美国Sigma-Aldrich公司;DAO和PAO检测试剂盒,上海酶联生物技术有限公司;β-巯基乙醇、磷酸吡哆醛,上海麦克林生化科技有限公司;L-谷氨酸,北京索莱宝科技有限公司;谷氨酸钠,北京奥博星生物技术有限责任公司;乙二胺四乙酸,辽宁泉瑞试剂有限公司。
CN-A323康丽发芽机,中山市飞鱼电器有限公司;Centrifuge 5424 R冷冻离心机,德国艾本德股份公司;Wonbio-96c多样品冷冻研磨仪,上海万柏生物科技有限公司;LNG-T88台式快速离心浓缩干燥器,太仓市华美生化仪器厂;JXDC-20氮气吹扫仪,上海净信实业发展有限公司;UHPLC液相色谱系统、Q-Exactive质谱仪,美国Thermo Fisher公司。
1.2 试验方法
1.2.1 MSG协同低温冻融发芽芸豆
参考张茜[9]的方法,将芸豆用1%(体积分数)次氯酸钠浸泡消毒15 min后用蒸馏水冲洗干净,于3 mg/mL MSG溶液中避光浸泡6 h。放入发芽机中,以3 mg/mL MSG溶液为培养液,每15 min喷雾1 min,发芽3 d后,参考尹永琪等[10]的方法并结合前期优化的最佳条件,将发芽芸豆放入-20 ℃冰箱冷冻17 h,然后在22 ℃解冻9 h。随后,部分样品烘干粉碎进行GABA含量测定,剩余样品液氮冷冻,-80 ℃保存。分组如下:FY为发芽芸豆;MFY为MSG处理的发芽芸豆;DFY为低温冻融的发芽芸豆;MDFY为MSG协同低温冻融的发芽芸豆。
1.2.2 GABA含量测定
参考YU等[11]的GABA测定方法,取0.5 发芽芸豆粉,加5 mL蒸馏水,混匀,70 ℃恒温水浴中振荡提取2 h,4 000 r/min离心30 min,上清液为样品提取液。取1 mL提取液加入1 mL四硼酸钠缓冲液(0.2 mol/L,pH 9.0)、2 mL 5%(体积分数)重蒸苯酚、1 mL 7%(体积分数)次氯酸钠,沸水浴10 min,冰浴20 min,蓝绿色出现后加入2.0 mL 60%(体积分数)乙醇,混合均匀,在检测波长645 nm下测量吸光度。绘制标准曲线,横坐标(X)为GABA质量浓度(mg/mL),纵坐标(Y)为吸光度,利用公式(1)计算GABA浓度:
(1)
式中:X,样品中γ-氨基丁酸的含量,mg/g;C,样品中γ-氨基丁酸的质量浓度,mg/mL;N,稀释倍数;M,称取样品的质量,g;V,样品的稀释体积,mL。
1.2.3 GAD、DAO和PAO活性测定
参考姚琪等[12]的测定方法,取1 g新鲜发芽芸豆样品去皮,加入5 mL的磷酸钾缓冲液(50 mmol/L,pH 5.9),其中含有0.2% (体积分数)β-巯基乙醇、乙二胺四乙酸(2 mmo1/L)、磷酸吡哆醛(0.2 mmol/L)、丙三醇(10%),冰浴研磨成浆,于4 ℃,10 000 r/min离心20 min,上清液为酶粗提液。取两份1 mL酶液,一份加入1 mL谷氨酸溶液(1%),另一份加1 mL磷酸钾缓冲液作为空白,将两份样品置于40 ℃反应2 h,90 ℃水浴5 min终止反应,8 000 r/min离心20 min,取上清液测定GABA含量,以每小时生成1 μmol GABA为一个酶活力单位(U)。DAO和PAO的活性按照ELISA试剂盒说明书测定。
1.2.4 差异代谢组学分析
1.2.4.1 样品预处理
参考鲍俊杰[13]的方法略作改进,将FY和MDFY组发芽芸豆用液氮研磨成粉末,取200 mg加入400 μL提取液[V(甲醇)∶V(水)=4∶1],混匀,低温超声波提取30 min(5 ℃,40 kHz),-20 ℃静置30 min,离心15 min,上机分析。另外,每个样品取20 μL上清液混合后作为质控(quality control, QC)样本。
1.2.4.2 色谱-质谱条件
参考ZENG等[14]的方法并结合实际情况改进,将3 μL样品进样到ACQUITY UPLC BEH C18(100 mm×2.1 mm,i.d.,1.7 μm;Waters,Milford,USA)色谱柱中。流动相A为乙腈水(2%,含0.1%甲酸),流动相B为乙腈(含0.1%甲酸),流速为0.4 mL/min,梯度为:0~0.5 min,98% A;0.5~7.5 min,98%~65% A;7.5~13 min,65%~5% A;13~14.4 min,5% A;14.4~14.5 min,5%~98% A;14.5~16 min,98% A,柱温保持在40 ℃。
电喷雾电离,采用正离子和负离子扫描方式采集质谱信号。具体参数如下:扫描范围为70~1 050 m/z;鞘气流速50 Arb;辅助气流速13 Arb;加热温度450 ℃;毛细管温度320 ℃;喷雾电压(正模式)3 500 V;喷淋电压(负模式)-3 000 V;S-Lens电压40;碰撞能20、40、60 eV。在仪器分析过程中,每5~15个分析样品插入1个QC样品,以考察整个检测过程的稳定性。
1.3 数据处理与分析
所有试验重复3次,结果以“平均值±标准方差”表示,使用SPSS 26软件进行数据处理(P<0.05为显著性差异),Graphpad Prism 8软件绘图。代谢组学数据使用Progenesis QI(Waters Corporation,Milford,USA)软件处理,得到保留时间、质荷比、峰强度等信息的数据矩阵。随后将质谱信息与内部数据库匹配,根据二级质谱匹配对代谢物进行鉴定。数据分析包含主成分分析(principal component analysis,PCA)和正交偏最小二乘判别分析(orthogonal partial least-squares discrimination analysis,OPLS-DA)。基于OPLS-DA模型获得的变量重要性投影(variable importance in project,VIP)进行评分,并筛选VIP>1和P<0.05的物质作为显著差异代谢物。利用KEGG代谢库将鉴定出的差异代谢物进行比对并注释,分析相关代谢通路。
2 结果与分析
2.1 MSG协同低温冻融对发芽芸豆GABA含量影响
由图1可知,经MSG和低温冻融处理后,发芽芸豆的GABA含量达到2.53 mg/g,是FY组的3.33倍,显著高于MFY组和DFY组(P<0.05),说明MSG协同低温冻融能够促进发芽芸豆中GABA富集。已有研究报道外源添加的MSG促使L-谷氨酸含量增加,L-谷氨酸在GAD催化下产生更多的GABA,同时,低温冻融过程使芸豆细胞膜破损,导致与酶反应的底物增加,促进GABA的合成[15-16]。结果显示,MDFY处理组GABA富集效果最好,故而选择该组发芽芸豆进行后续酶活性测定和代谢组学的研究。
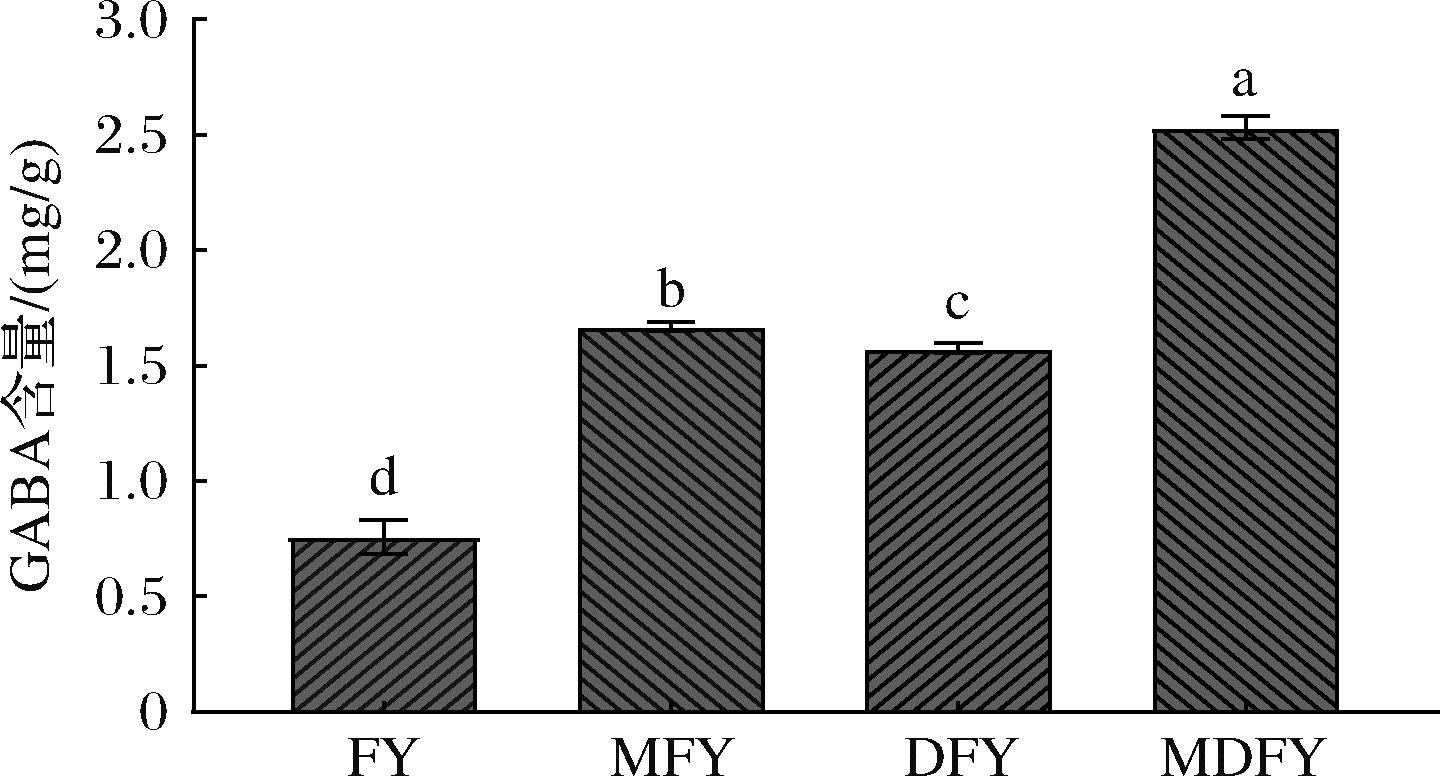
图1 不同处理组发芽芸豆GABA含量
Fig.1 GABA contents of germinated kidney beans in different treatment groups
注:不同小写字母表示组内不同水平之间存在显著差异 (P<0.05)(下同)。
2.2 MSG协同低温冻融对发芽芸豆GAD、DAO和PAO活性影响
由图2可知,MDFY组与FY组相比,GAD活性未发生显著变化,而DAO和PAO活性显著降低(P<0.05)。有研究表明[17],低温冻融过程中GABA含量升高,但GABA合成途径中的GAD等关键酶活性下降,推测GABA的富集并不依赖于相关酶活性的影响,与本研究结果一致。根据2.1节结果可知,MDFY组GABA含量最高,但MDFY组中GAD活性无明显变化,DAO和PAO活性下降,因此进一步通过代谢组学方法研究探讨其GABA富集机制。

a-GAD活性;b-DAO活性;c-PAO活性
图2 不同处理组发芽芸豆中GAD、DAO、PAO活性
Fig.2 Activities of GAD, DAO, and PAO of germinated kidney beans in different treatment groups
2.3 MSG协同低温冻融对发芽芸豆代谢组学影响
研究表明低温胁迫会使植物产生大量初级和次级代谢产物,而非靶向代谢组学可以分析特定生物体中所有代谢物及其整体变化规律,并寻找差异代谢物和代谢途径[18]。因此本研究利用非靶向代谢组学对MSG协同低温冻融促进发芽芸豆富集GABA过程中差异代谢产物以及相关代谢通路进行分析,对GABA富集机理进行探究。
2.3.1 多元统计分析
如图3-a,PCA评分图表明,第一主成分(PC1)和第二主成分(PC2)分别占总方差的40.10%和22.6%,两个样品均存在于95%置信区间内,说明该样品模型稳定可靠,可进行后续分析研究。在图3-b OPLS-DA图中,FY和MDFY组样品均在置信区间内,且存在较好的分离效果,说明两样本组间差异明显。为避免模型发生过拟合进行200次OPLS-DA置换检验分析,如图3-c,结果显示置换后R2和Q2左边点均低于右边,且Q2回归线截距<0,同时R2Y=0.995 Q2=0.959均接近1,说明该模型没有过拟合,模型稳定性良好。
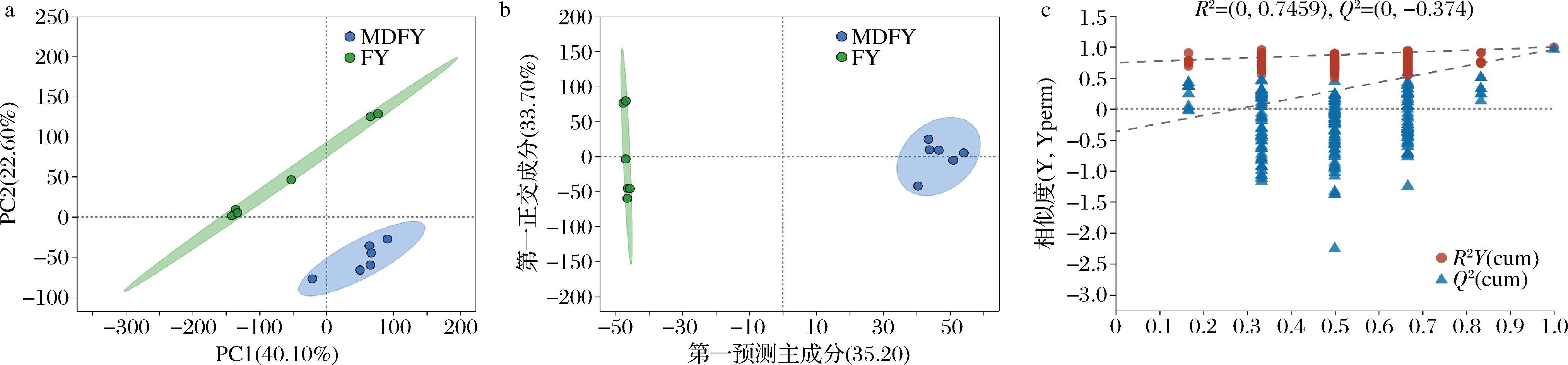
a-PAC得分图;b-OPLS-DA得分图;c-OPLS-DA置换检验图
图3 不同处理组发芽芸豆的PAC得分、OPLS-DA得分和OPLS-DA置换检验图
Fig.3 PAC score, OPLS-DA score and OPLS-DA replacement test diagram of germinated kidney beans in different treatment groups
2.3.2 差异代谢物分析
根据OPLS-DA模型的VIP≥1且P<0.05的代谢物筛选FY和MDFY组间差异显著代谢物,如图4-a,将筛选出来的差异组分结果以火山图的形式进行可视化处理,FY和MDFY间的差异显著代谢物为277种,其中上调的有171种,下调的有106种。如图4-b,差异显著代谢物主要为脂质(41种)、氨基酸及其衍生物(30种)、碳水化合物及其衍生物(15种)、核苷酸及其衍生物(9种)和维生素(1种),这表明MSG协同低温冻融处理使发芽芸豆体内的氨基酸类、脂质类和碳水化合物类物质发生显著变化(P<0.05)。
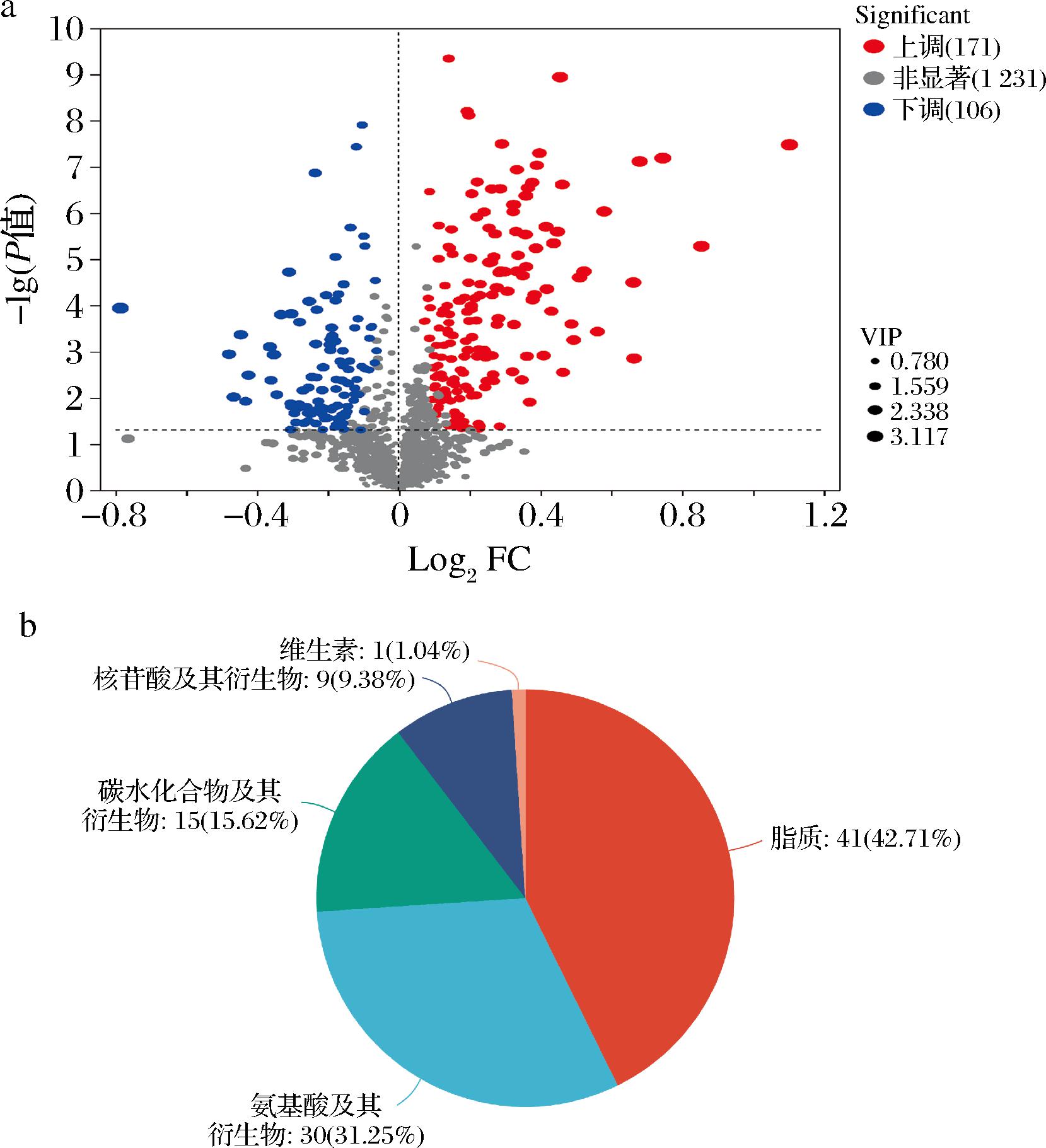
a-火山图;b-化合物分类图
图4 不同处理组发芽芸豆的差异代谢物火山图 和化合物分类图
Fig.4 Differential metabolite volcano map and compound classification map of germinated kidney beans in different treatment groups
如图5为丰度前50的显著差异代谢物相关性分析图,结果显示L-谷氨酸与GABA呈负相关,可溶性糖(蔗糖、棉子糖)、精胺、甜菜碱和甘氨酸与GABA呈正相关。研究证明MSG协同低温冻融处理后L-谷氨酸发生下调,原因可能是L-谷氨酸在相关酶作用下会发生催化反应生成谷氨酰胺、GABA和2-酮戊二酸等物质[19]。据报道,植物在受到低温胁迫时会通过生成可溶性糖、多胺类化合物和脯氨酸等渗透调节物质来维持正常的细胞渗透压和溶液浓度,防止植物细胞出现脱水、结晶等情况,稳定细胞结构[20]。另外,相关研究表明低温冻融会引起细胞内冰晶加剧破坏细胞膜,细胞膜通透性增强,激活GABA合成代谢,导致GABA含量提高[10]。结果推测可溶性糖(蔗糖、棉子糖)含量、精胺含量、甜菜碱含量和甘氨酸含量的增加可能会引起植物细胞结构的变化,影响GABA的合成。

图5 不同处理组发芽芸豆的显著差异代谢物相关性分析
Fig.5 Correlation analysis of metabolites with significant differences of germinated kidney beans in different treatment groups
注:图中不同颜色代表相关系数的大小,相关系数正、负值表示正相关和负相关,绝对值越接近于1,表示代谢物正相关或负相关性越高。
2.3.3 KEGG通路富集分析
为进一步研究MSG协同低温冻融对发芽芸豆GABA代谢途径的影响,将筛选出的显著差异代谢物与KEGG pathway数据库进行比对分析。如图6所示,筛选出前20条差异显著的代谢通路绘制气泡图,MSG协同低温冻融处理后发芽芸豆中显著变化的代谢通路主要为花生四烯酸代谢、赖氨酸降解、核苷酸代谢、ABC转运蛋白、泛酸和辅酶A生物合成、类黄酮生物合成、赖氨酸生物合成、异黄酮生物合成、精氨酸和脯氨酸代谢等代谢途径。
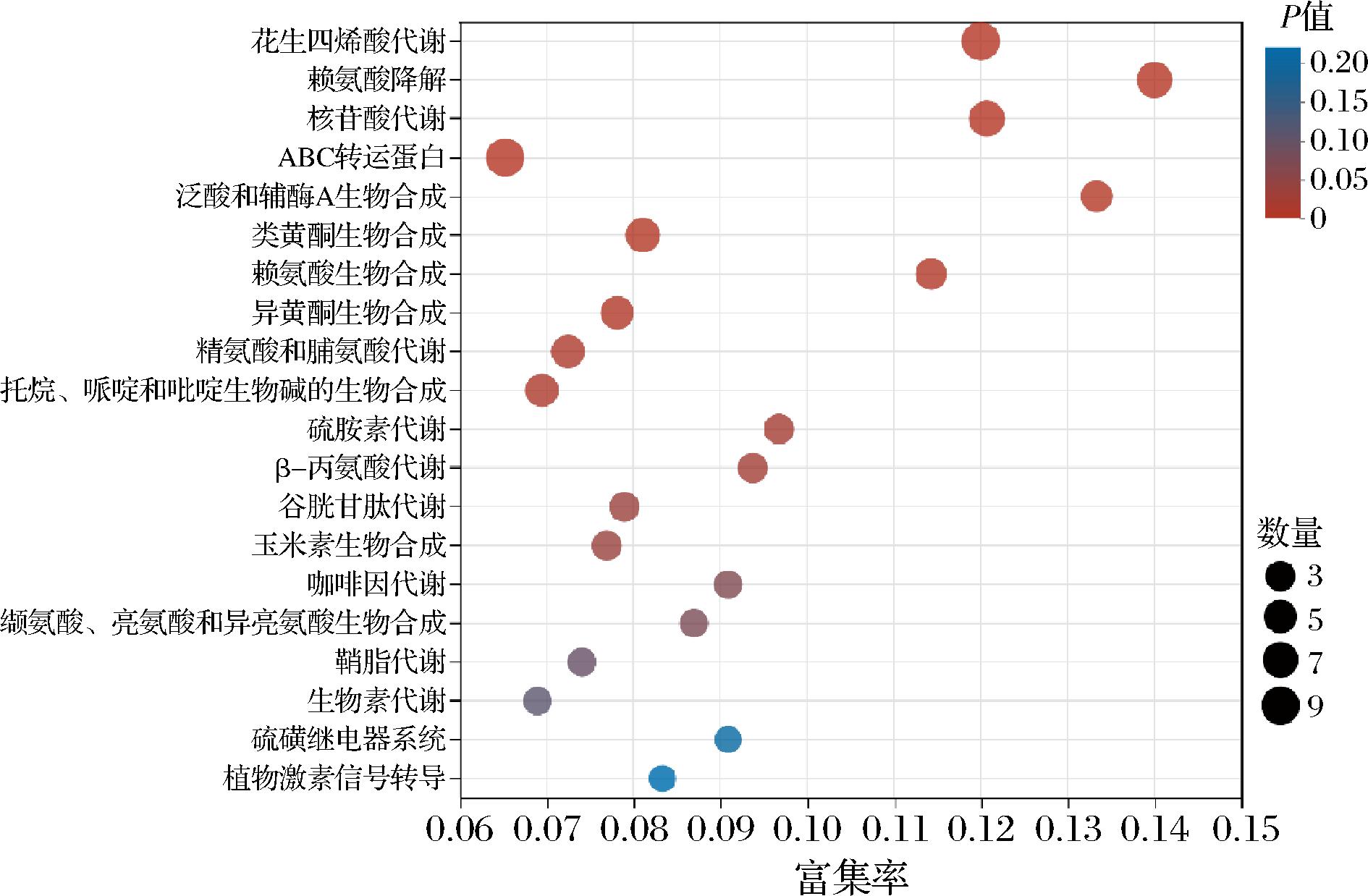
图6 KEGG富集通路气泡图
Fig.6 Bubble diagram of KEGG enrichment pathway
注:图中横坐标为富集率,纵坐标为KEGG通路。图中气泡的大小 代表该通路中富集到代谢集中成分的多少,气泡的颜色表示不同 富集显著性P值的大小。
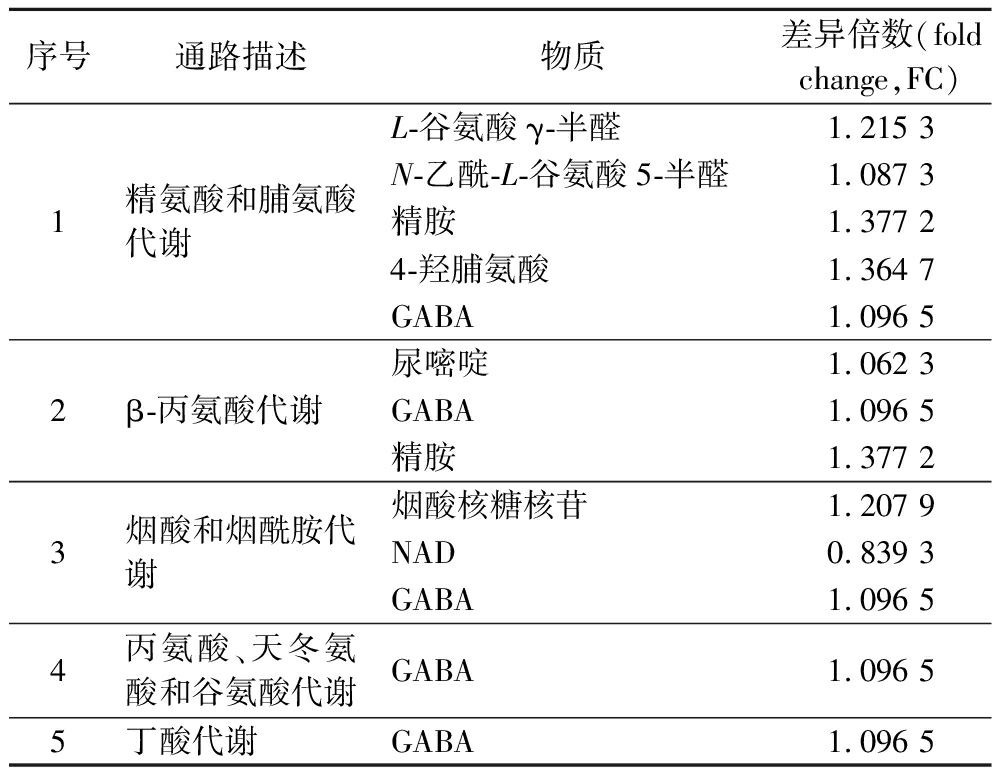
基于FY和MDFY组所有差异代谢物相关的KEGG通路,进一步筛选与GABA直接相关的代谢途径有5条,如表1所示,根据所含差异代谢物数量分别为精氨酸和脯氨酸代谢途径(5种),β-丙氨酸代谢途径(3种),烟酸和烟酰胺代谢途径(3种),丙氨酸、天冬氨酸和谷氨酸代谢途径(1种),丁酸代谢途径(1种)。已有大量研究显示,在精氨酸和脯氨酸代谢途径中,精氨酸可以在转氨酶的作用下相互转换,并参与三羧酸循环,精氨酸在一氧化氮合酶的催化作用下生成鸟氨酸,而后被鸟氨酸脱羧酶催化生成腐胺,腐胺作为多胺降解途径的底物物质被DAO催化生成GABA[21]。脯氨酸作为一种渗透调节物质,在植物受到低温胁迫时会发生积累来维持细胞内渗透压,影响细胞结构,细胞结构的改变会引起底物物质的变化,影响GABA的富集,另外,脯氨酸会在线粒体中被脯氨酸脱氢酶催化产生吡咯啉-5-羧酸,再通过吡咯啉-5-羧酸脱氢酶催化转化为L-谷氨酸,进而生成GABA[22]。在β-丙氨酸代谢途径以及丙氨酸、天冬氨酸和谷氨酸代谢途径中,谷氨酸可以在GAD催化作用下生成GABA,GABA在其他酶催化作用下生成琥珀酸进入三羧酸循环,同时,丙氨酸、天冬氨酸和谷氨酸作为植物体内的氨基酸也可以生成α-酮戊二酸进入三羧酸循环,影响GABA合成途径[23]。但目前对于烟酸和烟酰胺代谢途径以及丁酸代谢途径在MSG协同低温冻融发芽芸豆富集GABA过程中的作用机理仍需进行后续研究。
表1 GABA相关差异代谢途径
Table 1 GABA-related differential metabolic pathways
序号通路描述物质差异倍数(fold change,FC)1精氨酸和脯氨酸代谢L-谷氨酸γ-半醛1.215 3N-乙酰-L-谷氨酸5-半醛1.087 3精胺1.377 24-羟脯氨酸1.364 7GABA1.096 52β-丙氨酸代谢尿嘧啶1.062 3GABA1.096 5精胺1.377 23烟酸和烟酰胺代谢烟酸核糖核苷1.207 9NAD0.839 3GABA1.096 54丙氨酸、天冬氨酸和谷氨酸代谢GABA1.096 55丁酸代谢GABA1.096 5
注:FC值大小可以反映差异代谢物的差异表达倍数。
3 结论
本研究初步探讨了MSG协同低温冻融对发芽芸豆中GABA富集的潜在作用机制,结果显示MSG协同低温冻融显著降低发芽芸豆中DAO和PAO活性,但对GAD活性无显著影响,说明MSG协同低温冻融发芽芸豆富集GABA并不依赖于酶促作用。进一步根据非靶向代谢组学研究发现,MSG协同低温冻融主要影响发芽芸豆的氨基酸类、碳水化合物类和脂质类代谢物质,可能通过调控发芽芸豆精氨酸和脯氨酸代谢途径、β-丙氨酸代谢途径、烟酸和烟酰胺代谢途径、丙氨酸、天冬氨酸和谷氨酸代谢途、丁酸代谢途径促进GABA富集,但经MSG协同低温冻融处理发芽芸豆酶活变化规律与代谢途径的关联性及其关键性代谢途径仍需进一步探讨。
[1] DING J Z, ULANOV A V, DONG M Y, et al.Enhancement of Gama-aminobutyric acid (GABA) and other health-related metabolites in germinated red rice (Oryza sativa L.) by ultrasonication[J].Ultrasonics Sonochemistry, 2018, 40:791-797.
[2] 刘鸷驹, 张东星, 晏仁义, 等.γ-氨基丁酸的生物活性研究进展[J].现代药物与临床, 2022, 37(9):2167-2172.LIU Z J, ZHANG D X, YAN R Y, et al.Research progress on biological activities of γ-aminobutyric acid[J].Drugs &Clinic, 2022, 37(9):2167-2172.
[3] 陈惠. 发芽蚕豆γ-氨基丁酸富集与调控技术研究[D].南京:南京农业大学, 2012.CHEN H.Study on γ-aminobutyric acid accumulation and regulation techniques in germinated fava benas (Vicia faba L.)[D].Nanjing:Nanjing Agricultural University, 2012.
[4] 姜梦诗. 变温处理对发芽糙米γ-氨基丁酸的富集及产品开发研究[D].安徽:安徽科技学院, 2018.JIANG M S.Study on accumulation of γ-aminobutyric acid in germinated brown rice by variable temperature treatment and development of product[D].Anhui:Anhui Science and Technology University, 2018.
[5] 何旭东, 徐佳宁, 方维明, 等.亚精胺促进发芽大豆γ-氨基丁酸富集的工艺研究[J].现代食品, 2021, 29(20):115-118.HE X D, XU J N, FANG W M, et al.Study on the enrichment of γ-aminobutyric acid in germinated soybean by spermidine[J].Modern Food, 2021, 29(20):115-118.
[6] 张钰, 李静媛, 雷琦, 等.亚精胺和柠檬酸联合处理促进荞麦芽中γ-氨基丁酸的富集[J].现代食品科技, 2024, 40(3):200-208.ZHANG Y, LI J Y, LEI Q, et al.Improving the enrichment of γ-aminobutyric acid in buckwheat sprouts by combined treatments using spermidine and citric acid[J].Modern Food Science and Technology, 2024, 40(3):200-208.
[7] 叶夕苗, 李俊, 毛堂芬, 等.贵州不同品种芸豆营养品质差异分析[J].食品工业科技, 2021, 42(18):73-80.YE X M, LI J, MAO T F, et al.Analysis on the difference of nutritional quality of different kidney bean varieties in Guizhou[J].Science and Technology of Food Industry, 2021, 42(18):73-80.
[8] 于海燕, 廖晗雪, 陈臣, 等.盐胁迫协同抗坏血酸对芸豆萌发富集γ-氨基丁酸的影响[J].现代食品科技, 2023, 39(8):213-220.YU H Y, LIAO H X, CHEN C, et al.Effects of salt stress and ascorbic acid on the accumulation of γ-aminobutyric acid during kidney bean germination[J].Modern Food Science and Technology, 2023, 39(8):213-220.
[9] 张茜. 大豆发芽过程中营养成分变化对豆芽产出比影响的研究[D].哈尔滨:东北农业大学, 2023.ZHANG Q.Research on the effect of nutrient changes during soybean germination on the output ratio of soybean sprouts[D].Harbin:Northeast Agricultural University, 2023
[10] 尹永祺, 吴进贤, 刘春泉, 等.低氧与低温胁迫对发芽玉米籽粒中γ-氨基丁酸富集的影响[J].食品科学, 2015, 36(1):89-93.YIN Y Q, WU J X, LIU C Q, et al.Effects of hypoxia and cold stress on γ-aminobutyric acid accumulation in germinating maize[J].Food Science, 2015, 36(1):89-93.
[11] YU Y J, LI M, LI C X, et al.Accelerated accumulation of γ-aminobutyric acid and modifications on its metabolic pathways in black rice grains by germination under cold stress[J].Foods, 2023, 12(6):1290.
[12] 姚琪, 张永忠.大豆谷氨酸脱羧酶分离纯化及酶学性质研究[J].中国油脂, 2011, 36(11):26-30.YAO Q, ZHANG Y Z.Isolation and properties of soybean glutamate decarboxylase[J].China Oils and Fats, 2011, 36(11):26-30.
[13] 鲍俊杰, 王永杰, 陈红莲, 等.基于非靶向代谢组学分析两种日粮模式下克氏原螯虾肌肉的代谢差异[J].南方水产科学, 2023, 19(5):104-112.BAO J J, WANG Y J, CHEN H L, et al.Untargeted metabolomics analysis of metabolic differences of crayfish(Procambarus clarkii) meat with different diets[J].South China Fisheries Science, 2023, 19(5):104-112.
[14] ZENG C Z, LIN H Y, LIU Z X, et al.Analysis of young shoots of ‘Anji baicha’ (Camellia sinensis) at three developmental stages using nontargeted LC-MS-based metabolomics[J].Journal of Food Science, 2019, 84(7):1746-1757.
[15] 丁俊胄, 刘贞, 姚森, 等.谷氨酸钠、氯化钙对发芽糙米浆中γ-氨基丁酸积累的影响[C].第四届中国北京国际食品安全高峰论坛论文集.武汉:华中农业大学食品科技学院, 2011:52-55.DING J Z, LIU Z, YAO S, et al.Effects of MSG and CaCl2 on γ-aminobutyric acid content of germinated brown rice slurry[C].The Fourth International Food Safety Peak Forum (Beijing), Proceedings of the 4th China Beijing International Food Safety Summit Forum.Wuhan:College of Food Science and Technology, Huazhong Agricultural University, 2011:52-55.
[16] YANG R Q, FENG L, WANG S F, et al.Accumulation of γ-aminobutyric acid in soybean by hypoxia germination and freeze-thawing incubation[J].Journal of the Science of Food and Agriculture, 2016, 96(6):2090-2096.
[17] YANG R Q, HUI Q R, FENG X Y, et al.The mechanism of freeze-thawing induced accumulation of γ-aminobutyric acid in germinated soybean[J].Journal of the Science of Food and Agriculture, 2020, 100(3):1099-1105.
[18] 周丽霞, 曾春茹, 孙熹微, 等.基于非靶向代谢组学的椰肉代谢产物差异分析[J].分子植物育种, 2024,22(18):5985-5993.ZHOU L X, ZENG C R, SUN X W, et al.Analysis of metabolite differences in coconut meat through non-targeted metabolomics[J].Molecular Plant Breeding, 2024,22(18):5985-5993.
[19] FORDE B G, LEA P J.Glutamate in plants:Metabolism, regulation, and signalling[J].Journal of Experimental Botany, 2007, 58(9):2339-2358.
[20] YANG X X, LIU C, LI M D, et al.Integrated transcriptomics and metabolomics analysis reveals key regulatory network that response to cold stress in common bean (Phaseolus vulgaris L.)[J].BMC Plant Biology, 2023, 23(1):85.
[21] 杜克生. 食品生物化学[M].北京:中国劳动社会保障出版社, 2012.DU K S.Food Biochemistry[M].Beijing:China Labor and Social Security Press, 2012.
[22] 曾紫君. 外源脯氨酸对硼胁迫下棉花生长的调控作用[D].武汉:华中农业大学, 2022.ZENG Z J.Regulation of exogenous proline on cotton growth under boron stress[D].Wuhan:Huazhong Agricultural University, 2022.
[23] 纪大乙. 超声胁迫咖啡叶γ-氨基丁酸的积累及其机理初探[D].镇江:江苏大学, 2021.JI D Y.Investigation into the accumulation of γ-aminobutyric acid in coffee leaves and the associated mechanism in response to ultrasound stress[D].Zhenjiang:Jiangsu University, 2021.