重金属污染已成为世界性的农业生态环境问题,严重威胁着现代农业的生态安全。常见的重金属,如汞(Hg)、镉(Cd)、铅(Pb)和砷(As)等,可以进入土壤和地下水,在动植物体内生物积累,然后通过食物链进入人体,即使是微量的,也会对人体健康造成危害[1-2]。其中,汞离子(Hg2+)毒性强并广泛存在于环境中,水环境中的汞经食物链的富集可达到相当高的浓度,如在藻类[3]和鱼类[4]可分别达102.4~105.9倍和104~106倍,在贝类[5]中可高达上千倍。Hg2+可引起多种不良健康影响,如脑损伤、肾衰竭、免疫系统紊乱、肌肉无力和肢体瘫痪[6]。因此,研究水产品中Hg2+的脱除技术对保障食品安全和国民身体健康具有重大的现实意义。
目前国内外对于水产品中Hg2+的脱除主要分为两个途径:一是通过控制和脱除水产生长环境中的Hg2+,最终确保水产品中Hg2+含量达标,如净水暂养、养殖水体净化等方法,但这种依靠生物自身代谢脱除重金属存在耗时长、损耗大、且会造成水质污染等缺陷[7];二是对酶解液等进行处理从而达到去除超标重金属的目的,包括壳聚糖吸附法[8]、络合法[9]、膜分离法[10]、螯合树脂法[11]等。这些方法具有脱除范围大、效果好、操作简单等优点。但这些技术对重金属的脱除均为非选择性脱除,在脱除过程中易造成食品其他营养组分的损失。因此,现急需发展具有极高选择性、能最大限度地保留食品原有营养价值的净化技术,为重金属的高效精准脱除提供一种新的途径。
适配体是一类具有特异性识别的单链核苷酸分子,鉴于适配体靶标范围广、具有高亲和力和高特异性、不受免疫条件和免疫原性限制、制备简单、性质稳定、易于标记和保存等优点,使其在基础研究、临床诊断及药物筛选中都具有广阔的应用前景[12-14]。近年来,适配体作为固相萃取吸附剂,应用于亲和柱的制备,以达到富集或净化的目的。赵颖等[15]将适配体亲和柱应用于莲子黄曲霉毒素B1的测定,实验结果显示适配体亲和柱测定分离效果与免疫亲和柱无异,并且适配体亲和柱可重复循环使用,展示了适配体亲和柱良好的应用前景。目前,利用适配体亲和柱进行重金属离子净化的报道较少,本文拟采用高亲和力识别Hg2+的适配体制备亲和柱,对水产品中Hg2+进行去除,并考察其对水产品营养品质的影响。
1 材料与方法
1.1 试剂与仪器
Hg2+标准溶液(1 000 μg/mL),阿拉丁试剂(上海)有限公司;链霉素亲和素琼脂糖凝胶,北京博尔西科技有限公司;生物素标记的Hg2+适配体序列:5′-biotin-TTCTTTCTTCCCCTTGTTTGTT-3′(参考前期工作[16]),生工生物工程(上海)有限公司;其余试剂购于国药集团化学试剂有限公司。
Centrifuge5424R台式高速冷冻离心机,德国Eppendorf公司;Direct-Q3超纯水仪,美国Millipore公司;UV-Vis(-NIR)分光光度计(UVProbe2.33版),日本岛津公司;NexION350D电感耦合等离子体质谱,美国PE公司。
1.2 适配体亲和柱的制备
首先取500 μL链霉亲和素琼脂糖凝胶,于6 000 r/min离心3 min,弃去上清液。随后,加入1 mL结合缓冲液(20 mmol/L Na2PO4、150 mmol/L NaCl、pH 7.4)重复洗涤5次,4 ℃保存。然后将生物素修饰的Hg2+适配体溶解于结合缓冲液中,在95 ℃下加热10 min,慢慢冷却到室温。然后将得到的链霉亲和素琼脂糖与适配体25 ℃下充分孵育40 min后,于6 000 r/min离心3 min,弃去上清液,用结合缓冲溶液对产物洗涤5次。随后加入1 mL 2%(质量分数)的牛血清白蛋白(bovine serum albumin,BSA)溶液于25 ℃下充分孵育30 min。孵育结束后,于6 000 r/min离心3 min,弃去上清液。用结合缓冲液洗涤3次,将所得含有适配体的琼脂糖凝胶悬浮液移至含有下筛板的固相萃取柱管中,使凝胶沉降30 min形成稳定的筛层,将上筛板置于顶部完成适配体亲和柱的制备。在整个操作过程中,保持凝胶处于湿润状态。
1.3 Hg2+适配体亲和柱富集效果评价
用20 mmol/L Tris-HCl(pH 7.0)Hg2+标准溶液进行梯度稀释,随后取2 mL稀释好的Hg2+标准液以1 mL/min的速度缓慢注入亲和柱中,在出样口收集流出液,用电感耦合等离子质谱(inductively coupled plasma mass spectrometry,ICP-MS)检测流出液中的Hg2+含量,与样品的原始浓度进行对比,计算富集率及吸附量,其表达式如公式(1)、(2)。ICP-MS仪器工作参数见表1。
富集率![]()
(1)
(2)
表1 ICP-MS仪器工作参数
Table 1 Working parameters of ICP-MS instrument
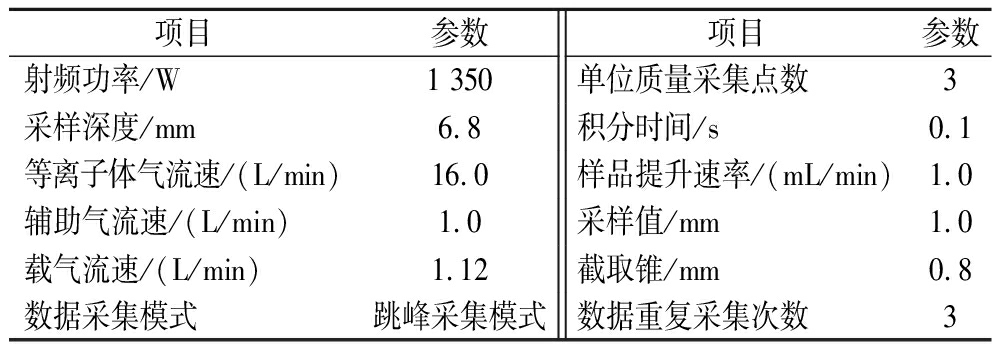
项目参数项目参数射频功率/W1 350单位质量采集点数3采样深度/mm6.8积分时间/s0.1等离子体气流速/(L/min)16.0样品提升速率/(mL/min)1.0辅助气流速/(L/min)1.0采样值/mm1.0载气流速/(L/min)1.12截取锥/mm0.8数据采集模式跳峰采集模式数据重复采集次数3
式中:ρ0,富集前Hg2+标准液的质量浓度,mg/L;ρ1,富集后Hg2+标准液的质量浓度,mg/L;V,吸附样液的体积,L;M,Hg2+适配体亲和柱的体积,L;Q,吸附量,mg/L。
1.4 实际样品处理
选择水产调味品鱼露作为实际样品。首先将鱼露按照体积比1∶20进行稀释,分别向稀释后鱼露样品中加入0.5、1.25、5.0 mg/L Hg2+溶液,然后将样品加入适配体亲和柱净化富集,收集流出液。之后用洗脱液进行洗脱,收集洗脱液。用ICP-MS测定脱除前后溶液中Hg2+浓度进行检测验证。
1.5 实际样品营养成分脱除前后的比对
为了探究实际样品中Hg2+的脱除是否会对其本身的营养成分造成影响,根据GB/T 42463—2023 《鱼露质量通则》中对于鱼露理化指标的规定,对其全氮和氨基酸态氮的含量进行测定。
1.5.1 全氮的测定
按照GB 5009.5—2016 《食品安全国家标准 食品中蛋白质的测定》中“第一法 凯式定氮法”的规定进行检验。
1.5.2 氨基酸态氮的测定
按照GB 5009.235—2016 《食品安全国家标准 食品中氨基酸态氮的测定》中“第一法 酸度计法”进行测定。
基本成分损失率计算如公式(3)。
成分损失率![]()
(3)
式中:ρ0,反应前营养成分的质量浓度,mg/L;ρ1,反应后营养成分的质量浓度,mg/L。
2 结果与分析
2.1 Hg2+适配体亲和柱的脱除原理
如图1所示,生物素标记的Hg2+适配体通过生物素与链霉亲和素的特异性结合被固定于琼脂糖凝胶表面,随后加入BSA封闭其他位点,形成了柱内体系。当体系内存在Hg2+时,Hg2+可以选择性地与适配体序列中的2个DNA胸腺嘧啶(T)碱基结合,并促进T-T错配形成稳定的T-Hg2+-T复合物(结合常数约为106 L/mol)[17],从而将Hg2+捕获于亲和柱内,从而实现对Hg2+的有效富集和脱除。
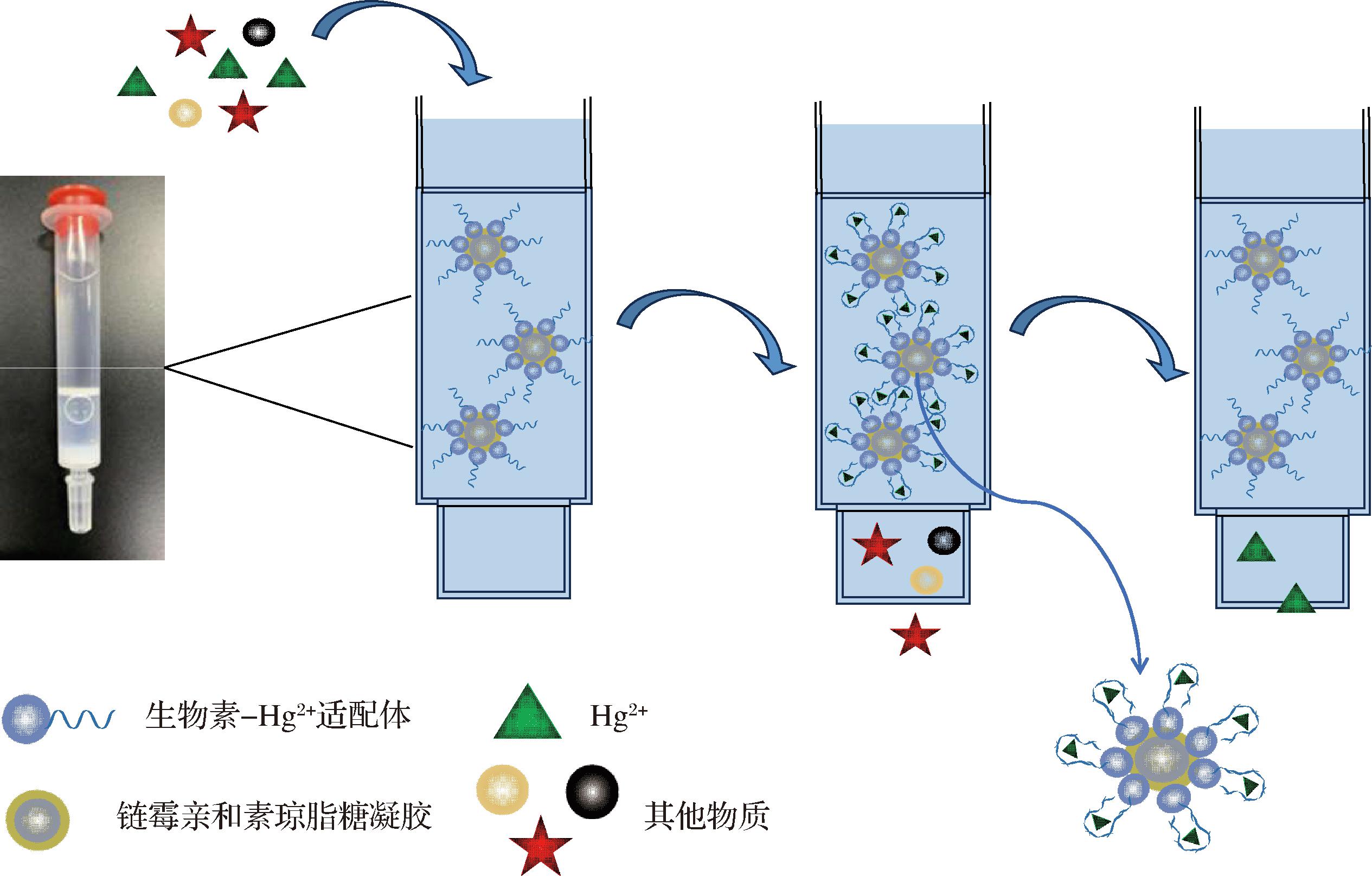
图1 适配体亲和柱成品图及基于特异性适配体结合重金属Hg2+的富集原理图
Fig.1 Aptamer affinity column image and schematic diagram of enrichment of heavy metal mercury ions based on specific aptamers
2.2 Hg2+适配体亲和柱的制备条件优化
为实现Hg2+适配体亲和柱对Hg2+的最大化高效富集,实验对亲和柱的制备条件,包括适配体浓度、偶联时间、反应pH和温度进行了优化。由于适配体在260 nm处具有紫外特性吸收峰,因此可通过扫描不同浓度下适配体原液以及适配体结合链霉亲和素琼脂糖凝胶后的上清液的紫外光谱,根据结合前后在吸光度260 nm的差值进行探索。如图2-a所示,随着Hg2+适配体浓度的增加,A260的差值也逐渐增大,当Hg2+适配体浓度为1 μmol/L时,差值达到最大,说明此时适配体已最大化固定于链霉亲和素琼脂糖凝胶表面。因此,实验中选择Hg2+适配体浓度为1 μmol/L为最佳反应条件,用于后续实验。
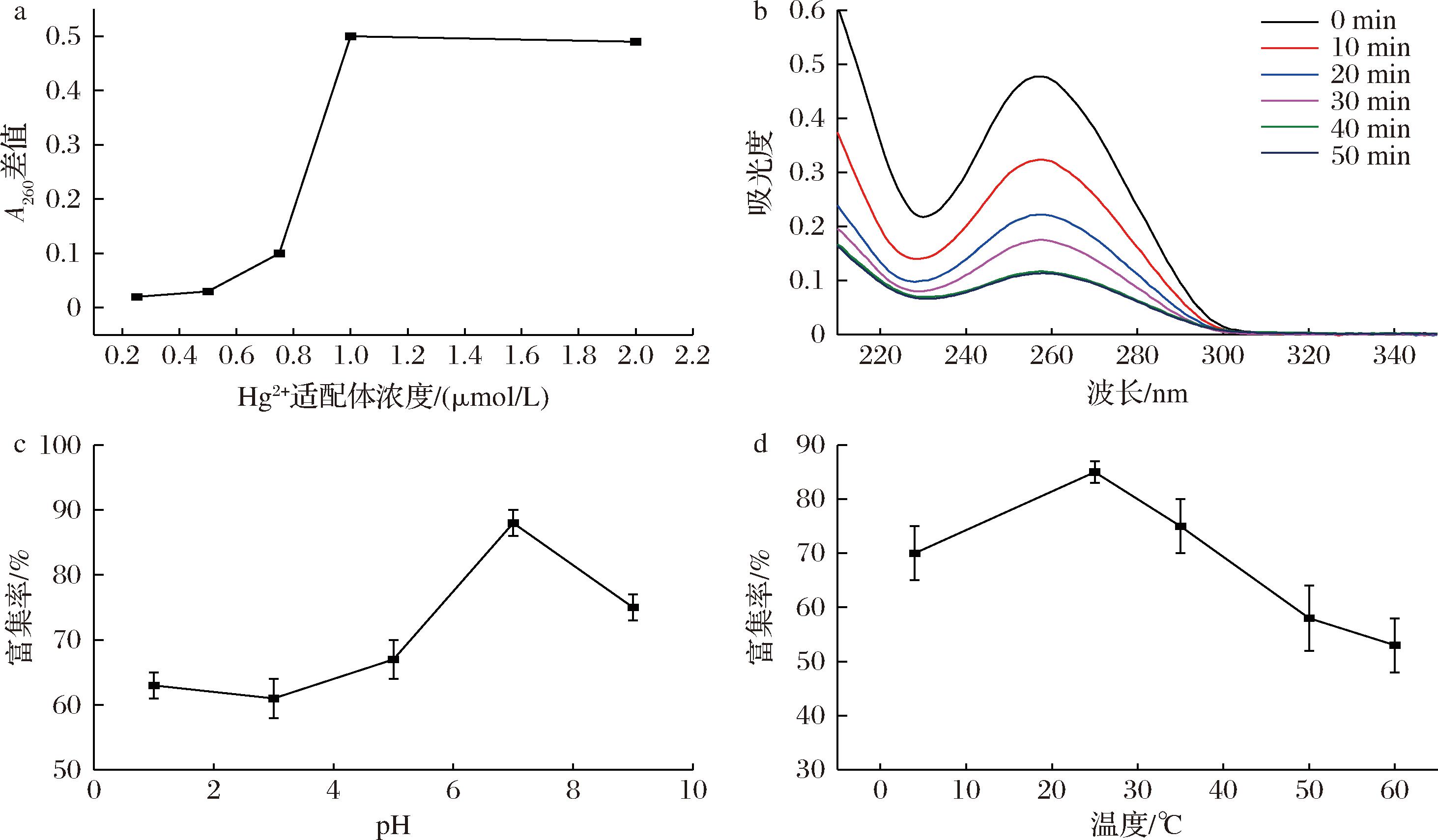
a-浓度;b-时间;c-pH;d-温度
图2 Hg2+适配体亲和柱的制备条件优化
Fig.2 Optimization analysis of the preparation of aptamer affinity column
根据相同的原则对适配体与链霉亲和素琼脂糖凝胶偶联时间进行优化,如图2-b所示,随着偶联时间的延长,A260的吸光度值逐渐降低,当时间为40 min时,吸光度最低,说明此时适配体已最大化固定于链霉亲和素琼脂糖凝胶表面。因此,实验中选择40 min作为最佳反应时间,用于后续实验。此外,pH和温度对于适配体与Hg2+的结合也起着重要的作用。如图2-c和图2-d所示,在中性条件(pH 7.4)和25 ℃条件下观察到高富集率,说明在此条件下有利于适配体空间构象的形成,提高了它与靶标的亲和力。
2.3 Hg2+适配体亲和柱的柱容量考察
为保证适配体亲和柱的使用效能,需对亲和柱的柱容量(即亲和柱可一次性结合的Hg2+的总量)进行考察,不同质量浓度Hg2+标准液(10、15、20、25、50、75、100 mg/L)上样进入适配体柱,收集洗脱液。利用ICP-MS进行检测,根据公式(1)、(2)计算出富集率及吸附量。结果如图3-a所示,富集率随装载量的增加而增加,说明所制备的适配体柱能有效地与靶标结合。当加载量为25 μg时,富集率达到最大值。然而,当加载量大于25 μg时,体系中存在一些游离的Hg2+不能完全被适配体柱结合导致富集率降低。
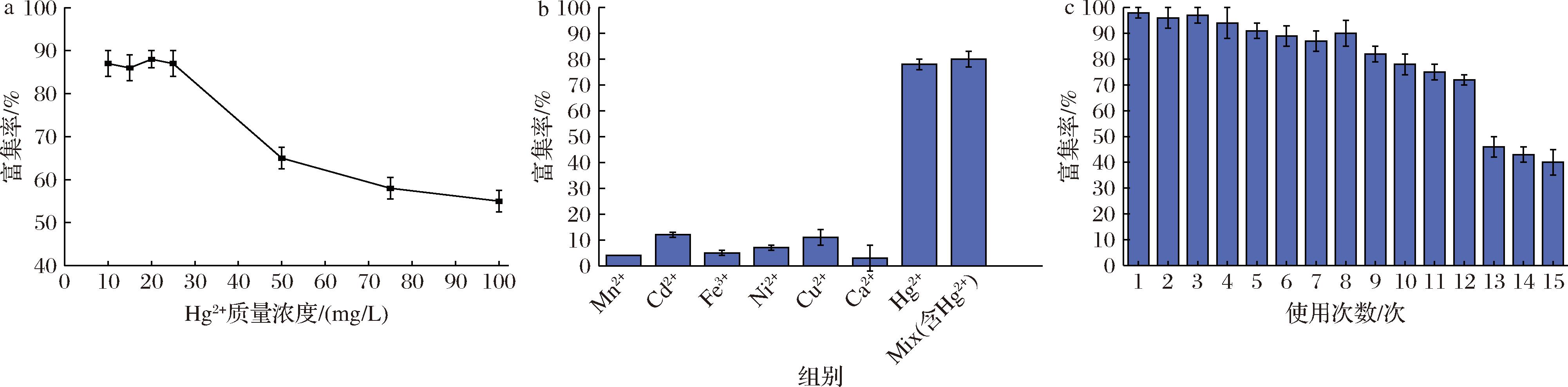
a-适配体亲和柱的柱容量;b-适配体亲和柱特异性验证;c-适配体亲和柱的再生性
图3 Hg2+适配体亲和柱的柱容量、特异性与再生性考察
Fig.3 The column capacity, specificity and regeneration of the as-prepared aptamer affinity column
2.4 Hg2+适配体亲和柱的特异性考察
通过验证适配体亲和柱与Hg2+、混合重金属溶液和其他重金属溶液(Ca2+、Cd2+、Ni2+、Fe3+、Cu2+、Mn2+)的结合特性,根据其靶标结合率,得出适配体亲和柱是否具有特异性,从而验证适配体对Hg2+的专一结合。结果如图3-b所示,适配体亲和柱对于除Hg2+以外的其他重金属表现出不与其结合,即Hg2+适配体亲和柱对Hg2+具有良好的特异性。
2.5 Hg2+适配体亲和柱的再生性考察
为了使亲和柱能够实现多次、环保、高效的利用,需要对其再生性进行考察。将制备好的适配体亲和柱与Hg2+标准液重复负载15次,采用体积分数为40%的乙腈溶液进行洗脱,每次洗脱后,适配体柱继续与Hg2+溶液结合。如图3-c所示,重复使用12次以后,富集率仍维持在70%左右,说明所制备的适配体柱至少可被重复使用12次,而不会影响亲和性适配体对目标的适应性。该亲和柱在重复使用12次后表现出明显的下降趋势,可能是因为适配体经历多次有机溶剂处理以及后续的高温变性和复性,其空间结构发生了较大的变化所致[18]。
2.6 Hg2+适配体亲和柱的吸附动力学模型拟合
为探讨吸附时间(1、5、10、20、30、40、50、60、90、120 min)对吸附量的影响,绘制动力学吸附曲线并获得拟合模型,其表达式如下:
(4)
(5)
式中:qe,平衡时Hg2+亲和柱对Hg2+的吸附量,mg/L;qt,t时刻的吸附量,mg/L;t,吸附时间,h;k1,一级吸附数率常数,min-1;k2,二级动力学常数,min-1;q1,一级动力学方程得出的理论吸附量,mg/L;q2,二级动力学方程得出的理论吸附量,mg/L。
这些模型的有效性是根据所作直线的线性来验证拟合的,对ln(qe-qt)对![]() 和对t分别作图,得到一级动力学曲线和二级动力学曲线。
和对t分别作图,得到一级动力学曲线和二级动力学曲线。
将实验数据带入吸附动力学的公式中,其中k值、相关系数R2及理论饱和吸附量见表2。
表2 Hg2+适配体亲和柱的吸附动力学参数
Table 2 Adsorption kinetics parameters of mercury ion ligand affinity column
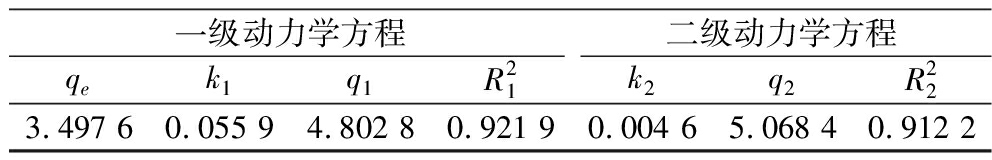
一级动力学方程二级动力学方程qek1q1R21k2q2R223.497 60.055 94.802 80.921 90.004 65.068 40.912 2
根据表格比较得出,Hg2+适配体亲和柱吸附的过程与一级吸附动力学模型相符。
2.7 Hg2+适配体亲和柱的吸附等温线模型探讨
吸附等温线是用于描述在特定温度下,Hg2+亲和柱饱和吸附容量和Hg2+平衡浓度关系的曲线。Langmuir方程和Freundlich方程是其中常见的两种吸附等温线数学模型。
其表达式分别如下:
(6)
(7)
式中:ρe,吸附平衡后溶液中的Hg2+质量浓度,mg/L;qe,平衡时Hg2+亲和柱对Hg2+的吸附量,mg/L;Qmax,Hg2+亲和柱对Hg2+的最大吸附量,mg/L;KL,Langmuir方程常数,其值越大表示吸附剂的吸附性能越强;KF和n,Freundlich方程常数。
Langmuir方程中以对![]() 对Ce做直线,
对Ce做直线,![]() 和
和![]() 分别是直线的截距和斜率,由此可计算出Qmax和KL。
分别是直线的截距和斜率,由此可计算出Qmax和KL。
Freundlich方程中以lnqe对lnCe作图,可计算出Freundlich常数,其中KF即理论饱和吸附量(mg/g),n值越大表明吸附剂的吸附性能越好。
将实验数据带入吸附等温线的公式中,Langmuir方程和Freundlich方程的参数计算如表3。
表3 Hg2+适配体亲和柱的吸附等温线参数
Table 3 Adsorption isotherm parameters of mercury ion adapter affinity column
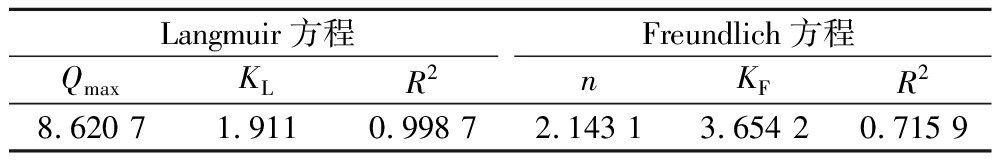
Langmuir方程Freundlich方程QmaxKLR2nKFR28.620 71.9110.998 72.143 13.654 20.715 9
数据说明Hg2+适配体亲和柱对Hg2+有较好的吸附效果。由Langmuir等温模型和Freundlich等温模型的拟合相关系数可知,在实验条件下,Langmuir方程的相关系数更大,Hg2+适配体亲和柱的吸附行为更加符合Langmuir等温吸附模型。
2.8 实际样品中Hg2+的脱除分析与营养组分的流失比对
首先采用ICP-MS对鱼露样品进行测定,结果未检出Hg2+,随后在样品中加入一定量Hg2+,过适配体亲和柱,考察所制备亲和柱对Hg2+的脱除效果,结果如表4所示,所制备亲和柱对鱼露样品中Hg2+的脱除率达70%~80%。进而根据国标方法对样品前后的营养成分进行检测。结果如表5所示,鱼露样品经适配体亲和柱处理后,其含有的全氮和氨基酸态氮并没有明显损失,说明制备的适配体亲和柱可实现对样品中Hg2+的脱除且不影响其营养价值。
表4 实际样品的加标分析
Table 4 Standard analysis of actual samples

鱼露样品加样量/(mg/L)检测浓度/(mg/L)Hg2+富集率/%10.50.41±0.0282.00±4.0021.51.21±0.0580.67±3.3335.04.05±0.1681.16±3.24
表5 实际样品的营养成分的前后变化
Table 5 Changes in the nutritional composition of the actual sample before and after
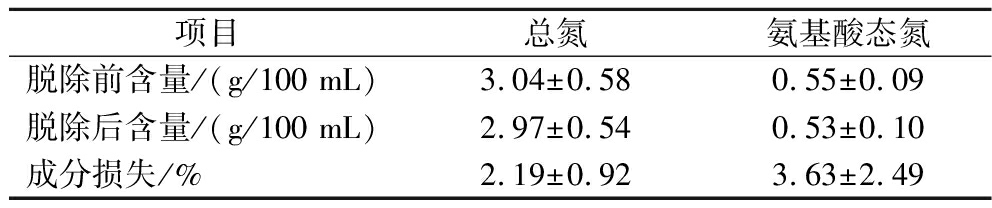
项目总氮氨基酸态氮脱除前含量/(g/100 mL)3.04±0.580.55±0.09脱除后含量/(g/100 mL)2.97±0.540.53±0.10成分损失/%2.19±0.923.63±2.49
3 结论与讨论
本文首次制备了Hg2+适配体亲和柱,鉴于适配体的高亲和力和高稳定性,该亲和柱可实现对水产品中Hg2+的高效富集,且对水产品中其他营养成分没有影响。因此,此适配体亲和柱对于水产品中Hg2+的去除具有良好的应用前景。对于未来食品中其他重金属元素的脱除,适配体亲和柱的开发对其不破坏营养组分的高效去除方法具有很高的使用价值。
[1] 蔡树英. 口腔科汞污染及其防护[J].广东牙病防治, 2000, 8(S1):428.CAI S Y.Mercurial pollution in oral medicine and its protection[J].Journal of Prevention and Treatment for Stomatological Diseases, 2000, 8(S1):428.
[2] 刘永懋. 中国松花江甲基汞污染防治与标准研究[M].北京:科学出版社, 1998.LIU Y M. Research on the Prevention and Control and Standards of Methyl Mercury Pollution in Songhua River, China[M]. Beijing: Science Press, 1998.
[3] SCHARTUP A T, QURESHI A, DASSUNCAO C, et al.A model for methylmercury uptake and trophic transfer by marine plankton[J].Environmental Science &Technology, 2018, 52(2):654-662.
[4] 王婷婷. 低氧对鱼体甲基汞生物富集的影响[D].武汉:华中农业大学, 2022.WANG T T.Effects of hypoxia on the bioaccumulation of methylmercury in fish[D].Wuhan:Huazhong Agricultural University, 2022.
[5] 李公海, 沈崇钰, 吴斌, 等.原子荧光法同时测定水产品中砷和汞[J].现代科学仪器, 2007(2):100-102.LI G H, SHEN C Y, WU B, et al.Simultaneous determination of arsenic and mercury in aquatic products by atomic fluorescence spectrometry[J].Modern Scientific Instruments, 2007(2):100-102.
[6] 赵健, 张林楠, 宋青岳, 等.水体中汞及其形态检测方法的研究进展[J].环境保护前沿, 2021, 11(2):243-251.ZHAO J, ZHANG L N, SONG Q Y, et al.Research progress on the detection method of mercury and its species in water[J].Advances in Environmental Protection, 2021, 11(2):243-251.
[7] HUA K, XU X L, LUO Z P, et al.Effective removal of mercury ions in aqueous solutions:A review[J].Current Nanoscience, 2020, 16(3):363-375.
[8] IFTHIKAR J, JIAO X, NGAMBIA A, et al.Facile one-pot synthesis of sustainable carboxymethyl chitosan-sewage sludge biochar for effective heavy metal chelation and regeneration[J].Bioresource Technology, 2018, 262:22-31.
[9] GHODBANE I, HAMDAOUI O.Removal of mercury(II) from aqueous media using Eucalyptus bark:Kinetic and equilibrium studies[J].Journal of Hazardous Materials, 2008, 160(2-3):301-309
[10] URGUN-DEMIRTAS M, BENDA P L, GILLENWATER P S, et al.Achieving very low mercury levels in refinery wastewater by membrane filtration[J].Journal of Hazardous Materials, 2012, 215:98-107.
[11] 卜凡玲, 纪春暖, 张秀娟, 等.聚苯乙烯负载双亚砜及三乙烯四胺螯合树脂的合成及其对Hg2+的吸附性能研究[J].离子交换与吸附, 2015, 31(6):505-513.BU F L, JI C N, ZHANG X J, et al.Polystyrene-supported chelating resins containing bis(sulfoxide and triethylene tetramine):Synthesis, characterization and adsorption properties for Hg2+[J].Ion Exchange and Adsorption, 2015, 31(6):505-513.
[12] 王嫦嫦, 郑思洁, 战艺芳, 等.结合纳米材料的适配体传感器在重金属检测中的应用研究进展[J].食品与发酵工业, 2021, 47(8):283-289.WANG C C, ZHENG S J, ZHAN Y F, et al.Research progress of aptasensors combined with nanomaterials in heavy metal detection[J].Food and Fermentation Industries, 2021, 47(8):283-289.
[13] 吕辰, 李钰金, 宋明燕, 等.基于核酸适配体-SYBR Green Ⅰ快速检测金刚烷胺的荧光传感技术[J].食品与发酵工业, 2021, 47(22):249-253.LYU C, LI Y J, SONG M Y, et al.Rapid detection of amantadine by fluorescence sensing technology based on nucleic acid aptamer-SYBR Green Ⅰ[J].Food and Fermentation Industries, 2021, 47(22):249-253.
[14] 宋亚宁, 胡超琼, 霍秋宇, 等.基于核酸适配体识别-时间分辨荧光共振能量转移检测牛奶中培氟沙星兽药残留[J].食品与发酵工业, 2021, 47(7):244-250.SONG Y N, HU C Q, HUO Q Y, et al.Detection of pefloxacin residue in milk based on aptamer recognizing and time-resolved fluorescence resonance energy transfer assay[J].Food and Fermentation Industries, 2021, 47(7):244-250.
[15] 赵颖, 王楠, 高华龙, 等.核酸适配体亲和柱净化-高效液相色谱法测定莲子中黄曲霉毒素B1[J].分析化学, 2020, 48(5):662-669.ZHAO Y, WANG N, GAO H L, et al.Determination of aflatoxin B1 in Lotus seed by high performance liquid chromatography with aptamer affinity column for purification and enrichment[J].Chinese Journal of Analytical Chemistry, 2020, 48(5):662-669.
[16] WU S J, YU Q R, HE C X, et al.Colorimetric aptasensor for the detection of mercury based on signal intensification by rolling circle amplification[J].Spectrochimica Acta.Part A, Molecular and Biomolecular Spectroscopy, 2020, 224:117387.
[17] TORIGOE P H, ONO P A, KOZASA T.Hg(II) ion specifically binds with T:T mismatched base pair in duplex DNA[J].Chemistry, 2010, 16(44):13218-13225.
[18] HAJDIN C E, DING F, DOKHOLYAN N V, et al.On the significance of an RNA tertiary structure prediction[J].RNA, 2010, 16(7):1340-1349.