中国毛竹资源丰富,富含膳食纤维等营养成分。相较于竹叶黄酮,竹叶膳食纤维有关的研究少[1]。开展毛竹叶可溶性膳食纤维(soluble dietary fiber,SDF)的研究对竹资源的利用有重要意义。目前水提法、化学法等[2-3]是常用的可溶性膳食纤维的提取方法。水提法成本低廉操作简单,但提取率低。传统的酸、碱化学提取法往往会产生二次污染,且提取过程中需要使用大量试剂调节pH,造成成本的增加。因此,环保温和的螯合试剂受到广泛关注。彭昕[4]利用不同方法提取雷竹SDF,发现几种化学试剂中螯合剂六偏磷酸钠的提取率最高。为了提升提取率,六偏磷酸钠也常与其他方法联合,例如CHEN等[5]利用微波辅助六偏磷酸钠从马铃薯浆中提取可溶性膳食纤维,相较于单一法更高效;何玉凤等[6]利用L-抗坏血酸结合六偏磷酸钠浸提法制备马铃薯渣水溶性膳食纤维,提取率高于六偏磷酸钠法。
蒸汽爆破利用蒸汽瞬间释放原理实现爆炸,不会造成任何污染且操作方式简捷、能耗低,因而作为对一种原料的预处理的方式在食品领域备受关注。已有文献表明,蒸汽爆破预处理可以使结构更加松散,促进可溶性膳食纤维的释放并提升其功能性质[7],与酸、碱、酶等方法结合后更是进一步提升了SDF产率与品质,XI等[8]探究了蒸汽爆炸辅助超声、柠檬酸、NaOH和纤维素酶处理对高原大麦麸可溶性膳食纤维特性的影响并发现几种联合方法具有不同优势。同理推测蒸汽爆破辅助六偏磷酸钠法也能提升SDF品质,并且在六偏磷酸钠的影响下保持高提取率,然而蒸汽爆破与六偏磷酸钠法联合提取SDF的研究鲜见报道。为此,论文以毛竹竹叶为原料,研究热水浸提法、蒸汽爆破法、六偏磷酸钠法、蒸汽爆破预处理联合六偏磷酸钠法提取毛竹叶可溶性膳食纤维的提取率及其单糖组成、粒径、zeta-电位、微观结构、晶体结构、光谱特征等结构特性和葡萄糖吸附能力、胆固醇吸附能力、抗氧化能力等功能特性,以期为竹叶资源开发利用提供新思路。
1 材料与方法
1.1 材料与试剂
毛竹叶,采自湖州市德清县;H2SO4、NaOH、六偏磷酸钠、乙酸、95%乙醇、H2O2、FeSO4、水杨酸,国药集团化学试剂有限公司;邻苯二甲醛、DPPH、磷酸盐缓冲溶液(pH=7),上海阿拉丁生化科技股份有限公司;DNS,杭州钠镁科技有限公司。以上试剂均为分析纯。
1.2 仪器与设备
SEF01粉碎机,浙江苏泊尔有限公司;SCIENTZ-12N冷冻干燥机,宁波新芝生物科技股份有限公司;UV759紫外分光光度计,上海奥普勒仪器有限公司;Gemini 500蔡司扫描电镜,德国Carl Zeiss;X’Pert PRO X射线衍射仪,荷兰PANalytical公司;Zetasizer Nano粒度电位仪,英国Malvern公司;QB-300型蒸汽爆破装置,苏州嘉成启宝装备科技有限公司;Nicolet6700傅里叶红外光谱、Thermo ICS 5000+离子色谱系统,美国Thermo Fisher Scientific公司。
1.3 毛竹叶可溶性膳食纤维的提取
1.3.1 预处理
将采集的新鲜毛竹叶用清水洗涤数次以去除表面灰尘,随后在阳光下自然晒干。将晒干的毛竹叶随机均分成4份,其中2份进行蒸汽爆破预处理(将毛竹叶放入预热完毕后的蒸汽爆破机的汽爆缸中,合盖通入高温饱和蒸汽,在1.5 MPa下维压180 s,在距离爆破终点还有3 s时,打开阀门瞬间泄压)。完成预处理后,4份毛竹叶均用高速粉碎机粉碎至80目,聚乙烯袋保存备用。
1.3.2 热水浸提工艺(W)
称取毛竹叶100 g,按料液比1∶20加入蒸馏水,在80 ℃的水浴中加热并搅拌3 h,抽滤取上清液并浓缩至1/3,加入95%(体积分数,下同)的乙醇静置过夜,离心取出沉淀,复溶后冷冻干燥,最终得到竹叶可溶性膳食纤维。
1.3.3 蒸汽爆破预处理后热水浸提工艺(SE)
称取经过蒸汽爆破预处理后的毛竹叶100 g,后续步骤按照1.3.2节进行。
1.3.4 六偏磷酸钠提取工艺(C)
称取毛竹叶100 g,按料液比1∶20加入2%(质量分数)六偏磷酸钠溶液并调节pH值至6.5,在60 ℃的水浴中加热并搅拌3 h,后续步骤按照1.3.2节进行。
1.3.5 蒸汽爆破预处理后六偏磷酸钠提取工艺(SEC)
称取经过蒸汽爆破预处理后的毛竹叶100 g,后续步骤按照1.3.4节进行。
1.4 可溶性膳食纤维提取率测定
按照1.3节提取出4组SDF,称量提取物质量并按照公式(1)计算4组工艺的提取率:
提取率![]()
(1)
式中:m1,干燥后竹叶SDF粗提物质量,g;m2,称取竹叶粉的质量,g。
1.5 结构特征分析
1.5.1 单糖组分分析
称取适量可溶性膳食纤维样品置于干净的色谱瓶,加入1 mL 2 mol/L 三氟乙酸溶液,121 ℃加热2 h。通N2,吹干。加入甲醇清洗并吹干,重复2~3次。加入无菌水溶解,转入色谱瓶中待测。采用DionexTM CarboPacTM PA20(150 mm×3.0 mm,10 μm)液相色谱柱;进样量为5 μL。流动相A(H2O),流动相B(0.1 mol/L NaOH),流动相C(0.1 mol/L NaOH,0.2 mol/L CH3COONa),流速0.5 mL/min;柱温为30 ℃。
1.5.2 粒径、zeta-电位
取适量提取的样品,用pH值为7的5 mol/L磷酸盐缓冲液进行稀释,使用粒度电位仪测定粒径和多分散指数(polydispersity index,PDI)与zeta-电位。
1.5.3 电镜的测定
使用扫描电镜仪观察可溶性膳食纤维样品的微观结构,从而比较研究几组提取工艺对竹叶可溶性膳食纤维微观结构的影响。具体方法如下:分别取少量的干燥样品,借助专用导电胶将其粘贴到一个固定的样品台上,喷金200 s,利用扫描电镜仪观察SDF并记录微观结构图。
1.5.4 X-射线衍射的分析
根据文献[9]设置扫描速度、角度、电压和电流,收集数据并作图。
1.5.5 红外光谱的分析
精确称取2 mg冻干的竹叶可溶性膳食纤维样品和200 mg干燥好(105 ℃条件下干燥3 h)的KBr粉末。将样品和KBr粉末充分混合,压片处理后,使用傅里叶变换红外光谱仪进行测量,测量的波长范围为400~4 000 cm-1。
1.6 功能特性分析
1.6.1 葡萄糖吸附能力(glucose adsorption capability,GAC)的测定
参考沈琳[10]的方法并稍作修改,称取0.1 g的样品于50 mL的离心管中,加入10 mL的50 mmol/L的葡萄糖溶液,37 ℃下反应5 h。吸附平衡后,采用DNS法测定上清液中葡萄糖含量。以蒸馏水代替葡萄糖溶液作为对应样品的空白组,540 nm处下测定吸光度。按照公式(2)换算GAC:
(2)
式中:n1,原溶液葡萄糖的量,mmol;n2,吸附后上清液葡萄糖的量,mmol;m,称取的SDF的质量,g。
1.6.2 胆固醇吸附能力(cholesterol adsorption capacity,CAC)的测定
参考沈琳[10]的方法,取新鲜蛋黄1枚,加9倍质量的蒸馏水,搅拌成乳状。再取0.5 g样品粉末和50 mL蛋黄溶液在离心管中充分混合,分别调节pH值为2、7,离心管在37 ℃振荡2 h后离心。采用邻苯二甲醛法测定溶液中胆固醇含量,在550 nm处测定吸光值,取未加入SDF的稀释鸡蛋作为对照,根据公式(3)换算CAC:
(3)
式中:m,称取的SDF质量,g;ρ1,对照组蛋黄液中胆固醇质量浓度,mg/mL;ρ2,经过SDF吸附后的蛋黄液中胆固醇质量浓度,mg/mL;V,蛋黄液体积,mL。
1.6.3 抗氧化能力的测定
1)清除DPPH自由基能力:参考郭娅[11]的方法并稍做修改,用去离子水将SDF样品稀释为1.0、2.0、3.0、4.0、5.0、6.0 mg/mL,吸取SDF溶液和DPPH-乙醇溶液各2 mL并混合,同时吸取SDF溶液和乙醇溶液2 mL并混合,混合溶液在室温下避光30 min,在517 nm处测定吸光度,蒸馏水与DPPH-乙醇溶液混合液的吸光度为空白对照,按照公式(4)计算DPPH自由基清除率。以维生素C溶液吸光值作阳性对照,比较各组SDF样品的清除DPPH自由基的能力。
DPPH自由基清除率![]()
(4)
式中:A1,2 mL SDF稀释溶液与2 mL DPPH-乙醇溶液在517 nm处的吸光度;A2,2 mL SDF稀释溶液与2 mL乙醇在517 nm处吸光度;A0,2 mL DPPH-乙醇溶液与2 mL蒸馏水在517 nm处的吸光度。
2)清除羟自由基能力:参考郭娅[11]的方法,以去离子水将SDF样品稀释为1.0、2.0、3.0、4.0、5.0、6.0 mg/mL,取1.0 mL各待测样液,加15 mL 4.5 mmol/L FeSO4溶液,5.0 mL H2O2溶液(0.5%,体积分数),0.5 mL 9 mmol/L水杨酸溶液,37 ℃水浴加温20 min,离心并取上清液,510 nm处测量吸光度。同时,用去离子水分别代替水杨酸与SDF稀释液溶液,测定吸光值。按照公式(5)计算羟自由基清除率。以维生素C溶液为阳性对照,比较各组SDF样品的清除羟自由基的能力。
羟自由基清除率![]()
(5)
式中:A0,以去离子水代替SDF稀释液时溶液的吸光度;Aa,加SDF稀释液的吸光度;Ab,以去离子水溶液代替水杨酸时溶液的吸光度。
1.7 数据处理与分析
本实验数据采用Excel 2021软件进行处理,采用Origin 2017软件绘图,使用SPSS Statistics 26软件分析数据,所有实验重复3次,实验结果以平均值±标准差表示。
2 结果与分析
2.1 可溶性膳食纤维提取率
不同方式提取毛竹叶中的SDF的提取率有明显差异(图1)。W、SE、C、SEC的提取率分别是(2.95±0.29)%、(5.24±0.33)%、(45.20±1.67)%、(51.15±1.38)%。W组作为传统的可溶性膳食纤维提取方法,提取率最低。SE、C、SEC提取率依次上升,SE组提取率上升归因于蒸汽爆破有利于竹叶细胞壁的破坏与纤维间氢键的断裂,增加了SDF的溶解和扩散。C组提取率上升是由于六偏磷酸钠溶液水解形成的正磷酸根离子与细胞壁中被束缚的SDF(如果胶多糖)发生了螯合作用,从而使SDF游离出来,溶于水中增加了提取率。另外,C组溶液体系呈弱酸性,可能导致不溶性的纤维素和半纤维素水解为可溶性糖,进一步提高了提取液中SDF含量。SEC组提取率在4组中最高,这个结果与XI等[8]发现的蒸汽爆破辅助柠檬酸/NaOH能进一步提高提取率的研究结论相一致,归因于蒸汽爆破预处理后破坏了物料物理结构,释放SDF的同时,使六偏磷酸钠更容易渗透进物料内部,从而进一步提升提取率。
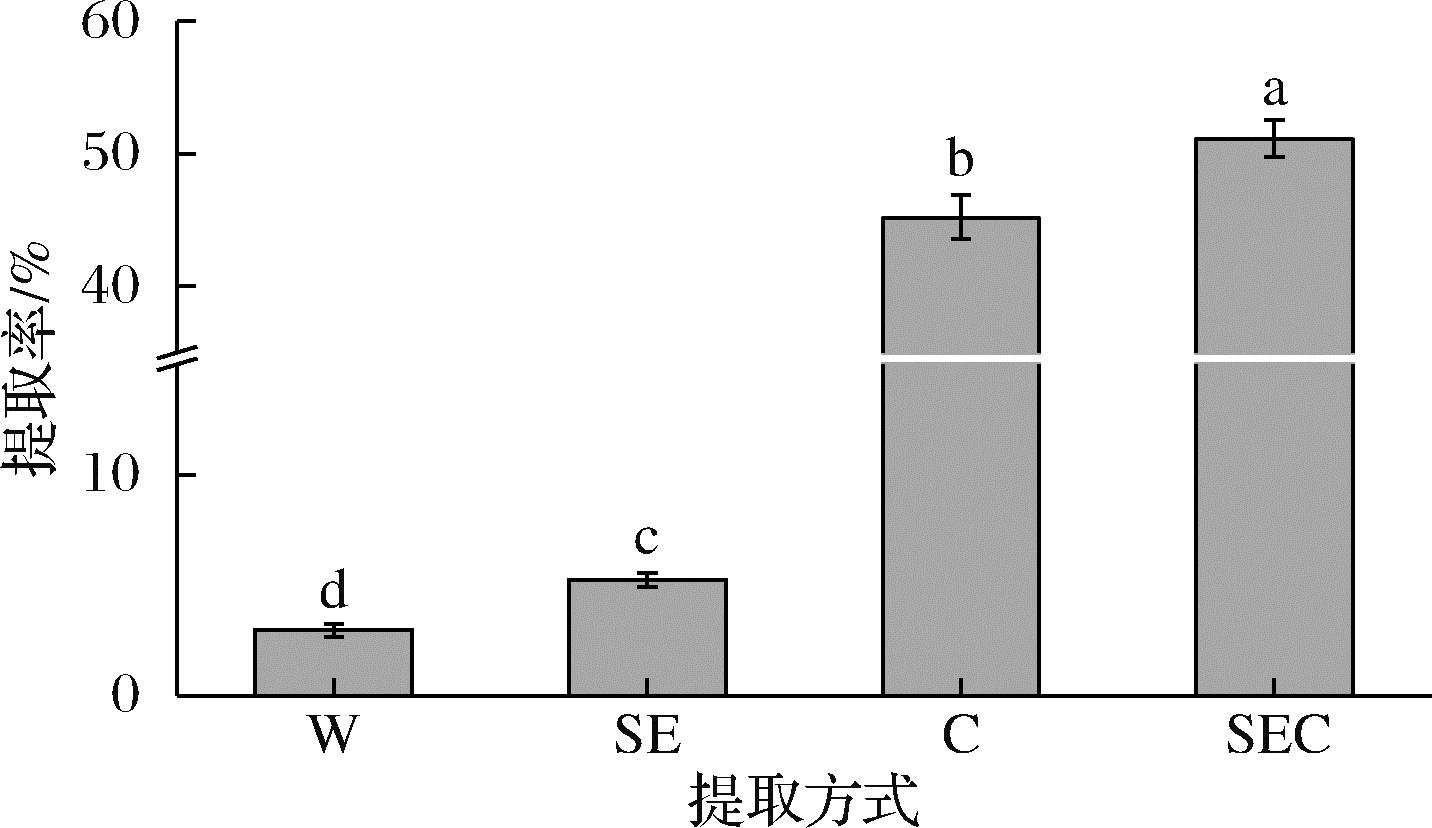
图1 不同提取方式对竹叶SDF的提取率的影响
Fig.1 Effects of different extraction methods on the extraction rate of SDF from bamboo leaves
注:不同小写字母表示差异显著(P<0.05)(下同)。
2.2 单糖组成分析
不同提取方式下竹叶SDF的单糖组成变化明显,检出的单糖类型为阿拉伯糖、半乳糖、葡萄糖、木糖、甘露糖、鼠李糖、岩藻糖、葡萄糖醛酸,以上单糖在W、SE组均被检出,而C组未检出鼠李糖、岩藻糖与葡萄糖醛酸,SEC组则未检出岩藻糖与葡萄糖醛酸(表1),所有SDF均以阿拉伯糖、半乳糖、葡萄糖、木糖为主。许多文献已证实,蒸汽爆破可以明显增加半纤维素降解产物的比例[8-9,12]。因而推测SE组与SEC组相较于W组木糖明显上升的原因来自于蒸汽爆破,蒸汽爆破处理将半纤维素降解为低聚木糖、木糖、甘露糖等。而其他糖成分可能进一步降解为单糖或小分子产物,而这些产品不能被乙醇沉淀,最后造成蒸汽爆破处理下阿拉伯糖、葡萄糖、半乳糖的下降。而SEC组相较于SE组的木糖占比更高归因于与热水相比,木糖更易溶于六偏磷酸钠。以上结果与ZHAO等[12]利用蒸汽爆破及酶处理苹果渣时其可溶性膳食纤维单糖变化相似。C组则是葡萄糖占比突出,这可能是由于大量纤维素、半纤维素在六偏磷酸钠作用下被水解为小分子葡萄糖。同时C组不含葡萄糖醛酸且木糖占比小,归因于被降解半纤维素的水解产物中,相较阿拉伯糖,木糖与葡萄糖醛酸难溶出[13-14]。葡萄糖醛酸是半纤维素侧链上常见的基团,W、SE组的葡萄糖醛酸可能来自可溶性半纤维素。
表1 不同提取方式下竹叶SDF的单糖组成 单位:mol%
Table 1 The monosaccharide composition of SDF from bamboo leaves under different extraction methods
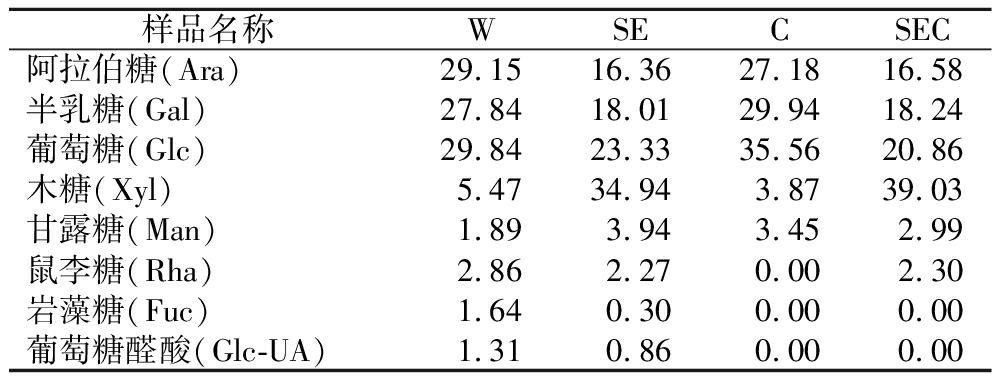
样品名称WSECSEC阿拉伯糖(Ara)29.1516.3627.1816.58半乳糖(Gal)27.8418.0129.9418.24葡萄糖(Glc)29.8423.3335.5620.86木糖(Xyl)5.4734.943.8739.03甘露糖(Man)1.893.943.452.99鼠李糖(Rha)2.862.270.002.30岩藻糖(Fuc)1.640.300.000.00葡萄糖醛酸(Glc-UA)1.310.860.000.00
2.3 粒径、zeta-电位
如图2所示,SEC、C、SE、W的粒径依次减小,zeta-电位的绝对值依次增大。W组提取的SDF的平均粒径约622.47 nm。根据电镜、红外结果,蒸汽爆破与六偏磷酸钠对SDF的结构有不同程度的影响,因而不同组别之间的粒径、zeta-电位存在差异。SE组与C组的粒径均减小,分别为579.47、552.13 nm,联合法SEC组粒径最小,为434.90 nm。同样,反映粒度均匀性的PDI、反映颗粒之间相互排斥或吸引力的强度的zeta-电位的绝对值都是SEC组最突出。以上结果说明蒸汽爆破能减小粒径,增大zeta-电位值,这与孙金淏等[7]研究结论相符。六偏磷酸钠对粒径、zeta-电位的作用也有相关报道[15]。且两者联合时由于协同作用效果更佳。粒径越小,比表面积越大,SDF的物化、生理特性,如吸附性等越佳。同样的,zeta-电位绝对值的增大,颗粒之间静电斥力增大,其溶液不易于絮凝,因此SEC组的SDF是后续应用的最佳选择。
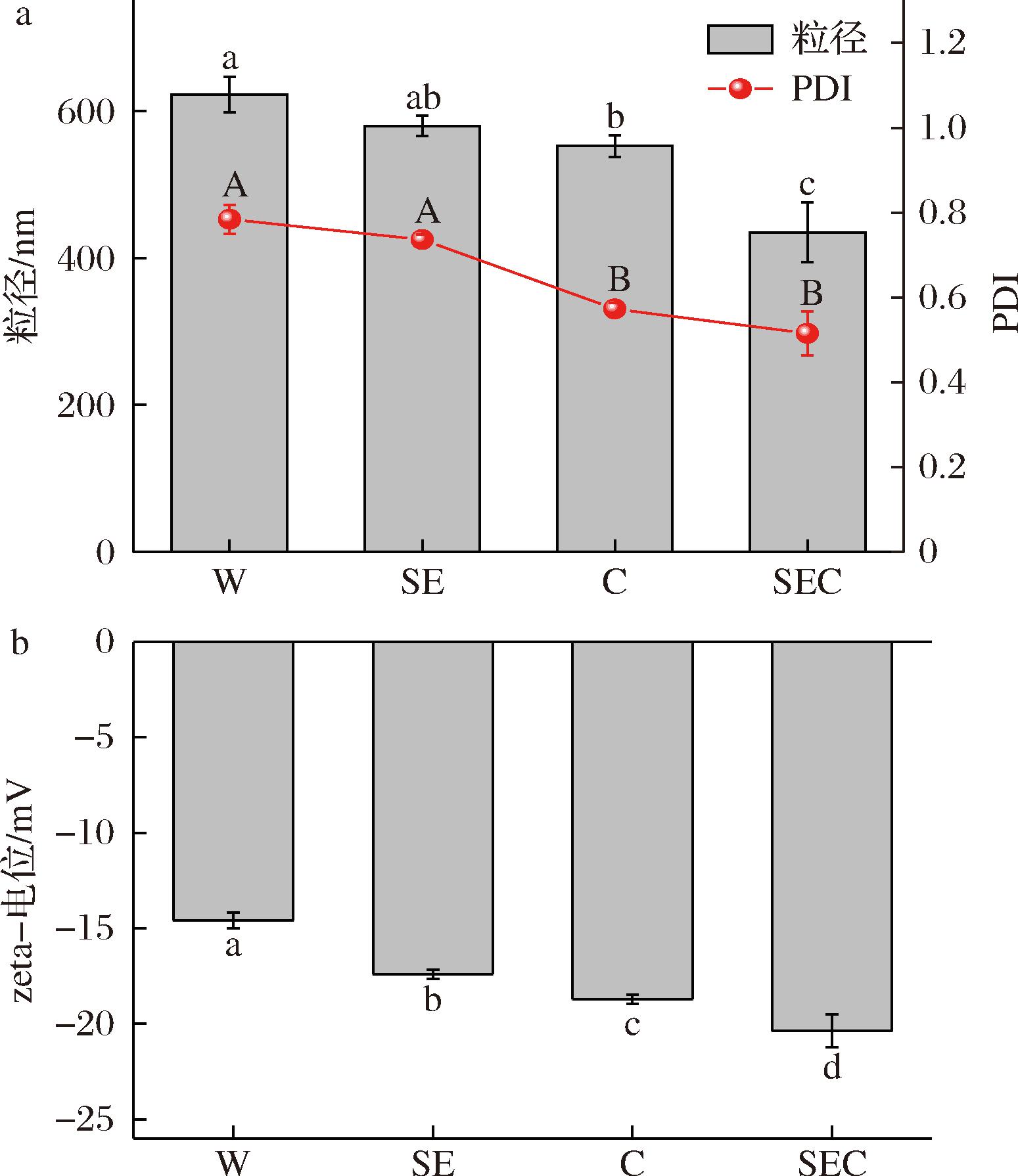
a-粒径;b-zeta-电位
图2 不同提取方式对竹叶SDF粒径、zeta-电位的影响
Fig.2 Effects of different extraction methods on SDF particle size and zeta-potential of bamboo leaves
注:不同大写字母代表差异显著,P<0.05(下同)。
2.4 电镜观察
在25 000倍放大条件下,选取较为完整的SDF颗粒,观察其内部结构。图3显示了各组的扫描电镜结果,SE组与W组形态相同,都呈现颗粒海绵状,C组结构形态与其他几组完全不同,呈片层结构,SEC组则更为复杂不规则。W组颗粒相对均匀,结构致密,说明水提法反应最为温和。SE组的SDF颗粒膨胀且不均匀,结构相对松散,蜂窝状孔隙增大,这归因于蒸汽爆破预处理破坏了纤维之间的紧密交联,同时这也解释了SDF产量的增加的现象。C组孔隙收缩,有一定程度的颗粒团聚,这种效应可能是由于六偏磷酸钠处理减少了纤维的粒径,增加了比表面积,同时增强了膳食纤维分子之间的相互作用,导致聚集[14]。SEC组的SDF表面有许多蜂窝状孔隙和碎片化物质,形状十分不规则,这表明蒸汽爆破预处理与六偏磷酸钠的联合处理加强了对竹叶的破坏,使SDF具备更大的比表面积,因而有更好的吸附能力。

a-水提SDF;b-蒸汽爆破预处理的水提SDF;c-六偏磷酸钠 处理的SDF;d-蒸汽爆破联合六偏磷酸钠处理的SDF
图3 不同提取方式下竹叶SDF形态的扫描电镜图
Fig.3 Scanning electron microscopy (SEM) of SDF morphology of bamboo leaves extracted by different methods
2.5 X-射线衍射
各组别的SDF的X-射线衍射如图4所示。所有SDF都显示为典型的非结晶聚合物的衍射图谱,其中W与SE图谱相似,均在2θ约为20°处显示出一个明显的衍射峰,而C的图谱与SEC的相似,两者在2θ为15°和30°处均各有一个峰。根据先前论文,19°~22°范围内的衍射峰是纤维素的特征结晶区,30°处的衍射峰是纤维素的无定形区域[16],说明六偏磷酸钠会改变SDF的晶体类型并产生无定形区域。此外,不同提取方式制备的SDF的衍射强度有一定差异,SE最高,SEC与W相当,C最低。
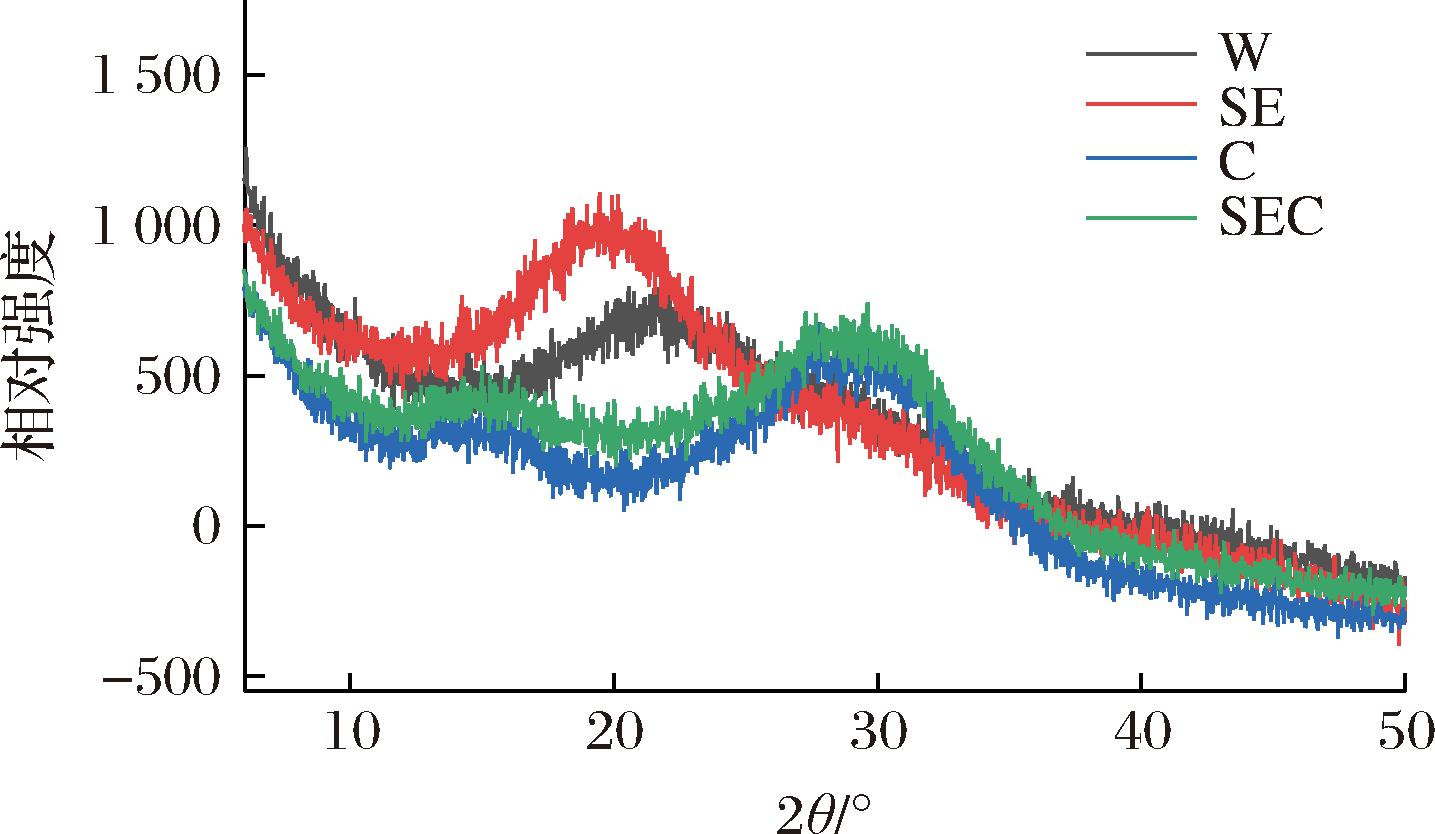
图4 不同提取方式下竹叶SDF X-射线衍射图
Fig.4 X-ray diffraction patterns of bamboo leaf SDF under different extraction methods
2.6 红外扫描
如图5所示,4种SDF大部分特征峰相似,所有SDF在3 443、1 6371 401、1 098 cm-1都有吸收峰,而C组与SEC组在1 000~800 cm-1处增加了一些新的特征峰,且在2 933 cm-1处吸收峰消失,表明六偏磷酸钠提取的SDF与水提法SDF组分不同,而蒸汽爆破提取的SDF则会保持与水提法SDF相似的物质组成,这与单糖组分测定的结果相一致。在3 443 cm-1附近的广泛吸收峰是由主要来自纤维素和半纤维素的—OH拉伸振动引起的,此处吸收峰强度SE组、C组比W组略高,表明蒸汽爆破破坏了纤维素分子之间连结,使其暴露了更多的羟基。在1 637 cm-1处表现出特征性的傅立叶变换红外光谱学吸收,归因于游离羧酸或羧酸盐C![]() O不对称拉伸振动[17-18]。1 098 cm-1代表半纤维素中醚键(C—O—C)的特征峰,而SE组在1 045.68 cm-1处出现的弱吸收峰为C—O的拉伸振动,这是一个典型的木聚糖吸收峰[8],这是因为蒸汽爆破处理降解了部分半纤维素与木质素[8,19],对应单糖组分中SE组木糖占比的增加。根据以前的研究,在1 000~1 200 cm-1的吸收峰归因于吡喃糖环中的C
O不对称拉伸振动[17-18]。1 098 cm-1代表半纤维素中醚键(C—O—C)的特征峰,而SE组在1 045.68 cm-1处出现的弱吸收峰为C—O的拉伸振动,这是一个典型的木聚糖吸收峰[8],这是因为蒸汽爆破处理降解了部分半纤维素与木质素[8,19],对应单糖组分中SE组木糖占比的增加。根据以前的研究,在1 000~1 200 cm-1的吸收峰归因于吡喃糖环中的C![]() O
O![]() C和C—OH。C组、SEC组在1 401 cm-1处的峰推测出现了红移,表明六偏磷酸钠对官能团结构有影响,与XRD结果对应。同时该现象与XI等[8]利用蒸汽爆破辅助酸处理时的红外结果相似。在993 cm-1处的吸收是表明D-吡喃葡萄糖的存在[16-17]。此外,峰值在880 cm-1处对应于β-糖苷键的拉伸振动,以上都是多糖的特征峰。而在2 933 cm-1处的峰是由C—H和CH2拉伸引起的[8,16,19],1 200~1 400 cm-1处的弱振动峰则是由C—H的变角振动引起[8]。在2 933 cm-1处吸收峰消失,表明C、SEC组纤维素多糖的氢键含量较低,其结晶区的比例远低于其他[19],在1 200~800 cm-1处C组与SEC组特征峰的增加,可能是由于糖苷键的增加,以上结果表明,六偏磷酸钠对纤维素、半纤维素的降解更彻底。此外,在521 cm-1处的吸光度表明芳香化合物(磷酸盐)的C
C和C—OH。C组、SEC组在1 401 cm-1处的峰推测出现了红移,表明六偏磷酸钠对官能团结构有影响,与XRD结果对应。同时该现象与XI等[8]利用蒸汽爆破辅助酸处理时的红外结果相似。在993 cm-1处的吸收是表明D-吡喃葡萄糖的存在[16-17]。此外,峰值在880 cm-1处对应于β-糖苷键的拉伸振动,以上都是多糖的特征峰。而在2 933 cm-1处的峰是由C—H和CH2拉伸引起的[8,16,19],1 200~1 400 cm-1处的弱振动峰则是由C—H的变角振动引起[8]。在2 933 cm-1处吸收峰消失,表明C、SEC组纤维素多糖的氢键含量较低,其结晶区的比例远低于其他[19],在1 200~800 cm-1处C组与SEC组特征峰的增加,可能是由于糖苷键的增加,以上结果表明,六偏磷酸钠对纤维素、半纤维素的降解更彻底。此外,在521 cm-1处的吸光度表明芳香化合物(磷酸盐)的C![]() O 弯曲[20]。
O 弯曲[20]。
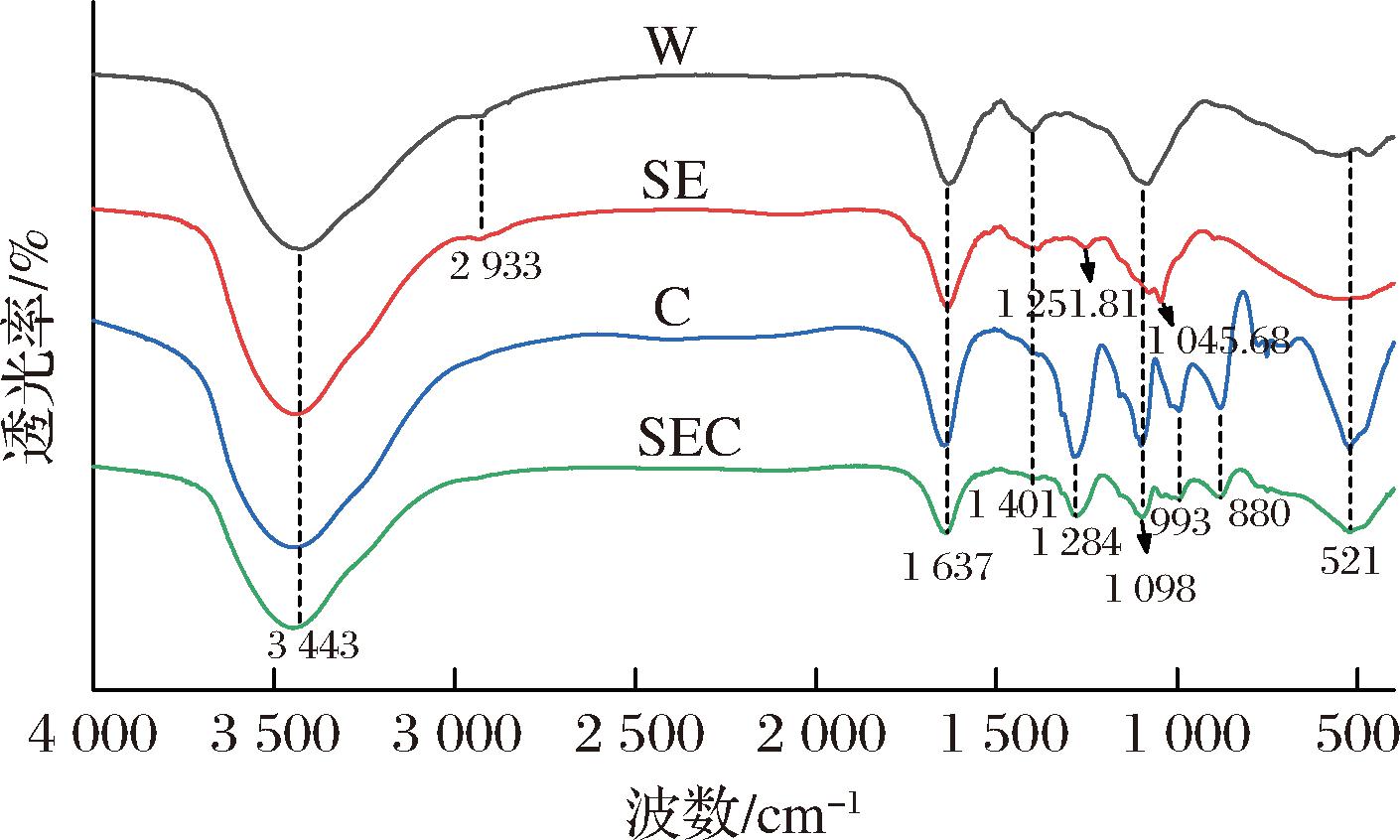
图5 不同提取方式下竹叶SDF红外光谱图
Fig.5 IR spectra of SDF from bamboo leaves with different extraction methods
2.7 葡萄糖吸附能力、胆固醇吸附能力
葡萄糖吸附能力/胆固醇吸附能力与比表面积和内部结构有关,更大的比表面积和疏松的内部结构,使可溶性膳食纤维能够暴露出更多的极性和非极性基团,有利于增强SDF与葡萄糖分子/胆固醇的相互作用,从而影响葡萄糖/胆固醇吸附能力。如图6所示,4种SDF葡萄糖吸附能力/胆固醇吸附能力依次为SEC>C>SE>W。联合法的葡萄糖吸附能力最优,可达(52.04±0.19)%,同时其胆固醇吸附能力在pH=2时可达(57.14±0.73)%,pH=7时为(62.53±5.31)%。红外分析结果中看出蒸汽爆破法或六偏磷酸钠法可以使SDF表面暴露出更多的羟基,从而增强了膳食纤维与葡萄糖/胆固醇分子之间的相互作用。同时根据电镜观察结果,蒸汽爆破与六偏磷酸钠联合作用下SDF的结构最为松散多孔,推测暴露的活性基团更多,葡萄糖/胆固醇吸附能力因而最佳,相似的结果在ZHAO等[12]的实验中出现。
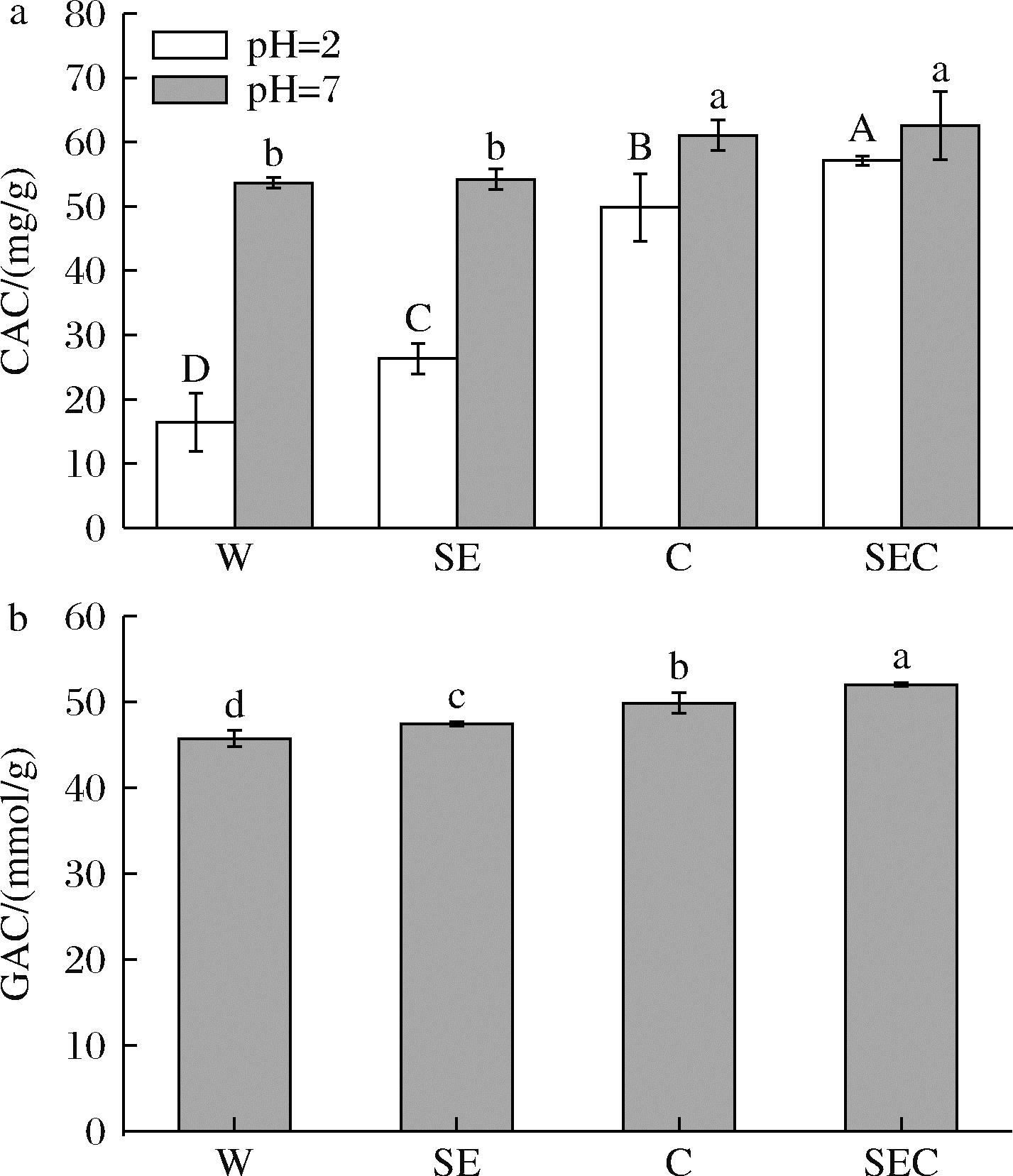
a-葡萄糖吸附能力;b-胆固醇吸附能力
图6 不同提取方式下竹叶SDF对葡萄糖吸附能力、 胆固醇吸附能力的影响
Fig.6 Effects of bamboo leaf SDF on glucose adsorption capacity and cholesterol adsorption capacity under different extraction methods
2.8 抗氧化能力
如图7所示,各组SDF的DPPH自由基清除能力和羟自由基清除能力均大致呈上升趋势,C组、SEC组的DPPH清除曲线呈“S”型,低浓度时清除率相对较低,高浓度时则高,这个结果与CHEN等[5]的实验结果相似。而W组、SE组的DPPH和羟自由基清除曲线相对平缓,对DPPH自由基表现出明显的清除作用,SE组的抗氧化能力略高于W组,这与XI等[8]的实验结果相似。几组的差异可能来自于单糖组成及其在SDF中的连接方式的不同[21]。此外,酚类物质与可溶性糖可形成协同抗氧化作用,且酚类物质的结构浓度以及与多糖之间的氢键强度都会影响协同作用的强弱[22],WU等[23]比较茶多酚、β-葡聚糖及其复合物和物理混合物之间的抗氧化区别,发现复合物对超氧自由基的清除作用最强,而混合物对羟基自由基的清除作用最强,β-葡聚糖与低质量浓度(<0.05 mg/mL)的茶多酚结合时,在DPPH清除试验中观察到协同效应,而高浓度时转变为拮抗作用。竹叶中含有丰富的酚类,而蒸汽爆破及六偏磷酸钠同样有助于提升酚类化合物的提取率[21,24]。虽然,两者都有利于酚类化合物提取,但蒸汽爆破的高温可能会导致酚类化合物发生不同程度的降解或聚合[25],综上所述,低浓度时W、SE组的DPPH自由基清除能力大于C、SEC组可能是由于低浓度时SDF与多酚的协同作用起主要作用,而蒸汽爆破组的协同作用更佳。而随着SDF浓度的增加,SDF本身抗氧化能力起主要作用。SEC组提取的SDF的抗氧化性最优,在6 mg/mL时,DPPH和羟自由基清除能力分别为95.35%、95.50%,与维生素C相当,这应当是蒸汽爆破与六偏磷酸钠共同作用的结果。
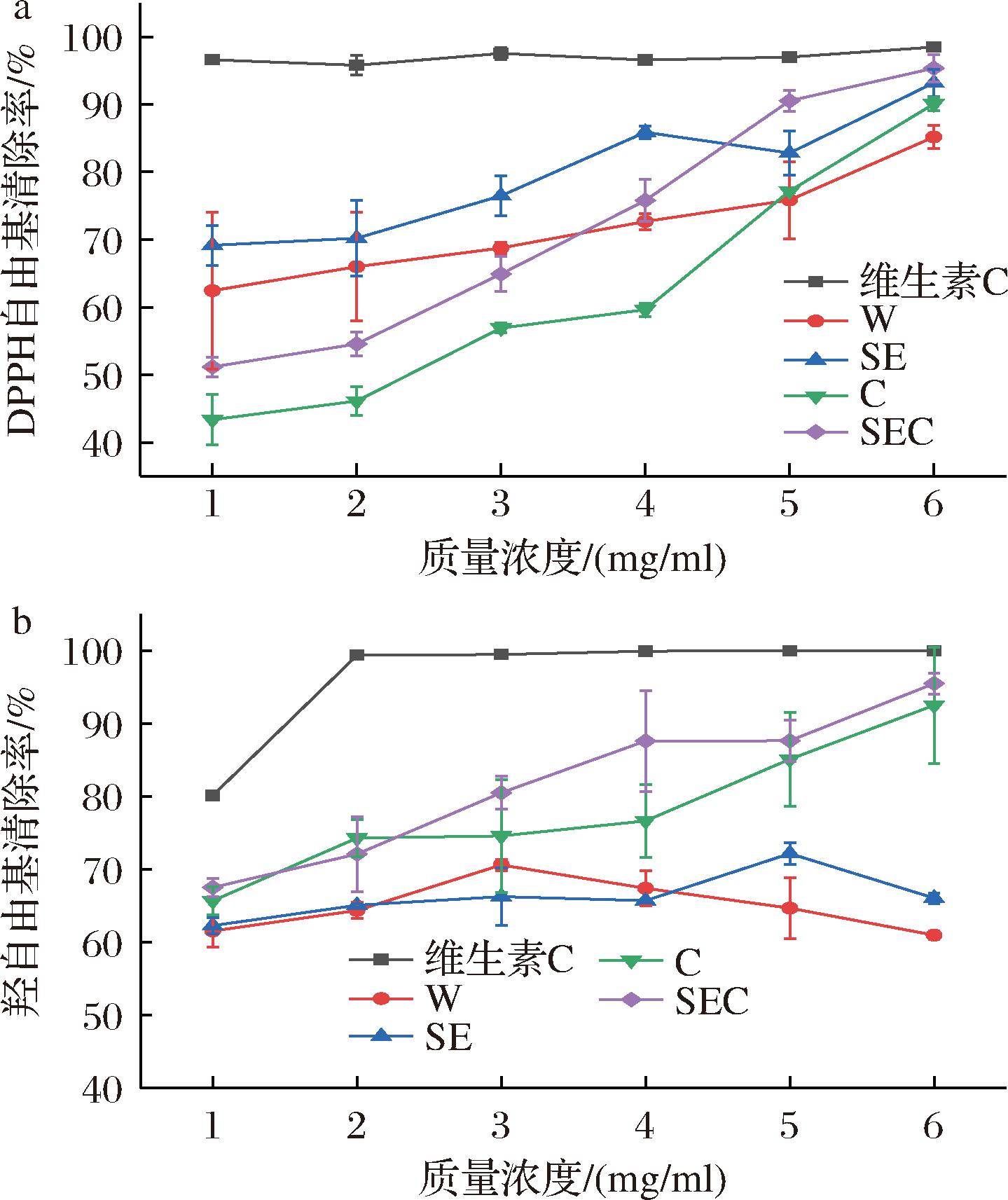
a-DPPH自由基清除能力;b-羟自由基清除能力
图7 不同提取方式下竹叶SDF对DPPH自由基清除能力、 羟自由基清除能力的影响
Fig.7 Effects of bamboo leaf SDF on DPPH radical scavenging capacity and · OH radical scavenging capacity under different extraction methods
3 结论
本文应用热水浸提法(W)、蒸汽爆破法(SE)、六偏磷酸钠法(C)、蒸汽爆破联合六偏磷酸钠法(SEC)提取毛竹叶中的SDF,探究了上述提取方式对毛竹叶SDF提取率、结构、功能性质的影响。结果表明,所有SDF的主要单糖组分均是阿拉伯糖、半乳糖和葡萄糖,W与SE单糖类型、红外光谱图、X-射线衍射图相似,C则与SEC相似。4种 SDF 中,SEC组的SDF无论是提取率还是功能性质(葡萄糖吸附能力,胆固醇吸附能力,羟自由基清除能力)都最为突出,分别为(51.15±1.38)%、(52.04±0.19)%、(57.14±0.73)%(pH=2)、(62.53±5.31)%(pH=7)、(95.50±1.46)%。SEC组的SDF与W、SE、C组相比,具有更疏松的结构、更小的粒径和更高的zeta-电位值。以上的结果表明,蒸汽爆破与六偏磷酸钠对SDF结构、组成变化造成的影响不同,两者联合可以使SDF获得了更好的吸附、抗团聚能力,因而几组SDF中SEC组有最佳的功能特性。综上所述,蒸汽爆破联合六偏磷酸钠法可作为提取毛竹叶中高品质 SDF 的有效方法,为毛竹叶资源的深度开发利用提供理论基础。
[1] 张雄. 基于赤水麻竹叶的膳食纤维制备工艺研究[D].贵阳:贵州民族大学, 2021.ZHANG X.Study on preparation technology of dietary fiber from Dendrocalamus latiflorus Munro leaves in Chishui County[D].Guiyang:Guizhou Minzu University, 2021.
[2] GAN J P, XIE L, PENG G Y, et al.Systematic review on modification methods of dietary fiber[J].Food Hydrocolloids, 2021, 119:106872.
[3] 许锡凯, 辛嘉英, 任佳欣, 等.水溶性膳食纤维的提取方法及其在食品中的应用[J].食品研究与开发, 2021, 42(4):203-208.XU X K, XIN J Y, REN J X, et al.Study on extraction method of soluble dietary fiber and its application in food[J].Food Research and Development, 2021, 42(4):203-208.
[4] 彭昕. 雷竹笋水溶性膳食纤维提取及其应用特性研究[D].长沙:中南林业科技大学, 2017.PENG X.Study on extraction methods, physicochemical and physiological functions of Phyllostachys pracecox dietary fiber[D].Changsha:Central South University of Forestry &Technology, 2017.
[5] CHEN X L, HUANG C G, JIAN R C, et al.Optimization of microwave-assisted extraction of soluble dietary fiber from potato pulp and its properties[J].Journal of Food Processing and Preservation, 2019, 43(10):e14204.
[6] 何玉凤, 张侠, 张玲, 等.马铃薯渣可溶性膳食纤维提取工艺及其性能研究[J].食品与发酵工业, 2010, 36(11):189-193.HE Y F, ZHANG X, ZHANG L, et al.Extracting technology of dietary fiber from potato pulp and its properties[J].Food and Fermentation Industries, 2010, 36(11):189-193.
[7] 孙金淏, 焦文雅, 吴超, 等.蒸汽爆破对膳食纤维的影响及应用研究进展[J].食品工业科技, 2023, 44(20):449-457.SUN J H, JIAO W Y, WU C, et al.Research progress in the effect of steam explosion on dietary fiber and its application[J].Science and Technology of Food Industry, 2023, 44(20):449-457.
[8] XI H H, WANG A X, QIN W Y, et al.The structural and functional properties of dietary fibre extracts obtained from highland barley bran through different steam explosion-assisted treatments[J].Food Chemistry, 2023, 406:135025.
[9] 唐鑫静. 蒸汽爆破对薏苡仁麸皮膳食纤维理化特性、结构及功能性质的影响[D].重庆:西南大学, 2023.TANG X J.The effect of steam explosion on the physicochemical properties,structure and functional properties of dietary fiber from adlay bran[D].Chongqing:Southwest University, 2023
[10] 沈琳. 大黄茎可溶性膳食纤维的提取、改性及其应用[D].绵阳:西南科技大学, 2022.SHEN L.Extraction, modification and application of soluble dietary fiber from rhubarb stem[D].Mianyang:Southwest University of Science and Technology, 2022.
[11] 郭娅. 红花籽粕可溶性膳食纤维的提取和生理活性研究及应用[D].邯郸:河北工程大学, 2021.GUO Y.Study on extraction technology and physiological activity of soluble dietary fiber from safflower seed meal and its application[D].Handan:Hebei University of Engineering, 2021.
[12] ZHAO Y, YU K M, TIAN X, et al.Combined modification of soluble dietary fibers from apple pomace by steam explosion and enzymatic hydrolysis to improve its structural, physicochemical and functional properties[J].Waste and Biomass Valorization, 2022, 13(12):4869-4879.
[13] 宋昕. 蒸煮中半纤维素在纤维素上的吸附特性研究[D].大连:大连工业大学, 2015.SONG X.Study on adsorption characteristics of hemicellulose on cellulose during cooking[D].Dalian:Dalian Polytechnic University, 2015.
[14] 王思远, 刘学铭, 杨晓泉, 等.交联大豆多糖的制备及性能研究[J].中国粮油学报, 2013, 28(12):33-36;46.WANG S Y, LIU X M, YANG X Q, et al.The research on preparation and characterization of cross-linked soybean polysaccharides[J].Journal of the Chinese Cereals and Oils Association, 2013, 28(12):33-36;46.
[15] THANDAPANI G, PRASAD S, SUDHA P, et al.Size optimization and in vitro biocompatibility studies of chitosan nanoparticles[J].International Journal of Biological Macromolecules, 2017, 104:1794-1806.
[16] 樊华, 刘夫国, 王玉堂, 等.球磨联合碱辅助酶法改善淡竹叶水溶性膳食纤维的物化和功能特性[J].食品科学, 2022, 43(24):74-82.FAN H, LIU F G, WANG Y T, et al.Ball milling combined with alkaline-assisted enzymatic extraction improved the physicochemical and functional properties of soluble dietary fiber from herba lophatheri[J].Food Science, 2022, 43(24):74-82.
[17] LI T G, LIU R Q, WANG T L, et al.Effects of steam explosion treatment on the physicochemical properties and biological activities of okara-derived soluble dietary fibre[J].International Journal of Food Science &Technology, 2023, 58(11):5926-5937.
[18] OUYANG H, WU L, HU Y, et al.Effect of steam explosion treatment on physicochemical, functional and structural properties of pomelo fruitlets[J].LWT, 2023, 184:114963.
[19] WU W J, HU J, GAO H Y, et al.The potential cholesterol-lowering and prebiotic effects of bamboo shoot dietary fibers and their structural characteristics[J].Food Chemistry, 2020, 332:127372.
[20] 刘玮. 大豆多糖胶的制备及其凝胶性研究[D].南昌:南昌大学, 2012.LIU W.Study of preparation and gelation capacity of soybean polysaccharide gel[D].Nanchang:Nanchang University, 2012.
[21] WAN F C, FENG C F, LUO K Y, et al.Effect of steam explosion on phenolics and antioxidant activity in plants:A review[J].Trends in Food Science &Technology, 2022, 124:13-24.
[22] WANG J Q, HU S Z, NIE S P, et al.Reviews on mechanisms of in vitro antioxidant activity of polysaccharides[J].Oxidative Medicine and Cellular Longevity, 2016, 2016:5692852.
[23] WU Z, MING J, GAO R P, et al.Characterization and antioxidant activity of the complex of tea polyphenols and oat β-glucan[J].Journal of Agricultural and Food Chemistry, 2011, 59(19):10737-10746.
[24] 杨博凯, 王志会, 张玉蕾, 等.核桃青皮多酚的六偏磷酸钠辅助提取工艺优化[J].化学与生物工程, 2022, 39(1):6-12.YANG B K, WANG Z H, ZHANG Y L, et al.Optimization in SHMP-assisted extraction of polyphenols from walnut green husk[J].Chemistry &Bioengineering, 2022, 39(1):6-12.
[25] GONG L X, HUANG L L, ZHANG Y.Effect of steam explosion treatment on barley bran phenolic compounds and antioxidant capacity[J].Journal of Agricultural and Food Chemistry, 2012, 60(29):7177-7184.