随着人们越来越重视饮食健康,全麦食品成为了大众的热点选择之一,食用全麦及其制品可有效预防肥胖、糖尿病和心血管等疾病[1]。与普通白面粉相比,全麦粉中富含膳食纤维、维生素、矿物质以及其他活性成分[2]。除此之外,因全麦粉包含麸皮和胚芽,还含有大量不饱和脂肪酸、内源性水解氧化酶以及微生物[3],这些物质在贮藏时极易导致全麦粉出现脂肪氧化降解现象,产生哈喇味,缩短货架期。贮藏过程中,全麦粉脂肪、淀粉和蛋白质之间也会相互影响,从而导致其食用品质下降,因此改善全麦粉的贮藏性能显得尤为重要。
射频处理作为一种新型热处理技术,它是通过上下两块极板产生高频交流电磁波,使电场中的样品极性分子往复旋转,带电粒子移动碰撞产热,具有加热速率快、穿透深度大、适合大体积加热等特点[4],主要应用于干燥、解冻、灭菌、灭酶、杀虫等领域。研究发现,使用射频处理小麦可以达到灭菌、灭酶及改进加工品质的效果[5-6],因此射频处理可应用于全麦粉贮藏期的延长和品质改善。然而,目前针对射频处理全麦的研究主要集中于射频处理全麦前后灭菌灭酶效果及对其品质的影响,而对射频处理全麦后制得的全麦粉在长时间的贮藏过程中品质变化的影响研究较少。为验证射频热处理技术对全麦粉的贮藏稳定性影响,研究经过射频处理的全麦粉在贮藏过程中脂肪氧化和淀粉、蛋白质结构性质的变化。同时为了优化射频处理后全麦粉的贮藏效果,在其基础上通过添加脱氧剂来进一步抑制全麦粉的氧化变质,改善其贮藏性能。
本论文将射频处理及射频后进一步脱氧处理的全麦粉在室温条件下贮藏6个月,并通过对其脂肪水解氧化相关指标(脂肪酸值、过氧化值、自由基强度)、淀粉结构性能相关指标(结晶度、短程有序性、热力学性质)以及蛋白质结构性能相关指标(巯基含量、蛋白二级结构、分子质量分布)进行检测,以探究全麦粉贮藏性能及品质是否有所改善,为射频处理技术在实际生产中的应用提供理论指导和实践基础。
1 材料与方法
1.1 材料与试剂
小麦品种为燕农15,购自青州禾益家食品有限公司(青州),于-20 ℃贮藏备用。聚乙烯(poly ethylen,PE)材质自封袋,无锡恒康医疗科技有限公司;30型脱氧剂,上海绘巢实业有限公司;5,5′-二硫代双(2-硝基苯甲酸),北京伊诺凯科技有限公司;95%乙醇、无水乙醚、三氯甲烷、冰醋酸、KOH、硫代硫酸钠滴定液、甘氨酸、盐酸胍、脲、巯基乙醇等试剂均为分析纯,国药集团化学试剂有限公司。
1.2 仪器与设备
27.12 MHz GJ-3-27-JY高频真空介质加热射频装置,河北华氏纪元高频设备有限公司;D2 PHASER X射线衍射仪、EMX plus-10/12电子自旋共振波谱仪,德国布鲁克科技有限公司;LXJ-IIB低速离心机,上海安亭科学仪器厂;PB-10型pH计,德国Sartorius公司;MSH-20A磁力搅拌器,德国明智公司;KF-25磨粉机,瑞安市康源药机有限公司;SF-400台式快速塑料封口机,合肥汉杰包装喷码有限公司;IS10傅立叶红外光谱仪,美国Nicolet公司;梅特勒DSC3+差式扫描量热仪,瑞士梅特勒-托利多公司。
1.3 实验方法
将射频处理后(样品质量500 g,极板间距135 mm,样品放置高度10 mm,目标温度85 ℃,补水1.5%,保温时间15 min)全麦磨粉过80目,贮藏全麦粉,并分为未添加脱氧剂和添加脱氧剂两种样品进行贮藏,分别记为射频组和射频脱氧组。脱氧贮藏方法为每300 g全麦粉中放入两袋30型脱氧剂,于PE自封袋中适当排除多余空气后封口贮藏,每袋脱氧剂总脱氧量≥240 mL,适用于180 g样品。未脱氧样品除未使用脱氧剂外,包装方法均同脱氧贮藏一致。贮藏条件为4~10月室内常温贮藏(图1),每60 d取样1次,共贮藏180 d,取样后放入-20 ℃冰柜备用。
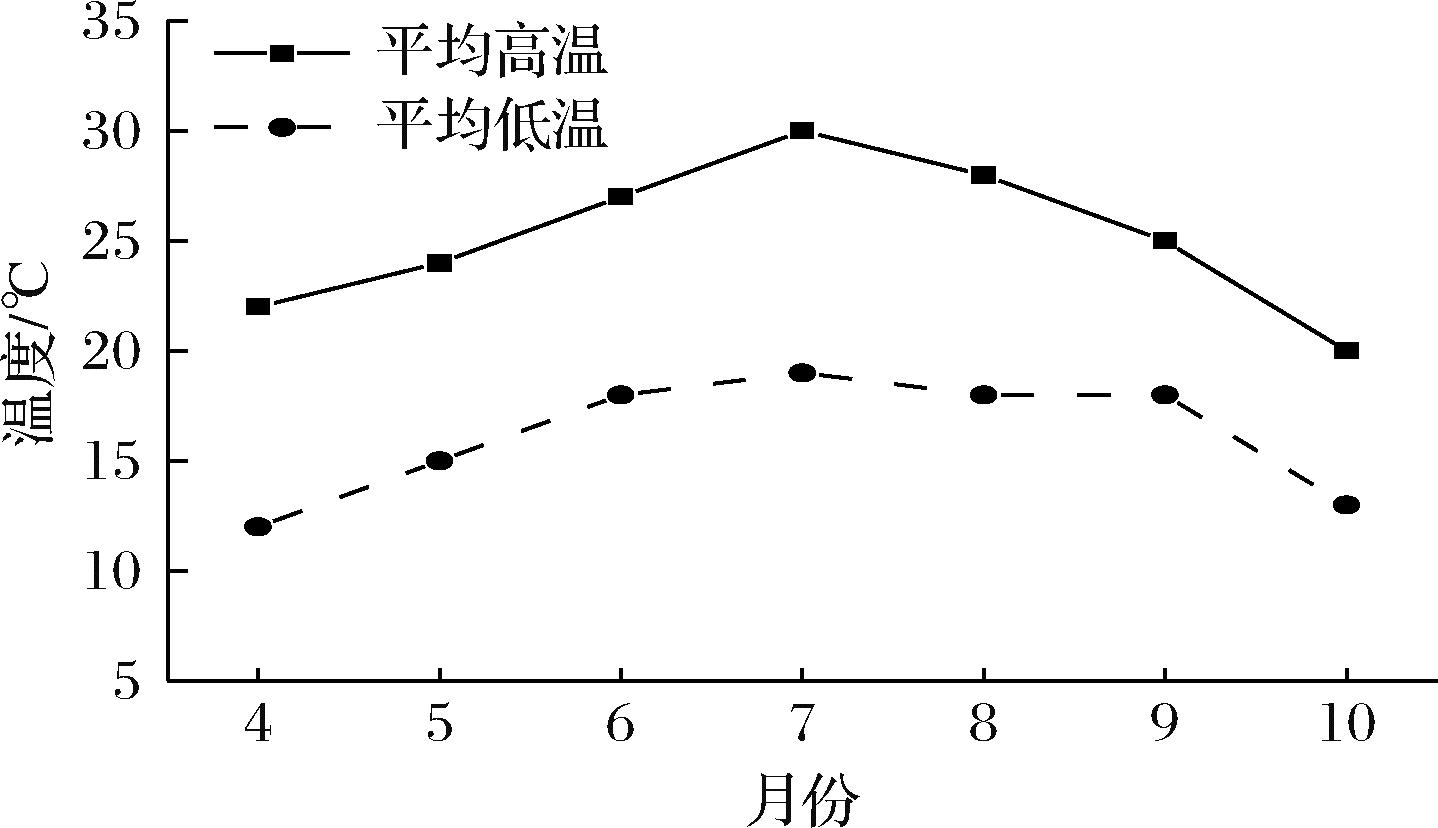
图1 无锡市2023年4月到10月的平均温度
Fig.1 Average temperature of Wuxi City from April to October 2023
1.3.1 脂肪酸值的测定
参照GB/T 15684—2015《谷物碾磨制品 脂肪酸值的测定》,并稍作修改,将以指示剂变色判断终点改为以pH=8为滴定终点进行实验。
1.3.2 过氧化值的测定
参照GB 5009.227—2023《食品安全国家标准 食品中过氧化值的测定》第一法滴定法,并稍作修改,用无水乙醚浸提24 h提取全麦粉油脂,挥发有机溶剂后测定过氧化值。
1.3.3 自由基强度的测定
称取全麦粉(60.0±0.5) mg于直径为9 mm的核磁管中。使用电子自旋共振波谱仪进行小麦粉自由基信号强度的测定。本方法条件测定以碳为中心的稳定自由基。测定条件如下:中心磁场3 370 G,扫场宽度100 G,扫描时间30 s,微波功率20 mW,g=2.000 0,水冷设定温度18 ℃。自由基信号强度用中心磁场的峰高与1 g样品(干基)质量的比值来表示。
1.3.4 结晶度变化的测定
采用X-射线衍射仪进行测定。样品前处理:将全麦粉样品装入样品片中,用载玻片压平。X-射线衍射扫描条件:管压30 kV,管流 10 mA,扫描范围5°~35°,扫描速率6°/min,步长0.05°。
1.3.5 短程有序结果的测定
采用傅里叶变换红外光谱仪测定全麦粉。扫描波数范围4 000~650 cm-1,分辨率4 cm-1,以空气为空白,扫描32次后取平均得到红外光谱图。选择波数范围1 200~800 cm-1的谱图进行去卷积,并根据1 047、1 022、995 cm-1处的峰强度,计算有序度(degree of order,DO)R1 047/1 022和双螺旋度(degree of double helicity,DD)R995/1 022。
1.3.6 热力学性质的测定
采用差示扫描量热仪测定全麦粉淀粉的热性能。准确称量3 mg全麦粉到铝坩埚中,加入6 μL蒸馏水,用压盘机进行密封,4 ℃条件下放置过夜,使全麦粉与水分充分接触。以空白坩埚为对照,加热程序为:从30 ℃以10 ℃/min的速率加热到100 ℃,然后冷却到30 ℃。记录淀粉样品糊化的起始温度、峰值温度、终止温度和糊化焓。
1.3.7 游离巯基含量的测定
75 mg全麦粉样品用1 mL Tris-甘氨酸缓冲液(10.4 g Tris,6.9 g甘氨酸,1.2 g EDTA,用0.1 mol/L HCl溶液调pH值至8.0,定容至1 000 mL)混匀加4.7 g盐酸胍,用缓冲液定容至10 mL。测定巯基时,取1 mL该液加4 mL脲-盐酸胍溶液(8 mol/L脲+5 mol/L盐酸胍)和0.05 mL Ellman’s试剂(4 mg/mL)避光反应30 min,于412 nm处测定吸光值。按公式(1)进行计算:
游离巯基含量![]()
(1)
式中:A,412 nm处吸光值;D,稀释因子;ρ,样品质量浓度,mg/mL。
1.3.8 蛋白质二级结构的测定
利用傅里叶红外光谱仪,使用衰减全反射法,取少量全麦粉样品进行数据采集。测试条件为:扫描次数32次,扫描波长范围4 000~650 cm-1,分辨率4 cm-1。使用OMNIC和Peakfit软件分析数据。
1.3.9 蛋白质分子质量分布的测定
采用SDS-PAGE,将10 mg全麦粉置于离心管中,加入400 μL浓度为0.01 mol/L的Tris-HCl缓冲液(pH值为6.8,含有10% SDS(w/v),10%甘油(体积分数),0.1%(w/v)溴酚蓝),混匀40 ℃水浴2 h,沸水浴5 min,冷却后离心(12 000 r/min,10 min)取上清液,冷冻备用。采用分离胶为12%,浓缩胶为5%,上样量10 μL,电压80 V,待进入分离胶后转为120 V。染色采用考马斯亮蓝R250,染色1 h后用脱色液脱色,然后用凝胶成像系统拍摄电泳图谱。
1.4 数据处理
每个实验3次平行,数据均采用均值±标准差表示,数据采用Excel 2019进行处理。使用IBM SPSS Statistics 26进行显著性分析,选择LSD检验和Duncan检验,显著性水平为P<0.05。采用Origin 2019绘图。
2 结果与分析
2.1 脂肪酸值的变化
脂肪酸值反映了样品中游离脂肪酸的含量,是衡量脂肪水解程度的重要指标。如图2所示,常温贮藏实验中样品脂肪酸值随贮藏时间的增加而增加,该结果和DANG等[7]的研究一致,本实验中射频处理前后全麦粉的脂肪酸值没有显著变化,但贮藏过程中未处理组的脂肪酸值迅速增加,射频组的脂肪酸值缓慢增加。这是由于脂肪可由脂肪酶水解为游离脂肪酸,未处理组脂肪酶活性高,随贮藏时间增加,脂肪水解迅速,导致游离脂肪酸大量积累,而射频组经过射频处理导致脂肪酶部分失活,在贮藏过程中脂肪水解受到抑制,游离脂肪酸缓慢积累。在贮藏6个月时,射频组的脂肪酸值为50.89 mg/100 g比未处理组(95.93 mg/100 g)低46.95%,射频处理使全麦粉脂肪水解得到控制,脂肪酸值显著降低。本实验中还对射频组进行脱氧处理,探究处理后氧气对脂肪水解的影响,贮藏6个月后射频脱氧组脂肪酸值为52.18 mg/100 g,脱氧处理会导致脂肪酸值轻微增加,可能是由于游离脂肪酸会进一步参与脂肪氧化,未脱氧处理的样品产生的游离脂肪酸会继续氧化成初级或次级氧化产物,使脂肪酸值增加速率下降,而脱氧不影响脂肪水解但延缓了脂肪氧化,使游离脂肪酸积累,因此脱氧组脂肪酸值轻微增加。整体上脱氧对射频处理后的全麦粉脂肪酸值变化影响不显著,与张晶晶[8]的研究结果一致。
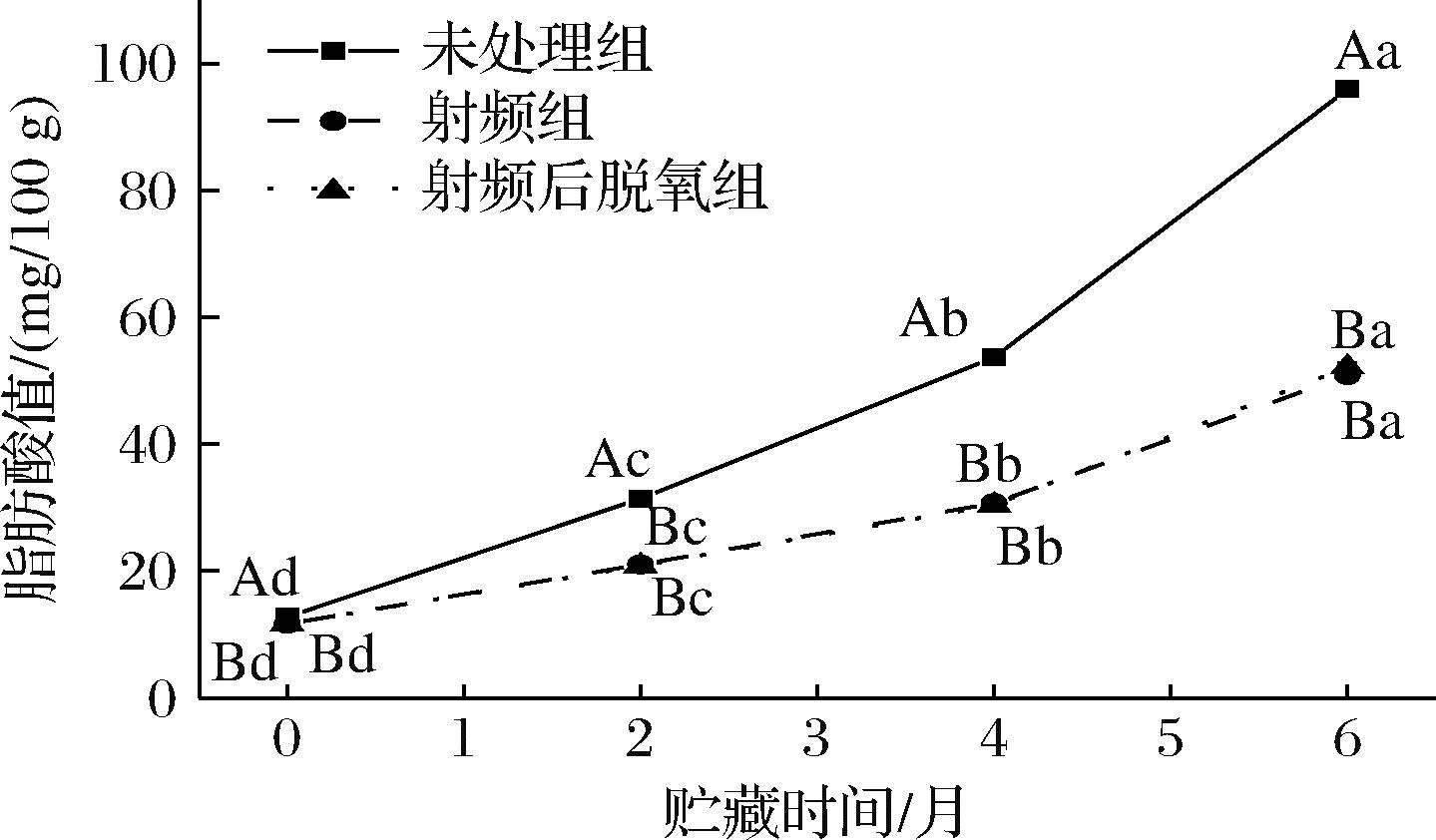
图2 常温贮藏期间全麦粉的脂肪酸值变化
Fig.2 Changes in the fatty acid values of whole wheat flour during storage at room temperature
注:同一分组不同小写字母表示差异显著(P<0.05), 同一贮藏时间不同大写字母表示差异显著(P<0.05), 反之差异不显著(下同)。
2.2 过氧化值的变化
过氧化值反映氢过氧化物含量的多少,是脂肪初级氧化的重要指标,可用来衡量贮藏过程中全麦粉脂肪氧化的劣变程度。如图3所示,本实验中全麦经过射频处理后制粉,过氧化值从0.043 g/100 g变为0.052 g/100 g,约上升20.93%,与SUN等[9]的研究中随微波处理全麦温度升高,过氧化值升高结果相似。研究发现,经过6个月的常温贮藏,未处理组、射频组和射频脱氧组的全麦粉过氧化值均先升高后降低,可能因为脂肪酸氧化产生氢过氧化物,氢过氧化物进一步氧化分解产生自由基及醛酮类物质[10],两步反应的平衡状态不断变化导致过氧化值处于不稳定的波动状态。经过6个月常温贮藏后,射频组及射频脱氧组的全麦粉过氧化值相较于未处理组(0.113 g/100 g)分别下降了8.85%和16.81%,是由于射频处理抑制了脂肪水解,使游离脂肪酸变少,且热处理后,脂肪氧化酶的酶活也受到影响,所以贮藏后射频组的全麦粉过氧化值低于未处理组,对射频组的全麦粉再进行脱氧后贮藏,又进一步抑制了脂肪的氧化酶促反应,降低了过氧化值。
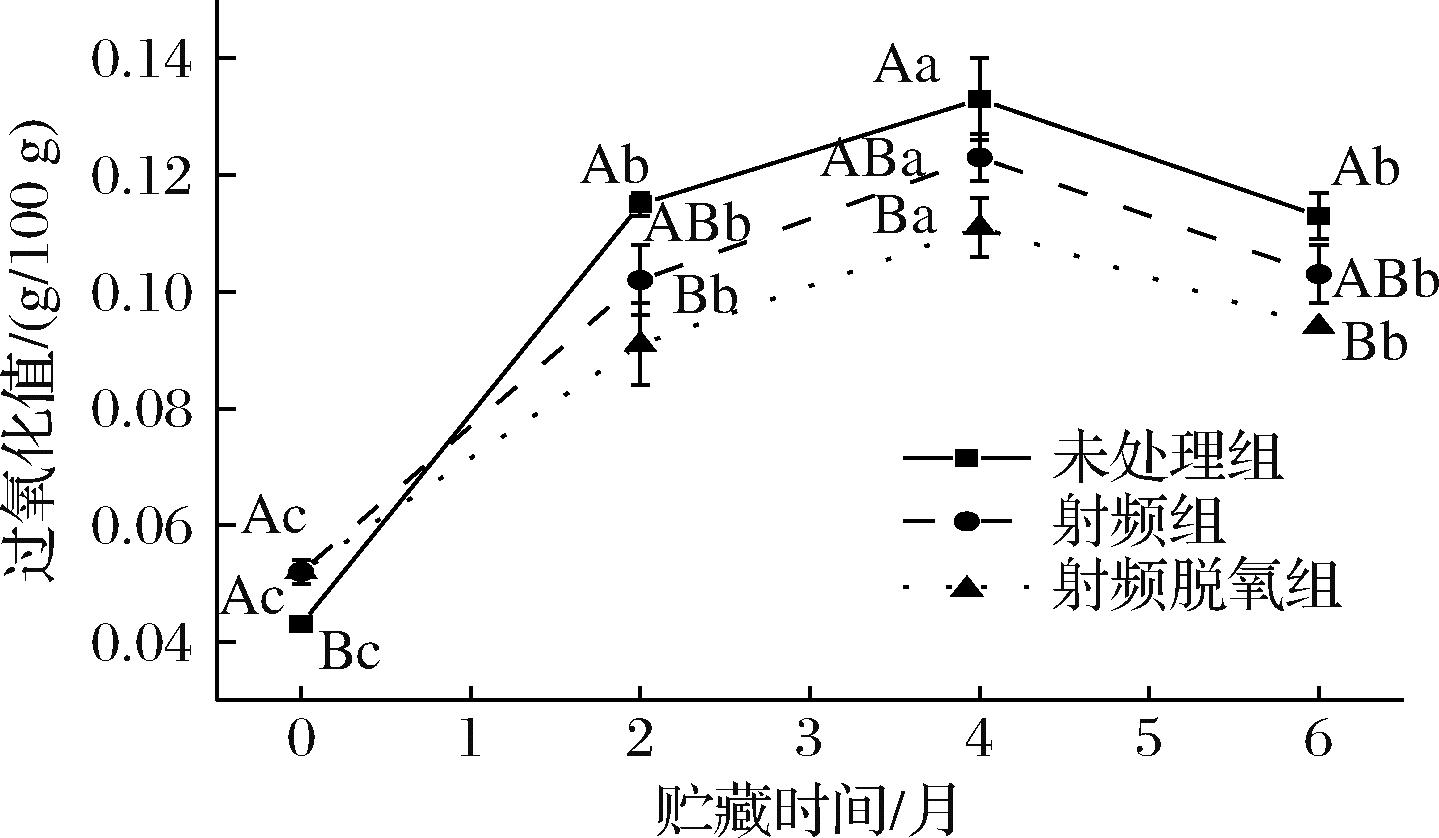
图3 常温贮藏期间全麦粉的过氧化值变化
Fig.3 Changes in the peroxide value of whole wheat flour during storage at room temperature
2.3 自由基强度的变化
热处理会诱导自由基的产生,从而加速贮藏过程中全麦粉样品的自氧化进程,LIN等[11]等在微波处理米糠时也发现类似现象,因此监测贮藏期间的自由基强度变化也极其重要。在本实验中,如图4所示,贮藏起始阶段各组全麦粉的自由基强度都较高,可能是由于磨粉过程中的热效应诱导了自由基的产生,而射频组和射频脱氧组由于射频前进行补水,水会在自由基产生后加速其流动分解,从而导致其强度降低[12],所以射频处理后全麦粉自由基强度(2.780)较未处理组(3.136)下降了11.35%,且在整个贮藏过程中射频组的全麦粉的自由基链式反应强度都低于未处理组,贮藏6个月后射频组全麦粉的自由基强度(1.627)较未处理组下降了23.44%。对射频组的全麦粉进一步脱氧处理后,贮藏后自由基强度为1.584,较射频组又有轻微的降低,可能是由于脱氧处理抑制了油脂的氧化酶促反应,使之产生的氢过氧化物减少,进一步的氢过氧化物裂解产生自由基就减少,使自由基强度降低。在常温贮藏过程中,未处理组、射频组和射频脱氧组样品的自由基强度均逐渐下降,发生衰减,自由基的衰减主要以两步的方式发生,即一般在32~38 h内的短寿命自由基的快速衰减和长寿命自由基的缓慢衰减,与BRA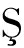 OVEANU等[13]的研究结果一致。
OVEANU等[13]的研究结果一致。
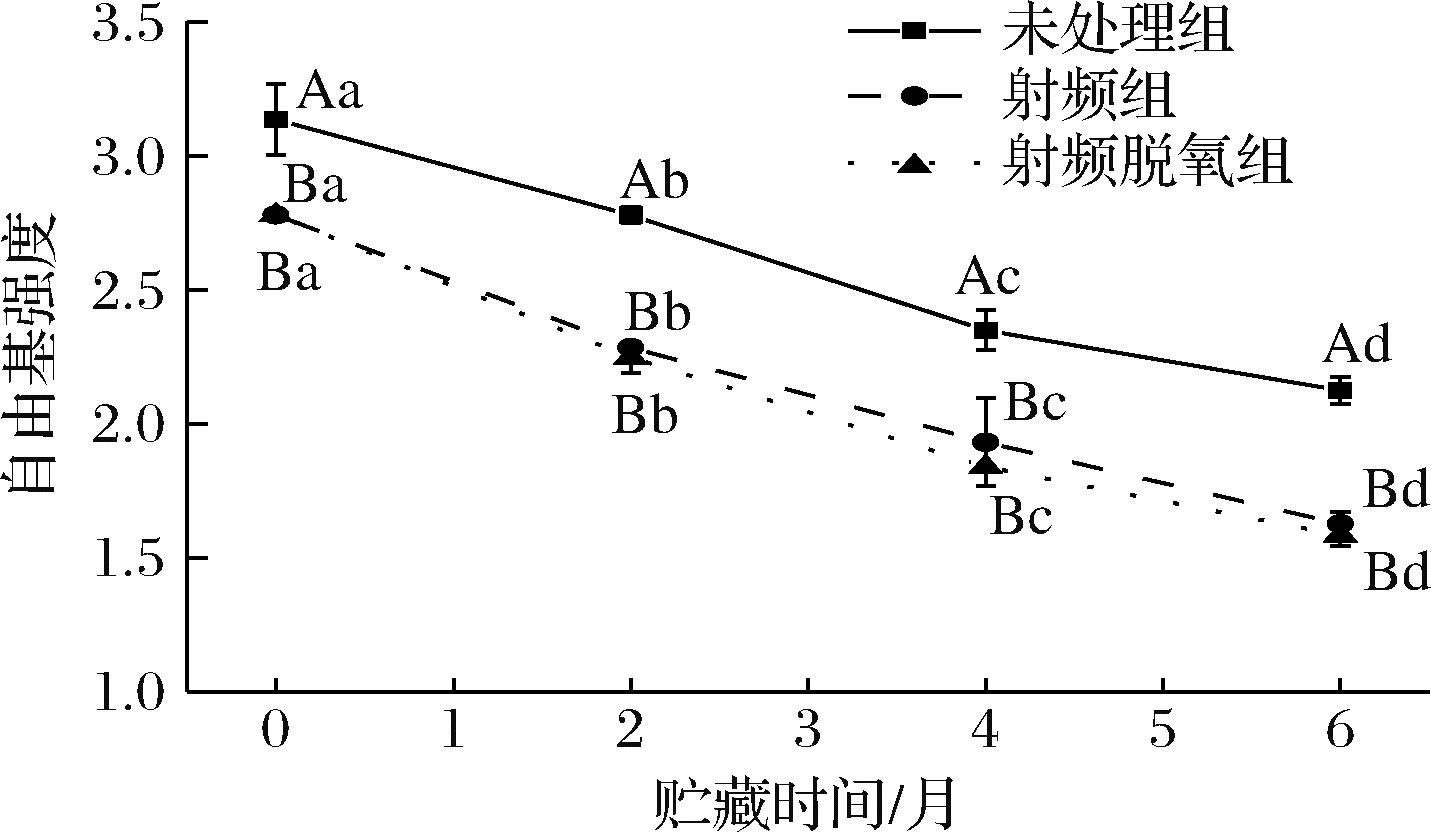
图4 常温贮藏期间全麦粉的自由基强度变化
Fig.4 Changes in the free radical strength of whole wheat flour during room temperature storage
2.4 结晶度的变化
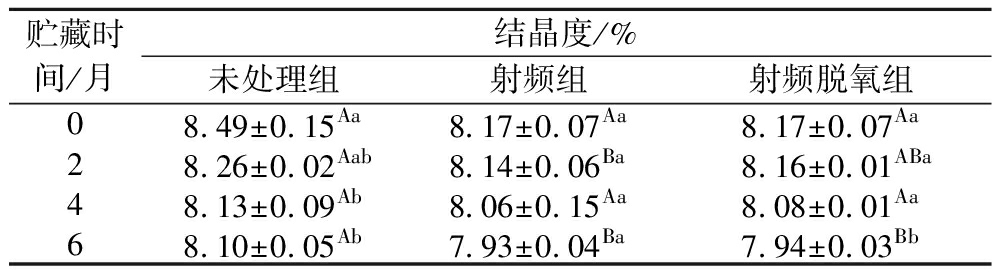
从X衍射图谱(图5)看,全麦粉为A型晶体结构,在15°、17°、18°和23°处有衍射峰,且由于A型结构晶体热稳定性高,射频处理后淀粉结晶特征峰的峰型和数量不变,但是强度变小。如表1所示,射频处理后样品结晶度较未处理组下降了约3.77%,可能是由于射频补水处理使淀粉糊化程度增加,淀粉分子间氢键断裂增多,淀粉颗粒内部结晶区域由排列紧密状态变为疏松状态,导致结晶度下降[14]。在贮藏过程中,X衍射图谱的峰型并未改变,说明贮藏也未引起全麦粉淀粉晶型的变化,但贮藏6个月后的未处理组、射频组及射频脱氧组的样品结晶度相较于贮藏前分别下降了4.59%、2.94%、2.82%,可能是由于在贮藏过程中构成结晶区的支链淀粉在脱支酶的作用下含量下降,导致了结晶度下降[15]。研究结果发现是否对射频后样品进行脱氧处理对结晶度的影响不大,可能是射频处理后的脱支酶活性较低或高温贮藏条件下氧气对脱支酶活性影响小。
表1 常温贮藏期间全麦粉的结晶度变化
Table 1 Changes in the crystallinity of whole wheat flour during storage at room temperature
贮藏时间/月结晶度/%未处理组射频组射频脱氧组08.49±0.15Aa8.17±0.07Aa8.17±0.07Aa28.26±0.02Aab8.14±0.06Ba8.16±0.01ABa48.13±0.09Ab8.06±0.15Aa8.08±0.01Aa68.10±0.05Ab7.93±0.04Ba7.94±0.03Bb
注:同一列不同小写字母表示差异显著(P<0.05),同一行不同大写字母表示差异显著(P<0.05),反之差异不显著(下同)。
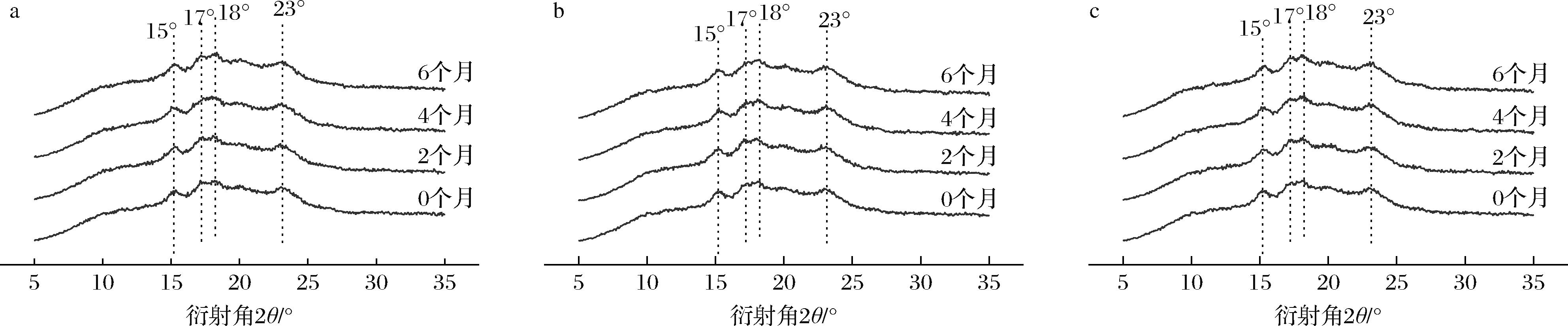
a-未处理组;b-射频组;c-射频脱氧组
图5 常温贮藏期间全麦粉的X-衍射图谱变化
Fig.5 Changes in the X-diffraction pattern of whole wheat flour during storage at room temperature
2.5 短程有序结果的变化
傅里叶变换红外结果中1 047、995 cm-1处的谱带与分子有序和结晶区有关,而1 022 cm-1处的谱带与淀粉颗粒的无序和无定型区相关。通常,将1 047 cm-1 与1 022 cm-1处的吸光度之比(R1 047/1 022)定义为淀粉的DO,表示结晶区和无定形区的比例,而用995 cm-1和1 022 cm-1处的吸光度之比(R995/1 022)表示DD。如表2所示,经过射频处理得到的全麦粉与未处理组相比DO下降,淀粉有序排列被打乱,LAN等[16]的研究结果表明长程有序比短程有序更脆弱,短程水平上的有序结构是长程有序发生的先决条件,因此DO下降,X射线衍射测得的样品结晶度下降。从双螺旋结果来看,淀粉中的双螺旋结构一部分通过氢键连接形成结晶,另一部分则分散在无定型区,因此DD不仅与晶体结构中短程有序程度有关,还反映了非晶结构的短程有序程度[17]。射频处理后样品的DD是有轻微上升的,可能因为射频处理导致连接相邻螺旋的氢键解离,而不影响双螺旋结构,且由射频补水诱导的淀粉糊化可导致结晶/无定形区域中的淀粉链断裂,使适合双螺旋排列的分子链有更多流动性,这可能导致处理组中双螺旋的量更高,与XU等[18]的研究中用高压灭菌处理鹰嘴豆和黄豌豆种子淀粉得到的结论一致。在贮藏过程中发现随贮藏时间增加,DD值轻微上升,DO值下降,可能由于脱支酶的作用使支链淀粉脱支,形成短侧链及直链淀粉,新增的短侧链淀粉可有效参与形成螺旋结构使DD增加,但短侧链淀粉形成的螺旋结构的局部排列更加无序,且构成淀粉无定形区的直链淀粉含量的升高会导致DO值下降。总的来看贮藏过程中各组淀粉短程有序结果变化不大,对射频后的样品再进一步脱氧后,其结果变化也基本与射频组一致。
表2 常温贮藏期间全麦粉的短程有序度和双螺旋度变化
Table 2 Changes in the degree of short-range molecular orders and double helix of whole wheat flour during storage at room temperature

分组DDDO0月未处理组1.13±0.01abc0.60±0.01ab0月射频组1.14±0.02abc0.59±0.01cde2月未处理组1.12±0.00c0.61±0.00a2月射频组1.15±0.00ab0.60±0.00abc2月射频脱氧组1.14±0.01abc0.60±0.00abc4月未处理组1.12±0.02bc0.60±0.00ab4月射频组1.15±0.00ab0.60±0.00abc4月射频脱氧组1.14±0.01abc0.60±0.00abc6月未处理组1.14±0.01abc0.60±0.00bcd6月射频组1.15±0.00ab0.58±0.00e6月射频脱氧组1.16±0.01a0.59±0.00de
2.6 热力学性质结果的变化
通过差示扫描量热仪检测淀粉分子在加热过程中晶体熔融与双螺旋结构的热解变化,得到起始温度、峰值温度、终止温度以及热糊化焓值。其中,糊化温度与淀粉分子链排列是否规则有关,排列越有序,结晶度越高,破坏所需的温度越高,糊化焓定义为糊化过程中破坏淀粉双螺旋结构所需的能量[19]。如表3所示,从热力学性质结果可以看出,经过射频处理的样品起始、峰值、终止温度和糊化焓均有所下降,且在贮藏过程中均低于未处理组,可能是由于未处理组的结晶度较高,射频处理后样品结晶度下降,热稳定性下降。未处理组和射频组的糊化焓在贮藏过程中均呈现下降趋势,但是射频组在贮藏6个月时糊化焓相较于4个月略有上升。可能是随贮藏的进行,支链淀粉降解和脱支形成直链和短侧链,结晶结构遭到破坏。但短链含量增加可能形成有缺陷的结晶层和不完整双螺旋,通过DD值的增加也可发现此现象,破坏此结晶结构及双螺旋所需能量低[20],且不完整的双螺旋大量积累,因此在贮藏6个月时其糊化焓有所升高。对射频组样品进一步脱氧后贮藏,其结果变化与射频组基本一致,脱氧对射频后样品的热力学性质影响较小。
表3 常温贮藏期间全麦粉的热力学性质结果变化
Table 3 Changes in the thermal properties of whole wheat flour during storage at room temperature

分组起始温度/℃峰值温度/℃终止温度/℃糊化焓/(J/g)0月未处理组59.61±0.28b64.72±0.37cd69.86±0.46abc5.08±0.24a0月射频组59.21±0.02c64.21±0.13e69.40±0.04c5.05±0.02a2月未处理组59.68±0.08b64.82±0.23bc69.90±0.13ab4.94±0.10ab2月射频组59.43±0.22bc64.31±0.00de69.42±0.11c4.79±0.02b2月射频脱氧组59.38±0.01bc64.40±0.12cde69.54±0.13bc4.81±0.04b4月未处理组60.26±0.22a65.14±0.23ab70.30±0.30a4.84±0.02ab4月射频组59.58±0.11b64.47±0.24cde69.65±0.21bc4.74±0.01b4月射频脱氧组59.59±0.01b64.65±0.01cd69.75±0.14bc4.79±0.11b6月未处理组60.27±0.16a65.23±0.11a70.28±0.00a4.73±0.08b6月射频组59.67±0.11b64.64±0.00cd69.73±0.05bc4.84±0.09ab6月射频脱氧组59.69±0.18b64.63±0.01cd69.77±0.06bc4.89±0.07ab
2.7 游离巯基含量的变化
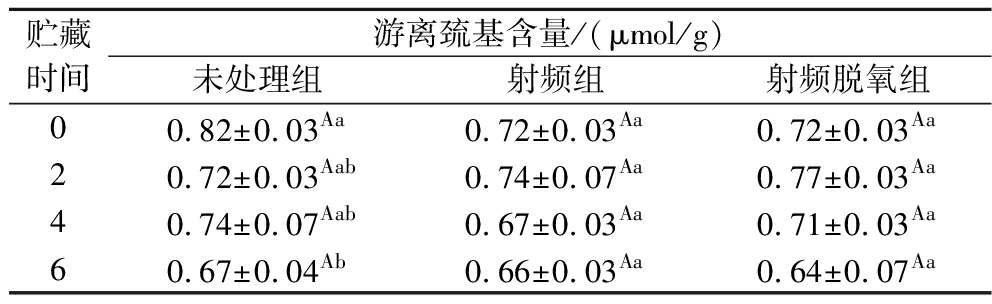
游离巯基含量与蛋白质中的半胱氨酸残基密切相关,蛋白质氧化可将巯基氧化为二硫键或其他氧化产物使蛋白质聚集,故游离巯基含量可作为蛋白质氧化程度的指标[21]。如表4所示,射频处理后,蛋白的结构被破坏,易氧化的半胱氨酸及其残基被暴露,游离巯基被氧化为二硫键后,含量下降了约12.20%,蛋白氧化程度增加,该结果与胡月明[2]用过热蒸汽处理小麦粉导致游离巯基含量下降结果一致。贮藏过程中,游离巯基也呈现下降趋势,经过6个月贮藏后,未处理组及射频组的游离巯基含量较贮藏前分别下降了18.29%、8.33%,由于蛋白氧化与脂肪氧化密切相关,因此射频处理降低了全麦粉的脂肪水解氧化速率,导致其游离巯基缓慢下降,未处理组脂肪氧化未被控制所以游离巯基迅速下降。对射频处理后样品进一步脱氧,贮藏过程中在前4个月的游离巯基含量均高于射频未脱氧组,第6个月游离巯基含量略低于射频未脱氧组,脱氧处理通过控制脂肪氧化进程来抑制蛋白氧化有一定的效果,但整体上射频组和射频脱氧组的游离巯基变化差异不显著,可能是由于包装时对自封袋中的空气进行了适当的排除,减弱了脱氧处理的效果,在贮藏4个月后射频组全麦粉的氧气被耗尽,游离巯基被氧化的程度也减小,变化趋于平缓,6个月时与脱氧组结果一致。贮藏过程中游离巯基含量下降的实验结果与HUANG等[22]相似,可能是脂质氧化产生的自由基和过氧化物导致了蛋白质游离巯基含量的下降,也可能是氧化使蛋白形成聚集体,导致部分巯基被覆盖,使测得数据下降。因此通过射频加脱氧处理不仅可以控制脂质氧化还能抑制蛋白氧化。
表4 常温贮藏期间全麦粉的游离巯基含量变化
Table 4 Changes in the sulfhydryl content of whole wheat flour during storage at room temperature
贮藏时间游离巯基含量/(μmol/g)未处理组射频组射频脱氧组00.82±0.03Aa0.72±0.03Aa0.72±0.03Aa20.72±0.03Aab0.74±0.07Aa0.77±0.03Aa40.74±0.07Aab0.67±0.03Aa0.71±0.03Aa60.67±0.04Ab0.66±0.03Aa0.64±0.07Aa
2.8 蛋白质二级结构的变化
对全麦粉的傅里叶变换红外光谱酰胺I带用peakfit高斯去卷积后,用二阶导拟合并计算蛋白各二级结构相对含量。蛋白质的二级结构中α-螺旋和β-折叠呈现周期性,而β-转角和无规则卷曲不呈现周期性,4种结构形式的自身稳定性均靠氢键维持。如表5所示,经过射频处理后β-折叠含量下降β-转角含量上升,与β-折叠相比,β-转角是一个开放的反向转角,需要更少的氢键,因此随着射频处理,射频使氢键弱化甚至裂解,β-折叠转化为β-转角[23]。但在贮藏过程中,β-折叠含量随贮藏时间的增加而逐渐增加,其变化趋势与α-螺旋、β-转角的变化相反,可能是由于全麦粉蛋白在受到脂质氧化产物作用时,相邻螺圈中的氢键遭到破坏,导致α-螺旋结构不稳定而展开,并进一步在分子间相互作用下转换为β-折叠结构,也可能是由于β-转角180°的反转结构再转变为β-折叠的伸展结构,造成β-折叠结构的增加[21]。总的来看常温贮藏及射频加脱氧对蛋白二级结构的影响较小,无规则卷曲及α-螺旋未见显著变化,β-折叠和β-转角存在少量的相互转化。与相关研究表明脂质氧化会导致蛋白质二级结构的部分重排结果一致[24],因此控制全麦粉的脂质氧化是非常有必要的。
表5 常温贮藏期间全麦粉的蛋白质二级结构变化 单位:%
Table 5 Changes in the protein secondary structure of whole wheat flour during storage at room temperature

分组β折叠无规则卷曲α螺旋β转角0月未处理组37.19±0.82ab12.20±0.13a24.82±0.43a25.79±0.51bcde0月射频组36.37±0.06b12.11±0.06a25.15±0.01a26.37±0.12a2月未处理组36.54±0.52b12.13±0.02a25.10±0.33a26.23±0.16ab2月射频组36.87±0.22ab12.10±0.16a24.96±0.13a26.06±0.07abc2月射频脱氧组36.73±0.15b12.18±0.02a25.09±0.12a26.00±0.05abcd4月未处理组36.78±0.54b12.09±0.12a25.10±0.22a26.02±0.2abc4月射频组37.07±0.09ab12.10±0.07a24.87±0.01a25.96±0.14abcd4月射频脱氧组37.22±0.43ab12.20±0.15a24.84±0.32a25.75±0.04bcde6月未处理组37.25±0.2ab12.28±0.11a24.95±0.14a25.52±0.17de6月射频组37.19±0.01ab12.27±0.1a24.84±0.12a25.69±0.20cde6月射频脱氧组37.74±0.29a12.23±0.01a24.67±0.19a25.36±0.09e
2.9 蛋白质分子质量分布的变化
根据不同分子质量的全麦粉蛋白在SDS-PAGE中迁移率不同,电泳将不同类型的蛋白质分离。80 kDa以上为高分子质量谷蛋白,30~80 kDa为醇溶蛋白,其中α-醇溶蛋白、β-醇溶蛋白、γ-醇溶蛋白在30~45 kDa,ω-醇溶蛋白在65~80 kDa,25 kDa以下为低分子质量蛋白质,主要包括清蛋白和球蛋白。如图6所示,从电泳图谱看,所有组别样品的条带均未发生减少和增加,蛋白分子质量分布大致相同,射频加脱氧及贮藏对全麦粉蛋白亚基组成影响较小。但经过射频加脱氧及贮藏处理后发现样品条带有轻微变浅,可能是由于射频热处理及贮藏后蛋白氧化导致形成了部分大分子质量蛋白聚合物,其溶解度低,没有被SDS提取液溶解,不能进入到分离胶中,该结果与蛋白二级结构及游离巯基的含量变化相一致。胡月明[2]用过热蒸汽处理小麦粉的研究也证明了热处理会诱导二硫键交联使蛋白聚集,ZHAO等[25]的研究中也表示大米经过贮藏后蛋白质发生氧化,其结构可能发生改变并通过二硫键和非二硫键共价键交联使蛋白质分子聚集。
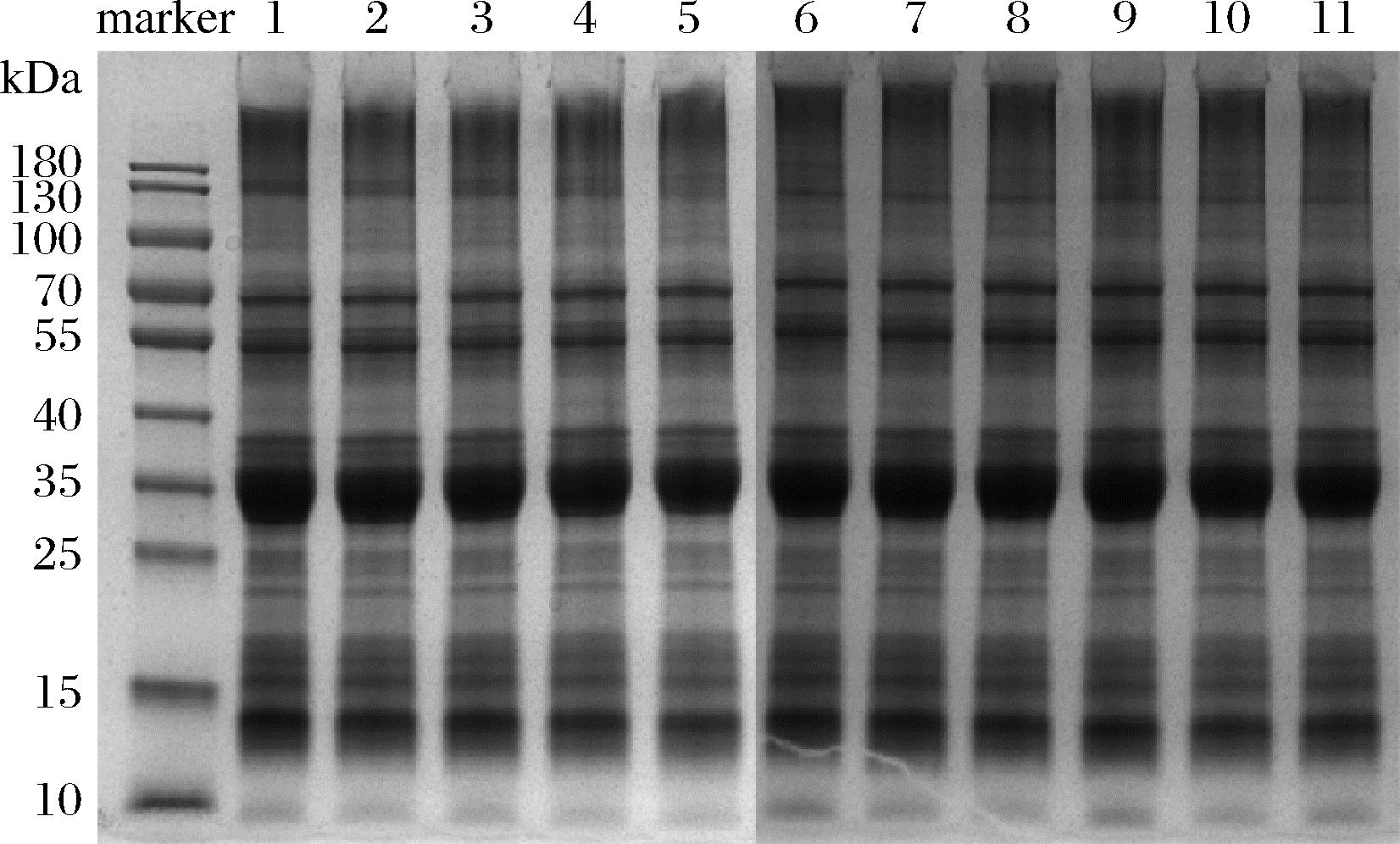
图6 常温贮藏期间全麦粉的SDS-PAGE电泳图谱变化
Fig.6 Changes in the SDS-PAGE pattern of whole wheat flour during storage at room temperature
注:条带1~2,贮藏前未处理组、射频组;条带3~5,贮藏2个月后的 未处理组、射频组、射频脱氧组;条带6~8,贮藏4个月后的未处理组、 射频组、射频脱氧组;条带9~11,贮藏6个月后的未处理组、 射频组、射频脱氧组。
3 结论
通过射频处理全麦,从脂肪氧化和淀粉、蛋白质结构变化3个方面探究其对全麦粉贮藏稳定性及品质的影响。结果表明,贮藏6个月后,射频组和射频脱氧组的脂肪酸值、过氧化值、自由基强度较未处理组均显著降低。贮藏过程中,射频组和射频脱氧组淀粉的结晶度、短程有序程度和糊化温度较未处理组轻微下降;所有组别游离巯基含量下降,蛋白质二级结构发生相互转化,与电泳条带轻微变淡的结果相吻合。但贮藏过程中射频组和射频脱氧组的淀粉、蛋白质结构性质相关指标变化较未处理组更缓慢。对射频组全麦粉添加脱氧剂贮藏,可以进一步降低其常温贮藏期间的过氧化值和自由基强度,延缓脂肪氧化,且对其淀粉和蛋白质结构的变化影响不显著。综上,射频加脱氧处理全麦能够有效抑制全麦粉的脂肪水解氧化,并延缓其淀粉和蛋白的结构变化,改善了全麦粉的贮藏稳定性及品质。
[1] LIU J, YU L L, WU Y B.Bioactive components and health beneficial properties of whole wheat foods[J].Journal of Agricultural and Food Chemistry, 2020, 68(46):12904-12915.
[2] 胡月明. 过热蒸汽处理对小麦及小麦粉品质的影响研究[D].北京:中国农业大学, 2018.HU Y M.Effect of superheated steam treatment on wheat and wheat flour quality[D].Beijing:China Agricultural University, 2018.
[3] LIAO M J, DAMAYANTI W, ZHAO Y Y, et al.Hot air-assisted radio frequency stabilizing treatment effects on physicochemical properties, enzyme activities and nutritional quality of wheat germ[J].Food and Bioprocess Technology, 2020, 13(5):901-910.
[4] HUANG Z, MARRA F, SUBBIAH J, et al.Computer simulation for improving radio frequency (RF) heating uniformity of food products:A review[J].Critical Reviews in Food Science and Nutrition, 2018, 58(6):1033-1057.
[5] 林碧莹. 不同物理结构小麦产品的射频杀菌技术研究[D].杨凌:西北农林科技大学, 2022.LIN B Y.Research on radiofrequency sterilization technology of wheat products with different physical structure[D].Yangling:Northwest A &F University, 2022.
[6] CHENG Y, JIANG J, CHEN Q M, et al.Radio-frequency treatment of medium-gluten wheat:Effects of tempering moisture and treatment time on wheat quality[J].Journal of the Science of Food and Agriculture, 2023, 103(9):4441-4449.
[7] DANG B, ZHANG W G, ZHANG J, et al.Effect of thermal treatment on the internal structure, physicochemical properties and storage stability of whole grain highland barley flour[J].Foods, 2022, 11(14):2021.
[8] 张晶晶. 薏仁米脂肪酶射频灭活效果及贮藏稳定性研究[D].无锡:江南大学, 2021.ZHANG J J.Study on radiofrequency inactivation effect and storage stability of lipase from barley[D].Wuxi:Jiangnan University, 2021.
[9] SUN Y, JI X Y, YAO Y Y, et al.Effect of low temperature microwave treatment on lipid stability and antioxidant capacity of whole wheat flour[J].LWT, 2023, 182:114854
[10] GREBENTEUCH S, KROH L W, DRUSCH S, et al.Formation of secondary and tertiary volatile compounds resulting from the lipid oxidation of rapeseed oil[J].Foods, 2021, 10(10):2417.
[11] LIN L F, HUANG L L, FAN D M, et al.Effects of the components in rice flour on thermal radical generation under microwave irradiation[J].International Journal of Biological Macromolecules, 2016, 93(Pt A):1226-1230.
[12] JENSEN P N, RISBO J.Oxidative stability of snack and cereal products in relation to moisture sorption[J].Food Chemistry, 2007, 103(3):717-724.
[13] BRA OVEANU M, CR
OVEANU M, CR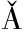 CIUN G, M
CIUN G, M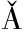 N
N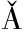 IL
IL E, et al.Evolution of the levels of free radicals generated on wheat flour and wheat bran by electron beam[J].Cereal Chemistry, 2013, 90(5):469-473.
E, et al.Evolution of the levels of free radicals generated on wheat flour and wheat bran by electron beam[J].Cereal Chemistry, 2013, 90(5):469-473.
[14] MA Y S, XU D, SANG S Y, et al.Effect of superheated steam treatment on the structural and digestible properties of wheat flour[J].Food Hydrocolloids, 2021, 112:106362.
[15] 赵军轻. 电子束处理对小麦储藏性能及加工品质的影响[D].无锡:江南大学, 2017.ZHAO J Q.Effects of electron beam treatment on storage performance and processing quality of wheat[D].Wuxi:Jiangnan University, 2017.
[16] LAN X H, XIE S C, WU J H, et al.Thermal and enzymatic degradation induced ultrastructure changes in Canna starch:Further insights into short-range and long-range structural orders[J].Food Hydrocolloids, 2016, 58:335-342.
[17] GUO P, YU J L, WANG S J, et al.Effects of particle size and water content during cooking on the physicochemical properties and in vitro starch digestibility of milled durum wheat grains[J].Food Hydrocolloids, 2018, 77:445-453.
[18] XU J B, MA Z, REN N M, et al.Understanding the multi-scale structural changes in starch and its physicochemical properties during the processing of chickpea, navy bean, and yellow field pea seeds[J].Food Chemistry, 2019, 289:582-590.
[19] DONG J L, HUANG L, CHEN W W, et al.Effect of heat-moisture treatments on digestibility and physicochemical property of whole quinoa flour[J].Foods, 2021, 10(12):3042.
[20] 董宇晴. 挤压对几种淀粉多尺度结构和理化性质影响的研究[D].济南:齐鲁工业大学, 2021.DONG Y Q.Effect of extrusion on multi-scale structure and physicochemical properties of several starches[D].Jinan:Qilu University of Technology, 2021.
[21] 张明慧. 基于蛋白质组学的富硒稻谷储藏过程中蛋白质氧化及功能特性研究[D].郑州:河南工业大学, 2023.ZHANG M H.Proteomics-based study on protein oxidation and functional characteristics of Se-enriched rice during storage[D].Zhengzhou:Henan University of Technology, 2023.
[22] HUANG Y R, HUA Y F, QIU A Y.Soybean protein aggregation induced by lipoxygenase catalyzed linoleic acid oxidation[J].Food Research International, 2006, 39(2):240-249.
[23] WANG Y, CHEN Y H, ZHOU Y, et al.Effects of konjac glucomannan on heat-induced changes of wheat gluten structure[J].Food Chemistry, 2017, 229:409-416.
[24] 黄友如. 脂肪氧合酶催化亚油酸诱导大豆蛋白聚集机理[D].无锡:江南大学, 2006.HUANG Y R.Mechanism of soybean protein aggregation induced by linoleic acid catalyzed by lipoxygenase[D].Wuxi:Jiangnan University, 2006.
[25] ZHAO Q Y, LIN J H, WANG C, et al.Protein structural properties and proteomic analysis of rice during storage at different temperatures[J].Food Chemistry, 2021, 361:130028.