玉米是我国重要的粮食作物,具有生产不均匀而消费均衡的特点,是国民经济发展的重要经济作物,是我国的主要储备粮种之一,我国玉米2022年总产量2.61亿t,约占全国粮食总产量的39%,其中约10%用于口粮,20%用于工业加工原料生产,70%用于饲料[1]。玉米籽粒具有水分含量高、成熟度不均匀、胚部大、生理活性强、胚部易吸湿、易酸败和易遭虫酶侵害的特点,在收获后的储存过程中,玉米籽粒依然是具有生命的活体,不断地进行合成、分解、代谢,并进行呼吸、后熟等生理活动[2]。玉米籽粒具有丰富的营养成分,极易发霉变质,直接影响玉米粒的色泽、口感、营养及加工特性[3],造成玉米品质下降,不利于储粮稳定性[4],甚至使其丧失种用、食用以及饲用价值[5]。
针对玉米储藏过程中玉米霉变、品质劣变等问题,一般采用降低玉米水分、降低微生态中氧气含量、降低玉米储藏温度的控制温、湿度条件等措施,但是常常不可避免的出现局部条件控制不到位的情况,从而引起粮情异常,并且耗能较高。一些化学药剂的采用,需要在长期储藏过程中多轮次施药,不但存在一定的安全性隐患,而且造成一定的环境和粮食污染,并不宜多用。在玉米长距离输送过程中,由于运载工具的空间有限,更限制了一些常规技术的应用。随着社会的发展和科学技术的进步,纳米技术研究的不断深入,被广泛应用于生产和生活中,在农业生产中的应用研究也逐渐普及。氧化锌纳米颗粒已被广泛用于食品、包装、纺织等行业领域[6],氧化锌作为添加剂已经广泛应用于饲料工业及农业中,还可以在粮食田间进行抑菌处理。在氧化锌纳米颗粒(zinc oxide nanopartilles,ZnO-NPs)和铁纳米颗粒(Fe-NPs)对小麦生长影响的研究中,不同添加量的ZnO-NPs 或Fe-NPs 处理小麦后,对小麦的光合作用有积极的影响[7]。前期开发的氧化锌纳米复合物,用于玉米的储藏过程中,抑菌谱广,抑菌时间长、对环境要求低、抑菌效果好,无毒无害[8],ZnO-NPs对玉米储藏过程中的金黄色葡萄球菌、大肠杆菌、黑曲霉、黄曲霉等细菌和真菌都有着良好的抑菌效果,并且没有毒副作用,使得纳米氧化锌成为一种较为理想的抑菌材料[9]。
在将所开发的ZnO-NPs应用至玉米储藏过程中时,前期研究结果表明氧化锌纳米颗粒对细菌和真菌有明显的抑菌效果,同时还有助于减缓玉米品质劣变,在此基础上,通过对玉米储藏过程中玉米籽粒细胞形态和结构的变化研究,进一步探究其在玉米储藏过程对玉米生理及细胞的影响,以期为科学评价ZnO-NPs对玉米储藏过程中品质的影响,为其在绿色安全储粮领域的应用提供依据。
1 材料与方法
1.1 试验材料
玉米:2023年收获于辽宁省丹东市。
ZnO-NPs:由本实验室采用水热法合成了ZnO-NPs,经过洗涤冻干成白色粉末状,质地均匀[10]。
1.2 主要试剂
无水乙醇(分析纯),国药集团化学试剂有限公司;硫代巴比妥酸、愈创木酚、三氯乙酸、甲硫氨酸、核黄素、乙二胺四乙酸二钠盐、二硫代硝基苯甲酸、Na2HPO4,NaH2PO4、H2O2(以上试剂均为分析纯),上海阿拉丁试剂有限公司;HNO3(优级纯),西陇科学股份有限公司;铝、钙、锰、铁、铜、锌、镉元素标准溶液,国家有色金属及电子材料分析测试中心;实验室用水为超纯水。
1.3 主要仪器与设备
Milli-Q去离子水发生器,美国Millipore公司;DW-86L630超低温冰箱,青岛澳柯玛股份有限公司;TDW-4000低温连续锤式旋风磨,浙江伯利恒仪器设备有限公司;101C-3电热鼓风干燥箱,上海实验仪器厂;JA2003电子天平,上海上平仪器有限公司;DNP-9082恒温恒湿培养箱,上海精胜科学仪器有限公司;DDSJ-307电导率仪,上海仪电科学仪器股份有限公司;Hitachi-7800透射电子显微镜(transmission electron microscope,TEM),日立高新技术集团;CR-410色差计,柯尼卡美能达有限公司;Ultimate 3000-ICP RQ型电感耦合等离子体发射光谱-质谱联用仪,美国赛默飞世尔科技公司;MARS6240/50型微波消解仪,美国CEM公司;T6新世纪紫外可见分光光度计,北京普析通用仪器有限责任公司;VELOCITY 14R台式高速冷冻离心机,英国Dynamica公司。
1.4 实验方法
将玉米过筛除杂,随机分成4份,每份1 kg。在玉米调水分时分4次将含有不同添加量的ZnO-NPs悬浮液的溶液用喷壶均匀喷洒在玉米上,使样品中 ZnO-NPs的添加量分别为 0 g/kg、0.5 g/kg、1.5 g/kg、2.5 g/kg,将样品封袋,并置于恒温恒湿培养箱中模拟储藏,每7 d监测1次相关指标的变化。
1.4.1 电导率值和丙二醛含量
参照LIU等[11]的方法进行测定。试验前称取25粒大小均匀的玉米籽粒(保证组间质量差异小于5%),用去离子水洗涤3次,然后浸泡在50 mL去离子水中12 h。最后,使用电导率仪测定玉米样品的电导率。
丙二醛含量参照王若兰等[12]的方法测定。将约1.00 g全玉米粉与5.00 mL 100 g/L三氯乙酸混合,然后在10 000×g和4 ℃下离心10 min。随后,取2.00 mL上清液与2.00 mL 6 g/L硫代巴比妥酸混合,煮沸15 min,迅速冷却至室温(25 ℃),10 000×g,4 ℃离心10 min。取上清液在450、532、600 nm处检测吸光度,以TCA溶液作为空白对照。
1.4.2 过氧化物酶(peroxidase,POD)活力和超氧化物歧化酶(superoxide dismutase,SOD)活力
过氧化物酶活力参照EMMANUEL等[13]的方法测定。将1.00 g玉米粉和10.00 mL磷酸盐缓冲液混合后,在4 ℃以10 000×g的速度离心10 min。然后,将1.00 mL上清液加入到含有2.00 mL磷酸盐缓冲液、1.00 mL H2O2溶液和1.00 mL愈创木酚溶液的混合物中;然后,每分钟在470 nm处测量吸光度,持续5 min。
超氧化物歧化酶活力参照PIASECKI等[14]的方法进行测定,用SOD活力检测试剂盒(BC0170),试剂盒来源于北京索莱宝科技有限公司。
1.4.3 过氧化氢含量和超氧阴离子产生速率
过氧化氢含量参照MUHAMMAD等[15]的方法,称取约1.0 g样品与5.0 mL预冷的TCA混合,在4 ℃、10 000×g条件下离心20 min。然后,准确称取1.0 mL上清液,1.0 mL磷酸盐缓冲液和1.0 mL 1.0 mol/L碘化钾混合,在黑暗和25 ℃下孵育1 h,在390 nm处测量吸光度。结果根据已知H2O2浓度的标准曲线计算。
超氧阴离子(·O2-)产生速率参照LIU[16]等的方法,将约2.0 g样品和5 mL磷酸盐缓冲液混合,在4 ℃和10 000×g下离心15 min。然后取0.5 mL上清液,加入0.5 mL磷酸盐缓冲液、1 mL 1 mmol盐酸羟胺,在25 ℃下孵育1 h,随后加入1 mL 50 mmol对氨基苯磺酸、1 mL 7 mmol α-萘胺,在25 ℃下孵育20 min,最后在530 nm处测定混合物的吸光度。
1.4.4 色泽
用色差计进行测定,选取L*值、a*值和b*值作为玉米色泽评价指标[17]。
1.4.5 锌离子迁移
参照PRERNA等[18]的方法进行测定。称取0.5 g样品置于聚四氟乙烯内罐中,加入5~7 mL硝酸,安装内盖和保护套,在微波消解仪中进行微波消解程序。此后,用去离子水稀释消解液,通过电感耦合等离子体质谱法测定Zn含量。
1.4.6 细胞结构完整性
参照SALAM等[19]的方法进行前处理,将处理过后的试样固定在铜网格上,并在TEM下进行扫描。
1.4.7 数据分析
使用Microsoft Excel 2016和SPSS软件对实验结果进行统计分析,并在图中用字母标注表示显著性差异,小写字母表示相同时间不同处理添加量下的差异,大写字母表示相同添加量不同处理时间下的差异,并运用Origin 2021进行作图。
2 结果与分析
2.1 玉米储藏期间细胞结构的变化
种子衰老与细胞超微结构损伤密切相关,玉米细胞的超微结构在透射电镜下呈现出来的形态和结构,对玉米生长发育及其生物学功能至关重要[20]。原始玉米细胞的形态和各细胞器呈现正常状态,表明其结构完整,功能良好。
在储藏前,细胞壁细胞膜结构紧密且光滑完整;细胞基质致密均匀,细胞核清晰可辨,核质均匀;线粒体数量丰富,呈比较规则的圆形或卵圆形(图1-a),说明储藏前玉米细胞能量代谢正常,细胞结构清晰可见。在储藏42 d后,对照组玉米与原始状态相比,细胞的超微结构发生明显变化,各细胞器明显受损,细胞壁开始溶解,细胞膜出现轻度内陷,其完整性受到破坏,完整的线粒体数量减少,并且出现内部空泡化,说明随着高温高湿的长时储藏,会使玉米细胞生命活力减弱,使其细胞结构的破坏(图1-b)。适宜添加量氧化锌纳米颗粒添加过后的玉米细胞结构无明显变化,细胞内部形态及各细细胞器均保持较好的结构,且氧化锌纳米颗粒并未进入到细胞内部且无累积,氧化锌纳米颗粒对细胞的超微结构无明显影响(图1-c)[21]。

a-储藏前0 g/kg ZnO-NPs组;b-储藏后0 g/kg ZnO-NPs组; c-储藏后0.5 g/kg ZnO-NPs组
图1 储藏期间不同添加添加量ZnO-NPs的玉米 细胞结构TEM图
Fig.1 TEM images of corn cell structure with different concentrations of ZnO-NPs during storage
注:CW-细胞壁;F-纤维丝;ICS-胞间隙;M-线粒体;N-细胞核; PM-细胞质膜;PB-蛋白体;L-脂肪体;Thy-类囊体。
2.2 对玉米籽粒电导率值的影响
电导率值通常是用来衡量粮食中水分、电解质含量以及其他可溶性物质的总体水平。在粮食研究中,电导率值可作为一种指标,用于评估种子活力、籽粒的损伤程度、细胞的完整性,并判断玉米品质的劣变程度。
随着玉米储藏时间的延长,玉米籽粒的电导率呈上升趋势[22]。在模拟储藏前期,各组之间的电导率值无显著性差异;在储藏42 d后,对照组玉米籽粒的电导率增加了9.17 μS/cm/g,3个ZnO-NPs添加量处理后的玉米电导率分别增加了7.45、8.11和9.80 μS/cm/g(图2),低添加量ZnO-NPs(0.5 g/kg和1.5 g/kg)添加的玉米电导率明显低于对照组(P<0.05),是因为低添加量氧化锌纳米颗粒减少了自由基的产生,减少电解质的泄漏,维持了玉米籽粒细胞内电解质等物质的动态平衡,较好保持了玉米籽粒细胞的通透性[23];但当ZnO-NPs添加量增加到2.5 g/kg时,玉米籽粒的电导率值增加明显,且高于对照组。实验结果表明,在玉米储藏过程中添加低添加量氧化锌纳米颗粒减小了玉米细胞的通透性,保护了玉米细胞膜的完整性,有延缓玉米品质劣变的作用。
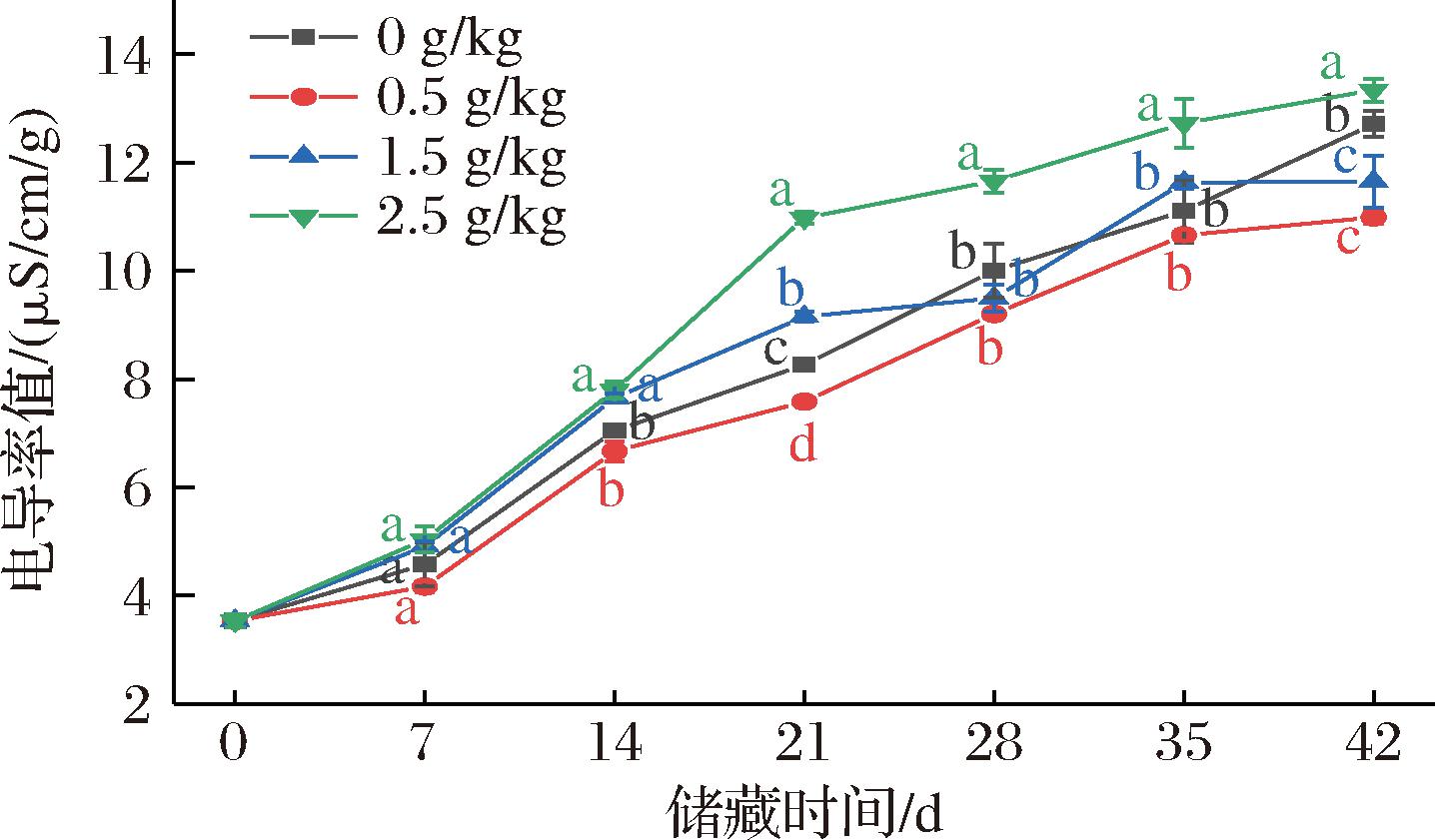
图2 玉米储藏期间电导率的变化
Fig.2 Changes of electrical conductivity of maize during storage
注:不同小写字母表示差异显著(P<0.05)(下同)。
2.3 对玉米籽粒丙二醛(malondialdehyde,MDA)含量的影响
丙二醛含量的高低可以反映玉米细胞膜脂过氧化程度,从而评估粮食的氧化损伤情况和储藏品质。当粮食储存条件不佳时,氧化应激会增加,促进脂质过氧化反应的发生,在这个过程中产生的MDA等物质,会进一步破坏细胞膜的完整性和功能,最终影响粮食品质[24]。
在模拟储藏前期,对照组和处理组无显著性差异。随着储藏时间的延长,丙二醛不断升高,在储藏42 d后,对照组MDA含量增加了1.26 μmol/g,3个ZnO-NPs添加量处理组分别增加了1.10、1.18和1.33 μmol/g(图3)。氧化锌纳米颗粒添加添加量为0.5 g/kg和1.5 g/kg的玉米丙二醛含量显著低于对照组玉米(P<0.05),可能是因为低添加量氧化锌纳米颗粒抑制玉米籽粒丙二醛的积累,最大限度地减少了脂质过氧化现象,同时保持了质膜的稳定性[25];但当ZnO-NPs添加量增加到2.5 g/kg时,玉米籽粒的丙二醛含量明显高于对照组。实验结果表明,适当添加量的氧化锌纳米颗粒不会对玉米的品质造成影响,且适量的添加对细胞膜有一定的保护作用,一定程度上延缓了细胞膜脂质过氧化。
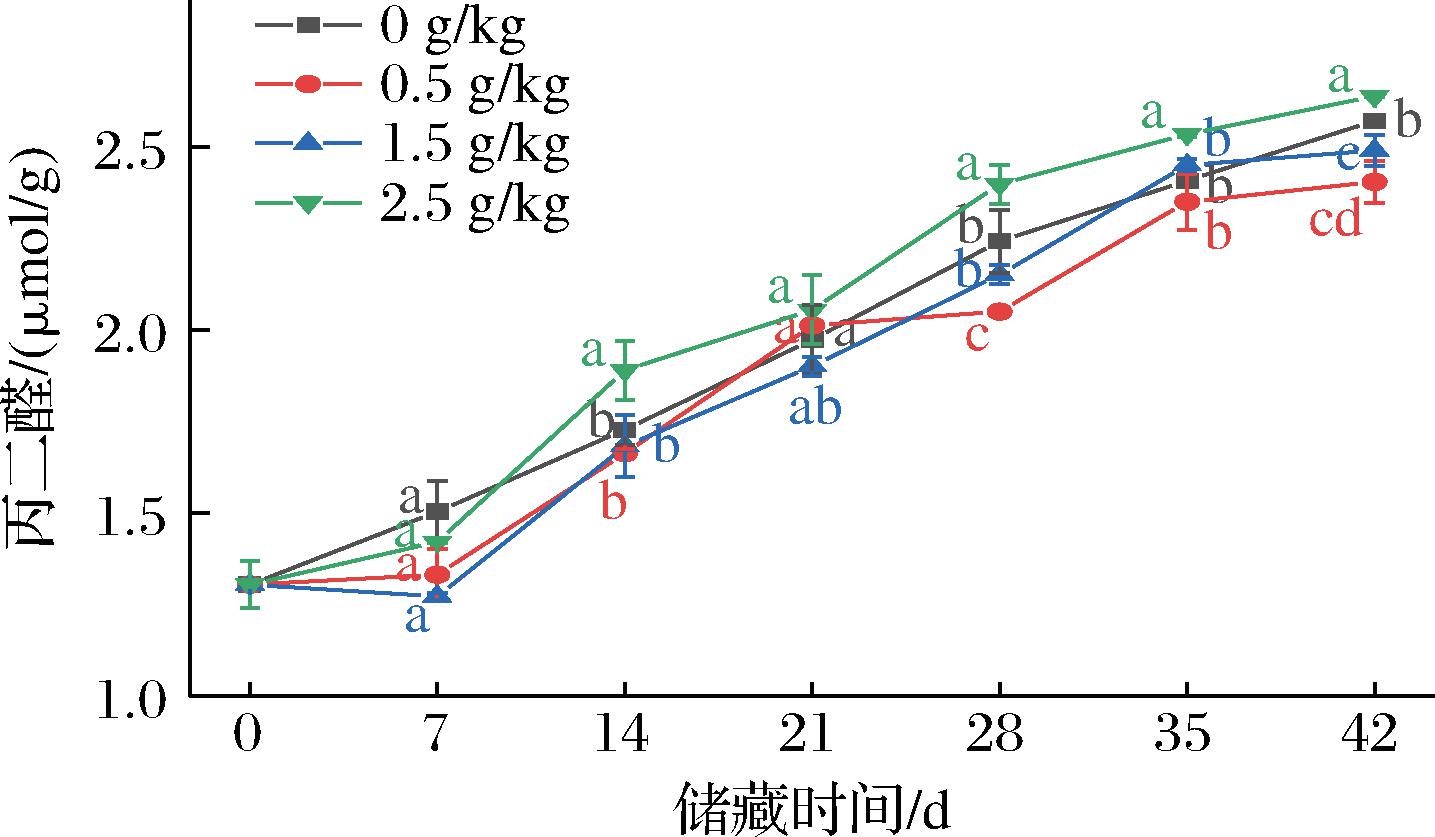
图3 玉米储藏期间丙二醛的变化
Fig.3 Changes of malondialdehyde during maize storage
2.4 对玉米籽粒POD活力的影响
在玉米籽粒中,POD是玉米细胞内高活力的一种氧化还原酶,影响细胞的呼吸作用、光合作用及生长素的氧化等,在细胞生长发育过程中其活性也不断变化[26]。POD活力的高低能够反映粮食细胞对氧化胁迫的反应能力和健康状态。随着储藏时间的延长,POD活力会减小,这种变化会影响粮食的抗氧化性能,从而影响储藏品质。
在模拟储藏前期,POD活力较初始酶活力短暂升高,可能是因为玉米籽粒受微生物侵染,自身的自我保护机制被激活,以提高自身的抗氧化机制来抵御活性氧物质的胁迫[27]。随着储藏时间的延长,POD活力呈现下降趋势,在储藏42 d后,对照组POD减小了28.73 U/g;3个ZnO-NPs添加量处理组分别下降了23.63、24.9和31.83 U/g(图4)。ZnO-NPs添加量为0.5 g/kg和1.5 g/kg的玉米POD活力显著高于对照组(P<0.05);但当ZnO-NPs添加量增加到2.5 g/kg时,玉米籽粒的过氧化物酶活力低于对照组,与PRAKASH等[28]研究的结果一致,该研究发现玉米能够通过自身调节POD活力,来增强清除活性氧物质的能力。实验结果表明,适量的添加氧化锌纳米颗粒能够在一定程度上缓解玉米的氧化伤害,并促进自身抗氧化机制的建立。
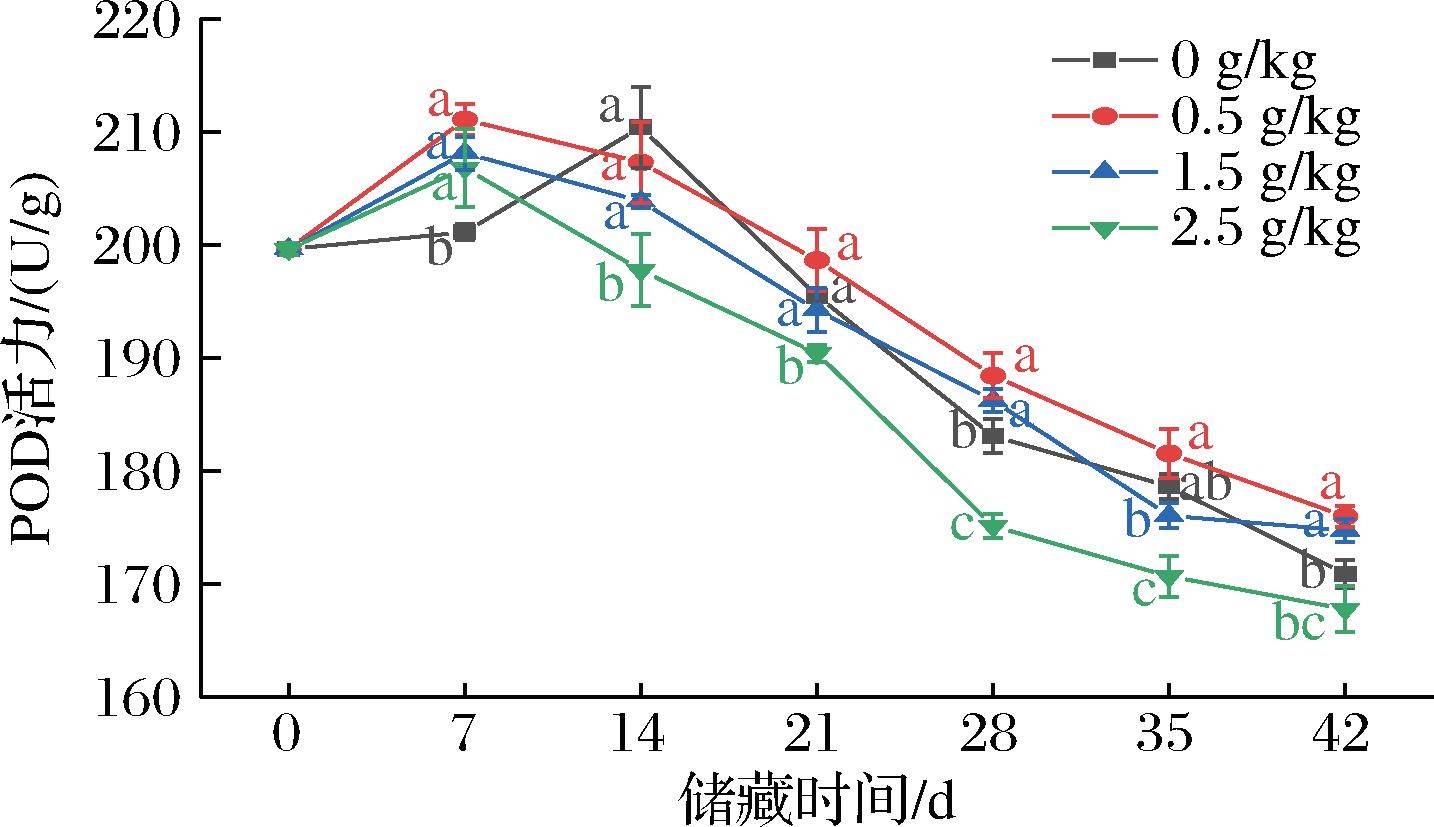
图4 玉米储藏期间POD活力的变化
Fig.4 Changes of peroxidase activity of maize during storage
2.5 对玉米籽粒SOD活力的影响
SOD是玉米细胞内催化自由基还原和保护细胞免受损害的主要物质,它参与催化中和自由基,并保护细胞不被氧化损伤;它也能够防止自由基引起的损害并帮助修复受损细胞,反映了其整体的抗氧化能力[29]。
在模拟储藏前期,SOD活力增高,可能是因为ROS含量的增加刺激了玉米自身的防御机制,使SOD活力增加以应对ROS的胁迫。随着储藏时间的延长,SOD活力呈现不断降低的趋势,在储藏42 d后,对照组玉米下降了3.06 U/g;3个ZnO-NPs添加量的玉米SOD活力分别下降了2.36、2.71和3.55 U/g(图5)。ZnO-NPs添加量为0.5 g/kg和1.5 g/kg的玉米呈缓慢下降的趋势且显著大于对照组(P<0.05),与MEHMOOD等[30]的研究结果一致;但当ZnO-NPs添加量增加到2.5 g/kg时,玉米籽粒的SOD活力低于对照组。说明在储藏后期,玉米自身清除过氧化物的能力下降,造成H2O2等活性氧积累,使SOD的活力降低。结果表明,低添加量的ZnO-NPs在一定程度上缓解了玉米自身的氧化,这和前面结果相同,也和SRIVASTAV等[7]研究结果相符合。
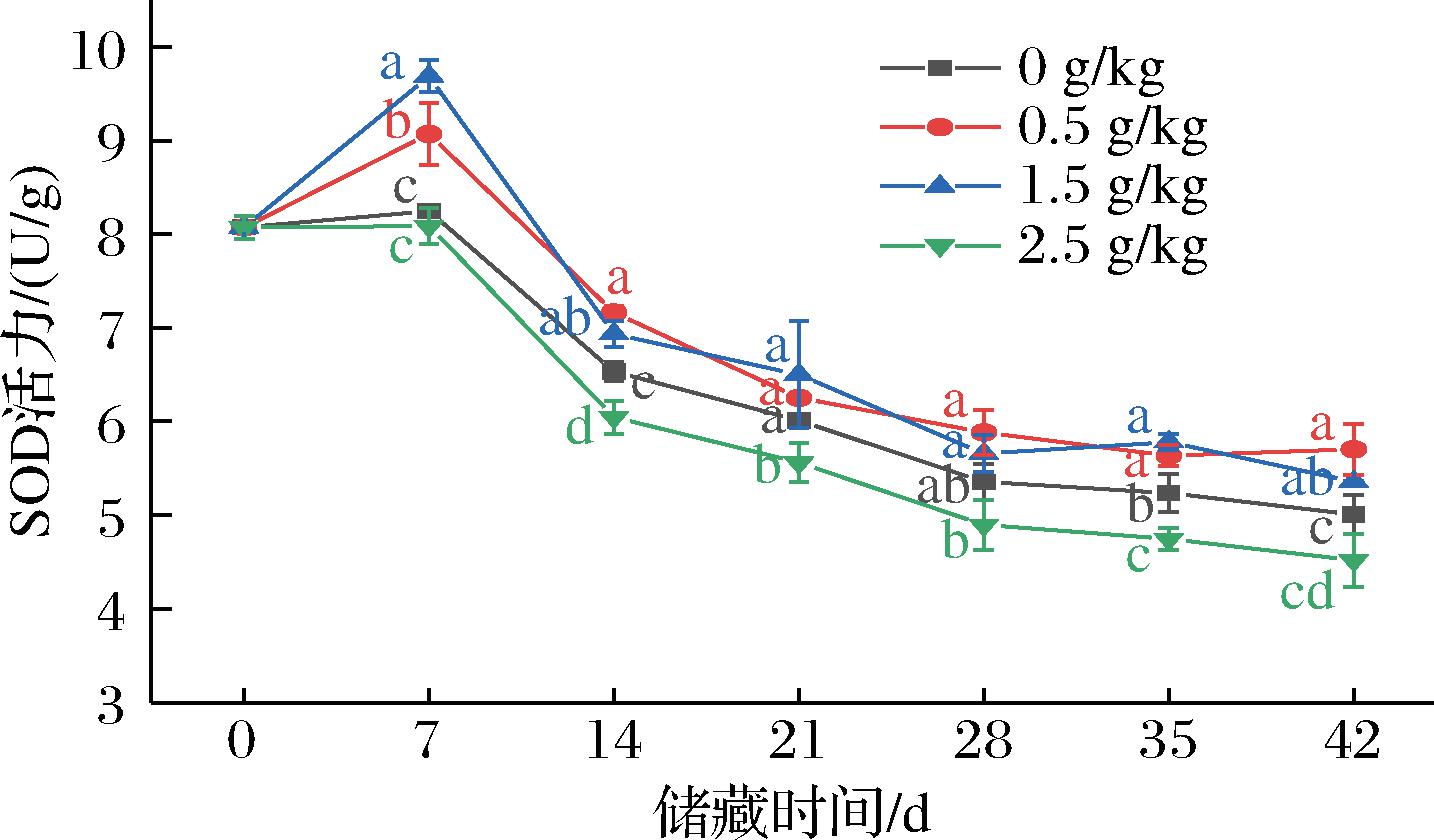
图5 玉米储藏期间SOD活力变化
Fig.5 Changes of superoxide dismutase activity during storage of maize
2.6 玉米储藏期间H2O2含量的变化
H2O2是关键的活性氧物质之一,在玉米胁迫响应中起着重要作用(包括细胞中的氧化应激)它是作为各种代谢过程的副产物产生的,如果玉米自身的抗氧化系统没有适当调节,会导致细胞损伤。H2O2的含量变化反映了玉米籽粒的氧化应激水平,在储藏期间,玉米籽粒细胞内不断发生着活性氧代谢,破坏细胞膜,从而加速细胞衰老和解体。
在模拟储藏前期,对照组和处理组之间无显著性差异。随着储藏时间的延长,H2O2含量整体呈增加趋势,是由于籽粒内部的抗氧化系统衰弱以及细胞膜的损伤,与前期TEM结果一致。在储藏42 d后,对照组H2O2含量增加了3.11 μmol/g,3个ZnO-NPs添加量处理组分别增加了2.42、2.69和3.38 μmol/g(图6)。ZnO-NPs添加量为0.5 g/kg和1.5 g/kg的玉米H2O2含量显著低于对照组(P<0.05),可能是因为ZnO-NPs通过激活抗氧化酶系统参与清除ROS,提高了SOD活力,从而降低了玉米籽粒的H2O2水平[23];但当ZnO-NPs添加量增加到2.5 g/kg时,玉米籽粒的过氧化氢含量增加明显,且高于对照组。结果表明,低添加量的ZnO-NPs不会诱导其产生过多的过氧化氢,延缓了玉米籽粒的劣变氧化,与KHAN等[31]的研究结果保持一致;而过高添加量的ZnO-NPs的添加使玉米籽粒的H2O2含量降低趋势明显。
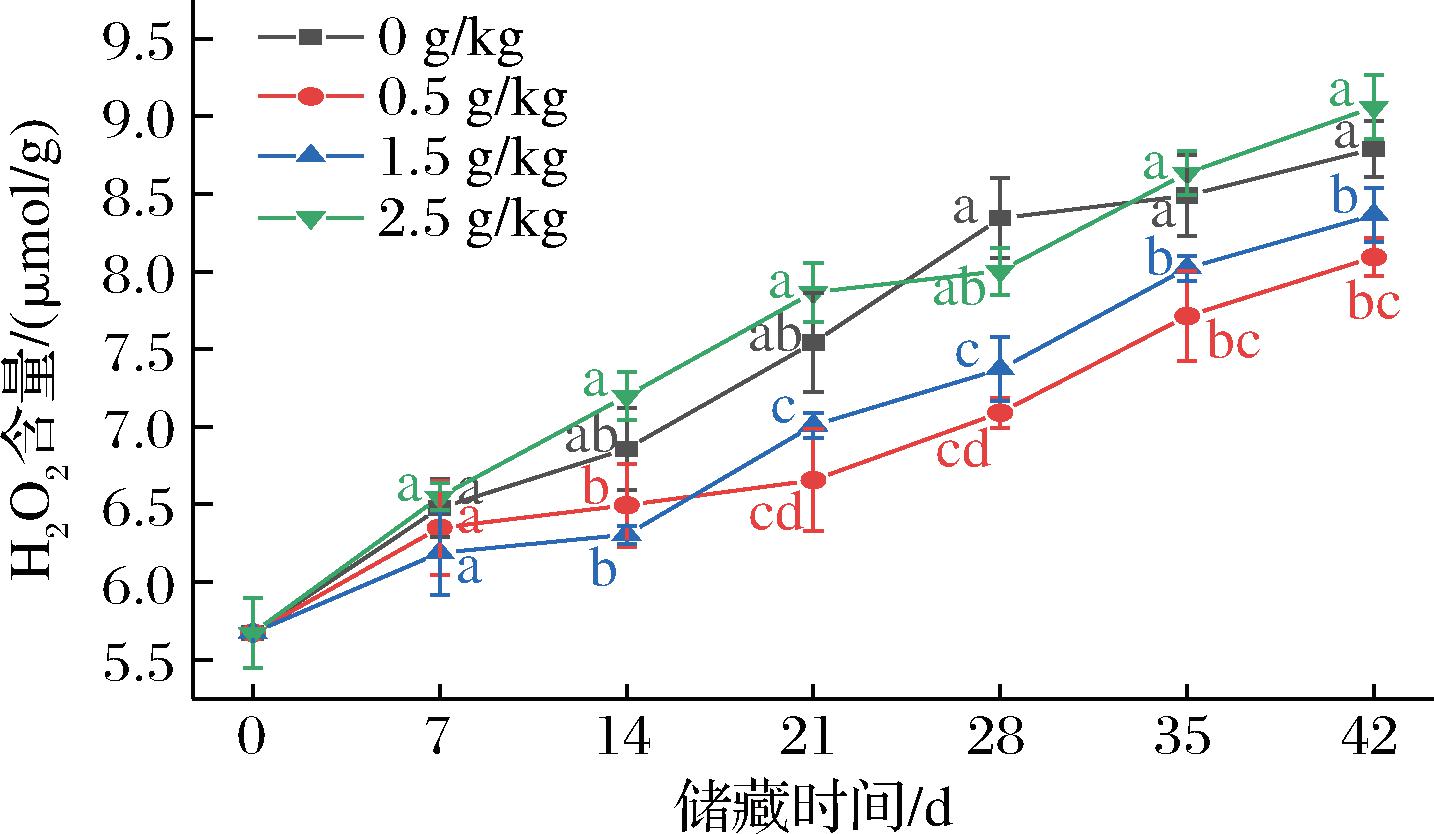
图6 玉米储藏期间H2O2含量变化
Fig.6 Changes of H2O2 during maize storage
2.7 玉米储藏期间·O2-产生速率的变化
·O2-是玉米籽粒细胞正常线粒体呼吸的副产物,可以氧化和破坏细胞质膜,加速体内脂质过氧化和膜损伤。·O2-产生速率是指在储藏期间细胞内·O2-这一ROS的生成速度,它是细胞应对环境胁迫以及储藏过程中自然衰老的一种典型反应,它不仅影响玉米籽粒的质量,还可能引起后续的氧化应激反应。
在模拟储藏前期,处理组和对照组之间无显著性差异。随着储藏时间的延长,·O2-产生速率呈上升趋势,在储藏42 d后,对照组的·O2-产生速率增加了65.95 nmol/(min·g),3个ZnO-NPs添加量处理组分别增加了57.55、60.62和68.23 nmol/min·g(图7)。ZnO-NPs添加量为0.5 g/kg和1.5 g/kg时,玉米·O2-产生速率增加趋势明显缓于对照组,且最终含量显著小于对照组(P<0.05)。这主要是由于低添加量的ZnO-NPs有利于降低玉米中超氧阴离子自由基的积累速度,减慢了玉米籽粒的老化速度;但当ZnO-NPs添加量增加到2.5 g/kg时,玉米籽粒的·O2-产生速率增加明显,且高于对照组。结果表明,适当添加量的ZnO-NPs并未影响玉米的品质且在一定程度上缓解了氧化损伤,从而减缓玉米的劣变进程,延长其安全储藏期。
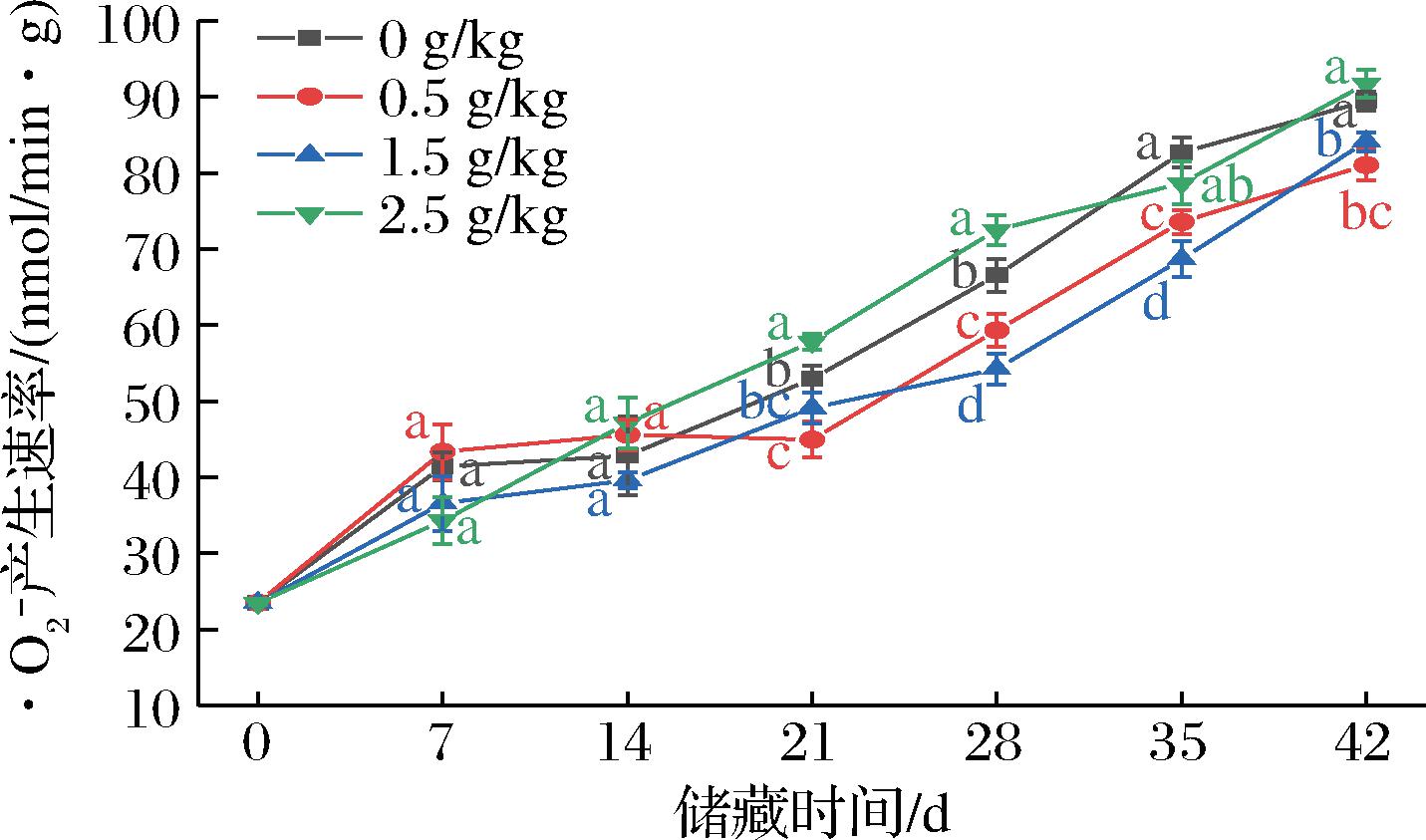
图7 玉米储藏期间·O2-产生速率变化
Fig.7 Changes of superoxide anion production rate during maize storage
2.8 玉米储藏期间色泽变化
色泽直观反映了玉米籽粒的品质变化。籽粒中的植物色素(如类胡萝卜素、黄酮类等)是影响玉米色泽的重要因素[32]。其中,类胡萝卜素中的胡萝卜素和叶黄素则是玉米呈现黄色的主要原因,且类胡萝卜素具有大量共轭双键,极易被氧化[33]。
随着储藏时间的延长,玉米的L*值和b*值随着储藏时间延长整体呈下降的趋势,a*值则呈缓慢上升趋势。3个ZnO-NPs添加量处理组的玉米L*值下降了0.70%、1.40%和3.26%;b*值下降了17.57%、18.19%和24.74%;a*值上升了2.22%、2.72%和6.27%(图8)。实验结果表明,ZnO-NPs添加量为0.5 g/kg和1.5 g/kg的玉米与对照组相比L*值、a*值和b*值均无显著性差异(P>0.05),一方面可能因为经过长期储藏温度和湿度会影响玉米的色泽,另一方面是因为玉米表面包裹的ZnO-NPs使其红度值和黄度值明显降低,且ZnO-NPs添加的量越高红度值和黄度值越小;也说明了低添加量ZnO-NPs较好的保持了玉米的色泽,会增加玉米产品的市场接受度。
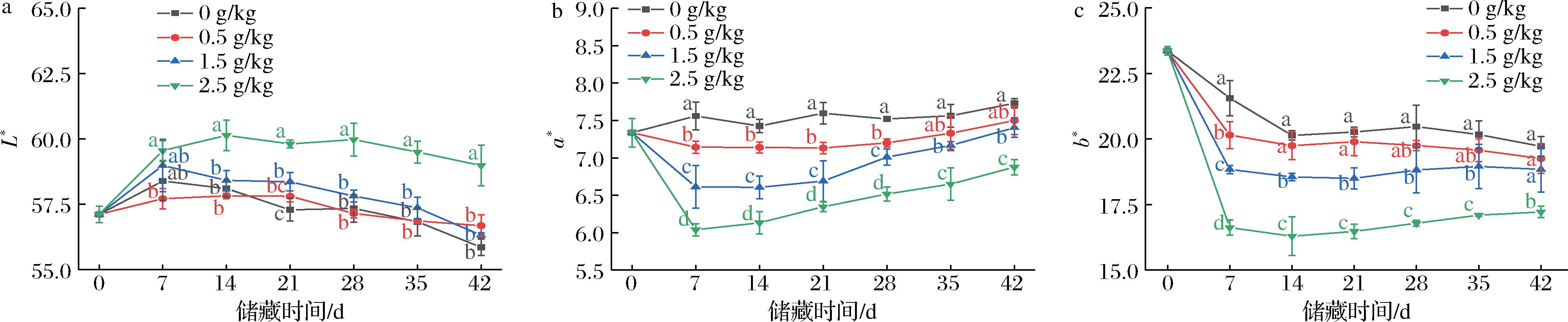
a-L*值;b-a*值;c-b*值
图8 玉米储藏期间色泽变化
Fig.8 Color changes of maize during storage
2.9 玉米储藏期间Zn2+迁移量的变化
Zn是必需的微量矿物元素之一,在粮食以及饲料方面具有重要的功能。具有提高粮食生长性能、抑制有害菌生长以及在饲料中为畜禽提供Zn等作用,低添加量的Zn积累有利于强化玉米的营养指标[34]。
在模拟储藏前期,玉米中Zn2+含量无显著性变化。随着储藏时间的延长,对照组玉米Zn2+含量无显著性变化;3个ZnO-NPs添加量的玉米Zn2+含量分别增加了3.59、6.95和20.13 mg/kg,迁移率分别为11.97%、23.16%和67.08%(图9)。ZnO-NPs添加量为0.5 g/kg和1.5 g/kg的Zn2+含量相对于对照组而言,无显著性变化;除此之外,ZnO-NPs添加量为0.5 g/kg和1.5 g/kg的Zn2+迁移率符合我国农业农村部第2625号公告规定的Zn最高限量为110 mg/kg,也符合在此基础上允许使用的ZnO至1.6 g/kg[35]。实验结果说明,在长期的储藏过程中,少量的ZnO-NPs的添加有效保持了玉米细胞结构的完整性和能量代谢能力,与TEM的观察结果相符,这可能是低添加量ZnO-NPs有效地向玉米供应微量营养素锌,有利于玉米下游的工业化发展,与前期实验结果一致。
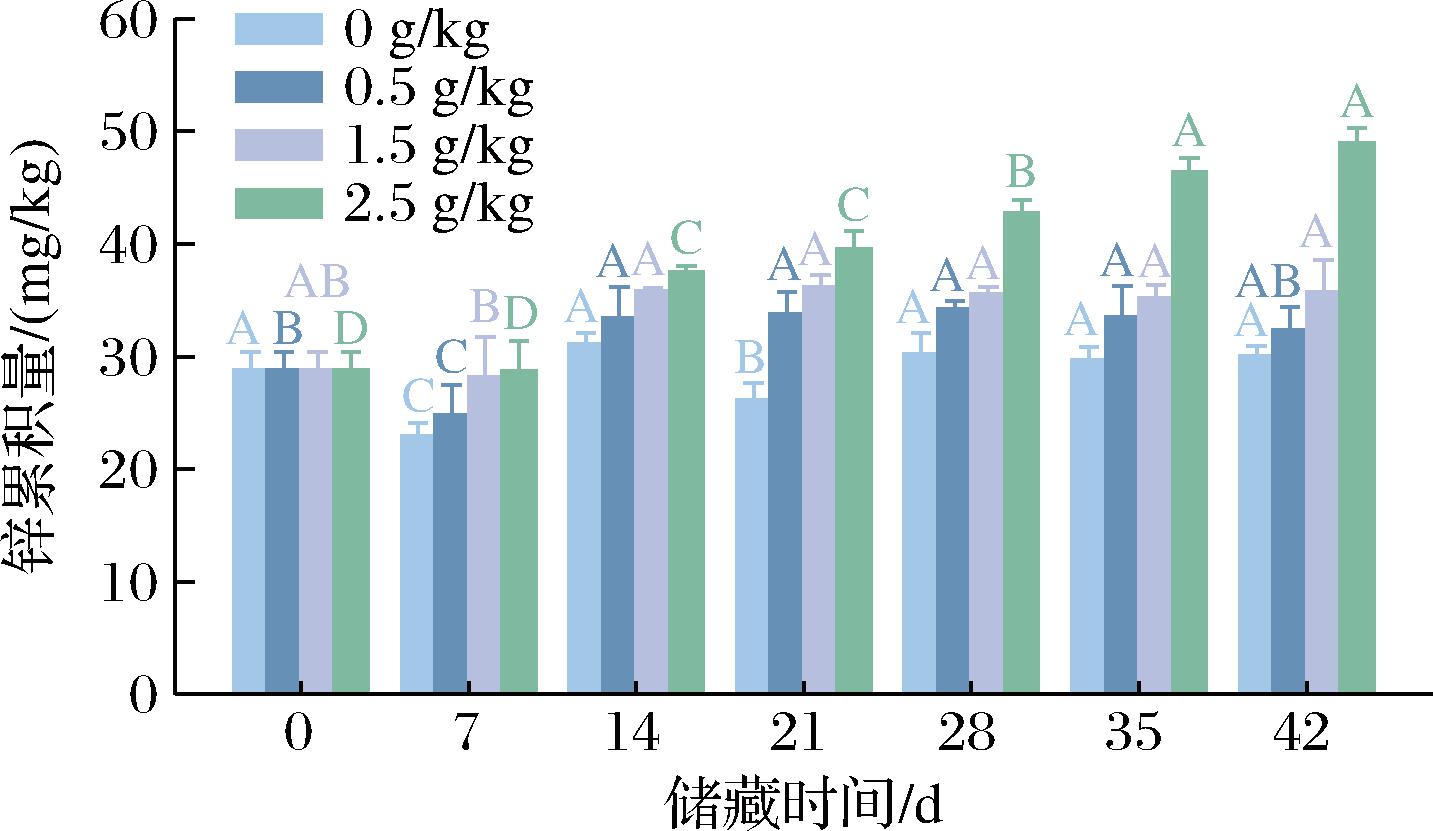
图9 玉米储藏期间锌积累量变化
Fig.9 Changes of zinc accumulation in maize during storage
3 结论与讨论
针对ZnO-NPs延缓粮食品质劣变的重要现象,研究聚焦在对细胞结构和生理活性的影响,研究结果表明,随储藏时间的延长,添加0.5 g/kg和1.5 g/kg ZnO-NPs的玉米,电导率、MDA、过氧化氢含量和超氧阴离子产生速率显著低于对照组,POD活力和SOD活力显著高于对照组,玉米色泽和细胞结构保持良好,Zn2+在细胞内无显著性积累,实验结果显著优于对照组。适当添加量ZnO-NPs的作用可能会提高玉米中某些生理活性物质并增加玉米的抗氧化能力,进而影响玉米在食品加工中的应用性能;改善玉米籽粒的色泽,能够更好的提高玉米下游产业的市场接受度。研究结果说明,一方面适宜ZnO-NPs添加量维持了玉米储藏过程中细胞的完整以及较好的生理活性,减缓了玉米储藏过程中的品质劣变,有利于玉米的安全储藏;另一方面有助于揭示ZnO-NPs对储藏过程中玉米品质的保护机制,为进一步开发玉米储藏品质保护剂提供了数据基础。
[1] TIMM N D, CORADI P C, BILHALVA N D, et al.Effects of corn drying and storage conditions on flour, starch, feed, and ethanol production:a review[J].Journal of Food Science and Technology-mysore, 2020, 46(5):1-8.
[2] LARA N, VIZUETE K, DEBUT A, et al.Underutilized maize kernels (Zea mays L.var.amylacea and var.saccharata) subjected to pan and microwave toasting:A comparative structure study in the whole kernel[J].Journal of Cereal Science, 2021, 100(5):14-25.
[3] NIU Y, XIANG Y.An overview of biomembrane functions in plant responses to high-temperature stress[J].Frontiers in Plant Science, 2018, 9(10):23-41.
[4] CORADI P C, NUNES M T, BELLOCHIO S D, et al.Effects of drying temperatures and storage conditions on the levels of lipids and starches in corn grains for yield ethanol industry[J].Biofuels-Uk, 2022, 13(6):745-754.
[5] 钱佳成. 不同储藏条件下玉米品质变化研究[D].南京财经大学, 2020.QIAN J C.Study on the changes of maize quality under different storage conditions[D].Nanjing University of Finance and Economics, 2020.
[6] HERNANDEZ-MELENDEZ D, SALAS-TELLEZ E, ZAVALA-FRANCO A, et al.Inhibitory effect of flower-shaped zinc oxide nanostructures on the growth and aflatoxin production of a highly toxigenic strain of aspergillus flavus link[J].Materials, 2018, 11(8):25-36.
[7] SRIVASTAV A, GANJEWALA D, SINGHAL R K, et al.Effect of zno nanoparticles on growth and biochemical responses of wheat and maize[J].Plants-Basel, 2021, 10(12):47-58.
[8] SELIM Y A, AZB M A, RAGAB I, et al.Green synthesis of zinc oxide nanoparticles using aqueous extract of deverra tortuosa and their cytotoxic activities[J].Scientific Reports, 2020, 10(1):15-20.
[9] ISCHENKO V, POLARZ S, GROTE D, et al.Zinc oxide nanoparticles with defects[J].Advanced Functional Materials, 2005, 15(12):1945-1954
[10] ZHANG D D, HU S, WU Q, et al.Construction of ZnO@mSiO2 antibacterial nanocomposite for inhibition of microorganisms during Zea mays storage and improving the germination[J].LWT-Food Science and Technology, 2022, 168:9-15.
[11] LIU Y L, CAO X S, YUE L, et al.Foliar-applied cerium oxide nanomaterials improve maize yield under salinity stress:Reactive oxygen species homeostasis and rhizobacteria regulation[J].Environmental Pollution, 2022, 299:31-47.
[12] 王若兰, 张丽丽, 曹志帅, 等.储藏微环境下小麦胚细胞超微结构变化及衰老机制研究[J].中国粮油学报, 2014, 29(10):77-82.WANG R l, ZHANG L L, CAO Z S, et al.Study on ultrastructural changes and senescence mechanism of wheat germ cells under storage microenvironment[J].Chinese Journal of Cereals and Oils, 2014, 29 (10):77-82.
[13] EMMANUEL E S C, ANANDKUMAR B, NATESAN M, et al.Efficacy of rare earth elements on the physiological and biochemical characteristics of Zea mays L[J].Australian Journal of Crop Science, 2010, 4(4):289-294.
[14] PIASECKI C, RIZZARDI M A, SCHONS J, et al.Interference of volunteer corn on stress metabolism and yield of dry beans[J].Planta Daninha, 2018, 36:17-23.
[15] MUHAMMAD I, YANG L, AHMAD S, et al.Melatonin-priming enhances maize seedling drought tolerance by regulating the antioxidant defense system[J].Plant Physiol, 2023, 191(4):10-15.
[16] LIU J, LIU S, ZHANG X, et al.Effect of gallic acid grafted chitosan film packaging on the postharvest quality of white button mushroom (Agaricus bisporus)[J].Postharvest Biology and Technology, 2019, 147:39-47.
[17] 马良. 超低水分含量小麦和玉米储藏稳定性研究[D];河南工业大学, 2015.MA L.Study on storage stability of ultra-low moisture content wheat and maize[D].Henan University of Technology, 2015.
[18] PRERNA D I, GOVINDARAJU K, TAMILSELVAN S, et al.Influence of nanoscale micro-nutrient alpha-Fe2O3 on seed germination, seedling growth, translocation, physiological effects and yield of rice (Oryza sativa) and maize (Zea mays)[J].Plant Physiology and Biochemistry, 2021, 162:564-580.
[19] SALAM A, KHAN A R, LIU L, et al.Seed priming with zinc oxide nanoparticles downplayed ultrastructural damage and improved photosynthetic apparatus in maize under cobalt stress[J].Journal of Hazardous Materials, 2022, 45(4):30-45.
[20] 薛飞, 王若兰, 肖蕾, 等.不同储藏条件对优质稻胚细胞超微结构及抗氧化酶系统活性影响的研究[J].河南工业大学学报(自然科学版), 2018, 39(05):51-57.XUE F, WANG R L, XIAO L, et al.Effects of different storage conditions on ultrastructure of embryo cells and activities of antioxidant enzyme system in high quality rice[J].Journal of Henan University of Technology (Natural Science Edition), 2018, 39 (05):51-57.
[21] XU Y Z, MA P G, NIU Z P, et al.Effects of artificial aging on physiological quality and cell ultrastructure of maize (Zea mays L.)[J].Cereal Research Communications, 2023, 51(3):615-626.
[22] 张腾. 施用纳米氧化锌对小麦锌营养以及籽粒品质的影响[D].杨凌:西北农林科技大学, 2018.ZHANG T.Effects of nano-zinc oxide on zinc nutrition and grain quality of wheat[D].Yangling:Northwest University of Agriculture and Forestry, 2018.
[23] SUN L Y, SONG F B, GUO J H, et al.Nano-ZnO induced drought tolerance is associated with melatonin synthesis and metabolism in maize[J].International Journal of Molecular Sciences, 2020, 21(3):18-25.
[24] 周显青, 赵金凤, 张咚咚, 等.氧化锌纳米颗粒对玉米储藏过程中霉菌区系及其品质的影响[J].食品安全质量检测学报, 2023, 14(03):252-259.ZHOU X Q, ZHAO J F, ZHANG D D, et al.Effects of ZnO nanoparticles on mold flora and quality of corn during storage[J].Journal of Food Safety and quality Inspection, 2023, 14 (03):252-259.
[25] MANAL E-Z, NASEEM A A-W, SAMEERA O B.Foliar sprayed green zinc oxide nanoparticles mitigate drought-induced oxidative stress in tomato[J].Plants, 2021, 10(11):2400-2414.
[26] 杨剀舟, 魏征, 栾霞, 等.水分调节协同微波处理米糠储藏期品质变化规律的研究[J].中国粮油学报:1-16.YANG X Z, WEI Z, LUAN X, et al.Study on the quality change of rice bran during storage by moisture regulation combined with microwave treatment[J].Chinese Journal of Cereals and Oils:1-16.
[27] KHAN M N, MOBIN M, ABBAS Z K, et al.Role of nanomaterials in plants under challenging environments[J].Plant Physiol Biochem, 2017, 110:194-209.
[28] PRAKASH M G, CHUNG I M.Determination of zinc oxide nanoparticles toxicity in root growth in wheat (Triticum aestivum L.) seedlings[J].Acta Biol Hung, 2016, 67(3):286-296.
[29] GANGWAR R.Comparative Insilco functional, structural and phylogenetic characterization of plant Mn-Superoxide Dismutase[J].BioRxiv, 2022.
[30] MEHMOOD S, OU W, AHMED W, et al.ZnO nanoparticles mediated by Azadirachta indica as nano fertilizer:Improvement in physiological and biochemical indices of Zea mays grown in Cr-contaminated soil[J].Environ Pollut, 2023,14(4):122-155.
[31] KHAN Z S, RIZWAN M, HAFEEZ M, et al.The accumulation of cadmium in wheat (Triticum aestivum) as influenced by zinc oxide nanoparticles and soil moisture conditions[J].Environ Sci Pollut Res Int, 2019, 26(19):1985-1987
[32] ZILIC S, MOGOL B A, AKILLIOGLU G, et al.Effects of infrared heating on phenolic compounds and Maillard reaction products in maize flour[J].Journal of Cereal Science, 2013, 58(1):1-7.
[33] ZHENG Z, NIU L Y, YANG W C, et al.Degradation of zearalenone by dielectric barrier discharge cold plasma and its effect on maize quality[J].Foods, 2023, 12(6):10-19.
[34] DONIA D T, CARBONE M.Seed priming with zinc oxide nanoparticles to enhance crop tolerance to environmental stresses[J].Int J Mol Sci, 2023, 24(24):34-42.
[35] 中华人民共和国农业部公告第2625号[J].乳业科学与技术, 2018, 41(1):47-51.Notice No.2625 of the ministry of agriculture of the people’s republic of china[J].Science and Technology of Dairy Industry, 2018, 41(1):47-55.