2-苯乙醇(2-phenethyl alcohol,2-PE)具有独特的玫瑰花香气,天然存在于多种蔬果花卉的精油中。因其具有香柔甜和的特性,2-苯乙醇也是啤酒、白酒、黄酒和葡萄酒中重要的风味物质,能够提升酒的品质[1]。在烘焙食品以及各类零食中可作为食用香精添加以丰富口感。2-苯乙醇也是调配其他香型香料的原料之一,作为香精应用在护肤品、化妆品、肥皂和香水等中。2-苯乙醇对革兰氏阴性菌、球菌、杆菌和一些真菌有抑菌作用,因此可作为原料生产果蔬保鲜剂、抑菌药物等。另外,2-苯乙醇还是一些药物的合成前体,例如乙酸苯乙酯是神经类药物的成分,1-异丙氨基-3-(对-(2-甲氧乙基)苯氧基)-2-丙醇是高血压、心脏病药物的成分等[2-3]。
随着食品、日化用品[4]、医药等产业的蓬勃发展,2-苯乙醇市场需求量在逐年上升[5]。2-苯乙醇传统获得方法是从植物的精油中萃取[6-7],所获得的产物具有安全、天然的特性。但该方法耗时耗力,流程复杂,产率较低,难以满足庞大的市场需求。目前工业上用来生产2-苯乙醇的方法主要还是化学合成法[8]。该方法效率高,但是所获得的产物中副产物和杂质偏多,并且所用的原料具有一定的致癌风险,所以化学合成法获得的产物使用范围受限[9]。所以研究者们普遍认为生物法生产2-苯乙醇最为可靠。
许多酵母菌中天然存在合成2-苯乙醇的代谢路径,因此可用安全可靠的底物,在温和的条件下,通过生物法合成2-苯乙醇。在酵母菌中,合成2-苯乙醇的途径主要有两个(图1)[10]。一是通过借助合成芳香族氨基酸的莽草酸途径(shikimate pathway),以葡萄糖为前体进行从头合成。二是经艾氏途径即埃里希途径(ehrlich pathway)合成2-苯乙醇[11]。具体反应途径如下:以L-苯丙氨酸(L-phenylalanine,L-phe)为前体,利用柠檬酸循环(tricarboxylic acid cycle,TCA)产生的α-酮戊二酸(α-ketoglutaric acid,α-KG)通过转氨反应生成苯丙酮酸(3-phenylpyruvic acid,PPA),再脱羧形成苯乙醛(phenylacetaldehyde,PPAL),PPAL在醇脱氢酶或苯乙醛还原酶的作用下生成2-PE。这两个代谢路径是同时存在的,而2-苯乙醇通过何种路径合成取决于培养基中氮源的种类。当培养基使用多种容易为菌体所利用的氮源即优质氮源时,如酵母粉、尿素,酵母细胞借助于芳香族氨基酸合成的莽草酸途径,将磷酸烯醇式丙酮酸(phosphoenolpyruvate,PEP)和赤藓糖-4-磷酸(erythrose 4-phosphate,E4P)合成3-脱氧-D-阿拉伯庚酮糖-7-磷酸(3-deoxy-D-arabino-heptulosonate-7-phosphate,DAHP),而后代谢产生莽草酸(shikimic acid,SHIK),而后通过合成2-苯乙醇;而当L-phe作为唯一氮源存在时,酵母则通过艾氏途径合成2-苯乙醇。此过程只需3个反应,路径较短,且受到的调控相对简单,因此更占优势。出于合成效率、收率、代谢改造及经济价值的多方面考虑,目前的研究大多是以通过艾氏途径以L-苯丙氨酸为前体合成2-苯乙醇为主。
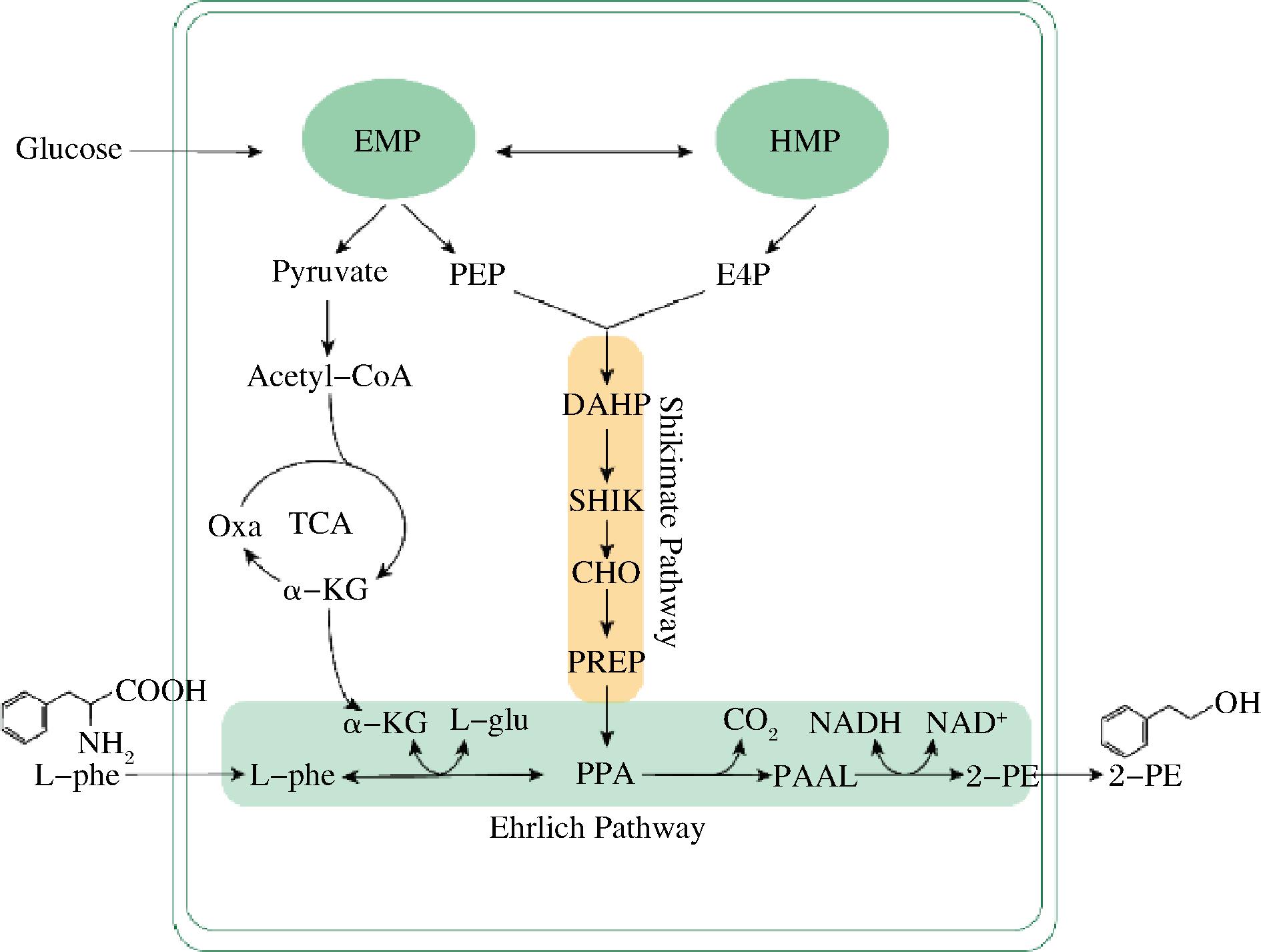
图1 酵母菌2-苯乙醇合成路径
Fig.1 Biosynthesis pathway of 2-phenylethanol in yeast
注:EMP:糖酵解途径(embden-meyerhof-parnas pathway); HMP:磷酸戊糖途径(hexose monophosphate pathway); TCA:三羧酸循环(tricarboxylic acid cycle); Oxa:草酰乙酸(oxaloacetic acid); α-KG:α酮戊二酸(α-ketoglutarate);PEP:磷酸烯醇式丙酮酸(phosphoenolpyruvate); E4P:赤藓糖-4-磷酸(erythrose-4-phosphate);DAHP:3-脱氧-D-阿拉伯-庚酮糖(3-deoxy-D-arabinoheptulosonate); SHK:莽草酸途径(shikimate);CHO:分支酸(chorismite); PREP:预苯酸(prephenate);L-phe:L-苯丙氨酸(L-phenylalanine); PPA:苯丙酮(phenylpyruvate); PAAL:苯乙醛(phenylacetaldehyde); 2-PE:2-苯乙醇(2-phenylethanol)。
利用微生物发酵法合成2-苯乙醇是实验室研究所常用的主要方法,但目前面临一些瓶颈问题。一是苯乙醇本身具有毒性[12],对细胞生长有抑制作用,大量研究表明当2-苯乙醇浓度达到3~4 g/L时就会完全抑制酵母菌株的生长。当发酵液中的2-苯乙醇的浓度超过致死浓度时,2-苯乙醇将不再合成,因此细胞对产物的耐受程度决定了菌株的生产能力。二是酵母菌对艾氏途径的底物L-苯丙氨酸的转运效率低[13],当培养基中有其他优质氮源时,细胞将不再利用L-苯丙氨酸从而无法生成2-苯乙醇[14-15]。生物转化[16]的方法是将生长到对数中后期的酵母菌收集,洗涤重悬在催化体系中,2-苯乙醇的产量为2.24 g/L。生物转化法使2-苯乙醇对细胞的毒性影响相对较小,且转化体系中不添加酵母粉和蛋白胨等优质氮源,酵母能够更大程度地利用L-phe。KIM等[17]用酿酒酵母W303-113菌株进行代谢工程改造,通过摇瓶发酵其2-苯乙醇产量达到4.8 g/L。WANG等[18]在大肠杆菌BW251113中构建了一种辅因子自给自足系统,用生物转化的方法使2-苯乙醇的产量达到5.32 g/L。筛选野生型菌株生物法合成2-苯乙醇也是一种非常有效的策略,本研究利用从发酵酱醪中筛选出的一株野生型生香酵母-贝酵母,通过发酵优化方法使2-苯乙醇的产量提高到了6.05 g/L。
1 材料与方法
1.1 材料与试剂
MgSO4·7H2O、葡萄糖、K2HPO4、KH2PO4、正庚烷、CuSO4·5H2O、FeSO4·7H2O、MnCl2·4H2O、CaCl2·2H2O、ZnCl2、甘油,上海国药集团化学试剂有限公司;L-phe,河北百灵威有限公司;2-苯乙醇,上海麦克林生化科技股份有限公司;蛋白胨、酵母粉,英国OXIOD公司;YNB无氨基酵母氮源,BBI生命科学有限公司;琼脂,德国biofroxx公司。
1.2 仪器与设备
HYL-C3摇床,太仓市强乐实验设备有限公司;PHSJ-4A实验室PH计,上梅特勒-托利多仪器有限公司;UV-1800紫外可见分光光度计,翱艺仪器(上海)有限公司;FilterMax F5/F3酶标仪,美国伯腾仪器有限公司。
1.3 培养基及溶液配制
a)YPD培养基(g/L):10酵母提取物,20蛋白胨,20葡萄糖,115 ℃灭菌30 min;
b)2×YPD培养基(g/L):20酵母提取物,40蛋白胨,40葡萄糖,115 ℃灭菌30 min;
c)转化体系(g/L):20葡萄糖,0.4 MgSO4·7H2O,5 KH2PO4,1.7 YNB,8 L-phe,115 ℃灭菌30 min;
d)PBS(g/L):称取8.5 NaCl,2.2 Na2HPO4和0.4 NaH2PO4,用HCl溶液调节pH至7.0即可。
e)离子混合营养液(g/L):0.05 CuSO4·5H2O,2 FeSO4·7H2O,0.2 MnCl2·4H2O,2 CaCl2·2H2O,0.5 ZnCl2,用HCl溶液将pH值调至6.0。
1.4 实验方法
1.4.1 菌株的保藏与活化
菌株保藏:将菌液与30%体积分数的甘油1∶1混合于保菌管中,至于-80 ℃冷冻保存。
菌株活化:将实验室保藏的菌液用平板划线于YPD平板上放置30 ℃的恒温培养箱进行培养1~2 d,获得活化菌株。
1.4.2 酵母的培养方法
将单菌落或菌液接种于2×YPD液体培养基中,置于30 ℃、250 r/min的摇床中培养12 h。
1.4.3 酵母的生物转化方法
在活化的平板中挑取单菌落于装有YPD的试管中,置于30 ℃、250 r/min摇床中培养12 h后,按照5%接种量转接于2×YPD液体培养基中培养12 h。收集湿菌体并用pH=7的PBS洗两次后,按照20%接种量接种于转化体系中,在30 ℃、250 r/min的摇床中转化60 h左右。
1.4.4 生物量的测定
按照一定的比例将菌液稀释至合适的浓度,加入96酶标仪板中,置于600 nm处测定其吸光值。
1.4.5 2-苯乙醇的紫外检测法
根据文献查询2-苯乙醇的紫外检测方法[19],将不同浓度的2-苯乙醇标准液或发酵液样品8 000 r/min离心10 min取上清液0.5 mL,加入5 mL正庚烷萃取,充分振荡后静置30 min。上层含有2-苯乙醇的正庚烷萃取液可直接加入酶标仪板中,检测其在258 nm处的吸光值。通过制备的标准曲线计算其2-苯乙醇的浓度。
1.4.6 2-苯乙醇标准曲线的制备
配制标准品2-苯乙醇质量浓度为1~8 g/L水溶液,按照1.4.5节方法制备正庚烷的2-苯乙醇萃取液,于波长258 nm处测定其吸光度,以2-苯乙醇质量浓度(C,g/L)为横坐标,A258为纵坐标,绘制成标准曲线如图。
如图2所示,2-苯乙醇在1~ 8 g/L质量浓度范围内与A258线性关系良好,得到回归方程A=0.096 8C+0.186,R2=0.997 9。由回归方程可直接计算出样品中的2-苯乙醇含量。
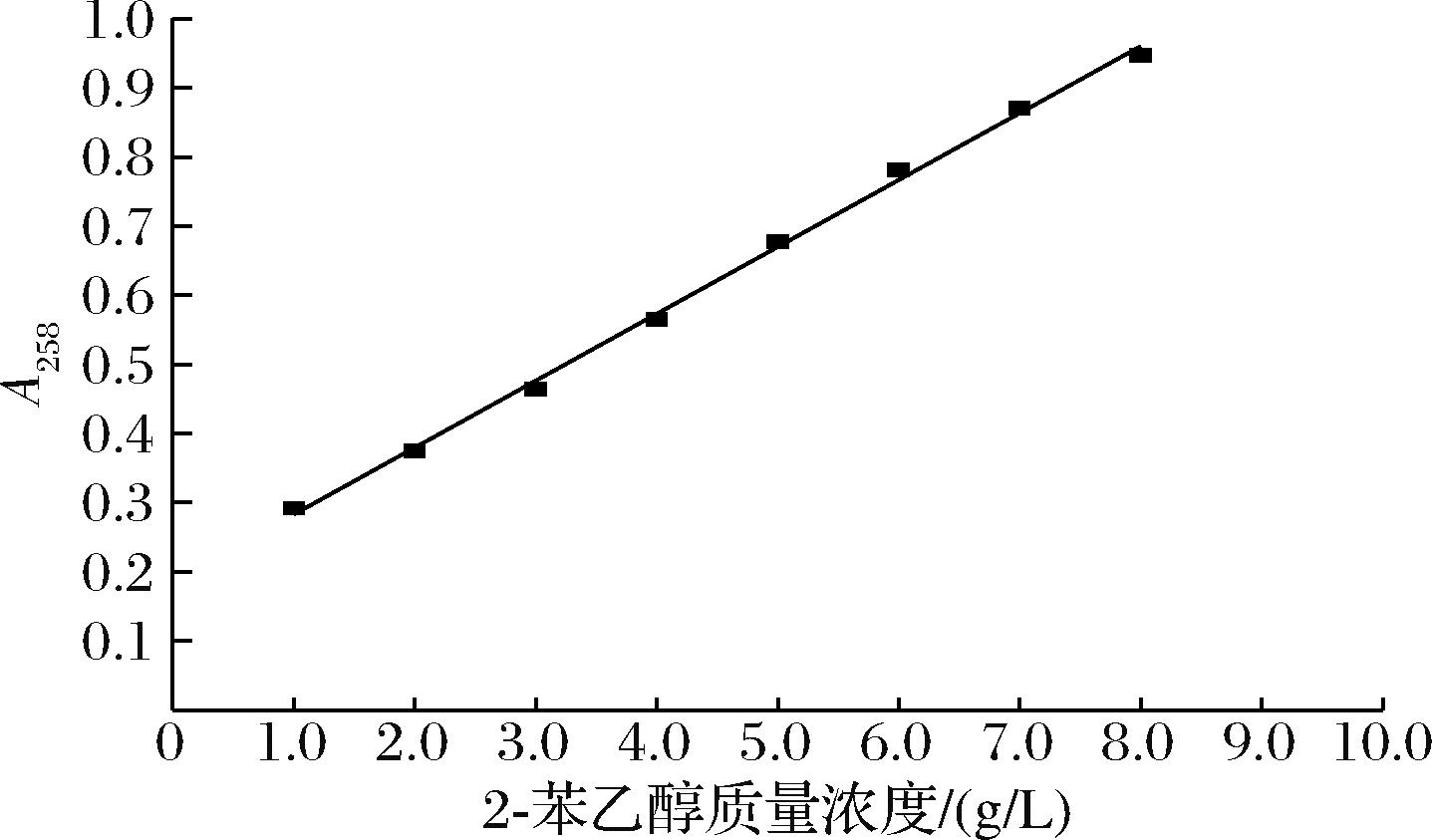
图2 2-苯乙醇质量浓度-A258标准曲线
Fig.2 2-PE concentration-A258 standard curve
1.4.7 菌株对2-苯乙醇耐受性检测
将生香酵母活化后在YPD培养基中培养至对数中后期,并稀释至OD600为1.0制备成菌体悬液。接种于在添加0~7 g/L 2-苯乙醇的YPD培养基中,30 ℃,250 r/min摇床培养48 h,每隔8 h取样测OD,绘制其生长曲线。另外再将菌悬液分别稀释10-3、10-4、10-5倍,取100 μL涂布在0~5 g/L 2-苯乙醇的YPD平板上置于30 ℃恒温培养箱中培养2 d观察其菌落情况。
1.4.8 2-苯乙醇合成优化实验
为提高转化率,需对转化体系中碳源种类(葡萄糖、果糖、蔗糖、麦芽糖、糖蜜、甘油和糊精)及其添加质量浓度(20、30、40、50、60、80、90、100 g/L)进行优化,并且额外添加氨基受体α-酮戊二酸(0、0.2、0.5、0.8、1、2、3 g/L)和离子混合营养液(0、0.2、0.5、0.8、1、2、3 mL/L)提高转化率,并且实验考察了pH(4.5、5、6、7、7.5、8),转化体系(10、20、30、40、50、60、70 mL/L)和温度条件(20、24、26、28、30、32、35、37 ℃)对2-苯乙醇转化的影响。
2 结果与分析
2.1 菌株耐受性检测
本研究从发酵酱醪中筛选出的贝酵母发酵后,产生的风味物质主要有2-苯乙醇、异戊酸、2-甲基丁酸、1-辛烯-3-醇、苯乙醛、异戊醛、乙偶姻、异丁酸、苯甲醛、壬醛等香气物质,属于一种生香酵母。2-苯乙醇对酵母具有的一定的毒性,这也是限制其产量的主要原因之一。而不同的酵母所受到的抑制情况不同,按照1.5.1节的方法考察酵母菌对2-苯乙醇的耐受性。结果显示(图3),不论是酿酒酵母还是生香酵母,2-苯乙醇对其都有着强烈的抑制作用,并且随着2-苯乙醇的浓度增加,抑制情况加剧。对于本研究所用的生香酵母菌株,当苯乙醇质量浓度达到4 g/L时,抑制情况明显,当达到5 g/L时,生香酵母生长完全受到抑制。而酿酒酵母在4 g/L质量浓度条件下已不再生长,由此可见生香酵母较酿酒酵母具有更好的耐受性。
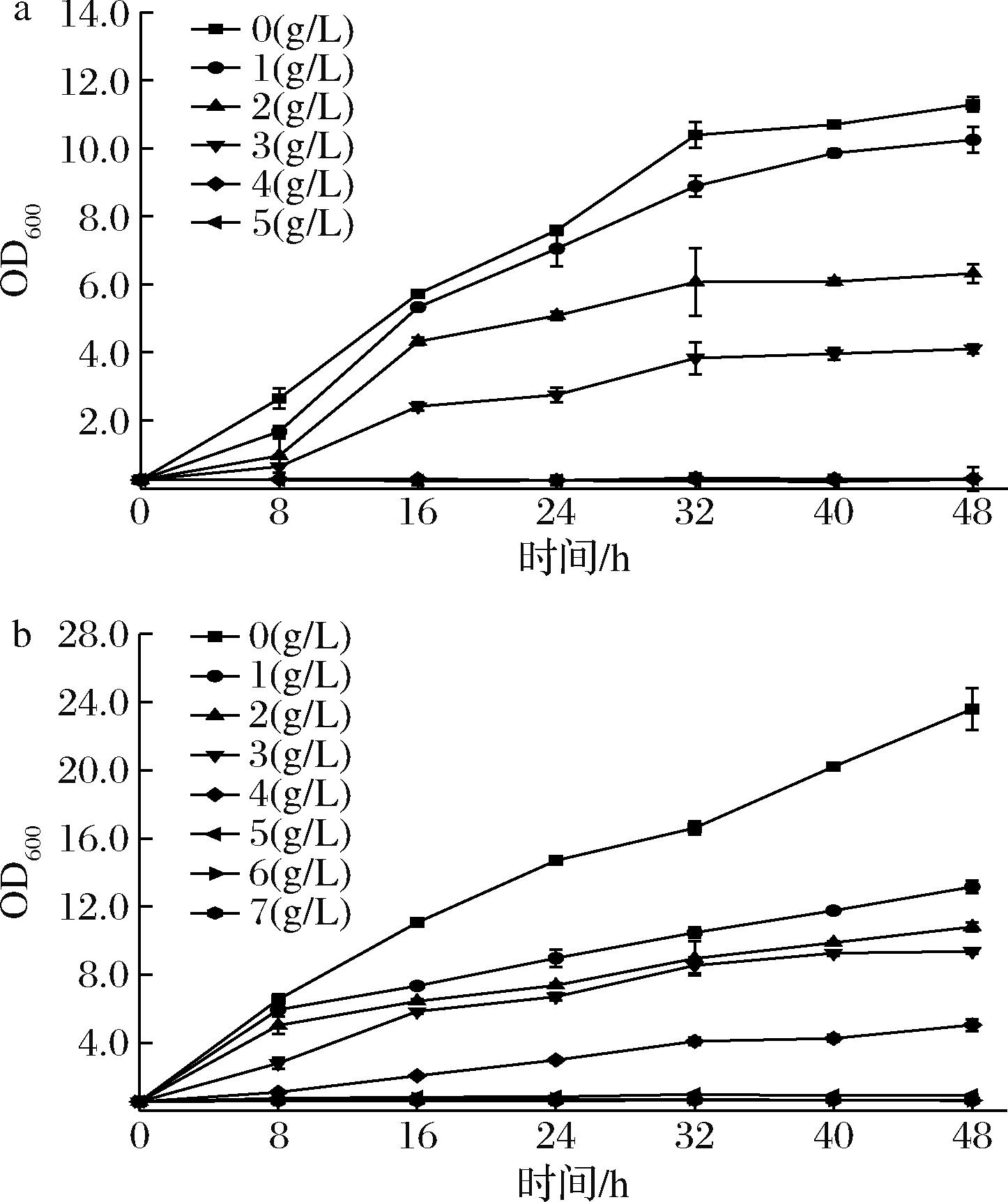
a-酿酒酵母;b-生香酵母
图3 酵母菌对2-苯乙醇耐受性曲线
Fig.3 Tolerance curve of S.bayanus to 2-PE
2.2 2-苯乙醇转化体系优化实验
2.2.1 接种量对转化的影响
接种量是影响产物积累的一个重要因素,接种量小会延长培养时间并降低目标产物的产量,而接种量大会导致新老细胞比例降低和溶解氧不足,影响产物合成。因此,本实验研究了不同接种量对2-苯乙醇生产的影响。接种量为20%(图4-a)时,2-苯乙醇产量达到2.90 g/L,与接种量为10%时相比2-苯乙醇产量增加了30%。随着接种量的增加,生长速率逐渐增加(图4-b),细胞密度也逐渐增加,从而促进2-苯乙醇的合成。然而,当接种量大于20%时,2-苯乙醇产量没有进一步增加。可能是由于过大的接种量导致体系中溶氧不足,细胞更易于产生乙醇,从而抑制2-苯乙醇的生成,导致其产量没有进一步增加。
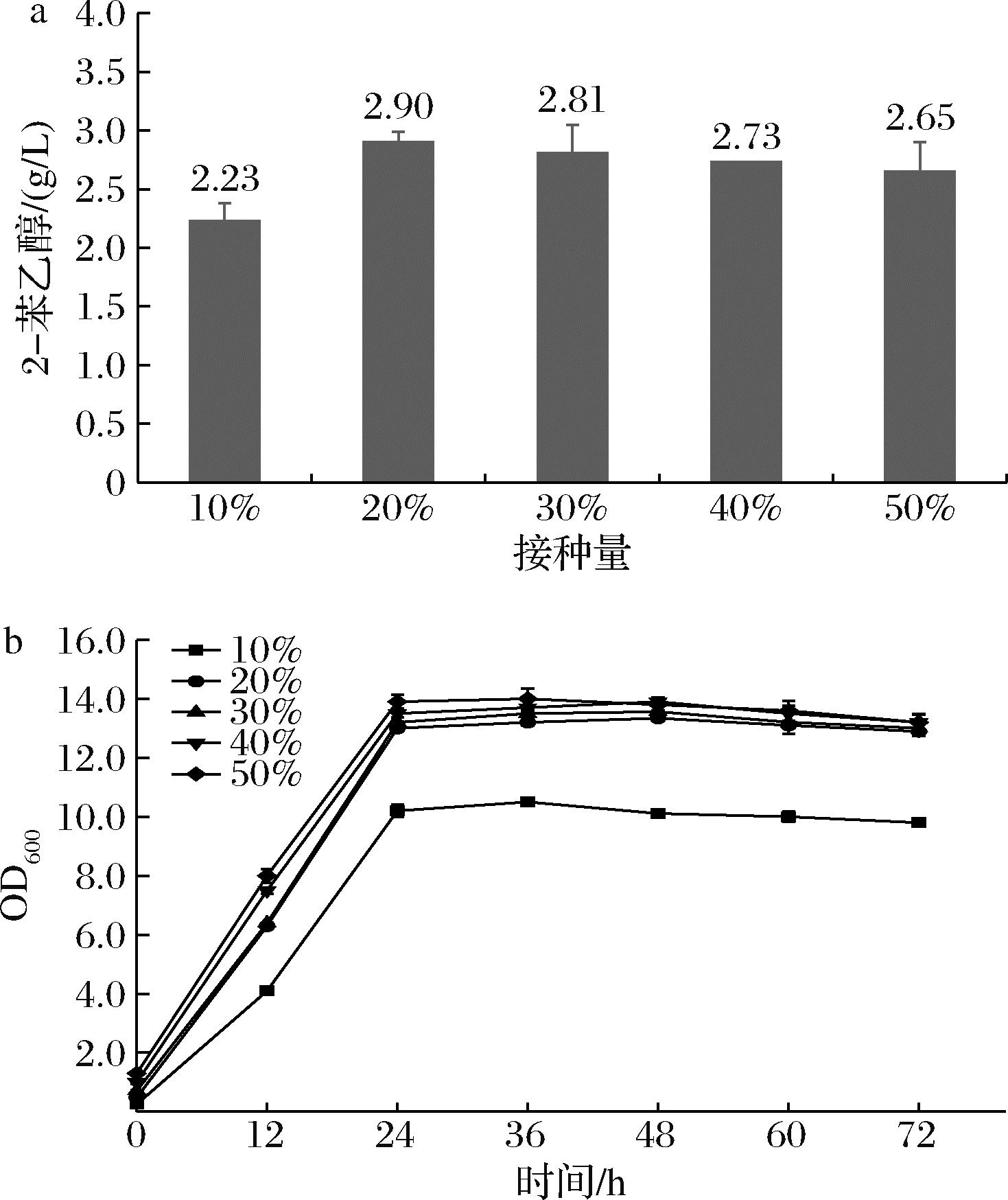
a-2-苯乙醇产量;b-细胞生长曲线
图4 接种量对2-苯乙醇转化的影响
Fig.4 Effects of inoculation amoun on the conversion and synthesis of 2-PE
2.2.2 碳源种类及其浓度对转化的影响
碳源不仅是供给菌体生长的能量来源也是构成菌体碳骨架的原料。为探究不同碳源对2-苯乙醇合成的影响,分别选用了葡萄糖、果糖、蔗糖、麦芽糖、糖蜜、甘油和糊精等7种碳源添加到转化体系中,添加量为20 g/L,其余成分均与1.3节中转化体系相同。转化48 h后2-苯乙醇浓度如图4所示,生香酵母利用这几种碳源均可以转化合成2-苯乙醇,其中葡萄糖、果糖、蔗糖和麦芽糖的产量较高可相差不大,以葡萄糖为碳源时,2-苯乙醇产量为2.89 g/L。以糖蜜、甘油和糊精为碳源时,2-苯乙醇产量分别为1.08、0.32、0.19 g/L,均明显低于以葡萄糖为碳源时2-苯乙醇的产量。因此,选用实验室常用的葡萄糖作为碳源进行后续转化实验。
在此实验基础上进一步考察了葡萄糖浓度对2-苯乙醇合成的影响,葡萄糖质量浓度设置为20~100 g/L。如图5所示,当葡萄糖添加量为20~40 g/L时,随着葡萄糖浓度的增加,2-苯乙醇的浓度显著增加,40 g/L葡萄糖浓度时2-苯乙醇的产量较20 g/L葡萄糖浓度时的产量提高了23.79%。当葡萄糖质量浓度超过40 g/L时,2-苯乙醇的产量呈现出先降低后提高的趋势,基于葡萄糖的利用率,选择葡萄糖的质量浓度为40 g/L进行后续优化。
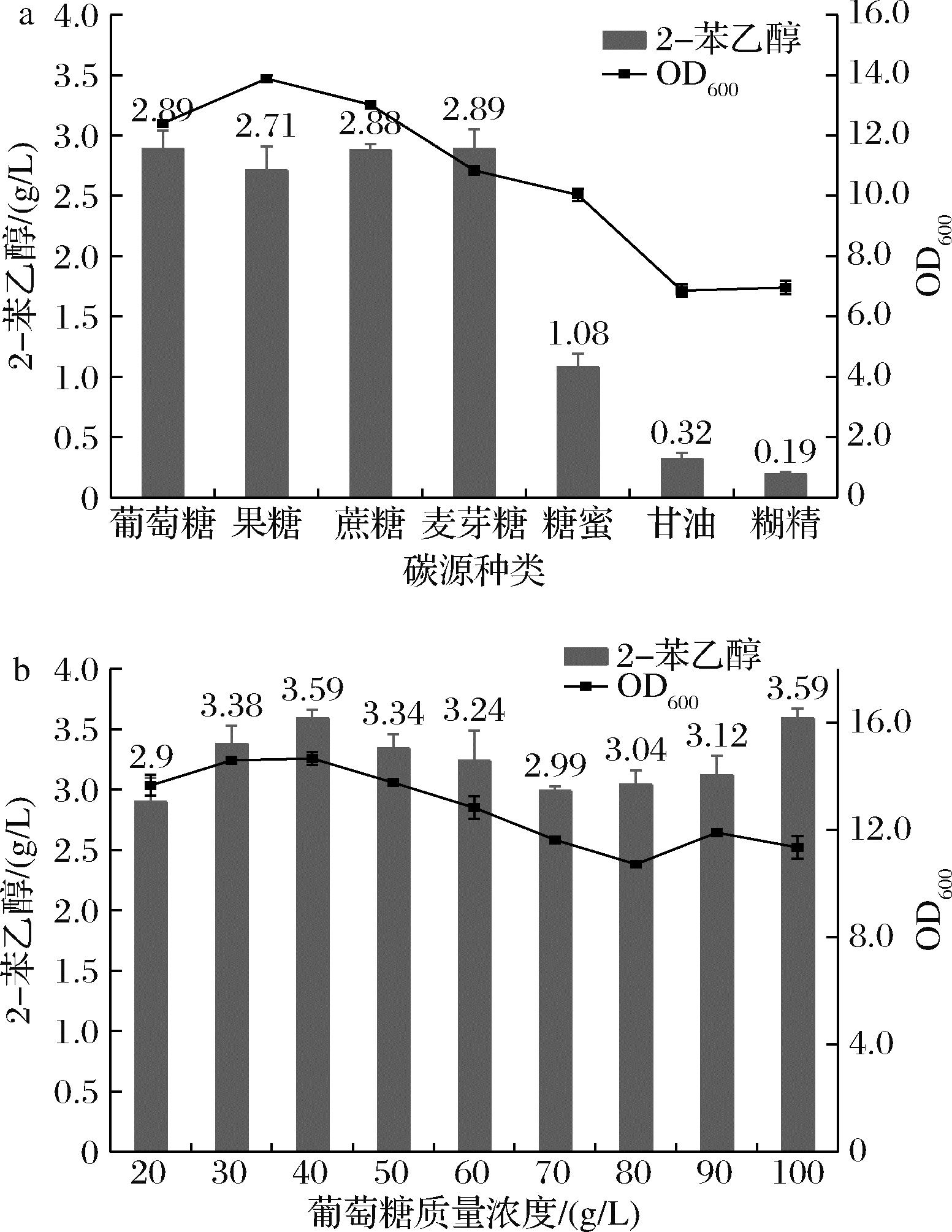
a-碳源种类;b-葡萄糖质量浓度
图5 碳源对2-苯乙醇转化合成的影响
Fig.5 Effects of carbon sources on the conversion and synthesis of 2-PE
2.2.3 添加氨基受体α-酮戊二酸对转化的影响
生香酵母主要通过艾氏途径以L-phe为底物经过转氨基反应、脱羧反应和脱氢反应合成2-苯乙醇。在以往的实验检测出转化体系中添加8 g/L的L-phe,当转化结束以后仍然有3~4 g/L的L-phe残余。在第一步的转氨反应中,α-酮戊二酸作为氨基受体主要来自于细胞内部,因此尝试在转化体系中额外添加α-酮戊二酸来促进转氨反应的进行,从而促进艾氏途径的代谢。设置 α-酮戊二酸的添加量为0~3 g/L,结果如图6所示,当其质量浓度为0.5 g/L时,2-苯乙醇的浓度最高,当α-酮戊二酸的添加量大于0.5 g/L时, 2-苯乙醇的浓度则不再增加。推测可能原因是由于已经达到了细胞能够利用的限值,或是添加α-酮戊二酸影响转化体系的pH,从而影响了菌体的生长以及相关酶的活性。
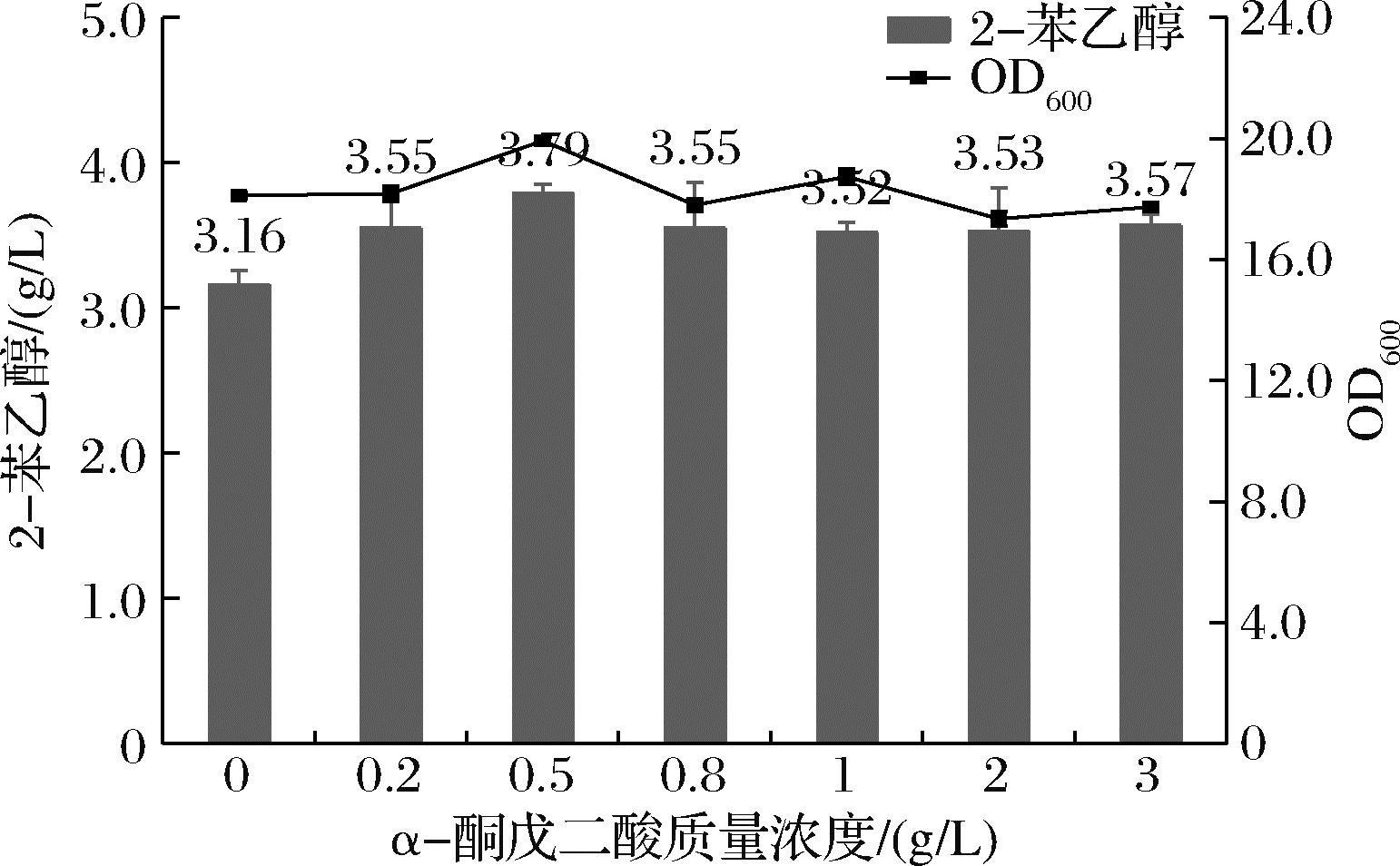
图6 α-酮戊二酸质量浓度对2-苯乙醇转化合成的影响
Fig.6 Effects of different α-ketoglutaric acid concentrations on the conversion and synthesis of 2-PE
2.2.4 无机离子对转化的影响
无机离子不仅是维持细胞生长和生命活动不可或缺的成分之一,也是酶的组成部分。影响着酶的活性,及氧化还原电位,因此无机离子的浓度也关乎着转化效率的高低。实验通过配置含有铜、铁、锰、钙和锌离子的混合营养液按照不同的浓度添加到转化体系中。其结果如图7所示,添加无机离子对2-苯乙醇的转化有促进作用,添加的浓度越高促进作用越明显。当添加2 mL/L的混合营养液时,2-苯乙醇的浓度达到最大值,为4.83 g/L,因此2 mL/L的浓度最适宜转化的进行。
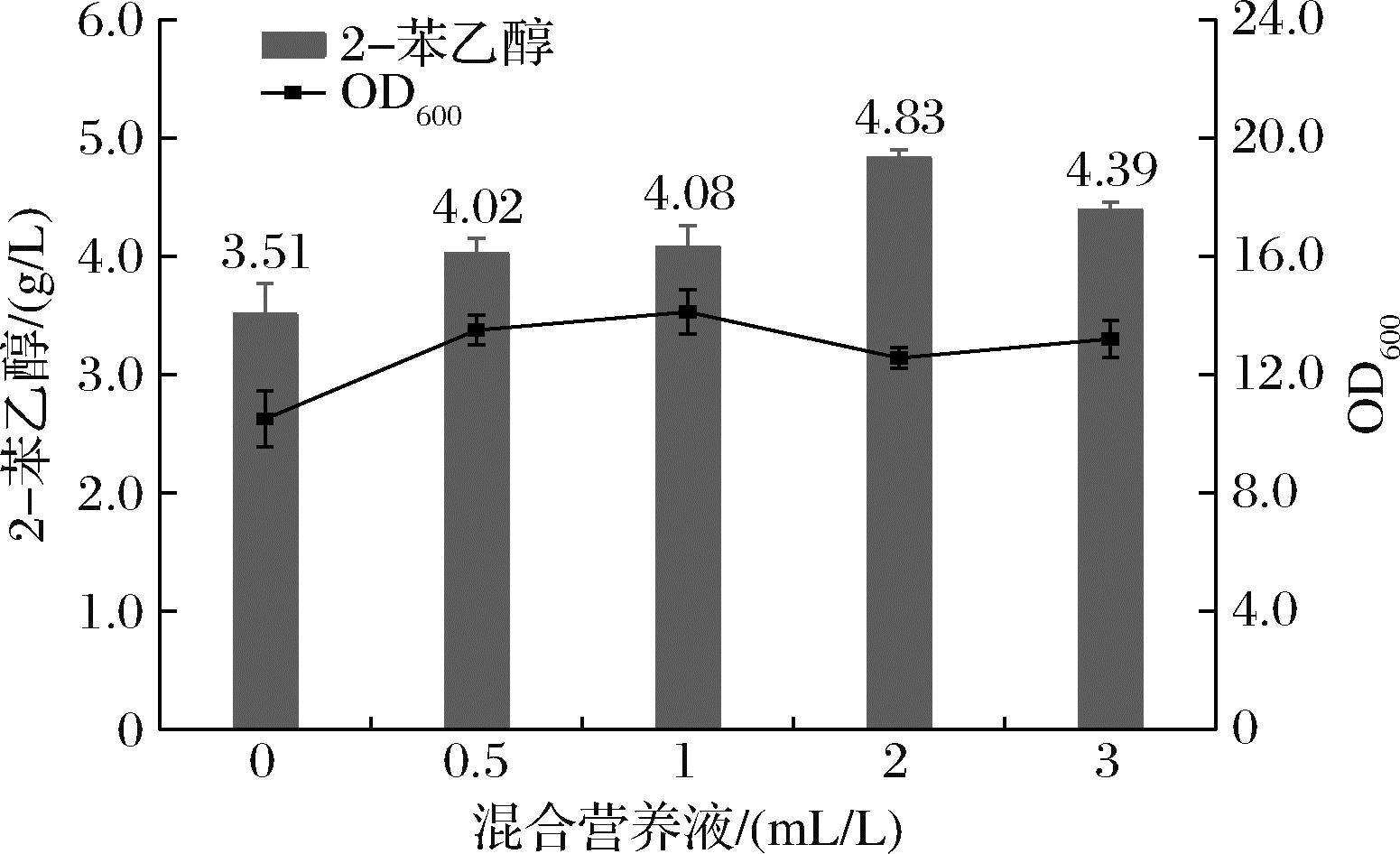
图7 混合营养液对2-苯乙醇转化的影响
Fig.7 Effects of different inorganic ion concentrations on the conversion and synthesis of 2-PE
2.3 2-苯乙醇转化条件的优化
2.3.1 初始pH对转化的影响
酵母嗜好偏酸性的环境,一般最适生长的pH值为5.0~6.0,而不同的pH值也关乎酶的催化效率。由于催化体系中添加的底物L-苯丙氨酸、α-酮戊二酸以及混合无机离子都会影响酸碱度,因此为避免添加物给催化酸碱环境带来的影响,实验研究不同初始pH条件下2-苯乙醇的转化情况。经检测催化体系的pH值为4.3,另外选择pH 5.0、6.0、7.0、7.5和8.0条件,测定转化结束后2-苯乙醇的含量。实验结果表明(图8),当pH值为5.0时,2-苯乙醇的产量最高,为5.11 g/L,因此在后续实验中将采用初始pH值为5作为初始条件。
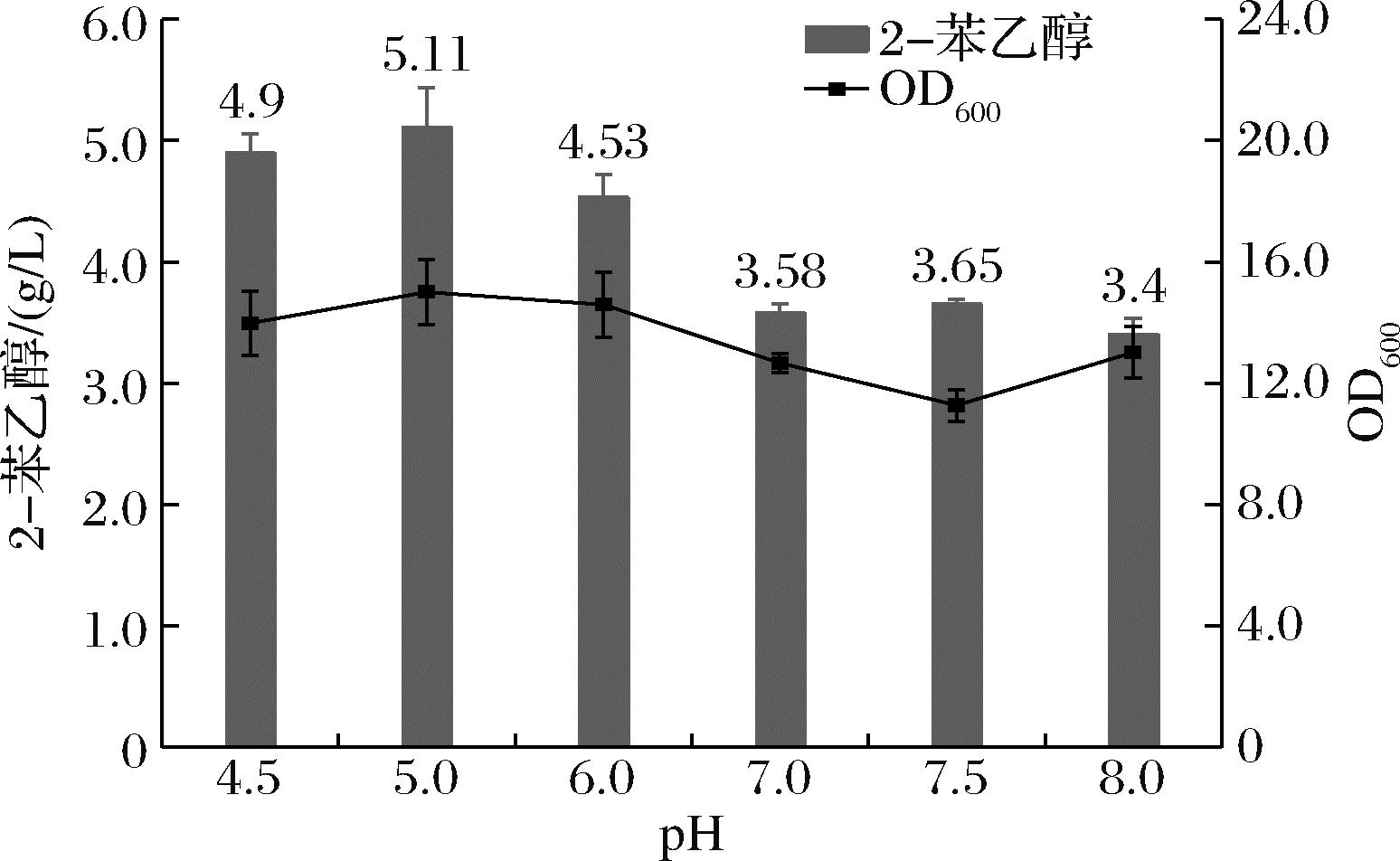
图8 pH对2-苯乙醇转化的影响
Fig.8 Effects of pH on the conversion and synthesis of 2-PE
2.3.2 温度对转化的影响
温度是调控转化的重要因素之一,不仅影响着菌体的生长情况还与酶的活性相关。实验探讨了转化温度分别为20、24、26、28、30、32、35、37 ℃情况下,温度对2-苯乙醇合成的影响。实验结果显示(图9),当转化温度为26 ℃时,2-苯乙醇的产量最高,为5.34 g/L,当转化温度高于30 ℃时,细胞的生长收到抑制,说明该条件更有利于2-苯乙醇的转化。
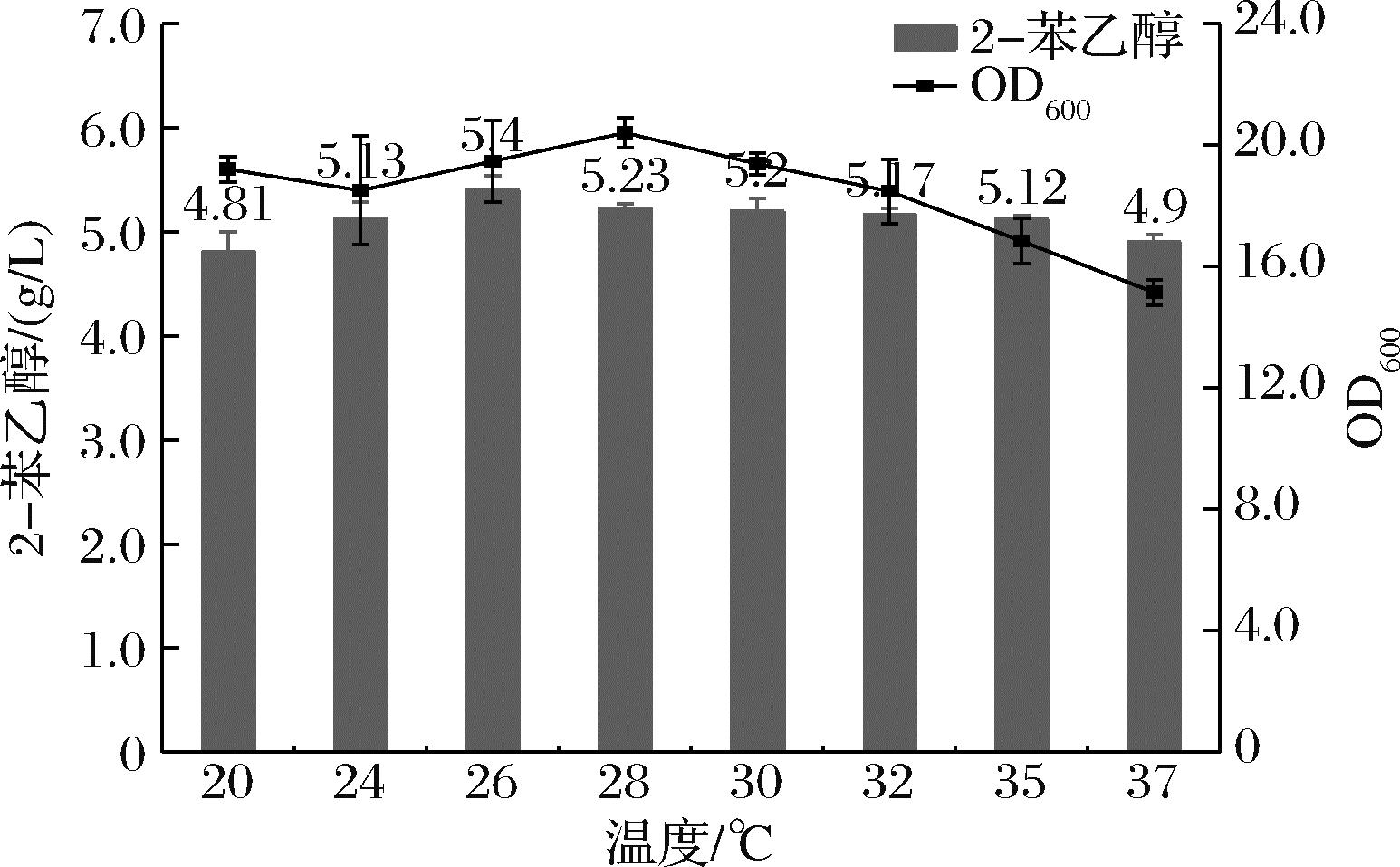
图9 温度对2-苯乙醇转化的影响
Fig.9 Effects of different temperature on the conversion and synthesis of 2-PE transformation
2.3.3 装液量对转化的影响
装液量与对菌体的供氧有关,氧气不足时菌体可利用葡萄糖产生乙醇,一方面经过莽草酸途径生成2-苯乙醇的路径会被分流,另一方面产生的乙醇会抑制菌体生长从而不利于艾氏途径的转化。实验设置在250 mL的锥形瓶中分别装有10、20、30、40、50、60、70 mL的转化液,结果如图10所示。用10 mL的转化体系可使2-苯乙醇的质量浓度达到6.05 g/L,较出发菌株的2-苯乙醇产量(2.89 g/L)提高了109.34%。
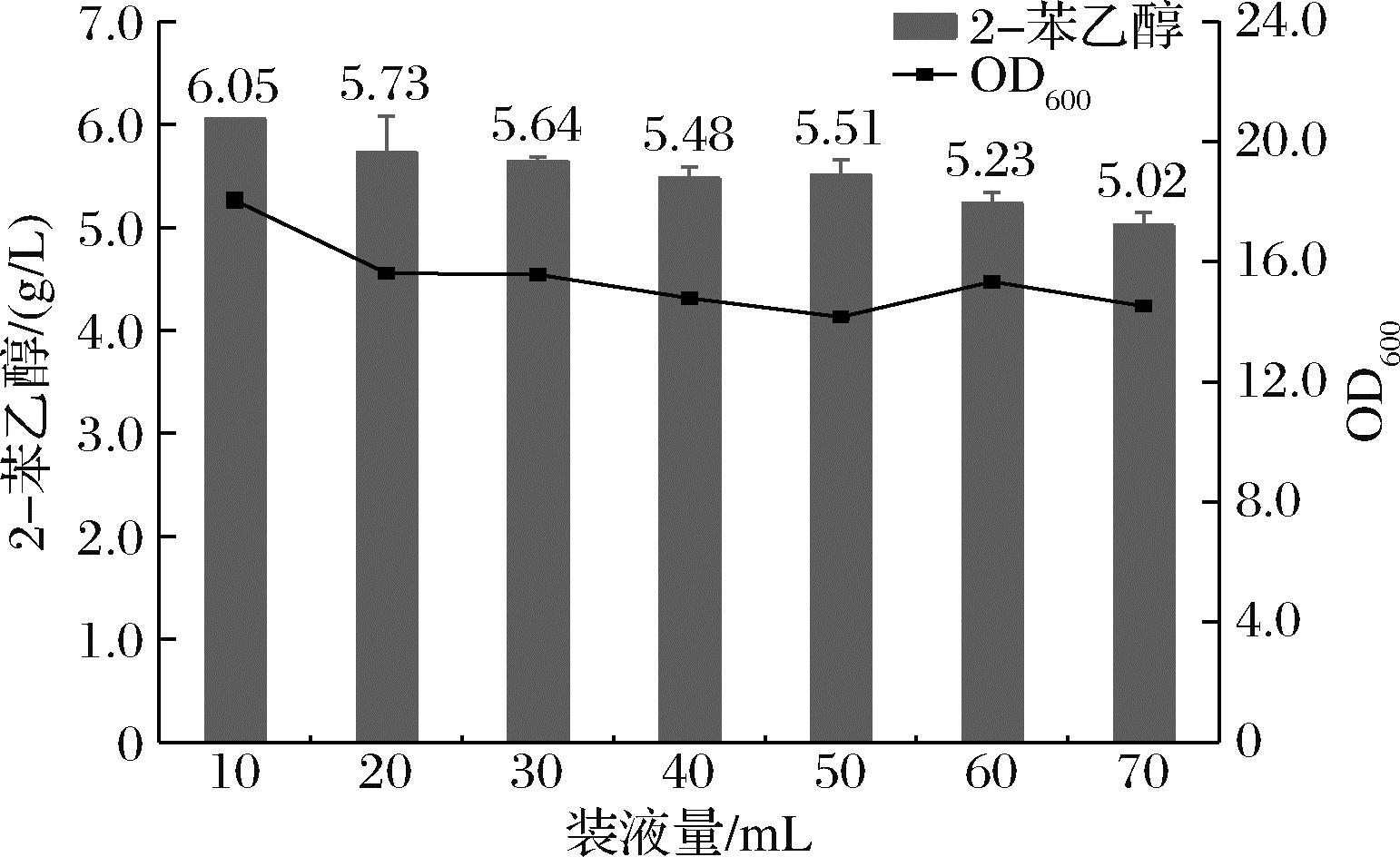
图10 装液量对2-苯乙醇的影响
Fig.10 Effects of liquid loading capacity on the conversion and synthesis of 2-PE transformation
3 讨论
目前应用于发酵法生产2-苯乙醇的菌株以酵母菌为主,包括例如酿酒酵母、毕赤酵母、梅奇酵母、解脂酵母、假丝酵母等。本实验所用菌株为从发酵酱醪中筛选分离出的1株生香酵母,其为1株双倍体菌株,从菌株的生长能力,对2-苯乙醇的耐受能力和产2-PE能力等方面都有其优势。生物转化的方法可以利用生香酵母合成天然香料2-苯乙醇,本实验通过优化实验得出最适合的转化条件:初始葡萄糖质量浓度为40 g/L,L-phe 8 g/L,YNB 1.7 g/L,MgSO4·7H2O 0.4 g/L,KH2PO45 g/L,α-酮戊二酸 0.5 g/L,pH值为5,在26 ℃,转速250 r/min,转化时间为48 h,2-苯乙醇的最终产量可达到6.05 g/L,较优化前大幅度提升,说明该菌株有着很大的生产和研究潜力。后续可以通过代谢改造、诱变育种等多种方式提高菌株的生产能力,并通过上罐条件优化,扩大生产体系,提高2-苯乙醇的产率适用于工业化生产。
[1] 范三红, 李颖星, 白宝清.涡旋辅助分散液液微萃取-气相色谱法测定清香型白酒中5种高级醇[J].中国酿造, 2020, 39(4):194-200.FAN S H, LI Y X, BAI B Q.Determination of 5 higher alcohols in light-flavor Baijiu by Vortex-assisted dispersion liquid-liquid microextraction-gas chromatography[J].China Brewing, 2020, 39(4):194-200.
[2] MART NEZ-AVILA O, S
NEZ-AVILA O, S NCHEZ A, FONT X, et al.Bioprocesses for 2-phenylethanol and 2-phenylethyl acetate production:Current state and perspectives[J].Applied Microbiology and Biotechnology, 2018, 102(23):9991-10004.
NCHEZ A, FONT X, et al.Bioprocesses for 2-phenylethanol and 2-phenylethyl acetate production:Current state and perspectives[J].Applied Microbiology and Biotechnology, 2018, 102(23):9991-10004.
[3] MITRI S, KOUBAA M, MAROUN R G, et al.Bioproduction of 2-phenylethanol through yeast fermentation on synthetic media and on agro-industrial waste and by-products:A review[J].Foods, 2022, 11(1):109.
[4] KRÖMER J O, NUNEZ-BERNAL D, AVERESCH N J H, et al.Production of aromatics in Saccharomyces cerevisiae—a feasibility study[J].Journal of Biotechnology, 2013, 163(2):184-193.
[5] DAI J, XIA H L, YANG C L, et al.Sensing, uptake and catabolism of L-phenylalanine during 2-phenylethanol biosynthesis via the Ehrlich pathway in Saccharomyces cerevisiae[J].Frontiers in Microbiology, 2021, 12:601963.
[6] AUBERT C, BAUMANN S, ARGUEL H.Optimization of the analysis of flavor volatile compounds by liquid-liquid microextraction (LLME).Application to the aroma analysis of melons, peaches, grapes, strawberries, and tomatoes[J].Journal of Agricultural and Food Chemistry, 2005, 53(23):8881-8895.
[7] HORBOWICZ M, WICZKOWSKI W, SAWICKI T, et al.Methyl jasmonate stimulates biosynthesis of 2-phenylethylamine, phenylacetic acid and 2-phenylethanol in seedlings of common buckwheat[J].Acta Biochimica Polonica, 2015, 62(2):235-240.
[8] HUA D L, XU P.Recent advances in biotechnological production of 2-phenylethanol[J].Biotechnology Advances, 2011, 29(6):654-660.
[9] YAMAGUCHI K, EBITANI K, KANEDA K.Hydrotalcite-catalyzed epoxidation of olefins using hydrogen peroxide and amide compounds[J].Journal of Organic Chemistry, 1999, 64(8):2966-2968
[10] GU Y, MA J B, ZHU Y L, et al.Refactoring Ehrlich pathway for high-yield 2-phenylethanol production in Yarrowia lipolytica[J].ACS Synthetic Biology, 2020, 9(3):623-633.
[11] DICKINSON J R, SALGADO L E J, HEWLINS M J E.The catabolism of amino acids to long chain and complex alcohols in Saccharomyces cerevisiae[J].Journal of Biological Chemistry, 2003, 278(10):8028-8034.
[12] CHEN H, FINK G R.Feedback control of morphogenesis in fungi by aromatic alcohols[J].Genes &Development, 2006, 20(9):1150-1161.
[13] CHEN X R, WANG Z Y, GUO X N, et al.Regulation of general amino acid permeases Gap1p, GATA transcription factors Gln3p and Gat1p on 2-phenylethanol biosynthesis via Ehrlich pathway[J].Journal of Biotechnology, 2017, 242:83-91.
[14] GARRETT J M.Amino acid transport through the Saccharomyces cerevisiae Gap1 permease is controlled by the Ras/cAMP pathway[J].International Journal of Biochemistry &Cell Biology, 2008, 40(3):496-502.
[15] SPRINGAEL J Y, ANDRÉ B.Nitrogen-regulated ubiquitination of the Gap1 permease of Saccharomyces cerevisiae[J].Molecular Biology of the Cell, 1998, 9(6):1253-1263.
[16] 史荣超, 刘洒洒, 侯阳阳, 等.梅奇酵母转化L-苯丙氨酸合成2-苯乙醇发酵条件优化[J].食品与发酵工业, 2021, 47(15):22-28.SHI R C, LIU S S, HOU Y Y, et al.Optimized bio-conversion of L-phenylalanine to 2-phenylethanol in Metschnikowia sp.[J].Food and Fermentation Industries, 2021, 47(15):22-28.
[17] KIM B, CHO B R, HAHN J S.Metabolic engineering of Saccharomyces cerevisiae for the production of 2-phenylethanol via Ehrlich pathway[J].Biotechnology and Bioengineering, 2014, 111(1):115-124.
[18] WANG P C, YANG X W, LIN B X, et al.Cofactor self-sufficient whole-cell biocatalysts for the production of 2-phenylethanol[J].Metabolic Engineering, 2017, 44:143-149.
[19] 陈虹, 梅建凤, 陈蔚青.紫外分光光度法测定发酵液中的2-苯乙醇含量[J].食品与发酵工业, 2007, 33(4):134-136.CHEN H, MEI J F, CHEN W Q.Determination of 2-phenylethanol in fermented liquid by ultraviolet spectrophotometry[J].Food and Fermentation Industries, 2007, 33(4):134-136.