马铃薯淀粉是由马铃薯中提取的主要多糖类化合物,是马铃薯的主要储存形式。作为一种重要的食品添加剂和工业原料,马铃薯淀粉在食品加工、医药制备、纺织印染等领域具有广泛的应用[1]。但马铃薯淀粉很容易在加工过程中因黏性较强、糊化温度低等导致应用受到限制。为了探索马铃薯淀粉在特定加工条件下的特性变化,通过技术改进和合理应用,最大程度地发挥其优势,减少其缺点带来的影响。儿茶素作为一种天然的多酚类化合物,被广泛应用于食品和医药等领域,其具有很强的抗氧化性能[2]。据研究显示,儿茶素可以影响淀粉的结构和性质,进而影响淀粉的功能性[3-5]。例如儿茶素可以降低板栗淀粉、玉米淀粉和莲藕淀粉的黏度,以及降低大米淀粉的凝胶强度、贮能模量和损耗模量使其更适用于3D打印技术[6-9]。
韧化处理是一种常见的改善淀粉性质的方法,能够使淀粉分子结构发生改变,从而提高淀粉的胶化温度和胶化热值等特性[10]。虽然儿茶素对淀粉的影响研究较多,但对于韧化条件下儿茶素对马铃薯淀粉的影响的探究仍然有限。因此,通过探究韧化处理条件下儿茶素对马铃薯淀粉性质的影响,可以帮助我们更好地理解淀粉与多酚类化合物之间的相互作用机制,从而为食品加工等领域的应用提供理论支持和指导。本文将初探韧化处理条件下儿茶素对马铃薯淀粉的影响,以期为淀粉的改性与儿茶素的应用提供参考,为淀粉的进一步改性和开发儿茶素相关产品提供理论基础。
1 材料与方法
1.1 材料与试剂
马铃薯淀粉,实验室自提;儿茶素(食品级,纯度为98%),河南三化生物科技有限公司;KBr(光谱纯),天津市科密欧化学试剂有限公司。
1.2 仪器与设备
TM3030Plus台式扫描电子显微镜,日本日立高新技术公司;VERTEX70傅立叶变换中远红外光谱仪,德国BRUKER公司;Bettersize2600激光粒度分布仪,丹东百特仪器有限公司;803302新型布拉班德黏度仪,德国Brabender公司;TA DHR-2食品流变仪,美国沃特斯公司;Xrite color i5色差计,东莞市凯得科技有限公司;DH360BS恒温干燥箱,上海坤天实验仪器。
1.3 实验方法
1.3.1 马铃薯淀粉的提取
称取马铃薯2 kg去皮后切丁,加混合液体(10 g/L氯化钠溶液∶2 g/L亚硫酸钠溶液=1∶1,体积比)后用组织搅碎机打碎,将打碎的混合物用纱布过滤弃去杂质,溶液静置沉淀并弃上清液,用清水反复冲洗沉淀物4~5次后放入烘箱中50 ℃烘干,粉碎过100目筛,放入封口袋中保存备用。
1.3.2 复合物的制备
以去离子水为溶剂配制淀粉乳(儿茶素的添加量是淀粉干基的0%、1%、3%、6%、10%,质量分数),配制成25%的淀粉乳,将其置于密闭容器中放到50 ℃烘箱中24 h后取出,并于烘箱内烘干研磨过筛(100目)备用。马铃薯淀粉样品和韧化处理后的马铃薯淀粉样品记为PS、H-PS,马铃薯淀粉-儿茶素复合物样品记为H-PS-C(H-PS-C 1%、H-PS-C 3%、H-PS-C 6%、H-PS-C 10%分别表示1%、3%、6%、10%添加量的儿茶素H-PS-C样品)。
1.3.3 粒径及白度的测定
1.3.3.1 粒径的测定
取1.3.2节的样品粉末加入到仪器的水箱中,获得10%左右的遮光率。采用具有水相(1.33)和淀粉粒(1.52)折射率的多分散分析模式,测定淀粉颗粒的粒径分布。
1.3.3.2 白度的测定
参考张本山等[11]的方法并稍作修改,取1.3.2节所制备好的淀粉样品用色差计测定其白度。每个样品测3次后平均值。
1.3.4 扫描电镜
取少量1.3.2节的样品放在导电胶上,放于扫描电镜上放大500倍观察复合物颗粒的形态。
1.3.5 红外光谱的测定
将1.3.2节的样品与KBr按照1∶100的比例混合后充分研磨,并于压片机上压成透明、无裂纹的薄片,用傅立叶变换中远红外光谱仪进行测定,扫描波数为400~4 000 cm-1,扫描次数为64次,分辨率为4 cm-1,纯KBr作为背景校正。用OMNIC软件对波数为800~2 000 cm-1的图谱进行自动基线校正、归一化及去卷积处理,峰宽为38,强度为1.9,计算样品1 047/1 022的比值。
1.3.6 黏度特性的测定
将1.3.2节的样品与去离子水配制成6%的淀粉乳,用布拉班德黏度仪进行测定。从30 ℃的温度以1.5 ℃/min的速率升到95 ℃,在95 ℃保持30 min,再以1.5 ℃/min的速率降到50 ℃保持30 min。记录其峰值时间、峰值黏度、糊化黏度、最终黏度、糊化温度和峰值温度。计算分解值(break down,BD)和回生值(setback,SB)。
1.3.7 流变特性的测定
参考ZHENG等[12]方法略作修改,取1.3.2节的样品用去离子水配制成6%的淀粉乳,于95 ℃的恒温水浴锅内糊化15 min后的样品静止至室温后于流变仪上测定其流变特性。测试采用直径为40 mm、间隙为1 mm的平行金属板,测试温度为37 ℃。在0~100 s-1的剪切速率范围内进行稳态流变测量,并记录样品剪切应力(τ)随剪切速率(γ)在0.1~100 s-1过程中的变化,采用Herschel-Bulkley模型(公式1)对流变曲线进行拟合分析。在1%的应变(在线性黏弹性区域内)条件下进行频率扫描,频率扫描范围为0.1~10 Hz,记录扫描过程中储能模量(G′)和损耗模量(G″)的变化。
τ=τ0+Kγn
(1)
式中:τ为剪切应力,Pa;τ0为屈服应力,Pa;γ为剪切速率,s-1;K为稠度系数,Pa·sn;n为流动行为指数。
1.4 数据统计分析
数据结果以平均值±标准差表示,SPSS 27对数据进行方差分析(ANOVA),采用邓肯多重比较,差异显著限定P<0.05。使用Origin 2018绘图。
2 结果与分析
2.1 粒径及白度的分析
马铃薯淀粉经韧化处理后的淀粉颗粒的粒径变大可能是由于在韧化处理过程中淀粉颗粒吸水膨胀的原因[10]。由表1可知,在1%和3%的儿茶素添加量下淀粉的粒径(D10、D50和D90)呈现增加的趋势,且在3%儿茶素的添加量下淀粉颗粒粒径最大,为17.87、39.72和72.73 μm。其原因可能是儿茶素与淀粉颗粒表面发生相互作用形成复合物,从而使得淀粉颗粒聚集并逐渐变大[13-14]。而在6%和10%的儿茶素添加量下复合物的粒径虽有降低但仍比PS的高得多。可能是在韧化处理过程中高浓度的溶剂限制了淀粉颗粒吸水而导致的。这与多酚对高直链玉米淀粉粒径影响类似,即儿茶素、单宁酸、芦丁、原花青素、槲皮素的加入增大了高直链玉米淀粉的粒径[15]。
表1 马铃薯淀粉、韧化马铃薯淀粉及其与儿茶素 复合物颗粒的粒径及白度
Table 1 Particle size and whiteness of potato starch, tough potato starch and its particles in complex with ferulic acid and catechin
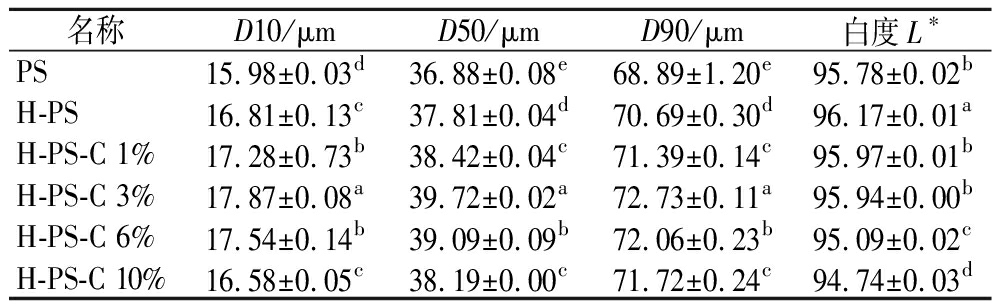
名称D10/μmD50/μmD90/μm白度L∗PS15.98±0.03d36.88±0.08e68.89±1.20e95.78±0.02bH-PS16.81±0.13c37.81±0.04d70.69±0.30d96.17±0.01aH-PS-C 1%17.28±0.73b38.42±0.04c71.39±0.14c95.97±0.01bH-PS-C 3%17.87±0.08a39.72±0.02a72.73±0.11a95.94±0.00bH-PS-C 6%17.54±0.14b39.09±0.09b72.06±0.23b95.09±0.02cH-PS-C 10%16.58±0.05c38.19±0.00c71.72±0.24c94.74±0.03d
注:同列数据标注不同的字母表示数据之间存在显著性差异(P<0.05),(下同)。D10指颗粒粒径小于该直径的淀粉颗粒占总数的10%;D50指颗粒粒径小于该直径的淀粉颗粒占总数的50%;D90指颗粒粒径小于该直径的淀粉颗粒占总数的90%,通常以D50表示该淀粉的平均粒径。
韧化处理后的马铃薯淀粉的白度增加可能是韧化处理过程中淀粉中的有色物质溶于水中被弃去所致。而在加入儿茶素后白度降低的原因可能是因为儿茶素本身是一种有色物质,当儿茶素与淀粉发生相互作用时,可能会导致淀粉的颜色变暗或减小白度。此外,儿茶素也可能会影响淀粉的结构或性质,导致淀粉颗粒之间的相互作用发生变化,从而影响其光学性质和白度表现,并且儿茶素可与空气中的氧气发生氧化反应,最终导致白度的降低。
2.2 扫描电镜分析
由图1可以看出经韧化处理的马铃薯淀粉与原淀粉相比外观无明显差别仍为光滑的椭圆形和圆形,只是颗粒较小的会有所聚集。而加入儿茶素后,马铃薯淀粉颗粒没有被破坏仍可以清楚地看到淀粉颗粒的完整结构。添加儿茶素的马铃薯淀粉颗粒表面变得凸出以及部分马铃薯淀粉颗粒会聚集,且随着儿茶素添加量的增加呈现先增加后降低的趋势,并在3%儿茶素的添加量下聚集最严重,这与上述粒径变化相一致。其原因可能是在低浓度下,儿茶素的存在可能促进颗粒之间的相互作用,导致颗粒聚集增加;而随着浓度的进一步增加,马铃薯淀粉颗粒表面的儿茶素覆盖层可能变得更厚或更密,改变了颗粒之间的相互作用力从而导致聚集减弱。并且随着儿茶素添加量的变化,溶剂的浓度和淀粉颗粒状态可能会发生变化,从而影响颗粒之间的相互作用。

a-PS;b-H-PS;c-H-PS-C1%;d-H-PS-C3%; e-H-PS-C6%;f-H-PS-C10%
图1 马铃薯淀粉、韧化马铃薯淀粉及其与儿茶素 复合物的电镜图片(×500)
Fig.1 Electron microscopic images of potato starch, tough potato starch and its complex with ferulic acid and catechin
2.3 红外分析
红外光谱分析通过测定物质在不同波长的红外光下的吸收情况,进而了解其分子结构和化学键信息。3 400 cm-1处附近的峰为淀粉的羟基伸缩振动,1 660 cm-1处的峰为淀粉的O—H弯曲振动[16-17]。由图2可知,所有样品的红外光谱图谱中皆没有新峰产生,即儿茶素的存在没有使其结构发生变化。3 400 cm-1左右的峰随着儿茶素添加量的增加逐渐向低波数移动,可能是儿茶素中的酚基团与淀粉中的羟基团之间形成的氢键导致3 400 cm-1峰的移动,且随着儿茶素添加量的增加,儿茶素中的酚基团与淀粉中的羟基团之间形成的氢键数量增加,导致3 400 cm-1峰的移动向低波数方向[18]。随着儿茶素添加量的增加,淀粉在1 640 cm-1附近的峰在不断蓝移并逐渐偏向于儿茶素的特定吸收峰(1 620 cm-1),可能是由于儿茶素的存在改变了淀粉分子的结构或环境,导致淀粉的吸收峰位置发生变化。
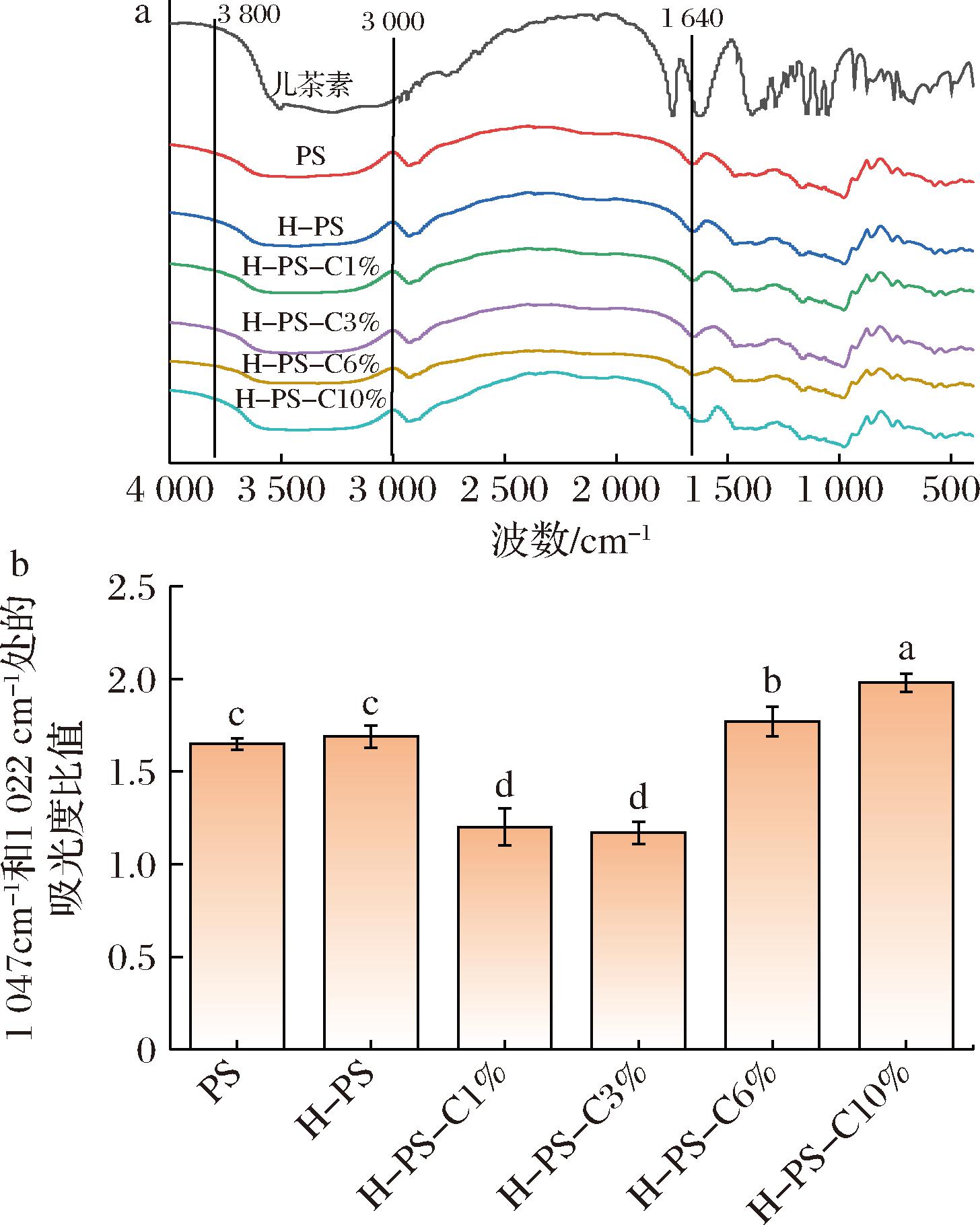
a-红外图谱;b-吸光度比值
图2 马铃薯淀粉、韧化马铃薯淀粉及其与儿茶素复合物的 红外图谱及1 047 cm-1和1 022 cm-1处的 吸光度比值(n=3)
Fig.2 IR map of potato starch, tough potato starch and its complex with catechin and the absorbance ratio at 1 047 cm-1 and 1 022 cm-1 (n=3)
注:同列数据标注不同的字母表示数据之间存在 显著性差异(P<0.05)。
在红外光谱中,1 047 cm-1处的吸收峰与淀粉分子中的C—O—C和C—OH伸缩振动有关,1 022 cm-1处的吸收峰主要与C—O伸缩振动相关,1 047/1 022的比值代表淀粉的有序程度[19]。由图2可知,除PS样品外其余淀粉样品的1 047/1 022的比值呈现先降低后升高的趋势,在儿茶素初期加入时,可能会通过氢键等非共价键与淀粉分子上的羟基等官能团形成相互作用,导致淀粉分子结构在一定程度上被破坏或松弛,使得1 047/1 022的比值降低;随着儿茶素浓度的进一步增加,可能促进了淀粉分子之间的重新排列,形成较为稳定的包合物或复合体,导致1 047/1 022比值上升。LI等[20]研究中发现马铃薯淀粉-咖啡酸、马铃薯淀粉-阿魏酸、马铃薯淀粉-没食子酸复合物的1 047/1 022比值皆比马铃薯淀粉的低,而支链淀粉-咖啡酸、支链淀粉-阿魏酸、支链淀粉-没食子酸复合物的1 047/1 022比值皆比玉米支链淀粉的高,其可能是淀粉优先与直链淀粉作用降低淀粉的有序程度,当直链淀粉不足时则会与支链淀粉作用升高淀粉的有序程度,所以当儿茶素含量过高且马铃薯淀粉中直链淀粉不足时淀粉的有序程度就会上升。
2.4 黏度分析
韧化处理和儿茶素会使马铃薯淀粉的黏度显著降低,主要包括峰值黏度、糊化黏度和最终黏度(图3、表2)。其原因可能是儿茶素与淀粉分子相互作用,降低淀粉颗粒的糊化程度,导致峰值黏度、糊化黏度和最终黏度降低[6]。韧化使淀粉颗粒变得致密从而导致糊化温度和峰值温度的升高,而加入儿茶素后糊化温度和峰值温度与H-PS相比呈现先降后升,其原因可能是:少量儿茶素会与淀粉分子通过非共价键相互作用使淀粉分子结构在一定程度上被破坏或松弛,导致H-PS糊化温度和峰值温度降低;随着儿茶素浓度的增加,部分儿茶素黏附在淀粉表面或儿茶素促进了淀粉分子之间的重新排列,使其形成较为稳定的包合物或复合体,最终导致糊化温度和峰值温度升高,但糊化温度和峰值温度皆比PS高,说明韧化后的复合物比PS的热稳定性高。马姝等[21]也发现韧化后的马铃薯淀粉具有更高的稳定性,并表现出更高的热浆稳定性。
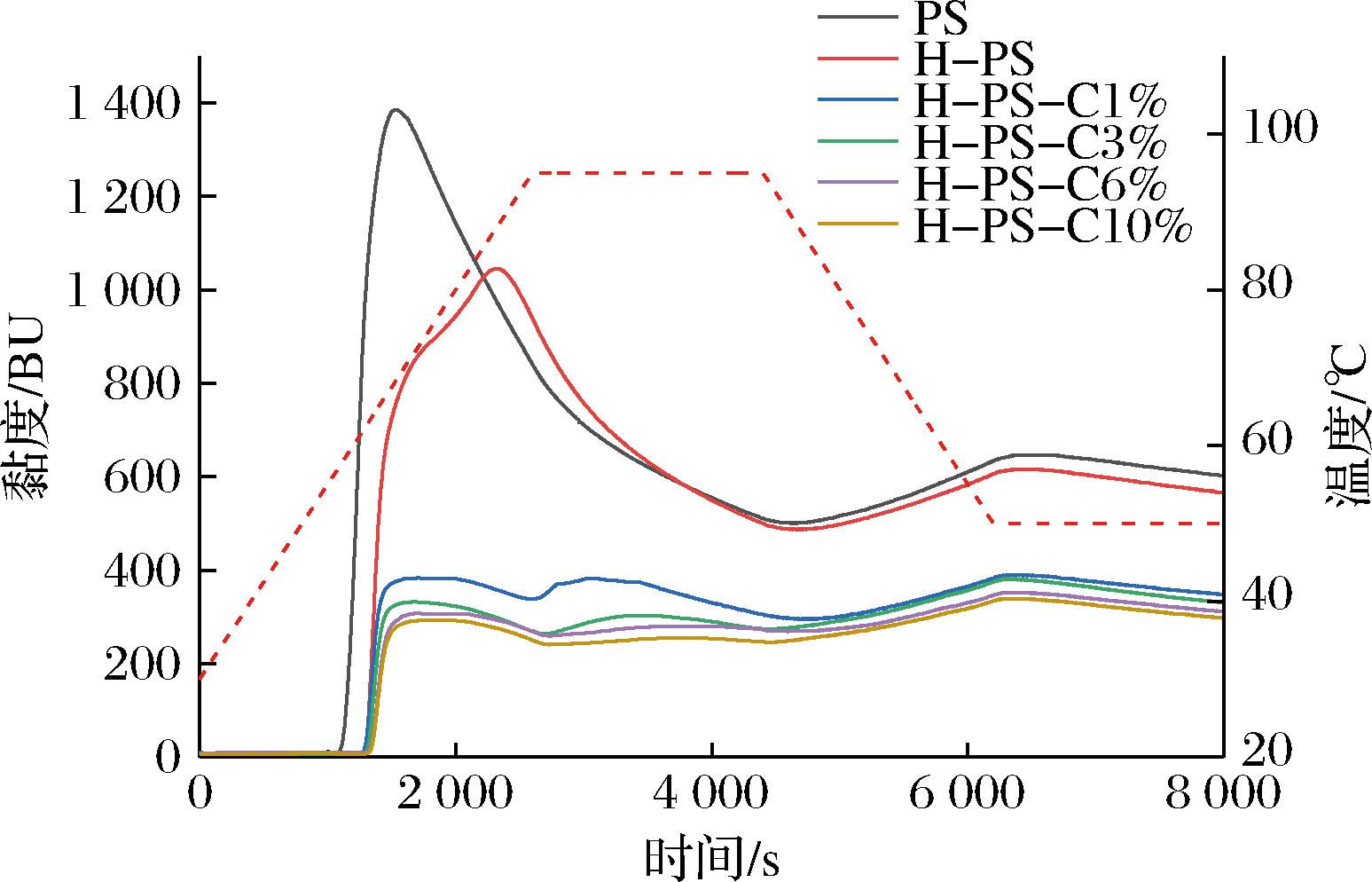
图3 马铃薯淀粉、韧化马铃薯淀粉及其与 儿茶素复合物黏度图谱
Fig.3 Plot of potato starch, tough potato starch and its complex with ferulic acid and catechins
表2 马铃薯淀粉、韧化马铃薯淀粉及其与儿茶素复合物布拉班德糊化特征参数
Table 2 Potato starch, tough potato starch and their characteristic parameters of gelapination in complex with catechin

样品峰值时间/min峰值黏度/BU糊化黏度/BU最终黏度/BU糊化温度/℃峰值温度/℃回生值(SB)崩解值(BD)PS25.33±0.02e1385±13a510±11a602±14a57.0±0.1d67.9±0.2d124±5a875±15aH-PS38.57±0.01a1045±15b500±14b565±15b61.6±0.4c87.7±0.1a106±8b545±17bH-PS-C 1%27.00±0.03d384±6c305±8c347±5c61.5±0.2c71.2±0.2c78±7d93±4cH-PS-C 3%27.57±0.05d332±8d274±10d330±7d62.0±0.1b71.5±0.5c74±7d60±3dH-PS-C 6%28.37±0.02c307±5e272±4d311±4e62.7±0.0a73.1±0.1b87±3c45±5eH-PS-C 10%30.17±0.01b292±9e247±8e298±2f62.9±0.6a73.2±0.2b101±9b33±2f
淀粉颗粒在加热过程中会发生凝胶化,这种凝胶化过程会导致淀粉颗粒间的连接变强,从而增加淀粉基质的稳定性和崩解值。加入儿茶素后其可能与淀粉分子结合,形成复合物或改变淀粉分子结构,导致淀粉颗粒在加热处理过程中形成的凝胶结构不够牢固或完整,使得淀粉基质的稳定性下降,崩解值降低。回生值表示淀粉的凝胶强度,其值越大则凝胶性越强,韧化处理改变了淀粉颗粒内部结构使淀粉颗粒更加稳定,降低了淀粉颗粒在加热后再次形成结晶的能力,从而降低了回生值。而加入儿茶素后其回生值呈现先降后升的变化可能是少量的儿茶素进入淀粉内部抑制了淀粉形成结晶的能力,从而使得回生值降低;随着儿茶素含量的增加,过多的儿茶素黏附在淀粉颗粒表面或儿茶素与淀粉分子之间的相互作用促进了新的分子连接或结合方式的形成,使得凝胶结构逐渐增强,从而导致回生值的上升,与红外分析中样品的1 047/1 022比值变化趋势一致。
2.5 流变学特性分析
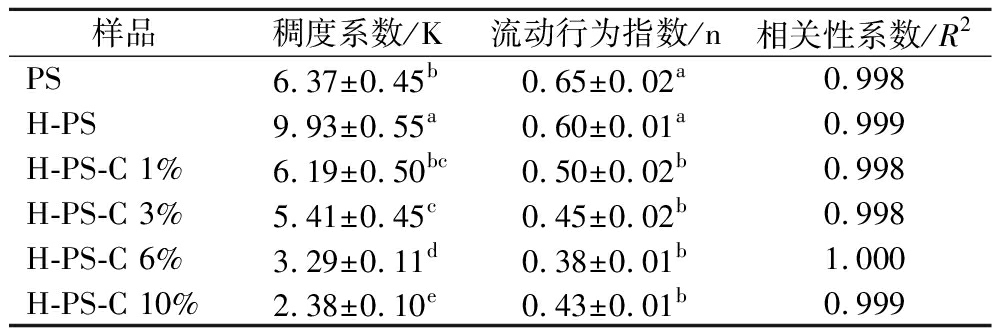
如图4所示,所有样品随着剪切速率增加其黏度在降低,表现的是非牛顿剪切稀化的流变学行为[22]。韧化处理使马铃薯淀粉颗粒结构致密导致在剪切速率下其黏度和剪切应力的升高[23]。加入儿茶素后黏度和剪切应力随着其添加量的增加而降低,与上述的黏度变化一致,在探究茶多酚对大米淀粉凝胶的影响时也有类似的结论[24]。对剪切速率和剪切应力的图谱用Herschel-Bulkley模型进行拟合,具有较高的相关性系数(R2>0.995),结果如表3所示。稠度系数(K)表示淀粉的表观黏度,其随着儿茶素的增加而降低;流动行为指数(n)表示淀粉的网络状结构,韧化处理后马铃薯淀粉的n值无显著变化,加入儿茶素后n值降低且与添加量无关。
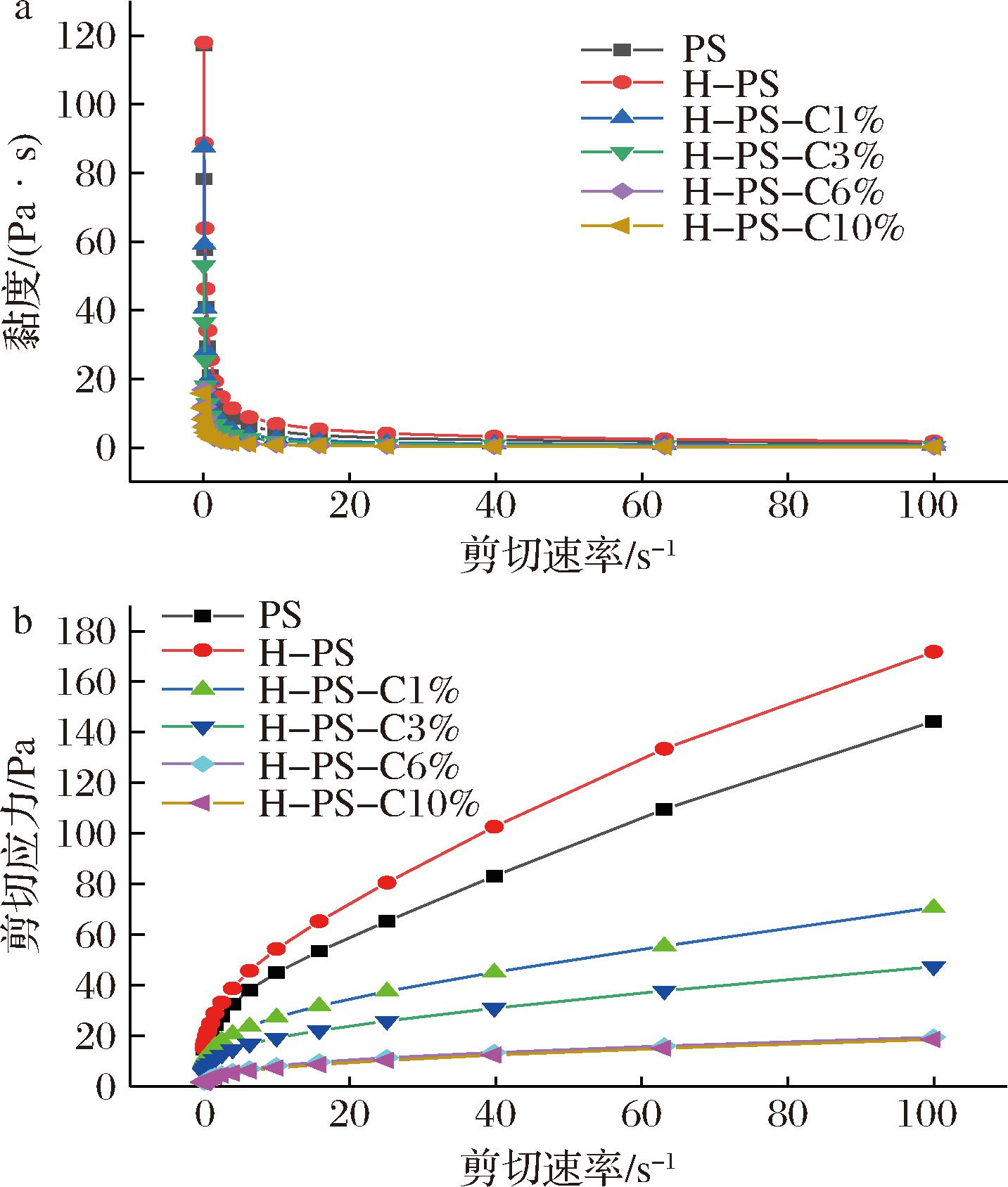
a-黏度随剪切速率的变化;b-剪切应力随剪切速率的变化
图4 马铃薯淀粉、韧化马铃薯淀粉及其与阿魏酸和 儿茶素复合物静态流动曲线
Fig.4 Static flow curves of potato starch, tough potato starch and their complexes with ferulic acid and catechin
表3 马铃薯淀粉与阿魏酸和儿茶素复合物的稳定 剪切特性的Herschel-Bulkley模型
Table 3 Herschel-Bulkley model for the stable shear properties of potato starch in complex with ferulic acid and catechins
样品稠度系数/K流动行为指数/n相关性系数/R2PS6.37±0.45b0.65±0.02a0.998H-PS9.93±0.55a0.60±0.01a0.999H-PS-C 1%6.19±0.50bc0.50±0.02b0.998H-PS-C 3%5.41±0.45c0.45±0.02b0.998H-PS-C 6%3.29±0.11d0.38±0.01b1.000H-PS-C 10%2.38±0.10e0.43±0.01b0.999
图5可以看出,在频率扫描范围内所有样品的G′均高于G″,淀粉凝胶表现出弱凝胶弹性的行为[25]。当马铃薯淀粉经过韧化处理后其淀粉凝胶的G′和G″明显升高,表明韧化处理强化了淀粉的凝胶结构,使淀粉凝胶的弹性大于黏性。加入儿茶素后其G′和G″的降低,说明儿茶素减弱淀粉的凝胶结构[8]。随着儿茶素添加量的增加,复合物G′和G″也在下降且G′的变化要大于G″,这可能是因为儿茶素与淀粉之间的相互作用限制了直链淀粉的浸出,干扰了网络的形成,从而导致凝胶较弱[8]。在研究PA对马铃薯淀粉流变特性的影响时也有相似的结果,即随着PA添加量的增加马铃薯淀粉凝胶的G′和G″在逐渐降低,且G′的变化大于G″[26]。
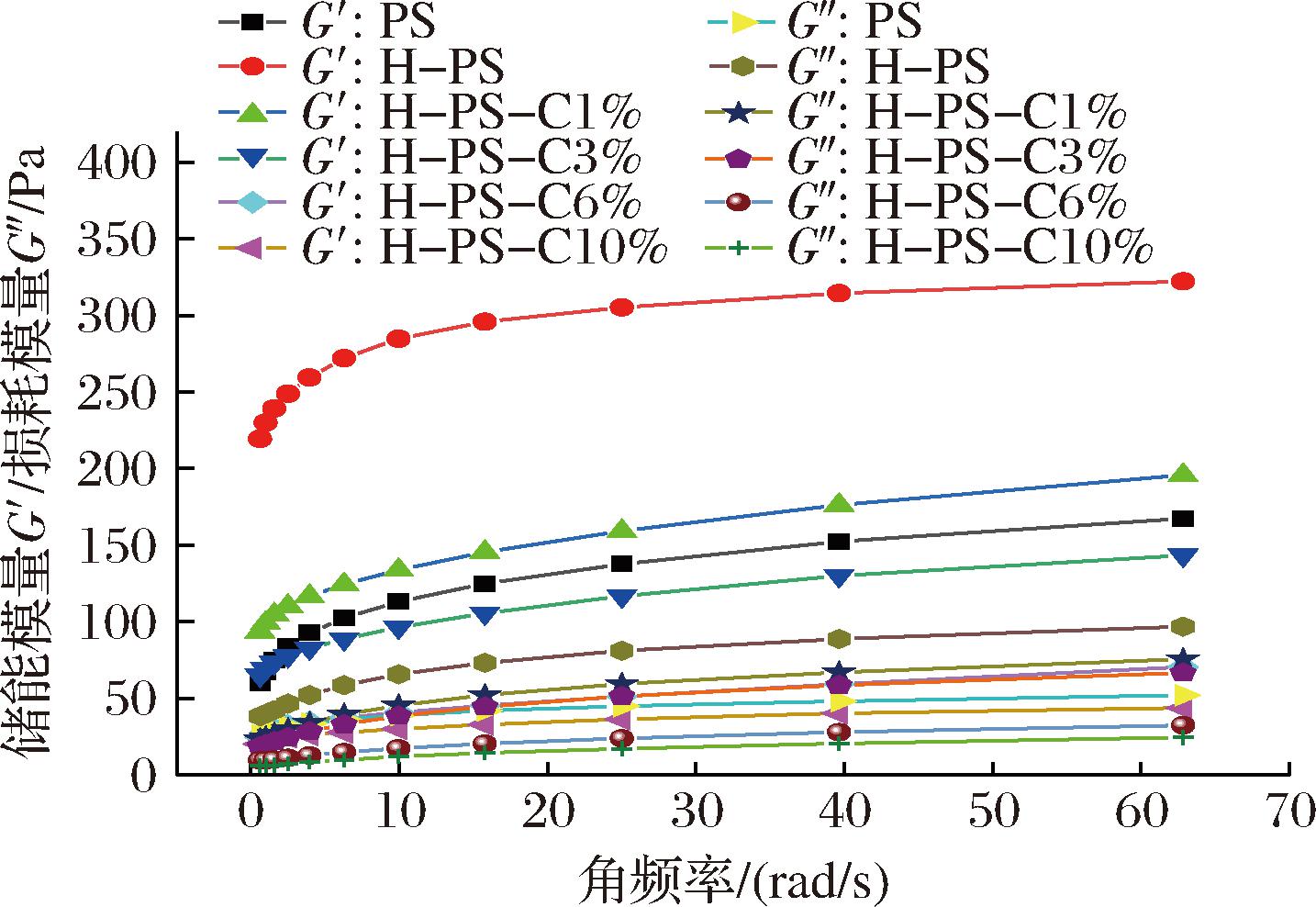
图5 马铃薯淀粉、韧化马铃薯淀粉及其儿茶素 复合物动态流变图谱
Fig.5 Dynamic rheological map of potato starch, tough potato starch and its complex with ferulic acid and catechin
3 结论
综上所述,韧化处理及韧化条件下添加儿茶素并未改变马铃薯淀粉颗粒的完整性,但增加了马铃薯淀粉颗粒的平均粒径。红外分析表明,韧化条件下添加儿茶素未使马铃薯淀粉产生新的峰,1 047/1 022的比值呈现先降低后升高的趋势。韧化条件下复合物淀粉的糊化特性、凝胶性和抗剪切能力降低。儿茶素的加入增强了淀粉凝胶的假塑性、剪切变薄的行为。韧化处理强化了淀粉糊的凝胶结构,而儿茶素加入又使淀粉的凝胶结构减弱且随着添加量的增加而呈现降低趋势。由此可见,适当的儿茶素添加量可以降低马铃薯淀粉的短程有序性,改善马铃薯淀粉易糊化特性,扩充了马铃薯淀粉在工业生产加工中的充分利用。
[1] 肖力力, 曹国璠, 何天久, 等.马铃薯果胶的提取、结构、活性及应用研究进展[J].食品研究与开发, 2021, 42(6):190-197.XIAO L L, CAO G F, HE T J, et al.Study on the extraction, structure, activity and application of potato pectin[J].Food Research and Development, 2021, 42(6):190-197.
[2] 管勤昊, 汤丽华, 张亮亮, 等.多酚类化合物结构对其与蛋白相互作用影响研究进展[J].食品研究与开发, 2023, 44(23):182-190.GUAN Q H, TANG L H, ZHANG L L, et al.Structure-activity relationships of polyphenols interacting with proteins[J].Food Research and Development, 2023, 44(23):182-190.
[3] 曾铭, 李蟠莹, 胡鹏, 等.多酚对淀粉理化性质影响的研究进展[J].食品工业科技, 2018, 39(22):334-340.ZENG M, LI P Y, HU P, et al.Research progress on the effects of polyphenols on the physicochemical properties of starch[J].Science and Technology of Food Industry, 2018, 39(22):334-340.
[4] 杨玉姣, 许飞, 陈洁, 等.儿茶素对糯小麦淀粉和普通小麦淀粉特性影响的对比研究[J].河南工业大学学报(自然科学版), 2023, 44(6):51-58.YANG Y J, XU F, CHEN J, et al.Comparative study on the effect of catechin on starch characteristics of waxy wheat and common wheat[J].Journal of Henan University of Technology (Natural Science Edition), 2023, 44(6):51-58.
[5] 郑波. 热挤压3D打印构建大米淀粉-儿茶素复合物的消化性能及抗肥胖机理研究[D].广州:华南理工大学, 2020.ZHENG B.The mechanism study on digestibility and anti-obesity effects of rice starch-catechin complex constructed by Hot-extrusion 3D printing[D].Guangzhou:South China University of Technology, 2020.
[6] XIE Y M, CHEN J, XU F, et al.Effect of catechin on the retrogradation and structural properties of chestnut starch[J].Starch-Stärke, 2022, 74(11-12):2200113.
[7] 王杰, 何燕, 李洁, 等.多酚对莲藕淀粉和玉米淀粉理化和消化特性的影响[J].中国粮油学报, 2024, 39(6):93-102.WANG J, HE Y, LI J, etc.Effects of polyphenols on the physicochemical and digestive properties of lotus root and maize starch[J/OL].Journal of the Chinese Cereals and Oils Association, 2024, 39(6):93-102.
[8] ZENG X X, LI T J, ZHU J C, et al.Printability improvement of rice starch gel via catechin and procyanidin in hot extrusion 3D printing[J].Food Hydrocolloids, 2021, 121:106997.
[9] WU Y, XU H L, LIN Q L, et al.Pasting, thermal and rheological properties of rice starch in aqueous solutions with different catechins[J].Journal of Food Processing and Preservation, 2015, 39(6):2074-2080
[10] 王嘉俊, 郑瑜雪, 柴子淇, 等.湿热和韧化处理对莜麦淀粉结构及消化特性的影响[J].食品安全质量检测学报, 2022, 13(20):6659-6666.WANG J J, ZHENG Y X, CHAI Z Q, et al.Effects of heat-moisture and annealing treatment on the structure and digestive properties of naked oat starch[J].Journal of Food Safety &Quality, 2022, 13(20):6659-6666.
[11] 张本山, 李为民, 侯成博, 等.淀粉白度耐高温特性研究[J].现代食品科技, 2015, 31(2):87-92.ZHANG B S, LI W M, HOU C B, et al.Study on the thermostability of starch whiteness[J].Modern Food Science and Technology, 2015, 31(2):87-92.
[12] ZHENG J, HUANG S, ZHAO R Y, et al.Effect of four viscous soluble dietary fibers on the physicochemical, structural properties, and in vitro digestibility of rice starch:A comparison study[J].Food Chemistry, 2021, 362:130181.
[13] 肖遥, 曹悦, 任顺成, 等.多酚与玉米淀粉相互作用研究[J].河南工业大学学报(自然科学版), 2020, 41(1):45-51.XIAO Y, CAO Y, REN S C, et al.Study on the interaction between polyphenols and corn starch[J].Journal of Henan University of Technology (Natural Science Edition), 2020, 41(1):45-51.
[14] KONG L Y, YUCEL U, YOKSAN R, et al.Characterization of amylose inclusion complexes using electron paramagnetic resonance spectroscopy[J].Food Hydrocolloids, 2018, 82:82-88.
[15] 任顺成, 胡海洋, 李柯柯.多酚对淀粉的热力学特性的影响[J].中国食品学报, 2021, 21(7):18-27.REN S C, HU H Y, LI K K.Effect of polyphenols on thermodynamic properties of starch[J].Journal of Chinese Institute of Food Science and Technology, 2021, 21(7):18-27.
[16] GONZ LEZ-CRUZ L, MONTA
LEZ-CRUZ L, MONTA EZ-SOTO J L, CONDE-BARAJAS E, et al.Spectroscopic, calorimetric and structural analyses of the effects of hydrothermal treatment of rice beans and the extraction solvent on starch characteristics[J].International Journal of Biological Macromolecules, 2018, 107:965-972.
EZ-SOTO J L, CONDE-BARAJAS E, et al.Spectroscopic, calorimetric and structural analyses of the effects of hydrothermal treatment of rice beans and the extraction solvent on starch characteristics[J].International Journal of Biological Macromolecules, 2018, 107:965-972.
[17] WANG M T, SHEN Q, HU L L, et al.Physicochemical properties, structure and in vitro digestibility on complex of starch with Lotus (Nelumbo nucifera Gaertn.) leaf flavonoids[J].Food Hydrocolloids, 2018, 81:191-199.
[18] WANG J J, XI J X, WANG Y Q.Recent advances in the catalytic production of glucose from lignocellulosic biomass[J].Green Chemistry, 2015, 17(2):737-751.
[19] LU H, TIAN Y Q, MA R R.Assessment of order of helical structures of retrograded starch by Raman spectroscopy[J].Food Hydrocolloids, 2023, 134:108064.
[20] LI M, PERNELL C, FERRUZZI M G.Complexation with phenolic acids affect rheological properties and digestibility of potato starch and maize amylopectin[J].Food Hydrocolloids, 2018, 77:843-852.
[21] 马姝, 郭双凤, 林倩, 等.韧化处理对马铃薯淀粉结构特性、理化特性及其凝胶3D打印性能的影响[J].食品科学, 2023, 44(20):1-7.MA S, GUO S F, LIN Q, et al.Effect of toughening treatment on the structural and physicochemical properties of potato starch and the 3D printing performance of potato starch gel[J].Food Science, 2023, 44(20):1-7.
[22] YOUSEFI A R, AKO K.Controlling the rheological properties of wheat starch gels using Lepidium perfoliatum seed gum in steady and dynamic shear[J].International Journal of Biological Macromolecules, 2020, 143:928-936.
[23] 潘俊娴, 吕杨俊, 蒋玉兰, 等.茶多酚对大米淀粉理化特性的影响[J].中国茶叶加工, 2023(3):45-51.PAN J X, LYU Y J, JIANG Y L, et al.Effect of tea polyphenols on the physicochemical properties of rice starch[J].China Tea Processing, 2023(3):45-51.
[24] AI Y F, JANE J L.Gelatinization and rheological properties of starch[J].Starch-Stärke, 2015, 67(3-4):213-224.
[25] POURFARZAD A, YOUSEFI A, AKO K.Steady/dynamic rheological characterization and FTIR study on wheat starch-sage seed gum blends[J].Food Hydrocolloids, 2021, 111:106380.
[26] CHEN N, GAO H X, HE Q, et al.Insight into property, function, and digestion of potato starch modified by phenolic compounds with varying structures[J].Journal of Food Science, 2023, 88(3):962-976.