蓝莓为杜鹃花科越橘属植物,富含维生素C、多酚、多糖、花色苷等营养成分,具有抗氧化、抗衰老、改善眼部血液循环等功能,被誉为“浆果之王”[1-2]。近年来,我国蓝莓种植产业发展迅速,其中2023年我国蓝莓种植面积已接近100万亩,产量达34.72万t,其中鲜果上市量达25万t(占比超过70%),位列全球第二位。但蓝莓果在常温下易腐烂不耐储存,且蓝莓的深加工较少,制约蓝莓产业的发展[3]。因此,近年来将蓝莓果加工成果汁产品成为解决蓝莓库存、滞留而导致经济严重损失的主要手段。
蓝莓果汁作为中国目前市场上最主要的蓝莓加工品,在品牌数量、消费总量、知名度方面均处于蓝莓加工品的前列[4]。但是,常用提取/制备蓝莓果汁方法存在出汁率低、汁液浑浊、酸涩味严重、营养成分及活性物质易被破坏等技术难点问题,因阻碍蓝莓加工产业发展而成为亟待解决的瓶颈问题[5]。粉碎方式作为果蔬汁加工必不可缺的关键环节,其参数变化对果蔬汁理化特性和品质变化具有显著影响[6]。目前,国内外对蓝莓及其产品的研究主要是某一工艺参数优化和产品品质改良等方面[7-8],而针对不同粉碎方式下蓝莓果汁理化性质、抗氧化活性及活性物质含量相关研究较少。
因此,本研究基于复合酶解技术,采用破壁机、胶体磨和湿法超微粉碎机制备蓝莓果汁,比较不同粉碎方式对蓝莓果汁加工特性(出汁率、粒径分布)、活性成分含量(花色苷、维生素C、总酚和总黄酮)和抗氧化活性[DPPH自由基清除率、ABTS阳离子自由基清除率和羟自由基(·OH)清除率]的影响,并采用代谢组学分析不同粉碎方式下蓝莓果汁中代谢物差异变化情况。以期为制备出高品质、高营养、高抗氧化蓝莓果汁提供理论依据,为提高蓝莓种植业经济效益和促进蓝莓产业发展提供技术支撑。
1 材料与方法
1.1 材料与试剂
蓝莓,采自贵州省黔东南州麻江县蓝莓种植基地;芦丁标准品(纯度≥95%)、没食子酸标准品(纯度≥95%),合肥博美科技生物有限公司;2,2′-联氮-二(3-乙基-苯并噻唑-6-磺酸)二铵盐(2,2′-azinobis-(3-ethylbenzthiazoline-6-sulphonate,ABTS)(纯度≥98%),合肥千盛生物科技有限公司;2,2-联苯基-1-苦基肼基(2,2-diphenyl-1-picrylhydrazyl,DPPH)(纯度≥90%),合肥巴斯夫生物科技有限公司;果胶酶、纤维素酶,上海源叶生物科技有限公司;其他化学试剂,南京化学试剂股份有限公司。
1.2 仪器与设备
QDSJ9000-2湿法超细精磨机,无锡轻大食品装备有限公司;DP-L-65胶体磨,北京亚欧德鹏科技有限公司;MJ-PB40E254D破壁机,美的集团股份有限公司;BT-9300S激光粒度仪,丹东百特仪器有限公司;Vanquish,Q Exactive Focus液相色谱串联质谱联用仪(liquid chromatography-mass spectrometer,LC-MS),美国Thermo Fisher Scientific公司;T-6vm可见分光光度计,南京菲勒仪器有限公司;EL204电子分析天平,特勒-托利多仪器有限公司。
1.3 试验方法
1.3.1 蓝莓汁制作工艺流程
工艺流程:
挑选蓝莓→清洗→热烫→冷却→称量→加水→粉碎→复合酶解→过滤→蓝莓汁
选取新鲜、成熟度好、无损伤的蓝莓果,清洗后热烫15 min,捞出冷却后按比例加入去离子水置于破壁机、胶体磨和湿法超微粉碎机中粉碎打浆,具体粉碎条件为料液比0.5 g/mL、粉碎时间8 min、复合酶添加量0.15%,酶解时间120 min,匀浆液经复合酶酶解后采用200目筛网过滤,收集滤液即为蓝莓汁。蓝莓汁样品放置于4 ℃冰箱中保存备用。
1.3.2 蓝莓出汁率的计算
出汁率按公式(1)计算:
(1)
式中:C,出汁率,%;M1,酶解前蓝莓果浆的质量,g;M2,酶解后澄清汁的质量,g。
1.3.3 蓝莓汁粒径测定
取25 mL蓝莓汁样品,采用激光粒度仪测定蓝莓汁D10、D50、D90和Dav(平均粒径)。
1.3.4 蓝莓汁活性物质含量测定
参照李晨等[9]的方法测定蓝莓汁花色苷、总黄酮、总酚含量。
采用2, 6-二氯靛酚钠法测定蓝莓汁维生素C含量。用移液管准确移取2 mL蓝莓汁样品,加入2 mL体积分数2%草酸溶液,混匀后用2, 6-二氯靛酚钠溶液滴定至微红色,平行滴定3次。维生素C含量按公式(2)计算:
(2)
式中:C,维生素C含量,mg/mL;V1,消耗的2, 6-二氯靛酚钠溶液的体积,mL;V2,样品溶液的体积,mL;C0,2, 6-二氯靛酚钠溶液质量浓度,mg/mL。
1.3.5 蓝莓汁抗氧化活性测定
各实验组蓝莓果汁分别取1 mL,参照程宏桢等[10]方法测定蓝莓果汁的DPPH自由基清除率、ABTS阳离子自由基清除率和羟自由基清除率。
1.3.6 代谢组学分析
精确移取适量样本2 mL于离心管中,加入400 μL甲醇溶液,涡旋1 min,4 ℃,12 000 r/min离心10 min,取全部上清液浓缩干燥,准确加入150 μL体积分数为80%甲醇水配制的2-氯-L-苯丙氨酸(4 mg/L)溶液复溶样品,取上清液过0.22 μm滤膜,采用LC-MS检测蓝莓汁中酚类物质组成。
色谱条件:使用ACQUITY UPLC® HSS T3(2.1 mm×100 mm,1.8 μm)色谱柱,0.3 mL/min的流速,40 ℃的柱温,进样量2 μL。正离子模式,流动相为体积分数为0.1%甲酸乙腈(B2)和体积分数为0.1%甲酸水(A2),梯度洗脱程序为:0~1 min,8% B2;1~8 min,8%~98% B2;8~10 min,98% B2;10~10.1 min,98%~8% B2;10.1~12 min,8% B2。负离子模式,流动相为乙腈(B3)和5 mmol/L甲酸铵水(A3),梯度洗脱程序为:0~1 min,8% B3;1~8 min,8%~98% B3;8~10 min,98% B3;10~10.1 min,98%~8% B3;10.1~12 min,8% B3。
质谱条件:Thermo Q-Exactive Focus质谱检测器,电喷雾离子源(ESI),正负离子模式分别采集数据。正离子喷雾电压为3.50 kV,负离子喷雾电压为-2.50 kV,鞘气40 arb,辅助气10 arb。毛细管温度325 ℃,以分辨率70 000进行一级全扫描,一级离子扫描范围m/z 100~1 000,并采用HCD进行二级裂解,碰撞能量为30 eV,二级分辨率为17 500,采集信号前3离子进行碎裂,同时采用动态排除去除无必要的MS/MS信息。
采用KNApSAcK、HMDB、LipidMaps、PubChem及KEGG等公共数据库进行物质的鉴定,参数设置为ppm<30 ppm。采用QC-SVRC归一化方法实现数据矫正,消除系统误差。数据质控中过滤掉QC样本中RSD>30%的物质。采用R软件包Ropls分别对样本数据进行主成分分析(principal component analysis,PCA)、偏最小二乘判别分析(partial least squares-discriminant analysis,PLS-DA)、正交偏最小二乘判别分析(orthogonal partial least squares-discriminant analysis,OPLS-DA)降维分析。并分别绘制得分图、载荷图和S-plot图,展示各样本间代谢物质组成的差异。
1.4 数据处理及分析
实验数据均以“平均值±标准差”表示,使用SPSS 22.0和Origin 9.1进行统计分析和方差分析,显著性差异水平设置为P<0.05。
2 结果与分析
2.1 粉碎方式对蓝莓出汁率和粒径的影响
不同粉碎方式对蓝莓出汁率和粒径的影响如图1所示。不同粉碎方式下蓝莓出汁率高低依次为湿法超微粉碎机(88.23%)>胶体磨(87.12%)>破壁机(84.97%),湿法超微粉碎机制备的蓝莓汁平均果浆粒径最小(64.26 μm),显著低于胶体磨(77.26 μm)和破壁机(78.04 μm),其原因可能是湿法超微粉碎机和胶体磨均利用固定磨子和高速旋转磨体的相对运动产生强烈的高频振动、剪切、摩擦和冲击等作用力粉碎物料,相比于破壁机简单的高速切割和粉碎方式,湿法超微粉碎机和胶体磨能更有效地提高果汁出汁率并降低残渣量[11]。
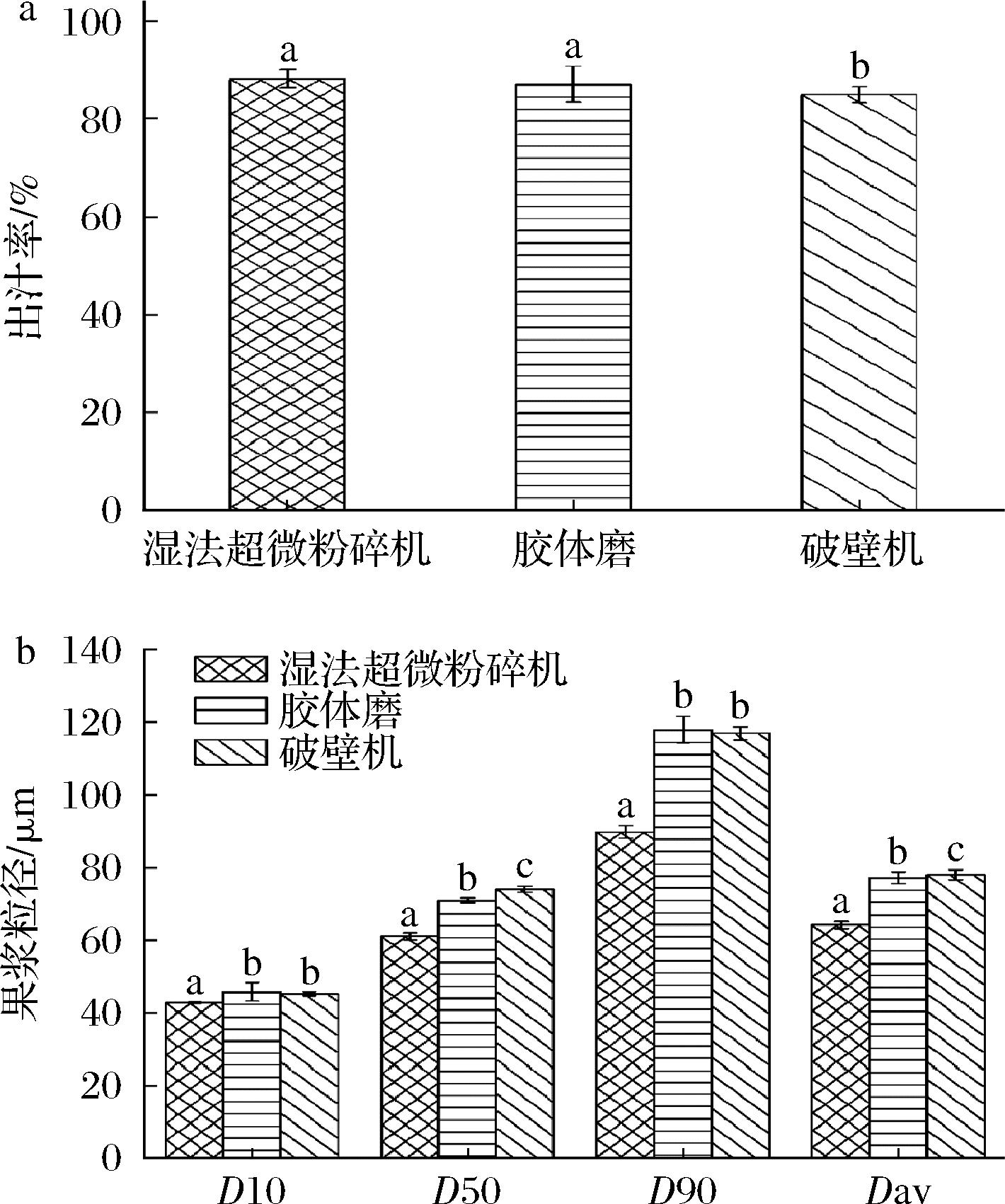
a-出汁率;b-粒径
图1 不同粉碎方式下蓝莓出汁率及粒径变化
Fig.1 Changes in juice yield and particle size of blueberries under different grinding methods
注:图中不同小写字母表示各组间差异显著(P<0.05),下同。
D10、D50和D90是评价果蔬汁粒径大小的重要参数,其中D50表示粒度分布中占50%所对应的粒径(又称电位径),D10表示粒度分布中占10%所对应的粒径,D90表示粒度分布中占90%所对应的粒径。与胶体磨和破壁机相比,湿法超微粉碎机制备的蓝莓汁具有更小的D10(42.73 μm)、D50(61.13 μm)和D90(89.79 μm),这说明湿法超微粉碎机制备的蓝莓汁颗粒较均匀,较大和较小的颗粒占比较小,其原因可能是湿法超微粉碎机分级系统一方面严格限制了大颗粒,另一方面又避免了物料过碎[12],进而得到了粒径分布更均匀的蓝莓汁。
2.2 粉碎方式对蓝莓汁活性物质含量的影响
不同粉碎方式下蓝莓果汁中维生素C、花色苷、总黄酮和总酚含量变化如图2所示。湿法超微粉碎组和胶体磨组蓝莓果汁中维生素C含量显著高于破壁机组(P<0.05),分别为94.63、95.28 mg/L和86.06 mg/L(图2-a),其原因可能是湿法超微粉碎机和胶体磨不会局部升温破坏蓝莓中的营养成分,但是破壁机破碎蓝莓时内部高速旋转的刀片会产生较大热量增加了维生素C的氧化程度[11],进而导致蓝莓汁中维生素C含量减少。

a-维生素C含量;b-花色苷含量;c-总黄酮含量;d-总酚含量
图2 不同粉碎方式下蓝莓汁活性物质变化
Fig.2 Changes of active substances in blueberry juice under different grinding methods
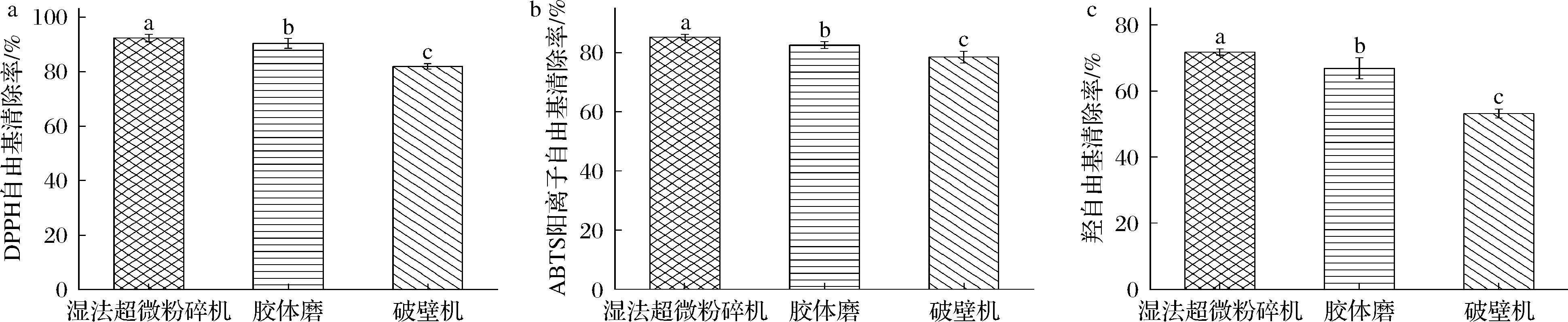
a-DPPH自由基清除率;b-ABTS阳离子自由基清除率;c-羟自由基清除率
图3 不同粉碎方式下蓝莓汁抗氧化活性变化
Fig.3 Changes in antioxidant activity of blueberry juice under different grinding methods
在湿法超微粉碎组蓝莓果汁中花色苷、总黄酮和总酚含量分别为613.64 mg/L、2.94 g/L和3.46 g/L,胶体磨组蓝莓果汁中花色苷、总黄酮和总酚含量分别为589.17 mg/L、2.61 g/L和2.97 g/L,破壁机组蓝莓果汁中花色苷、总黄酮和总酚含量分别为508.62 mg/L、2.49 g/L和3.03 g/L(图2-b~图2-d)。湿法超微粉碎组蓝莓果汁中花色苷、总黄酮和总酚含量均明显高于胶体磨组和破壁机组,其原因可能是:a)湿法超微粉碎机的粉碎速度快,在相同的粉碎时间下,蓝莓果汁中物质的粒径显著降低,其粒度更加细微均匀,比表面积增大,促进了花色苷、黄酮和多酚等活性物质溶出[13];b)湿法超微粉碎机相比于其他粉碎技术,粉碎粒度最小,能够将蓝莓充分粉碎,有效破坏蓝莓细胞壁,使细胞内部的活性物质充分溶出[14];c)湿法超微粉碎机不会局部升温,而破壁机在粉碎过程中存在明显的机械局部升温现象[11],进而破坏了活性物质或诱导其氧化而导致含量降低。
2.3 粉碎方式对蓝莓汁抗氧化活性的影响
不同粉碎方式下蓝莓果汁中抗氧化活性变化如图3所示。不同粉碎方式对蓝莓果汁DPPH自由基、ABTS阳离子自由基和羟自由基清除率的影响均存在显著差异(P<0.05),其中湿法超微粉碎组蓝莓果汁对3种自由基的清除率最高(分别为92.31%、85.29%和71.76%),而破壁机组蓝莓果汁对3种自由基的清除率最低(分别为81.89%、78.49%和53.17%),推测其原因可能是粉碎过程中温度过高时,酚类物质受热后引起氧化损失效应,导致花色苷、总黄酮和总酚含量降低,进而导致蓝莓果汁抗氧化活性降低[15]。不同粉碎方式对蓝莓果汁3种自由基清除率的影响变化趋势与3种活性物质含量变化趋势相似,进一步验证了蓝莓果汁的抗氧化能力与其花色苷、总黄酮和总酚的含量密切相关[16]。此外,3种粉碎组蓝莓果汁对DPPH自由基清除率均>80%、对ABTS阳离子自由基清除率均>78%,说明蓝莓果汁抗氧化作用主要表现为对DPPH自由基、ABTS阳离子自由基的强清除作用,这与崔燕等[17]的研究结果一致。
2.4 不同粉碎方式下蓝莓果汁中代谢物差异分析
2.4.1 蓝莓果汁差异代谢物总谱统计分析
基于UPLC-Q-Exactive Focus/MS的非靶向代谢组学分析用于鉴定和量化蓝莓果汁中的代谢产物,获得质荷比、保留时间和强度数据,在正模式和负模式下共分别检测到17 531和11 222个前体分子。图4为各实验组蓝莓果汁的总离子流图。
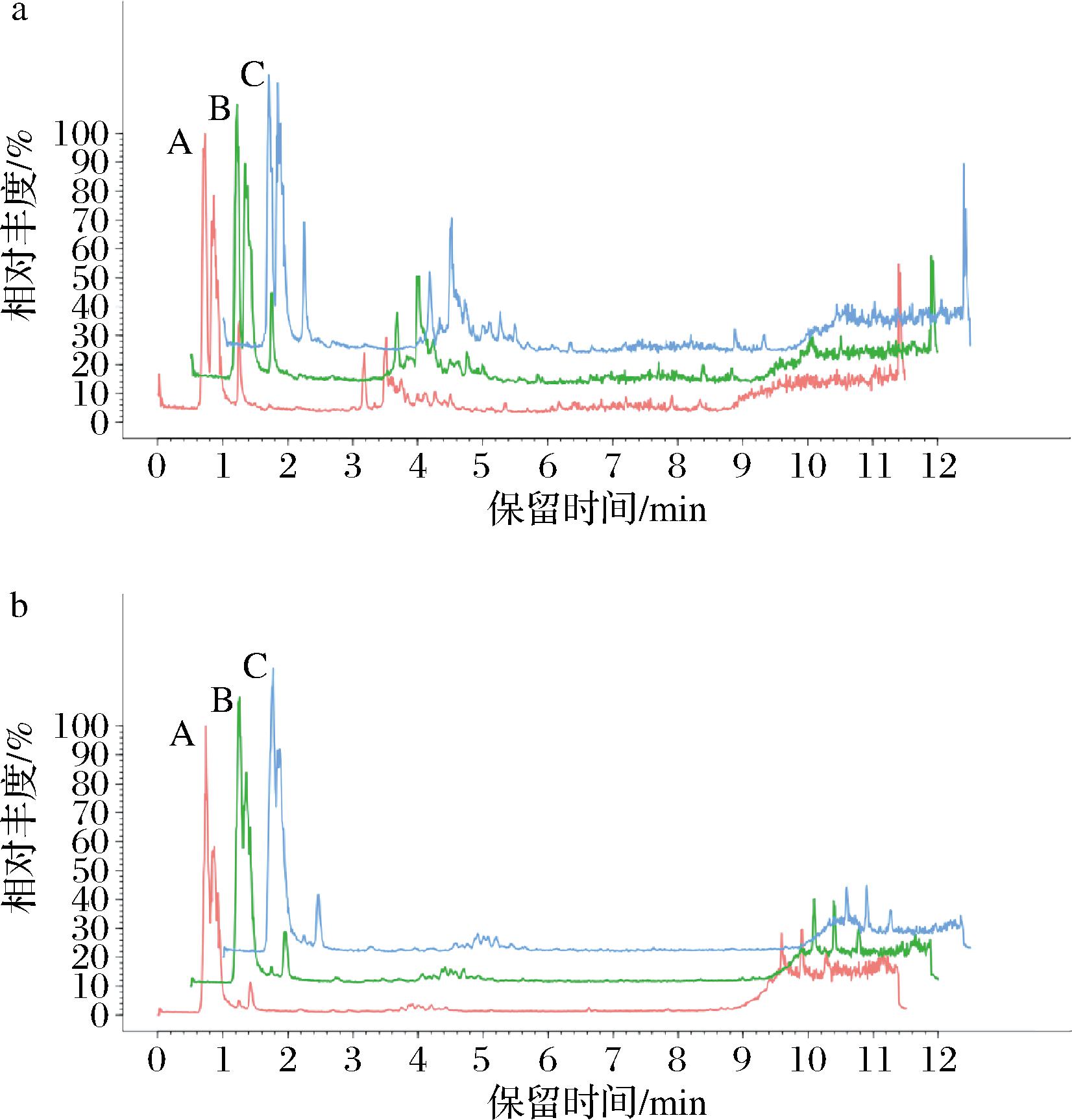
a-正离子基峰图;b-负离子基峰图
图4 蓝莓果汁代谢物总离子图
Fig.4 Total ion diagram of metabolites in blueberry juice
注:图中A、B、C分别表示破壁机组、胶体磨组和湿法 超微粉碎组蓝莓果汁(下同)。
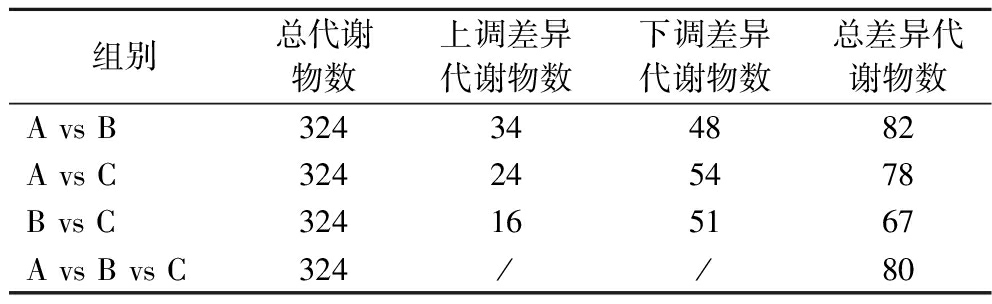
在总体代谢谱的基础上,进一步探讨了不同实验组蓝莓果汁之间差异表达的代谢产物。使用HMDB、massbank、LipidMaps、mzcloud以及KEGG等谱图数据库对蓝莓果汁代谢物质鉴定进行检索比对,将定量列表中含有二级谱图的代谢物与数据库中每个二级谱图的碎片离子等信息进行比较、匹配,实现代谢物的二级定性鉴定。经对比分析,各实验组蓝莓果汁中共鉴定到324种代谢物,进一步采用PLS-DA模型用于组间配对比较分析,PLS-DA模型中VIP值>1、Fold Change≥2或≤0.5作为阈值,筛选得到各组间二级差异表达的代谢物(表1)。破壁机和胶体磨组间差异代谢物数为82种,其中34种显著上调,48种显著下调;破壁机和湿法超微粉碎组间差异代谢物数为78个,其中24种显著上调,54种显著下调;胶体磨和湿法超微粉碎组间差异代谢物数为67个,其中16种显著上调,51种显著下调;而3种粉碎方式下蓝莓果汁组间的总差异代谢物数为80个。
表1 蓝莓果汁各组间代谢物数量
Table 1 Number of metabolites between different groups in blueberry juice
组别总代谢物数上调差异代谢物数下调差异代谢物数总差异代谢物数A vs B324344882A vs C324245478B vs C324165167A vs B vs C324//80
2.4.2 蓝莓果汁二级代谢物差异分析
对3种粉碎方式制备蓝莓果汁的差异代谢物进行聚类热图分析,结果如图5所示(渐变颜色表示定量值的大小,颜色越红表达量越高,越蓝表达量越低)。由图5可知,胶体磨组和湿法超微粉碎组蓝莓果汁差异代谢物表达量总体显著高于破壁机组蓝莓果汁,破壁机组蓝莓果汁中仅有30种代谢物相对表达量较高。其中,破壁机组蓝莓果汁中表达量较高的代谢物有D-阿洛酮糖、阿洛糖、亚精胺、黄豆黄素和大豆苷元,胶体磨组蓝莓果汁中表达量较高的代谢物有秦皮素、L-高脯氨酸、磷酸胆碱、芥子酸和异阿魏酸,湿法超微粉碎组蓝莓果汁中表达量较高的代谢物有圣草酚、绿原酸、异槲皮素、杨梅素和原花青素B2。
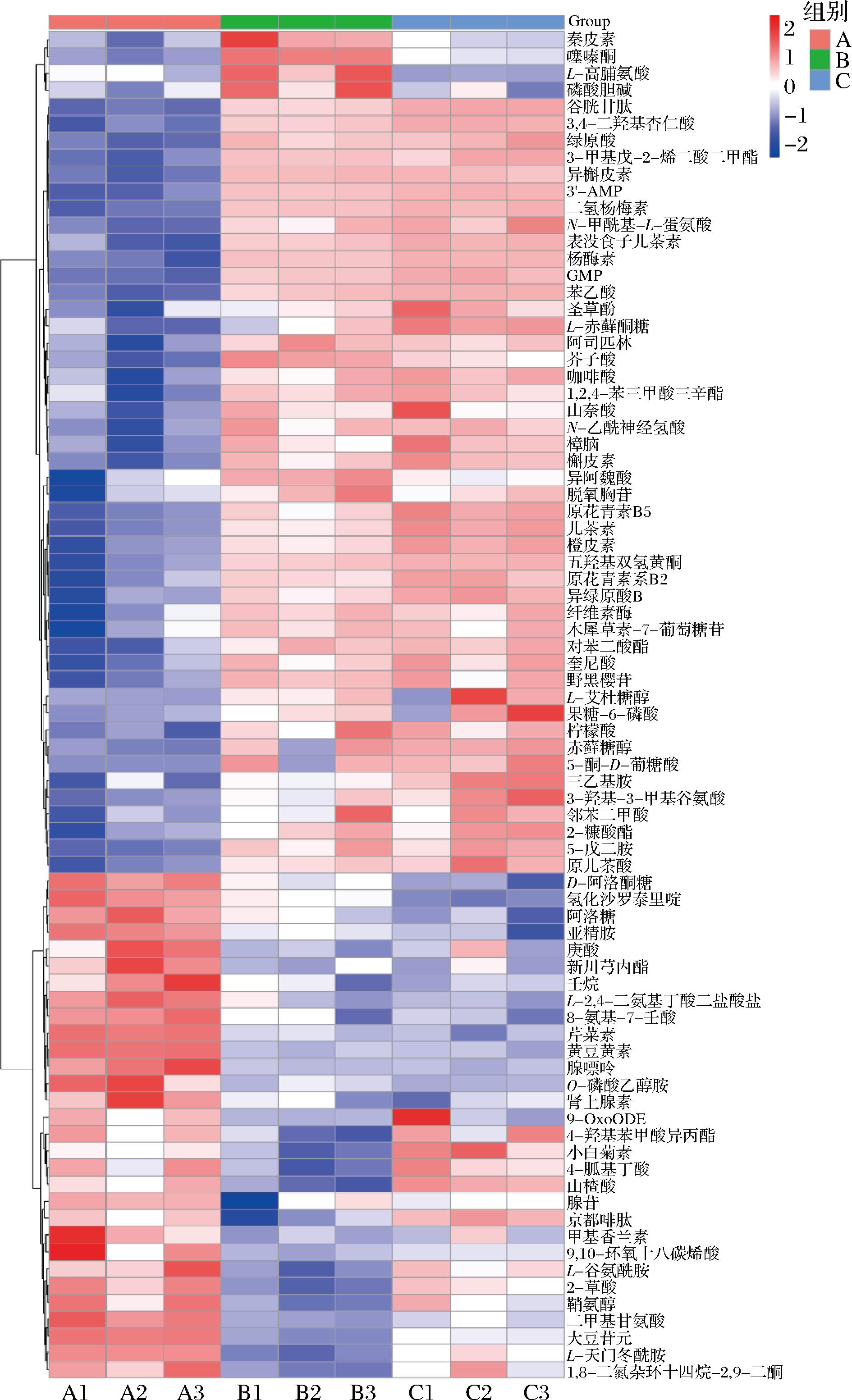
图5 不同粉碎方式下蓝莓果汁差异代谢物表达量变化
Fig.5 Changes in differential metabolite expression levels of blueberry juice under different grinding methods
2.4.3 蓝莓果汁多酚类代谢物差异分析
对3种粉碎方式制备蓝莓果汁的多酚类差异代谢物进行聚类热图分析,结果如图6所示。在破壁机组中,仅有7种多酚类代谢物表达量上调,分别是三叶豆紫檀苷、芹菜素、黄豆黄素、没食子儿茶素、矢车菊素-3-半乳糖苷、大豆苷元和甘草西定。与破壁机组和胶体磨组相比,湿法超微粉碎组蓝莓果汁中黄豆苷表达量显著上调。其原因可能是因为结合型异黄酮糖苷(黄豆苷)容易在酶催化、酸碱、高温等条件下水解脱去糖基,进而形成异黄酮苷元(黄豆黄素、大豆苷元)[18]。有研究表明,游离型苷元比其结合型糖苷具有更强的不愉快风味[19],这也说明湿法超微粉碎组蓝莓果汁在风味上更具有优势。
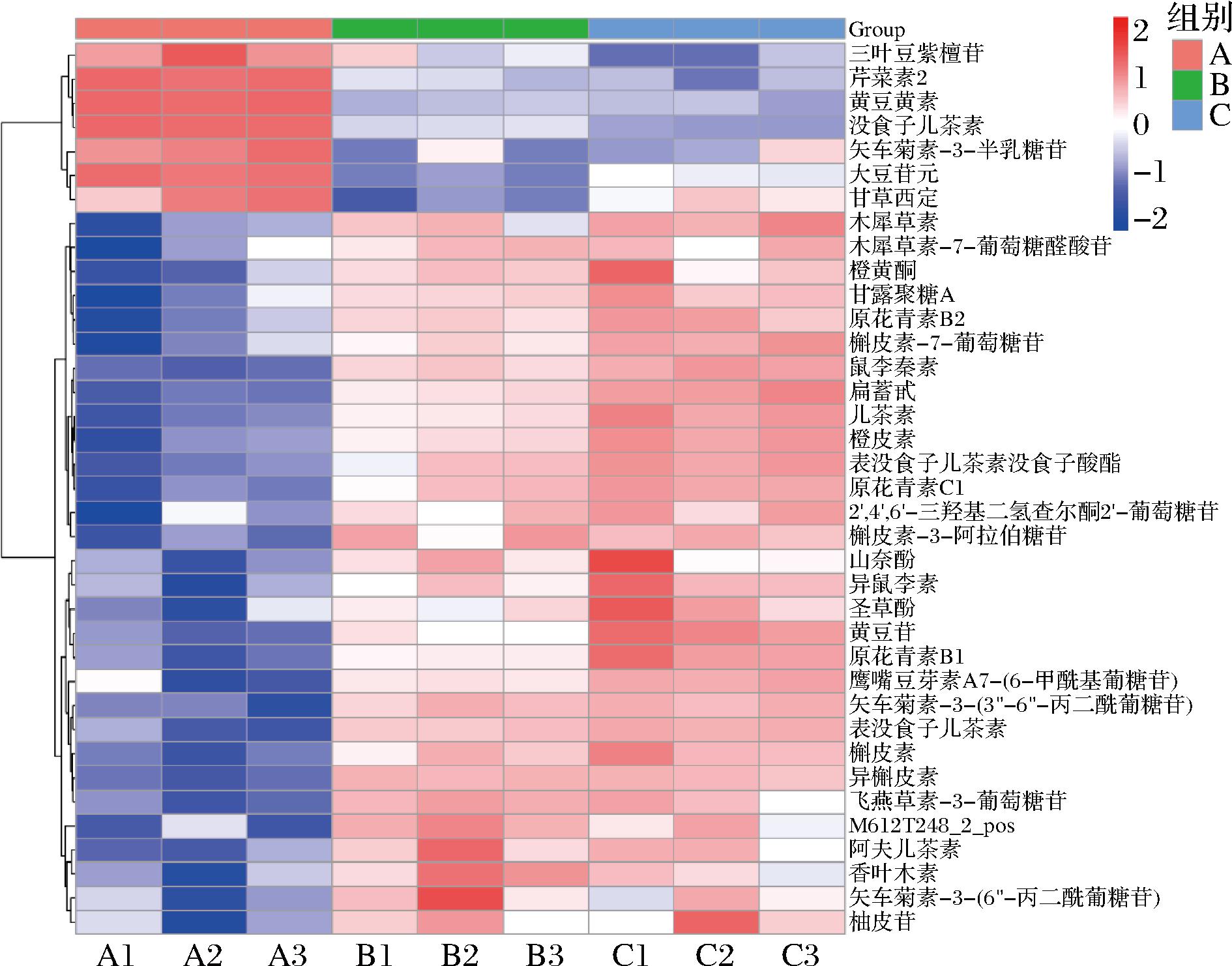
图6 不同粉碎方式下蓝莓果汁多酚类差异 代谢物表达量
Fig.6 Expression levels of differential metabolites of polyphenols in blueberry juice under different crushing methods
与破壁机组相比,胶体磨组和湿法超微粉碎组蓝莓果汁中大多数多酚类差异代谢物表达量表现为上调趋势,其中湿法超微粉碎组差异代谢物表达量上调趋势更显著。特别是,湿法超微粉碎组蓝莓果汁中3种原花青素B1、B2和C1均显著高于破壁机组和胶体磨组,与不同粉碎方式下蓝莓果汁中花色苷含量变化趋势相似。原花青素是植物中广泛存在的一类多酚类化合物,其具有强抗氧化、消除自由基的作用,可有效消除超氧阴离子自由基和羟自由基[20]。THUY等[21]采用密度泛函理论和分子对接方法探究了原花青素B1的抗氧化潜力,结果表明原花青素B1抗氧化作用是通过其与金属离子的螯合作用来实现,其中与结合能较低的金属离子(如Cu2+)形成的络合物更稳定,分子对接结果显示原花青素B1抗氧化作用是通过与必需残基相互作用抑制酪氨酸酶活性来实现,主要集中在两个苯环的羟自由基基团上。此外,CHEN等[22]评估了葡萄籽中原花青素结构与其抗氧化活性之间的关系,结果表明原花青素(B1、B2、B3、B4、B1-G、B2-G和C1)处理降低了活性氧和丙二醛的含量,增加了抗氧化酶谷胱甘肽过氧化物酶、过氧化氢酶和超氧化物歧化酶的活性。以上研究表明,果蔬中原花青素B1、B2和C1均具有较强抗氧化性,这也解释了本研究中湿法超微粉碎组蓝莓果汁中具有强抗氧化性源于高含量的花色苷和多酚。
同时,湿法超微粉碎组蓝莓果汁中槲皮素、异槲皮素、槲皮素-7-葡萄糖苷和槲皮素-3-阿拉伯糖苷显著高于破壁机组和胶体磨组。槲皮素是广泛存在于水果、蔬菜、中草药中的活性物质,具有抗氧化、抗菌、抗病毒、抗癌、提高免疫力等作用[23]。近年来,大量研究[24]已揭示了果蔬中槲皮素和异槲皮素含量与其抗氧化活性显著相关,本研究酚类代谢物和抗氧化活性结果进一步验证了这一关系。此外,WANG等[25]在高丛蓝莓的抗炎和抗氧化作用研究中发现,高丛蓝莓抗氧化活性与槲皮素3-半乳糖苷、槲皮素3-阿拉伯糖苷和槲皮素3-鼠李糖苷密切相关;MOTHANA等[26]研究发现,蓝莓中槲皮素-3-阿拉伯糖苷含量与抗氧化酶活性(超氧化物歧化酶、愈创木酚过氧化物酶、谷胱甘肽过氧化物酶、抗坏血酸过氧化物酶、脱氢抗坏血酸还原酶、单脱氢抗坏血酸还原酶和谷胱甘肽还原酶)以及非酶成分(抗坏血酸、谷胱甘肽)显著相关,并揭示了槲皮素-3-阿拉伯糖苷能促进抗氧化性能和清除活性氧。综上所述,本研究中湿法超微粉碎组蓝莓果汁槲皮素及其异构体分子显著上调,并且与其抗氧化活性变化规律、总酚和总黄酮含量变化趋势相吻合,说明槲皮素及其异构体分子是蓝莓果汁具有强抗氧化作用的关键活性物质。
3 结论
本研究利用破壁机、胶体磨、湿法超微粉碎机结合复合酶法制备蓝莓果汁,分析不同粉碎方式对蓝莓果汁加工特性、活性物质含量和抗氧化活性的影响,并采用代谢组学分析蓝莓果汁中代谢物差异变化。结果表明,不同粉碎方式下蓝莓出汁率无显著差异,但湿法超微粉碎组蓝莓果汁平均果浆粒径最小,活性物质含量和抗氧化活性均最高;湿法超微粉碎组蓝莓果汁中黄豆苷、原花青素、槲皮素及其异构体分子表达量显著上调,是其抗氧化活性显著高于胶体磨组和破壁机组的根本原因。该研究结果可为拓宽湿法超微粉碎技术应用和制备高营养高品质蓝莓汁提供理论依据。
[1] 李梓旋, 郭佳婧, 苏东林, 等.蓝莓花色苷生理活性、提取纯化及稳态化研究进展[J].中国食品学报, 2024, 24(2):407-417.LI Z X, GUOJIA J, SU D L, et al.Research progress on physiological activity, extraction and purification, and stabilization of anthocyanins in blueberry[J].Journal of Chinese Institute of Food Science and Technology, 2024, 24(2):407-417.
[2] TOBAR-BOLA OS G, CASAS-FORERO N, ORELLANA-PALMA P, et al.Blueberry juice:Bioactive compounds, health impact, and concentration technologies-a review[J].Journal of Food Science, 2021, 86(12):5062-5077.
OS G, CASAS-FORERO N, ORELLANA-PALMA P, et al.Blueberry juice:Bioactive compounds, health impact, and concentration technologies-a review[J].Journal of Food Science, 2021, 86(12):5062-5077.
[3] 汤丽娟. 贵州省麻江县蓝莓产业融合发展模式研究[D].贵阳:贵州大学, 2023.TANG L J.Research on the integrated development model of blueberry industry in Majiang county, Guizhou province[D].Guiyang:Guizhou University, 2023.
[4] PILAND D, BROWNING L.Acceptability of 100% blueberry juice, fiber-fortified, antioxidant-rich rooibos tea containing sorbet developed to help prevent type 2 diabetes[J].Journal of the Academy of Nutrition and Dietetics, 2022, 122(9):A13.
[5] 刘慧, 刘杰超, 吕真真, 等.加工工艺对蓝莓汁和蓝莓酒中花色苷及类黄酮的影响[J].中国酿造, 2018, 37(8):158-162.LIU H, LIU J C, LV Z Z, et al.Effect of processing technology on the contents of anthocyanins and flavonoids in blueberry juice and wine[J].China Brewing, 2018, 37(8):158-162.
[6] 冯晶晶, 郭建峰, 马心茹, 等.超微粉碎对沙棘茶粉颗粒结构及理化特性的影响[J].食品与发酵工业, 2023, 49(7):198-204.FENG J J, GUO J F, MA X R, et al.Effects of ultrafine grinding on powder structure and physicochemical properties of sea buckthorn tea[J].Food and Fermentation Industries, 2023, 49(7):198-204.
[7] WU Y M, XU L Q, LIU X Y, et al.Effect of thermosonication treatment on blueberry juice quality:Total phenolics, flavonoids, anthocyanin, and antioxidant activity[J].LWT, 2021, 150:112021.
[8] CHEN T S, LI B, SHU C, et al.Combined effect of thermosonication and high hydrostatic pressure on bioactive compounds, microbial load, and enzyme activities of blueberry juice[J].Food Science and Technology International, 2022, 28(2):169-179.
[9] 李晨, 张秀玲, 李凤凤, 等.五种小浆果抗氧化活性和相关营养物质的测定及主成分分析[J].食品与发酵工业, 2022, 48(14):226-234.LI C, ZHANG X L, LI F F, et al.Determination of antioxidant activity, nutrients and quality evaluation using principal component analysis of five kinds of small berries[J].Food and Fermentation Industries, 2022, 48(14):226-234
[10] 程宏桢, 蔡志鹏, 王静, 等.百香果全果酒发酵工艺优化及体外抗氧化性比较分析[J].中国酿造, 2020, 39(4):91-97.CHENG H Z, CAI Z P, WANG J, et al.Optimization of fermentation process for whole passion fruit wine and comparative analysis of antioxidant activity in vitro[J].China Brewing, 2020, 39(4):91-97.
[11] 潘浪, 胡筱, 丁胜华, 等.湿法超微粉碎对脐橙全果浆多酚及抗氧化活性的影响[J].湖南农业科学, 2018(10):95-99.PAN L, HU X, DING S H, et al.Effects of wet superfine grinding on polyphenols and antioxidant activities of whole fruit pulp of navel orange[J].Hunan Agricultural Sciences, 2018(10):95-99.
[12] 孟庆然. 超微粉碎对天然可食植物组织理化性质及营养素释放效率影响的研究[D].南京:江南大学, 2019.MENG Q R.Study on the effects of superfine grinding on physicochemical properties and nutrients release efficiency of natural edible plant tissues[D].Nanjing:Jiangnan University, 2019.
[13] 陈菊红, 顾正彪, 洪雁.湿法超微粉碎对马铃薯渣的改性及对其物理性质的影响[J].食品与发酵工业, 2008, 34(10):58-62.CHEN J H, GU Z B, HONG Y.Effect of ultra-fine pulverization by wet processing on modification and physical properties of potato pulp[J].Food and Fermentation Industries, 2008, 34(10):58-62.
[14] 杨蕾, 贾艳菊, 刘敬科, 等.超微粉碎技术对粮食产品营养物质及特定生理功能影响的研究进展[J].食品与机械, 2023, 39(12):200-207; 213.YANG L, JIA Y J, LIU J K, et al.Research progress on the effects of ultrafine grinding technology on nutrients and specific physiological functions of grain products[J].Food &Machinery, 2023, 39(12):200-207; 213.
[15] 蔡亭, 汪丽萍, 刘明, 等.超微粉碎对苦荞多酚及抗氧化活性的影响研究[J].中国粮油学报, 2015, 30(10):95-99; 106.CAI T, WANG L P, LIU M, et al.The influence of micronization on polyphenols and antioxidant activity of buckwheat powder[J].Journal of the Chinese Cereals and Oils Association, 2015, 30(10):95-99; 106.
[16] 田竹希, 戴梦玲, 李咏富, 等.蓝莓果浆不同形态多酚的酶法转化工艺优化及抗氧化活性分析[J].食品工业科技, 2023, 44(9):207-215.TIAN Z X, DAI M L, LI Y F, et al.Optimization of enzymatic transformation process for different forms of polyphenols from blueberry pulp and its antioxidant activity analysis[J].Science and Technology of Food Industry, 2023, 44(9):207-215.
[17] 崔燕, 宣晓婷, 朱宏芬, 等.不同品种蓝莓制汁特性评价[J].食品工业科技, 2024, 45(15):304-312.CUI Y, XUAN X T, ZHU H F, et al.Evaluation of juice processing characteristics of blueberry from different cultivars[J].Science and Technology of Food Industry, 2024, 45(15):304-312.
[18] LU C W, LI F Y, YAN X X, et al.Effect of pulsed electric field on soybean isoflavone glycosides hydrolysis by β-glucosidase:Investigation on enzyme characteristics and assisted reaction[J].Food Chemistry, 2022, 378:132032.
[19] 李紫微, 曹庸, 苗建银.大豆异黄酮及其苷元的研究进展[J].食品工业科技, 2019, 40(20):348-355.LI Z W, CAO Y, MIAO J Y.Research progress of soy isoflavones and aglycones[J].Science and Technology of Food Industry, 2019, 40(20):348-355.
[20] 崔海鹏, 郭健龙, 王大全, 等.花青素加工稳定性及其研究进展[J].食品与发酵工业, 2024, 50(13):388-397.CUI H P, GUO J L, WANG D Q, et al.Stability of anthocyanins during processing and research progress[J].Food and Fermentation Industries, 2024, 50(13):388-397.
[21] THUY P T, QUAN P M, DUC D X, et al.The antioxidative potential of procyanidin B1:DFT (density functional theory) and docking approaches[J].Journal of Molecular Modeling, 2022, 28(11):356.
[22] CHEN J, CHEN Y X, ZHENG Y F, et al.The relationship between procyanidin structure and their protective effect in a Parkinson’s disease model[J].Molecules, 2022, 27(15):5007.
[23] 肖敏, 陈宇, 韩林, 等.银杏叶黄酮提取物对秀丽线虫抗氧化和衰老的效果研究[J/OL].食品与发酵工业, 2024.DOI:10.13995/j.cnki.11-1802/ts.038307.XIAO M, CHEN Y, HAN L, et al.Effects of flavonoid extract from Ginkgo biloba leaves on antioxidation and anti-aging of Caenorhabditis elegans[J/OL].Food and Fermentation Industries, 2024.DOI:10.13995/j.cnki.11-1802/ts.038307.
[24] ZYMONE K, BENETIS R, TRUMBECKAS D, et al.Different effects of quercetin glycosides and quercetin on kidney mitochondrial function-uncoupling, cytochrome C reducing and antioxidant activity[J].Molecules, 2022, 27(19):6377.
[25] WANG S Y, CHEN C T.Effect of allyl isothiocyanate on antioxidant enzyme activities, flavonoids and post-harvest fruit quality of blueberries (Vaccinium corymbosum L., cv.Duke)[J].Food Chemistry, 2010, 122(4):1153-1158.
[26] MOTHANA R A A, AL-SAID M S, AL-REHAILY A J, et al.Anti-inflammatory, antinociceptive, antipyretic and antioxidant activities and phenolic constituents from Loranthus regularis Steud.ex Sprague[J].Food Chemistry, 2012, 130(2):344-349.