甜菊糖苷是从甜菊叶中提取的一类高甜度、低热量的天然甜味剂[1-2]。这类甜味剂具有良好的稳定性,不会引起血糖升高,且无发酵与褐变反应,并具有广泛的药理活性[3-5]。近几年来甜菊糖苷作为无公害的食品添加剂受到了全球消费者和开发商的欢迎。2008年起,甜菊糖苷被世界卫生组织食品添加剂联合专家委员会等官方组织批准作为食品药品添加剂[6]。但是,甜菊糖苷的主要成分莱鲍迪苷A(rebaudioside A, RA)和甜菊苷(stevioside, Stv)有令人不愉悦的后苦味,严重影响口感。研究表明,RA后苦涩味源于其自身的化学结构[5]。RA的结构如图1所示,实验证明,甜菊苷和甜叶悬钩子苷在甜菊醇骨架C-13位点碳水化合物部分的单(α1→4)-葡萄糖基化可显著改善产品的甜味强度和甜味质量[7-8]。然而,甜菊醇的β1→C-19位点的(α1→4)-葡萄糖基化导致苦味余味增加和甜味强度降低[9-10]。因此,对甜菊糖苷进行糖基化修饰成为降低甜菊糖苷后苦味的有效方法,即通过将葡萄糖基附着在决定其口感的C-19和/或C-13位点上,获得口感更佳的甜菊糖苷糖基化产物,同时也保留了其低热量的特性。
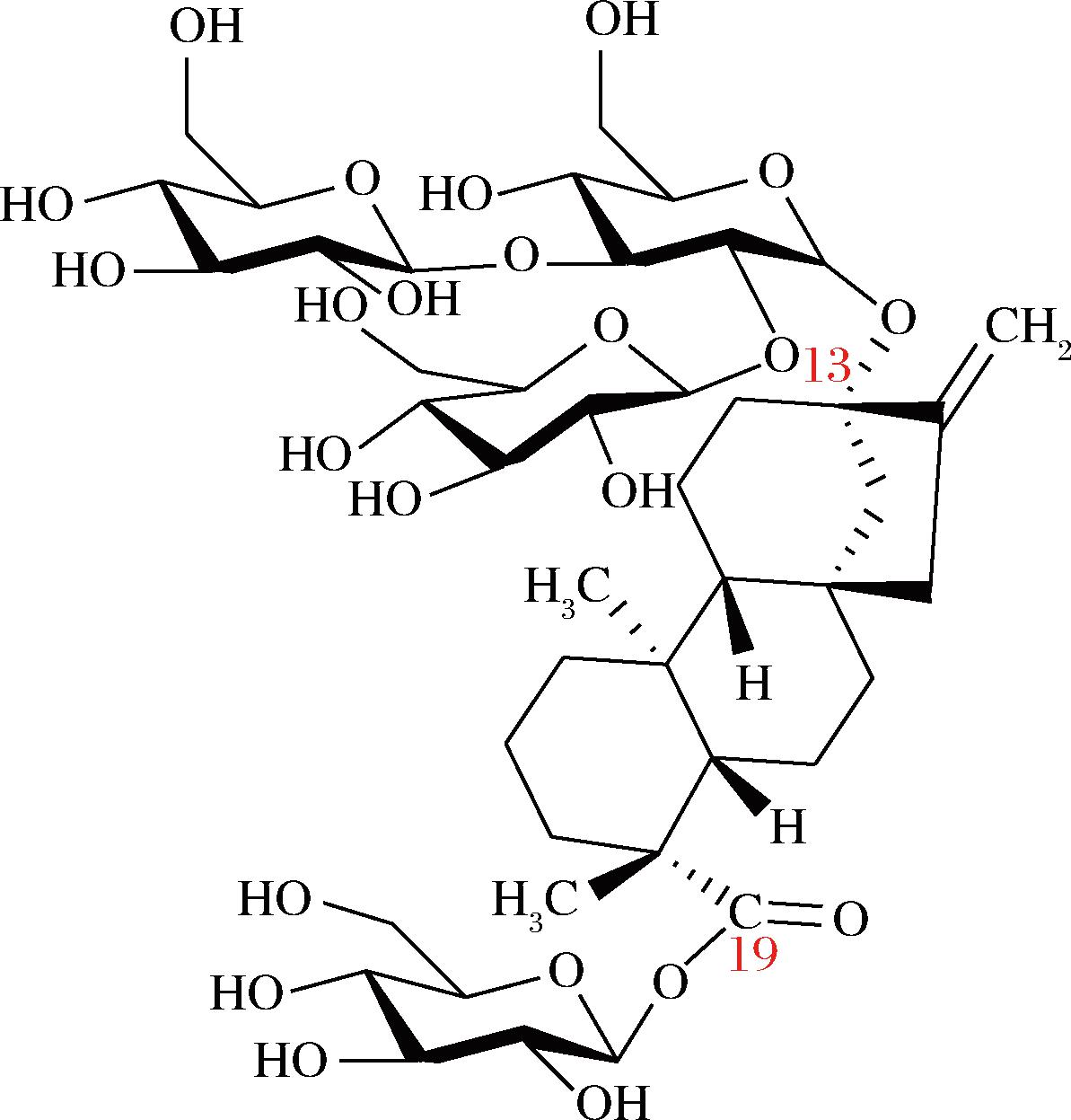
图1 莱鲍迪苷A结构
Fig.1 Structure of rebaudioside A
目前,用于甜菊糖苷糖基化修饰的酶主要有UDP-葡萄糖基转移酶(uridine diphosphate glycosyltransferase, UGTase)[11-12]和环糊精葡萄糖基转移酶(cyclodextrin glucosyltransferase, CGTase)[13-15],然而,由于UGTase属于Leloir-糖基转移酶,需要依赖昂贵的核苷酸激活糖(如UDPG)作为糖基供体,所以不适合工业化应用[11]。而CGTase属于非Leloir-糖基转移酶,应用成本较低,因此常被用于甜菊糖苷糖基化修饰。CGTase属于α-淀粉酶家族(GH 13),可通过分子内转糖基作用(环化作用)生成环糊精[16],同时具有歧化、偶合、水解的作用[17],其中偶合和歧化作用在分子间转糖基反应中发挥关键作用。因此CGTase可用于将供体底物糖基转移到各种受体化合物(如糖、醇、维生素、甜菊糖苷、多元醇和黄酮类化合物),改善其性质[17]。然而,CGTase的产物特异性较差,例如CGTase催化甜菊糖苷糖基化反应,生成不同糖链长度的糖基化产物混合物[18]。据报道,单-和双-α-1,4-葡萄糖基化可显著改善甜菊苷的甜味强度和感官品质,但当转糖基个数超过3个时,甜菊苷的甜味强度和感官质量急剧下降[8]。CGTase的糖基化效率和产物特异性极大地影响了产品的品质。因此,目前迫切需要挖掘高效且高产物特异性的CGTase用于甜菊糖苷糖基化修饰。
从产品角度来看,以RA为底物转化的糖基化甜菊糖苷具有更好的口感。此外,目前已知口感好的化合物都是在RA的基础上进行糖基化,且“糖基化程度”较低[1,19-20],例如莱鲍迪苷D(rebaudioside D, RD),在RA的C19上加一个葡萄糖基和莱鲍迪苷M(rebaudioside M, RM),在RD的C19上添加一个葡萄糖基。因此,对于RA的酶法修饰,提高RA的转化率、增加短链糖基化产物的含量对于口感改善具有重要意义。因此,在本研究中,通过筛选不同来源的CGTase,并优化催化条件来达到优化RA转化率,增加短链糖基化产物的目的。
1 材料与方法
1.1 材料与试剂
表达菌株Escherichia coli BL21(DE3)感受态细胞购于中国诺维信公司;含有不同来源CGTase基因的重组质粒pET28a/α-cgt[GenBank:JX412224,来源于浸麻芽孢杆菌(Paenibacillus macerans)]、pET28a/β-cgt[GenBank:P31797,来源于嗜热脂肪芽孢杆菌(Bacillus stearothermophilus)]、pET28a/γ-cgt(GenBank:WP_090889670,来源于Evansella caseinilytica),由苏州亦欣生物科技有限公司合成;RA,浩天药业有限公司;水溶性淀粉、麦芽糊精,上海阿拉丁生化科技公司;α-环糊精、β-环糊精,上海生工有限公司;其他试剂均为分析级,中华试剂网。
LB培养基(g/L):胰蛋白胨10,酵母提取物5,NaCl 10,固体培养基即加入琼脂粉20,去离子水溶解并分装随后灭菌。
TB培养基(g/L):胰蛋白胨12,酵母提取物24,K2HPO4·3H2O 16.43,KH2PO4 2.31,甘油5,去离子水溶解并分装随后灭菌。
1.2 仪器和设备
DK-8D数显控温水浴锅,常州金坛荣华仪器厂;DKT200-2加热型金属浴,杭州米欧仪器有限公司;12-0625 Mini Protein 3蛋白电泳仪、XR+ GelDoc-it凝胶成像系统、Gel Doc XR核酸电泳仪,美国Bio-Rad公司;Aligent 1260高效液相色谱仪,美国Aligent科技有限公司;CT90A立式圆形压力蒸气灭菌器,南京庚辰科学仪器有限公司;LE438 pH测定仪,梅特勒-托利多公司;XBridge BEH Amide氨基色谱柱,美国沃特世公司;HYL-C、ZQZY-88CN、ZQZY-85AN恒温培养振荡器, 上海博讯实业有限公司医疗设备厂; 991超低温冰箱、Thermo Nanodrop 2000 Nanodrop、nexus GX2基因扩增仪、Centrifuge 5810R台式冷冻离心机,德国Eppendorf公司;PowerWave XS2酶标仪,BIOTEK基因有限公司;MALDI SYNAPT MS串联四极杆飞行时间质谱仪,美国沃特世公司;AVANCE NEO 600MHz核磁共振谱仪,德国布鲁克公司。
1.3 重组酶的表达与纯化
将带有重组质粒pET28a/α-cgt、pET28a/β-cgt、pET28a/γ-cgt的E.coli BL21(DE3)菌株接种于含有50 μg/mL卡纳抗生素的5 mL LB培养基中,于37 ℃进行过夜培养,随后按照1%接种量转移到含有50 μg/mL卡纳抗生素的40 mL TB培养基,继续在37 ℃扩大培养,待OD600值达到0.8~1.0,使用IPTG(终浓度为0.05 mmol/L)对其进行诱导,诱导条件为16 ℃,18~20 h。
通过离心(8 000 r/min、5 min)收集细胞,并将细胞重悬于缓冲液A(pH 7.4,20 mmol/L咪唑,0.5 mol/L NaCl,20 mmol/L PBS),在冰水浴中超声波破碎10 min。离心后取上清液加载到用缓冲液A预平衡的Ni-NTA亲和柱(Qiagen,Chatsworth,CA,USA)上。缓冲液B(pH 7.4,200 mmol/L咪唑,0.5 mol/L NaCl,20 mmol/L PBS)用于洗脱目的蛋白。随后,用缓冲液C(pH 6.0,50 mmol/L PBS)通过超滤管脱盐除去咪唑后得到纯化的酶蛋白,最后在液氮中冷冻并储存于-80 ℃冰箱备用。
1.4 环糊精糖基转移酶活性测定
使用甲基橙法分析CGTase的环化活力[21]。测活反应体系包括100 μL稀释酶溶液(25 μg/mL),50 μL水溶性淀粉溶液(40 g/L)与100 μL PBS(pH 6.0,50 mmol/L),将反应体系在40 ℃下孵育10 min。反应结束后加入250 μL HCl溶液(1.0 mol/L)终止反应,随后加入150 μL甲基橙溶液(0.5 mmol/L),室温下(25 ℃)孵育20 min后,在酶标仪上测定505 nm处吸光度。使用浓度为1、2、4、6、8、10 mmol/L α-环糊精做标准溶液,空白对照中用PBS替换酶溶液。一个单位的环化活力定义为每分钟产生1 μmol α-环糊精所需的CGTase酶量。
使用4,6-亚乙基-对硝基苯-α-D-麦芽七糖苷(4-nitrophenyl-α-D-maltoheptaoside-4-6-O-ethylidene,EPS)为底物分析CGTase歧化活力[22]。其中EPS作为糖基供体,麦芽糖作为糖基受体,通过CGTase将EPS上的葡萄糖基转移至麦芽糖上。首先,将300 μL EPS(4 mmol/L)和300 μL麦芽糖(0.2 mmol/L)溶解在PBS(pH 6.0,50 mmol/L)中并在50 ℃下预热。然后将它们混合并加入100 μL稀释的酶溶液,在50 ℃下孵育10 min。随后,将样品与100 μL α-葡萄糖苷酶在60 ℃下孵育1 h,释放对硝基苯酚以形成非封闭的线性寡糖。然后加入100 μL Na2CO3(1 mol/L)以调节pH至8.0。在400 nm处测量对硝基苯酚的吸光度。一个单位的歧化活力定义为每分钟转化1 μmol EPS的酶量。
CGTase水解活性可通过DNS比色法分析[23]。将50 μL稀释的酶溶液与200 μL可溶性淀粉溶液(10 g/L)在50 ℃下孵育10 min。然后加入500 μL DNS溶液在100 ℃煮沸7 min终止反应,并立即在冰水浴中冷却。使用等体积的水稀释后,在540 nm处测量溶液的吸光度。一个单位的水解活力定义为每分钟产生1 μmol还原糖的酶量。
1.5 RA的糖基化反应
在初始反应中,将RA(5 mg/mL)和麦芽糊精(10 mg/mL)溶于PBS(pH 6.0,50 mmol/L)中,加入纯化后的CGTase(25 μg/mL),并将混合物在50 ℃下孵育12 h以进行反应。基于初始反应条件,分别对反应温度(35、40、45、50、55、60 ℃),糖基供体(麦芽糖、水溶性淀粉、麦芽糊精、α-环糊精、β-环糊精),底物质量比(RA∶水溶性淀粉=1∶0.5、1∶1、1∶1.5、1∶2、1∶3、1∶5、1∶6.5),反应pH(5.0、5.5、6.0、6.5、7.0、7.5、8.0),加酶量(1、2.5、5、10、25、50、100、250 μg/mL)、反应时间(1、2、3、4、6、8、10、12、16、24 h)进行优化。
1.6 HPLC检测方法
RA糖基化产物通过HPLC方法进行分析。采用带有紫外检测器的液相色谱仪,色谱柱(4.6 mm×250 mm,5 μm),柱温为30 ℃,在210 nm分析产物及底物峰。流动相为乙腈和水的混合物,洗脱梯度为0~2 min:V(乙腈)∶V(水)=80∶20;2~50 min:V(乙腈)∶V(水)=50∶50,流速为1 mL/min。体系内物质得率的计算如公式(1)~公式(3)所示:
产物占比![]()
(1)
转化率![]()
(2)
产率![]()
(3)
式中:SRA-nG,产物峰面积;S产物,产物峰面积总和;SRA,底物峰面积;S0,底物初始峰面积。
1.7 数据处理
所有实验组为3组数据的平均值,数据和误差使用Origin 8.0软件进行处理与分析。
2 结果与分析
2.1 CGTase的筛选
分别以RA和麦芽糊精作为糖基受体和糖基供体,通过4种不同的CGTase进行糖基化反应。这4种CGTase分别为来源于P. macerans的CGTase(α-CGTase),来源于B. stearothermophilus的CGTase(β-CGTase)和来源于E. caseinilytica的CGTase(γ-CGTase)及一种商业化的来自地下热厌氧杆菌属(Thermoanaerobacter)的CGTase(Toruzyme 3.0L)。如图2-a所示,在不同的CGTase催化下,产生了不同糖链长度的RA糖基化产物。相较于Toruzyme 3.0L和β-CGTase,α-CGTase在催化RA糖基化反应出现的产物峰的个数较少,说明其中α-CGTase催化生成的主要产物种类相对较少。相较于γ-CGTase,α-CGTase产生的短链产物峰面积较大,说明其短链产物特异性较好。如图2-b所示,对不同CGTase催化RA糖基化反应中残余底物RA和生成产物的峰面积进行比较,发现α-CGTase催化产生的短链糖基化产物占比较高,从而导致较好的口感。为了进一步提高α-CGTase催化RA糖基化的转化率以及短链产物特异性,提升其工业化潜力,本研究对α-CGTase的反应条件进行进一步的优化。
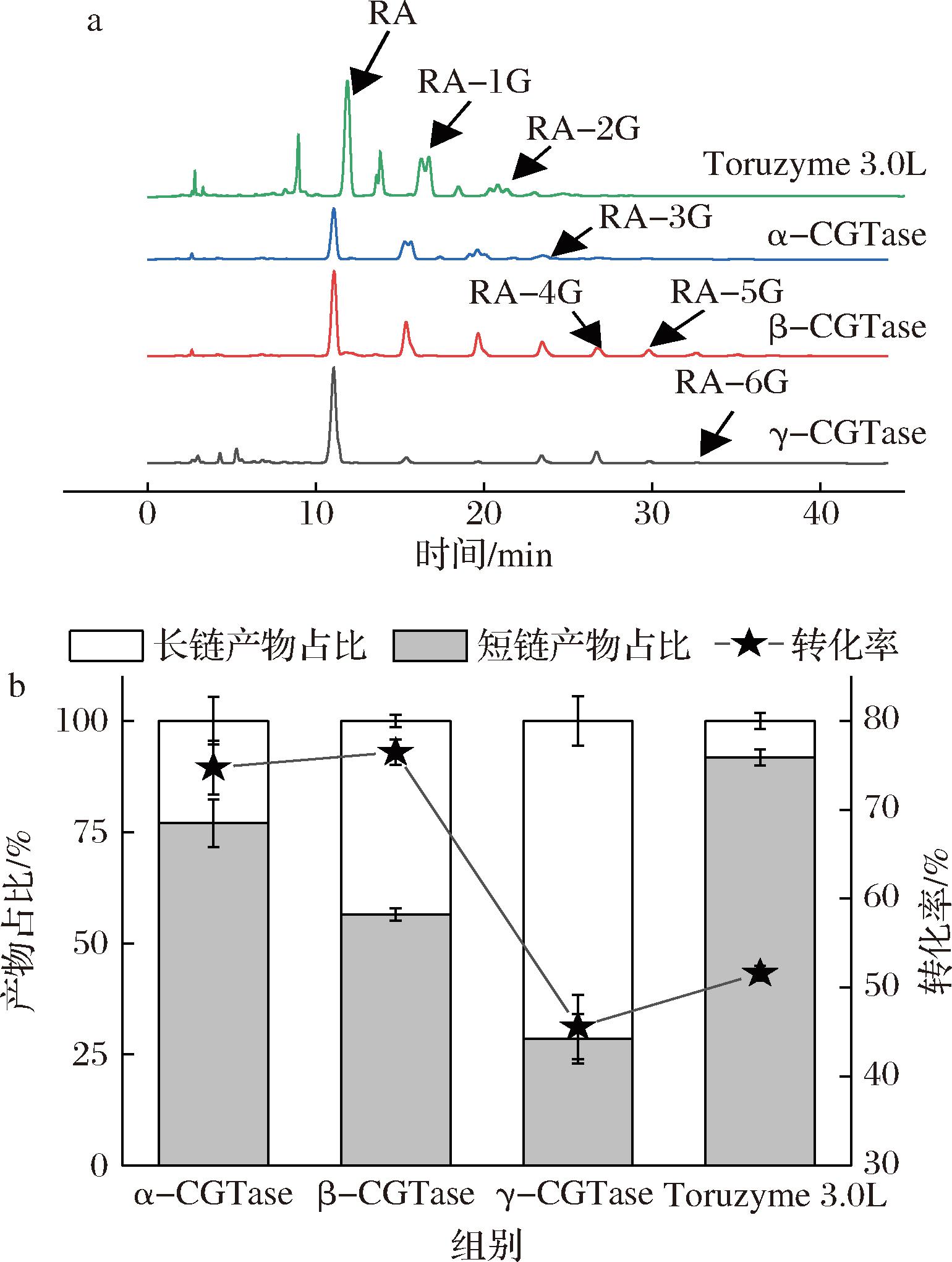
a-反应产物高效液相色谱;b-产物占比及转化率
图2 不同来源的CGTase催化RA糖基化反应
Fig.2 Various CGTases from different sources for RA glycosylation
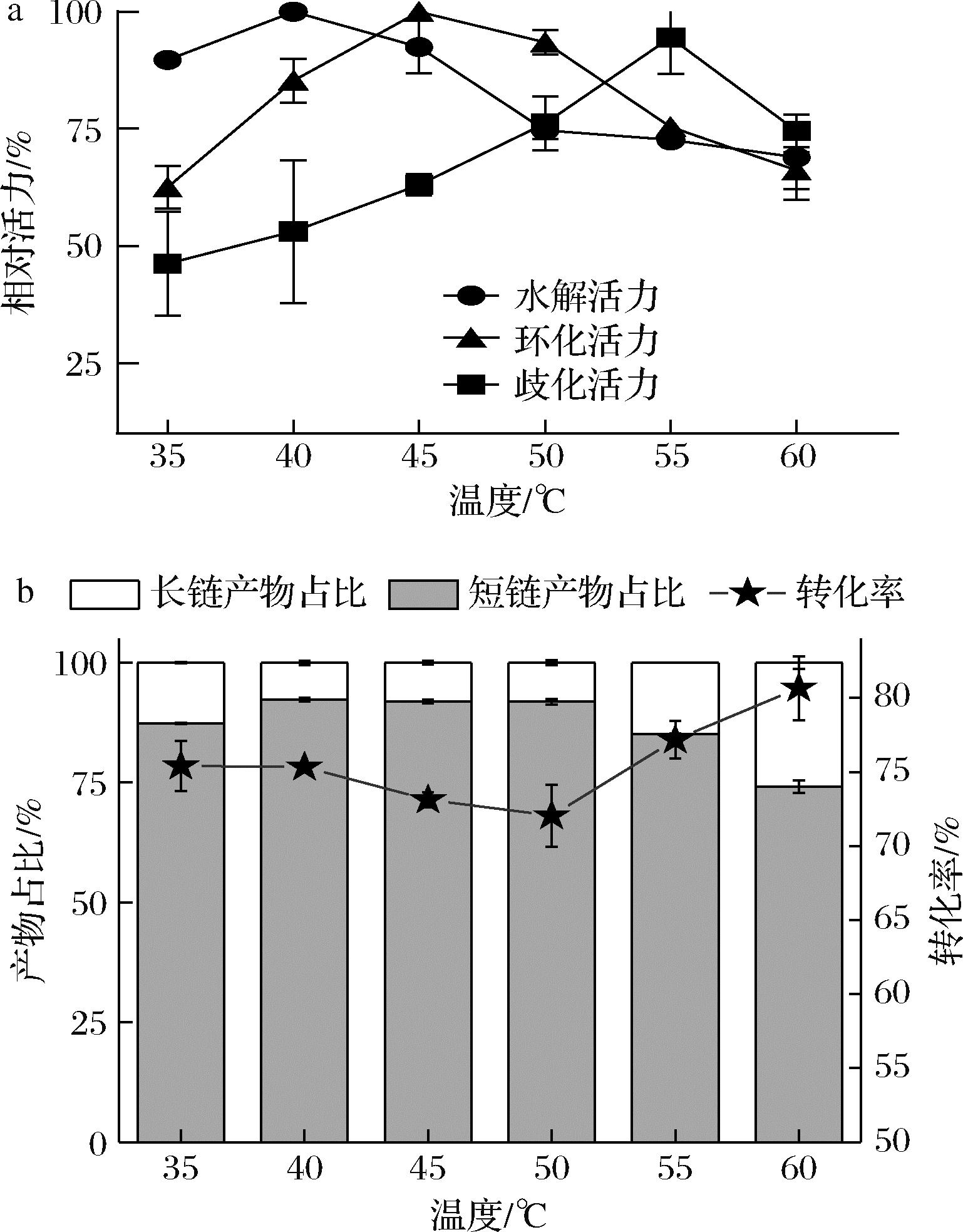
a-温度对α-CGTase活力的影响;b-产物占比及转化率
图3 温度对转糖基化的影响
Fig.3 Effects of temperature on the transglycosylation
注:使用5 mg/mL RA、5 mg/mL水溶性淀粉(1∶1,质量比)和 25 μg/mL α-CGTase在35~60 ℃进行12 h反应。
2.2 温度对转糖基的影响
在不同温度条件下,CGTase的水解活力和歧化活力具有不同表现,因此温度可作为调节反应进行程度的有效方法。如图3-a所示,α-CGTase水解活力最适温度为40 ℃,随着温度继续升高,水解活力急剧下降。环化活力最适温度为45 ℃。歧化活力随着温度升高逐渐上升,55 ℃时达到最大值,温度继续升高歧化活力开始下降。图3-b为反应液中底物RA和各产物所占比率随温度变化,当反应温度低于50 ℃,水解活力发挥较大作用,长链产物被水解为短链产物,使得反应产物中有较多的短链产物。但反应转化率有所降低,原因可能是部分短链产物也被水解为底物。而当反应温度高于50 ℃时,歧化活力发挥主导作用,反应产物的糖基化程度加深,在提高反应转化率的同时,产物中长链糖基化产物的占比增多。综合考虑转化率和短链产物占比,本研究选用40 ℃作为反应温度。
2.3 糖基供体种类对糖基化反应的影响
为了考察糖基供体对产物特异性的影响,本研究选用了不同的糖基供体(麦芽糖、水溶性淀粉、麦芽糊精、α-环糊精和β-环糊精)。如图4所示,相对于长链糖基供体,麦芽糖作为糖基供体能获得更大的短链糖基化产物占比,但反应转化率较低,底物残留较多。而水溶性淀粉等长链糖基供体被利用时具有较高的底物转化率,但长链产物占比也随之增加。水溶性淀粉较其他糖基供体,表现出较高的底物转化率(残留底物相对较少),且生产成本相对α-环糊精和β-环糊精较低,更具有工业化应用潜力。所以,本研究选用水溶性淀粉作为RA糖基化反应的糖基供体。
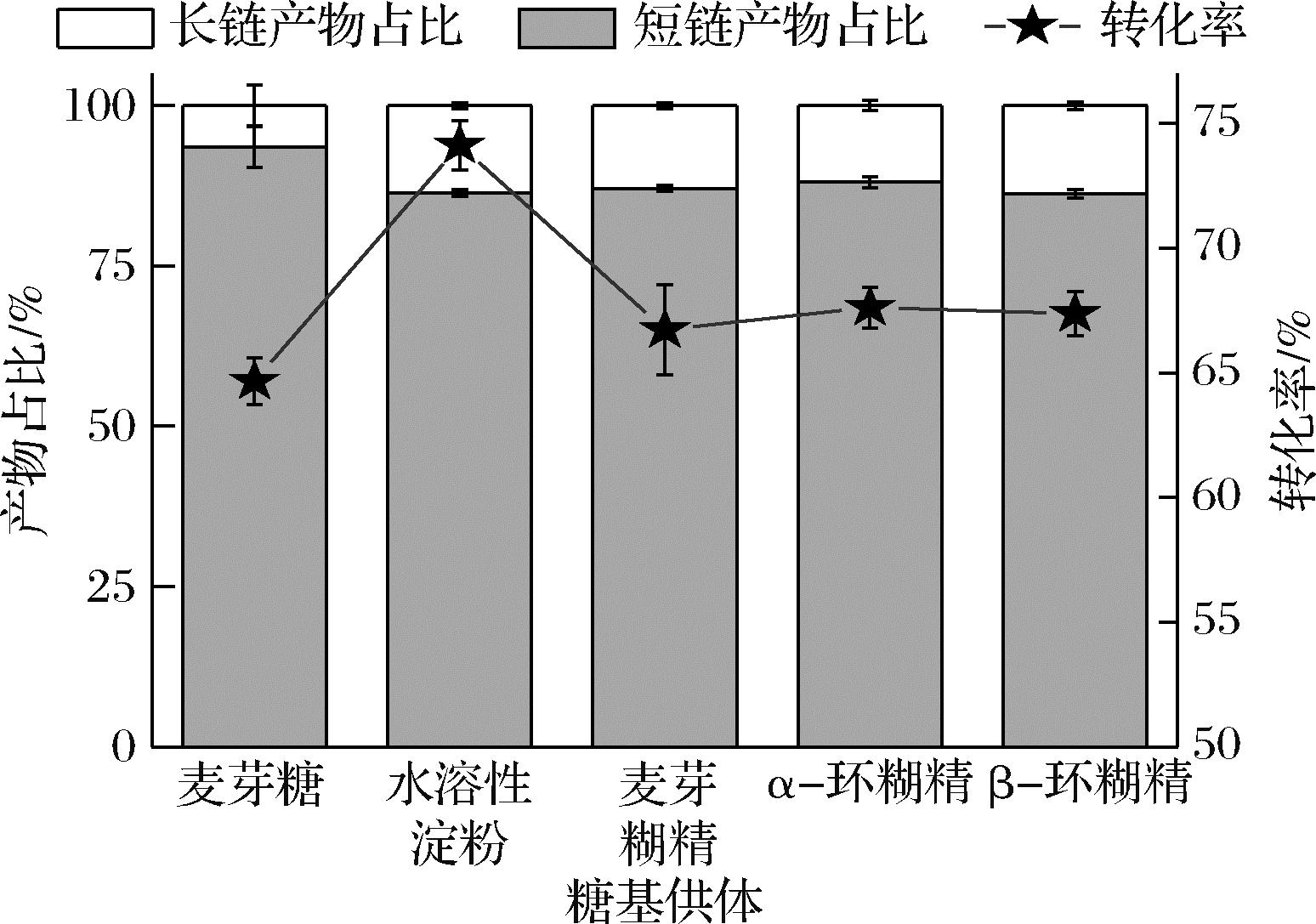
图4 糖基供体对转糖基化的影响
Fig.4 Effects of glycosyl donors on the transglycosylation
注:使用5 mg/mL RA、5 mg/mL糖基供体(1∶1,质量比)和 25 μg/mL α-CGTase在40 ℃反应12 h。
2.4 底物质量比对糖基化反应的影响
底物质量比即RA与糖基供体的质量比。如图5所示,增加反应混合物中水溶性淀粉的比例使长链产物的比例增多。在RA∶水溶性淀粉(质量比)=1∶0.5~1∶1阶段内,增加糖基供体可增加转化率,但同时造成产物糖基化程度加深,增大了长链产物比例。而在底物质量比在1∶1~1∶2阶段时,随着糖基供体的增多,转化率存在下降趋势;而随着糖基供体的进一步增多(1∶2~1∶6.5阶段),长链产物占比提高的同时底物转化率增高。造成这一现象的原因可能是由于增加糖基供体会促进RA的糖基化,有利于转化率的提升。但是,随着水溶性淀粉比例的增加,更有利于长链糖基化产物的生成,导致口感下降。因此,本研究选用RA∶水溶性淀粉质量比为1∶1。LI等[24]曾用玉米淀粉作为糖基供体,与RA最适质量比也为1∶1,与本研究结果一致。

图5 水溶性淀粉与RA底物质量比对转糖基化的影响
Fig.5 Effects of substrates mass ratio of cornstarch to RA/soluble starch on the transglycosylation
注:使用5 mg/mL RA和25 μg/mL α-CGTase在40 ℃反应12 h。
2.5 pH对糖基化反应的影响
不同的pH环境下CGTase的4种不同催化作用(环化、歧化、偶合、水解)表现出不同的活力。我们曾经的研究显示,在pH 5.0~8.0范围内,CGTase的活力均随pH升高而降低,在pH=5.0时,具有最高活力,在pH 6.0~7.0附近,水解活力相对于歧化活力有更好的表现,在pH 8.0附近水解活力有较大损失[25]。如图6所示,在pH 5.0~7.0,α-CGTase催化RA糖基化的转化率变化不大,基本上维持在75%左右,且短链产物占比也均在80%以上。当pH由7.5上升到8.0时,转化率由75%迅速上升到82%,但是短链产物占比较弱酸性环境相对较低,维持在70%左右。其原因可能是由于在弱酸性环境下,水解活力作用较强,底物转化率被抑制。但有利于短链产物生成,尤其是在pH 6.0时,短链产物占比最高,达到将近87%。但在弱碱性环境下,歧化活力增强但水解活力渐弱,底物转化率增高,长链产物占比增多。此外,根据CGTase催化机理,Glu257(pI=3.2)的酸/碱催化作用和Asp229(pI=3.0)的亲核催化作用,酸性环境比碱性环境更有利于催化反应进行[24]。因此,本研究选用反应初始pH为6.0。
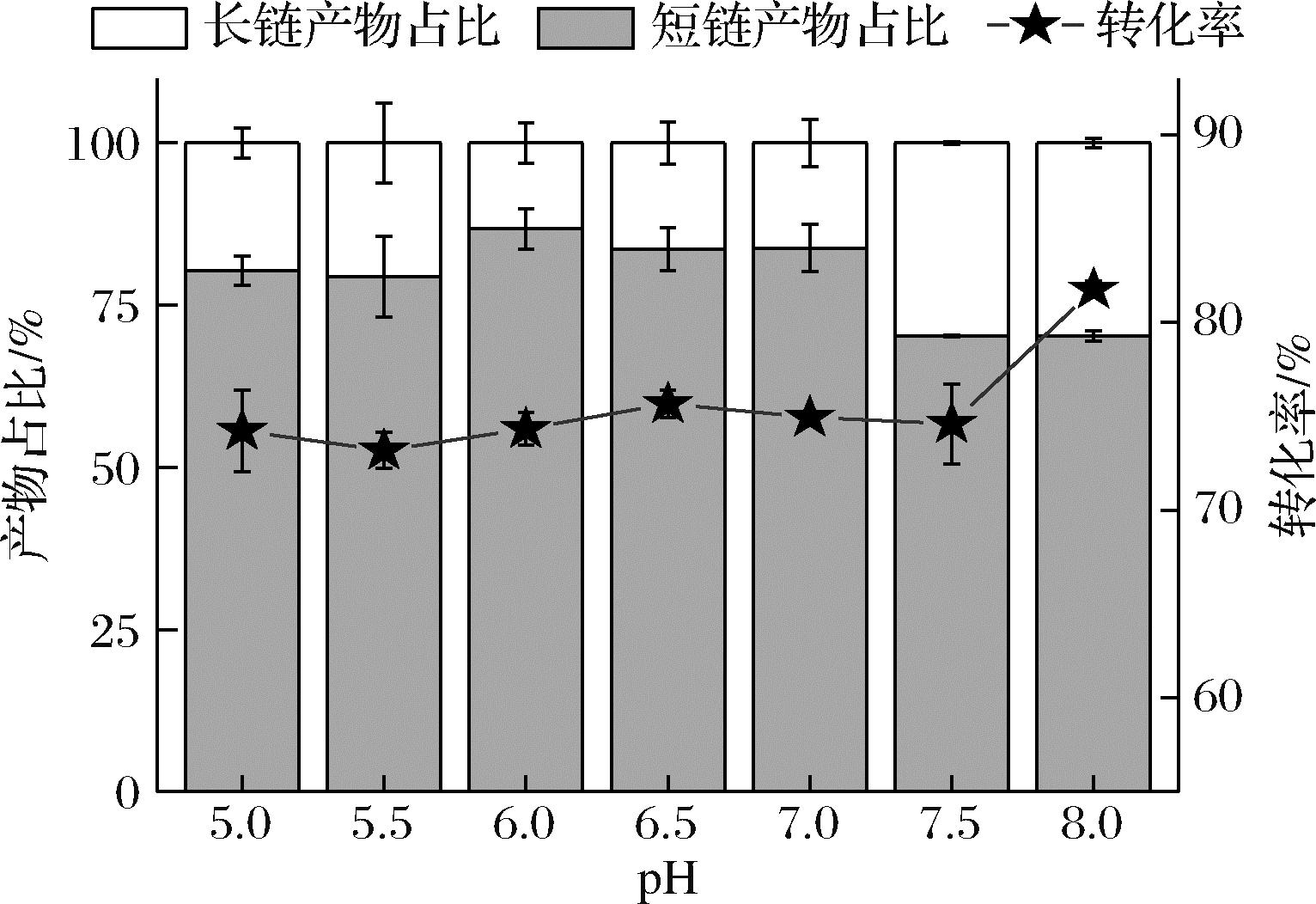
图6 pH对转糖基化的影响
Fig.6 Effects of pH on the transglycosylation
注:使用5 mg/mL RA、5 mg/mL水溶性淀粉(1∶1,质量比)和 25 μg/mL α-CGTase在40 ℃反应12 h,用PBS获得pH 6~8。
2.6 加酶量对糖基化反应的影响
加酶量对CGTase糖基化反应具有一定的影响。如图7所示,在2.5 μg/mL的纯酶质量浓度下,该反应具有最高的转化率(84%)。而随着酶浓度的提升,底物转化率呈下降趋势,短链产物比例逐渐增高,而长链产物比例逐渐减少。说明随着酶量的增加,其水解活力也逐渐提升,更有利于长链产物水解生成短链产物。由于水解作用增加也同时会将部分短链产物水解为底物RA,因此转化率反而随着酶浓度增加而急剧下降。所以,高的加酶量虽然有助于短链糖基化产物比例的提升,但是并不利于RA的转化率。因此,本研究选用同时具有相对较高的短链产物特异性(>82%)和底物转化率(>75%)的纯酶质量浓度25 μg/mL作为最适加酶量。

图7 酶加量对转糖基化的影响
Fig.7 Effects of enzyme loading on the transglycosylation
注:使用5 mg/mL RA和5 mg/mL水溶性淀粉(1∶1,质量比) 在40 ℃反应12 h。
2.7 糖基化反应的时间进程
前期我们曾报道过CGTase糖基化反应机制[25],首先通过歧化作用将长链糖基转化至受体上,然后通过水解作用将长链产物水解为短链产物。本研究中通过对反应时间进行监控(图8),在前1 h内,残留的底物RA和一糖基产物(RA-1G)相对较少。随着反应时间的延长,RA和RA-1G逐渐提高,而长链糖基化产物RA-nG(n≥2)逐渐减少。说明在前1 h内,CGTase已通过转糖基活力将大部分RA转化为其糖基化产物,且长链糖基化产物较多。而随着时间的延长,CGTase通过其水解活力将长链糖基化产物的葡萄糖基逐渐水解,导致一糖基产物(RA-1G)和底物RA逐渐增多,而长链糖基化产物逐渐减少。此结果跟我们前期报道的CGTase糖基化反应机制相一致,为该理论机制提供了案例支持。
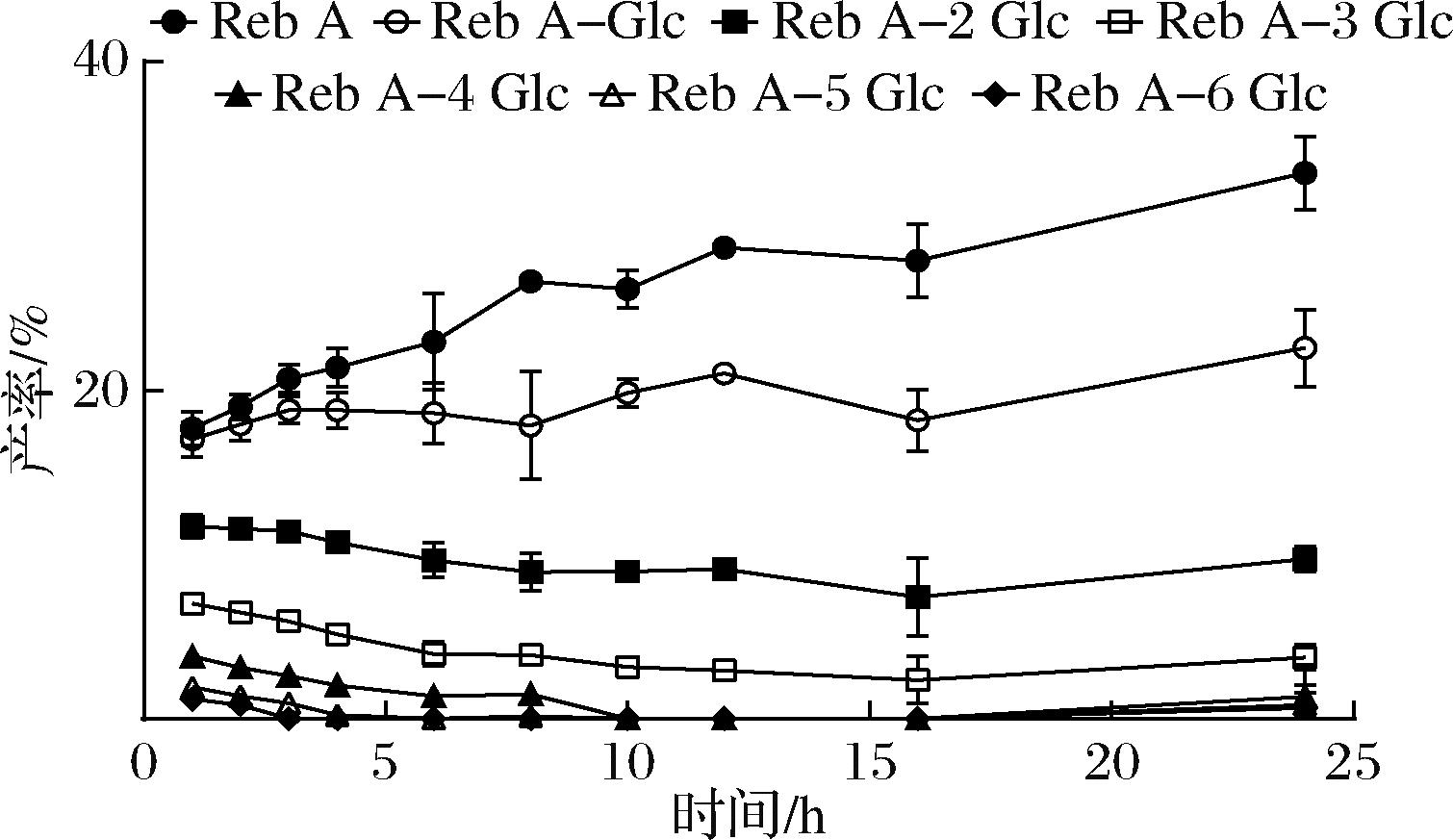
图8 反应时间对转糖基化的影响
Fig.8 Effects of reaction time on the transglycosylation
注:使用5 mg/mL RA、5 mg/mL水溶性淀粉(1∶1,质量比)和 25 μg/mL α-CGTase在40 ℃反应。
近期关于RA转糖基报道中,CGTase-13的突变体Y189F/G255A将短链产物占比由约70%提高至约72%,转化率由62.9%提高到69.6%[15]。本研究通过对α-CGTase反应条件的优化,最终RA转化率维持在74.8%,短链产物占总产物的占比为86.5%。无论从转化率还是短链产物占比,α-CGTase较CGTase-13-Y189F/G255A都有了较大的提升。由于RA转化率和短链产物占比在反应过程中处于此消彼长的状态,因此通过反应条件优化很难将两者同时提高。后续可通过对α-CGTase进行分子改造来进一步提高RA转化率和短链产物占比。
3 结论
环糊精糖基转移酶是一种甜菊糖苷结构修饰的常用酶类,在改善甜菊糖苷口感上发挥着重要的作用。本研究利用一种来源于P.macerans的α-CGTase催化RA的转糖基反应来制备脱苦甜菊糖苷,40 ℃下,底物比为RA/水溶性淀粉=1/1(质量比),加酶量为25 μg/mL,pH 6.0的PBS为反应介质,反应12 h后RA的最终转化率为74.8%,短链产物占总产物的比例为86.5%,较优化前提高了10%,有利于产品的口感和质量。后期研究将进一步对α-环糊精糖基转移酶的结构进行修饰,进一步提高RA转化率和短链产物占比,提升该技术的工业利用度。
[1] GERWIG G J, TE POELE E M, DIJKHUIZEN L, et al.Chapter one Stevia glycosides chemical and enzymatic modifications of their carbohydrate moieties to improve the sweet-tasting quality[J].Advances in Carbohydrate Chemistry and Biochemistry, 2016, 73:1-72.
[2] KASAI R, KANEDA N, TANAKA O, et al.Sweet diterpene-glycosides of leaves of Stevia rebaudiana Bertoni-Synthesis and structure-sweetness relationship of rebaudiosides-A,-D,-E, and their related glycosides[J].Nippon Kagaku Kaishi, 1981(5):726-735.
[3] WANG T C, GUO M Y, SONG X J, et al.Stevioside plays an anti-inflammatory role by regulating the NF-κB and MAPK pathways in S.aureus-infected mouse mammary glands[J].Inflammation, 2014, 37(5):1837-1846.
[4] PHILIPPAERT K, PIRONET A, MESUERE M, et al.Steviol glycosides enhance pancreatic beta-cell function and taste sensation by potentiation of TRPM5 channel activity[J].Nature Communications, 2017, 8:14733.
[5] CEUNEN S, GEUNS J M C.Steviol glycosides:Chemical diversity, metabolism, and function[J].Journal of Natural Products, 2013, 76(6):1201-1228.
[6] TADA A, TAKAHASHI K, ISHIZUKI K, et al.Absolute quantitation of stevioside and rebaudioside A in commercial standards by quantitative NMR[J].Chemical &Pharmaceutical Bulletin, 2013, 61(1):33-38.
[7] DARISE M, MIZUTANI K, KASAI R, et al.Enzymic transglucosylation of rubusoside and the structure-sweetness relationship of steviol-bisglycosides[J].Agricultural and Biological Chemistry, 1984, 48(10):2483-2488.
[8] FUKUNAGA Y, MIYATA T, NAKAYASU N, et al.Enzymic transglucosylation products of stevioside:Separation and sweetness-evaluation[J].Agricultural and Biological Chemistry, 1989, 53(6):1603-1607.
[9] OHTANI K, AIKAWA Y, ISHIKAWA H, et al.Further study on the 1, 4-alpha-transglucosylation of rubusoside, a sweet steviol-bisglucoside from Rubus suavissimus[J].Agricultural and Biological Chemistry, 1991, 55(2):449-453
[10] OHTANI K, AIKAWA Y, FUJISAWA Y, et al.Solubilization of steviolbioside and steviolmonoside with gamma-cyclodextrin and its application to selective syntheses of better sweet glycosides from stevioside and rubusoside[J].Chemical &Pharmaceutical Bulletin, 1991, 39(12):3172-3174.
[11] YANG T, ZHANG J Z, KE D, et al.Hydrophobic recognition allows the glycosyltransferase UGT76G1 to catalyze its substrate in two orientations[J].Nature Communications, 2019, 10(1):3214.
[12] ZHANG S S, LIU Q, LYU C C, et al.Characterizing glycosyltransferases by a combination of sequencing platforms applied to the leaf tissues of Stevia rebaudiana[J].BMC Genomics, 2020, 21(1):794.
[13] JAITAK V, KAUL V K, BANDNA, et al.Simple and efficient enzymatic transglycosylation of stevioside by β-cyclodextrin glucanotransferase from Bacillus firmus[J].Biotechnology Letters, 2009, 31(9):1415-1420.
[14] ZHANG R Q, TANG R Q, BI J H, et al.Efficient bioconversion of stevioside and rebaudioside A to glucosylated steviol glycosides using an Alkalihalobacillus oshimesis-derived cyclodextrin glucanotransferase[J].Molecules, 2023, 28(3):1245.
[15] ZHANG R Q, TANG R Q, WANG W, et al.Engineering of cyclodextrin glycosyltransferase improves the conversion efficiency of rebaudioside A to glucosylated steviol glycosides and increases the content of short-chain glycosylated steviol glycoside[J].Microbial Cell Factories, 2023, 22(1):113.
[16] WANG L, DUAN X G, WU J.Enhancing the α-cyclodextrin specificity of cyclodextrin glycosyltransferase from Paenibacillus macerans by mutagenesis masking subsite-7[J].Applied and Environmental Microbiology, 2016, 82(8):2247-2255.
[17] COSTA H, DEL CANTO S, FERRAROTTI S, et al.Structure-function relationship in cyclodextrin glycosyltransferase from Bacillus circulans DF 9R[J].Carbohydrate Research, 2009, 344(1):74-79.
[18] ABELIAN V A, BALAIAN A M, KOCHIKIAN V T, et al.Transglycosylation of stevioside by cyclodextrin glucanotransferases of various group of microorganisms[J].Prikladnaia Biokhimiia i Mikrobiologiia, 2004, 40(2):153-158.
[19] GUO Q B, ZHANG T T, WANG N F, et al.RQ3, A natural rebaudioside D isomer, was obtained from glucosylation of rebaudioside A catalyzed by the CGTase toruzyme 3.0 L[J].Journal of Agricultural and Food Chemistry, 2019, 67(28):8020-8028.
[20] TIAN X Y, ZHONG F, XIA Y X.Dynamic characteristics of sweetness and bitterness and their correlation with chemical structures for six steviol glycosides[J].Food Research International, 2022, 151:110848.
[21] LEJEUNE A, SAKAGUCHI K, IMANAKA T.A spectrophotometric assay for the cyclization activity of cyclomaltohexaose (α-cyclodextrin) glucanotransferase[J].Analytical Biochemistry, 1989, 181(1):6-11.
[22] VAN DER VEEN B A, VAN ALEBEEK G J, UITDEHAAG J C, et al.The three transglycosylation reactions catalyzed by cyclodextrin glycosyltransferase from Bacillus circulans (strain 251) proceed via different kinetic mechanisms[J].European Journal of Biochemistry, 2000, 267(3):658-665.
[23] KONG D M, WANG L, SU L Q, et al.Effect of Leu277 on disproportionation and hydrolysis activity in Bacillus stearothermophilus NO2 cyclodextrin glucosyltransferase[J].Applied and Environmental Microbiology, 2021, 87(12):e0315120.
[24] LI S, LI W, XIAO Q Y, et al.Transglycosylation of stevioside to improve the edulcorant quality by lower substitution using cornstarch hydrolyzate and CGTase[J].Food Chemistry, 2013, 138(2-3):2064-2069.
[25] HAN R Z, NI J, ZHOU J Y, et al.Engineering of cyclodextrin glycosyltransferase reveals pH-regulated mechanism of enhanced long-chain glycosylated sophoricoside specificity[J].Applied and Environmental Microbiology, 2020, 86(7):e00004-20.