罗汉果(Siraitia grosvenorii)又名拉汉果,罗晃子,金不换等,是一种葫芦科多年生藤本植物的果实,主要分布在我国广西[1]。罗汉果素有“东方神果”的美誉,有降糖护肝、免疫调控、防癌抑癌及抗炎的功效。其中,罗汉果的抗炎作用被认为是其传统功效和拓展功能的活性基础[2]。罗汉果是典型的中药材植物资源,富含罗汉果皂苷、多糖类、黄酮类等药用成分及矿物质元素、氨基酸等营养物质[3]。研究表明,罗汉果皂苷作为罗汉果果实中最具代表性的三萜成分,除甜味剂应用外,在小鼠急性肺损伤、结肠炎以及高脂饮食诱发的慢性炎症等病症中都有较好的疗效[4-7]。罗汉果富含的黄酮类内源成分,能够缓解慢性睡眠剥夺小鼠的氧化应激损伤及炎症反应[8]。多糖是罗汉果果实中含量较高的成分之一,GONG等[9]提取分离的罗汉果多糖在糖尿病肾病小鼠模型中亦表现出良好的抗炎和抗氧化效果。作为药食同源资源,罗汉果提取物及其组分兼具药品与食品属性,应用于功效产品中,既能发挥代糖作用,又能提高保健价值。
成熟罗汉果采收后常温存储期短,通常需要干制,而干燥工艺易引起各类化学成分的变化,进而导致生物活性的差异。如多糖和挥发油类成分易受高温影响,黄酮类成分适宜低温烘干,皂苷类成分应根据不同成分需求选择干燥方式[10]。因此,本文采用冷冻干燥、微波干燥和不同温度鼓风干燥方式对罗汉果成熟果实进行干制处理,并对其甲醇提取物中的总糖、总黄酮、总皂苷及皂苷类物质(罗汉果苷V,11-氧化-罗汉果苷V,赛门苷I,罗汉果苷IV、IIIE和IIE)进行检测,旨在寻找罗汉果功能成分变化的规律与抗炎作用的相关性。通过采用脂多糖(Lipopolysaccharide, LPS)诱导的小鼠单核巨噬细胞白血病细胞RAW 264.7炎症模型评价罗汉果不同干制样品的抗炎活性,对比4种干燥方式对抗炎活性的影响,为罗汉果资源的开发与利用提供参考依据。
1 材料与方法
1.1 试验材料与细胞
罗汉果采自广西壮族自治区桂林市,经卢凤来副研究员鉴定为葫芦科罗汉果属植物罗汉果Siraitia grosvenorii。RAW 264.7细胞购于中国典型培养物保藏中心细胞库。
微波干燥罗汉果,桂林市美福浓食品有限公司;山奈苷(纯度≥98%),上海源叶生物科技有限公司;D(+)-无水葡萄糖(纯度≥98%),成都曼斯特生物科技有限公司;罗汉果苷V(纯度≥98%),成都乐美天医药;11-氧化-罗汉果苷V、赛门苷I、罗汉果苷V、IV、IIIE和IIE(自制,纯度≥98%),广西植物研究所天然产物化学研究中心实验室;CCK-8检测试剂盒,百赛生物公司;TNF-α、IL-6检测试剂盒,Elabscience公司;NO检测试剂盒,上海碧云天生物技术有限公司;活性氧(reactive oxygen species,ROS)试剂盒,北京索莱宝科技有限公司。其他试剂均为分析纯级别。
1.2 仪器与设备
FDU-2110冷冻干燥机,东京理化有限公司;DHG-9240A电热鼓风干燥箱,上海一恒科学仪器有限公司;LC-2030C液相色谱仪,日本岛津公司;T6新世纪紫外可见分光光度计,北京普析通用仪器有限责任公司;SP-Max 3500FL Spark酶标仪,瑞士Tecan公司;BSP-150生化培养箱,上海博讯医疗生物仪器股份有限公司;Model-311 5% CO2细胞培养箱,赛默飞Thermo公司。
1.3 实验方法
1.3.1 含量检测
1.3.1.1 样品的制备
采收的成熟罗汉果分别于实验室进行冷冻干燥、鼓风70 ℃(72 h)和100 ℃(24 h)完全干燥,与采购的微波干燥果对应标记为冷冻干燥、微波、70 ℃、100 ℃样品。同时,100 ℃恒温下分别进行5、10、15 h的干燥,并将各时间段的样品冷冻干燥至恒重,分别标记为100 ℃ 5 h、100 ℃ 10 h和100 ℃ 15 h。所有样品打成粉末。准确称取待测样品粉末各100 mg,加入10 mL体积分数为50%的甲醇溶液,密塞,称定质量;超声(功率240 W,频率50 kHz)提取1 h,放冷,再称定质量,50%(体积分数)甲醇补足失重,摇匀,4 000 r/min离心10 min,上清液即为待测样品溶液,置于4 ℃冰箱备用。
1.3.1.2 总糖、总黄酮和总皂苷含量测定
总糖含量采用苯酚-硫酸法[11]。以葡萄糖浓度为横坐标,吸光度为纵坐标建立标准曲线,得到回归方程Y=13.45X+0.000 8(R2=0.999 8)。通过标准曲线计算总糖的含量。
总黄酮含量采用硝酸铝比色法[12]。以山奈苷的浓度和吸光度为横坐标和纵坐标绘制标准曲线。其线性方程为Y=18.233X+0.001(R2=0.999 9)。通过标准曲线计算总黄酮的含量。
总皂苷采用香草醛-高氯酸显色反应[13]。以罗汉果苷V含量为横坐标,以其吸光度值为纵坐标,得到回归方程Y=11.14X+0.001 7(R2=0.999 5)。通过标准曲线计算总皂苷的含量。
1.3.1.3 高效液相色谱分析
上述罗汉果干燥样品溶液各取2 mL通过12 000 r/min离心10 min取上清液进行HPLC分析。色谱柱:ZORBAX SB-C18(4.6 mm×250 mm,5 μm);洗脱剂:纯水(A)和乙腈(B);检测波长203 nm;流速0.8 mL/min;柱温35 ℃;进样量10 μL。其中,洗脱梯度为:0~8 min,3%~13.5% B;8~35 min,13.5%~35% B;35~40 min,35%~3% B。
标准品溶液制备和测定:分别精确称取11-氧化-罗汉果皂苷V、罗汉果皂苷V、IV、IIIE、IIE和赛门苷I标准品,用色谱甲醇溶解稀释至刻度,摇匀,罗汉果皂苷V、IV和赛门苷I配制成0.2 mg/mL,11-氧化-罗汉果皂苷V与罗汉果苷IIIE配制成0.01 mg/mL的标准品溶液,罗汉果苷IIE配制成0.001 mg/mL的标准品溶液。11-氧化-罗汉果皂苷V与罗汉果苷IIIE、IIE以5、10、20、30和40 μL,其他标准品溶液以5、10、15、20和25 μL注入高效液相色谱仪。以峰面积(Y)对其进样量(X)进行线性回归,并根据标准曲线方程进行该物质的定量定性分析。其各种标准品的回归方程分别为:11-氧化-罗汉果苷V,Y=809 014 226.77X-338.85(R2=0.999 9);罗汉果苷V,Y=237 389 341.143 2X+6 107.9(R2=1.000 0);赛门苷I,Y=268 530 090.05X+5 689.53(R2=1.000 0);罗汉果皂苷IV,Y=270 875 007.95X+9 740.33(R2=1.000 0);罗汉果皂苷IIIE,Y=334 940 192.51X+57.62(R2=0.999 9);罗汉果皂苷IIE,Y=7 111 726.29X-41.49(R2=0.999 8)。
1.3.2 抗炎活性
1.3.2.1 罗汉果提取物制备
分别称取5 g各待测罗汉果样品粉末,加入25 mL甲醇超声(功率240 W,频率50 kHz)提取1 h后,超滤,经旋转蒸发浓缩后,于防潮柜保存,以供进一步实验。
1.3.2.2 细胞毒评估
将RAW 264.7细胞以2×105细胞/mL密度接种于96孔板内,5% CO2,37 ℃恒温箱中培养至增殖80%左右。设置空白组、样品组、背景组。样品组加入不同质量浓度(50、100、200、400、800 μg/mL)待测样品,空白组不加药,背景组无细胞,继续培养24 h。加入10 μL的CCK-8试剂,在37 ℃的恒温箱中继续培养1 h后,酶标仪450 nm检测波长测得各孔吸光度,依据公式(1)计算细胞增殖率。
细胞活力![]()
(1)
式中:OD1、OD2和OD3分别为样品组、空白组和背景组的吸光度值。
1.3.2.3 NO检测
设置空白组、LPS组、样品组和阳性对照组。其中,LPS组加入1 μg/mL LPS溶液,样品组与阳性对照组分别加入不同质量浓度待测样品(50、100、200、400、800 μg/mL)和地塞米松(5、10、20、40和80 μg/mL)预处理1 h后,再加入1 μg/mL LPS溶液。培养箱中继续培养24 h后取上清液,按照试剂盒说明书操作,计算NO含量。
1.3.2.4 酶联免疫吸附剂测定
设置空白组、LPS组和样品组。其中,LPS组加入1 μg/mL LPS溶液,样品组加入终质量浓度200 μg/mL待测样品预处理1 h后,再加入1 μg/mL LPS溶液继续培养24 h,取上清液,采用酶联免疫吸附(ELISA)试剂盒,按照试剂盒说明书操作,检测TNF-α和IL-6水平。
1.3.2.5 ROS检测
细胞培养与1.3.2.4节相同。孵育24 h后,弃上清液,每孔加入100 μL DCFH-DA溶液,37 ℃孵育20 min。用无血清的DMEM洗涤3次,再加入100 μL无血清的DMEM重悬细胞。在488 nm激发波长,525 nm发射波长的荧光酶标仪测量荧光强度。
1.4 统计学分析方法
所有实验重复3次,结果以平均值±标准差表示,使用Excel进行数据基本统计描述,采用GraphPad Prism 9.5软件作图,并对数据进行显著性分析。使用SPSS 22进行相关性分析及主成分分析。
2 结果与分析
2.1 不同干燥方式下罗汉果主要功能成分分析
2.1.1 总糖、总黄酮和总皂苷分析
罗汉果果实主要含有三萜皂苷类、黄酮类、多糖类、蛋白质氨基酸、挥发性成分等多种物质,具有止咳平喘、抗炎抗氧化、抗糖尿病、保肝抗肿瘤等多种生物活性作用[1]。由表1可知,4种干燥方式处理的罗汉果中总糖、总黄酮和总皂苷含量存在显著性差异(P<0.05)。
表1 不同干燥处理对罗汉果主要功能成分的影响
Table 1 Effects of different drying methods on the content of functional components in S. grosvenorii
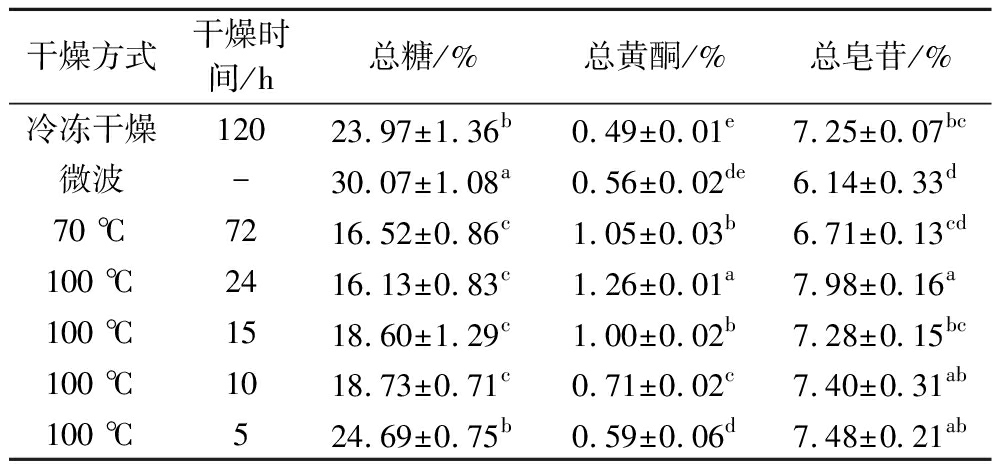
干燥方式干燥时间/h总糖/%总黄酮/%总皂苷/%冷冻干燥12023.97±1.36b0.49±0.01e7.25±0.07bc微波-30.07±1.08a0.56±0.02de6.14±0.33d70 ℃7216.52±0.86c1.05±0.03b6.71±0.13cd100 ℃2416.13±0.83c1.26±0.01a7.98±0.16a100 ℃1518.60±1.29c1.00±0.02b7.28±0.15bc100 ℃1018.73±0.71c0.71±0.02c7.40±0.31ab100 ℃524.69±0.75b0.59±0.06d7.48±0.21ab
注:同列不同小写字母表示差异显著(P<0.05)(下同)。
微波干燥样品总糖含量显著高于冷冻干燥样品(P<0.05),70和100 ℃完全干燥样品中的总糖含量相当(P>0.05),显著低于冷冻干燥样品。恒温100 ℃干制过程中,样品中总糖含量随干燥时间的延长显著下降后趋于稳定,表明微波干燥可提高总糖含量,但鼓风中高温处理会引起总糖的降低。罗汉果富含酸性杂多糖和不同种类的还原性单糖,在干燥过程中,高温促使多糖发生部分降解,而还原糖逐步发生美拉德反应[14],从而引起总糖含量的下降。
与冷冻干燥样品相比,100 ℃完全干燥罗汉果中的总黄酮含量最高(P<0.05),且总黄酮含量随干燥时间的增加而显著升高(P<0.05)。在干制过程中,还原糖的美拉德反应也会生成类黄酮化合物[15],从而引起总黄酮含量的提高。此外,有文献报道,干燥的罗汉果中黄酮的种类与新鲜果实有明显差异[16]。因此,推测干燥过程中黄酮苷的转化也是引起总黄酮含量变化的主要因素。
4种干燥处理的罗汉果总皂苷含量依次为100 ℃完全干燥>冷冻干燥>70 ℃完全干燥>微波干燥,其中冷冻干燥与70 ℃完全干燥、70 ℃完全干燥与微波干燥总皂苷含量差异不显著(P>0.05)。在100 ℃干制过程中,总皂苷的含量相对稳定,受干燥时间的影响较小。与赖文等[17]对不同干燥林下参总皂苷含量无显著性差异的研究结果相一致,说明不同干燥处理对罗汉果总皂苷含量的影响最小。
2.1.2 HPLC分析
罗汉果皂苷是成熟罗汉果果实中特有的甜味成分,在新鲜果实中含量约为1.42%~1.62%[18],具有零热量、高甜度的特点,已作为天然甜味剂应用于食品行业。在化学结构上,罗汉果皂苷属葫芦烷型四环三萜类化合物,以不同糖苷键连接数量不等的葡萄糖基,有镇咳平喘、抗炎、抗氧化,及抗癌等药理作用[4]。研究表明,罗汉果主要皂苷成分如11-氧化-罗汉果皂苷V、罗汉果皂苷V、罗汉果苷IV、赛门苷I、罗汉果苷IIIE和罗汉果苷IIE等表现出良好的抗炎活性[19],因此,本文基于代表性罗汉果皂苷成分探讨了不同干燥处理下皂苷种类与相对含量的变化。标准物质和罗汉果的HPLC图如图1所示。
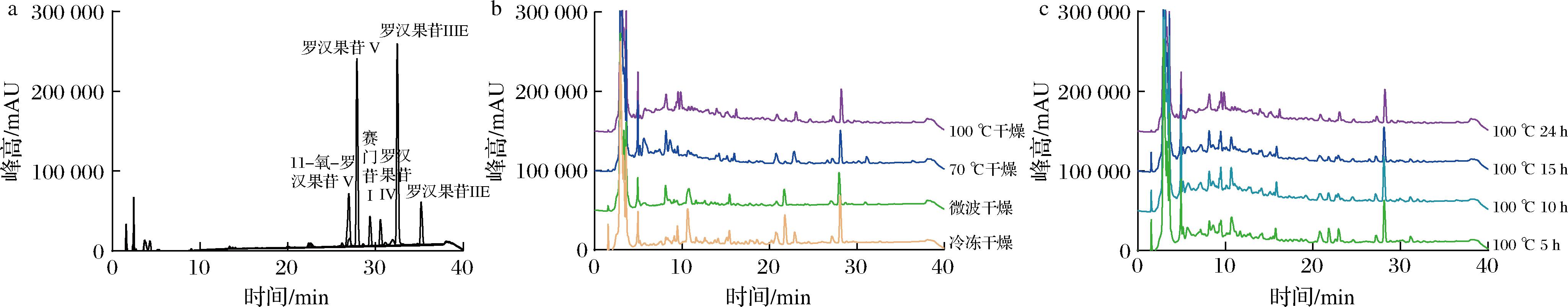
a-对照品;b-干燥方式;c- 100 ℃干燥时间
图1 不同干燥处理的罗汉果样品HPLC图
Fig.1 HPLC spectra of S. grosvenorii by different drying methods
注:203 nm检测的HPLC图。
如表2所示,不同干燥方式引起罗汉果皂苷成分的显著变化(P<0.05);在定量的6个皂苷类化合物中,冷冻干燥的11-氧化-罗汉果苷V和罗汉果苷V含量最高,而100 ℃干燥的罗汉果中含有的低糖苷最多。干燥处理造成罗汉果苷V含量的下降,同时次级苷含量升高。其中,100 ℃干燥样品中的赛门苷I和罗汉果苷IV含量最高,表明罗汉果苷V在干制过程中会发生降解而产生多种次级苷,各类皂苷含量达到一种动态的平衡,从而维持总皂苷含量的基本稳定。有研究表明,罗汉果苷IIIE、IIE具有优异的抗炎效果[20-21]。在本研究中干燥处理后的罗汉果样品中苷IIIE、IIE等次级苷的含量有所增加,可能引起各样品抗炎活性的差异。
表2 不同干燥处理对罗汉果皂苷种类及含量的影响
Table 2 Effects of different drying methods on the species and contents of mogrosides in S. grosvenorii
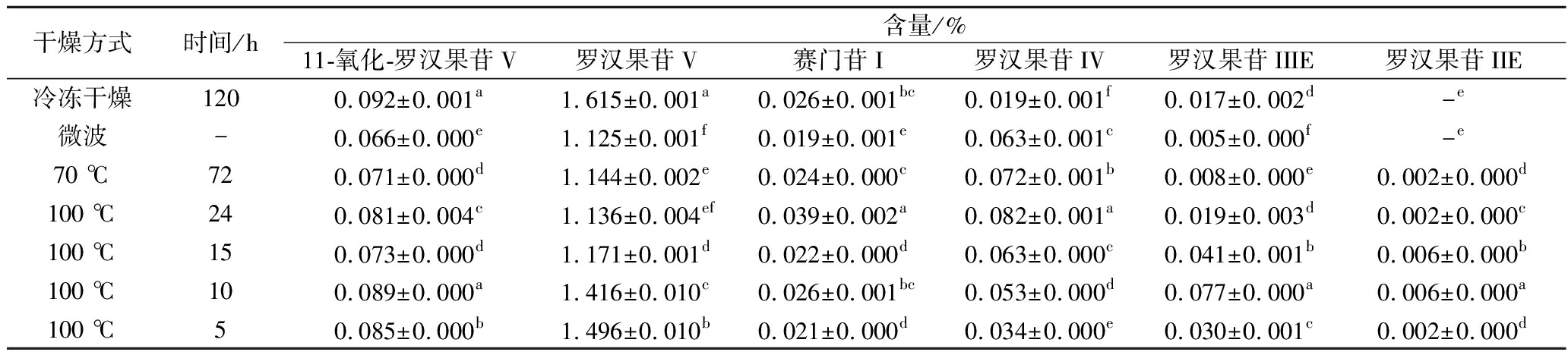
干燥方式时间/h含量/%11-氧化-罗汉果苷V罗汉果苷V赛门苷I罗汉果苷IV罗汉果苷IIIE罗汉果苷IIE冷冻干燥1200.092±0.001a1.615±0.001a0.026±0.001bc0.019±0.001f0.017±0.002d-e微波-0.066±0.000e1.125±0.001f0.019±0.001e0.063±0.001c0.005±0.000f-e70 ℃720.071±0.000d1.144±0.002e0.024±0.000c0.072±0.001b0.008±0.000e0.002±0.000d100 ℃240.081±0.004c1.136±0.004ef0.039±0.002a0.082±0.001a0.019±0.003d0.002±0.000c100 ℃150.073±0.000d1.171±0.001d0.022±0.000d0.063±0.000c0.041±0.001b0.006±0.000b100 ℃100.089±0.000a1.416±0.010c0.026±0.001bc0.053±0.000d0.077±0.000a0.006±0.000a100 ℃50.085±0.000b1.496±0.010b0.021±0.000d0.034±0.000e0.030±0.001c0.002±0.000d
2.2 化学模式识别
2.2.1 聚类分析
采用SPSS 22软件用组间联接法、平方欧氏距离为度量标准对不同干燥处理的罗汉果6种皂苷成分含量进行系统聚类分析。结果表明,平方欧氏距离为25时,不同干燥处理的罗汉果可聚为2类,其中冷冻干燥、100 ℃干燥5 h、100 ℃干燥10 h为一类;微波干燥、70、100 ℃干燥15 h、100 ℃完全干燥为一类。聚类分析树状图如图2所示。
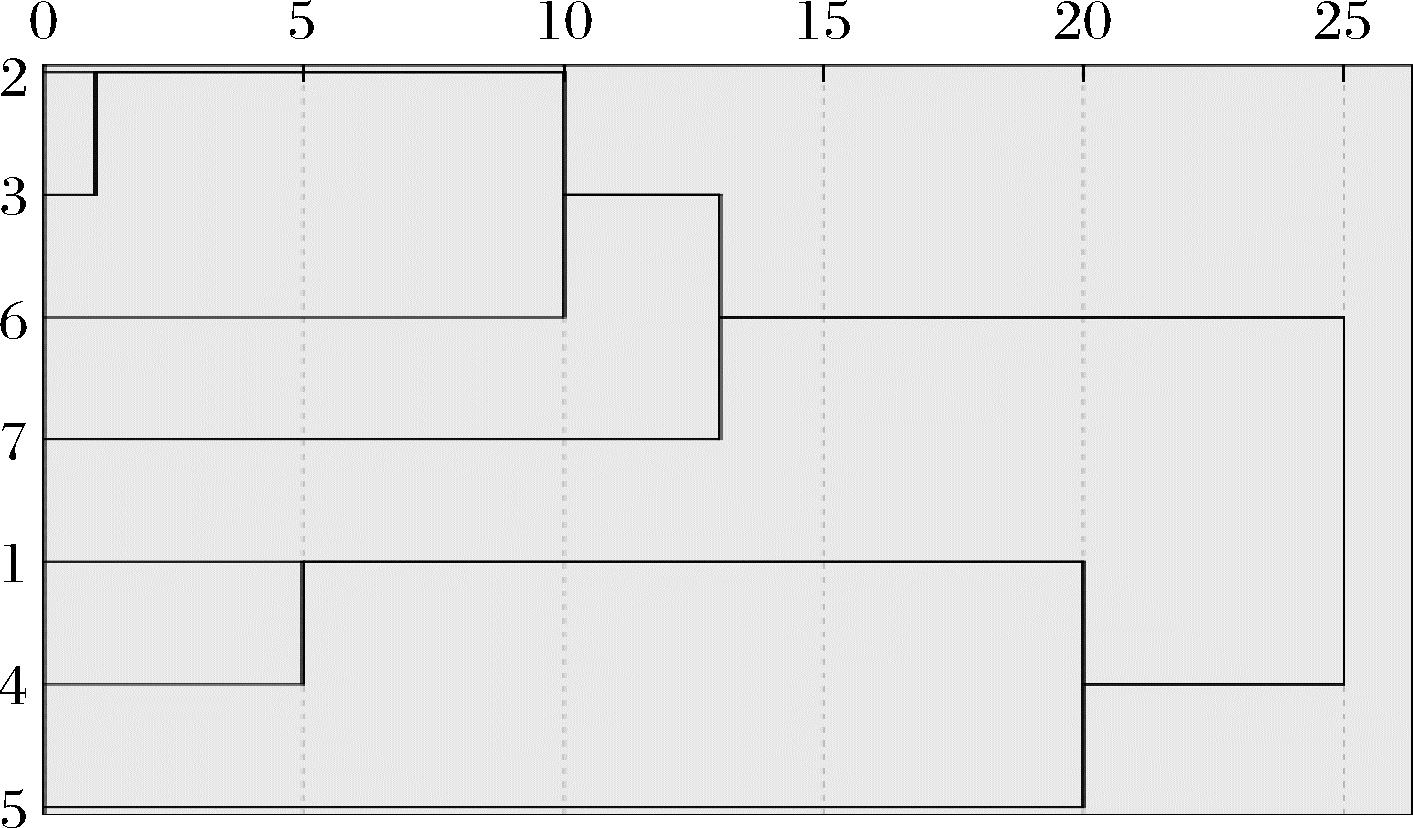
图2 罗汉果聚类分析树状图
Fig.2 Tree diagram of cluster analysis of S. grosvenorii
注:1-冷冻干燥;2-微波干燥;3-70 ℃干燥;4-100 ℃ 5 h; 5-100 ℃ 10 h;6-100 ℃ 15 h;7-100 ℃ 24 h。
2.2.2 主成分分析(principal component analysis,PCA)
为了进一步研究不同干燥处理的罗汉果化学成分的差异,通过皂苷成分含量构建PCA模型,采用降维分析中的因子分析法,将特征值大于1设置为提取标准,结果Bartlett球形检验显著性值P<0.05,说明拒绝变量相互独立的假设,即主成分分析成立。在PCA得分图中共提取3个主成分,累计方差贡献率为96.82%,即表明该3个主成分可以解释原有变量96.82%的信息。因此可用该3个主成分代替指纹图谱6个共有峰来评价罗汉果药材,特征值及贡献率如表3所示。
表3 主成分特征值、方差贡献率及累计方差贡献率
Table 3 Principal component eigenvalues, variance contribution rate, and cumulative variance contribution rate
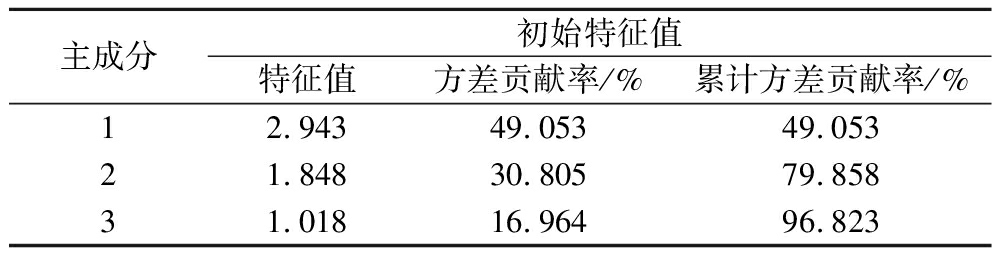
主成分初始特征值特征值方差贡献率/%累计方差贡献率/%12.94349.05349.05321.84830.80579.85831.01816.96496.823
选用3个主成分因子对不同干燥处理的罗汉果进行综合评价,以方差贡献率为分配系数,计算各批次罗汉果的主成分因子得分及综合得分,并对综合得分进行排序。根据矩阵系数可得到3个主成分的得分函数表达式,分别为Y1、Y2和Y3。由得分系数矩阵表4可知,5个变量与主成分Y1呈现正相关性,其中以11-氧化-罗汉果苷V和罗汉果苷V贡献率最大;4个变量均与主成分Y2呈正相关性,其中以罗汉果苷IIIE和罗汉果苷IIE贡献率最大;3个变量与主成分Y3呈现正相关性,其中以赛门苷I和罗汉果苷IV贡献率最大。对上述主成分的载荷值进行计算,得各主成分的线性模型。
Y1=0.553X1+0.555X2+0.238X3-0.474X4+0.312X5+0.085X6;
Y2=0.000X1-0.174X2-0.132X3+0.261X4+0.610X5+0.716X6;
Y3=0.181X1-0.186X2+0.874X3+0.409X4-0.037X5-0.001X6;
Y=0.507Y1+0.318Y2+0.175Y3;
表4 成分得分系数矩阵
Table 4 Component score coefficient matrix
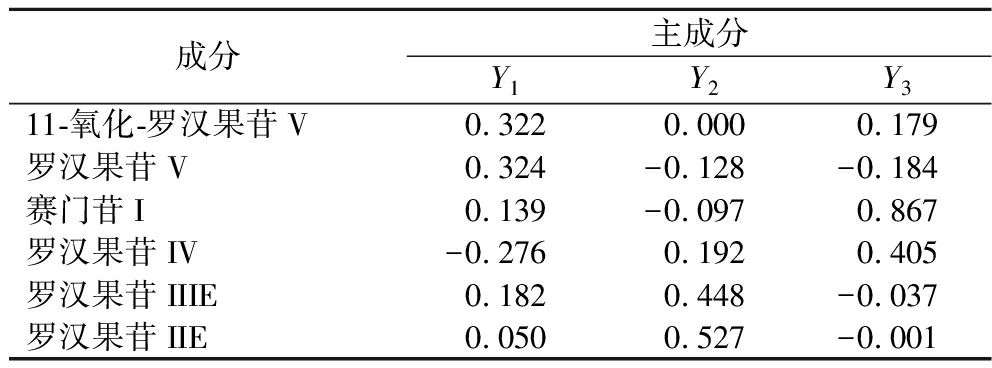
成分主成分Y1Y2Y311-氧化-罗汉果苷V0.3220.0000.179罗汉果苷V0.324-0.128-0.184赛门苷I0.139-0.0970.867罗汉果苷IV-0.2760.1920.405罗汉果苷IIIE0.1820.448-0.037罗汉果苷IIE0.0500.527-0.001
其中Y1、Y2和Y3分别为主成分1、2和3的得分情况,X1、X2、X3、X4、X5、X6分别为标准化后的11-氧化-罗汉果苷V、罗汉果苷V、赛门苷I、罗汉果苷IV、罗汉果苷IIIE和罗汉果苷IIE含量。将样品数值代入计算模型,最后得出各样品的综合效果,如表5所示,即100 ℃ 10 h>100 ℃ 5 h>冷冻干燥>100 ℃ 15 h>100 ℃>70 ℃>微波干燥。排序顺序提示该干燥处理下的罗汉果皂苷成分与其在100 ℃ 10 h果实中接近程度。
表5 不同干燥处理罗汉果的主成分评分、综合评分和排名
Table 5 Principal component score and ranking of S. grosvenorii at different drying methods
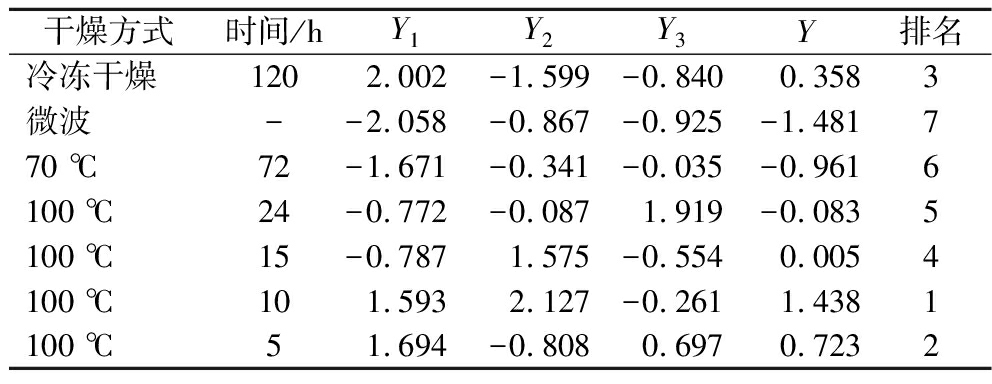
干燥方式时间/hY1Y2Y3Y排名冷冻干燥1202.002-1.599-0.840 0.3583微波--2.058 -0.867-0.925-1.481770 ℃72-1.671-0.341-0.035-0.9616100 ℃24-0.772-0.0871.919-0.0835100 ℃15-0.7871.575-0.5540.0054100 ℃101.593 2.127-0.2611.4381100 ℃51.694-0.8080.6970.7232
2.3 不同干燥方式对罗汉果抗炎活性的影响
2.3.1 不同干燥样品的NO生成抑制活性
LPS可诱导巨噬细胞产生多种炎症细胞因子和炎症介质,进而引发机体内一系列的炎症反应[22]。在LPS诱导RAW 264.7细胞炎症模型中,NO作为炎症介质之一,过量的NO会与超氧阴离子发生反应产生过氧化亚硝酸盐,从而导致局部组织损伤促进炎症的发生,因此,NO生成抑制活性是评估抗炎潜力最简单有效的方法[23]。
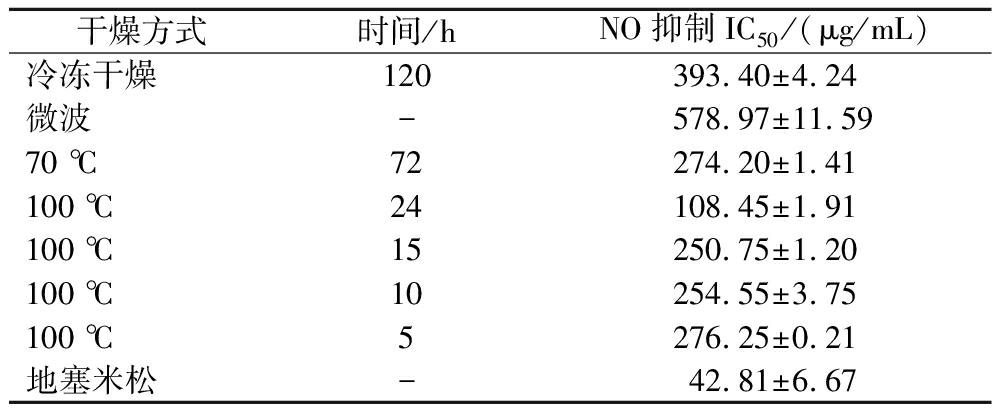
首先,CCK-8法检测了不同罗汉果样品对RAW 264.7细胞活力的影响。如图3所示,各样品在50~800 μg/mL对RAW 264.7细胞无毒性,且呈浓度依赖性促进细胞的增殖。由表6可知,不同干制罗汉果样品对RAW 264.7细胞NO生成抑制活性显著不同。冷冻干燥、微波、鼓风70 ℃、100 ℃样品与地塞米松NO抑制IC50分别为(393.40±4.24)、(578.97±11.59)、(274.20±1.41)、(108.45±1.91)和(42.81±6.67) μg/mL,表明随着干燥温度的升高,罗汉果样品体外抗炎活性显著增强。进一步测定了100 ℃干燥过程中各样品对NO生成的抑制能力,发现干燥时间影响罗汉果提取物的抗炎活性。同时,在恒温干制过程中,干燥时间的延长增强了罗汉果提取物对NO生成的抑制活性。这可能与100 ℃样品中增加的低糖苷有关,研究发现,罗汉果苷IIE能抵御胰腺炎以及罗汉果苷IIIE可以减轻高糖诱导的炎症[20]。
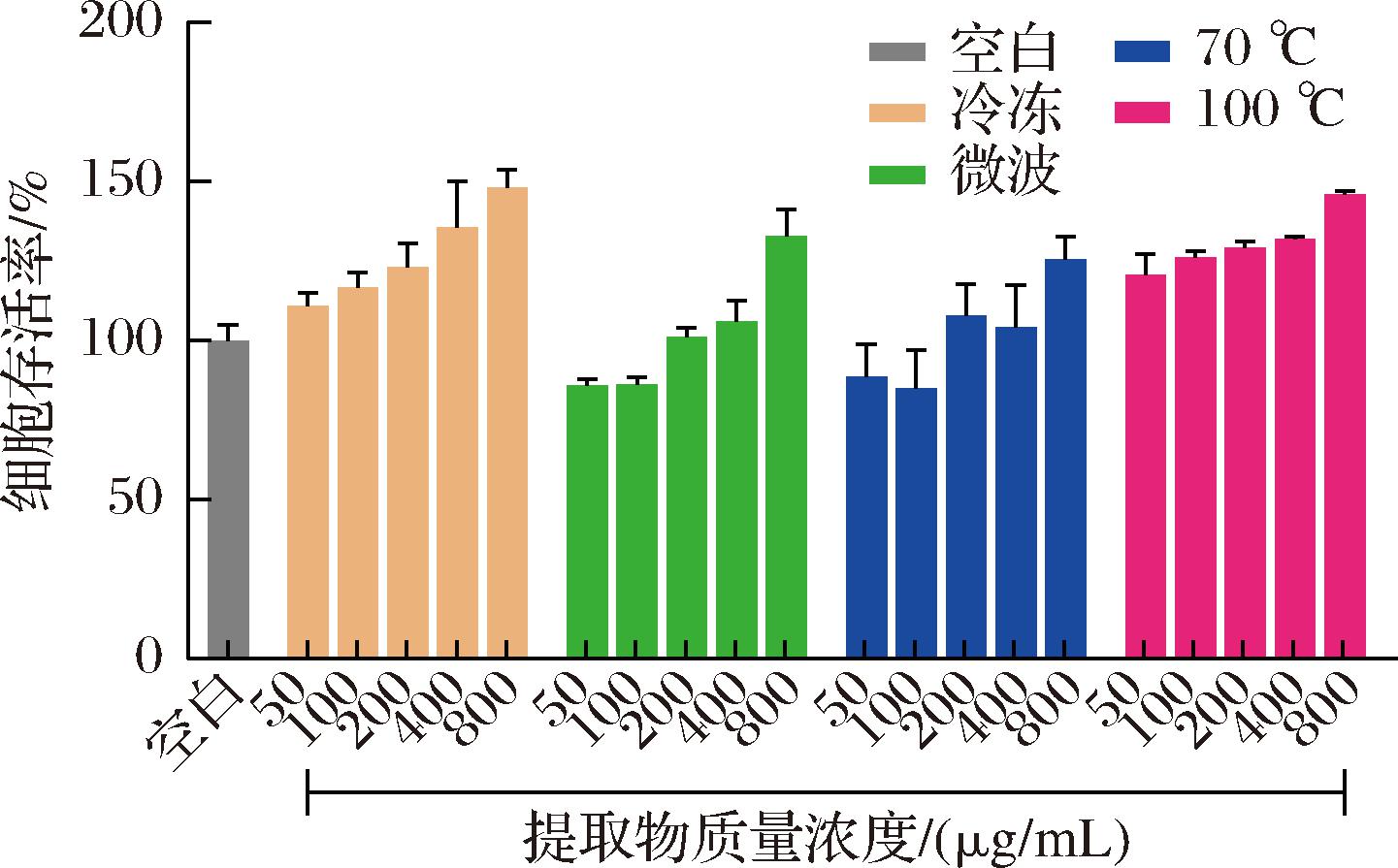
图3 不同干燥处理的罗汉果对RAW 264.7 细胞存活率的影响
Fig.3 Effects of S. grosvenorii by different drying methods on cell viabilities of RAW 264.7
表6 不同干燥处理的罗汉果对NO的抑制作用
Table 6 Effects of SG by different drying methods on NO inhibition
干燥方式时间/hNO抑制IC50/(μg/mL)冷冻干燥120393.40±4.24微波-578.97±11.5970 ℃72274.20±1.41100 ℃24108.45±1.91100 ℃15250.75±1.20100 ℃10254.55±3.75100 ℃5276.25±0.21地塞米松-42.81±6.67
2.3.2 不同干燥样品的炎症因子分泌抑制活性
TNF-α和IL-6是两种典型的促炎因子,可以增强巨噬细胞的敏感性,促进其他促炎因子的释放,从而加剧局部炎症反应,对其分泌的抑制能力是药物发挥抗炎作用的一个重要因素[24]。此外,ROS作为细胞内第二信使分子在细胞生理中具有广泛的意义。一方面,适量的ROS具有杀灭入侵病原体、促进伤口愈合和修复的作用;另一方面,过量的ROS的产生会破坏氧化还原的稳态,触发炎症反应[25]。
由图4可知,与空白组相比,模型组经LPS诱导显著提高了RAW 264.7细胞TNF-α、IL-6和ROS的分泌水平,但200 μg/mL罗汉果样品处理后这些炎症因子的分泌水平显著下降。冷冻干燥、微波、70 ℃和100 ℃干燥的罗汉果提取物对TNF-α分泌抑制率分别为12.33%、2.52%、13.59%和28.40%;对IL-6的抑制率分别为25.42%、4.43%、38.09%和46.30%;对ROS分泌的抑制率分别为59.14%、40.87%、74.72%和72.16%。恒温100 ℃干燥过程中,样品均具有一定的TNF-α、IL-6和ROS抑制活性,且抑制活性随样品质量浓度的递增而增加。干燥时间的延长有利于罗汉果提取物对两种炎症因子分泌抑制活性的提高,100 ℃完全干燥的罗汉果提取物抑制效果最优,其原因可能是100 ℃完全干燥罗汉果提取物含有较丰富的总黄酮和总皂苷。
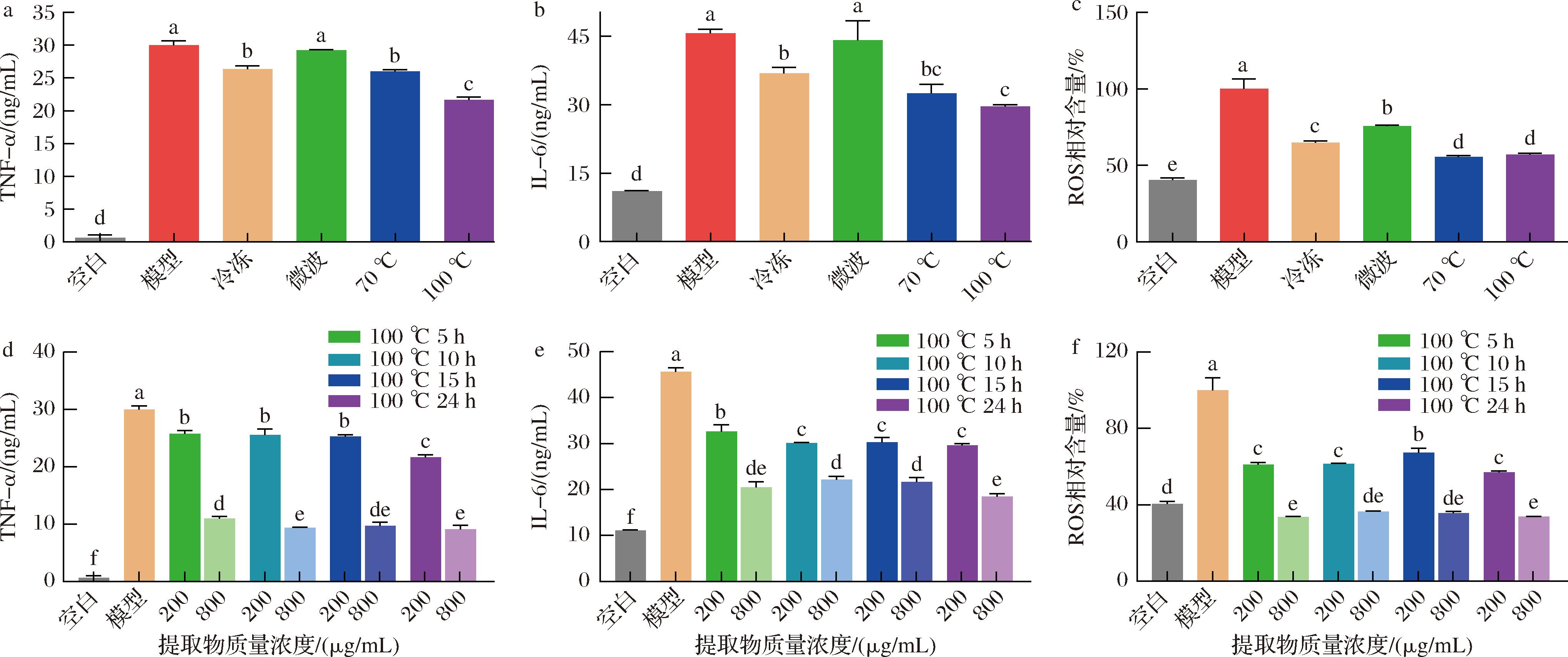
a-不同干燥方式处理罗汉果对TNF-α生成量的影响;b-不同干燥方式处理罗汉果对IL-6生成量的影响;c-不同干燥方式处理罗汉果对 ROS生成量的影响;d-100 ℃热风干燥的罗汉果对TNF-α生成量的影响;e-100 ℃热风干燥的罗汉果对IL-6生成量的影响; f-100 ℃热风干燥的罗汉果对ROS生成量的影响
图4 不同干燥处理的罗汉果对TNF-α、IL-6和ROS的抑制活性影响
Fig.4 Effects of S. grosvenorii by different drying methods on TNF-α、IL-6 and ROS inhibitions
注:不同小写字母表示差异显著(P<0.05)(下同)。
2.4 罗汉果功能成分与抗炎活性相关性分析
为了探索干燥处理的罗汉果功能成分与抗炎活性之间的相互关系,运用SPSS中Spearman相关系数检验分析。结果如表7所示,NO、TNF-α、IL-6、ROS抑制率与总糖、总黄酮、总皂苷含量的Spearman相关系数较高,其中NO和TNF-α抑制率与总糖含量呈显著负相关性(P<0.05),但与总黄酮、总皂苷含量呈显著正相关(P<0.05)。NO生成抑制率与赛门苷I、罗汉果苷IV和罗汉果苷IIE相关系数较高(0.385~0.630),呈正相关。对TNF-α的抑制率与11-氧化-罗汉果苷V、赛门苷I、罗汉果苷IV、IIIE及IIE呈正相关,相关系数0.202~0.712。IL-6抑制率与罗汉果各皂苷呈正相关,且与罗汉果苷IIIE和IIE的相关系数较高。所测罗汉果皂苷与ROS抑制活性均呈正相关,其中与赛门苷I的相关系数较高。这些结果提示,干燥处理引起的罗汉果抗炎活性差异与其功能成分的变化相关,其中总黄酮、总皂苷、及次级皂苷如赛门苷I和罗汉果苷IIE与抗炎能力有一定的量效关系,可能是罗汉果发挥抗炎活性的基础成分。
表7 相关性分析表
Table 7 Table of correlation analysis
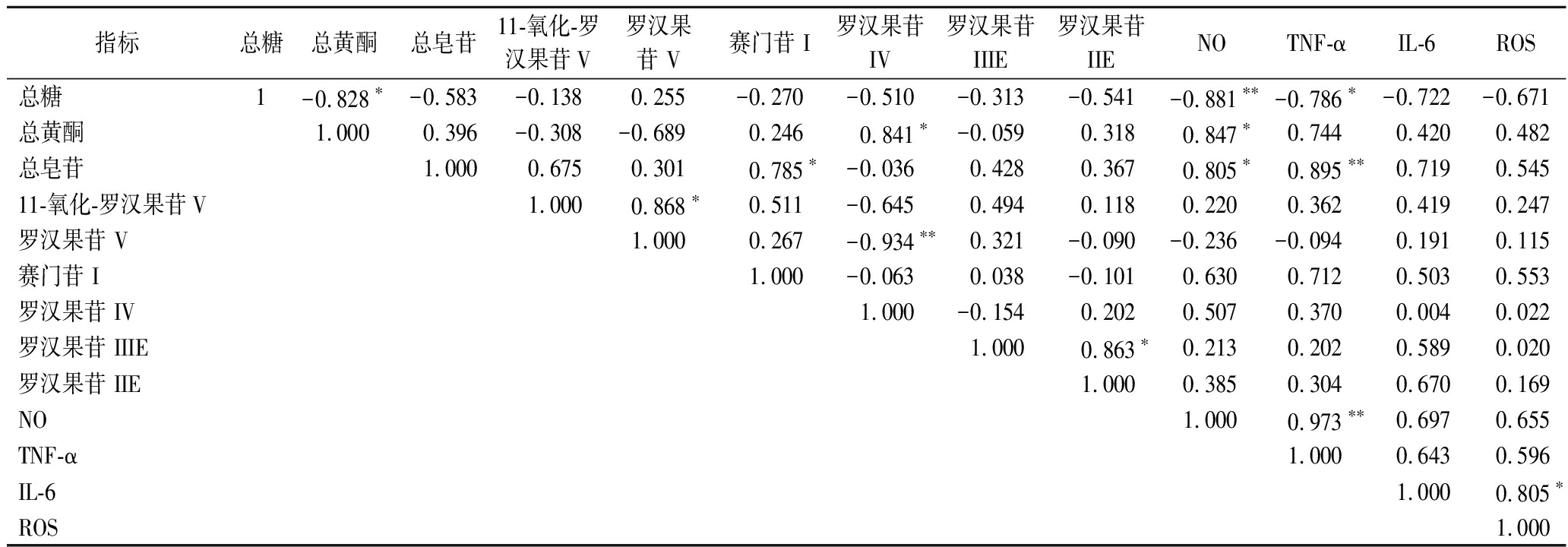
指标总糖总黄酮总皂苷11-氧化-罗汉果苷V罗汉果苷 V赛门苷 I罗汉果苷 IV罗汉果苷IIIE罗汉果苷 IIENOTNF-αIL-6ROS总糖1-0.828∗-0.583 -0.138 0.255 -0.270 -0.510 -0.313 -0.541 -0.881∗∗-0.786∗-0.722 -0.671 总黄酮1.000 0.396 -0.308 -0.689 0.246 0.841∗-0.059 0.318 0.847∗0.744 0.420 0.482 总皂苷1.000 0.675 0.301 0.785∗-0.036 0.428 0.367 0.805∗0.895∗∗0.719 0.545 11-氧化-罗汉果苷V1.000 0.868∗0.511 -0.645 0.494 0.118 0.220 0.362 0.419 0.247 罗汉果苷 V1.000 0.267 -0.934∗∗0.321 -0.090 -0.236 -0.094 0.191 0.115 赛门苷 I1.000 -0.063 0.038 -0.101 0.630 0.712 0.503 0.553 罗汉果苷 IV1.000 -0.154 0.202 0.507 0.370 0.004 0.022 罗汉果苷 IIIE1.000 0.863∗0.213 0.202 0.589 0.020 罗汉果苷 IIE1.000 0.385 0.304 0.670 0.169 NO1.000 0.973∗∗0.697 0.655 TNF-α1.000 0.643 0.596 IL-61.000 0.805∗ROS1.000
注:*双侧显著相关(P<0.05),**双侧极显著相关(P<0.01)。
3 结论与讨论
罗汉果作为我国首批药食同源中草药资源,在功能食品等大健康领域有极大应用价值。目前,罗汉果的研究主要集中于甜苷及其生物活性,关于罗汉果其他功能成分及这些成分含量变化对罗汉果抗炎活性的影响还知之甚少。因此,本研究检测了不同干燥处理的罗汉果果实中代表性功能物质即总糖、总黄酮、总皂苷及其特有的三萜皂苷成分的变化,并在细胞水平比较了其体外抗炎活性。结果表明,微波干燥样品中总糖含量最高,鼓风干燥则降低了总糖含量。干制处理均引起罗汉果总黄酮含量的升高,且总黄酮含量在干燥过程中逐渐增加。微波干燥与70 ℃鼓风干燥造成总皂苷含量的显著下降,100 ℃鼓风干燥对总皂苷含量的影响相对较小,且干燥处理会引起罗汉果苷V的降解与次级苷的生成。恒温100 ℃干制过程中,罗汉果苷V含量逐渐降低,苷IV、IIIE、IIE等次级苷含量逐渐升高,完全干燥后赛门苷I和罗汉果苷IV的含量达到最高,苷IIIE与苷IIE含量则先升后降。聚类分析与PCA进一步验证了这些变化。体外抗炎活性结果显示,鼓风干燥的罗汉果对NO生成抑制活性优于冷冻干燥和微波干燥果,干燥时间的延长引起NO抑制IC50值的下降。然而,不同温度鼓风干燥样品对RAW 264.7细胞TNF-α、IL-6和ROS分泌的抑制能力无显著性差异。相关性分析发现,罗汉果总黄酮、总皂苷含量与NO、TNF-α、IL-6、ROS抑制率呈正相关,总糖含量与4类抗炎指标呈负相关。综上所述,在罗汉果干制加工中,上述三大功能成分存在显著的变化,并对抗炎活性产生直接影响,而鼓风干燥更有利于罗汉果抗炎活性的提高。该研究可为罗汉果功能产品的开发工艺和质量控制提供理论依据。后续将分别对罗汉果中的黄酮物质群和多糖成分进行富集与分离,进一步探讨其与皂苷组分在抗炎作用上互作关系。
[1] 王苗苗, 娄华勇, 张妮, 等.罗汉果化学成分及药理研究进展[J].贵州中医药大学学报, 2021, 43(5):80-84.WANG M M, LOU H Y, ZHANG N, et al.Research progress on chemical constituents and pharmacological activities of Siraitia grosvenorii Swingle[J].Journal of Guizhou University of Traditional Chinese Medicine, 2021, 43(5):80-84.
[2] 魏炳琦, 高小雨, 刘延鑫, 等.罗汉果苷的功能及应用研究进展[J].食品工业科技, 2023, 44(11):434-441.WEI B Q, GAO X Y, LIU Y X, et al.Research progress on function and application of mogroside[J].Science and Technology of Food Industry, 2023, 44(11):434-441.
[3] LIU H S, WANG C C, QI X Y, et al.Antiglycation and antioxidant activities of mogroside extract from Siraitia grosvenorii (swingle) fruits[J].Journal of Food Science and Technology, 2018, 55(5):1880-1888.
[4] WANG Q, QIN H H, WANG W, et al.The pharmacological research progress of Siraitia grosvenorii[J].Journal Guangxi Traditional Chinese Medicine University, 2010, 13:75-76.
[5] 刘博昊, 何如愿, 熊锐, 等.罗汉果醇对脂多糖诱导急性肺损伤的作用及机制研究[J].中华急诊医学杂志, 2022, 31(6):777-782.LIU B H, HE R Y, XIONG R, et al.Effect and mechanism of mogrol on lipopolysaccharide-induced acute lung injury[J].Chinese Journal of Emergency Medicine, 2022, 31(6):777-782.
[6] LIANG H, CHENG R, WANG J Y, et al.Mogrol, an aglycone of mogrosides, attenuates ulcerative colitis by promoting AMPK activation[J].Phytomedicine, 2021, 81:153427.
[7] CHEN J, JIAO D M, LI Y, et al.Mogroside V inhibits hyperglycemia-induced lung cancer cells metastasis through reversing EMT and damaging cytoskeleton[J].Current Cancer Drug Targets, 2019, 19(11):885-895.
[8] 李浩雨, 徐兴军, 李雪涵, 等.罗汉果总黄酮对慢性睡眠剥夺小鼠抗氧化能力及炎症反应的影响[J].动物营养学报, 2023, 35(7):4668-4677.LI H Y, XU X J, LI X H, et al.Effects of total flavonoids of Siraitia grosvenorii on antioxidant ability and inflammatory responses in mice with chronic sleep derivation[J].Chinese Journal of Animal Nutrition, 2023, 35(7):4668-4677.
[9] GONG P, CUI D D, GUO Y X, et al.A novel polysaccharide obtained from Siraitia grosvenorii alleviates inflammatory responses in a diabetic nephropathy mouse model via the TLR4-NF-κB pathway[J].Food &Function, 2021, 12(19):9054-9065
[10] 范天慈, 窦志英, 李捷, 等.不同干燥方式对中药成分影响的研究进展[J].中国现代中药, 2021, 23(11):2017-2024.FAN T C, DOU Z Y, LI J, et al.Effects of different drying methods on chemical components of traditional Chinese medicine:A review[J].Modern Chinese Medicine, 2021, 23(11):2017-2024.
[11] 于迪, 杨辛欣, 王莹, 等.防风趁鲜切制的含水率及不同干燥方式对饮片质量的影响[J].中草药, 2022, 53(9):2678-2686.YU D, YANG X X, WANG Y, et al.Effect onquality of decoction pieces by different drying methods and moisture content of fresh Saposhnikoviae Radix cutting[J].Chinese Traditional and Herbal Drugs, 2022, 53(9):2678-2686.
[12] 王雅倩, 安可婧, 黄桂颖, 等.不同年份老香黄活性成分、抗氧化活性及挥发性成分分析[J].食品与发酵工业, 2023, 49(21):221-228.WANG Y Q, AN K J, HUANG G Y, et al.Analysis of active components, antioxidant activities and volatile components of Laoxianghuang in different years[J].Food and Fermentation Industries, 2023, 49(21):221-228.
[13] 周欣欣. 市售制剂中罗汉果总皂苷的含量测定[J].中成药, 2007, 29(1):152-153.ZHOU X X.Luo-han-guo momorsides content determining in market preparatiotis[J].Chinese Traditional Patent Medicine, 2007, 29(1):152-153.
[14] 吴少雄, VAN BOEKE M A J S, MARTINS S I FS, 等.温度对美拉德反应的研究[J].食品科学, 2005, 26(7):663-66.WU S X, VAN BOEKE M A J S, MARTINS S I FS, et al.Effects of temperatures on Maillard reactions[J].Food Science, 2005, 26(7):63-66.
[15] 迟晓君, 王桢, 李苗苗, 等.干燥方式对老山芹功能成分及抗氧化性的影响[J].食品工业科技, 2021, 42(24):165-171.CHI X J, WANG Z, LI M M, et al.Effect of different drying methods on functional components and antioxidant activity of Heracleum moellendorffii hance[J].Science and Technology of Food Industry, 2021, 42(24):165-171.
[16] 卢凤来, 李典鹏, 刘金磊, 等.不同干燥处理的罗汉果化学成分色谱指纹图谱分析[J].广西农业科学, 2009, 40(6):625-628.LU F L, LI D P, LIU J L, et al.Chromatographic fingerprinting analysis on chemical compositions of Siraitia grosvenorii fruit with different drying treatments[J].Guangxi Agricultural Sciences, 2009, 40(6):625-628.
[17] 赖文, 杨利民, 韩佳宏, 等.不同干燥方法对林下参品质的影响[J].中国野生植物资源, 2023, 42(2):62-68.LAI W, YANG L M, HAN J H, et al.Effects of different drying methods on the quality of ginseng in forest[J].Chinese Wild Plant Resources, 2023, 42(2):62-68.
[18] PAWAR R S, KRYNITSKY A J, RADER J I.Sweeteners from plants:With emphasis on Stevia rebaudiana (bertoni) and Siraitia grosvenorii (swingle)[J].Analytical and Bioanalytical Chemistry, 2013, 405(13):4397-4407.
[19] 牟俊飞, 王韶旭, 罗琴, 等.HPLC-MS法测定罗汉果中6种罗汉果甜苷含量[J].食品研究与开发, 2018, 39(15):139-144.MOU J F, WANG S X, LUO Q, et al.Determination of content of 6 kinds of mogrosides in Siraitia grosvenorii by using HPLC-MS/MS[J].Food Research and Development, 2018, 39(15):139-144.
[20] XIAO J, HUANG K, LIN H M, et al.Mogroside IIE inhibits digestive enzymes via suppression of interleukin 9/interleukin 9 receptor signalling in acute pancreatitis[J].Frontiers in Pharmacology, 2020, 11:859.
[21] XUE W, MAO J H, CHEN Q J, et al.Mogroside IIIE alleviates high glucose-induced inflammation, oxidative stress and apoptosis of podocytes by the activation of AMPK/SIRT1 signaling pathway[J].Diabetes, Metabolic Syndrome and Obesity, 2020, 13:3821-3830.
[22] LEE S B, LEE W S, SHIN J S, et al.Xanthotoxin suppresses LPS-induced expression of iNOS, COX-2, TNF-α, and IL-6 via AP-1, NF-κB, and JAK-STAT inactivation in RAW 264.7 macrophages[J].International Immunopharmacology, 2017, 49:21-29.
[23] 杨刚, 崔小燕, 张佳雄, 等.东紫苏化学成分及其抗炎活性研究[J].中草药, 2023, 54(12):3777-3784.YANG G, CUI X Y, ZHANG J X, et al.Chemical constituents from Elsholtzia bodinieri and their anti-inflammatory activities[J].Chinese Traditional and Herbal Drugs, 2023, 54(12):3777-3784.
[24] GAO X, LIN X R, HO C T, et al.Chemical composition and anti-inflammatory activity of water extract from black cocoa tea (Camellia ptilophylla)[J].Food Research International, 2022, 161:111831.
[25] 伍芳芳. 猴头菇多糖的结构表征、免疫调节活性及其机理研究[D].广州:华南理工大学, 2018.WU F F.Structural characterization, immunomodulatory activities and underlying mechanism of Hericium erinaceus polysaccharide[D].Guangzhou:South China University of Technology, 2018.