西藏传统青稞酒历史悠久,文化深厚,与藏族人民的日常生活戚戚相关,为西藏地区特色民族食品之瑰宝。相对于其他酒,青稞酒含有丰富的β-葡聚糖、生长素以及微量元素等物质,具有提高人体免疫力、清除体内毒素、防癌、抗癌及增加藏族人民抵抗力等多种功效[1-2]。
然而,与其他食品相比,西藏传统青稞酒具有工艺过程复杂与独特的多菌种发酵等特点,例如青稞酒是以霉菌、酵母和细菌为主的多菌种共栖发酵,发酵风味的形成与菌群相互作用、发酵环境改变引起的代谢通路相关酶的基因表达变化有关,多菌种发酵中微生物区系及其在发酵过程的活性决定了最终的发酵风味[3-4]。其次,传统青稞酒中除主要发酵物质外,还有成百上千种其他代谢产物,众多微量成分的有机协调搭配,形成了传统青稞酒独特的产品风格。但是这些风味物质并非是单一微生物功能的简单迭加,而是由群体微生物协同代谢复合作用的结果[5],因此对传统青稞酒酿造微生物群体所形成的复杂酿造生物学过程认识不清,是影响藏区传统青稞酒酿造技术发展的主要限制因素。
宏基因组学是以特定环境中整个微生物基因组作为研究对象的,在微生物总DNA提取后,经建库、测序及质控后进行物种分类注释,并与KEGG、Clusters of Orthologous Groups (COG)、Carbohydrate-active enzymes (CAZy)等功能数据库进行代谢功能及通路的注释分析,对整个环境中微生物群体的群落结构、功能基因进行研究分析,该技术既提供了对无法分离培养的微生物进行研究的途径,同时也避免了样品在实验过程中由环境改变引起的微生物序列变化所带来的变差,在客观还原微生物群落结构的基础上,还可以对微生物群落的代谢功能变化进行研究[6]。候强川等[7]以2种不同类型的强化酒曲为研究对象,通过宏基因组测序技术对菌群群落结构及功能进行解析,酒曲不仅包含较多的酿酒酵母,还拥有众多与白酒风味物质产生相关的功能菌,如米根霉、类肠膜魏斯氏菌、融合魏斯氏菌、蜡样芽孢杆菌等,在功能方面具有潜在更强的风味物质产生能力。麻颖垚[8]利用宏基因组技术对酱香型白酒第4轮次窖内酒醅进行研究,揭示了窖内微生物菌群结构与风味物质代谢的关系,其中细菌门14个,细菌属409个,真菌门4个,真菌属40个,通过KEGG数据库进行注释分析,发现微生物代谢功能中碳水化合物代谢(17.20%)与氨基酸代谢(15.37%)丰度较高,同时确定了关键酶。宏基因组与风味物质分析结合在一起,有助于进一步了解酿造过程中风味物质的代谢途径及其与微生物代谢之间的关系。
本研究采用宏基因组学技术解析不同青稞小曲酿造的青稞酒中微生物群落结构和功能,利用GC-MS技术检测青稞酒发酵期间关键风味物质的变化规律,解析青稞酒发酵过程关键功能微生物以及功能微生物与风味物质间的关联度,为实现传统青稞酒关键风味的定向调控奠定理论基础。
1 材料与方法
1.1 材料与试剂
藏曲及青稞(藏青2000)由西藏自治区农牧科学院提供,其中两种藏曲来自西藏2个不同海拔的青稞酒企业,分别是海拔3 600 m的拉萨地区和海拔4 000 m的日喀则地区,编号分别是A和B。
1.2 仪器与设备
DVB/CAR/PDMS固相微萃取头,美国Supelco公司;DB-FFAP色谱柱(60 m×0.25 mm,0.25 μm)、Clarus680-Clarus600T型GC-MS,美国Agilent公司;Miseq高通量测序仪,美国Illumina公司。
1.3 青稞酒制作工艺
称取250 g青稞原料清洗,使用纯水浸泡12 h后换水,再次浸泡12 h(水面高于粮面5 cm),将浸泡后的青稞洗净,平铺于屉布上沥干,放于蒸锅中蒸粮,待冒汽10 min后将青稞翻拌1次,继续蒸粮60 min,使粮粒裂口率达80%,将蒸后的青稞放入搪瓷盆中摊晾至32 ℃,拌入2 g酒曲,搭窝,于30 ℃培养箱中进行糖化及发酵,48 h后转入已灭菌的广口瓶中,加入无菌水(约500 g)使青稞干重∶水(g∶mL)为1∶2,混匀,于30 ℃继续发酵96 h,过滤、离心,得到青稞酒样品。以总糖含量变化为依据,青稞酒酿造过程中分为4个阶段取样,发酵初期青稞发酵液(1);发酵中期青稞发酵液(2);发酵后期青稞发酵液(3);青稞酒(4)。试验设3个重复,各阶段样品混合后进行分析。
1.4 青稞酒理化指标的测定
酒精度、总糖、总酸和pH值等常规理化指标参照GB/T 13662—2018《黄酒》中规定的方法测定。所有检测指标重复3次。
1.5 青稞酒挥发性风味物质检测
采用固相微萃取与GC-MS技术分析,分别称取3 g NaCl和5 g样品装入30 mL玻璃瓶中。气相条件:载气高纯氦气(纯度≥99.99%);流速1 mL/min;进样0.5 min前不分流,1 min后分流比为10∶1;起始温度40 ℃,恒温2 min,以4 ℃/min升温至230 ℃,保持7 min;进样口温度230 ℃。质谱条件:离子源温度230 ℃;离子源电压450 V;传输线温度230 ℃;电子轰击源70 eV;扫描范围:29~300 amu[9]。
定性方法:通过对GC-MS总离子流色谱图与美国国家标准技术研究所质谱库中化合物进行比对;定量方法:采用内标法对样品中挥发性行成分进行定量分析,叔戊醇作为内标物,根据内标物峰面积与各组分峰面积之比定量各组分的相对浓度。
1.6 基因组DNA提取
利用FastDNA® Spin Kit for Soil试剂盒进行样品DNA抽提。完成DNA抽提后,检测DNA浓度和纯度,利用1%琼脂糖凝胶电泳检测DNA完整性。同时,使用超声波破碎仪将DNA打断,并筛选约为400 bp的片段,用于构建PE文库。
1.7 文库构建和桥式PCR测序
使用NEXTFLEX Rapid DNA-Seq建库,具体操作见说明书。首先,使用磁珠筛选去除接头自连片段;其次,利用PCR扩增进行文库模板的富集;最后,磁珠回收PCR产物得到最终的文库。使用Illumina NovaSeq测序平台进行宏基因组测序,首先,文库分子一端与引物碱基互补,经过一轮扩增,将模板信息固定在芯片上,固定在芯片上的分子另一端随机与附近的另外一个引物互补,也被固定住,形成桥;其次,PCR扩增,产生DNA簇,DNA扩增子线性化成为单链后,加入改造过的DNA聚合酶和带有4种荧光标记的dNTP,每次循环只合成一个碱基,再使用激光扫描反应板表面,读取每条模板序列第1轮反应所聚合上去的核苷酸种类,将荧光基团和终止基团化学切割,恢复3′端黏性,继续聚合第2个核苷酸;最后,统计每轮收集到的荧光信号结果,获知模板DNA片段的序列。
1.8 质量控制和组装
使用Fastp(https://github.com/OpenGene/fastp,version 0.20.0)去除剪切后长度小于50 bp、平均碱基质量值低于20以及含N碱基的reads,保留高质量的pair-end reads和single-end reads;通过软件BWA(http://bio-bwa.sourceforge.net,version 0.7.9a)将reads比对宿主DNA序列,并去除比对相似性高的污染reads[10]。
使用软件MEGAHIT(https://github.com/voutcn/megahit,version 1.1.2)对优化序列进行拼接组装。在拼接结果中筛选≥300 bp的contigs作为最终的组装结果[11]。使用Prodigal/MetaGene(http://metagene.cb.k.u-tokyo.ac.jp/)对拼接结果中的contigs进行ORFs预测。选择核酸长度大于等于100 bp的基因,并将其翻译为氨基酸序列[12]。
1.9 物种分类与功能注释
为了预测青稞酒发酵过程中菌落组成和功能基因,共使用6个数据库,包括NR、evolutionary genealogy of genes:Non-supervised Orthologous Groups(EGGNOG)、KEGG、CAZy、antibiotic resistance database(ARDB)、virulent factor database(VFDB),并进行BLAST搜索,BLASTP比对参数设置期望值e-value为1e-5[13]。
1.10 多元统计分析
使用SPSS 26.0软件进行统计分析。
2 结果与分析
2.1 青稞酒基本理化指标分析
如表1所示,随着发酵进行,A、B样品总糖呈下降趋势,酒精度呈上升趋势,总酸变化不大,表明两种藏曲均能够完成酒精发酵。在发酵中期时,A、B样品pH值有较大幅度变化,原因是糖化发酵第1阶段在青稞酒醅中进行一定量的补水。发酵结束后,两种样品总糖与酒精度无显著性差异,B样品中总酸与pH值高于A样品,主要原因是不同藏曲间曲内微生物种类与丰度存在差异,可能体现在产酸微生物上的区别。
表1 青稞酒样品的理化指标
Table 1 Physicochemical indexes of highland barley wine samples

样品编号发酵时间/d总糖/(g/L)总酸/(g/L)pH值酒精/%volA1150.42±1.856.53±0.012.52±0.022.91±0.08A2318.26±1.006.61±0.023.75±0.025.33±0.01A359.86±2.865.85±0.013.78±0.025.52±0.01A475.38±1.505.90±0.053.79±0.015.64±0.03B1146.29±2.156.93±0.032.54±0.032.68±0.01B2315.86±1.007.12±0.033.82±0.014.95±0.03B358.73±2.006.52±0.023.85±0.055.12±0.01B475.75±1.006.58±0.013.88±0.015.27±0.01
2.2 青稞酒挥发性风味物质分析
风味是评价青稞酒品质的关键指标[14],本研究在两种藏曲发酵青稞酒的4个发酵阶段样品中,共检测出37种挥发性风味物质,主要包括酯类、醇类、醛酮类和酚类物质。从整体看,在1阶段,风味物质种类和含量最少;在2、3、4这3个发酵阶段,风味物质种类和含量依次增多;在3、4发酵阶段,风味物质的组成基本稳定,是构成酒体风格的重要组成部分。其中,酯类物质有乙酸乙酯、乙酸苯乙酯、乙酸异戊酯、己酸乙酯、油酸乙酯、乳酸乙酯和乳酸异戊酯;醇类物质有正丙醇、异丙醇、正丁醇、异戊醇、3-甲基-3-丁烯-1-醇、正己醇、异辛醇、β-苯乙醇、甲醇、活性戊醇、甲醇、2-戊醇、1,3-丁二醇、2,3-丁二醇和丙二醇;醛类物质有乙醛、丙醛和糠醛;酚类物质有4-乙基愈创木酚和4-甲基愈创木酚。
1)酯类物质
由图1显示,根据A和B两种藏曲样品结果,在第4阶段发酵结束时,A、B样品中乙酸乙酯、乳酸乙酯、乙酸异戊酯三者占比较高,但其含量呈现差异性,A样品酯类物质总含量高于B样品,说明A样品提供花香和果香贡献度大于B样品[15]。其中,A样品中乙酸乙酯、乙酸异戊酯和乙酸苯乙酯等乙酸酯类含量和乳酸乙酯、乳酸异戊酯等乳酸酯类含量高于B样品,可能原因是A藏曲中产酯微生物的种类和丰度高于B藏曲。但是B样品中己酸乙酯、辛酸乙酯、癸酸乙酯、油酸乙酯和棕榈酸乙酯等中长链脂肪酸酯类含量高于A样品,可能原因是B藏曲的脂肪酸代谢效率高于A藏曲[16]。
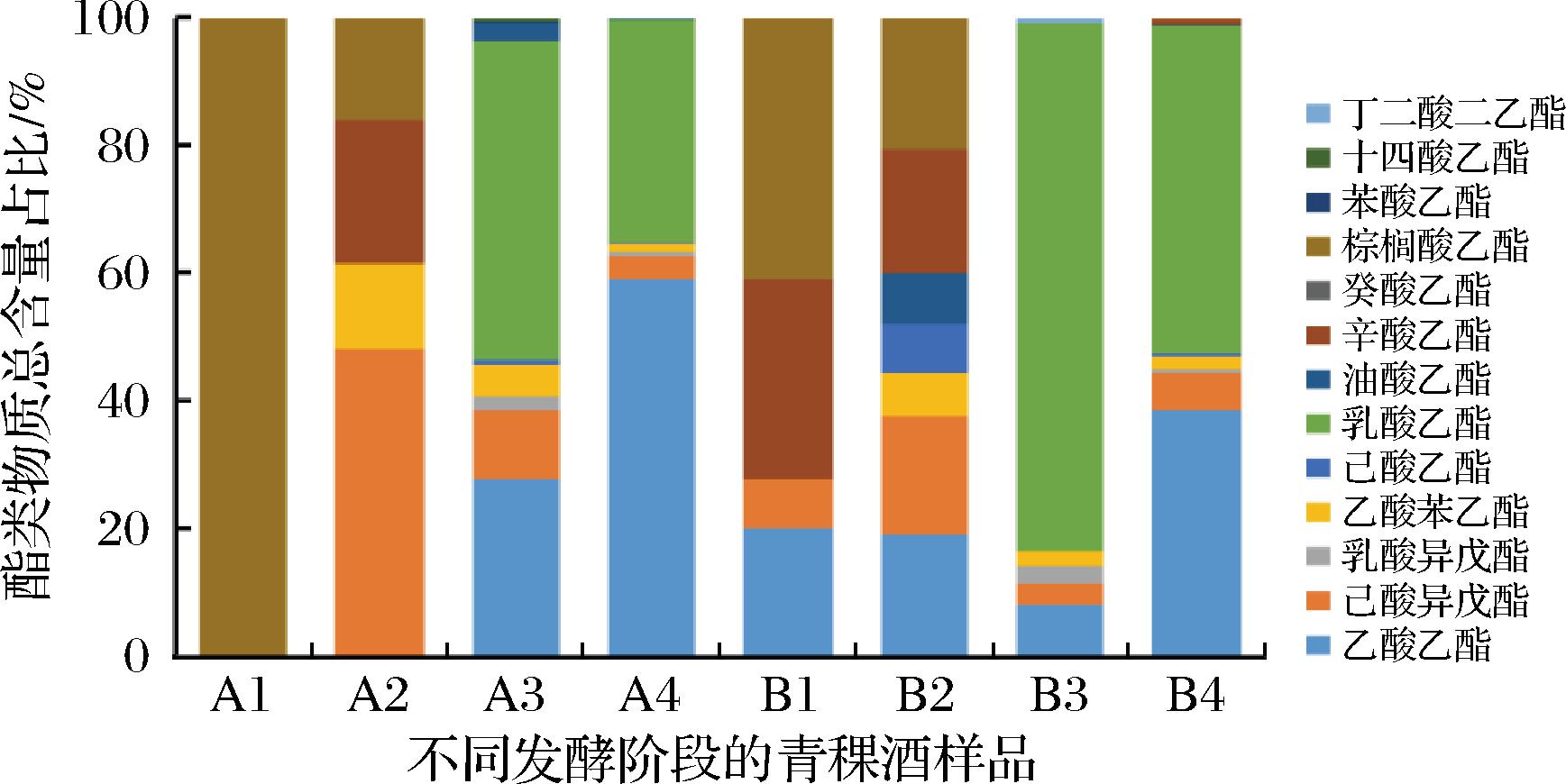
图1 不同发酵阶段青稞酒样品的酯类物质含量
Fig.1 Ester contents of highland barley wine samples at different fermentation stages
2)醇类物质
由图2显示,根据A和B这两种藏曲样品结果,在第4阶段发酵结束时,A、B样品中异戊醇、β-苯乙醇两者占比最高,B样品醇类物质异丁醇、异戊醇、正丁醇、1-辛烃-3-醇、2-戊醇总含量和种类多于A样品,说明B样品中杂醇油味、青草味、蘑菇味和果香味等风味的复杂度强于A样品[17]。A样品中正丙醇、正己醇、异辛醇、β-苯乙醇、活性戊醇、丙二醇和2,3-丁二醇高于B样品,其中A样品中含量最高的是正丙醇,比B样品增加了3.6倍,异辛醇和丙二醇仅存在于A样品中,说明A样品中醇香、甜香风味物质要高于B样品。然而B样品中甲醇、正丁醇、异丁醇、异戊醇、1,3-丁二醇高于A样品,其中正丁醇、2-戊醇仅存在于B样品中。可能原因是2种藏曲中微生物在高级醇代谢中合成效率不一致,进一步导致高级醇含量存在差异。
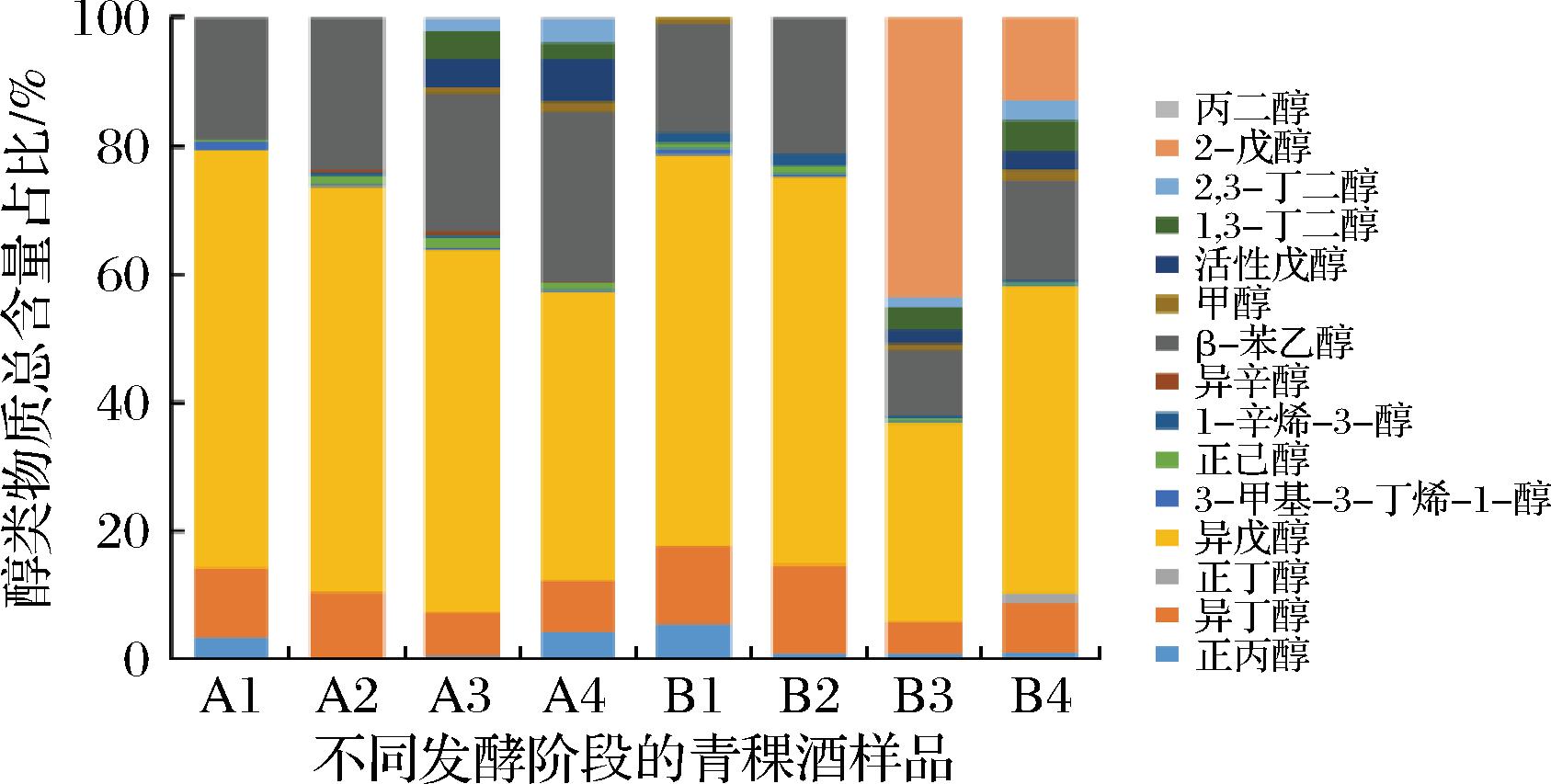
图2 不同发酵阶段青稞酒样品的醇类物质含量
Fig.2 Alcohol contents of highland barley wine samples at different fermentation stages
3)醛酮酚类物质
由图3显示,根据A和B这两种藏曲样品结果,在第4阶段发酵结束时,酮类物质含量为0。醛类物质有乙醛、丙醛和糠醛,丙醛仅存在于B样品中。A样品和B样品均含有4-乙基愈创木酚,4-甲基愈创木酚和四甲基吡嗪仅存在于A样品,说明A样品丁香味和烘烤味强于B样品[18]。
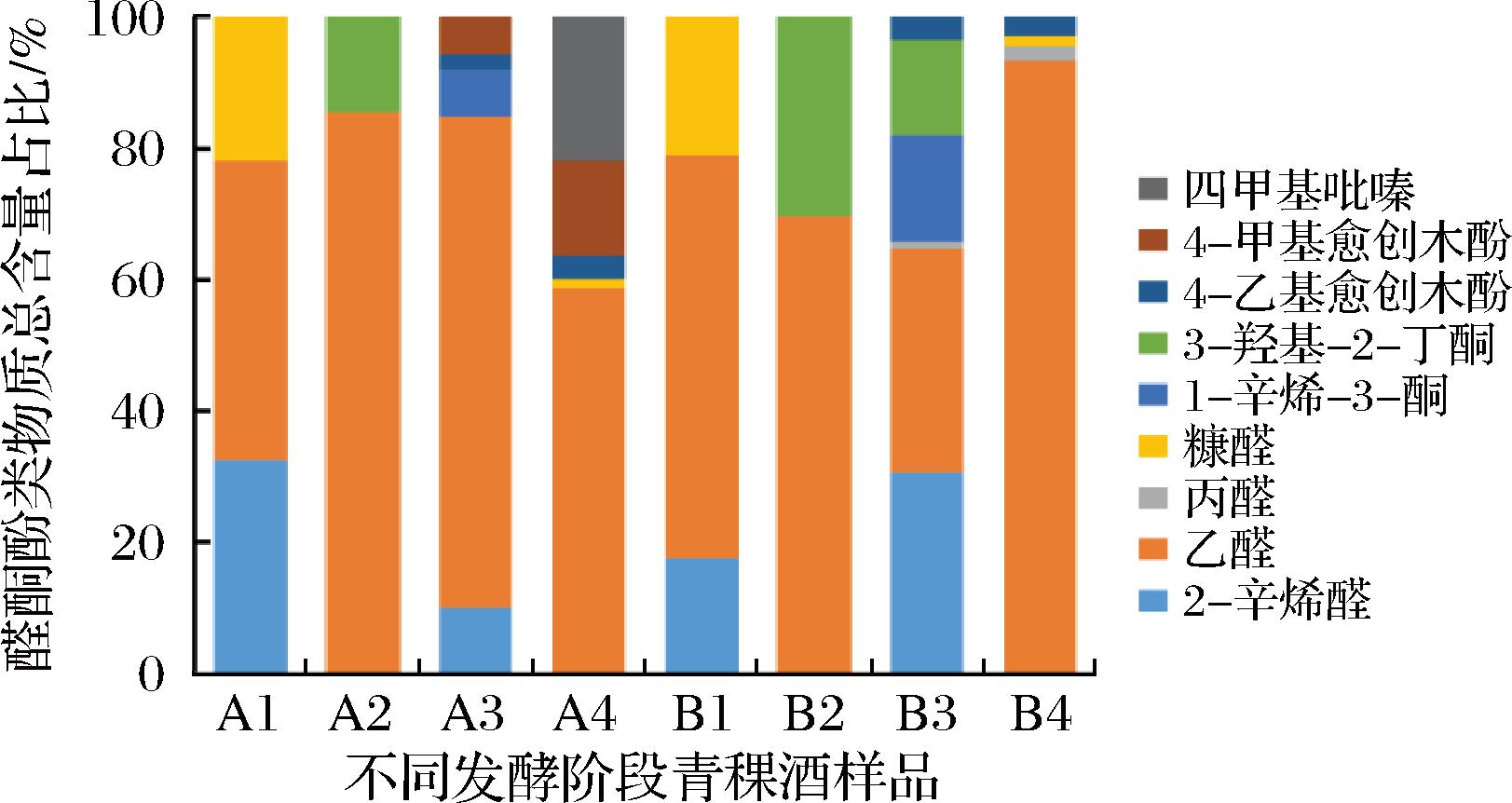
图3 不同发酵阶段青稞酒样品的醛酮酚类物质含量
Fig.3 Aldehyde-ketone phenolic substances contents of highland barley wine samples at different fermentation stages
综上所述,根据样品风味种类、含量以及风味特点,A、B样品在主要风味物质乙酸乙酯、乳酸乙酯、β-苯乙醇等含量占比呈现相似性,整体风味物质轮廓呈现一定的差异性,A样品在醇香、甜香味、丁香味和烘烤味的强度上可能强于B样品。B样品在杂醇油味、青草味、蘑菇味、果香味等风味的复杂度上可能强于A样品,推测A、B这两种藏曲中存在优势菌属在发酵结束时呈现相似性,部分微生物组成存在显著差异对青稞酒的风味产生了影响,因此进一步分析了二者在青稞酒发酵过程中微生物多样性和代谢通路丰度,对青稞酒风味物质的形成机理提供理论依据。
2.3 宏基因组数据质控分析
为了分析青稞酒糖化发酵过程中的微生物组成和功能基因,分别对不同发酵时期样品进行了宏基因组测序。根据测序结果,总共读取原始数据是942 268 394,原始碱基对是142.28 Gbp。进行质量控制后,总共获得高质量数据是919 521 040,占原始数据的97.58%;高质量碱基对是138.33 Gbp,占原始碱基对的97.22%。基因预测后,共有823 072个ORFs,平均碱基长度为602.75 bp,同时去冗长获得823 072个基因,去冗长平均碱基长度为640.65 bp。
2.4 分类学分析
2.4.1 微生物群落Alpha多样性分析
Alpha多样性可以反映样品间的物种多样性与物种丰富度之间的差别,常用Chao1指数、Shannon指数、Simpson指数等作为数据的衡量指标。由表2可知,A、B样品的覆盖率均在0.99以上,说明此次测序深度已基本覆盖到样品中所有的微生物[19]。Chao1指数主要表示物种丰富度情况,数值越大表示物种丰度越高;A样品在发酵过程中细菌群落Chao1指数由最低值184逐渐升高至245,真菌群落Chao1指数波动幅度不大,均值在633。B样品在发酵过程中细菌群落Chao1指数值呈现波动趋势由发酵初期最高值400逐渐降低至194后在发酵后期逐渐升高,真菌群落Chao1指数无明显变化,说明青稞酒发酵过程中细菌群落的丰度在不断变化,真菌群落的丰度变化较为平缓。细菌群落Shannon指数与Simpson指数主要表示菌群结构的多样性,Shannon指数越大表示物种的多样性越高,Simpson指数则相反。A、B样品在发酵过程中细菌群落Shannon指数呈下降趋势,Simpson指数呈上升趋势,真菌群落Shannon指数与Simpson指数趋势与细菌群落相反,说明青稞酒发酵过程中细菌多样性逐渐减少,而真菌多样性逐渐增加,这可能与酒曲中微生物的耐受性相关,因为随着发酵进行,酒精度升高,部分细菌生长受到抑制,而耐酒精度的真菌进一步繁殖,导致细菌多样性减少,而真菌多样性增加。
表2 青稞酒发酵过程中Alpha多样性
Table 2 Alpha diversity of highland barley wine during fermentation
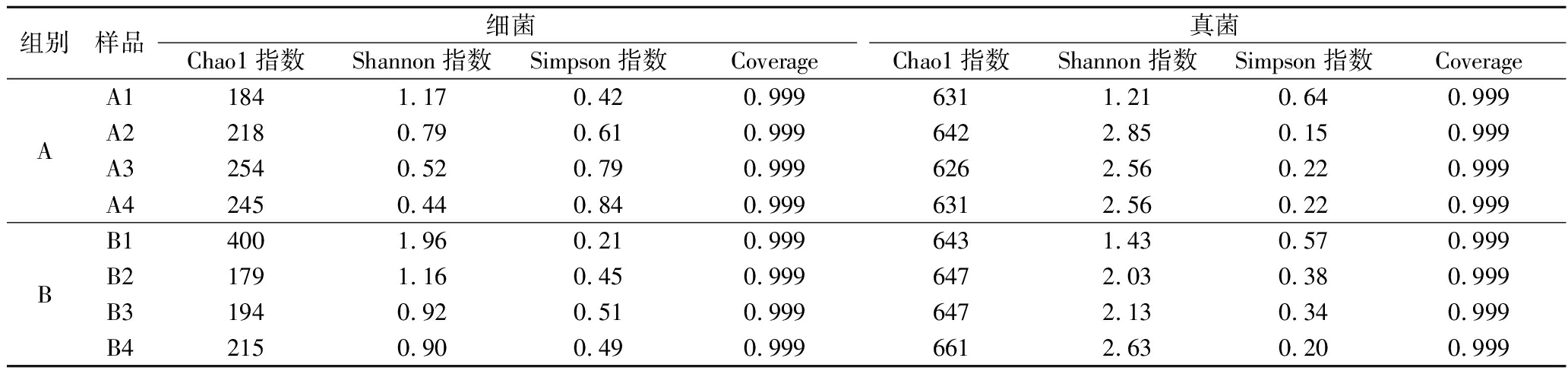
组别样品细菌真菌Chao1指数Shannon指数Simpson指数CoverageChao1指数Shannon指数Simpson指数CoverageAA11841.170.420.9996311.210.640.999A22180.790.610.9996422.850.150.999A32540.520.790.9996262.560.220.999A42450.440.840.9996312.560.220.999BB14001.960.210.9996431.430.570.999B21791.160.450.9996472.030.380.999B31940.920.510.9996472.130.340.999B42150.900.490.9996612.630.200.999
2.4.2 样品不同发酵阶段OTU数目分析
由图4-a可知A样品中共有的细菌OTU数目为157,A1单独含有细菌OTU为184个,A2单独含有细菌OTU为218个,A3单独含有细菌OTU为254个,A4单独含有细菌OTU为245个。由图4-b可知B样品中共有的细菌OTU为153个,B1单独含有细菌OTU为400个,B2单独含有细菌OTU为179个,B3单独含有细菌OTU为194个,B4单独含有215个。从整体看,B1含有细菌OTU数目最多,说明B样品在发酵前期其细菌群落丰富度最高[20]。这也与上面结果相对应,即随着发酵过程的进行,酒精度升高,部分细菌耐受性能差,导致其多样性逐渐降低。
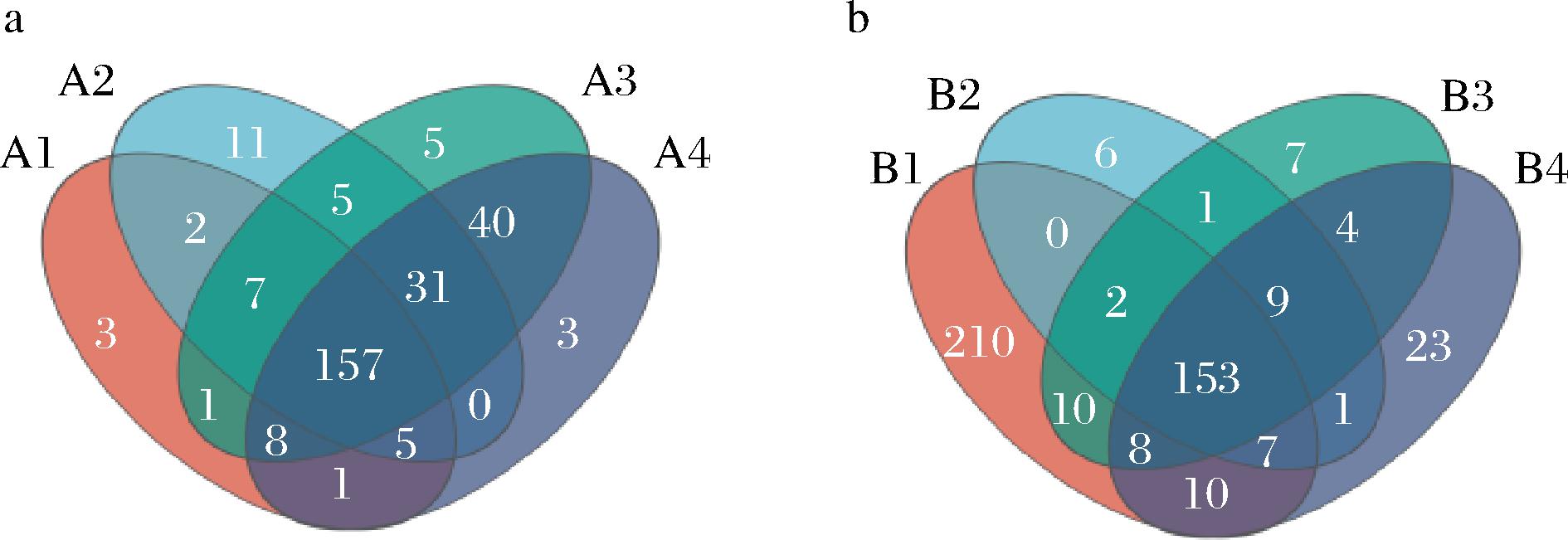
a-A样品的细菌OTU数目;b-B样品的细菌OTU数目
图4 细菌OTU数目Venn图
Fig.4 Venn diagram of OTU number of bacteria
由图5-a可知,A样品中共有的真菌OTU数目为570个,A1单独含有真菌OTU为631个,A2单独含有真菌OTU为642个,A3单独含有真菌OTU为626个,A4单独含有真菌OTU为631个。由图5-b可知B样品中共有的真菌OTU数目为570个,B1单独含有OTU为643个,B2单独含有OTU为647个,B3单独含有OTU为647个,B4单独含有OTU为661个。在整个发酵阶段,B样品真菌OTU普遍多于A样品,其中B4含有真菌OTU数目最多,说明B样品在随着发酵结束时,酒精度随之升高,部分真菌耐受性能高于细菌,所以,导致真菌群落丰富度最高。
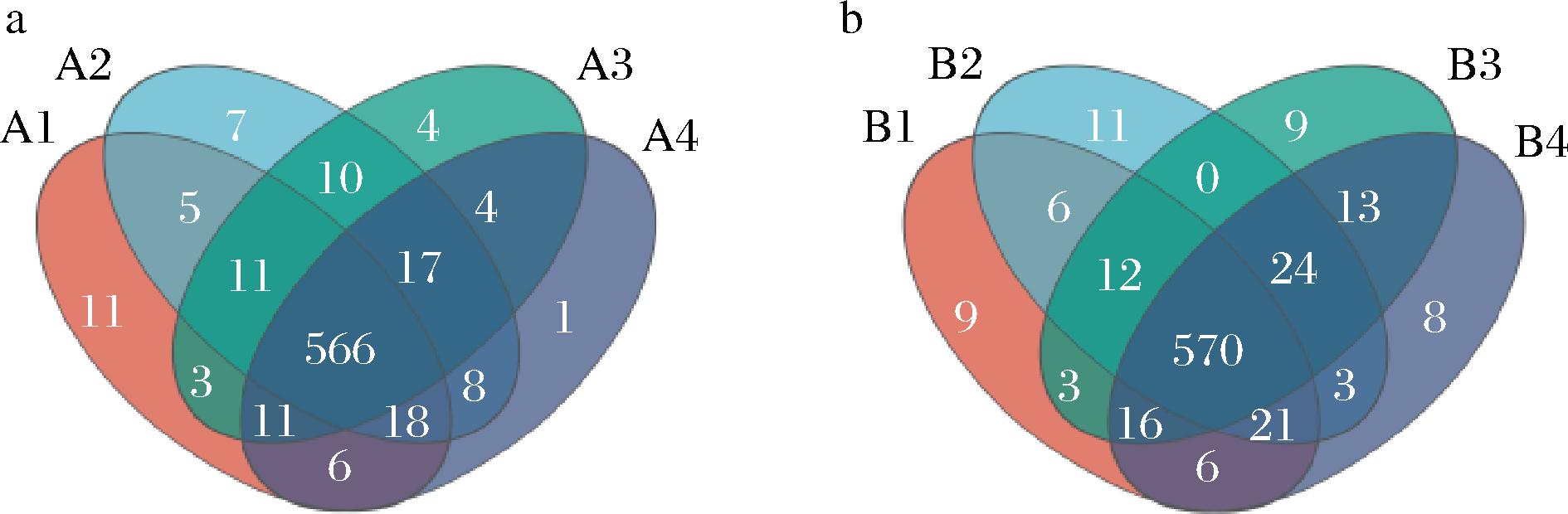
a-A样品的真菌群落Venn图;b-B样品的真菌群落Venn图
图5 真菌OTU数目Venn图
Fig.5 Venn diagram of OTU number of fungi
2.4.3 样品不同发酵阶段微生物群落分析
藏曲中主要由霉菌、酵母菌和细菌组成。因此微生物群落组成和代谢变化是发酵中重要的研究指标,能够直接反映产品的物质组成和感官质量。如图6-a所示,门水平中,从A、B样品发酵不同阶段共检测到2个细菌菌门,分别为厚壁菌门(Firmicutes)与变形菌门(Proteobacteria),厚壁菌门为样品中的优势菌门,在整个发酵阶段,其物种丰度不断增加占细菌群落相对丰度的98.3%成为第一优势菌门,变形菌门逐渐降低。厚壁菌门丰度的增高对驱动酒醅活性微生物群落变化起重要作用[21]。如图6-b所示,属水平中,A、B样品共检测到10个细菌属,分别为红蝽菌属(Coriobacteriaceae)、酒球菌属(Oencoccus)、代尔夫特菌属(Delftia)、链球菌属(Streptococcus)、芽孢杆菌属(Bacillus)、明串珠菌属(Leuconostoc)、乳酸杆菌属(Lactobacillus)、片球菌属(Pediococcus)、醋杆菌属(Acetobacter)、假单胞菌属(Pseudoalteromonas),这与孟凡冰等[22]在研究青稞酒曲微生物多样性中细菌菌属的一致性较高。在整个发酵阶段,乳酸杆菌属相对丰度不断增加,A样品从42.4%增至93.6%,B样品从25.6%增至62.7%,成为细菌群落的第一优势菌属,说明乳酸杆菌属在A、B样品发酵过程中起到主导作用,在发酵结束时,A样品乳酸杆菌属的相对丰度高于B样品,导致A样品乳酸酯类含量高于B样品。有研究学者发现,在发酵过程中乳酸菌属参与多种分解代谢活动,能够产生丰富的酯酶与脂肪酶[23],可以为青稞酒提供前体物质,提升青稞酒的醇厚感。片球菌属在A样品中,随着发酵时间的延长,呈现逐步下降的趋势,从46.4%降至5.1%。B样品在整个发酵阶段呈现小幅度的波动35.6%~40.4%,推测可能是制作青稞曲的环境与工艺不同影响了酒曲中初始微生物组成,且随着发酵的进行,发酵环境参数的变化也导致了部分细菌不耐受现有环境而进入衰亡期,从而产生群落丰度变化的差异[24]。B样品中片球菌属和醋酸杆菌属的相对丰度高于A样品,导致B样品脂肪酸酯类含量高于A样品,有报道称片球菌属与醋酸杆菌属产酸能力强,对脂肪酸产生协同作用,可进一步合成脂肪酸酯类[25-26]。
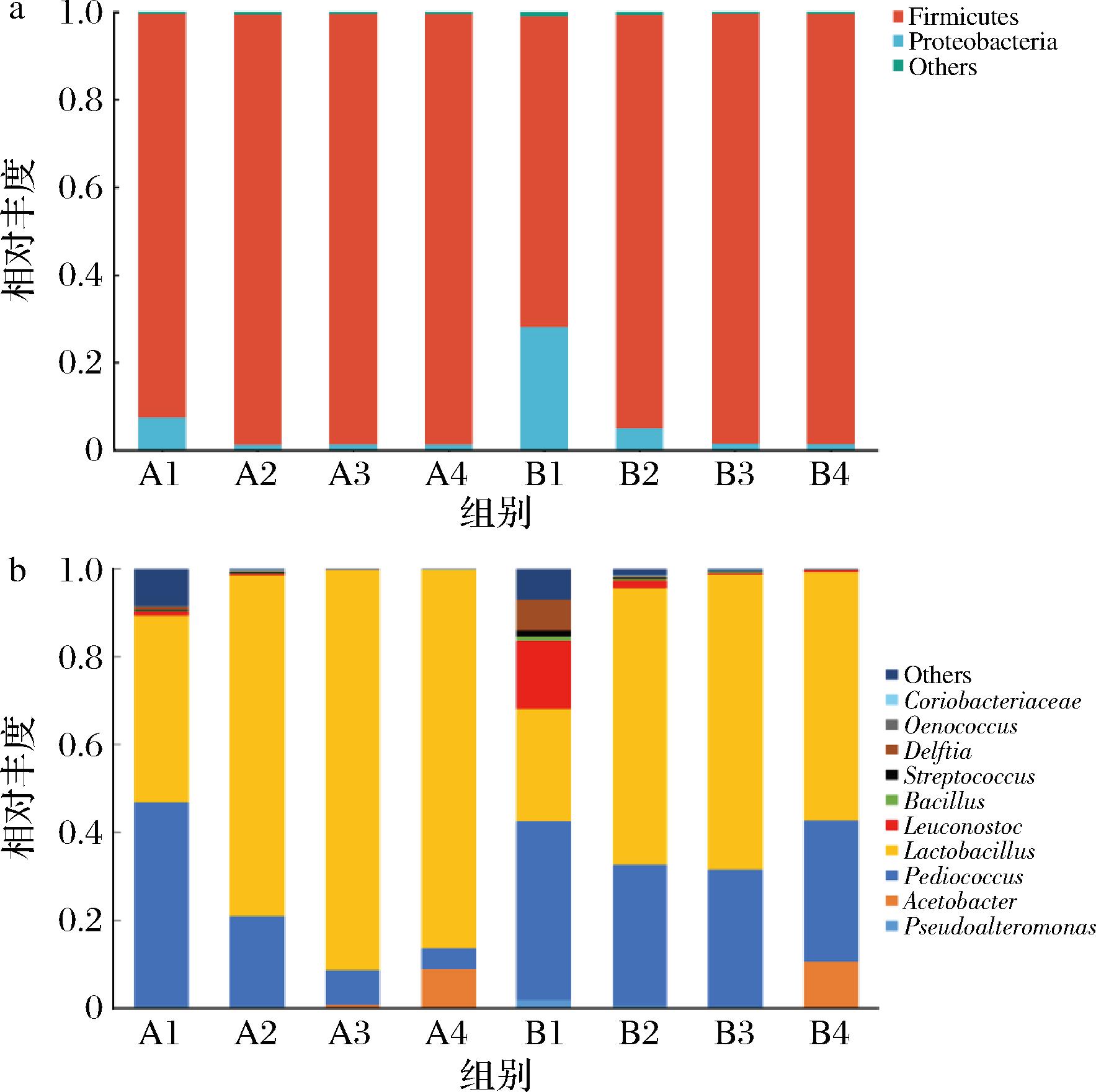
a-门水平;b-属水平
图6 细菌门水平和属水平微生物群落结构
Fig.6 Microorganism community structure at phyla level and genus level
注:Others(其他类相对含量<1%)。
如图7-a所示,在真菌门水平下A、B样品不同发酵阶段共检测到5个优势真菌门,分别为毛霉门(Mucoromycota)、子囊菌门(Ascomycota)、担子菌门(Basidiomycota)、链藻门(Streptophyta)、壶菌门(Chytridiomycota)。在整个发酵阶段主要优势菌门为毛霉门、子囊菌门,且A、B样品发酵初期毛霉门与子囊菌门的相对丰度分别为80%、85.5%与13.4%、18.3%,随着发酵时间的进行,子囊菌门相对丰度逐渐增加,在发酵后期与毛霉门的相对丰度持平,造成此差异的原因可能是由于发酵后期样品中酒精含量的增加,部分适应环境的真菌开始缓慢生长,渐趋稳定。如图7-b所示,共检测到21个真菌属,分别为根霉属(Rhizopus)、须眉属(Phycomyces)、克鲁维酵母属(Kluyveromyces)、毕赤酵母属(Pichia)、威克汉姆酵母属(Wickerhamomyces)、汉逊酵母属(Hanseniaspora)、管囊酵母属(Pachysolen)、德巴利酵母属(Debaryomyces)、法夫驹形氏酵母属(Komagataella)、犁头霉属(Absidia)、生丝毕赤酵母属(Hyphopichia)、毛霉属(Mucor)、Cyberlindnera、米勒酵母属(Millerozyma)、复膜孢酵母属(Saccharomycopsis)、假丝酵母属(Candida)、耶氏酵母属(Yarrowia)、酵母属(Saccharomyces)、树干毕赤酵母属(Scheffersomyces)、洛德酵母属(Lodderomyces)。在A、B样品的整个发酵阶段,根霉属的相对丰度随着发酵进行在逐步降低,但其相对丰度的平均占比保持在50%左右,成为第一优势菌属。根霉属主要产糖化酶,将青稞中的淀粉分解转化成可利用的糖类,能够提高A、B样品的出酒率。威克汉姆酵母属为第二优势菌属,A样品在发酵初期相对丰度占比2%,发酵中后期迅速生长,其相对丰度占比高达20%,B样品在整个发酵阶段也呈递增的状态由3%增至10%。在发酵结束时,A样品威克汉姆酵母属、毕赤酵母属等常见产酯酵母属的相对丰度含量高于B样品,导致A样品酯类物质含量高于B样品。同时,A样品酵母属的相对丰度高于B样品,因此A样品酒精度高于B样品,从整体来看,也解释了上文中青稞酒酯类物质含量A样品高于B样品的原因。有研究表明,该酵母可促进酒类酿造过程中酯类的合成,尤其是己酸乙酯、乙酸乙酯等酒中重要的酯类物质,改善原酒品质[27],A、B样品虽然其相对丰度有所差异,但两者都含有威克汉姆酵母属,也解释了前文中主要风味物质呈现一致性的原因。富志磊等[28]通过模拟白酒固态发酵方法,发现以10%的接种量能明显提高乙酸乙酯含量,显著增加白酒中酯类等风味化合物,改善白酒品质。毕赤酵母属为第三优势酵母属,王倩倩等[29]通过较高比例接种发酵毕赤酵母显著提高了干白葡萄酒的品种香气成分与发酵香气成分的含量。可见,在A、B样品的发酵过程中非酿酒酵母属具有较强的产酯产香能力,其群落结构的丰富与复杂度,有利于青稞酒风味物质的增加。
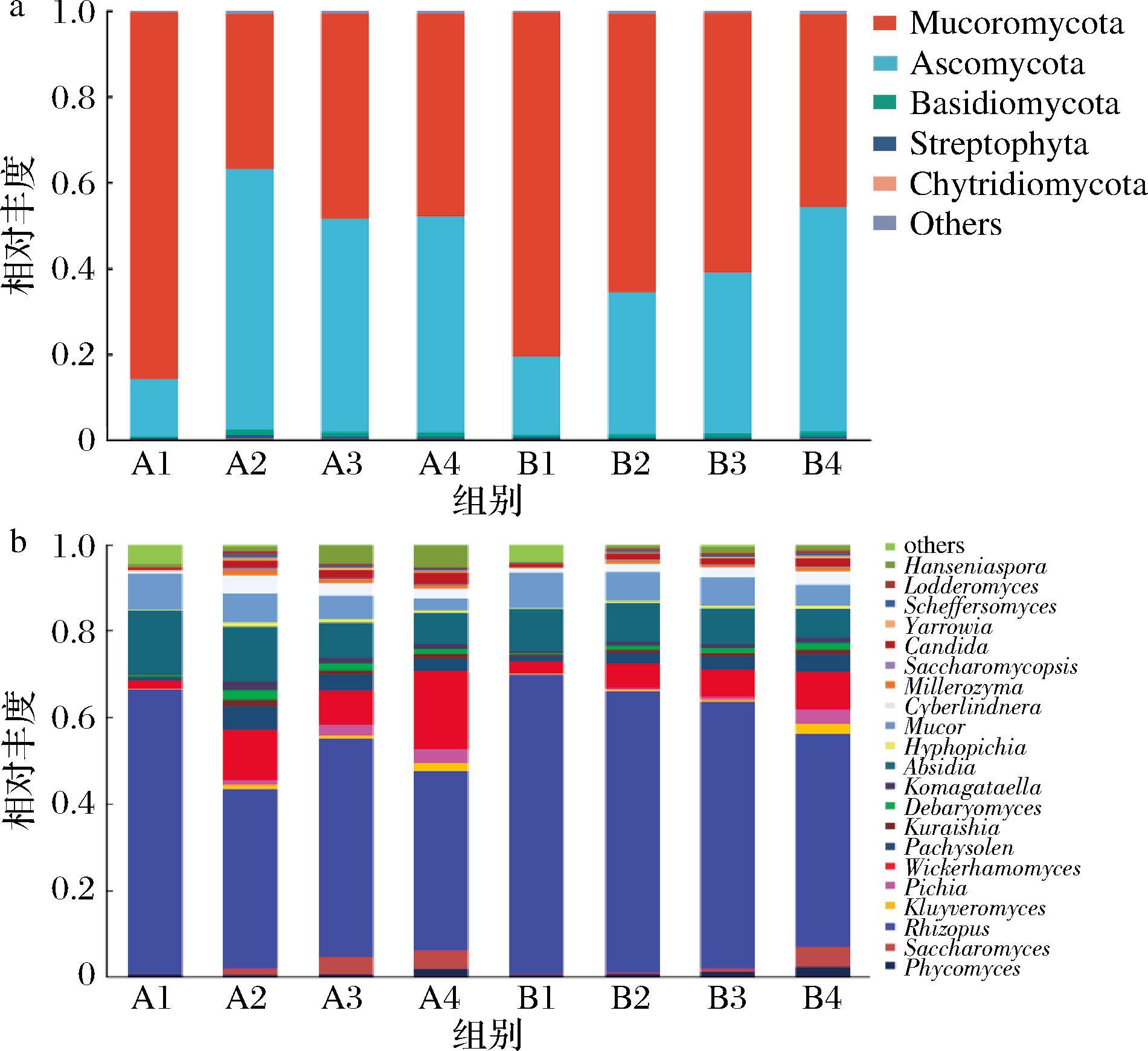
a-门水平;b-属水平
图7 真菌门水平属水平微生物群落结构
Fig.7 Microbial community structure at the level of phyla and genus
2.4.4 微生物群落主坐标分析
对不同发酵时间阶段青稞酒细菌、真菌微生物群落进行主坐标分析(principal co-ordinates analysis,PCoA)。由图8-a可知,PC1与PC2的方差贡献率分别为73.6%和17.55%,两个主成分共解释了91.15%的变量,表明这两个主成分可代表细菌群落结构的相似度。A2、B3、B4在第一象限,距离结构较近,说明A样品在发酵中期与B样品发酵后期及青稞酒成品的细菌群落结构相似度高。A1、B2在第二象限,A3、A4在第三象限。B1单独在第四象限,与其他样品发酵阶段距离较远,菌群结构相似度较低,说明B样品在发酵初期的细菌群落结构与青稞曲的添加有关,不同地区制作的青稞曲,受环境与工艺的影响,其微生物结构也不一。
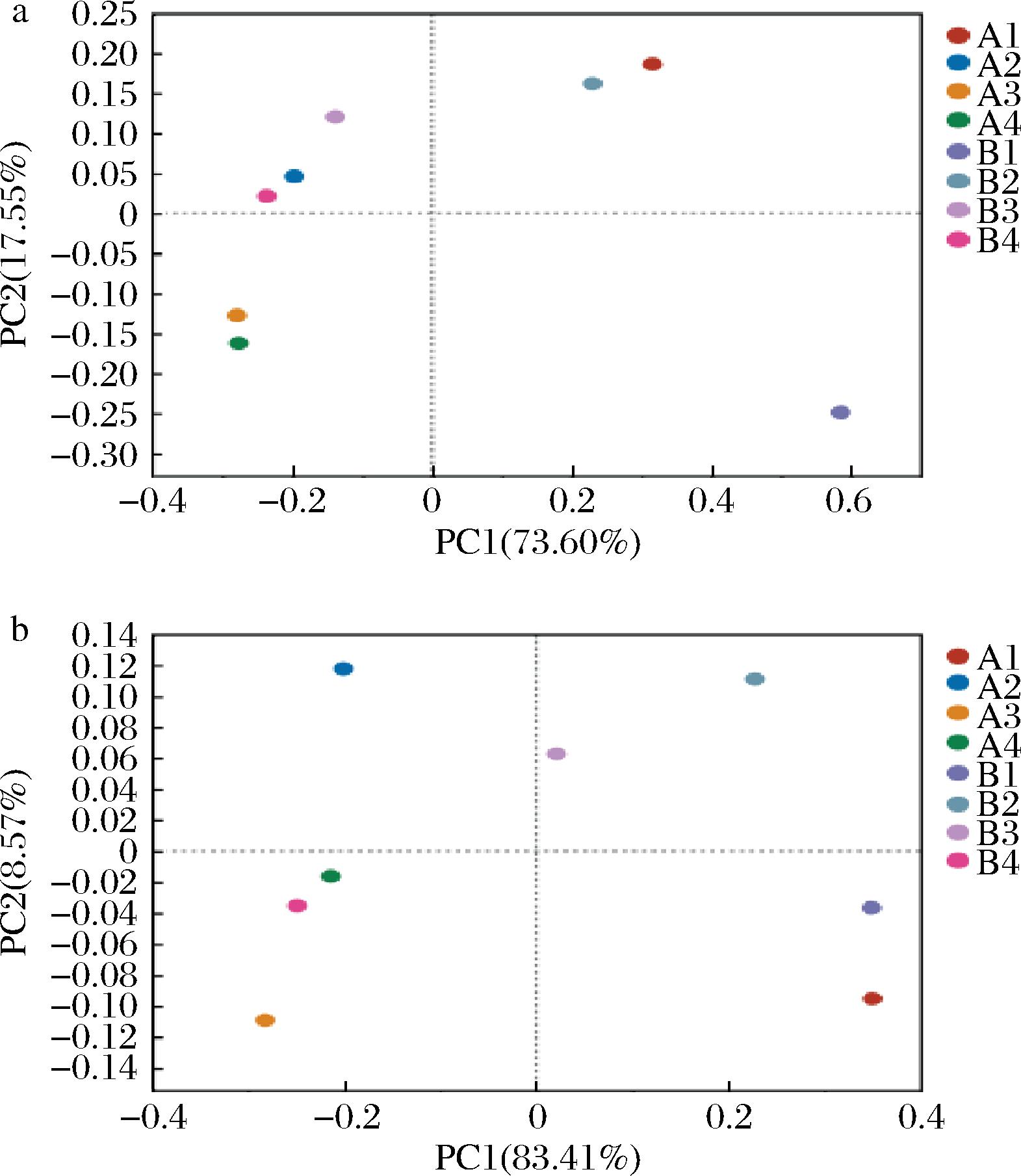
a-细菌;b-真菌
图8 细菌和真菌PCoA分析图
Fig.8 PCoA analysis diagram of bacteria and fungi
由图8-b可知,PC1与PC2的方差贡献率分别为83.41%和8.57%,两个主成分共解释了91.98%的变量,表明这两个主成分可代表真菌群落结构的相似度。A2单独在第一象限,与其他样品发酵阶段距离较远,说明A样品在发酵中期时真菌群落结构与其他发酵时期的群落结构相似度较低,具有显著差异,原因是A、B酒曲分别来自西藏不同地区的小曲,这两个区域海拔高度不同,因此小曲中微生物种类存在差异。传统青稞酒发酵时间比较短,发酵初期是固态糖化阶段,发酵中期添加了一定量的水分,呈现为固液结合的边糖化、边发酵阶段,由于发酵基质状态的变化,对发酵液中微生物的影响也存在差异,因此导致群落结构的变化。
A1、B1在第四象限,B2、B3在第二象限,A3、A4、B4在第三象限,且A4与B4位置集中,距离结构较近,表明A样品和B样品在成酒阶段的群落结构相似度较高,说明了随着样品发酵的进行,pH与总糖降低、酒精度升高,这些因素均抑制了大多数酿酒酵母和非酿酒酵母的繁殖,而只有少数细菌可在此环境下生长,如耐受性较强的醋酸菌、乳酸菌等,因此在发酵末期两个样品的菌群结构比较类似,使得最初藏曲中微生物群落结构发生了结构性演替[30]。
2.5 KEGG代谢通路基因分析
为了分析青稞酒中微生物的代谢潜力,对823 072个非冗余基因进行KEGG数据库基因功能注释。在KEGG通路水平1中显示,代谢的基因数最多,然而环境信息过程基因数最少,具体如图9和图10所示。从A和B这两种藏曲样品分析,在KEGG水平2中,全局和概述图谱(global and overview maps)、碳水化合物代谢(carbohydrate metabolism)、信号传导(signal transduction)、能量代谢(energy metabolism)和氨基酸代谢(amino acid metabolism)的相对丰度处于高水平,这与白酒酒曲研究结果相一致[31]。A样品中碳水化合物代谢和氨基酸代谢的丰度高于B样品,但是A样品两个代谢丰度在发酵过程中呈现下降趋势,B样品则相反,因此在相同的条件下,推测发酵结束后A样品的蛋白质和碳水化合物含量会高于B样品,这也是两种不同小曲酿造的青稞酒风味化合物差异的原因所在[32]。
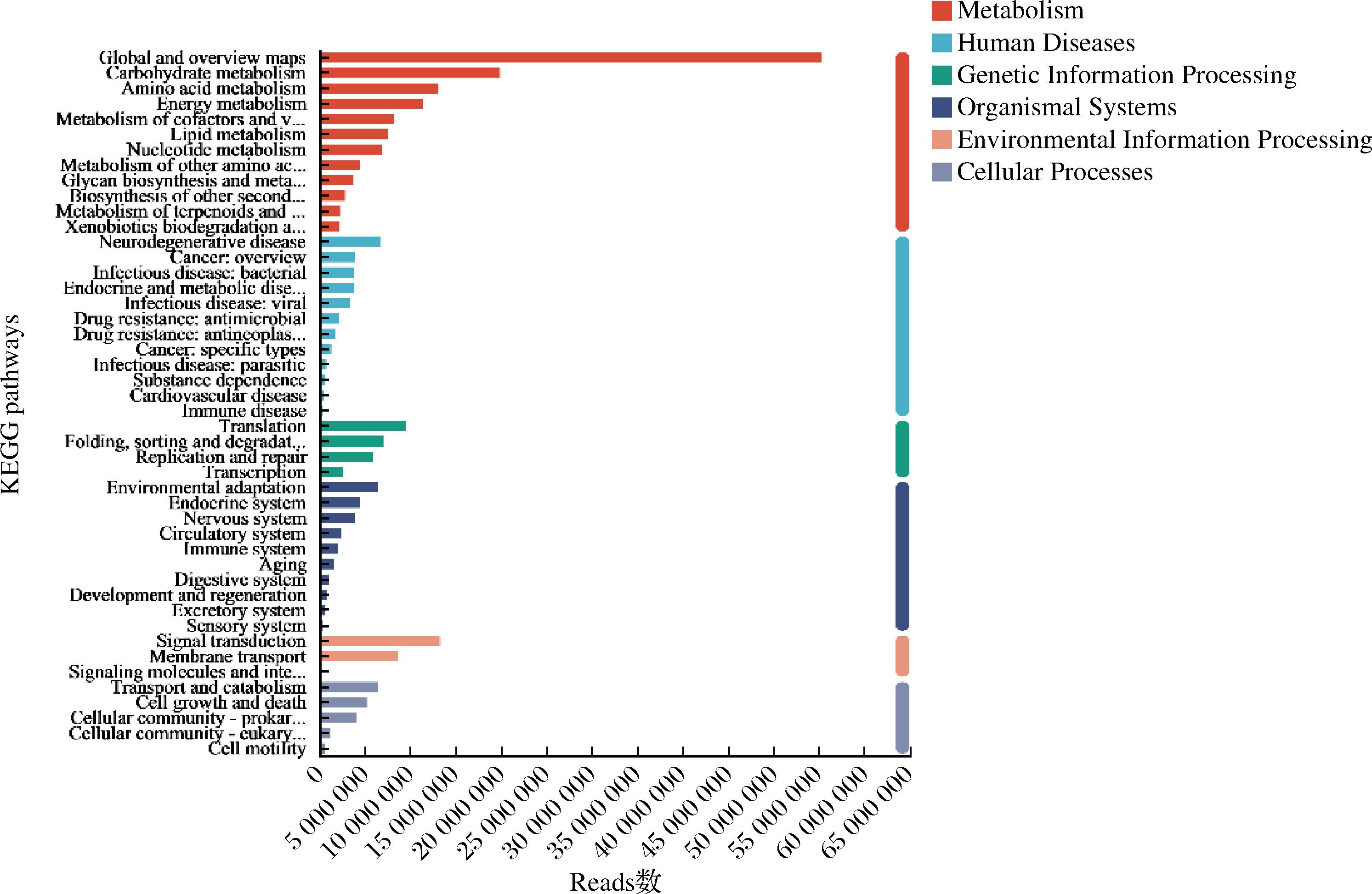
图9 不同发酵阶段青稞酒样品的KEGG通路水平1功能注释
Fig.9 Functional annotation of KEGG pathway Level 1 in highland barley wine samples at different fermentation stages

图10 不同发酵阶段青稞酒样品的KEGG通路水平2功能注释丰度
Fig.10 KEGG channel level 2 functional annotation abundance of highland barley wine samples at different fermentation stages
2.6 青稞酒挥发性风味物质的关联性分析
根据KEGG数据库水平2预测得出,在相对丰度处于前10的代谢通路中,贡献度前5的微生物依次有乳酸杆菌、根霉属、片球菌属、酵母属、毕赤属。结合图10,从整体看乳酸杆菌对水平2代谢贡献度最大,其中,膜转运(membrane transport)丰度最大,辅因子和维生素代谢(metabolism of cofactors and vitamins)、碳水化合物代谢、氨基酸代谢次之。片球菌属丰度较大的是膜转运、辅因子和维生素代谢。酵母菌属丰度较大的是翻译(translation)、碳水化合物代谢、折叠、分类和降解(folding, sorting and degradation),具体分析如图11所示。

图11 不同发酵阶段青稞酒样品的KEGG通路水平3与功能微生物关联度
Fig.11 Correlation between KEGG pathway level 3 and functional microorganisms in different fermentation stages of highland barley wine samples
碳水化合物代谢路径中的糖酵解和糖异生途径、磷酸戊糖途径和三羧酸循环,构成了中枢代谢路径,碳源主要包含葡萄糖、果糖、麦芽糖、蔗糖、淀粉、海藻糖、甘露糖和核糖。微生物可以通过淀粉和蔗糖代谢途径,将淀粉和蔗糖降解为葡萄糖和果糖,再进入糖酵解途径,生成风味的重要前体物质丙酮酸和乙酰辅酶A[33]。根据图11可看出,藏曲微生物代谢路径的丰度存在差异,根霉、毛霉和曲霉的葡萄糖淀粉酶和淀粉酶可以将淀粉代谢为葡萄糖。酵母菌属和毕赤酵母属、异常威克酵母属等非酿酒酵母,在酿造过程中分别产生酒精和香气物质。
丙酮酸代谢支路一通过丙酮酸脱羧酶生成乙醛,其次,一方面通过乙醇脱氢酶生成乙醇;另一方面通过乙醛脱氢酶生成乙酸,再利用乙酰辅酶A合酶生成重要的中间产物-乙酰辅酶A。微生物在胞内通过乙酰辅酶A和乙醇(高级醇)在乙醇酰基转移酶催化下生成乙酸乙酯、乙酸异戊酯、乙酸苯乙酯等乙酸酯类,另一方面,短-中链脂肪酸乙酯是乙酰辅酶A家族(如酰基辅酶A)和乙醇在醇酰基转移酶催化下合成[34]。在第4阶段,A样品中生成乙酰辅酶A的三类酶丰度高于B样品,与上文A样品中乙酸乙酯等乙酸酯类含量高于B样品的结果相一致。在第3,4阶段,B样品的乙酰辅酶A羧化酶和脂肪酸合成酶等脂肪酸合成中关键酶丰度呈现上升趋势,进一步促进脂肪酸乙酯的合成,A样品则呈现趋势。这一结果与上文B样品中己酸乙酯等中长链脂肪酸乙酯含量高于A样品相一致。
丙酮酸代谢重要产物-乙酰辅酶A,它参与三羧酸循环,产生柠檬酸、2-酮戊二酸、琥珀酸、延胡索酸、苹果酸和草酰乙酸,进一步转化成谷氨酸、精氨酸、脯氨酸、鸟氨酸和赖氨酸。青稞酒发酵过程中香气的形成与氨基酸代谢密切相关,支链氨基酸(缬氨酸、亮氨酸和异亮氨酸)的生物合成并通过Ehrlich途径调控高级醇的生成。首先,氨基酸在转氨酶作用下,生成α-酮酸,然后α-酮酸脱羧形成相应的杂醇醛,最后通过醇脱氢酶生成相应的高级醇[35]。本次研究显示,在1阶段,出现的高级醇类有正丙醇、异丁醇、异戊醇和β-苯乙醇。据研究报道,葡萄酒主要是在发酵过程中期进行氨基酸代谢,而青稞酒是在发酵前期,已经发生氨基酸代谢[36],可能原因是青稞酒发酵中存在根霉属、毛霉属等均具有较高的蛋白酶活性,蛋白酶将原料中的蛋白质分解为氨基酸,氨基酸可进一步被酵母菌代谢,形成酒中高级醇或酯[37]。在4阶段,高级醇类的种类增加,依次有甲醇、活性戊醇、1,3-丁二醇、2,3-丁二醇和丙二醇,说明发酵过程中不同微生物能够进行多种氨基酸代谢,可能是乳酸杆菌属、片球菌属和毕赤酵母属在碳水化合物代谢中进行氨基酸合成。
由图12可知,共有10种细菌菌属、10种真菌菌属与13种酯类、15种醇类、2种醛类、2种酮类、2种酚类、1种吡嗪类,共计35种香气物质存在较强相关性。其中乳酸杆菌属、片球菌属、醋酸杆菌属、毕赤属、根霉属、威克汉姆酵母属与乙酸乙酯、已酸异戊酯、乙酸苯乙酯、己酸乙酯、乳酸乙酯、正丙醇、正丁醇、4-乙基愈创木酚、4-甲基愈创木酚、四甲基吡嗪等挥发性风味物质存在较强的正相关,说明这5种菌属对上述香气物质的贡献度较大;片球菌属、芽孢杆菌属、Deftia、德巴利酵母属与乙酸苯乙酯、异戊醇、异丁醇、β-苯乙醇等挥发性风味物质存在负相关,说明这4种菌属对上述香气物质的积累具有一定的负面影响。综上所述,在青稞酒发酵过程中乳酸杆菌属、醋酸杆菌属、毕赤属、根霉属、威克汉姆酵母属可能对青稞酒的挥发性风味物质产生重要影响,最终影响产品品质。

a-细菌与青稞酒香气物质相关性分析热图;b-真菌与青稞酒香气物质相关性分析热图
图12 细菌、真菌与青稞酒香气物质相关性分析热图
Fig.12 Heatmap of correlation analysis between microorganism of barley koji and aroma substances of barley wine
3 结论
本次研究通过宏基因组分析了青稞酒在不同发酵阶段中,微生物多样性及风味物质的变化规律,进一步揭示了微生物群落结构的变化与多样性、优势微生物与风味物质形成的贡献度。在整个发酵阶段,A、B样品整个微生物群落结构在发酵初期呈现显著差异,随着后期发酵的进行整体群落结构呈现一定的相似性。在发酵过程中2个细菌门、5个真菌门与10个细菌属、21个真菌属(相对丰度>1%)占据优势,A、B样品在细菌群落结构门水平中,厚壁菌门为第一优势菌门;属水平中,乳酸杆菌属为第一优势菌属。真菌群落结构门水平中毛霉门、子囊菌门为主要优势菌门;属水平中,根霉属、威克汉姆酵母属、发酵毕赤酵母属为主要优势菌属,影响主要风味物质的形成。研究表明,核心微生物的组成可以驱动整个发酵过程的进行,对维持发酵系统的稳定性以及产品的风味与品质起着重要作用[38]。同时得出不同微生物参与底物的代谢网络和风味形成存在差异,A样品中乙酸乙酯、乙酸异戊酯和乙酸苯乙酯等乙酸酯类含量和乳酸乙酯、乳酸异戊酯等乳酸酯类含量高于B样品,可能原因是在第4阶段发酵结束时,A样品中威克汉姆酵母属、汉逊酵母属、毕赤酵母属和假丝酵母属等常见产酯酵母属与乳酸杆菌属的相对丰度高于B样品。B样品中己酸乙酯、辛酸乙酯、癸酸乙酯、油酸乙酯和棕榈酸乙酯等含量高,是由于B样品的乙酰辅酶A羧化酶和脂肪酸合成酶等脂肪酸合成中关键酶丰度呈现上升趋势,进一步促进脂肪酸乙酯的合成。另外,以酵母菌属和乳酸杆菌属为主在启动糖酵解和丙酮酸代谢过程中,会产生两种重要的中间物质分别是丙酮酸与乙酰辅酶A,为下一步进入丙酮酸代谢、三羧酸循环、脂肪酸代谢和氨基酸代谢以及最终完成风味物质的形成提供必要条件。因此,确定优势菌及其碳水化合物代谢和氨基酸代谢可为青稞酒风味物质的形成提供重要的物质基础,有助于改善青稞酒的发酵工艺,对提高青稞酒的质量有重要意义。
[1] 卢灏泽, 杨帆, 贾福晨, 等.西藏传统青稞酒的相关研究及前景分析[J].轻工科技, 2021, 37(5):19-21.LU H Z, YANG F, JIA F C, et al.Research and prospect analysis of traditional highland barley wine in Tibet[J].Light Industry Science and Technology, 2021, 37(5):19-21.
[2] 焦兴弘. 舟曲青稞酒的营养价值及保健功能[J].食品安全导刊, 2020(12):95.JIAO X H.Nutritional value and health function of Zhouqu Qingke wine[J].China Food Safety Magazine, 2020(12):95.
[3] 陈占秀, 李善文, 黄和强, 等.高原青稞酒的功能性酿造微生物及代谢产物研究[J].酿酒科技, 2022(11):72-81.CHEN Z X, LI S W, HUANG H Q, et al.Study on functional microorganisms and their metabolites in highland barley Baijiu[J].Liquor-Making Science &Technology, 2022(11):72-81.
[4] GODILLOT J, SANCHEZ I, PEREZ M, et al.The timing of nitrogen addition impacts yeast genes expression and the production of aroma compounds during wine fermentation[J].Frontiers in Microbiology, 2022, 13:829786.
[5] MA W R, GENG X J, JIA F C, et al.Investigation of microbial composition and functional characterization of Zangqu using high throughput sequencing[J].LWT, 2021, 136:110342.
[6] 古兴波, 胡小霞, 左乾程, 等.宏基因组学在白酒酿造领域中的研究及应用[J].酿酒科技, 2020(6):17-25; 36.GU X B, HU X X, ZUO Q C, et al.Research and application of metagenomics in Baijiu production[J].Liquor-Making Science &Technology, 2020(6):17-25; 36.
[7] 侯强川, 王玉荣, 田龙新, 等.基于宏基因组测序技术解析市售强化酒曲微生物群落结构和功能特征[J].食品与发酵工业, 2023, 49(10):100-107.HOU Q C, WANG Y R, TIAN L X, et al.Microbial community structure and functional characteristics of commercial intensified Jiuqu based on metagenomic sequencing technology[J].Food and Fermentation Industries, 2023, 49(10):100-107.
[8] 麻颖垚. 宏基因组学对酱香型白酒第四轮次窖内发酵微生物代谢通路的研究[D].贵阳:贵州大学, 2020.MA Y Y.Study on the metabolic pathway of microorganism in the fourth round pit fermentation of Maotai-flavor liquor by metagenomics[D].Guiyang:Guizhou University, 2020.
[9] 王雪薇, 江伟, 孙志伟, 等.藏区传统青稞发酵酒的风味特征剖析[J].食品与发酵工业, 2018, 44(11):286-291.WANG X W, JIANG W, SUN Z W, et al.Analysis of flavor characteristics of traditional highland barley in Tibetan area[J].Food and Fermentation Industries, 2018, 44(11):286-291
[10] CHEN S F, ZHOU Y Q, CHEN Y R, et al.Fastp:An ultra-fast all-in-one FASTQ preprocessor[J].Bioinformatics, 2018, 34(17):i884-i890.
[11] LI D H, LIU C M, LUO R B, et al.MEGAHIT:An ultra-fast single-node solution for large and complex metagenomics assembly via succinct de Bruijn graph[J].Bioinformatics, 2015, 31(10):1674-1676.
[12] NOGUCHI H, PARK J, TAKAGI T.MetaGene:Prokaryotic gene finding from environmental genome shotgun sequences[J].Nucleic Acids Research, 2006, 34(19):5623-5630.
[13] BUCHFINK B, XIE C, HUSON D H.Fast and sensitive protein alignment using DIAMOND[J].Nature Methods, 2015, 12(1):59-60.
[14] 侯若婷, 赵鹏, 徐馨莹, 等.德尔布有孢圆酵母与四种酿酒酵母顺序发酵对草莓酒香气与感官喜好性的影响[J].食品与发酵工业, 2024, 50(14):165-172.HOU R T,ZHAO P,XU X Y, et al.Effect of sequential fermentation with Torulaspora delbrueckii and four Saccharomyces cerevisiaes on volatile aromatic compounds and sensory preferences of strawberry wines[J].Food and Fermentation Industries, 2024, 50(14):165-172.
[15] 孔彩琳, 许引虎, 黄杰, 等.酿酒酵母多糖对葡萄酒果香酯类物质水解呈香的表观基质效应[J].中国农业科学, 2023, 56(6):1168-1176.KONG C L, XU Y H, HUANG J, et al.Apparent matrix effect of yeast polysaccharides from S.cerevisiae on the hydrolysis of wine fruity esters[J].Scientia Agricultura Sinica, 2023, 56(6):1168-1176.
[16] 龚小会, 张东亚, 谢玲, 等.米酒微生物与其风味品质形成关系研究进展[J].食品科学, 2024, 45(16):358-366.GONG X H, ZHANG D Y, XIE L, et al.Research progress on the relationship between microbial community and flavor quality formation in rice wine[J].Food Science, 2024, 45(16):358-366.
[17] 陈子凡, 成莲, 曾石峭.气相色谱-质谱法快速测定客家黄酒中的醇类物质[J].化学分析计量, 2019, 28(4):57-60.CHEN Z F, CHENG L, ZENG S Q.Rapid determination of alcohols in Hakka rice wine by gas chromatography-mass spectrometry[J].Chemical Analysis and Meterage, 2019, 28(4):57-60.
[18] 孙啸涛, 王宗元, 刘淼, 等.涡旋辅助液液微萃取结合GC-MS法检测67种白酒中四甲基吡嗪、4-甲基愈创木酚和4-乙基愈创木酚[J].食品科学, 2017, 38(18):73-79.SUN X T, WANG Z Y, LIU M, et al.Determination of tetramethylpyrazine-4-methyl guaiacol and 4-methyl guaiacol in 67 Chinese Baijiu samples by Vortex assisted liquid-liquid microextration combined with gas chromatography-mass spectrometry[J].Food Science, 2017, 38(18):73-79.
[19] 张咚咚, 赵金凤, 谢思源, 等.基于高通量测序的玉米中微生物多样性分析[J].中国食品学报, 2023, 23(10):305-314.ZHANG D D, ZHAO J F, XIE S Y, et al.Analysis of microbial diversity in maize based on high throughput sequencing[J].Journal of Chinese Institute of Food Science and Technology, 2023, 23(10):305-314.
[20] 张隋鑫, 陈腊梅, 王宇, 等.基于高通量基因测序分析火锅蘸料原料微生物多样性[J].食品工业, 2023, 44(6):113-118.ZHANG S X, CHEN L M, WANG Y, et al.Analysis of microbial diversity of hot pot dipping materials based on high-throughput sequencing[J].The Food Industry, 2023, 44(6):113-118.
[21] 王康丽. 基于宏转录组学的浓香型酒醅微生物群落多样性及代谢特征研究[D].郑州:郑州轻工业大学, 2021.WANG K L.Study of the diversity and metabolic characteristics of microbial community harbored in fermented grains for the Chinese strong-flavor Baijiu production based on metatranscriptome[D].Zhengzhou:Zhengzhou University of Light Industry, 2021.
[22] 孟凡冰, 付郑旭, 李云成, 等.青稞酒曲微生物多样性分析及低温耐盐乳酸菌的分离鉴定[J].成都大学学报(自然科学版), 2022, 41(4):361-367, 372.MENG F B, FU Z X, LI Y C, et al.Analysis of microbial diversity and isolation of low temperature and salt tolerant lactic acid bacteria from highland barley koji[J].Journal of Chengdu University (Natural Science Edition), 2022, 41(4):361-367, 372.
[23] SONG Z Y, HU Y Z, CHEN X, et al.Correlation between bacterial community succession and propionic acid during gray sufu fermentation[J].Food Chemistry, 2021, 353:129447.
[24] 苏泽佳, 熊若冰, 梁景龙, 等.豉香型白酒微生物的研究进展[J].现代食品科技, 2024, 40(1):319-324.SU Z J, XIONG R B, LIANG J L, et al.Research progress on microorganisms in Chi-flavored Baijiu[J].Modern Food Science &Technology, 2024, 40(1):319-324.
[25] BALAKRISHNAN G, AGRAWAL R.Antioxidant activity and fatty acid profile of fermented milk prepared by Pediococcus pentosaceus[J].Journal of Food Science and Technology, 2014, 51(12):4138-4142.
[26] YIN H S, ZHANG R K, XIA M L, et al.Effect of aspartic acid and glutamate on metabolism and acid stress resistance of Acetobacter pasteurianus[J].Microbial Cell Factories, 2017, 16(1):109.
[27] 石馨, 惠明, 田青, 等.异常威克汉姆酵母Y-1对模拟固态发酵白酒酒醅理化指标及风味的影响[J].中国酿造, 2022, 41(9):31-36.SHI X, HUI M, TIAN Q, et al.Effects of Wickerhamomyces anomalus Y-1 on physicochemical parameters and flavor of Baijiu fermented grains with simulated solid-state fermentation[J].China Brewing, 2022, 41(9):31-36.
[28] 富志磊, 马景浩, 周泉宇, 等.模拟白酒固态发酵中异常威克汉姆酵母的提酯增香作用[J].中国食品学报, 2023, 23(5):175-183.FU Z L, MA J H, ZHOU Q Y, et al.Effect of Wickerhamomyces anomalus on increasing ester compounds and aroma in simulated solid-state fermentation for Baijiu production[J].Journal of Chinese Institute of Food Science and Technology, 2023, 23(5):175-183.
[29] 王倩倩, 覃杰, 马得草, 等.优选发酵毕赤酵母与酿酒酵母混合发酵增香酿造爱格丽干白葡萄酒[J].中国农业科学, 2018, 51(11):2178-2192.WANG Q Q, QIN J, MA D C, et al.Aroma enhancement of ecolly dry white wine by co-inoculation of selected Pichia fermentans and Saccharomyces cerevisiae[J].Scientia Agricultura Sinica, 2018, 51(11):2178-2192.
[30] 张二豪, 奉综涛, 何萍, 等.西藏地区青稞酒曲微生物群落结构及多样性分析[J].中国食品学报, 2024, 24(5):381-392.ZHANG E H, FENG Z T, HE P, et al.Tibetan areas chang qu microbial community structure and diversity analysis[J].Chinese Journal of Food, 2024, 24(5):381-392.
[31] ZHU C T, CHENG Y X, SHI Q L, et al.Metagenomic analyses reveal microbial communities and functional differences between Daqu from seven provinces[J].Food Research International, 2023, 172:113076.
[32] LIU S P, CHEN Q L, ZOU H J, et al.A metagenomic analysis of the relationship between microorganisms and flavor development in Shaoxing mechanized Huangjiu fermentation mashes[J].International Journal of Food Microbiology, 2019, 303:9-18.
[33] KRIVORUCHKO A, ZHANG Y M, SIEWERS V, et al.Microbial acetyl-CoA metabolism and metabolic engineering[J].Metabolic Engineering, 2015, 28:28-42.
[34] LIU G F, HUANG L, LIAN J Z.Alcohol acyltransferases for the biosynthesis of esters[J].Biotechnology for Biofuels and Bioproducts, 2023, 16(1):93.
[35] CORDENTE A G, SCHMIDT S, BELTRAN G, et al.Harnessing yeast metabolism of aromatic amino acids for fermented beverage bioflavouring and bioproduction[J].Applied Microbiology and Biotechnology, 2019, 103(11):4325-4336.
[36] CRÉPIN L, TRUONG N M, BLOEM A, et al.Management of multiple nitrogen sources during wine fermentation by Saccharomyces cerevisiae[J].Applied and Environmental Microbiology, 2017, 83(5):e02617-16.
[37] YAO D, XU L, WU M N, et al.Microbial community succession and metabolite changes during fermentation of BS sufu, the fermented black soybean curd by Rhizopus microsporus, Rhizopus oryzae, and Actinomucor elegans[J].Frontiers in Microbiology, 2021, 12:665826.
[38] XU Y Q, WU M Q, ZHAO D, et al.Simulated fermentation of strong-flavor Baijiu through functional microbial combination to realize the stable synthesis of important flavor chemicals[J].Foods, 2023, 12(3):644.