鲜切菠萝由于切割处理破坏了组织结构完整性,加速细胞老化,引发一系列的生理代谢反应,如褐变、软化、变味等。同时果肉表面丰富的营养物质为微生物提供了良好的生长环境,导致鲜切菠萝的营养损失、品质下降和货架期缩短[1-2]。鲜切菠萝保鲜与果实内部的生理反应和外部的包装贮藏条件均相关。如何保持品质、延长货架期是鲜切菠萝保鲜技术亟待解决的问题[3]。
果蔬品质损失主要由于氧气和水蒸气在包装内外的持续变化,包装的结构及尺寸均会影响阻隔性能,通过改变渗透分子的扩散长度和曲折路径来改变其扩散率[4]。有研究把食品根据水分活度分为了Aw<0.6、Aw>0.9以及新鲜食品,并对各类食品贮藏的适宜包装阻隔性进行了统计[5]。通过结合强阻气性的尼龙和高阻湿性的聚乙烯,有效减缓了鲜切莴笋的水分、褐变和维生素C含量的下降,抑制了微生物的生长[6]。BEN TEZ等[7]发现低渗透性的可食性涂膜延缓了鲜切菠萝维生素C的降解,维持了较好的品质。此外,鲜切果蔬的风味化合物会受氧含量的影响,高阻隔性包装虽然对果蔬的呼吸速率、褐变和硬度等具有一定的效果,但会抑制风味化合物的合成[8],如低氧条件下降低了苹果中挥发性酯类的合成[9],由此表明适宜的包装阻隔性能有效地保持果蔬的风味和品质,延长货架期。由于鲜切菠萝具有采后呼吸作用,针对包装的不同阻隔性能,其保鲜效果不同。
TEZ等[7]发现低渗透性的可食性涂膜延缓了鲜切菠萝维生素C的降解,维持了较好的品质。此外,鲜切果蔬的风味化合物会受氧含量的影响,高阻隔性包装虽然对果蔬的呼吸速率、褐变和硬度等具有一定的效果,但会抑制风味化合物的合成[8],如低氧条件下降低了苹果中挥发性酯类的合成[9],由此表明适宜的包装阻隔性能有效地保持果蔬的风味和品质,延长货架期。由于鲜切菠萝具有采后呼吸作用,针对包装的不同阻隔性能,其保鲜效果不同。
本研究分析了包装阻隔性对鲜切菠萝在贮藏期间理化性质的影响,并采用顶空固相微萃取-气相色谱质谱联用仪(headspace solid phase microextraction-gas chromatography-mass spectrometry,HS-SPME-GC-MS)对挥发性化合物进行鉴定,气味阈值(odor threshold,OT)和气味活性值(odor active value,OAV)用于分析鲜切菠萝的特征风味物质并研究其在不同阻隔性包装内的浓度变化规律,为适宜鲜切菠萝保鲜的包装阻隔性选择提供理论依据和为消费者的使用提供借鉴。
1 材料和方法
1.1 材料与试剂
‘巴厘’品种菠萝(Ananas comosus (L.) Merr.),摘自广东湛江市徐闻县,泡沫箱装好后当天运至实验室,于次日进行保鲜实验。
草酸、NaHCO3、2,6-二氯靛酚、福林酚,上海源叶生物科技有限公司;1 mg/mL抗坏血酸(ascorbic acid,AA)标准溶液,广州泛宏科技有限公司;环己酮、正构烷烃,上海阿拉丁生化科技股份有限公司;平板计数琼脂培养基,广东环凯微生物科技有限公司;NaCl,上海麦克林生化科技股份有限公司;H2O2,广州化学试剂厂;ClO2,广州闪电生物科技有限公司。ClO2为食品级,其余试剂为分析纯。
1.2 仪器与设备
OGT-01型顶空气体分析仪,山东泉科瑞达仪器设备有限公司;QTS型质构仪,美国Brook eld公司;SY3060型分光测色仪,深圳市威福光电科技有限公司;HCS-265A-A型生化培养箱,广州恒创实验仪器有限公司;KLCZ-880A型超净工作台,北京亚泰科隆仪器技术有限公司;5804-R型高冷冻离心机,艾本德中国有限公司;infinite M200PRO型酶标仪,瑞士帝肯公司;平面袋真空保鲜机,深圳瑞朗克斯科技有限公司;7890A-5975C型气相色谱-质谱联用仪,美国Agilent公司;DVB/CAR/PDMS 50/30 μm萃取头,上海安谱实验科技股份有限公司。
eld公司;SY3060型分光测色仪,深圳市威福光电科技有限公司;HCS-265A-A型生化培养箱,广州恒创实验仪器有限公司;KLCZ-880A型超净工作台,北京亚泰科隆仪器技术有限公司;5804-R型高冷冻离心机,艾本德中国有限公司;infinite M200PRO型酶标仪,瑞士帝肯公司;平面袋真空保鲜机,深圳瑞朗克斯科技有限公司;7890A-5975C型气相色谱-质谱联用仪,美国Agilent公司;DVB/CAR/PDMS 50/30 μm萃取头,上海安谱实验科技股份有限公司。
1.3 实验方法
1.3.1 鲜切菠萝处理
选取成熟度一致(可溶性固形物含量为13%~15%)、大小均一(1.0~1.5 kg)的菠萝(cv.Bali),清洗干净后去皮去眼,切成1.5~2 cm的四分之一扇形(10~15 g)块状,浸泡在前处理溶液(10%盐水+1 mg/L ClO2)中10 min,取出沥干、晾干。
1.3.2 包装处理
不同阻隔性保鲜袋的信息如表1所示,均来自同一家公司。将处理好的鲜切菠萝以10~15 g装进保鲜袋(12 cm×9 cm)中,于(4±1) ℃贮藏。根据鲜切菠萝市场及生产企业的评估,其保鲜期在5~7 d内,因此本实验以7 d为贮藏时间,在取样点随机选取鲜切菠萝块进行分析。以不包装的鲜切菠萝作为对照组(blank group,BK)。
表1 包装材料参数
Table 1 The parameters of package barrier property
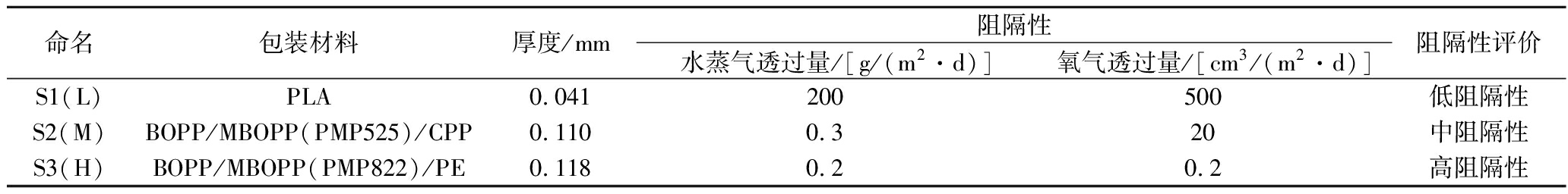
命名包装材料厚度/mm阻隔性水蒸气透过量/[g/(m2·d)]氧气透过量/[cm3/(m2·d)]阻隔性评价S1(L)PLA0.041200500低阻隔性S2(M)BOPP/MBOPP(PMP525)/CPP0.1100.320中阻隔性S3(H)BOPP/MBOPP(PMP822)/PE0.1180.20.2高阻隔性
1.3.3 顶空气体含量分析
测量前在保鲜袋上贴紧密封垫片,将采样针头和出气针头通过密封垫片刺入袋内顶空部分,以保持袋内总气体含量不变。测试完后用密封垫圈密封针口,取样量为标准模式下<3 mL。使用前于空旷区域大气中的O2和CO2浓度进行校准,每组数据测3次。
1.3.4 理化性质测定
1.3.4.1 失重率和硬度的测定
用称量法测定失重率。分别测定鲜切菠萝在不同取样点的质量并根据公式(1)计算。
(1)
式中:X为失重率,%;A、B为储存前、后的质量,g。
硬度参照朱萍[10]的方法并稍作修改,釆用TA44型探头的质构仪,测试样品深度5 mm,测试速度1.5 mm/s,返回速度1.5 mm/s,循环2次。
1.3.4.2 褐变指数的测定
测色仪使用前用标准黑白板进行校准。L*(亮度)、a*(红绿度)、b*(黄蓝度)值用于描述鲜切菠萝的颜色。褐变指数(browning index,BI)计算如式(2)和(3)所示。
(2)
(3)
1.3.4.3 抗坏血酸和总酚含量的测定
抗坏血酸参照GB 5009.86—2016《食品安全国家标准 食品中抗坏血酸的测定》的2,6-二氯靛酚法进行测定。
总酚测定参考胡晓敏[11]的方法并稍作修改。取2 g样品于研钵并加入4倍(mL∶g)的70%(体积分数)乙醇溶液冰浴研磨,均质30 s,在4 ℃避光浸提2 h,于10 000 r/min离心20 min,取1 mL上清液,加入5 mL 10%(体积分数)福林酚与4 mL 7.5%(体积分数)Na2CO3溶液,混匀后避光反应2 h,于765 nm测OD值。以没食子酸标准溶液制作标准曲线计算总酚含量,结果以mg/g表示。
1.3.4.4 菌落总数的测定
参考GB 4789.2—2022《食品安全国家标准 食品微生物学检验 菌落总数测定》进行测定。
1.3.5 挥发性风味物质测定
采用HS-SPME-GC-MS对鲜切菠萝在不同阻隔性包装经贮藏后的挥发性化合物进行分析,以新鲜和腐败的鲜切菠萝作为对照。参照STEINGASS等[12]方法并稍作修改。
1.3.5.1 样品前处理
将15 g鲜切菠萝用1.36 g蒸馏水和4.09 g NaCl进行研磨,并加标10 μL 1.104 45 g/L环己酮溶液作为内标(internal standard,IS),即每个样品的IS质量浓度为674.68 μg/L,涡旋均质2 min,使用IS的总离子色谱峰面积对单个化合物进行半定量分析。
1.3.5.2 HS-SPME条件
称取(1±0.1) g前处理样品于5 mL的顶空瓶中,立即密封。将顶空瓶放置在加热装置上(已达到70 ℃)平衡样品30 min,将SPME萃取针插入顶空瓶并推出萃取头暴露于顶空中,于70 ℃萃取15 min后将萃取头取出插进气相色谱的进样口,于250 ℃下解吸15 min。
1.3.5.3 GC-MS条件
气相色谱条件:色谱柱DB-5MS(30 m×0.25 mm,0.25 μm);升温程序:初始温度50 ℃,保持1 min,以2 ℃/min升至80 ℃,保持1 min,以3 ℃/min升至110 ℃保持2 min,以5 ℃/min升至170 ℃,保持2 min,以5 ℃/min升至200 ℃,保持1 min,以10 ℃/min升至220 ℃,保持1 min,总时间为52 min。载气(He)流速1.0 mL/min;进样量1 μL;不分流进样;传输线(辅助加热器)温度280 ℃。
质谱条件:电子轰击离子源;电离能量70 eV;离子源温度230 ℃;四极杆温度150 ℃;检测方式全扫描模式;选择离子监测模式;质量扫描范围(m/z)25~600。测定结果以NIST 17谱库、保留时间和保留指数进行定性。
1.3.5.4 OAV分析
为评估每种挥发性化合物对整体香气分布的贡献,将每种挥发物的浓度除以从文献中获得的OT值来计算每种物质的OAV。当OAV≥1时视为对整体风味具有重要贡献,值越大,则风味贡献越大。
1.4 数据处理与分析
数值以平均值±标准偏差表示,采用Origin 2023和SPSS Statistics 22对数据进行绘图和显著性分析(P<0.05为显著性差异),Data Analysis和MS-DILE用于谱图的谱库匹配和分析,采用ChiPlot (https://www.chiplot.online/)绘制热图。
2 结果与分析
2.1 顶空气体含量分析
如图1所示,袋内CO2浓度随包装阻隔性的增强而上升(P<0.05),O2浓度随包装阻隔性的增强而降低,3组均在第3天接近稳定状态。达稳定状态时S1(L)和S2(M)组的O2浓度分别约为13.04%和10.06%,而S3(H)组袋内O2开始降至8.82%左右。当环境中O2含量达10%时为植物的无氧呼吸消失点[13],说明S3(H)组即高阻隔包装的鲜切菠萝在第3天前就开始进行无氧呼吸并生成相应的产物,促进异味的发生,不利于鲜切菠萝的贮藏保鲜。
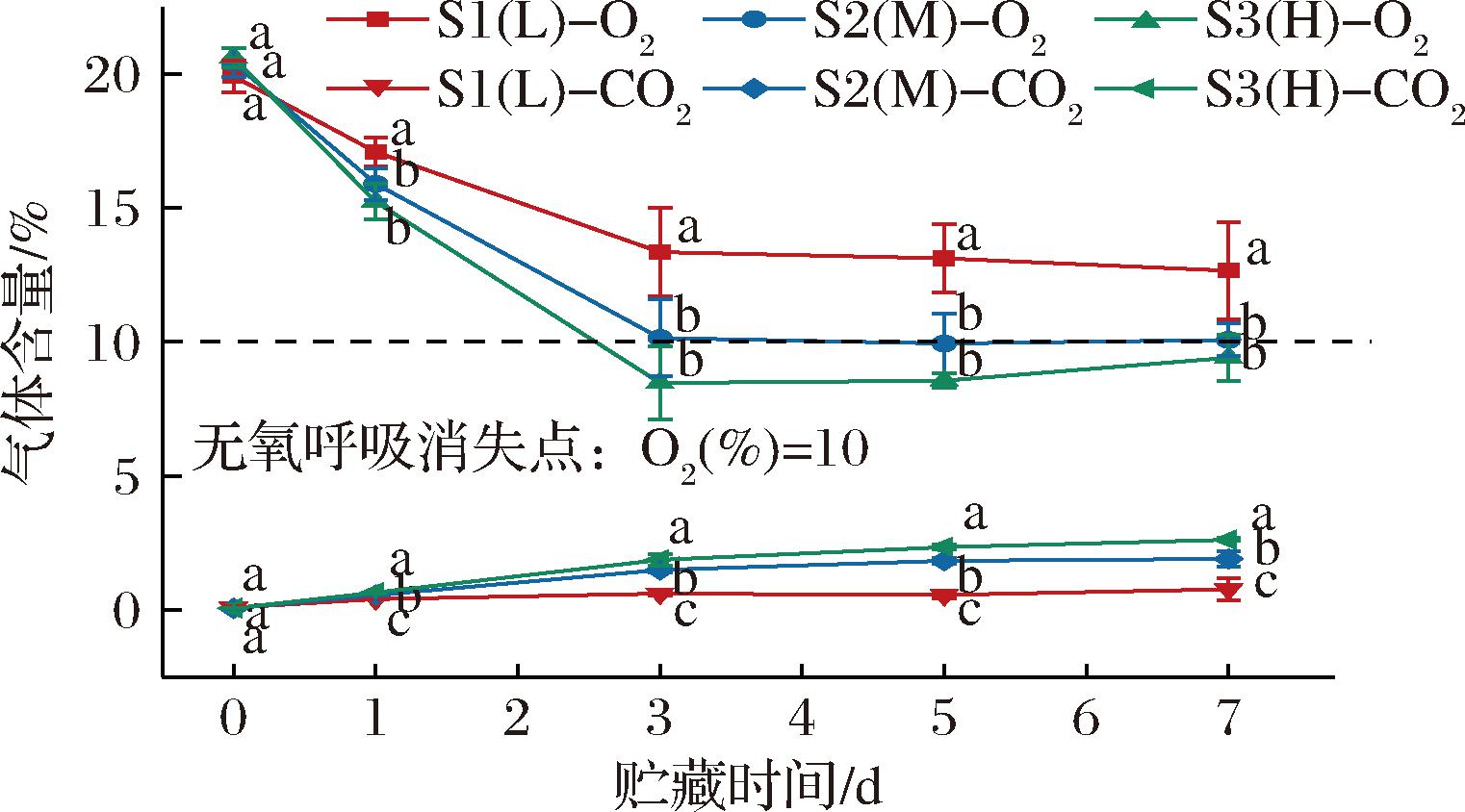
图1 鲜切菠萝在不同阻隔性包装内气体含量的变化
Fig.1 Variations of gas contents in different packaging barrier properties of fresh-cut pineapple
注:不同小写字母表示差异显著(P<0.05)(下同)。
2.2 理化性质分析
2.2.1 失重率和硬度分析
如图2-a所示,贮藏期间鲜切菠萝的失重率整体呈上升的趋势,低阻隔S1(L)组鲜切菠萝失重率显著大于其他两组(P<0.05)。研究表明短期缺氧处理保持了鲜切菠萝细胞膜的完整性并延缓了脂质的过氧化,使其失重率降低[14]。因此,S2(M)和S3(H)组由于较高阻隔性延缓了鲜切菠萝细胞膜脂质的氧化和失水作用,减少了质量损失。如图2-b所示,贮藏结束时3组鲜切菠萝的硬度分别下降了41.28%、11.56%和24.72%。研究表明微生物侵染产生的酶对果实的细胞壁成分具有降解作用[15-17],S1(L)组由于低阻隔性使微生物大量生长,破坏细胞壁结构导致果肉软化,S3(H)由于过高的阻隔性使鲜切菠萝快速地进入无氧呼吸,促进了菠萝的软化,而S2(M)组对于保持鲜切菠萝的硬度具有更优的效果。
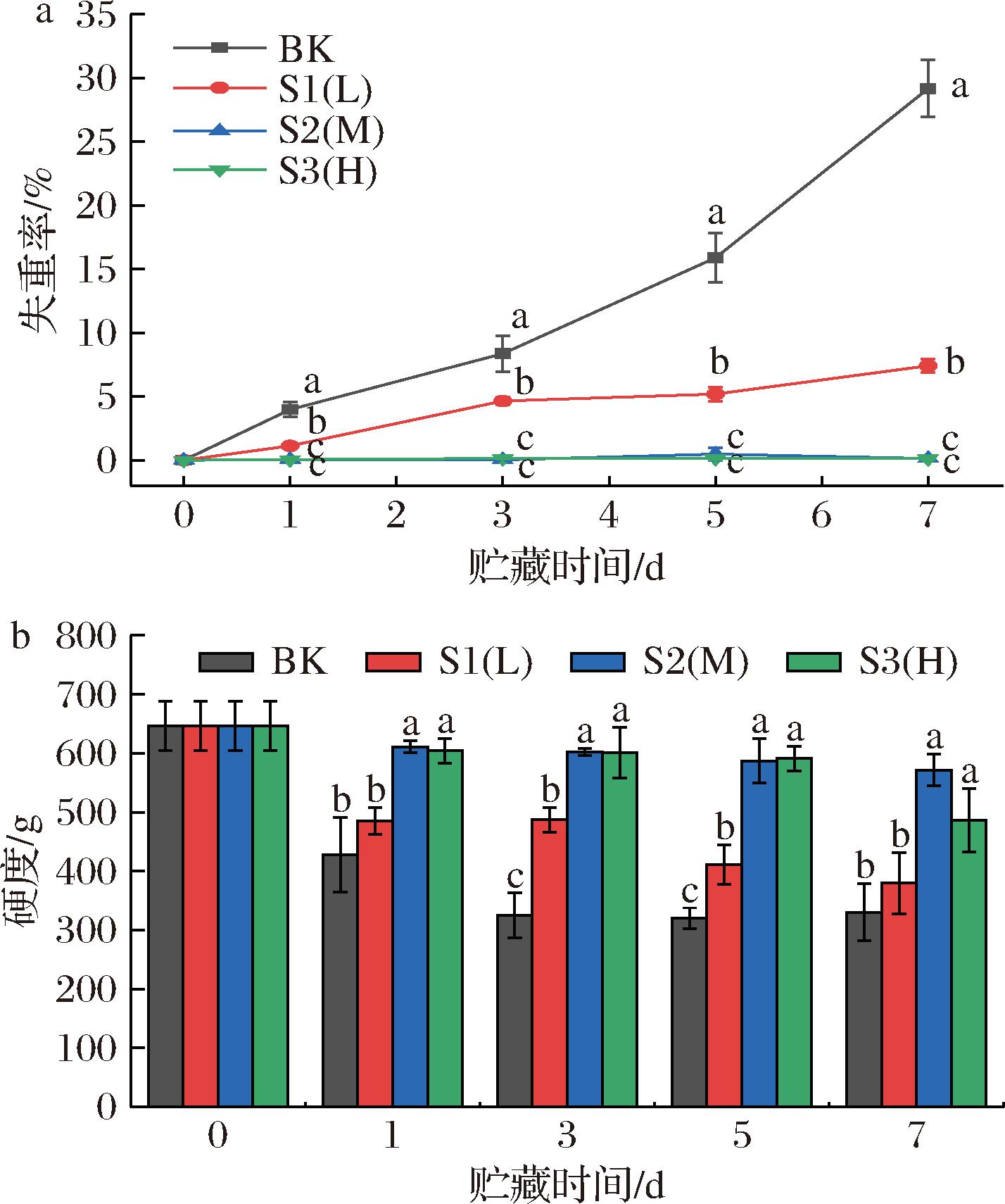
a-失重率;b-硬度
图2 包装阻隔性对鲜切菠萝失重率和硬度的影响
Fig.2 Effect of packaging barrier properties on weight loss and hardness of fresh-cut pineapple
2.2.2 BI分析
BI反映果肉从新鲜状态到褐变状态的程度,与多酚氧化酶的褐变反应相关。如图3所示,鲜切菠萝的BI整体随贮藏时间呈上升趋势(P>0.05),S1(L)组中对O2的低阻隔性促进了果肉中多酚氧化酶氧化酚类形成醌及其聚合物,导致BI明显高于其他处理组,S2(M)组的鲜切菠萝保持了较好的表面感官品质。
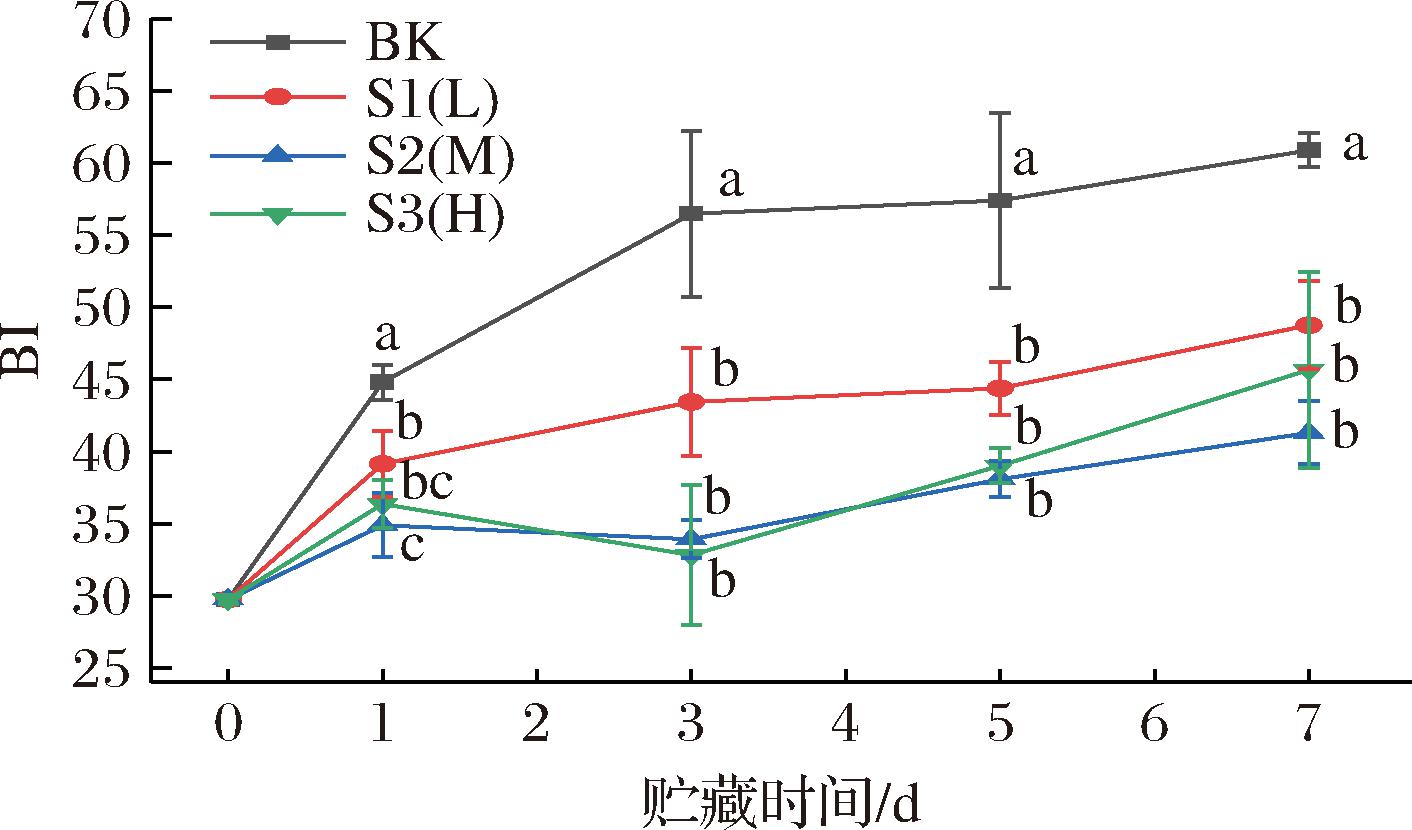
图3 包装阻隔性对鲜切菠萝褐变指数的影响
Fig.3 Effect of packaging barrier properties on the browning index of fresh-cut pineapple
2.2.3 AA和总酚含量分析
鲜切菠萝中AA和总酚是提供抗氧化剂的良好来源,但极易被氧化[18-19];逆境条件下植物进行适应性反应会诱导抗氧化剂用以清除活性氧ROS[11]。如图4-a所示,贮藏期间AA含量整体呈下降趋势,贮藏结束时S1(L)组显著低于S2(M)和S3(H)组(P<0.05),其中S2(M)组保持了最高的AA含量。
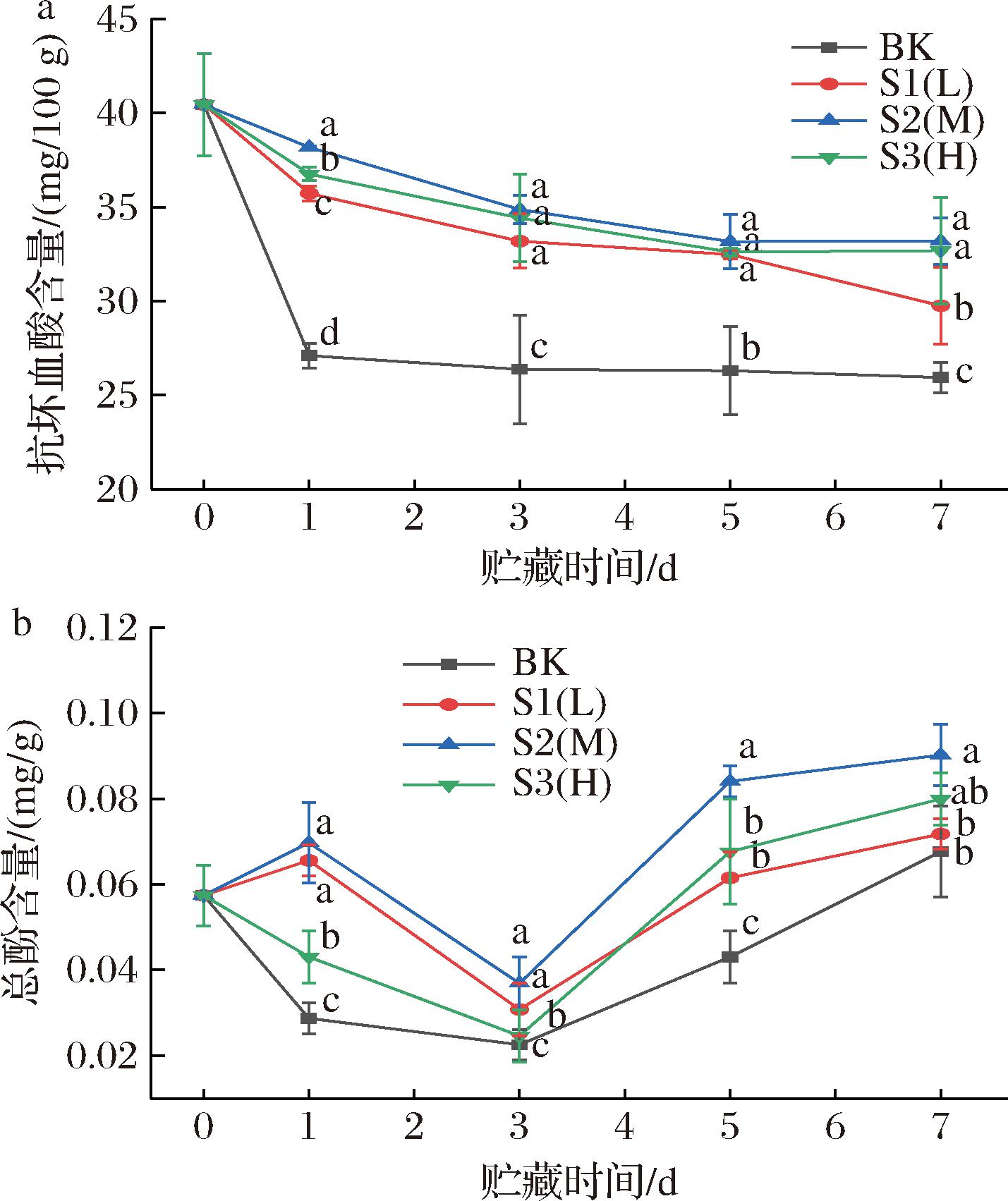
a-抗坏血酸含量;b-总酚含量
图4 包装阻隔性对鲜切菠萝抗坏血酸和总酚含量的影响
Fig.4 Effect of packaging barrier properties on ascorbic acid and total phenol content of fresh-cut pineapple
如图4-b所示,鲜切菠萝的总酚含量呈下降后上升的趋势,前期由于鲜切菠萝的生理代谢反应使酚类的消耗量大于生成量;后期由包装阻隔性与水果的呼吸作用形成的自发气调环境减缓了总酚的消耗,并可能促进苯丙氨酸解氨酶合成酚类,使酚类的生成量大于消耗量。BK组的总酚在后期的上升归因于果肉中水分的大量减少。由于高阻隔性形成的缺氧环境促使细胞产生适应性反应,催化了酚类的降解,使后期S3(H)组总酚含量仅次于S2(M)组。贮藏结束时BK和S1(L)组显著低于另外两组(P<0.05),说明较高阻隔性包装可延缓酚类的氧化和消耗,其中S2(M)组更有效地减缓了鲜切菠萝总酚含量的降解消耗。
2.2.4 菌落总数变化分析
鲜切菠萝因表面水分高和丰富的营养物质为微生物的生长提供了良好的环境,6 lg CFU/g为鲜切果蔬的微生物安全限量标准[15]。如图5所示,贮藏期间鲜切菠萝的菌落总数整体呈上升趋势,贮藏的第5天开始S1(L)组显著上升(P<0.05),贮藏结束时菌落总数已超过6 lg CFU/g。此外,S3(M)组比S2(M)组的菌落总数高,归因于高阻隔性形成的低氧环境促进了厌氧菌的生长,导致品质劣变。S2(M)组的鲜切菠萝在保鲜期内菌落总数始终低于6 lg CFU/g,符合市场上鲜切果蔬售卖的安全标准。
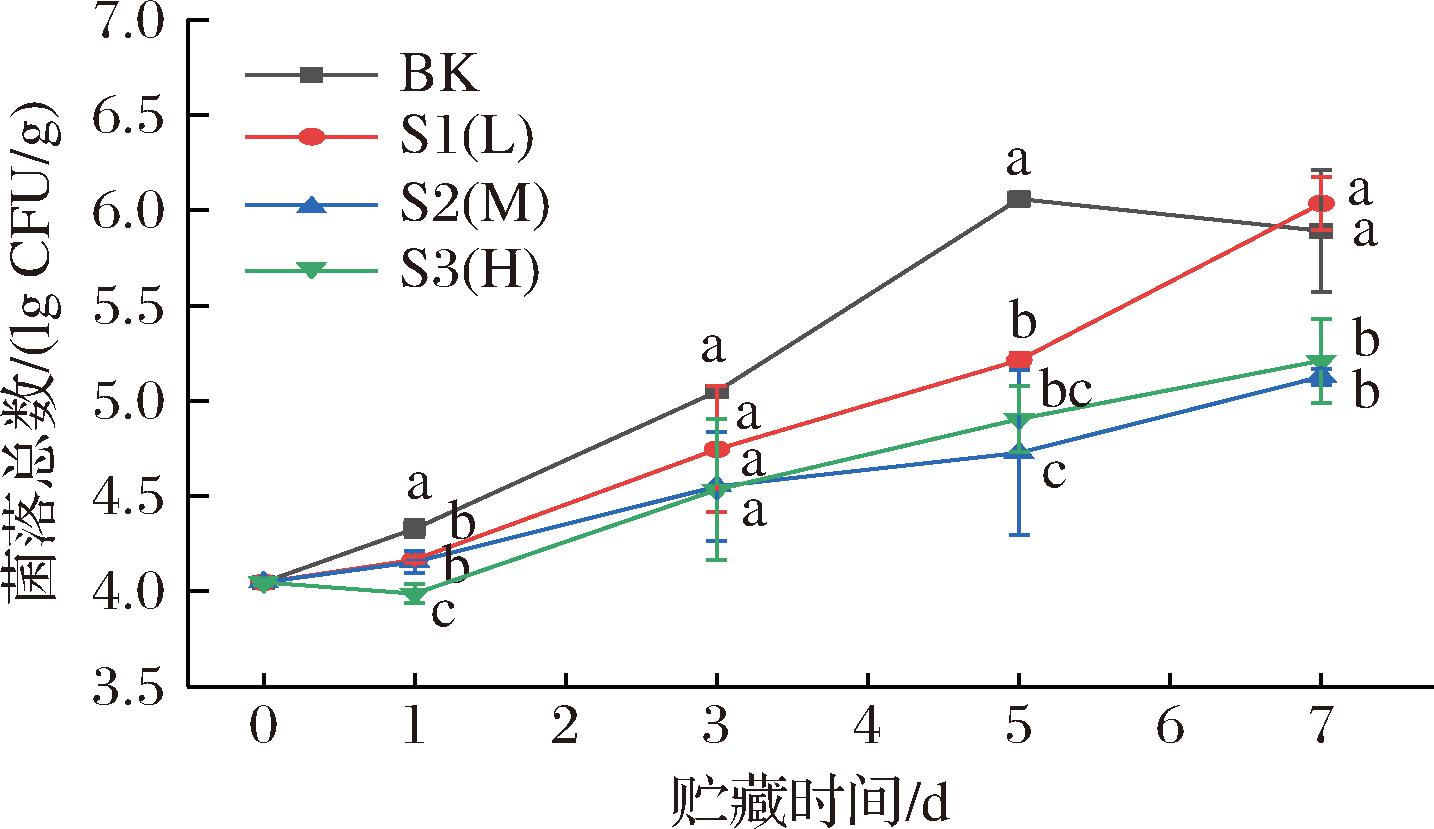
图5 包装阻隔性对鲜切菠萝菌落总数的影响
Fig.5 Effect of packaging barrier properties on aerobic plate count of fresh-cut pineapple
2.3 挥发性物质分析
2.3.1 挥发性化合物的定性和定量
所有样品中共鉴定出66种挥发性化合物,包括38种酯类、5种醇类、5种酸类、2种内酯类、1种萜烯类、1种呋喃酮和14种其他化合物。酯类是提供菠萝风味的主要化合物,占总挥发性化合物的57.58%,主要由直链和支链脂肪酸的甲酯和乙酯所形成的羟基化和乙酰基化衍生物组成[20]。己酸甲酯是含量最丰富的化合物,呈菠萝似水果香味,其次是3-甲硫基丙酸甲酯、醋酸异丙酯、6-氨基己酸、2-甲基戊酸甲酯、正己酸乙酯、2-甲基丁酸甲酯和异己酸乙酯。其中己酸甲酯、3-甲硫基丙酸甲酯、2-甲基戊酸甲酯、2-甲基丁酸甲酯是新鲜菠萝主要的特征风味物质[21]。腐败样品中醇类和酸类含量明显上升,异丁酸是最丰富的风味物质,呈黄油似酸味,其次是乙酸乙酯、丁酸乙酯、丙二醇、苯乙醇和乙醇。其中乙酸乙酯导致酯类总体含量升高,研究表明乙酸乙酯是水果中有机化合物在有氧条件下发生腐烂而生成,与微生物污染有关[22],MATTHEIS等[23]提出厌氧条件下苹果中乙醇内源水平的大量增加导致酯的合成相应地增加;KNEE等[24]研究发现果醇的缺乏是气调保鲜的苹果中缺乏酯类的原因。
如图6所示,与新鲜样品相比,贮藏后S1(L)、S2(M)和S3(H)组的酯类和酸类均增加了2种,分别为丙二酸二乙酯、乙酸苯乙酯、异丁酸和辛酸。贮藏后除了主要风味化合物浓度增强外,醇类和酸类浓度也会增加。酯类含量明显随包装阻隔性的增强而降低,而酸类随包装阻隔性的增强而增强,表明鲜切菠萝经贮藏后酯类不断生成,并具有氧依赖性;较高阻隔性中酸类和醇类的上升是由于缺氧环境促进了鲜切菠萝无氧呼吸并发生发酵反应,表明不适宜的包装贮藏条件会导致鲜切菠萝酸类和醇类等异味增加,并降低其货架期。
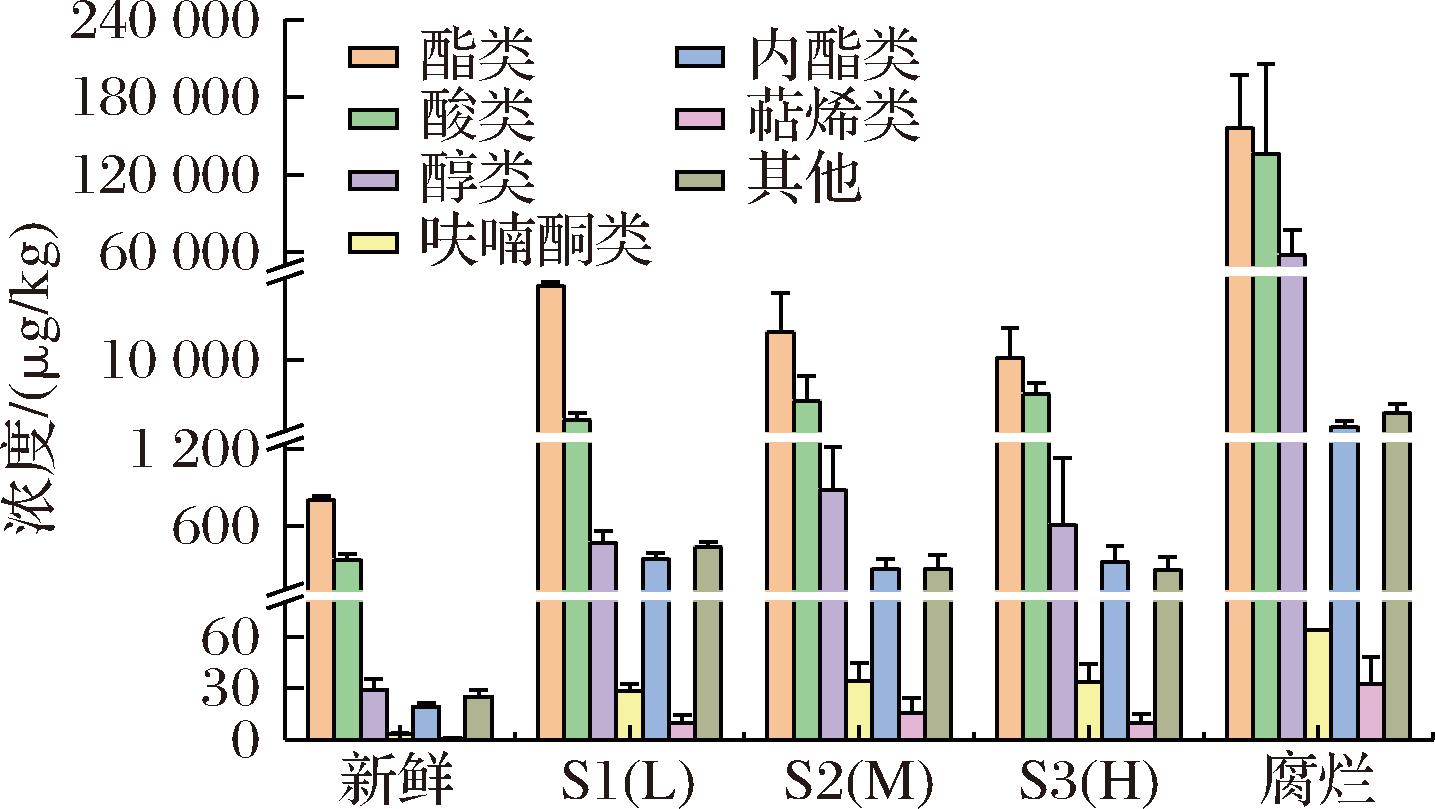
图6 新鲜的、腐烂的、S1(L)、S2(M)和S3(H)阻隔性 包装鲜切菠萝的主要物质分类的总浓度
Fig.6 Total concentrations of the main substance classes of fresh, rotten, S1 (L), S2 (M), and S3 (H) of pineapple pulp
2.3.2 OAV分析
如图7所示,共得到26种OAV≥1的挥发性化合物,S1(L)、S2(M)和S3(H)组分别包括17、18和16种。丁酸乙酯、2-甲基丁酸乙酯、己酸乙酯、异己酸乙酯和3-甲硫基丙酸乙酯在3组处理中均具有较高的OAV,呈水果似香甜气味,可能是经贮藏后鲜切菠萝呈成熟风味的主要贡献者。随包装阻隔性的增大,这5种挥发性物质的贡献越小,说明阻隔性高阻碍了鲜切菠萝香气物质的形成。

图7 鲜切菠萝中26种挥发性化合物(OAV≥1)的浓度分布情况
Fig.7 Concentration distribution of 26 volatile compounds (OAV≥1) in fresh-cut pineapple
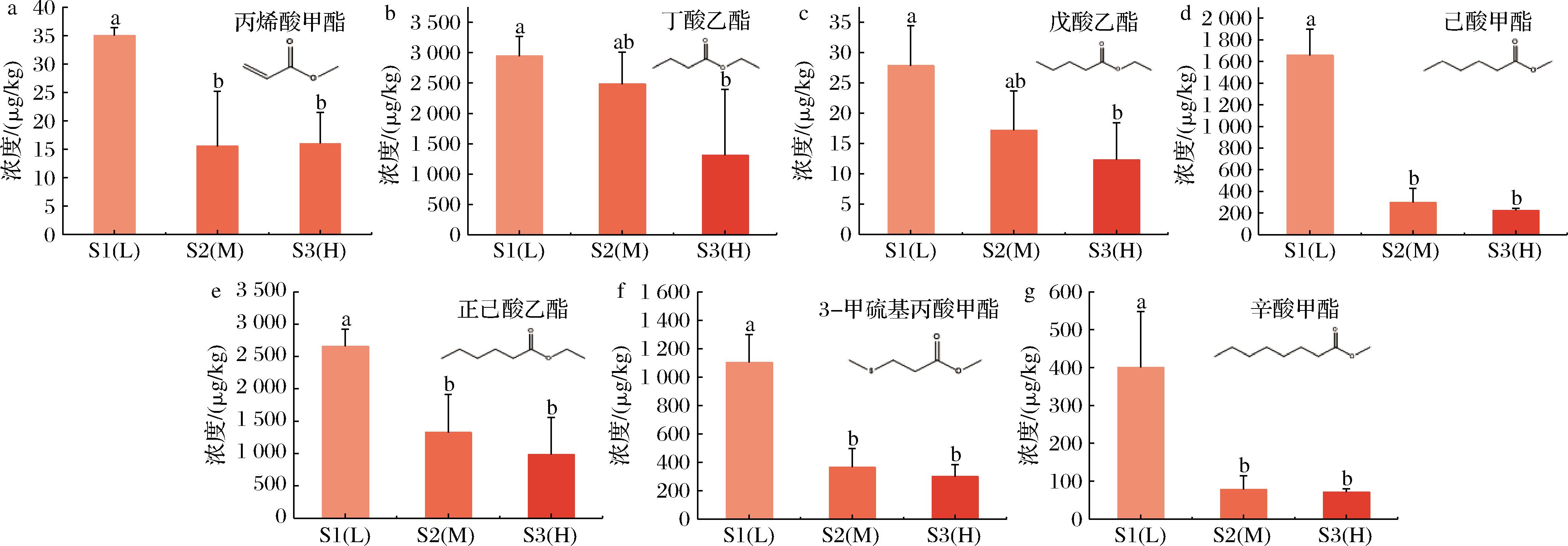
图8 S1(L)、S2(M)和S3(H)袋内鲜切菠萝香气化合物的浓度及其与阻隔性的相关性
Fig.8 Average concentrations of aroma compounds in fresh-cut pineapple with S1 (L), S2 (M), and S3 (H) barrier properties and their correlation with packaging barrier properties
2.3.3 特征风味物质的浓度变化规律
为得到鲜切菠萝在不同阻隔性包装贮藏后引起风味不同的原因,对OAV≥1的物质进行ANOVA方差分析(表8),得到丙烯酸甲酯、丁酸乙酯、戊酸乙酯、己酸甲酯、正己酸乙酯、3-甲硫基丙酸甲酯和辛酸甲酯在3组中具有显著性差异(P<0.05),主要呈菠萝、苹果和橙子香甜气味。值得注意的是,7种挥发性化合物浓度都与包装阻隔性呈负相关。ARAGÜEZ等[25]研究发现苹果中酯的生成源于氧依赖性反应,O2的消耗对酯类的生成具有负面影响。因此,包装阻隔性对O2的阻隔可能是形成鲜切菠萝风味差异化的原因,阻隔性越大,酯的生成量越小。鲜切菠萝的特征风味物质与氧依赖性反应和袋内顶空气体差异化效应密切相关,被认为是影响风味物质浓度不同的潜在原因。
3 结论
本研究主要评估了包装阻隔性对鲜切菠萝在4 ℃贮藏期间的品质差异和风味物质浓度变化规律。结果表明,S2(M)组阻隔性包装有效减少了鲜切菠萝在贮藏期间的质量损失,减缓了抗坏血酸和总酚含量的氧化消耗,保持了较好的果肉硬度和色泽,同时减缓了微生物的增长。HS-SPME-GC-MS分析发现酯类是鲜切菠萝的主要风味物质且具有氧依赖性效应,而酸类和醇类是主要的异味化合物并与包装阻隔性呈正相关。26种风味物质被认为对鲜切菠萝风味具有主要贡献(OAV≥1),其中丙烯酸甲酯、丁酸乙酯、戊酸乙酯、己酸甲酯、正己酸乙酯、3-甲硫基丙酸甲酯和辛酸甲酯含量与包装阻隔性显著相关(P<0.05)。高阻隔性包装不仅抑制了鲜切菠萝贮藏期间特征风味物质的生成,还促进了异味的形成,降低了货架期。总体而言,S2(M)组阻隔性包装在7 d的保鲜期内可显著维持鲜切菠萝的品质,并有效减少特征风味的损失和异味的形成,满足鲜切菠萝在4 ℃保鲜的品质及货架期要求。
[1] 李崇高, 黄建初, 邱红妹.响应面法优化鲜切菠萝壳聚糖涂膜保鲜的研究[J].食品与发酵工业, 2018, 44(9):182-187.LI C G, HUANG J C, QIU H M.Study on fresh-keeping pineapple chitosan coating by response surface methodology[J].Food and Fermentation Industries, 2018, 44(9):182-187.
[2] MA L, ZHANG M, BHANDARI B, et al.Recent developments in novel shelf life extension technologies of fresh-cut fruits and vegetables[J].Trends in Food Science &Technology, 2017, 64:23-38.
[3] MONTERO-CALDER N M, ROJAS-GRAÜ M A, MART
N M, ROJAS-GRAÜ M A, MART N-BELLOSO O.Effect of packaging conditions on quality and shelf-life of fresh-cut pineapple (Ananas comosus)[J].Postharvest Biology and Technology, 2008, 50(2-3):182-189.
N-BELLOSO O.Effect of packaging conditions on quality and shelf-life of fresh-cut pineapple (Ananas comosus)[J].Postharvest Biology and Technology, 2008, 50(2-3):182-189.
[4] BASAVEGOWDA N, BAEK K H.Advances in functional biopolymer-based nanocomposites for active food packaging applications[J].Polymers, 2021, 13(23):4198.
[5] SILVA F A G S, DOURADO F, GAMA M, et al.Nanocellulose bio-based composites for food packaging[J].Nanomaterials, 2020, 10(10):2041.
[6] 王羽, 云雪艳, 李见森, 等.PA/PE复合膜对鲜切莴笋保鲜效果的影响[J].食品科学, 2015, 36(24):343-347.WANG Y, YUN X Y, LI J S, et al.Effect of PA/PE composite membrane on preservation of fresh-cut Asparagus lettuce[J].Food Science, 2015, 36(24):343-347.
[7] BEN TEZ S, SORO L, ACHAERANDIO I, et al.Combined effect of a low permeable film and edible coatings or calcium dips on the quality of fresh-cut pineapple[J].Journal of Food Process Engineering, 2014, 37(2):91-99.
TEZ S, SORO L, ACHAERANDIO I, et al.Combined effect of a low permeable film and edible coatings or calcium dips on the quality of fresh-cut pineapple[J].Journal of Food Process Engineering, 2014, 37(2):91-99.
[8] AMARO A L, ALMEIDA D P F, MALCATA F X, et al.Volatile composition and quality of fresh-cut Cucumis melo var.cantaloupensis and inodorus as affected by modified and controlled atmospheres[J].Acta Horticulturae, 2010(877):603-609.
[9] MATTHEIS J P, BUCHANAN D A, FELLMAN J K.Volatile compounds emitted by ‘Gala’ apples following dynamic atmosphere storage[J].Journal of the American Society for Horticultural Science, 1998, 123(3):426-432
[10] 朱萍. 乙醛熏蒸改善鲜切菠萝风味技术研究[D].海口:海南大学, 2012.ZHU P.Study the technology of acetaldehyde fumigation of fresh-cut pineapple to improve flavor[D].Haikou:Hainan University, 2012.
[11] 胡晓敏. 乳酸钙浸渍和短波紫外光照射对鲜切猕猴桃品质及抗氧化活性的影响[D].成都:四川农业大学, 2022.HU X M.lmpact of calcium lactate dips combinedwith UV-C irradiation on the quality attributes and antioxidant capacities of fresh-cut kiwi fruit slices[D].Chengdu:Sichuan Agricultural University, 2022.
[12] STEINGASS C B, GRAUWET T, CARLE R.Influence of harvest maturity and fruit logistics on pineapple (Ananas comosus[L.]Merr.) volatiles assessed by headspace solid phase microextraction and gas chromatography-mass spectrometry (HS-SPME-GC/MS)[J].Food Chemistry, 2014, 150:382-391.
[13] 李合生. 现代植物生理学[M].北京:高等教育出版社, 2012.LI H S. Modern Plant Physiology[M]. The third edition. Beijing: Higher Education Press, 2012.
[14] SUPAPVANICH S, TECHAVUTHIPORN C.Efficiency of pre-process Anoxia treatment on quality of fresh-cut pineapples cv.‘Phulae’ during storage[J].International Journal of Food Science &Technology, 2022, 57(3):1679-1687.
[15] PRAKASH A, BASKARAN R, VADIVEL V.Citral nanoemulsion incorporated edible coating to extend the shelf life of fresh cut pineapples[J].LWT, 2020, 118:108851.
[16] GUERREIRO A C, GAGO C M L, MIGUEL M G C, et al.The influence of edible coatings enriched with citral and eugenol on the raspberry storage ability, nutritional and sensory quality[J].Food Packaging and Shelf Life, 2016, 9:20-28.
[17] TANADA-PALMU P S, GROSSO C R F.Effect of edible wheat gluten-based films and coatings on refrigerated strawberry (Fragaria ananassa) quality[J].Postharvest Biology and Technology, 2005, 36(2):199-208.
[18] HOSSAIN M A, MIZANUR RAHMAN S M.Total phenolics, flavonoids and antioxidant activity of tropical fruit pineapple[J].Food Research International, 2011, 44(3):672-676.
[19] SHARMA L, SAINI C S, SHARMA H K.Development of crosslinked sesame protein and pineapple extract-based bilayer coatings for shelf-life extension of fresh-cut pineapple[J].Journal of Food Processing and Preservation, 2018, 42(2):e13527.
[20] VOLLMER K, CZERNY M, V SQUEZ-CAICEDO A L, et al.Non-thermal processing of pineapple (Ananas comosus[L.]merr.) juice using continuous pressure change technology (PCT):HS-SPME-GC-MS profiling, descriptive sensory analysis, and consumer acceptance[J].Food Chemistry, 2021, 345:128786.
SQUEZ-CAICEDO A L, et al.Non-thermal processing of pineapple (Ananas comosus[L.]merr.) juice using continuous pressure change technology (PCT):HS-SPME-GC-MS profiling, descriptive sensory analysis, and consumer acceptance[J].Food Chemistry, 2021, 345:128786.
[21] ELSS S, PRESTON C, HERTZIG C, et al.Aroma profiles of pineapple fruit (Ananas comosus[L.]Merr.) and pineapple products[J].LWT, 2005, 38(3):263-274.
[22] ZHANG Y N, LIANG Z S, TANG C C, et al.Malodorous gases production from food wastes decomposition by indigenous microorganisms[J].Science of the Total Environment, 2020, 717:137175.
[23] MATTHEIS J P, BUCHANAN D A, FELLMAN J K.Change in apple fruit volatiles after storage in atmospheres inducing anaerobic metabolism[J].Journal of Agricultural and Food Chemistry, 1991, 39(9):1602-1605.
[24] KNEE M, HATFIELD S G S.The metabolism of alcohols by apple fruit tissue[J].Journal of the Science of Food and Agriculture, 1981, 32(6):593-600.
[25] ARAGÜEZ I, FERN NDEZ D V V.Metabolic engineering of aroma components in fruits[J].Biotechnology Journal, 2013, 8(10):1144-1158.
NDEZ D V V.Metabolic engineering of aroma components in fruits[J].Biotechnology Journal, 2013, 8(10):1144-1158.