藤椒,学名竹叶花椒(Zanthoxylum armatum DC.),属芸香科,是我国传统药食两用食物[1],其主要分布在中国西南地区,如眉山、雅安、绵阳、重庆等地[2]。目前已从藤椒中分离鉴定出60多种化学成分[3-4],其中芳樟醇、D-柠檬烯、月桂烯等物质在藤椒精油中的占比较高,并且藤椒还具有消炎镇痛、解热保肝、抗氧化等多种药用价值[5-6]。新鲜藤椒水分含量高,采摘后容易腐烂变质,且运输过程中油泡容易破碎[7],从而导致品质降低。目前,干燥是加工鲜藤椒的主要方法之一,干燥后的藤椒水分含量较低,可以延长藤椒的贮藏时间,抑制微生物的活性,并且能更好的储存和运输[8],最大程度的对鲜藤椒中的酰胺类和挥发性物质进行保留和储存。
目前花椒干燥方式的主要为单一干燥方法的研究,如杨森等[9]比较了不同温度对竹叶花椒品质和挥发性成分等的影响,得出热风干燥45 ℃有利于竹叶花椒品质的保护和挥发性风味成分的保留;孟国栋等[10]探究了真空干燥的工艺条件,在干燥温度为62.18 ℃、真空度为-0.054 MPa、装载量为37.23 g下花椒的干燥结果最佳;张艺等[11]探究了青花椒果皮表面油胞的完整性对青花椒色泽的影响,发现未破油泡组干青花椒青绿色泽保持效果最好。
基于以上研究结果本试验采用自然阴干、自然晒干、热风干燥(hot air drying,HD)和真空冷冻干燥(vacuum freeze drying,VFD)4种方式来探究新鲜花椒干燥方式的选择,并从色差、挥发油含量、水分、挥发性物质等指标进行分析和评价,以期为干燥方式的选择提供理论依据。
1 材料与方法
1.1 材料与试剂
新鲜藤椒,四川眉山;甲醇、乙腈(色谱级),成都市科隆化学品有限公司;羟基-α-山椒素、羟基-β-山椒素、羟基-γ-山椒素,成都普思生物科技股份有限公司;环己酮,北京坛墨质检科技有限公司。
1.2 仪器与设备
ME-204分析天平,Mettler Toledo(上海)有限公司;FD-15-F-500A粉碎机,浙江永康市奋斗工程有限公司;YM-040S超声波清洗器,深圳市方奥微电子有限公司;SHSL调温电热套,上海树立仪器仪表有限公司;电热干燥箱,永光明医疗仪器有限公司;SCIENTZ-10YG/A冷冻干燥机,宁波新芝冻干设备股份有限公司;CR10手持色差仪,柯尼卡美能达;1260 HPLC、8890-5977B GC-MS/MS、Agilent 120 μm DVB/CWR/PDMS型萃取头,美国安捷伦;L6S紫外分光光度计,上海仪电分析有限公司。
1.3 实验方法
1.3.1 干燥实验
取适量鲜藤椒,称重记录质量,分别采用自然晒干(阳光下晒干,室外温度36~38 ℃)、自然阴干(干燥阴凉通风处)、VFD(真空冷冻干燥机,预冻48 h,冷冻温度-20 ℃)和HD(电热干燥箱,温度45 ℃)[12]等方式对藤椒进行处理,处理完成后真空包装,于-20 ℃中保存备用。
1.3.2 水分测定
参照GB 5009.3—2016《食品安全国家标准 食品中水分的测定》测量干藤椒中的水分含量。
1.3.3 色差测定
使用色差仪测定样品L*(亮度/暗度),a*(红色/绿色)和b*(黄色/绿色),ΔE*计算如公式(1)所示。
(1)
1.3.4 山椒素含量的测定
1.3.4.1 样品处理
准确称取0.5 g(精确至0.000 1 g)样品置于锥形瓶中,加入50 mL甲醇,超声30 min,样品冷却至室温后转移到100 mL容量瓶中,定容,移取1 ml样液于10 mL容量瓶定容,用0.22 μm尼龙滤膜过滤。
1.3.4.2 色谱条件
色谱柱:Eclipse Plus C18(4.6 mm×150 mm, 5 μm);检测器:VWD;流动相:水(A)-乙腈(B);检测波长268 nm;柱温35 ℃;流速1.0 mL/min;进样量10 μL。洗脱程序:0~5 min,35%溶液B;5~10 min,40%溶液B;10~30 min,50%溶液B;30~35 min,35%溶液B。
1.3.5 挥发性成分的测定
1.3.5.1 样品前处理
参照GB/T 17527—2009《胡椒精油含量的测定》提取挥发油进行挥发性物质的测定。取不同干燥方式的藤椒挥发油使用正己烷稀释50倍,并加入无水Na2SO4于-20 ℃下保存,加入20 μL环己酮(1.333 mg/mL)内标溶液,定容,过0.22 μm微孔滤膜。
1.3.5.2 仪器条件
色谱条件:色谱柱:HP-5 MS(30 m×0.25 mm ID×0.25 μm);升温程序:初始温度50 ℃,保持2 min,以3 ℃/min升至230 ℃,保持3 min;载气为高纯He;进样口温度250 ℃,检测器温度260 ℃,进样量1 μL,分流比为10∶1;溶剂延迟时间3 min。MS条件:离子源温度230 ℃,四极杆温度150 ℃,扫描范围(m/z)40~550。
1.3.5.3 定性和定量分析
定性分析:干藤椒挥发油的检测结果使用NIST11.1标准谱库检索,选择匹配度>80%的挥发性风味成分,并结合相关文献,确定其化学组成,进行定量分析。
定量分析:以环己酮为内标,计算样品中各组分的绝对含量,如公式(2)所示:
绝对含量![]()
(2)
式中,ρ,环己酮浓度,mg/mL;A1,各挥发性组分的峰面积;A2,内标物质的峰面积;V1,内标物体积,mL;V2,挥发油的体积,mL。
1.4 数据统计与分析
采用SPSS 26.0对数据进行统计分析,使用Origin 2022软件进行分析及作图,SIMCA14.1软件进行偏最小二乘判别分析(partial least squares discriminant analysis,PLS-DA),计算变量投影重要性(variable importance in projection,VIP)。
2 结果与分析
2.1 四种不同干燥方式处理藤椒色泽分析
色泽是干藤椒重要的质量指标之一[12],如表1所示,4种干燥方式处理后的L*值差异显著,其中VFD样品值最大,为33.84±0.80,自然晒干样品值最小,为24.52±0.61,这可能是晒干时紫外线对样品有轻微的碳化、褐变以及生成了脱镁叶绿素等原因[2,13-14];VFD的a*值最小为-1.36±0.15,说明该样品偏绿,表明VFD处理后的藤椒中的叶绿素破坏相对较小,能在一定程度上减少新鲜藤椒中叶绿素的损失。HD和VFD干燥所得的样品在b*维度上差异不显著,但自然晒干的藤椒b*差异最大,表明自然晒干后的藤椒的偏红,与新鲜藤椒偏绿有较大差异。4种干燥方式所得的色差值中自然阴干、HD和VFD的差异不显著,自然晒干的样品差异最大。
表1 四种干燥方式对藤椒色泽的影响
Table 1 Effects of four drying methods on the color of Z. armatum DC

方法L∗a∗b∗ΔE∗自然阴干28.48±0.59d0.62±0.11b18.02±0.67b6.02±0.25bHD30.18±1.78c-0.16±0.18c21.14±1.69a5.56±0.40b自然晒干24.52±0.61b4.70±0.39a14.84±0.41c12.02±0.73aVFD33.84±0.80a-1.36±0.15d21.90±2.05a6.50±1.21b
注:同列中不同小写字母表示差异显著(P<0.05),相同小写字母表示差异不显著(P>0.05),下同。
2.2 四种不同干燥方式处理藤椒水分含量分析
水分测定结果如图1所示,自然阴干处理藤椒的水分含量最高为18.81 g/100 g,HD处理藤椒的水分含量最低为15.16 g/100 g。自然阴干虽然操作简单,能够避免光照对藤椒的影响,但自然阴干极易受天气影响,干燥时间明显比其他干燥方式时间长,并且在干燥过程中容易受到微生物和昆虫等的污染,造成发霉等品质劣变现象。VFD使新鲜藤椒中的水分直接从液态迅速变成固态,又从固态直接升华为气态,快速的除去新鲜藤椒水分[15]。由于水分从固态到气态的时间较短,能够有效减少藤椒细胞状态的破裂,并且能够抑制新鲜藤椒体内的生物酶活性和微生物的繁殖,最大程度的保留藤椒的品质。
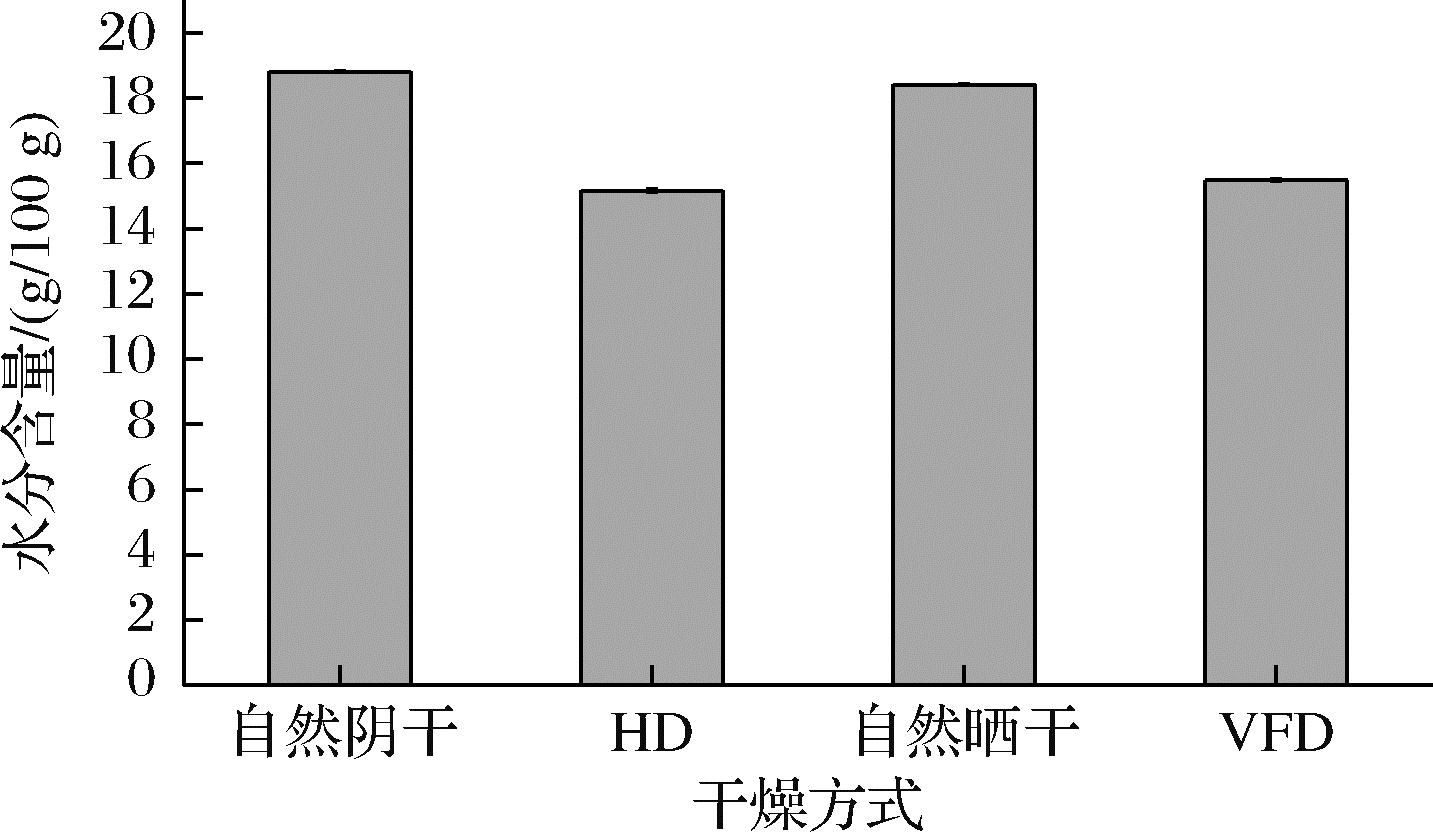
图1 四种干燥方式藤椒水分含量比较
Fig.1 Comparison of moisture content of Z. armatum DC in four drying methods
2.3 四种不同干燥方式处理藤椒山椒素含量分析
如图2所示,干燥后藤椒中山椒素含量差异较大。羟基-α-山椒素是藤椒麻味物质的主要成分,VFD和自然阴干能够显著的保留新鲜藤椒中的羟基-α-山椒素的含量,自然晒干能显著降低藤椒中的羟基-α-山椒素的含量,严雅丽等[16]研究结果显示紫外线能显著降低山椒素尤其是羟基-α-山椒素含量,侧面证明藤椒的干燥过程中应尽可能避免紫外线对藤椒品质的影响;干燥过程对羟基-β-山椒素和羟基-γ-山椒素含量影响较小,可能是由于这两种山椒素相比于羟基-α-山椒素更稳定,能应对环境条件的变化,维持自身的含量。
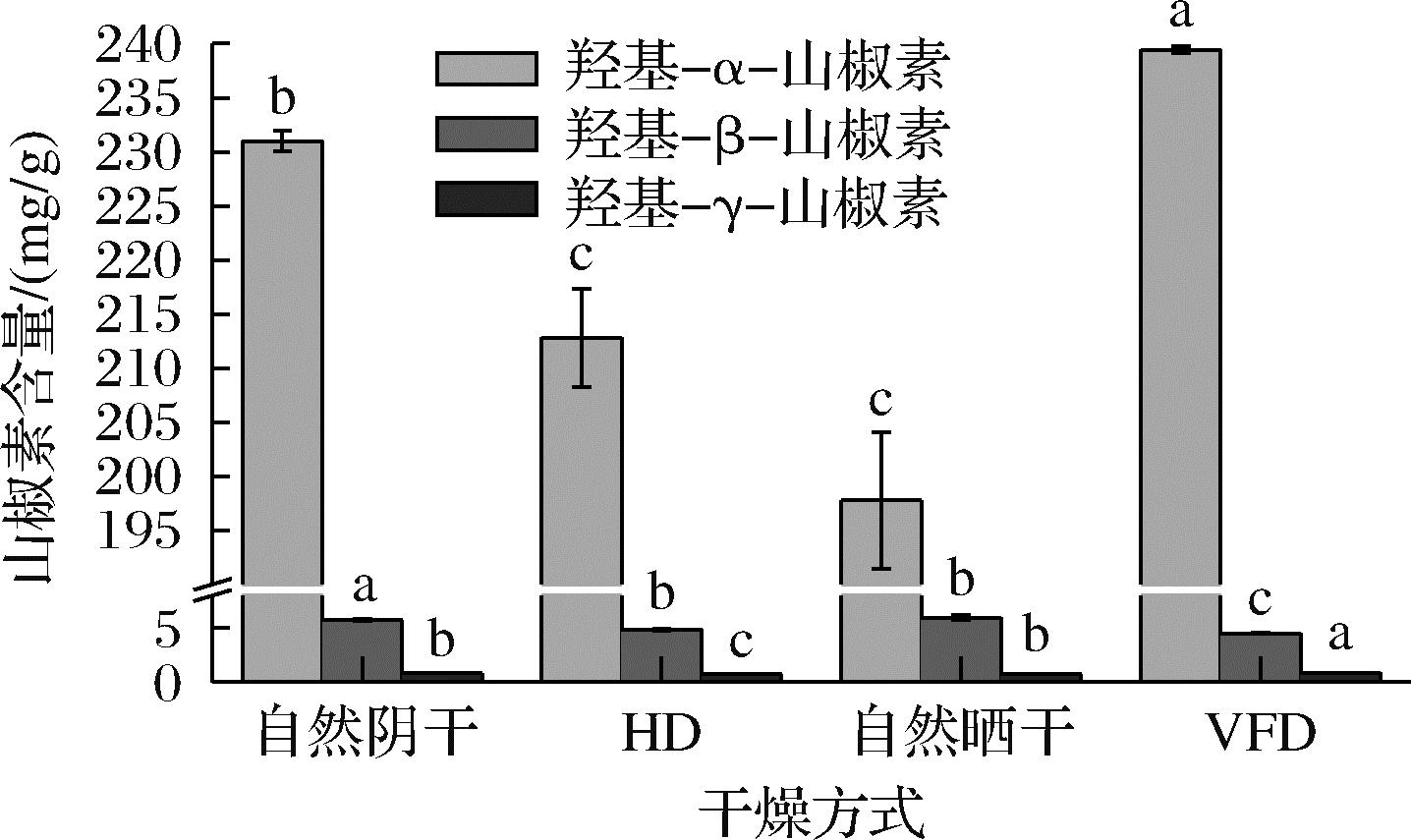
图2 四种干燥方式藤椒山椒素含量对比
Fig.2 Comparison of content of zanthoxylin in four dry Z. armatum DC
2.4 四种不同干燥方式处理藤椒挥发性风味物质种类和含量分析
如表2所示,VFD处理后的藤椒挥发性物质含量最多,共有2 235.407 mg/mL,醇类和烯烃类物质占挥发性物质总量的98.17%;自然晒干得到的藤椒挥发性物质含量最低,共有1 755.604 mg/mL,醇类和烯烃类物质占挥发性物质总量的97.93%。藤椒中主要挥发性风味物质D-柠檬烯、月桂烯、乙酸芳樟酯、芳樟醇、β-水芹烯等都在干燥后的藤椒中有检出。烯烃类物质风味强烈,阈值较低,并且烯烃类物质多具有辛香、木香、柑橘香、樟脑香、柠檬香及热带水果香气,多种烯烃类物质共同作用,赋予藤椒独特香气。醇类物质的阈值较高,但能与藤椒中的某些酸类物质形成藤椒特有的酯味香气[17]。根据挥发性风味物质含量由高到低排序为:VFD>自然阴干>HD>自然晒干。
表2 四种干燥方式藤椒的挥发性风味物质含量对比
Table 2 The flavor material content of dried Z. armatum DC in four drying methods
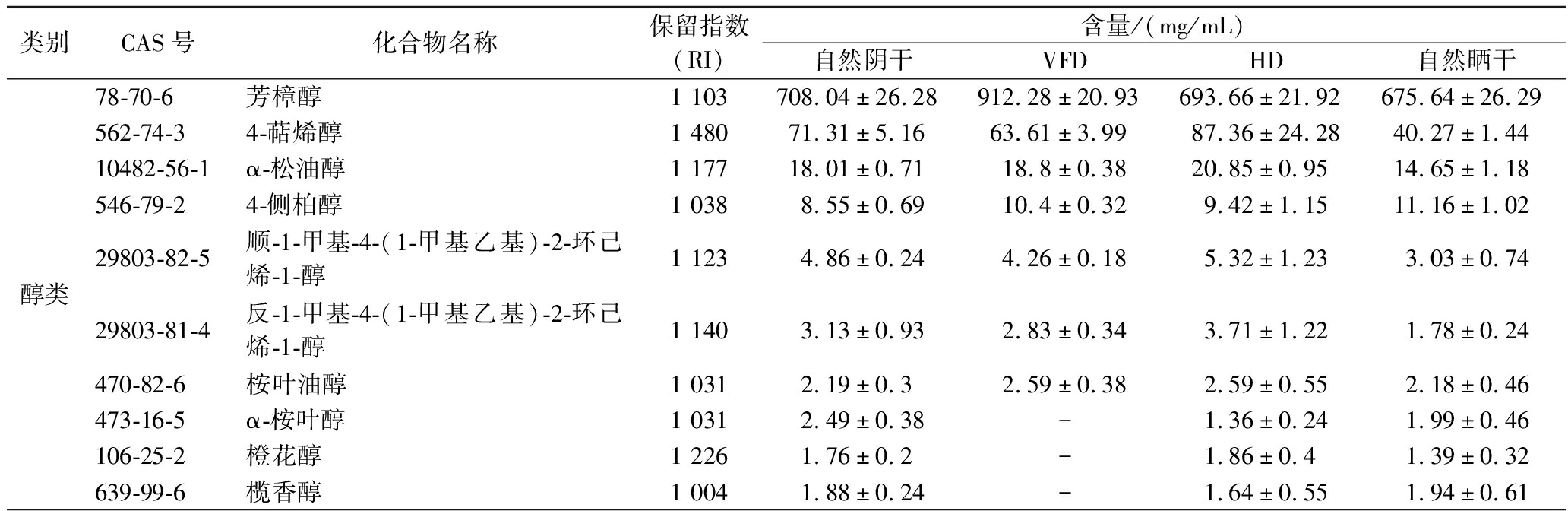
类别CAS号化合物名称保留指数(RI)含量/(mg/mL)自然阴干VFDHD自然晒干醇类78-70-6芳樟醇1 103708.04±26.28912.28±20.93693.66±21.92675.64±26.29562-74-34-萜烯醇1 48071.31±5.1663.61±3.9987.36±24.2840.27±1.4410482-56-1α-松油醇1 17718.01±0.7118.8±0.3820.85±0.9514.65±1.18546-79-24-侧柏醇1 0388.55±0.6910.4±0.329.42±1.1511.16±1.0229803-82-5顺-1-甲基-4-(1-甲基乙基)-2-环己烯-1-醇1 1234.86±0.244.26±0.185.32±1.233.03±0.7429803-81-4反-1-甲基-4-(1-甲基乙基)-2-环己烯-1-醇1 1403.13±0.932.83±0.343.71±1.221.78±0.24470-82-6桉叶油醇1 0312.19±0.32.59±0.382.59±0.552.18±0.46473-16-5α-桉叶醇1 0312.49±0.38-1.36±0.241.99±0.46106-25-2橙花醇1 2261.76±0.2-1.86±0.41.39±0.32639-99-6榄香醇1 0041.88±0.24-1.64±0.551.94±0.61
续表2

类别CAS号化合物名称保留指数(RI)含量/(mg/mL)自然阴干VFDHD自然晒干醇类473-15-4β-桉叶醇9262.02±0.32-1.38±0.411.64±0.36418-34-5α-毕橙茄醇1 191--1.7±0.931.5±0.5491-04-36-(异丙基)-3-甲基环己-2-烯-1-醇1 207--2.06±1.011.24±0.14烯烃类5989-27-5D-柠檬烯1 029400.22±3.25443.36±3.15397.42±13.4347.92±10.91555-10-2β-水芹烯975357.82±4.94361.25±4.59318.24±11.74293.94±5.14123-35-3月桂烯1 058114.41±2.05113.18±20.94102.5±1.2793.92±1.2413744-15-5荜澄茄油烯1 06763.03±0.5372.19±2.2545.85±1.2255.09±1.1287-44-5β-石竹烯1 41834.72±0.6636.32±1.5726.09±0.6828.16±0.627785-70-8蒎烯93237.2±1.1230.01±1.2833.42±1.6528.12±1.3329050-33-7蒈烯1 05825.01±0.7216.66±1.2631.68±1.2817.25±1.3399-85-4γ-松油烯1 05835.88±1.1430.13±1.0038.47±1.1219.6±1.0913466-78-93-蒈烯1 01020.05±0.7419.5±1.4917.8±1.3116.96±0.8224703-35-3双环大牛儿烯1 49518.57±0.3919.87±1.4512.61±0.7815.25±0.636753-98-6α-律草烯1 06715.9±0.3816.4±0.9712.08±1.1713.05±0.772867-05-2侧柏烯1 14011.15±0.288.29±0.827.96±0.67.27±0.7199-83-2水芹烯1 1228.93±0.559.36±1.238.68±0.647.7±0.57483-76-1杜松烯1 0162.76±0.353.22±1.352.03±0.111.6±0.5179-92-5莰烯1 0491.02±0.07-1.12±0.37-99-86-5松油烯1 01613.28±0.21--1.66±0.433779-61-1罗勒烯1 038---1.61±0.77586-62-9萜品油烯933--15.41±0.9811.69±0.73酯类115-95-7乙酸芳樟酯1 17713.65±0.414±0.6411.97±0.4813.42±1.2141-12-8(Z)-3,7-二甲基-2,6-辛二烯-1-醇乙酸酯1 1971.29±0.25-1.6±0.671.12±0.24628-97-7棕榈酸乙酯992-1.08±0.3--醛类〛112-31-2癸醛1 4187.47±0.518.01±1.367.23±0.236.53±1.1518486-69-6桃金娘烯醛1 3924.39±0.445.24±1.135.18±1.064.5±0.765392-40-5柠檬醛1 031--3.85±0.62-106-23-0香茅醛1 1032.86±0.383.01±0.963.16±0.382.85±0.28106-26-3橙花醛1 117--3.6±0.43-酮类471-15-8(-)-宁酮1 0886.57±0.297.84±1.517.59±0.886.59±0.9767690-48-6桧酮1 028-1.72±0.551.63±0.211.41±0.38
4种干燥方式处理后的藤椒在挥发性风味物质的种类存在明显的差别。4种干燥方式处理后的藤椒中,检测出的挥发性风味物质有41种,其中醇类13种,烯烃类18种,酯类3种,醛类5种,酮类2种;共有的挥发性风味物质有26种,其中醇类7种,烯烃类14种,酯类1种,醛类3种,酮类1种。HD处理后藤椒的挥发性风味物质种类最多,共38种,其中烯烃类物质16种,醇类物质13种,酯类物质2种,醛类物质5种,酮类物质2种;VFD处理后藤椒挥发性风味物质种类最少,共28种,其中醇类物质7种,烯烃类物质14种,酯类物质2种,醛类物质3种,酮类物质2种。VFD处理后藤椒的挥发性物质的种类在4种干燥方式中最少,可能是由于新鲜藤椒长时间处于真空环境,导致损失较多的香气种类。图3为4种干燥方式处理后得到的所有挥发性风味物质相对含量的热图,红色代表同种物质在某一样品中的含量高,蓝色则代表该物质在对应样品中的含量低[18]。自然阴干、VFD和HD处理后的挥发性物质种类的差别不大,而自然晒干后物质中有较大的损失,并且从颜色上能明显观察到VFD处理后的挥发性物质种类的相对含量较高。

图3 四种干燥方式藤椒挥发性风味物质相对含量热图对比
Fig.3 A thermogram comparison of the relative contents of volatile flavouring substances in Z. armatum DC following the application of four drying methods.
2.5 四种干燥方式新鲜藤椒挥发性物质PLS-DA分析
为进一步揭示不同干燥方式下新鲜藤椒挥发性物质的特征和差异,采用有监督的PLS-DA模型,模型中![]() 和
和![]() 表示所建模型对X和Y矩阵的解释率,Q2表示所建模型的预测能力,理论上R2和Q2接近1.0就说明模型拟合程度较好。通常情况下R2和Q2高于0.4即可接受,两者之差不应过大[19]。从图4-a可知,不同干燥方式处理后的藤椒样品分布在不同区域,说明样本成分之间存在较大差异,且拟合模型预测成分的累计统计量
表示所建模型对X和Y矩阵的解释率,Q2表示所建模型的预测能力,理论上R2和Q2接近1.0就说明模型拟合程度较好。通常情况下R2和Q2高于0.4即可接受,两者之差不应过大[19]。从图4-a可知,不同干燥方式处理后的藤椒样品分布在不同区域,说明样本成分之间存在较大差异,且拟合模型预测成分的累计统计量![]() 模型解释率参数
模型解释率参数![]() 预测能力参数Q2=0.94,均大于0.55,表示PLS-DA模型对不同干燥方式处理后干藤椒挥发性风味物质分析具有较好的可解释度和预测能力。4组样品在PLS-DA的分散点图聚类良好,各样本组间差异小,不同样本之间实现完全分离。置换检验结果如图4-b所示,模型Q2回归线与横坐标交叉,且交于Y轴负半轴,表明该模型可靠,不存在过拟合现象,表明该研究建立的PLS-DA模型稳定可靠,具有一定的统计学意义。
预测能力参数Q2=0.94,均大于0.55,表示PLS-DA模型对不同干燥方式处理后干藤椒挥发性风味物质分析具有较好的可解释度和预测能力。4组样品在PLS-DA的分散点图聚类良好,各样本组间差异小,不同样本之间实现完全分离。置换检验结果如图4-b所示,模型Q2回归线与横坐标交叉,且交于Y轴负半轴,表明该模型可靠,不存在过拟合现象,表明该研究建立的PLS-DA模型稳定可靠,具有一定的统计学意义。
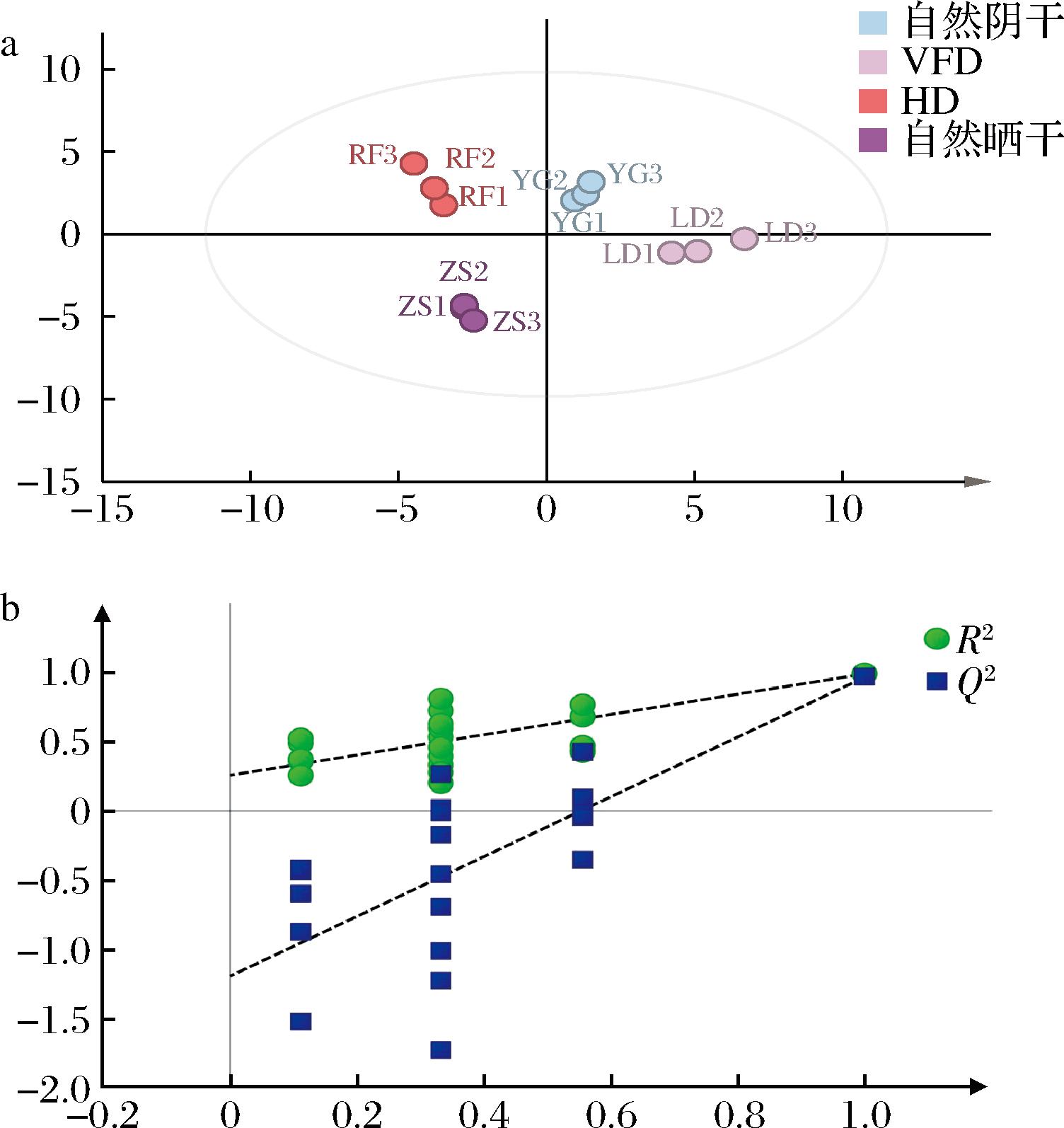
a-PLS-DA得分图;b-S-plot图
图4 不同干燥方式藤椒挥发性物质的PLS-DA
Fig.4 PLS-DA of Z. armatum DC volatiles with different drying methods
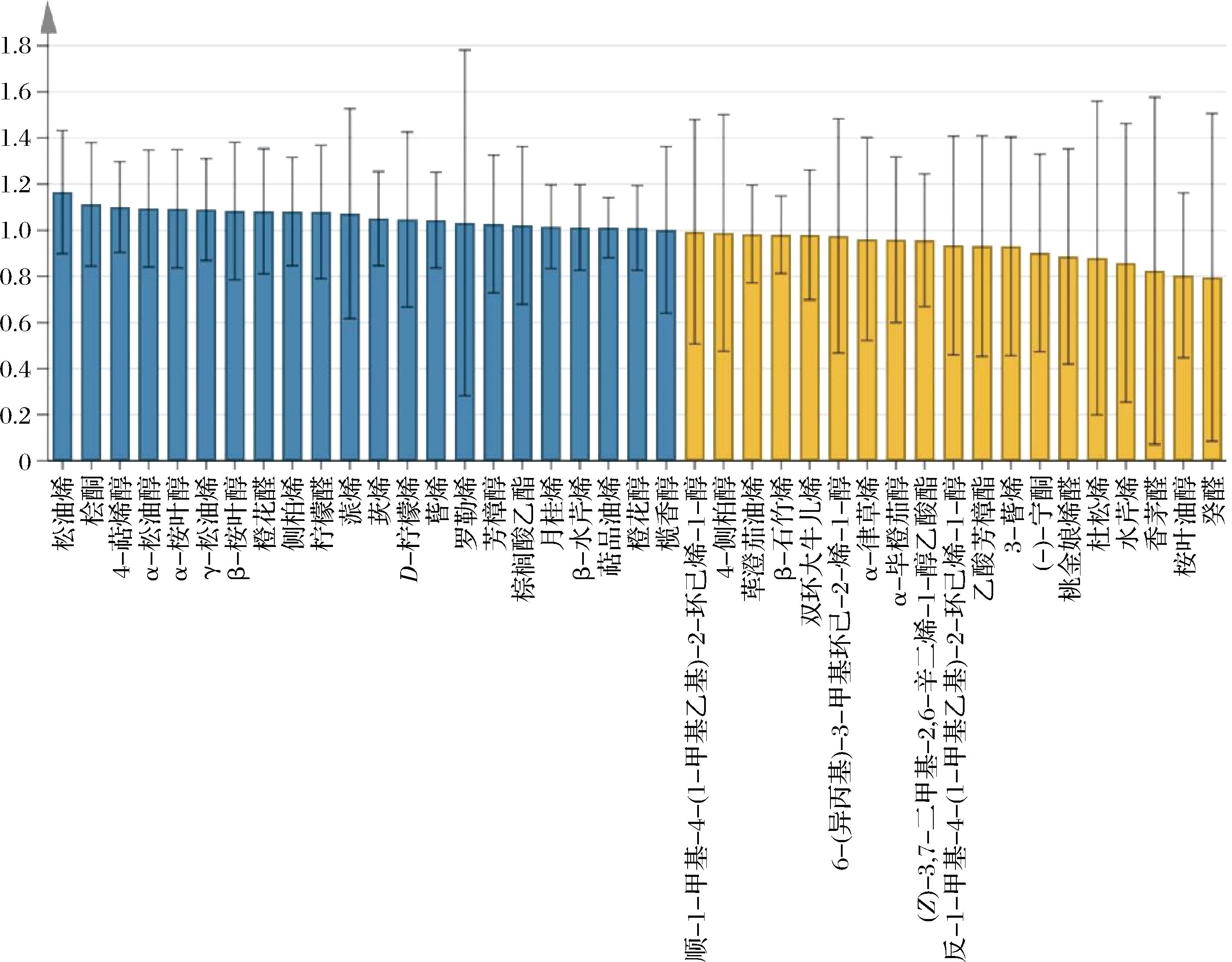
图5 不同干燥方式藤椒挥发性物质的VIP值
Fig.5 VIP values of Z. armatum DC volatiles with different drying methods
为进一步分析样本之间差异性挥发物质,进行了VIP值分析,VIP可反映风味物质对模型分类的贡献程度,衡量各组分累计差异对样本分类判别的影响程度和解释能力,VIP值越大其贡献率越大,通常将VIP>1作为筛选差异物质的标准[20]。由图4可知,共筛选出22种VIP>1的化合物,主要为烯烃类和醇类,包括松油醇(1.16),桧酮(1.11),4-萜烯醇(1.10),α-松油醇(1.09),α-桉叶醇(1.09),γ-松油烯(1.09),β-桉叶醇(1.08),橙花醛(1.08),侧柏烯(1.08),柠檬烯(1.08),蒎烯(1.07),莰烯(1.05),D-柠檬烯(1.05),蒈烯(1.04),罗勒烯(1.03),芳樟醇(1.03),棕榈酸乙酯(1.02),月桂烯(1.02),β-水芹烯(1.01),萜品油烯(1.01),橙花醇(1.01),榄香烯(1.00)。结合PLS-DA与挥发性风味物质含量分析可知,关键差异性物质在不同干燥过程中存在不同的变化趋势,烯烃类和醇类物质对干燥后的藤椒的风味具有重要的贡献,并且烯烃类和醇类物质含量的变化是造成新鲜藤椒在干燥过程中风味品质变化的重要因素。
3 结论
本研究对不同干燥方式处理的藤椒品质及风味成分进行测定。结果表明,4种干燥方式处理后的藤椒色泽存在较大差异,其中VFD处理后藤椒的色差优于另外3种处理方式。水分含量结果表明,HD处理后藤椒的水分含量最低,VFD的水分含量稍次于HD,但与HD处理后藤椒的水分含量差异不大。山椒素含量结果显示VFD处理后藤椒的山椒素含量最高。此外,不同干燥方式处理后藤椒的风味物质差异显著,HD处理后藤椒的风味物质的种类最多有38种,而VFD处理后藤椒的风味物质的含量最高共有2 235.407 mg/mL,并且使用PLS-DA分析筛选出22种(7种醇类、1种酮类、12种烯烃类、1种醛类、1种酯类)标志性差异化合物。综合上述指标结果进行评判,VFD是新鲜藤椒最适宜的干燥方式,并且由于利用HS-SPME-GC-MS/MS结合PLS-DA对干燥后藤椒风味物质的分析存在一定局限性,在后续的研究中,将进一步将GC-O、电子鼻和电子舌等分析检测技术与其他计量学技术相结合,为干燥处理后的藤椒的品质评定提供更加客观的依据。
[1] 闫紫玮, 谢天芳, 王佳琳, 等.藤椒果实成熟期麻味物质及其挥发性香气组分的变化规律[J].食品与发酵工业, 2024, 50(7):304-312.YAN Z W, XIE T F, WANG J L, et al.Variation of numb and volatile components in Zanthoxylum armatum DC.at different maturity stages[J].Food and Fermentation Industries, 2024, 50(7):304-312.
[2] 祝磊, 陈茜, 黎江华, 等.不同藤椒商品风味成分的分析研究[J].中国调味品, 2019, 44(1):141-146.ZHU L, CHEN X, LI J H, et al.Analysis and research on the flavor components of different Zanthoxylum armatum DC.commodities[J].China Condiment, 2019, 44(1):141-146.
[3] 陈艳, 李美凤, 饶朝龙, 等.新型藤椒酱加工工艺的研究[J].中国调味品, 2019, 44(2):114-117; 133.CHEN Y, LI M F, RAO C L, et al.Research on processing technology of new-type Zanthoxylum armatum sauce[J].China Condiment, 2019, 44(2):114-117; 133.
[4] PHUYAL N, JHA P K, PRASAD RATURI P, et al.Zanthoxylum armatum DC.:Current knowledge, gaps and opportunities in Nepal[J].Journal of Ethnopharmacology, 2019, 229:326-341.
[5] ALAM F, DIN K M, RASHEED R, et al.Phytochemical investigation, anti-inflammatory, antipyretic and antinociceptive activities of Zanthoxylum armatum DC extracts-in vivo and in vitro experiments[J].Heliyon, 2020, 6(11):e05571.
[6] 郭涛, 孙莉, 黄艳, 等.药食两用植物竹叶椒近五年药理活性研究进展[J].中国现代中药, 2013, 15(2):109-111.GUO T, SUN L, HUANG Y, et al.Review research progress on pharmacological activities of past five years on Zanthoxylum armatum DC[J].Modern Chinese Medicine, 2013, 15(2):109-111.
[7] XIA D, JIANG L Y, CHENG J X, et al.Influence of drying methods on quality of Zanthoxylum armatum DC.and mathematical modelling of the drying kinetics[J].E3S Web of Conferences, 2021, 269:02005.
[8] SRIWICHAI T, SOOKWONG P, SIDDIQUI M W, et al.Aromatic profiling of Zanthoxylum myriacanthum (makwhaen) essential oils from dried fruits using different initial drying techniques[J].Industrial Crops and Products, 2019, 133:284-291.
[9] 杨森, 冯靖雯, 刘友平, 等.热风干燥温度对竹叶花椒干燥特性及品质的影响[J].食品与发酵工业, 2021, 47(12):203-209.YANG S, FENG J W, LIU Y P, et al.The effect of hot air drying temperature on the drying characteristics and quality of Zanthoxylum armatum DC[J].Food and Fermentation Industries, 2021, 47(12):203-209
[10] 孟国栋, 彭桂兰, 罗传伟, 等.基于响应面法的花椒真空干燥工艺参数优化[J].食品与发酵工业, 2017, 43(10):137-143.MENG G D, PENG G L, LUO C W, et al.Optimization of vacuum drying parameters of Zanthoxylum bungeanum based on the response surface methodology[J].Food and Fermentation Industries, 2017, 43(10):137-143.
[11] 张艺, 张甫生, 宋莹莹, 等.干燥条件对青花椒色泽的影响[J].食品科学, 2014, 35(5):23-27.ZHANG Y, ZHANG F S, SONG Y Y, et al.Effects of different drying conditions on color change of green prickleyashes(Zanthoxylum schinifolium zucc.)[J].Food Science, 2014, 35(5):23-27.
[12] 周秀梅. 花椒间歇式热风干燥试验研究[D].重庆:西南大学, 2008.ZHOU X M.Experimental study on intermittent hot air drying of pepper[D].ChongQing:Southwest University, 2008.
[13] 吕健. 桃脆片加工工艺优化及品质评价研究[D].北京:中国农业科学院, 2013.LYU J.Research on the Processing optimization and quality evaluation for explosion puffing dried peach chips[D].Beijing:Chinese Academy of Agricultural Sciences, 2013.
[14] 汪洋, 阚建全.光照对鲜青花椒干燥过程中叶绿素降解的影响[J].食品科学, 2014, 35(3):10-15.WANG Y, KAN J Q.Chlorophyll breakdown in green prickleyash with illumination during drying[J].Food Science, 2014, 35(3):10-15.
[15] SUHARTA S, HUNAEFI D, WIJAYA C H.Changes in volatiles and aroma profile of andaliman (Zanthoxylum acanthopodium DC.) upon various drying techniques[J].Food Chemistry, 2021, 365:130483.
[16] 严雅丽, 刘福权, 赵志峰, 等.花椒羟基-α-山椒素在紫外照射下的降解动力学及其转化机理研究[J].食品与机械, 2017, 33(9):26-29.YAN Y L, LIU F Q, ZHAO Z F, et al.Degradation kinetics and transformation mechanism research of hydroxy-α-sanshool from Zanthoxylum bungeanum exposed to UV radiation[J].Food &Machinery, 2017, 33(9):26-29.
[17] 张宇, 彭子芯, 严雨寒, 等.花椒油和藤椒油加速氧化过程中风味品质变化[J].中国油脂, 2024, 49(2):33-41.ZHANG Y, PENG Z X, YAN Y H, et al.Changes of flavor quality of Zanthoxylum bungeanum Maxim.oil and Zanthoxylum armatum DC.oil during accelerated oxidation[J].China Oils and Fats, 2024, 49(2):33-41.
[18] 高夏洁, 高海燕, 赵镭, 等.SPME-GC-MS结合OAV分析不同产区花椒炸花椒油的关键香气物质[J].食品科学, 2022, 43(4):208-214.GAO X J, GAO H Y, ZHAO L, et al.Analysis of key aroma components in fried Zanthoxylum bungeanum oil from different production areas by solid phase microextraction-gas chromatography-mass spectrometry combined with odor activity value[J].Food Science, 2022, 43(4):208-214.
[19] 马雪莲, 王鹏, 耿敬章, 等.感官评价联合GC-MS与OPLS-DA解析加热温度对椒麻鸡赋味汤料呈香品质影响规律[J].食品科学, 2024, 45(17):127-134.MA X L, WANG P, GENG J Z, et al.Effect of heating temperature on the flavor quality of Xinjiang spicy chicken seasoning sauce investigated by sensory evaluation combined with GC-MS and OPLS-DA[J].Food Science, 2024, 45(17):127-134.
[20] 邵淑贤, 徐梦婷, 林燕萍, 等.基于电子鼻与HS-SPME-GC-MS技术对不同产地黄观音乌龙茶香气差异分析[J].食品科学, 2023, 44(4):232-239.SHAO S X, XU M T, LIN Y P, et al.Differential analysis of aroma components of Huangguanyin oolong tea from different geographical origins using electronic nose and headspace solid-phase microextraction-gas chromatography-mass spectrometry[J].Food Science, 2023, 44(4):232-239.