胶原蛋白是动物体内含量最多的蛋白质之一[1],在动物有机体蛋白质中约占33%[2]。根据结构,胶原蛋白可分为29种,其中I型胶原蛋白是脊椎动物结缔组织中最为常见的胶原蛋白[3]。胶原蛋白是由3条肽链构成的三螺旋结构,肽链中出现频率最高的氨基酸序列是-Gly-Y-Z,其中Gly是甘氨酸,X多为脯氨酸,Y多为4-羟基脯氨酸[4]。胶原蛋白单独应用于食品中时存在机械性能差、性能单一等问题,而当胶原蛋白与其他大分子互作后可有效改善胶原蛋白的相关功能特性。多糖是一类分子质量高、稳定性高、亲水性和可生物降解的天然聚合物,具有价格低廉、易获取、安全、无毒、可体内降解代谢、生物活性高等特点[5],常被用于与胶原蛋白互作制备复合物,如图1所示,加入多糖可以改善胶原蛋白的乳化性、凝胶特性和起泡性等特性,从而为胶原蛋白在食品中的应用提供新的研究思路[6-7],如用于制备纳米颗粒、水凝胶、保鲜薄膜和肠衣等。因此,本文通过综述胶原蛋白与多糖之间的互作机理,胶原蛋白与多糖互作对胶原蛋白微观结构和功能特性的影响、互作调控方法以及其在食品领域的应用进展,以期为后续胶原蛋白与多糖复合物在食品加工中新产品的研发、食品体系的改良等提供参考。
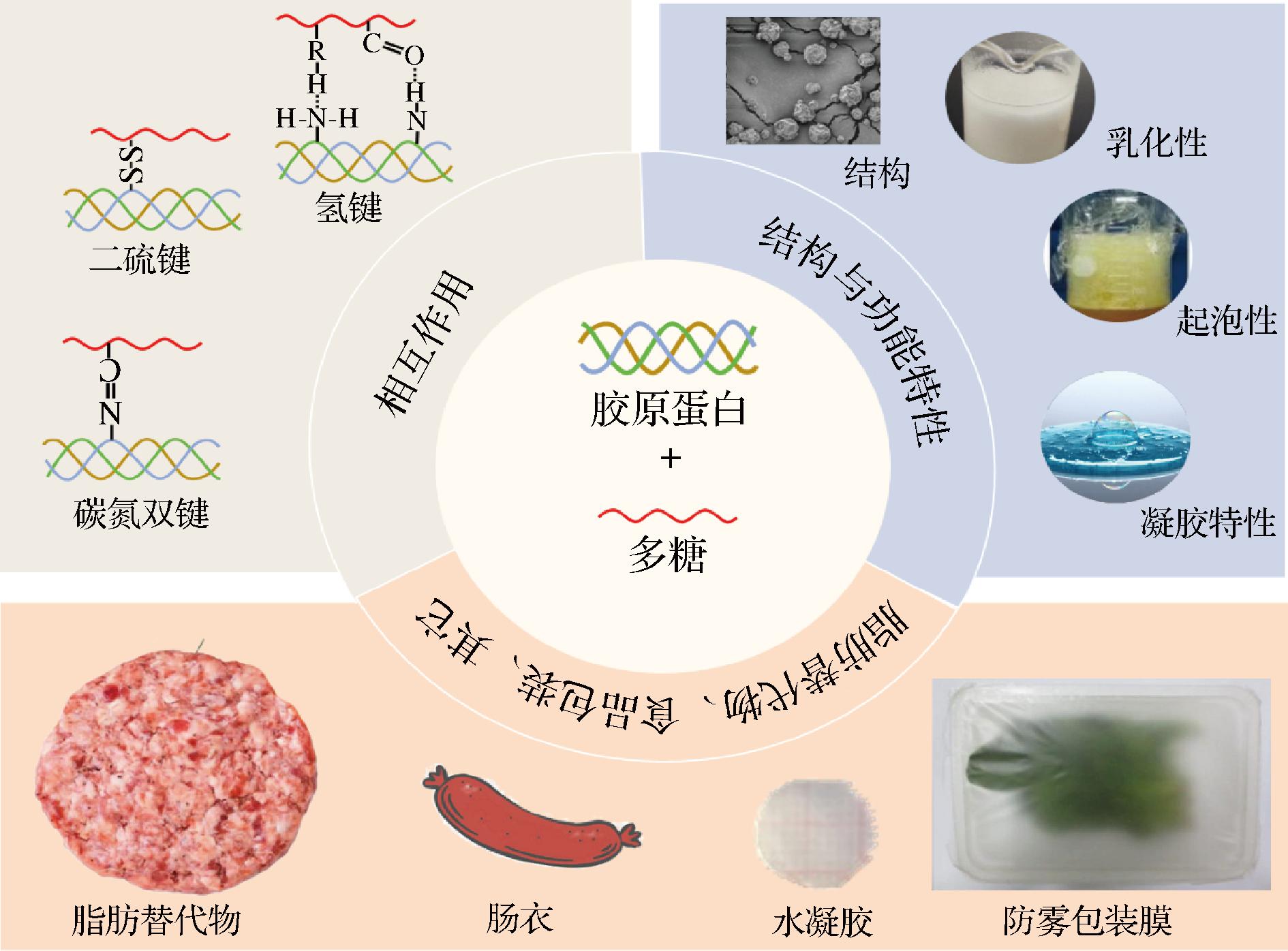
图1 胶原蛋白与多糖互作及其在食品中的应用
Fig.1 Interaction between collagen and polysaccharide and its application in food
1 胶原蛋白与多糖互作
胶原蛋白与多糖的相互作用是指胶原蛋白经物理、化学或生物处理后,在一定的浓度、体系pH等条件下与多糖物质进行互作。
近年来,胶原蛋白与多糖互作机理和调控方法研究逐渐深入,其互作复合物在食品领域应用范围越来越广,因此充分了解胶原蛋白与多糖相互作用机理和调控方法有利于深入研究胶原蛋白在食品中的应用。
1.1 胶原蛋白与多糖互作机理
胶原蛋白与多糖之间的相互作用力可简单分为共价作用和非共价作用,其中共价相互作用力主要是离子键、共价键,非共价相互作用力主要是静电相互作用、氢键、疏水相互作用等[8]。胶原蛋白与多糖共价作用主要指胶原蛋白的氨基和多糖的羧基共价结合形成酰胺以及其他共价键,如通过C![]() N键及糖苷键[9]等产生高度特异、不可逆的永久性共价结合。如图2所示,氧化藻酸钠经高碘酸盐氧化后形成的海藻酸双醛与胶原蛋白支链可通过C
N键及糖苷键[9]等产生高度特异、不可逆的永久性共价结合。如图2所示,氧化藻酸钠经高碘酸盐氧化后形成的海藻酸双醛与胶原蛋白支链可通过C![]() N键共价交联,而半乳甘露聚糖与胶原蛋白可通过美拉德反应形成共价复合物。因此胶原蛋白与多糖可以通过不同基团之间的共价作用不可逆结合,从而形成胶原蛋白与多糖复合物。
N键共价交联,而半乳甘露聚糖与胶原蛋白可通过美拉德反应形成共价复合物。因此胶原蛋白与多糖可以通过不同基团之间的共价作用不可逆结合,从而形成胶原蛋白与多糖复合物。
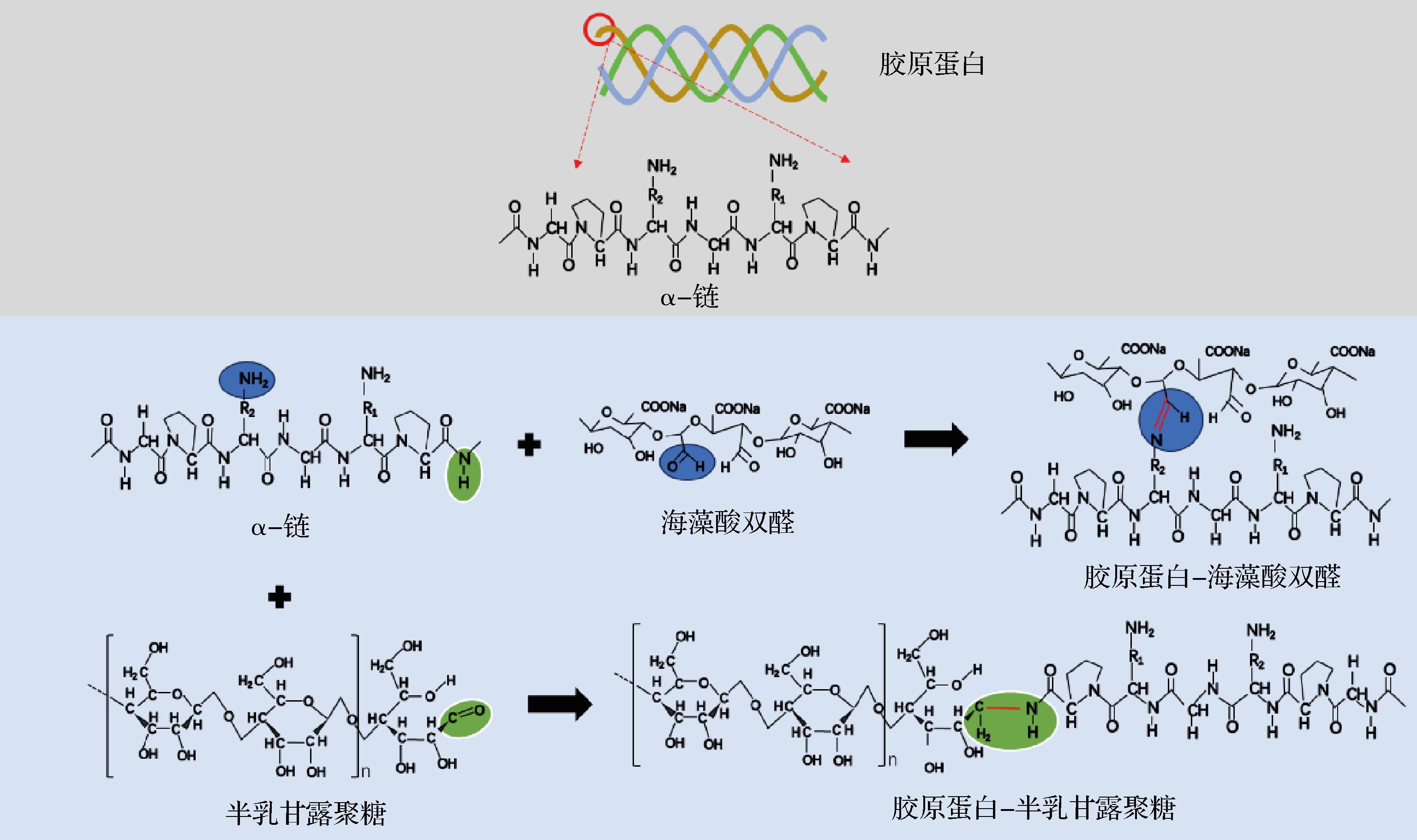
图2 胶原蛋白与多糖共价作用示例图[10-11]
Fig.2 An example of the covalent action of polysaccharide and collagen[10-11]
胶原蛋白与多糖也可通过疏水相互作用、静电相互作用或氢键形成非共价复合物[11]。SIONKOWSKA[12]研究表明,胶原蛋白-壳聚糖复合物形成中氢键和静电相互作用发挥主要作用,同时胶原蛋白中的阴离子基团与壳聚糖(阳离子多糖)之间形成了离子键。此外,MUHOZA等[13]和ANDONEGI等[14]研究发现胶原蛋白与壳聚糖之间的相互作用还存在氢键和范德华力。胶原蛋白与多糖相互作用研究如表1所示,由于多糖结构的多变性和介质环境的影响,造就了胶原蛋白与多糖复合物结构多样性,同时其互作的复杂性也随之增加,在胶原蛋白与多糖复合物的形成中大多是由共价和非共价作用共同发挥作用。
表1 胶原蛋白与多糖相互作用研究
Table 1 Study on interaction between polysaccharide and collagen

时间复合物作用类型参考文献1996胶原蛋白-壳聚糖静电相互作用、氢键[15]2004胶原蛋白-壳聚糖离子键、氢键[12]2008胶原蛋白-壳聚糖氢键、离子键[16]2011胶原蛋白-糖胺聚糖离子键、疏水相互作用[17] 2018胶原蛋白-葡甘聚糖氢键[18]2022胶原蛋白-海藻低聚糖羰氨缩合反应[9]
胶原蛋白与多糖互作复合物结构受胶原蛋白与多糖的性质、浓度、溶液pH、温度和相互作用力等因素的影响,体系中胶原蛋白与多糖浓度极低时两者不发生相互作用,只有当两者浓度升高到一定程度时才有相互作用发生。胶原蛋白与多糖相互作用模式如图3所示。当胶原蛋白与多糖带相反的电荷时,两者会团聚形成可溶性复合物(单相)或不溶性沉淀物(两相系统),如HU等[20]研究结果表明,胶原蛋白和海藻酸双醛相互作用形成的是不溶性沉淀物;而当两种非相互作用的胶原蛋白与多糖混合在一起时,它们或同时均匀分布于单相系统中,或胶原蛋白与多糖作为两个不同的相各自存在。当整个体系pH值发生改变时,会引起胶原蛋白与多糖的聚集或分离[19]。当pH>pI时,胶原蛋白与阴离子多糖之间相互排斥,两者倾向于发生相分离形成两相,此时两者之间若存在疏水相互作用,会形成不可溶性复合物;而当pH
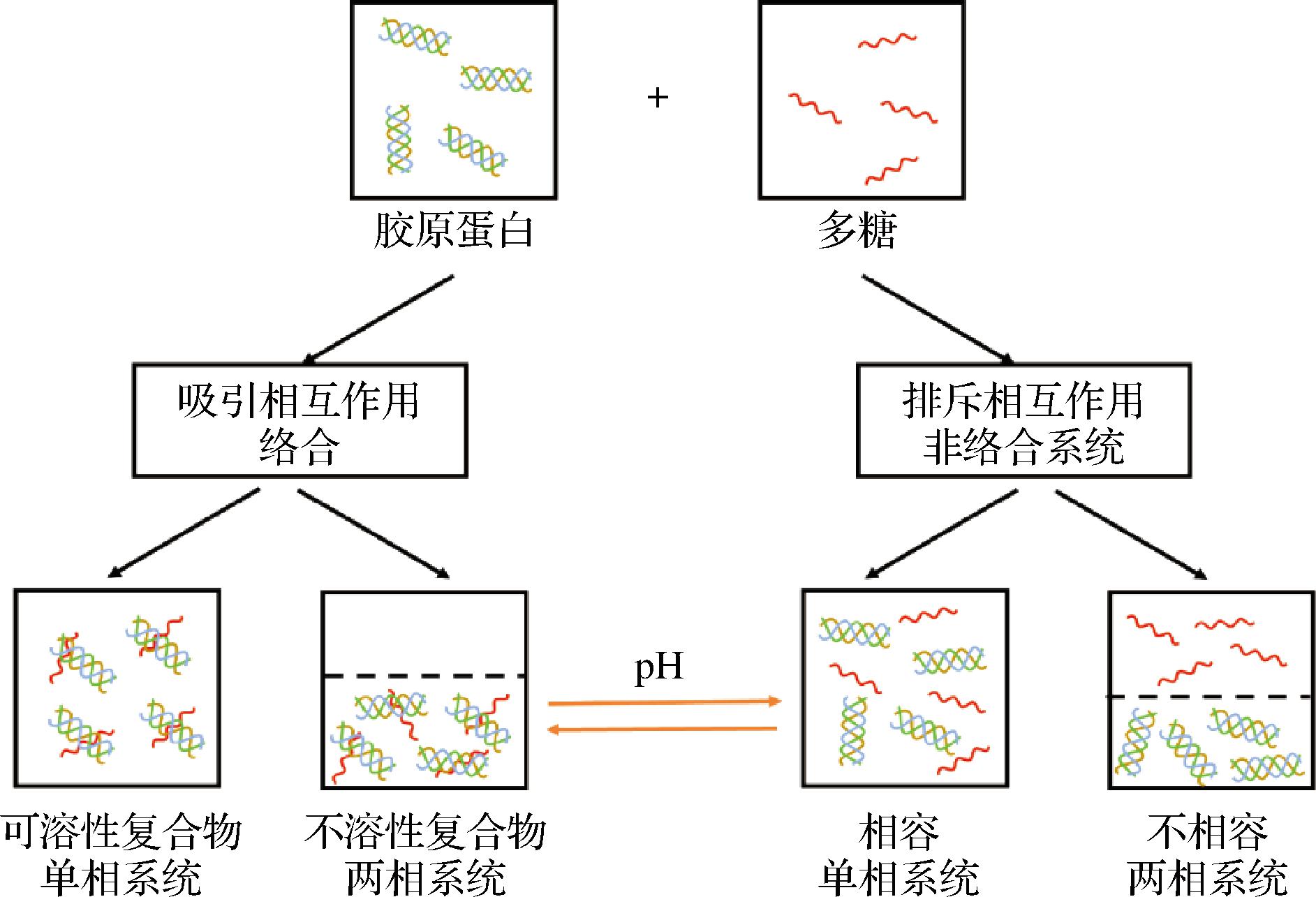
图3 胶原蛋白与多糖之间相互作用模式的示意图[19]
Fig.3 Schematic diagram of the interaction pattern between polysaccharide and collagen[19]
1.2 胶原蛋白与多糖互作调控
在食品工业中,常通过调控胶原蛋白与多糖之间的相互作用改善胶原蛋白相关特性,胶原蛋白与多糖互作的调控方法主要可分为3类:化学交联法、物理交联法和酶法交联[21],其互作交联示意图如图4所示。
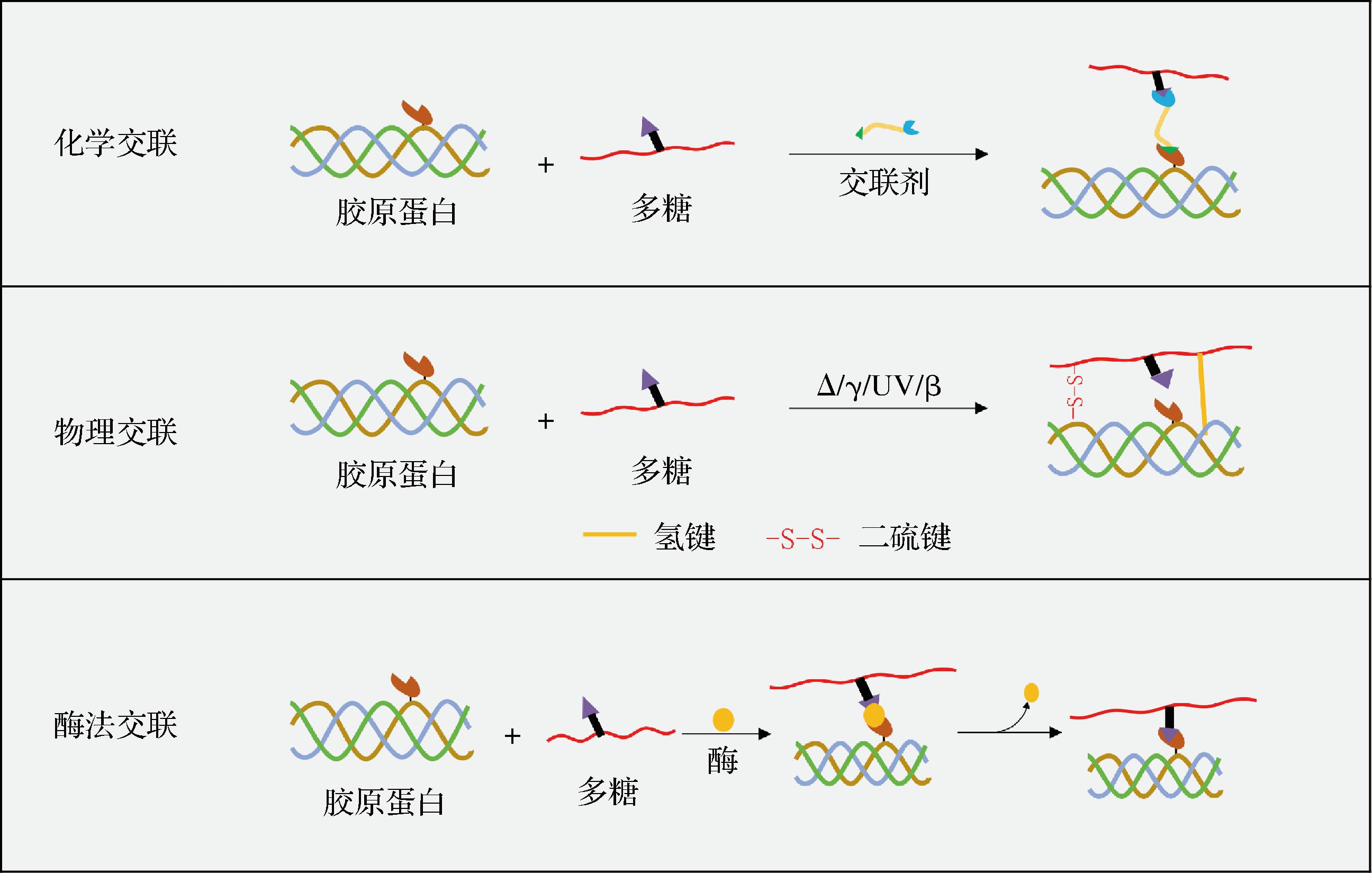
图4 胶原蛋白与多糖互作交联示意图[22]
Fig.4 Cross-linking diagram of collagen and polysaccharide[22]
1.2.1 化学交联法
化学交联法是在添加不同的化学交联剂后,引起多糖和胶原蛋白的氨基反应诱导胶原蛋白与多糖分子间进行交联产生新的互作复合物[22],常用化学交联试剂有戊二醛、乙二醛、甲醛、单宁酸和碳二胺等。MICHALSKA-SIONKOWSKA等[23]以单宁酸为交联剂制备了β-葡聚糖-鱼皮胶原蛋白膜,研究表明该β-葡聚糖-鱼皮胶原蛋白膜具有更好的力学性能,通过添加30% β-葡聚糖,该膜的抗撕裂性增强并使拉力增加了约 6.5 倍。FLOCEA等[24]以戊二醛为交联剂制备了壳聚糖/胶原蛋白为基料的水凝胶,结果表明,含有85%壳聚糖的胶原蛋白水凝胶可使毛果芸香碱缓释5 h以上,达到较好缓释效果。故通过使用化学交联法制备胶原蛋白-多糖复合物能有效改善胶原蛋白的部分功能特性,但由于某些交联剂可能存在毒性或生物不相容性,从而使化学交联法制备的胶原蛋白-多糖复合物的应用受到限制。
1.2.2 物理交联法
物理交联法主要是改变胶原蛋白与多糖互作环境的温度或利用紫外光、电离辐射等使得两者的氢键或其他键能活化,这些高度反应活性的自由基可催化胶原蛋白的肽骨架并产生分子间交联,在静电相互作用下诱导不同带电性的组分相互作用[22],主要包括热处理和电磁辐射(UV,γ,and β)等方法。DELGADO等[25]研究表明,紫外光可将单线态的核黄素激发为三线态,三线态的核黄素可与空气中的氧相互作用,将氧气转化为单线态,单线态的氧与胶原蛋白和葡甘聚糖通过分子相互作用,从而形成葡甘聚糖-胶原蛋白复合物。CHEN等[16]采用静电纺丝法制备了胶原蛋白-壳聚糖复合纳米纤维,其傅里叶变换红外光谱、差示扫描仪和单纳米纤维的力学表征结果表明,胶原的羰基、羟基、氨基与壳聚糖的羟基、氨基、羰基之间均产生了氢键从而形成胶原蛋白-壳聚糖复合纳米纤维。物理交联法制备胶原蛋白-多糖复合物可有效避免外源有毒化学物质进入组织,并产生了具有良好生物相容性的生物材料,但其交联位点及交联度的可控性还需要进一步研究。
1.2.3 酶法交联
酶法交联是指胶原蛋白与多糖在酶的作用下,促进胶原蛋白与多糖分子内和分子间的交联作用,交联后胶原蛋白分子结构发生变化,可有效改善胶原蛋白的持水性、凝胶性等功能特性[26]。酶法交联受酶的催化专一性影响,其交联位点专一性与可控性强,但交联过程及复合物性能易受所用酶的酶学特性限制。根据催化反应的类型,酶法交联剂中所用的酶可分为氧化还原酶、转移酶和水解酶,其中由于谷氨酰胺转氨酶具有良好的生物相容性,在胶原蛋白与多糖酶法交联中有较多研究[27]。如SCHWAB等[28]利用转氨酶使透明质酸和I型胶原蛋白在温和的条件下互作,成功制备了复合水凝胶。FAN等[29]以谷氨酰胺转移酶为生物催化剂合成壳聚糖与胶原蛋白复合膜。故酶法交联反应条件温和、专一性强,但其价格相对高昂。
2 胶原蛋白与多糖互作对胶原蛋白的影响
2.1 胶原蛋白与多糖互作对胶原蛋白微观结构的影响
胶原蛋白与多糖互作形成复合物会使胶原蛋白微观结构发生改变,从而影响胶原蛋白功能特性,通常可使用原子力显微镜、扫描电镜、荧光显微镜等观察胶原蛋白-多糖复合物的微观结构变化。刘磊[30]通过扫描电镜直观观察到胶原蛋白复合凝胶中添加凝结多糖后,多糖分子紧密吸附于胶原蛋白活性肽链上,使胶原蛋白与凝结多糖形成稳定的复合物,从而印证了该复合物质构、流变学特性的变化特点(图5-A)。MICHALSKA-SIONKOWSKA等[23]通过扫描电镜观察到胶原蛋白与β-葡聚糖复合膜呈现均匀光滑、材致密料,无孔结构,且由于β-葡聚糖允许水分子和活性物质通过的特性,使其较胶原蛋白膜有更好的通透性与生物相容性(图5-B)。VARGAS-MU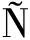 OZ等[31]通过荧光显微镜照片分析了水解胶原蛋白-麦芽糊精复合物制备的微胶囊粒径分布(图5-C),可清晰看到水解胶原蛋白-麦芽糊精复合颗粒呈中空、小孔隙结构,可有效负载5-咖啡酰奎宁酸并达到缓释的作用。
OZ等[31]通过荧光显微镜照片分析了水解胶原蛋白-麦芽糊精复合物制备的微胶囊粒径分布(图5-C),可清晰看到水解胶原蛋白-麦芽糊精复合颗粒呈中空、小孔隙结构,可有效负载5-咖啡酰奎宁酸并达到缓释的作用。

A-凝结多糖(TBR)-胶原蛋白(Col)复合凝胶材料的微观结构[30](a:放大倍数为1 000的V5%TBR∶VCol=1∶1; b:放大倍数为5 000的V5%TBR∶VCol=1∶1; c:放大倍数为1 000的V10%TBR∶VCol=1∶1; d:放大倍数为5 000的V10%TBR∶VCol=1∶1; e:放大倍数为1 000的V15%TBR∶VCol=1∶1; f:放大倍数为5 000的V15%TBR∶VCol=1∶1);B-胶原蛋白/β-葡聚糖(BG)材料横截面的扫描电子显微镜图像[23] (a:Col∶BG= 100∶0; b:Col∶BG=90∶10; c:Col∶BG=70∶30; d:Col∶BG= 50∶50(ω/ω));C-水解胶原蛋白-麦芽糊精微胶囊包封椰子粉荧光显微图像(a:使用10×物镜;b: 使用40×物镜,麦芽糊精:水解胶原蛋白的比例(MD∶HC)为20∶80)[31]
图5 胶原蛋白与多糖复合物微观结构
Fig.5 Microstructure of polysaccharide and collagen complex
2.2 胶原蛋白与多糖互作对胶原蛋白微观结构的影响
长期以来,胶原蛋白的功能特性一直都是研究重点,而胶原蛋白与多糖互作对胶原蛋白功能特性的影响是研究的热点内容之一。已有研究表明胶原蛋白与多糖互作可改善胶原蛋白的乳化特性、凝胶特性和起泡性及起泡稳定性等诸多功能特性。
2.2.1 胶原蛋白与多糖互作对胶原蛋白乳化特性的影响
胶原蛋白的乳化特性包括乳化性与乳化稳定性,乳化性是指胶原蛋白能使油与水形成稳定乳状液的能力,乳化稳定性是指胶原蛋白保持油和水混合不分离的乳化特性耐外部条件应变的能力[32]。胶原蛋白与多糖互作使胶原蛋白内部疏水基团暴露,从而胶原蛋白能快速迁移到油水界面,同时多糖的存在可以使油滴之间产生一定的空间排斥力,抑制乳液液滴之间的聚集和絮凝,从而有效改善胶原蛋白的乳化特性。申璇等[33]研究发现,通过美拉德反应糖基化,可一定程度上改善胶原蛋白的乳化活性及乳化稳定性。FU等[34]的研究也表明,通过超声波辅助木糖对大鲵鱼皮胶原蛋白进行糖化改性,其乳化活性和乳化稳定性得到显著增强,乳化活性约15 m2/g,乳化稳定性达60%以上。
2.2.2 胶原蛋白与多糖互作对胶原蛋白凝胶特性的影响
凝胶特性指胶原蛋白分子在水溶液中受到诱导因子影响,体系内作用力达到平衡状态,形成具有三维网络空间结构的蛋白质体系[35]。胶原蛋白的凝胶特性使其能将各类食品成分结合在一起,既能起到增稠的作用,还可以形成固态凝结[36]。胶原蛋白与多糖互作对胶原蛋白凝胶特性的影响机理研究尚未完全明晰,但已有研究表明,胶原蛋白与多糖互作可能通过降低其永久形变的幅度而增强凝胶弹性。FRANCIS-SEDLAK等[37]研究了糖基化对I型胶原蛋白凝胶特性的影响,结果表明糖基化使鼠尾胶原蛋白的黏弹性增强。PROESTAKI等[38]研究表明,添加足够高浓度的透明质酸,透明质酸与胶原蛋白互作所形成的凝胶更呈线性和更具弹性。故通过胶原蛋白与多糖相互作用,能有效改善胶原蛋白的凝胶特性。
2.2.3 胶原蛋白与多糖互作对胶原蛋白起泡性及其稳定性的影响
起泡性是指溶液中的蛋白质分子在空气-水界面处的吸附能力及在界面处发生构象的重排,通过分子间相互作用形成黏弹性膜的能力[39]。胶原蛋白起泡性及其稳定性对食品质地等感官品质能够产生重大影响,有研究表明,胶原蛋白与多糖互作是改善胶原蛋白起泡性和起泡稳定性的有效手段。LEWANDOWSKA等[40]研究了胶原蛋白、透明质酸和壳聚糖的二元和三元复合物的结构和表面性质,研究表明,与二元复合物相比,含有透明质酸和壳聚糖的胶原蛋白混合物的稳定性更好。胶原蛋白与壳聚糖聚集体的泡沫稳定性较胶原蛋白强[41],在啤酒乳制品加工中具有较好的应用前景。
3 胶原蛋白与多糖复合物在食品中的应用
由于胶原蛋白与多糖互作可改善胶原蛋白的凝胶特性、乳化特性、起泡性及其稳定性等功能特性,使其广泛应用于保持或改善食品的结构、质地、风味、口感等品质。
3.1 胶原蛋白与多糖复合物在食品降脂中的应用
过度肥胖可能引发健康问题,随着大众消费观念和水平的改变,对低脂肪食品需求量增加的同时对其感官品质也有了更高的要求。已有研究表明,胶原蛋白与多糖复合物可用于替代香肠食品中的脂肪。HAM等[42]研究发现,使用胶原蛋白与膳食纤维复合物替代猪肉脂肪,对于发酵香肠冷藏期间感官颜色、风味、异味或整体可接受性(P>0.05)等方面均无显著影响,故该复合物可作为发酵香肠中猪肉背脂肪的替代品。FAN等[43]用燕麦β-葡聚糖-海洋胶原肽混合形成了具有较高硬度、黏结性、弹性和嚼劲的典型凝胶,并具有较高的持水和吸油能力,可作为减脂香肠中的猪脂肪替代品,从而提高产品的营养价值。BAJCIC等[44]研究得出,用胶原蛋白-菊粉悬浮液完全替代煮熟乳化香肠生产中猪肉背膘的香肠具有良好的感官性能,且游离脂肪和胆固醇含量较低。多糖-胶原蛋白复合物也可作为低脂鸡肉饼的脂肪替代物使用。KIM等[45]研究在低脂鸡肉饼中加入20%胶原蛋白、10%小麦芽纤维和70%冰的预乳液部分替代猪脂肪,可使低脂鸡肉饼色泽、蒸煮损失等品质特性得到改善,从而满足消费者需要。
3.2 胶原蛋白与多糖复合物在食品包装中的应用
胶原蛋白与多糖复合物所制备的纳米颗粒、水凝胶、薄膜和肠衣等材料,能有效避免活性分子(香料和生物活性物质)、肉制品、新鲜蔬果等受到外部剧烈条件(如热、剪切力、温度、光、氧气、水分等)的影响[19]。WANG等[46]制备了琼脂/海藻酸盐/胶原蛋白与银纳米颗粒和葡萄柚籽提取物水凝胶薄膜的三元混合物,结果表明,掺入银纳米颗粒或葡萄柚籽提取物的三元共混水凝胶薄膜不仅可以用作高呼吸新鲜农产品的防雾包装膜,还可以利用其强大的抗菌活性制备活性食品包装材料。MICHALSKA-SIONKOWSKA等[23]研究了胶原蛋白-壳聚糖复合凝胶对山竹提取物的释放能力,结果表明,胶原蛋白-壳聚糖凝胶复合凝胶显示出高溶胀值,有利于山竹提取物的释放。ARPORNMAEKLONG等[47]研究表明,含有5%纳米羟基磷灰石颗粒-壳聚糖/胶原水凝胶的1%碳酸钙微胶囊可用于输送槲皮素,能够达到缓释目的。KRKI 等[48]制备了胶原蛋白-壳聚糖复合膜作为香肠肠衣,其研究发现胶原蛋白-壳聚糖复合膜与胶原蛋白膜相比,其阻氧性能得到了显著提高,故该复合膜更适合作为香肠肠衣。ZHENG等[49]开发了用于监测4 ℃贮藏猪肉新鲜度的基于胶原蛋白、壳聚糖、ZnO纳米颗粒和桑葚提取物的pH敏感薄膜,结果表明当猪肉中总挥发性碱性氮含量超过最大允许限值(15 mg/100 g)时,该薄膜的颜色由深紫色变为蓝色,从而达到监测效果。大量研究表明,由于胶原蛋白与多糖复合物膜较好的通透性与生物相容性,使其在食品包装等领域具有较大的应用潜力,用于制备农产品的防雾包装膜、活性成分缓释载体、肠衣、智能包装材料等。
等[48]制备了胶原蛋白-壳聚糖复合膜作为香肠肠衣,其研究发现胶原蛋白-壳聚糖复合膜与胶原蛋白膜相比,其阻氧性能得到了显著提高,故该复合膜更适合作为香肠肠衣。ZHENG等[49]开发了用于监测4 ℃贮藏猪肉新鲜度的基于胶原蛋白、壳聚糖、ZnO纳米颗粒和桑葚提取物的pH敏感薄膜,结果表明当猪肉中总挥发性碱性氮含量超过最大允许限值(15 mg/100 g)时,该薄膜的颜色由深紫色变为蓝色,从而达到监测效果。大量研究表明,由于胶原蛋白与多糖复合物膜较好的通透性与生物相容性,使其在食品包装等领域具有较大的应用潜力,用于制备农产品的防雾包装膜、活性成分缓释载体、肠衣、智能包装材料等。
3.3 其他应用
近几年来,研究学者发现,胶原蛋白-多糖复合物还可用于改善食品感官品质、作为3D打印生物墨水、制备胶原蛋白制剂和保健食品等。VARGAS-MU OZ等[31]研究了胶原蛋白、组织化大豆蛋白和麦芽糊精两两相互作用对牛肉汉堡品质的影响,结果表明加入胶原蛋白-麦芽糊精复合物的牛肉汉堡在感官接受度方面的认可度高于加入麦芽糊精和大豆蛋白-胶原蛋白复合物。LIU等[50]研究表明,胶原蛋白-壳聚糖复合水凝胶有用于原位3D生物打印生物墨水的潜力。SUO等[51]使用胶原蛋白-壳聚糖复合溶液制备了一系列具有良好印刷适性的生物墨水。HUA等[52]以鱼皮胶原蛋白和壳聚糖溶液为原料,采用离子交联法制备生物活性胶原蛋白/壳聚糖复合物,研究发现该复合物是具有增强抗氧化和抑制黑色素合成的潜在口服蛋白制剂。胶原蛋白-多糖复合物由于其更优的功能特性和生物活性,在食品工业中表现出了较大的应用价值与推广潜力。
OZ等[31]研究了胶原蛋白、组织化大豆蛋白和麦芽糊精两两相互作用对牛肉汉堡品质的影响,结果表明加入胶原蛋白-麦芽糊精复合物的牛肉汉堡在感官接受度方面的认可度高于加入麦芽糊精和大豆蛋白-胶原蛋白复合物。LIU等[50]研究表明,胶原蛋白-壳聚糖复合水凝胶有用于原位3D生物打印生物墨水的潜力。SUO等[51]使用胶原蛋白-壳聚糖复合溶液制备了一系列具有良好印刷适性的生物墨水。HUA等[52]以鱼皮胶原蛋白和壳聚糖溶液为原料,采用离子交联法制备生物活性胶原蛋白/壳聚糖复合物,研究发现该复合物是具有增强抗氧化和抑制黑色素合成的潜在口服蛋白制剂。胶原蛋白-多糖复合物由于其更优的功能特性和生物活性,在食品工业中表现出了较大的应用价值与推广潜力。
4 结论与展望
胶原蛋白与多糖互作中,多糖种类、结构与性质和改性方法等对胶原蛋白结构和功能特性的改善作用存在差异,使其成为胶原蛋白改性研究中的重点研究内容。本文主要对胶原蛋白与多糖相互作用以及其互作复合物在食品工业中的应用进行了综述。但目前有关胶原蛋白互作仍有许多问题亟待进一步深入研究:a)利用新技术(如分子模拟)、先进的设备进一步明晰胶原蛋白与多糖相互作用的复杂过程;b)通过胶原蛋白与不同类型多糖互作,比较其作为食品乳化剂、增稠剂等的能力差异,选择出更佳的互作复合物应用于食品工业中;c)通过胶原蛋白与多糖互作制备的低脂食品、食品包装材料、3D打印生物墨水、胶原蛋白制剂和保健品等如何进行工业化生产和应用。随着这些研究工作的不断深入,胶原蛋白与多糖互作及其复合物在食品及其他相关领域的应用将会得到进一步的推动和拓展。
[1] 高玲玲, 侯成立, 高远, 等.胶原蛋白热稳定性研究进展[J].中国食品学报, 2018, 18(5):195-207.GAO L L, HOU C L, GAO Y, et al.Research advances of thermal stability of collagen[J].Journal of Chinese Institute of Food Science and Technology, 2018, 18(5):195-207.
[2] ESPINALES C, ROMERO-PE A M, CALDER
A M, CALDER N G, et al.Collagen, protein hydrolysates and chitin from by-products of fish and shellfish:An overview[J].Heliyon, 2023, 9(4):e14937.
N G, et al.Collagen, protein hydrolysates and chitin from by-products of fish and shellfish:An overview[J].Heliyon, 2023, 9(4):e14937.
[3] LIU H, ZHANG H R, WANG K Y, et al.Impact of ultrasonication on the self-assembly behavior and gel properties of bovine bone collagen I[J].Molecules, 2023, 28(7):3096.
[4] ZHAO Y D, LU K Y, PIAO X Y, et al.Collagens for surimi gel fortification:Type-dependent effects and the difference between type I and type Ⅱ[J].Food Chemistry, 2023, 407:135157.
[5] SIONKOWSKA A.Collagen blended with natural polymers:Recent advances and trends[J].Progress in Polymer Science, 2021, 122:101452.
[6] ZHU L L, LI J W, WANG Y C, et al.Structural feature and self-assembly properties of type Ⅱ collagens from the cartilages of skate and sturgeon[J].Food Chemistry, 2020, 331:127340.
[7] 刘睿, 蔡朔, 赵珂璇, 等.鹿皮胶Ⅰ型胶原赖氨酸位点的羟基化与O-糖基化修饰分析[J].中国中药杂志, 2021, 46(3):591-598.LIU R, CAI S, ZHAO K X, et al.Analysis of hydroxylation and O-glycosylation on lysine sites in Deer-hide gelatin[J].China Journal of Chinese Materia Medica, 2021, 46(3):591-598.
[8] DICKINSON E.Biopolymer-based particles as stabilizing agents for emulsions and foams[J].Food Hydrocolloids, 2017, 68:219-231.
[9] YANG B X, JOE G H, LI W Z, et al.Comparison of Maillard-type glycated collagen with alginate oligosaccharide and glucose:Its characterization, antioxidant activity, and cytoprotective activity on H2O2-induced cell oxidative damage[J].Foods, 2022, 11(15):2374
[10] HUANG X T, ZHANG Y, ZHENG X, et al.Origin of critical nature and stability enhancement in collagen matrix based biomaterials:Comprehensive modification technologies[J].International Journal of Biological Macromolecules, 2022, 216:741-756.
[11] LI Y, CHEN K N, YANG Q F, et al.Development and characterization of novel antioxidant films based on chitosan and Maillard reaction products[J].LWT, 2021, 141:110886.
[12] SIONKOWSKA A.Molecular interactions in collagen and chitosan blends[J].Biomaterials, 2004, 25(5):795-801.
[13] MUHOZA B, XIA S Q, ZHANG X M.Gelatin and high methyl pectin coacervates crosslinked with tannic acid:The characterization, rheological properties, and application for peppermint oil microencapsulation[J].Food Hydrocolloids, 2019, 97:105174.
[14] ANDONEGI M, HERAS K L, SANTOS-VIZCA NO E, et al.Structure-properties relationship of chitosan/collagen films with potential for biomedical applications[J].Carbohydrate Polymers, 2020, 237:116159.
NO E, et al.Structure-properties relationship of chitosan/collagen films with potential for biomedical applications[J].Carbohydrate Polymers, 2020, 237:116159.
[15] TARAVEL M N, DOMARD A.Collagen and its interactions with chitosan Ⅲ.Some biological and mechanical properties[J].Biomaterials, 1996, 17(4):451-455.
[16] CHEN Z G, MO X M, HE C L, et al.Intermolecular interactions in electrospun collagen-chitosan complex nanofibers[J].Carbohydrate Polymers, 2008, 72(3):410-418.
[17] ORI A, WILKINSON M C, FERNIG D G.A systems biology approach for the investigation of the heparin/heparan sulfate interactome[J].Journal of Biological Chemistry, 2011, 286(22):19892-19904.
[18] LIU L L, WEN H G, RAO Z Q, et al.Preparation and characterization of chitosan-collagen peptide/oxidized konjac glucomannan hydrogel[J].International Journal of Biological Macromolecules, 2018, 108:376-382.
[19] AMIT K, BANDYOPADHYAY P.Polysaccharide-protein Interactions and Their Relevance in Food Colloids[M].Intech Open, 2012.
[20] HU Y, LIU L, GU Z P, et al.Modification of collagen with a natural derived cross-linker, alginate dialdehyde[J].Carbohydrate Polymers, 2014, 102:324-332.
[21] HU T Y, LO A C Y.Collagen-alginate composite hydrogel:Application in tissue engineering and biomedical sciences[J].Polymers, 2021, 13(11):1852.
[22] BENBETTAÏEB N, GAY J P, KARBOWIAK T, et al.Tuning the functional properties of polysaccharide-protein bio-based edible films by chemical, enzymatic, and physical cross-linking[J].Comprehensive Reviews in Food Science and Food Safety, 2016, 15(4):739-752.
[23] MICHALSKA-SIONKOWSKA M, ![]() 'G1SKA O, KACZMAREK-SZCZEPA
'G1SKA O, KACZMAREK-SZCZEPA SKA B, et al.Preparation and characterization of fish skin collagen material modified with β-glucan as potential wound dressing[J].Materials, 2021, 14(6):1322.
SKA B, et al.Preparation and characterization of fish skin collagen material modified with β-glucan as potential wound dressing[J].Materials, 2021, 14(6):1322.
[24] FLOCEA P, VERESTIUC L, POPA M, et al.Crosslinked networks based on polysaccharides and collagen for pilocarpine sustained release[J].Journal of Macromolecular Science, Part A, 2010, 47(6):616-625.
[25] DELGADO L M, FULLER K, ZEUGOLIS D I. Collagen cross-linking:Biophysical, biochemical, and biological response analysis[J].Tissue Engineering.Part A, 2017, 23(19-20):1064-1077.
[26] GU L S, SHAN T T, MA Y X, et al.Novel biomedical applications of crosslinked collagen[J].Trends in Biotechnology, 2019, 37(5):464-491.
[27] YUAN Y, LI M, CHEN Q Z, et al.Crosslinking enzyme lysyl oxidase modulates scleral remodeling in form-deprivation myopia[J].Current Eye Research, 2018, 43(2):200-207.
[28] SCHWAB A, HÉLARY C, RICHARDS R G, et al.Tissue mimetic hyaluronan bioink containing collagen fibers with controlled orientation modulating cell migration and alignment[J].Materials Today Bio, 2020, 7:100058.
[29] FAN L H, WU H, ZHOU X Y, et al.Transglutaminase-catalyzed grafting collagen on chitosan and its characterization[J].Carbohydrate Polymers, 2014, 105:253-259.
[30] 刘磊. 罗非鱼鳞胶原蛋白与多糖复合材料的制备及表征[D].南宁:广西大学, 2022.LIU L.Peparation and characterization of tilapia scale collagen and polysaccharide composites[D].Nanning:Guangxi University, 2022.
[31] VARGAS-MU OZ D P, CARDOSO DA SILVA L, NEVES DE OLIVEIRA L A, et al.5-caffeoylquinic acid retention in spray drying of cocona, an Amazonian fruit, using hydrolyzed collagen and maltodextrin as encapsulating agents[J].Drying Technology, 2021, 39(12):1854-1868.
OZ D P, CARDOSO DA SILVA L, NEVES DE OLIVEIRA L A, et al.5-caffeoylquinic acid retention in spray drying of cocona, an Amazonian fruit, using hydrolyzed collagen and maltodextrin as encapsulating agents[J].Drying Technology, 2021, 39(12):1854-1868.
[32] HECK T, FACCIO G, RICHTER M, et al.Enzyme-catalyzed protein crosslinking[J].Applied Microbiology and Biotechnology, 2013, 97(2):461-475.
[33] 申璇, 袁久刚, 王强, 等.糖化改性对胶原蛋白乳化性能的影响[J].生物学杂志, 2017, 34(5):20-23; 42.SHEN X, YUAN J G, WANG Q, et al.Effects of glycosylated modification on emulsifying properties of collagen[J].Journal of Biology, 2017, 34(5):20-23; 42.
[34] FU J J, YU J X, HE F Y, et al.Physicochemical and functional characteristics of glycated collagen protein from giant salamander skin induced by ultrasound Maillard reaction[J].International Journal of Biological Macromolecules, 2024, 254:127558.
[35] 刘思迪, 王百龙, 黄敏丽, 等.淀粉-蛋白混合体系的制备、理化特性及应用研究进展[J].食品科学, 2022, 43(1):345-352.LIU S D, WANG B L, HUANG M L, et al.Progress in the preparation, physicochemical properties and application of starch-protein mixed systems[J].Food Science, 2022, 43(1):345-352.
[36] 陈峰, 杨帅伶, 刘宾.微藻蛋白质及其在食品中的应用研究进展[J].中国食品学报, 2022, 22(6):21-32.CHEN F, YANG S L, LIU B.Microalgal protein and research progress on application in foods[J].Journal of Chinese Institute of Food Science and Technology, 2022, 22(6):21-32.
[37] FRANCIS-SEDLAK M E, URIEL S, LARSON J C, et al.Characterization of type I collagen gels modified by glycation[J].Biomaterials, 2009, 30(9):1851-1856.
[38] PROESTAKI M, SARKAR M, BURKEL B M, et al.Effect of hyaluronic acid on microscale deformations of collagen gels[J].Journal of the Mechanical Behavior of Biomedical Materials, 2022, 135:105465.
[39] 丁俭, 黄祯秀, 杨梦竹, 等.食源蛋白水解物/多肽与糖类物质美拉德反应产物在食品应用中的研究进展[J].食品科学, 2023, 44(1):305-318.DING J, HUANG Z X, YANG M Z, et al.Review and prospect of Maillard reaction products from food-derived protein hydrolysates/peptides and saccharides in food application and research[J].Food Science, 2023, 44(1):305-318.
[40] LEWANDOWSKA K, SIONKOWSKA A, GRABSKA S, et al.Surface and thermal properties of collagen/hyaluronic acid blends containing chitosan[J].International Journal of Biological Macromolecules, 2016, 92:371-376.
[41] 叶童. 三文鱼鱼皮胶原/壳聚糖自聚集行为研究[D].上海:上海海洋大学, 2022.YE T.Study on the self-aggregation behavior of collagen/chitosan in salmon (salmo salar)skin[D].Shanghai:Shanghai Ocean University, 2022.
[42] HAM Y K, HWANG K E, KIM H W, et al.Effects of fat replacement with a mixture of collagen and dietary fibre on small calibre fermented sausages[J].International Journal of Food Science &Technology, 2016, 51(1):96-104.
[43] FAN R, ZHOU D, CAO X L.Evaluation of oat β-glucan-marine collagen peptide mixed gel and its application as the fat replacer in the sausage products[J].PLoS One, 2020, 15(5):e0233447.
[44] BAJCIC A, PETRONIJEVIC R, SUVAJDZIC B, et al.Use of inulin-collagen suspension for the total replacement of pork backfat in cooked-emulsified sausages[J].Journal of Food and Nutrition Research, 2023, 62(1):35-45.
[45] KIM T K, HWANG K E, SUNG J M, et al.Replacement of pork back fat with pre-emulsion of wheat (Triticum aestivum L.) sprout and collagen and its optimization for reduced-fat patties[J].Journal of Food Processing and Preservation, 2018, 42(4):e13576.
[46] WANG L F, RHIM J W.Preparation and application of agar/alginate/collagen ternary blend functional food packaging films[J].International Journal of Biological Macromolecules, 2015, 80:460-468.
[47] ARPORNMAEKLONG P, JAIMAN N, APINYAUPPATHAM K, et al.Effects of calcium carbonate microcapsules and nanohydroxyapatite on properties of thermosensitive chitosan/collagen hydrogels[J].Polymers, 2023, 15(2):416.
[48] KRKI N, LAZIC V, PETROVIC L, et al.Properties of chitosan-laminated collagen film[J].Food Technology and Biotechnology, 2012, 50:483-489.
N, LAZIC V, PETROVIC L, et al.Properties of chitosan-laminated collagen film[J].Food Technology and Biotechnology, 2012, 50:483-489.
[49] ZHENG T T, TANG P P, LI G Y.Development of a pH-sensitive film based on collagen/chitosan/ZnO nanoparticles and mulberry extract for pork freshness monitoring[J].Food Chemistry, 2023, 402:134428.
[50] LIU Y D, LUO X, WU W, et al.Dual cure (thermal/photo) composite hydrogel derived from chitosan/collagen for in situ 3D bioprinting[J].International Journal of Biological Macromolecules, 2021, 182:689-700.
[51] SUO H R, ZHANG J Y, XU M G, et al.Low-temperature 3D printing of collagen and chitosan composite for tissue engineering[J].Materials Science &Engineering.C-Materials for Biological Applications, 2021, 123:111963.
[52] HUA Y Y, MA C J, WEI T T, et al.Collagen/chitosan complexes:Preparation, antioxidant activity, tyrosinase inhibition activity, and melanin synthesis[J].International Journal of Molecular Sciences, 2020, 21(1):313.