大豆不仅是全球种植最广泛的经济作物之一,而且是可持续和可再生的优质蛋白质来源[1]。大豆蛋白含有多种必需氨基酸、其生物效价与动物蛋白相当,营养价值突出,并具有乳化性、凝胶性等多种功能特性,以大豆蛋白为基础的功能蛋白配料的研究和开发广受研究者青睐。凝胶特性是大豆蛋白作为食品成分的重要功能特性之一,利用大豆蛋白的凝胶性加工食品已有两千多年历史,比如传统豆制品(豆腐)及现代肉类类似物、肉类制品和香肠制品的黏合剂、大豆酸奶、活性物质的载体等[2]。
蛋白凝胶是由蛋白质分子间通过氢键、离子键、范德华力以及静电相互作用进行交联所形成的三维凝胶网络[3]。凝胶中蛋白-蛋白间相互作用在很大程度上决定了蛋白质的凝胶强度。凝胶网络的强度和稳定性决定了肉类类似物及其他相关产品基质的流变、质地、微观结构和感官特性,对食品加工有重要意义[4]。大豆蛋白以球蛋白和伴球蛋白为主,在形成凝胶时,聚集驱动力以非共价相互作用为主。由于大豆蛋白本身溶解性不佳、聚集体结构无序、含硫基团少,导致其形成的凝胶质地粗糙、结构松散、稳定性差,无法满足消费者对凝胶产品的品质需求[5]。通过不同修饰技术对大豆蛋白的结构基础进行修饰可获得具有良好功能特性的蛋白配料,有助于现代食品工业的发展。
在大豆蛋白凝胶特性改善的方式中,物理、化学和酶修饰等方法已被广泛应用。其中物理修饰和酶修饰是常用的绿色、高效修饰方法,两者通过调控大豆蛋白的结构来改善其凝胶特性。酶修饰是目前蛋白质修饰研究的热点,包括酶交联和酶水解,因其高效、安全、反应条件温和、反应速度快和底物特异性而在食品工业中广受欢迎[6]。基于大豆蛋白分子的球状结构特征,致密的高疏水性结构域意味大量的功能基团被掩蔽在蛋白质分子内部,降低了酶水解和酶交联效果。因此,适度地预处理可破坏大豆蛋白的有序结构,改变大豆蛋白因分子间化学作用力而产生的聚集行为,进而暴露更多的作用位点,有利于促进酶水解或酶交联反应的进行,改善大豆蛋白的凝胶特性[7-8]。物理修饰和酶修饰可以相互协同作用,通过物理场的作用促进生物酶的催化效果,从而实现更好的大豆蛋白凝胶修饰效果。
1 大豆蛋白的凝胶性
1.1 大豆蛋白凝胶的形成机理
大豆蛋白按沉降系数可分为2S、7S、11S、15S四种。大豆蛋白凝胶主要是球蛋白凝胶,其凝胶化可以通过加热、加酸、加酶和加盐等方式诱导,按诱导方式的不同可分为两大类:热致凝胶和非热致凝胶。
大豆蛋白热致凝胶的形成是一个复杂的过程,可以分为4个步骤:天然蛋白变性、球蛋白小聚集体解离、随机聚集形成聚集体、聚集体延伸形成凝胶网络[9](如图1)。加热处理可诱导球状蛋白质分子发生不可逆展开,暴露出与相邻蛋白质分子形成的功能性基团,包括疏水基团和巯基。疏水基团的暴露促进蛋白质分子之间的疏水相互作用,巯基的暴露可以引发二硫化物-巯基交换反应,以疏水相互作用和二硫键为主的蛋白间分子作用力是凝胶形成过程中蛋白质聚集和交联的主要驱动力,此时形成可逆的自相似聚集体且颗粒尺寸增加。最后,超过临界蛋白质浓度,聚集体间进一步交联,形成三维网络结构,即形成蛋白凝胶[10-11]。凝胶网络的形成是蛋白-蛋白和蛋白-水吸引和排斥相互平衡作用的结果。大豆蛋白的凝胶特性在食品中起着至关重要的作用,其质构特性和流变特性以及持水性影响着消费者对食品的选择[12]。
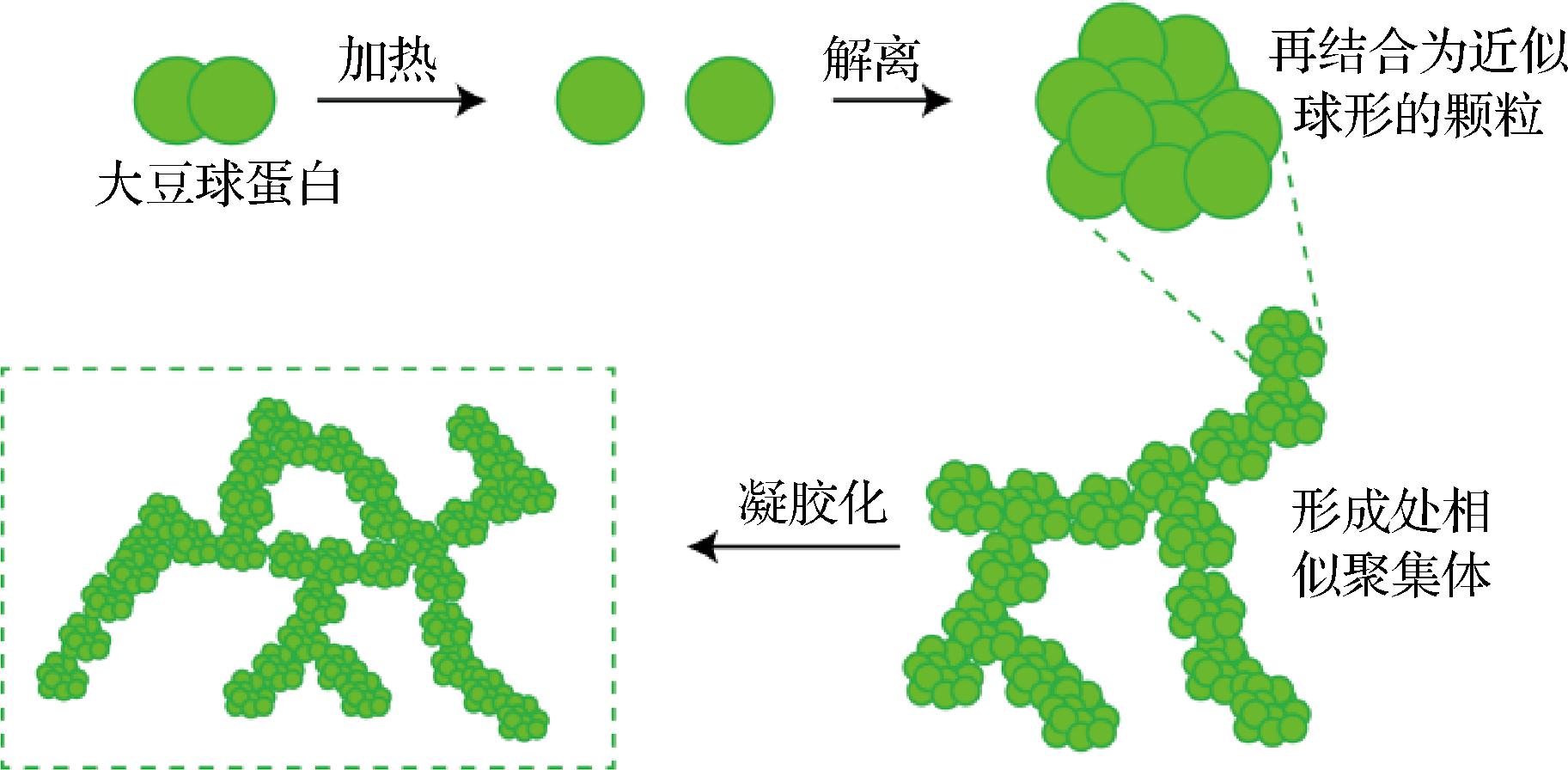
图1 大豆球蛋白热诱导凝胶形成过程示意图[9]
Fig.1 Schematic representation of the different steps leading to gelation of soy protein isolate in aqueous solutions during heating[9]
大豆蛋白非热致凝胶是由所加盐、酸或酶诱导形成的蛋白凝胶。蛋白凝胶的具体形成机制虽然不同,但其形成过程的基本原理是一致的。从本质上讲,所有蛋白基凝胶的形成都是蛋白质分子通过各种分子间作用力聚集在一起或紧密相互作用,形成一个三维网络空间结构的过程[13]。在非热致蛋白凝胶形成的过程中,加盐能屏蔽带负电荷的蛋白质分子免受静电相互作用的影响,可有效诱导蛋白质聚集交联,影响凝胶形成;加酸是通过改变体系pH,影响蛋白所带净电荷数,从而改变蛋白质分子所处环境,使蛋白质分子发生聚集和凝胶化;酶是通过酶催化交联蛋白质分子形成凝胶。
1.2 大豆蛋白凝胶特性的修饰方法
目前常用的大豆蛋白凝胶修饰方法主要包括3类,分别为物理、化学以及酶法修饰。这些修饰方法的单独或联合作用导致蛋白质结构发生改变,进而影响蛋白质的聚集状态和理化性质,以达到改善大豆蛋白凝胶特性的目的。
物理修饰是指利用外界物理场的作用来改变蛋白分子间聚集体大小和蛋白质的高级结构,进而改善蛋白质的凝胶特性。常见的物理修饰方法包括热处理、高压均质处理、超声波处理、微波处理等[14]。这些方法可通过改变大豆蛋白的分子结构和相互作用力来调控其凝胶特性。物理修饰方法条件较温和、操作简单、节能环保、可持续性好,在保持蛋白质营养特性的同时,还可对其功能特性加以改善[15]。
化学修饰是指利用化学手段对大豆蛋白的表面基团进行修饰。常见的化学修饰方法有碱处理、酸处理、糖基化、磷酸化和酰化等。这些化学手段可诱导蛋白质构象的改变,从而改变蛋白质的聚集和凝胶行为。化学修饰虽然具有反应简单、应用普遍和效果显著等特点,但在此过程中可能会产生一些有毒的化学副产物,存在一些有争议的安全问题,限制其广泛应用[16]。
酶修饰是指利用生物酶催化作用来改变大豆蛋白的结构和功能。生物酶可以通过水解、交联等反应来改变大豆蛋白的化学结构和功能基团的暴露及交联程度,从而影响其凝胶特性。由于酶的高生物降解性、特异性、效率和催化速率,使酶修饰技术备受关注,越来越多的研究者使用酶来改善大豆蛋白的凝胶特性[17]。复合修饰法能结合多种修饰方法的优点,进一步改善蛋白的凝胶性能。比如谷氨酰胺转氨酶(transglutaminase,TG)能够单独用于蛋白质的修饰,改善蛋白凝胶性能,但若与其他修饰方法联合使用时,对凝胶性能的改善效果则更加显著[18]。
2 物理场对大豆蛋白凝胶特性的影响
2.1 热处理对大豆蛋白凝胶特性的影响
大豆蛋白经热处理后分子结构发生变化是形成凝胶的重要基础。在热处理过程中,大豆蛋白发生分子变性与结构解离,导致隐藏的活性位点暴露,促使不同蛋白质中的功能基团通过共价键(二硫键)与非共价键(例如疏水相互作用、静电作用和氢键等)相互作用,从而形成较大尺寸的聚合体,并最终形成具有三维网络结构的凝胶体系[19]。
热处理过程中加热条件的改变,如加热温度、加热时间等,可以改变大豆蛋白的变性和聚集程度,进而改善其凝胶性能[20]。加热温度不同,大豆蛋白变性程度也不同,大豆7S球蛋白和11S球蛋白的变性温度分别在75 ℃和85 ℃左右。LI等[21]在80、90、100 ℃的预热温度和10~180 s预热时间下对大豆分离蛋白(soybean protein isolate,SPI)进行热诱导变性,得到不同热变性程度的SPI,结果表明,一定程度的预变性能改善蛋白凝胶的性能,部分预变性蛋白(SPI 22.28%和SPI 86.11%)凝胶的微观形态比天然蛋白(SPI 0)和完全预变性蛋白(SPI 100%)凝胶的微观形态更致密、更均匀,且随热变性程度的增加,SPI的凝胶硬度、储能模量和持水能力随之增加,凝胶形成所需的加热时间减少,但过度预变性使蛋白形成更大聚集体,凝胶空腔大,形态不均匀,凝胶性能变差。武雅琴[22]也证实了这个观点,与天然SPI、60 ℃热处理SPI和95 ℃热处理SPI相比,80 ℃热处理的SPI暴露的疏水基团和巯基基团的含量显著增多,储能模量也显著增加,进而对凝胶性能有显著性改善。对大豆蛋白分子进行一定程度的预热处理可改善其凝胶性能,而过度的预热处理则对其凝胶性能有不利影响。
2.2 高压均质处理对大豆蛋白凝胶特性的影响
高压均质处理是一种非热物理修饰方法,在保持加工食品营养成分的同时,还可改善其感官特性,因而被广泛应用于大豆蛋白凝胶的制备。高压均质过程中大豆蛋白在压力和剪切力作用下,分子间氢键和疏水相互作用发生改变,分子结构重组、交联,多数球状蛋白的三、四级结构被破坏,影响大豆蛋白凝胶能力[23]。
一定范围内,随着高压均质处理压力和次数的增加,大豆蛋白的凝胶能力逐渐增强。KEERATI-U-RAI等[24]发现均质过程中的高机械力使大豆蛋白分子结构被破坏,7S球蛋白和11S球蛋白聚集且聚集体重排,11S球蛋白比7S球蛋白更易形成可溶性聚集体。KANG等[25]探究了不同均质压力水平(50~150 MPa)对大豆11S球蛋白凝胶性能的影响,发现100 MPa高压均质处理能够显著提高蛋白溶解度,同时减小颗粒尺寸,增加表面疏水性和二硫键含量,其起泡能力和稳定性、凝胶性能均有所改善。KANG等[26]亦证实蛋白质溶解性的提高和分子间作用力的增加能够有效促进凝胶的形成,并改善凝胶质地。SUN等[27]研究发现在100 MPa高压下,循环次数的增加能促使SPI形成相对稳定和坚硬的凝胶结构,以抵抗较大的外力。此外,高压均质的压力和循环次数对SPI二级结构也有着显著影响,在100 MPa高压均质条件下循环3次,大豆蛋白中β-折叠的相对含量最高,此时微观形态更加均匀、致密,这是由于更高的β-折叠含量意味着更多的侧链,可以为分子链之间的相互作用和蛋白质的结构变化提供有利的环境,提高凝胶体系的硬度[28]。高压均质处理有利于大豆蛋白分子疏水区域的暴露,增强蛋白质之间的疏水相互作用,使凝胶的硬度、咀嚼性和弹性均得到改善。高压均质处理具有加工时间短、压力小、对营养和感官品质影响小等优点,是一种安全的物理修饰技术。
2.3 超声波处理对大豆蛋白凝胶特性的影响
超声被认为是一种绿色且有效改善蛋白理化性质的技术,在食品工业中用于蛋白修饰。超声波作用于物质时所产生的空化剪切力具有破坏蛋白质之间或内部非共价键(如氢键和疏水键)的作用能力,导致蛋白质内部的疏水基团、巯基得以暴露,并影响聚集体颗粒的尺寸,同时增加可溶性聚集体的含量[29]。
超声波处理时间和功率影响蛋白颗粒尺寸和分子间作用力,进而对蛋白的凝胶特性产生影响。ZHENG等[30]研究了不同高强度低频超声波处理时间(0、10和25 min)对天然SPI理化性质的影响,结果表明超声波处理25 min后,SPI的二级和三级结构发生改变,颗粒尺寸减小,溶解度增加,SPI凝胶的强度和持水性均有显著提高,同时超声波时间越长,凝胶网络越厚,分布更均匀。HU等[31]发现经高强度超声波处理20 min后,蛋白间共价相互作用(二硫键)和非共价相互作用(静电相互作用、疏水相互作用、氢键)增强,SPI的粒径减小,凝胶的微观形态光滑平整、均匀致密,孔隙小,此时SPI凝胶的持水量、凝胶强度和凝胶硬度均达到最高。刘冉等[32]发现与低功率超声波和高功率超声波处理相比,中功率(200~600 W)超声波可以显著改善SPI凝胶性能,加速凝胶三维网状结构的形成。极端的高超声波强度(特别是在高功率水平或长超声波时间下)会对蛋白质的理化特性和最终食品产品的质量产生负面影响[33]。一定的超声波时间(15~25 min)和功率(200~600 W)处理大豆蛋白,其凝胶的持水性和凝胶硬度均有所提高,凝胶的微观形态更加均匀和致密,大豆蛋白凝胶性能得到改善。超声波处理使加工食品功能特性得到显著提高,能较好地保存热不稳定的食品成分,并且经济环保、能耗少、实施和操作简单,是一种很有前途和实用的蛋白修饰技术。
2.4 微波处理对大豆蛋白凝胶特性的影响
微波辐射作为电磁场的一部分,对蛋白质的影响是热效应和非热效应的混合[34]。微波直接渗透到食物内部,利用偶极子旋转和离子电导加热内部,实现快速加热,使得二硫键和氢键等遭到破坏,蛋白质分子结构的展开,在疏水相互作用、氢键以及二硫键等分子间相互作用的协同作用下,蛋白质分子聚集形成较高分子质量的集合体[35]。
微波处理时间和功率的不同对蛋白凝胶特性产生的影响也不同。BHATTACHARYA等[36]对脱脂豆粉分散体在微波中进行不同时间(0~75 s)的处理,随着微波处理时间的增加,凝胶的硬度和弹性亦随之增加,大豆蛋白凝胶形成了具有纤维的多孔排列凝胶网络结构。QIN等[37]研究证实微波处理可以使大豆与小麦混合蛋白的疏水基团暴露、游离巯基含量降低,凝胶网络的微观形貌更致密和均匀,进而提高了TG酶诱导的混合蛋白凝胶强度、持水性和硬度,并改变了动态黏弹性,且在微波预处理700 W时,凝胶强度、持水性和储能模量均达到最大值。LIU等[38]发现与传统沸水浴加热处理相比,微波加热处理的葡萄糖-内酯诱导的SPI凝胶,具有较优良的黏弹性和微观结构。致密均匀的微观结构可能有助于将水结合在凝胶中,与结构不均匀的蛋白凝胶相比,结构均匀且精细的凝胶往往具有更高的持水性和凝胶强度。微波处理可以提高大豆蛋白凝胶的凝胶强度、稳定性和持水性,并且是一种快速、方便和经济高效的蛋白修饰方法,由于加热时间短,与其他加热方式相比对营养物质的保存效果更好。
2.5 挤压处理对大豆蛋白凝胶特性的影响
挤压技术作为一种物理修饰方法,利用高温、高压和机械剪切来改变了蛋白的聚集性质和构象,蛋白质分子展开可暴露其内部的疏水基团,在非共价键和共价键的共同作用下形成分子质量较大的聚集体结构,随着持续的挤压处理,蛋白质分子进一步聚集、交联和分离,沿着轴向有序排列,并最终形成网络状结构。
挤压过程中的一些参数,如水分含量、挤压温度、进料速度和螺杆速度等对蛋白质结构变化和交联聚集行为有很大影响,这使得蛋白挤出物具有不同的理化性质和结构特性,进而对凝胶特性产生影响[39]。CHEN等[40]对SPI进行低水分(28%)和高水分(60%)挤出,发现60%高水分挤出可增加SPI分子间二硫键与氢键、二硫键与疏水键之间的相互作用,这些结构的变化改善了大豆蛋白的凝胶特性,且无论挤出水分含量如何,二硫键与疏水相互作用、静电相互作用、氢键等非共价键及其相互作用共同保持了蛋白质挤出物的结构,非共价键的贡献>共价键。SINGH等[41]研究发现,挤压温度从150 ℃降低至110 ℃,挤出物的成胶能力呈增加趋势。110 ℃的挤压温度使大豆蛋白变性,从而使疏水性氨基酸暴露在蛋白质分子表面,高表面疏水性通常有利于蛋白质的凝胶形成能力。而在较高的挤压温度下可能会发生更广泛的蛋白质聚集,导致一些疏水位点被掩埋,使它们难形成凝胶。作为挤压关键参数之一的挤压温度,对巯基-二硫键的交换和疏水相互作用有重要影响,挤压温度决定了挤压产品的外观和质地。挤压处理被明确地应用于蛋白质中,以形成新的结构,如组织化蛋白和膨化食品,其中高水分挤压是一种新兴的、有前途的物理修饰技术。
2.6 冷等离子体处理对大豆蛋白凝胶特性的影响
冷等离子体作为一种非热食品加工技术,通常在30~60 ℃下进行,由于其具有消灭食品中微生物和蛋白质修饰的能力,逐渐受到了研究者的广泛关注。冷等离子体产生的活性物质可以暴露蛋白质表面的活性位点,并促进蛋白中巯基的氧化,从而增加蛋白-蛋白间和蛋白-水分子之间的相互作用[42]。
王然等[43]采用冷等离子体技术处理SPI,结果发现经冷等离子体处理60 s后,SPI的二、三级结构发生变化,游离巯基含量增多,表面疏水性提高,SPI的微观形态呈现更均匀的聚集。分子间疏水相互作用增强以及游离巯基氧化形成分子间的二硫键,均有利于蛋白质凝胶的形成。冷等离子体技术的使用可能对凝胶产品的物理和功能特性产生积极的影响,是一种极具潜力的蛋白质修饰技术。
3 生物酶对大豆蛋白凝胶特性的影响
酶修饰是通过蛋白水解酶和蛋白交联酶来改变蛋白质的结构进而改善其功能特性的技术。20世纪70年代末,蛋白酶(水解酶)是蛋白质修饰酶的主要类别。然而,随着参与蛋白质交联的TG出现,蛋白质修饰技术的种类得到了拓展[44]。TG、漆酶、过氧化物酶和酪氨酸酶等已被证明具有促进蛋白质交联的能力。其中,TG在食品工业中的应用最为广泛[17]。酶修饰蛋白质的技术与其他修饰技术相比有许多优点,比如高反应特异性;副反应频率低;并且不需要高温高压条件或化学溶剂,对环境友好。
3.1 水解酶对大豆蛋白凝胶特性的影响
酶水解是是一种极具潜力的蛋白修饰方法,通过酶催化作用将大豆蛋白分解成小分子物质,可以改变大豆蛋白的溶解度、表面疏水性、分子质量和暴露的巯基含量,从而改善大豆蛋白的功能特性,包括凝胶能力[45]。
通过控制加酶量和酶解时间可对蛋白质的水解度进行调控,不同水解度下,蛋白质的聚集和凝胶特性也不同,从而导致凝胶强度增加或降低。LI等[46]研究了木瓜蛋白酶酶解大豆蛋白对TG交联豆腐凝胶特性的影响,发现通过疏水相互作用和共价相互作用适度酶解,将α-螺旋和β-转角转化为β-折叠和无规则卷曲结构,形成更致密的凝胶网络结构,所得到的豆腐凝胶在硬度和储能模量方面均高于经TG直接凝固的豆腐凝胶,当木瓜蛋白酶用量为50 μL/100 mL豆浆时,大豆蛋白被分解,结构展开,暴露了更多蛋白质分子内的疏水性基团和氨基酸残基,且大豆蛋白中的二硫键也被破坏,此条件下蛋白凝胶特性最佳。YANG等[47]使用碱性蛋白酶(alcalase)水解SPI制备大豆水解蛋白,发现与未经水解的SPI相比,适度酶解(水解度为1.37~2.17%)可改善大豆蛋白的溶解度,使β-折叠、无规则卷曲和二硫键含量增加、浊度降低,之后使用TG促进交联制备凝胶,经水解的SPI表现出优异的胶凝行为,其凝胶网络均匀,空腔小,黏弹性高,持水性好。过度酶解(3.12%~6.61%)导致蛋白质水解成小分子的肽段,不利于TG交联成大分子聚集体,限制强凝胶网络的形成。适度酶解可以改善蛋白质结构,增加蛋白间相互作用,促进TG的交联,从而形成质地更好的凝胶结构。酶水解作为一种“绿色”修饰方法,已经受到越来越多关注,因为其作用条件温和,保护大豆蛋白营养价值[48]、降低大豆蛋白致敏性和提高大豆蛋白功能特性[49]。
3.2 交联酶对大豆蛋白凝胶特性的影响
TG是一种催化酰基供体(蛋白质或肽链上谷氨酰胺残基的γ-羧酰胺基团)和酰基受体(蛋白质侧链中赖氨酸的ε-氨基)发生酰基转移反应[形成ε-(γ-谷氨酰胺)赖氨酸共价键]的转移酶(如图2),也可以催化蛋白质的解离和变性,暴露蛋白质中不同的官能团,促进相邻蛋白质分子间共价和非共价相互作用使网络结构被改变,从而形成致密、均匀的三维网络凝胶结构[50-51],进而增强了诸如持水性和凝胶形成能力等功能特性,因此酶交联有助于改善蛋白质的凝胶性能[44]。
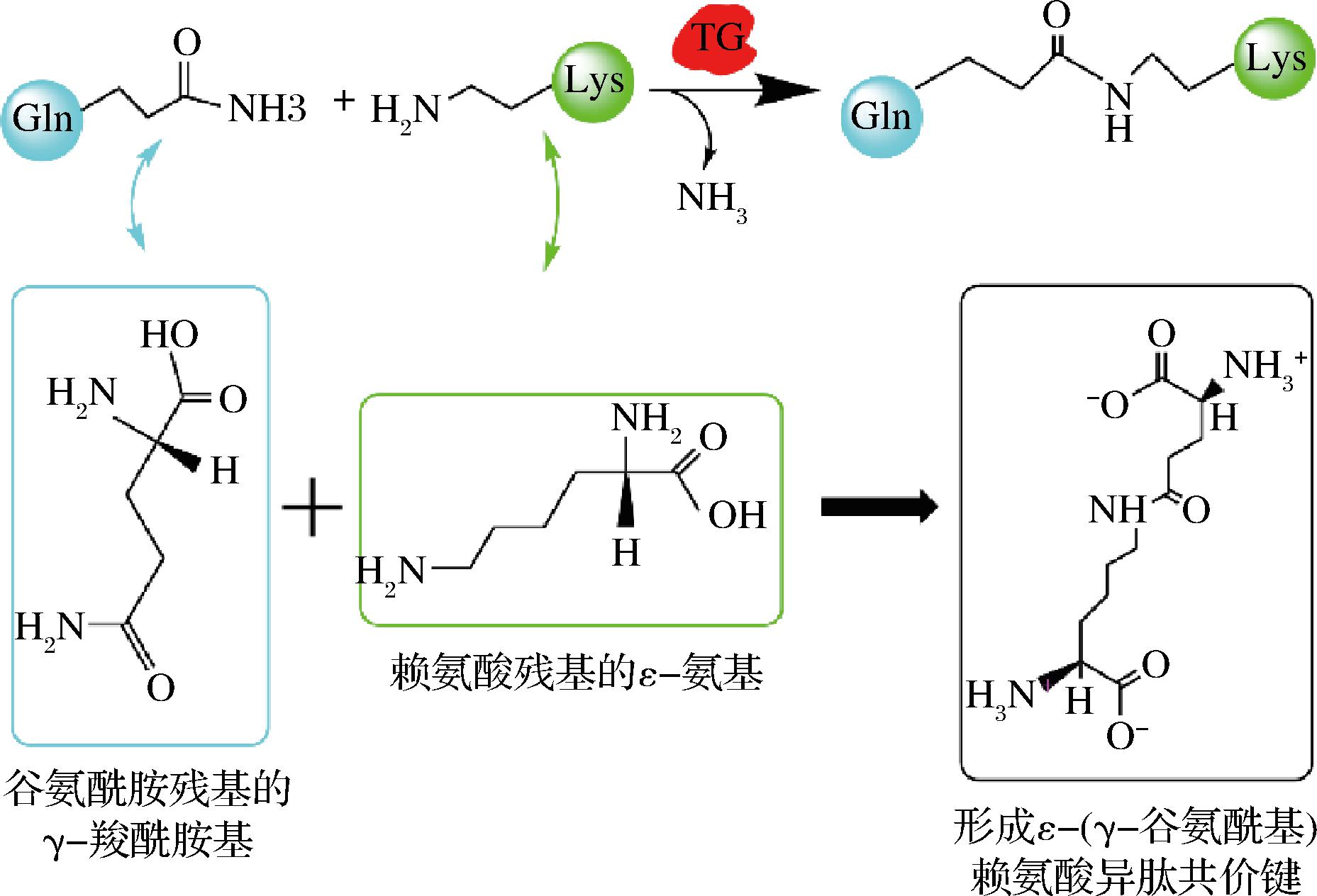
图2 TG催化的共价交联反应
Fig.2 TG-catalyzed covalent cross-coupling reactions
酶的添加量是影响酶催化反应的关键因素之一。在未达到酶反应饱和的情况下,增加酶的添加量有助于提高反应速率,缩短反应时间,进而对反应交联程度产生影响。LIU等[52]研究了源自枯草芽孢杆菌的TG诱导交联对SPI性能的影响,结果发现经TG处理后,SPI中所有蛋白亚基(α、α′、β、A、B)都可以发生交联反应,蛋白分子间共价交联显著提高了SPI平均粒径、改善了凝胶的质构特性(硬度、黏结性、弹性和咀嚼性)和持水性。LI等[53]发现0.4% TG促进了大豆蛋白分子间共价交联,形成了大粒径、高剪切应力和高储能模量的蛋白聚合物,在此条件下SPI形成了致密、光滑、高度有序的凝胶网络结构,并且凝胶的持水性和凝胶强度均显著提高;而当TG添加量为0.8%和1.0%时,凝胶强度急剧下降。MI等[54]研究也指出高浓度的TG交联,会抑制蛋白分子有序凝胶基质的形成,不利于凝胶强度的进一步改善。
近些年来,TG还被用来催化大豆蛋白与其他组分的交联,比如催化SPI与大豆膳食纤维[55]、Salecan[56]、表没食子儿茶素-3-没食子酸酯[57]、小麦面筋蛋白[58]等组分的交联。与催化单组分相比,多组分间的共价交联对凝胶食品的微观结构和质构特性有更显著的改善。TG在促进蛋白质聚合和改善蛋白质功能特性方面的独特性能,使其能提供具有改进或创新属性的食品,以满足消费者的需求,进而扩大在食品工业中的应用[59]。
4 物理-酶耦合修饰处理对大豆蛋白凝胶特性的影响
大豆蛋白中的7S和11S蛋白均为球蛋白,与纤维蛋白不同,球蛋白的官能团隐藏在分子中,限制了酶对底物中作用位点的可及性,降低酶催化效率,不利于凝胶品质改善。而适当的加工预处理(物理修饰)可能促进蛋白表面的结构展开和活性基团暴露,从而促进水解反应和交联反应,使大豆蛋白凝胶的质构特性和流变性能得到改善,形成更致密、更均匀的凝胶网络。
4.1 水解酶和物理修饰技术结合对大豆蛋白凝胶特性的影响
酶水解与其他物理修饰技术(如超声波、热处理和高压均质等)相结合,物理修饰处理可以使大豆蛋白分子结构展开,暴露大豆蛋白的酶切位点,水解酶使多肽链展开,暴露的官能团经疏水相互作用聚集,从而影响其凝胶特性。
水解酶可与热处理、挤压处理、超声波处理等物理技术耦合修饰大豆蛋白,改善其凝胶特性。LIANG等[60]用热处理调控大豆蛋白酶解物(900 U/g胃蛋白酶酶解60 min)发现,55 ℃的预热处理诱导酶解前蛋白质分子部分或全部展开,促进了胃蛋白酶酶切位点的暴露。LIU等[61]发现先经适当的挤出处理(螺旋速度130 r/min,水分含量22%,挤出温度150 ℃)再加酶解(1 850 U/g alcalase酶解10 min)会使蛋白质构象重新排列,改变空间结构,暴露更多的疏水基团,蛋白粒径更小。李扬等[62]发现,与未经处理SPI和经单一改性处理(超声波改性处理、木瓜蛋白酶改性处理)的SPI相比,300 W下超声波20 min联合25 U/g木瓜蛋白酶处理30 min的蛋白二级结构中,α-螺旋和β-转角相对含量降低,β-折叠和无规则卷曲相对含量上升,超声波处理的机械力和空化作用与木瓜蛋白酶的水解作用相互协同使蛋白致密结构展开,促使游离巯基和疏水基团暴露,提高了SPI游离巯基含量和表面疏水性,超声波联合酶处理后的SPI凝胶表现出最佳效果,形成了均匀致密的凝胶网络,其凝胶强度和持水率均高于未经处理和单一改性处理。WU等[63]将经100 U/g alcalase酶解30 min后的SPI分散液400 W超声波处理20 min,发现alcalase与超声波联合处理使分散液颗粒尺寸减小,游离巯基含量增加,游离巯基和疏水基团暴露在蛋白分子表面,促进了二硫键的形成和分子间疏水相互作用,利于形成致密的凝胶网络结构,凝胶强度和持水性与未修饰或单一修饰相比均显著改善。LIANG等[8]采用800 U/g alcalase酶解2 h和60 MPa高压下均质耦合修饰大豆浓缩蛋白,结果表明,改性后的大豆浓缩蛋白的粒径减小,二级结构中无规则卷曲含量和表面疏水性增加。结构的变化使其理化性质也随之改变,功能特性提高。适度酶解并与其他物理技术的耦合处理可显著改善大豆蛋白的凝胶特性,有助于大豆蛋白修饰技术的多样化,促进大豆蛋白的可持续和高值化应用。
4.2 交联酶和物理修饰技术结合对大豆蛋白凝胶特性的影响
将酶交联与物理修饰技术相结合可显著改善大豆蛋白的凝胶性能。物理修饰技术使蛋白质展开,暴露在分子表面的游离巯基和疏水基团可能为形成更大的蛋白质聚集体提供了更多相互作用的机会,并且蛋白质分子内部基团的暴露,增加TG作用位点的数量。TG还能形成各分子间或分子内的共价交联,通过上述可用的官能团之间的分子间和分子内交联,形成强大而均匀的三维凝胶网络[64]。
交联酶可与超声波处理、高压处理、热处理等物理技术耦合修饰大豆蛋白,从而改善其凝胶特性。MA等[65]将经50 U/g木瓜蛋白酶酶解30 min后的SPI分散液进行300 W超声波处理20 min后发现,联合处理后β-折叠和无规则卷曲含量显著升高,游离巯基和疏水性基团暴露,SPI分子质量降低,粒径显著减小。与未处理的SPI相比,经木瓜蛋白酶和超声波联合20 U/g TG处理制备的SPI凝胶形成了均匀致密的凝胶网络,凝胶强度和持水能力显著提高。MAO等[66]发现480 W超声波30 min结合400 MPa高压处理5 min促进了SPI中共价键二硫键和ε-(γ-谷氨酰基)赖氨酸异肽键的形成以及非共价疏水相互作用,与单独超声波或高压作用相比,凝胶强度、持水性和储能模量都得到了提高,微观形态更加均匀致密,凝胶网络结构得到改善,进一步提高了SPI的凝胶性能。WANG等[67]对SPI进行95 ℃预热30 min处理,结果发现适当的热处理可显著加速TG的交联,形成了更多的异肽键,且只有部分7S和11S酸性亚基参与催化反应,11S碱性亚基几乎不发生交联。与未加热的样品相比,此条件下形成的凝胶表现出最好的凝胶性能,储能模量显著增加,而过度加热(95 ℃,60~120 min)会导致SPI严重聚集,形成不溶性聚集体,导致交联效率差,凝胶性能变弱。物理-交联酶耦合处理大豆蛋白的凝胶强度和持水性均高于单独物理处理或酶处理,说明物理处理与酶处理对大豆蛋白凝胶特性的改善具有协同作用。交联酶和其他技术相结合对大豆蛋白凝胶性能的影响如表1所示。
表1 不同物理-酶耦合修饰技术下大豆蛋白凝胶的强度和持水性
Table 1 Strength and water-holding properties of soy protein gels under different coupled physical-enzymatic modification techniques
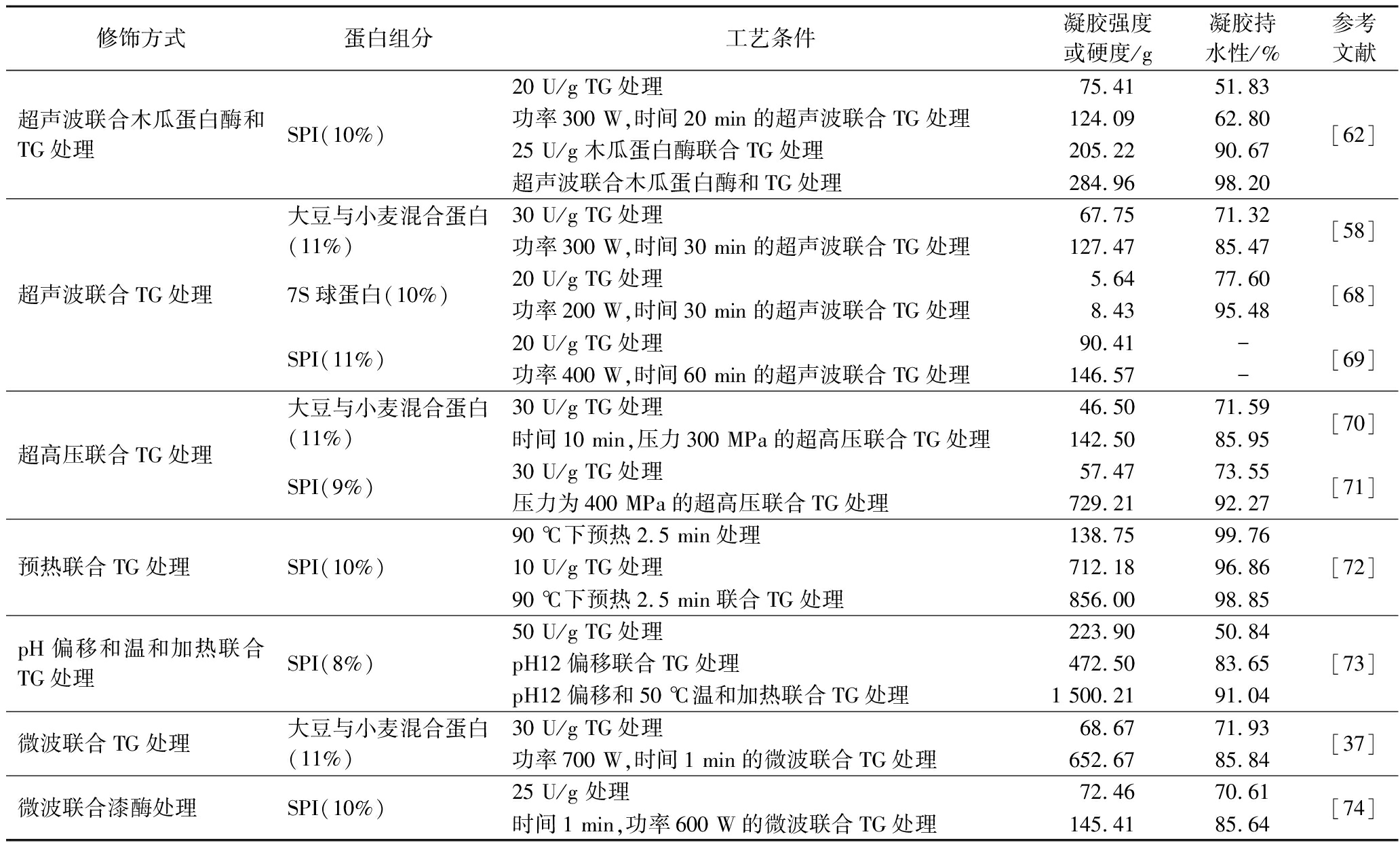
修饰方式蛋白组分工艺条件凝胶强度或硬度/g凝胶持水性/%参考文献超声波联合木瓜蛋白酶和TG处理SPI(10%)20 U/g TG处理75.4151.83功率300 W,时间20 min的超声波联合TG处理124.0962.8025 U/g木瓜蛋白酶联合TG处理205.2290.67超声波联合木瓜蛋白酶和TG处理284.9698.20[62]超声波联合TG处理大豆与小麦混合蛋白(11%)7S球蛋白(10%)SPI(11%)30 U/g TG处理67.7571.32功率300 W,时间30 min的超声波联合TG处理127.4785.4720 U/g TG处理5.6477.60功率200 W,时间30 min的超声波联合TG处理8.4395.4820 U/g TG处理90.41-功率400 W,时间60 min的超声波联合TG处理146.57-[58][68][69]超高压联合TG处理大豆与小麦混合蛋白(11%)SPI(9%)30 U/g TG处理46.5071.59时间10 min,压力300 MPa的超高压联合TG处理142.5085.9530 U/g TG处理57.4773.55压力为400 MPa的超高压联合TG处理729.2192.27[70][71]预热联合TG处理SPI(10%)90 ℃下预热2.5 min处理138.75 99.7610 U/g TG处理712.1896.8690 ℃下预热2.5 min联合TG处理856.0098.85[72]pH偏移和温和加热联合TG处理SPI(8%)50 U/g TG处理223.90 50.84pH12偏移联合TG处理472.5083.65pH12偏移和50 ℃温和加热联合TG处理1 500.2191.04[73]微波联合TG处理大豆与小麦混合蛋白(11%)30 U/g TG处理68.6771.93功率700 W,时间1 min的微波联合TG处理652.6785.84[37]微波联合漆酶处理SPI(10%)25 U/g 处理72.4670.61时间1 min,功率600 W的微波联合TG处理145.4185.64[74]
5 总结及展望
目前,以大豆蛋白凝胶特性为基础的产品开发较多、研究较广,但由于其凝胶强度不高,无法满足现阶段食品工业对植物蛋白基凝胶强度的要求,限制了其在高凝胶强度食品中的应用。近年来,随着绿色、安全、可持续发展理念的倡导,物理修饰和酶修饰方法因其环保、不需要外源性化学试剂且能显著改善大豆蛋白凝胶特性而受到人们的重视。但天然大豆蛋白致密的球状结构,使一些功能基团和活性位点掩埋在蛋白内部,不利于酶水解和酶交联。物理预处理可使大豆蛋白分子链打开,功能基团和活性位点暴露,有利于酶水解和酶交联的进行,进而改善其凝胶特性。物理-酶耦合修饰技术与单一修饰技术相比,可更有效地改善大豆蛋白凝胶的质构特性、流变特性和持水能力。物理-酶耦合修饰大豆蛋白凝胶特性的研究有助于拓宽物理预处理辅助酶水解和酶交联在大豆蛋白相关食品体系中的生产研究思路。但目前关于物理-酶耦合修饰改善大豆蛋白凝胶特性的机制尚不清晰,其作用机理有待深入探讨。在未来研究中,可以从以下几个方面对大豆蛋白的凝胶化进行深入研究:(a)在物理-酶耦合修饰基础上,通过将大豆蛋白组分差异、蛋白-蛋白或蛋白-非蛋白的相互作用与改善大豆蛋白凝胶性的作用机制相联系,阐明物理-酶耦合修饰处理改善大豆蛋白凝胶特性的机理。(b)在物理修饰、酶修饰和物理-酶耦合修饰下,探究大豆蛋白凝胶网络中网络蛋白含量的变化及其对凝胶质构特性的影响,阐明蛋白凝胶三维网络形成机制。(c)开发新型非热物理加工技术,探索其与酶耦合修饰技术对蛋白结构和功能特性的调控,阐明蛋白凝胶网络结构形成机制。物理-酶耦合修饰对大豆蛋白凝胶品质和功能特性影响机制的研究,可为开发高凝胶强度的大豆蛋白凝胶产品提供理论依据,促进大豆蛋白在食品工业中深层次、高水平应用与多元化、高质量发展。
[1] YAO F, CHEN F S, DU Y, et al.Functional and structural properties of soy 11S globulin:Influence of reverse micelle extraction[J].Journal of Food Science, 2021, 86(8):3403-3412.
[2] ZHENG L, REGENSTEIN J M, ZHOU L Y, et al.Soy protein isolates:A review of their composition, aggregation, and gelation[J].Comprehensive Reviews in Food Science and Food Safety, 2022, 21(2):1940-1957.
[3] SHRESTHA S, VAN ’T HAG L, HARITOS V, et al.Rheological and textural properties of heat-induced gels from pulse protein isolates:Lentil, mungbean and yellow pea[J].Food Hydrocolloids, 2023, 143:108904.
[4] BANGAR S P, ESUA O J, SHARMA N, et al.Ultrasound-assisted modification of gelation properties of proteins:A review[J].Journal of Texture Studies, 2022, 53(6):763-774.
[5] 曾剑华, 杨杨, 刘琳琳, 等.热处理过程中大豆11S球蛋白解离缔合行为研究进展[J].食品科学, 2019, 40(11):303-312.ZENG J H, YANG Y, LIU L L, et al.Recent progress in the dissociation-association behavior of 11S glycinin during heat treatment[J].Food Science, 2019, 40(11):303-312.
[6] FANG L Y, XIANG H, SUN-WATERHOUSE D, et al.Enhancing the usability of pea protein isolate in food applications through modifying its structural and sensory properties via deamidation by glutaminase[J].Journal of Agricultural and Food Chemistry, 2020, 68(6):1691-1697.
[7] LIU Y H, DONG L Z, LI Y, et al.Soy protein isolate-Citrus pectin composite hydrogels induced by TGase and ultrasonic treatment:Potential targeted delivery system for probiotics[J].Food Hydrocolloids, 2023, 143:108901.
[8] LIANG Y R, GUO Y N, ZHENG Y X, et al.Effects of high-pressure homogenization on physicochemical and functional properties of enzymatic hydrolyzed soybean protein concentrate[J].Frontiers in Nutrition, 2022, 9:1054326.
[9] NICOLAI T, CHASSENIEUX C.Heat-induced gelation of plant globulins[J].Current Opinion in Food Science, 2019, 27:18-22
[10] WU C, MA W C, HUA Y F.The relationship between breaking force and hydrophobic interactions or disulfide bonds involved in heat-induced soy protein gels as affected by heating time and temperature[J].International Journal of Food Science &Technology, 2019, 54(1):231-239.
[11] RUAN Q J, CHEN Y M, KONG X Z, et al.Heat-induced aggregation and sulphydryl/disulphide reaction products of soy protein with different sulphydryl contents[J].Food Chemistry, 2014, 156:14-22.
[12] WU C, WANG T, REN C, et al.Advancement of food-derived mixed protein systems:Interactions, aggregations, and functional properties[J].Comprehensive Reviews in Food Science and Food Safety, 2021, 20(1):627-651.
[13] LV X H, HUANG X, MA B, et al.Modification methods and applications of egg protein gel properties:A review[J].Comprehensive Reviews in Food Science and Food Safety, 2022, 21(3):2233-2252.
[14] ABEDI E, POURMOHAMMADI K.Physical modifications of wheat gluten protein:An extensive review[J].Journal of Food Process Engineering, 2021, 44(3):e13619.
[15] RATHNAKUMAR K, BALAKRISHNAN G, RAMESH B, et al.Impact of emerging food processing technologies on structural and functional modification of proteins in plant-based meat alternatives:An updated review[J].Journal of Texture Studies, 2023, 54(4):599-612.
[16] AKHARUME F U, ALUKO R E, ADEDEJI A A.Modification of plant proteins for improved functionality:A review[J].Comprehensive Reviews in Food Science and Food Safety, 2021, 20(1):198-224.
[17] SULAIMAN N S, SINTANG M D, MOHD ZAINI H, et al.Applications of protein crosslinking in food products[J].International Food Research Journal, 2022, 29(4):723-739.
[18] 陈凤莲, 吉语宁, 贺殷媛, 等.基于凝胶特性的蛋白改性方法研究进展[J].食品研究与开发, 2023, 44(2):190-195.CHEN F L, JI Y N, HE Y Y, et al.Research progress on protein modification methods based on gel properties[J].Food Research and Development, 2023, 44(2):190-195.
[19] WANG J M, NA X K, NAVICHA W B, et al.Concentration-dependent improvement of gelling ability of soy proteins by preheating or ultrasound treatment[J].LWT, 2020, 134:110170.
[20] MALAKI NIK A, TOSH S M, WOODROW L, et al.Effect of soy protein subunit composition and processing conditions on stability and particle size distribution of soymilk[J].LWT-Food Science and Technology, 2009, 42(7):1245-1252.
[21] LI X F, CHEN L Y, HUA Y F, et al.Effect of preheating-induced denaturation during protein production on the structure and gelling properties of soybean proteins[J].Food Hydrocolloids, 2020, 105:105846.
[22] 武雅琴. 改性大豆蛋白与鱼类肌原纤维蛋白的相互作用及复合凝胶特性[D].上海:上海海洋大学, 2019.WU Y Q.Interaction between modified soybean protein and fish myofibrillar protein and characteristics of composite gel[D].Shanghai:Shanghai Ocean University, 2019.
[23] FLOURY J, DESRUMAUX A, LEGRAND J.Effect of ultra-high-pressure homogenization on structure and on rheological properties of soy protein-stabilized emulsions[J].Journal of Food Science, 2002, 67(9):3388-3395.
[24] KEERATI-U-RAI M, CORREDIG M.Effect of dynamic high pressure homogenization on the aggregation state of soy protein[J].Journal of Agricultural and Food Chemistry, 2009, 57(9):3556-3562.
[25] KANG Z L, BAI R, LU F, et al.Effects of high pressure homogenization on the solubility, foaming, and gel properties of soy 11S globulin[J].Food Hydrocolloids, 2022, 124:107261.
[26] KANG Z L, ZHANG X H, LI X, et al.The effects of sodium chloride on proteins aggregation, conformation and gel properties of pork myofibrillar protein Running Head:Relationship aggregation, conformation and gel properties[J].Journal of Food Science and Technology, 2021, 58(6):2258-2264.
[27] SUN D Y, WU M, BI C H, et al.Using high-pressure homogenization as a potential method to pretreat soybean protein isolate:Effect on conformation changes and rheological properties of its acid-induced gel[J].Innovative Food Science &Emerging Technologies, 2022, 82:103195.
[28] ZHENG L, WANG Z J, KONG Y, et al.Different commercial soy protein isolates and the characteristics of Chiba tofu[J].Food Hydrocolloids, 2021, 110:106115.
[29] GHARIBZAHEDI S M T, SMITH B.The functional modification of legume proteins by ultrasonication:A review[J].Trends in Food Science &Technology, 2020, 98:107-116.
[30] ZHENG T, LI X H, TAHA A, et al.Effect of high intensity ultrasound on the structure and physicochemical properties of soy protein isolates produced by different denaturation methods[J].Food Hydrocolloids, 2019, 97:105216.
[31] HU H, FAN X, ZHOU Z, et al.Acid-induced gelation behavior of soybean protein isolate with high intensity ultrasonic pre-treatments[J].Ultrasonics Sonochemistry, 2013, 20(1):187-195.
[32] 刘冉, 曾庆华, 王振宇, 等.超声波处理对大豆分离蛋白凝胶流变性和凝胶形成的影响[J].食品工业科技, 2020, 41(21):87-92; 98.LIU R, ZENG Q H, WANG Z Y, et al.Effects of ultrasonic treatment on gel rheological properties and gel formation of soybean protein isolate[J].Science and Technology of Food Industry, 2020, 41(21):87-92; 98.
[33] ZOU Y, YANG H, LI P P, et al.Effect of different time of ultrasound treatment on physicochemical, thermal, and antioxidant properties of chicken plasma protein[J].Poultry Science, 2019, 98(4):1925-1933.
[34] AFKHAMI R, VARIDI M J, VARIDI M, et al.Improvement of heat-induced nanofibrils formation of soy protein isolate through NaCl and microwave[J].Food Hydrocolloids, 2023, 139:108443.
[35] LI Y Y, WANG S N, LIU X L, et al.Improvement in texture and color of soy protein isolate gel containing capsorubin and carotenoid emulsions following microwave heating[J].Food Chemistry, 2023, 428:136743.
[36] BHATTACHARYA S, JENA R.Gelling behavior of defatted soybean flour dispersions due to microwave treatment:Textural, oscillatory, microstructural and sensory properties[J].Journal of Food Engineering, 2007, 78(4):1305-1314.
[37] QIN X S, LUO S Z, CAI J, et al.Effects of microwave pretreatment and transglutaminase crosslinking on the gelation properties of soybean protein isolate and wheat gluten mixtures[J].Journal of the Science of Food and Agriculture, 2016, 96(10):3559-3566.
[38] LIU H H, KUO M I.Effect of microwave heating on the viscoelastic property and microstructure of soy protein isolate gel[J].Journal of Texture Studies, 2011, 42(1):1-9.
[39] CHEN Y, LIANG Y, LIU H, et al.Extrusion of wheat gluten-peanut oil complexes and their rheological characteristics[J].Food Chemistry, 2021, 364:130435.
[40] CHEN F L, WEI Y M, ZHANG B.Chemical cross-linking and molecular aggregation of soybean protein during extrusion cooking at low and high moisture content[J].LWT-Food Science and Technology, 2011, 44(4):957-962.
[41] SINGH R, KOKSEL F.Effects of particle size distribution and processing conditions on the techno-functional properties of extruded soybean meal[J].LWT, 2021, 152:112321.
[42] ZHANG S T, HUANG W J, ROOPESH M S, et al.Pre-treatment by combining atmospheric cold plasma and pH-shifting to prepare pea protein concentrate powders with improved gelling properties[J].Food Research International, 2022, 154:111028.
[43] 王然, 龚维, 郭晓璐, 等.冷等离子体处理改性大豆分离蛋白及改善其界面性能[J].现代食品科技, 2022, 38(12):101-109.WANG R, GONG W, GUO X L, et al.Modification of soybean protein isolate by cold plasma treatment and improvement of its interface properties[J].Modern Food Science and Technology, 2022, 38(12):101-109.
[44] MIWA N.Innovation in the food industry using microbial transglutaminase:Keys to success and future prospects[J].Analytical Biochemistry, 2020, 597:113638.
[45] CHEN D, CAMPANELLA O H.Limited enzymatic hydrolysis induced pea protein gelation at low protein concentration with less heat requirement[J].Food Hydrocolloids, 2022, 128:107547.
[46] LI C Y, WU X F, MU D D, et al.Effect of partial hydrolysis with papain on the characteristics of transglutaminase-crosslinked tofu gel[J].Journal of Food Science, 2018, 83(12):3092-3098.
[47] YANG J J, ZHU B, DOU J J, et al.Structural characterization of soy protein hydrolysates and their transglutaminase-induced gelation properties[J].LWT, 2023, 179:114668.
[48] LOPES-DA-SILVA J A, MONTEIRO S R.Gelling and emulsifying properties of soy protein hydrolysates in the presence of a neutral polysaccharide[J].Food Chemistry, 2019, 294:216-223.
[49] 郑环宇, 赵晓明, 张梦, 等.不同酶切方式引发大豆蛋白构象变化及功能特性评价[J].中国粮油学报, 2022, 37(6):103-111.ZHENG H Y, ZHAO X M, ZHANG M, et al.Evaluation on changes and functional properties of soy protein conformation due to different enzymolysis methods[J].Journal of the Chinese Cereals and Oils Association, 2022, 37(6):103-111.
[50] WANG C Y, LI T Q, MA L, et al.Consequences of superfine grinding treatment on structure, physicochemical and rheological properties of transglutaminase-crosslinked whey protein isolate[J].Food Chemistry, 2020, 309:125757.
[51] FATIMA S W, KHARE S K.Current insight and futuristic vistas of microbial transglutaminase in nutraceutical industry[J].Microbiological Research, 2018, 215:7-14.
[52] LIU Y X, ZHANG Y F, GUO Z H, et al.Enhancing the functional characteristics of soy protein isolate via cross-linking catalyzed by Bacillus subtilis transglutaminase[J].Journal of the Science of Food and Agriculture, 2021, 101(10):4154-4160.
[53] LI Y Y, WANG S N, LIU X L, et al.Characterization of enzymatic cross-linking soy protein isolate xerogels and its shape memory effect induced by ethylcellulose[J].Food Chemistry, 2023, 412:135564.
[54] MI H B, ZHAO Y M, LI Y, et al.Combining effect of soybean protein isolate and transglutaminase on the gel properties of Zhikong scallop (Chlamys Farreri) adductor muscle[J].LWT, 2021, 138:110727.
[55] LV Y Q, TANG T T, XU L L, et al.Influence of soybean dietary fiber with varying particle sizes and transglutaminase on soy protein isolate gel[J].Food Research International, 2022, 161:111876.
[56] GAN J, SUN L R, GUAN C X, et al.Preparation and properties of salecan-soy protein isolate composite hydrogel induced by thermal treatment and transglutaminase[J].International Journal of Molecular Sciences, 2022, 23(16):9383.
[57] XU J J, GUO S Y, LI X J, et al.Gel properties of transglutaminase-induced soy protein isolate-polyphenol complex:Influence of epigallocatechin-3-gallate[J].Journal of the Science of Food and Agriculture, 2021, 101(9):3870-3879.
[58] QIN X S, LUO S Z, CAI J, et al.Transglutaminase-induced gelation properties of soy protein isolate and wheat gluten mixtures with high intensity ultrasonic pretreatment[J].Ultrasonics Sonochemistry, 2016, 31:590-597.
[59] ZHAO L, CHEN M H, BI X Z, et al.Physicochemical properties, structural characteristics and in vitro digestion of brown rice-pea protein isolate blend treated by microbial transglutaminase[J].Food Hydrocolloids, 2023, 141:108673.
[60] LIANG G J, CHEN W P, QIE X J, et al.Modification of soy protein isolates using combined pre-heat treatment and controlled enzymatic hydrolysis for improving foaming properties[J].Food Hydrocolloids, 2020, 105:105764.
[61] LIU Y Q, HUANG Y Y, DENG X Q, et al.Effect of enzymatic hydrolysis followed after extrusion pretreatment on the structure and emulsibility of soybean protein[J].Process Biochemistry, 2022, 116:173-184.
[62] 李杨, 马召蕾, 郑丽, 等.超声联合酶处理下TG酶交联大豆分离蛋白凝胶特性研究[J].农业机械学报, 2022, 53(4):394-402.LI Y, MA Z L, ZHENG L, et al.Effect of ultrasonic combined with enzyme treatment on glutamine transaminase cross-linked soybean protein isolate gels[J].Transactions of the Chinese Society for Agricultural Machinery, 2022, 53(4):394-402.
[63] WU X X, GAO T, XU Z, et al.Effect of combined enzyme and ultrasound treatment on the structure and gel properties of soy protein isolate:A comparative study of alkaline protease and pepsin[J].Colloids and Surfaces A:Physicochemical and Engineering Aspects, 2024, 687:133533.
[64] ZHANG P P, HU T, FENG S L, et al.Effect of high intensity ultrasound on transglutaminase-catalyzed soy protein isolate cold set gel[J].Ultrasonics Sonochemistry, 2016, 29:380-387.
[65] MA Z L, LI L J, WU C L, et al.Effects of combined enzymatic and ultrasonic treatments on the structure and gel properties of soybean protein isolate[J].LWT, 2022, 158:113123.
[66] MAO Y X, ZHAO C B, QI Q, et al.Transglutaminase-induced soybean protein isolate cold-set gels treated with combination of ultrasound and high pressure:Physicochemical properties and structural characterization[J].International Journal of Biological Macromolecules, 2023, 253:127525.
[67] WANG X F, WANG Y Q, WANG X S, et al.Influence of substrate aggregation state on the enzymatic-induced crosslinking of soy protein isolate[J].Food Chemistry, 2024, 442:138484.
[68] ZHANG L, ZHANG J X, WEN P P, et al.Effect of high-intensity ultrasound pretreatment on the properties of the transglutaminase (TGase)-induced β-conglycinin (7S) gel[J].Foods, 2023, 12(10):2037.
[69] ZHANG P, BAO Z Y, WANG H, et al.Ultrasonic pretreatment improved the physicochemical properties and riboflavin delivery ability of transglutaminase-catalyzed soy protein isolate gel[J].Food Hydrocolloids, 2022, 131:107782.
[70] QIN X S, CHEN S S, LI X J, et al.Gelation properties of transglutaminase-induced soy protein isolate and wheat gluten mixture with ultrahigh pressure pretreatment[J].Food and Bioprocess Technology, 2017, 10(5):866-874.
[71] 史乾坤, 王心雅, 甄诺, 等.超高压预处理对TGase交联的大豆分离蛋白凝胶的影响[J].中国粮油学报, 2021, 36(9):94-100.SHI Q K, WANG X Y, ZHEN N, et al.Effects of ultra high pressure pretreatment on TGase cross-linked soy protein isolate gel[J].Journal of the Chinese Cereals and Oils Association, 2021, 36(9):94-100.
[72] ZHANG M Q, YANG Y J, ACEVEDO N C.Effects of pre-heating soybean protein isolate and transglutaminase treatments on the properties of egg-soybean protein isolate composite gels[J].Food Chemistry, 2020, 318:126421.
[73] SUN P, ZHANG Q, ZHAO Y, et al.Improving gel properties of soy protein isolate through alkaline pH-shifting, mild heat treatment, and TGase cross-linking[J].Food Hydrocolloids, 2023, 144:108924.
[74] MU D D, LI H W, LI X J, et al.Enhancing laccase-induced soybean protein isolates gel properties by microwave pretreatment[J].Journal of Food Processing and Preservation, 2020, 44(4):e14386.