果胶是一种复杂的阴离子多糖,广泛存在于自然界植物细胞壁中。其是由半乳糖醛酸单体通过α-1,4-糖苷键连接而成,通常在不同程度上被部分甲基酯化或乙酰化[1]。多聚半乳糖醛酸酶(polygalacturonase,PG)是研究最为广泛的果胶酶之一,属于糖苷水解酶(glycosyl hydrolases)第28家族,能特异性催化果胶分子中α-1,4糖苷键的断裂,其按照作用方式的不同可以分为内切型和外切型两种[2]。其中,内切多聚半乳糖醛酸酶可将果胶不完全降解,生成寡聚的果胶寡糖(pectic oligosaccharide,POS)。果胶寡糖作为一类新兴的益生元,具有改善脂代谢、抗氧化、抗肿瘤及增强免疫力等特性,具有较好的应用价值[3]。
目前关于内切多聚半乳糖醛酸酶的研究仍然较少,且其催化活力仍难以满足相关工业化生产的需求。随着生物信息学和分子生物学的高速发展,除了进行新酶筛选外,计算机辅助的蛋白质理性设计成为了改进酶功能、扩展酶应用范畴的有效手段。如同源建模可以简单准确地根据已知的蛋白结构模型预测目标蛋白的三维结构,分子对接则可以帮助理解蛋白与底物的相互作用方式,指导人们理性选取氨基酸改造靶点,有效地对蛋白进行改造[4]。TU等[5]通过同源建模和分子对接,在一种嗜酸真菌的内聚半乳糖醛酸酶BiPG28A中鉴定出了与底物结合相关的关键残基。进一步分析其构象、氢键相互作用和结合自由能,发现129位突变为赖氨酸能够显著增强其底物亲和力和催化效率。此外,许多预测软件也被用来计算突变对蛋白质构象可能产生的影响,常用的软件包括FoldX[6]、Rosetta[7]、PoPMuSiC[8]、FireProt[9]等。ZHENG等[10]对来源于黑曲霉的纤维素酶AnCel5A进行了理性设计改造,选择了α螺旋外侧的非保守性氨基酸作为突变热点,并基于FoldX算法计算的折叠自由能对其进行了评估,筛选获得了催化效率和热稳定性显著提高的突变体。郝梦洁[11]利用在线预测软件ABACUS、FireProt和Disulfide by Design进行内切多聚半乳糖醛酸酶的热稳定性位点预测及二硫键设计,获得的组合突变体在55 ℃下处理60 min后残余酶活能达到野生型的11.6倍。
在前期研究中,本实验室挖掘获得了一个来自青霉Penicillium arizonens的内切多聚半乳糖醛酸酶,并在毕赤酵母中实现了异源表达。为了进一步提高其催化活力,本研究基于序列与结构比对确定了该酶的突变热点,并结合FoldX软件预测突变体结合自由能的变化对该酶进行理性设计与改造,以期在不损失其热稳定性的基础上获得催化性能提高的突变体,从而为其在益生元加工、果蔬汁澄清、动物饲料制造等领域提供应用基础。
1 材料与方法
1.1 材料
1.1.1 菌株与质粒
菌株P.arizonense、Escherichia coli TOP10和Komagataella phaffii X33(原先命名为Pichia pastoris)由本实验室保藏。克隆及表达载体pPICZαA-pePGB由本实验室保藏。
1.1.2 酶与主要试剂
限制性内切酶(Sac I, Dpn I)、PrimerSTAR Max DNA Polymerase、Lysis Buffer for Microorganism to Direct PCR、蛋白Marker、DNA Marker,宝生物(TaKaRa)有限公司;超级感受态细胞制备试剂盒、Plasmid Mini-PREPS Kit、PCR Product Purification Kit、DNA Gel Extraction Kit、12.5% SDS-PAGE Color Preparation kit、琼脂糖、氨苄青霉素,上海生工生物工程有限公司;博莱霉素,赛默飞世尔科技公司;Bradford蛋白浓度测定试剂盒,上海碧云天生物技术有限公司;多聚半乳糖醛酸钠(相对分子质量约为411 kDa)、苹果果胶,美国默克有限公司;D-(+)-半乳糖醛酸一水合物标准品,翁江化学试剂有限公司;其他分析纯及以上试剂,国药集团化学有限公司。
1.1.3 培养基与主要溶剂
LLB培养基(g/L):胰蛋白胨10,酵母粉5,NaCl 5,固体培养基在此基础上加入20 g/L琼脂粉,必要时培养基中添加终质量浓度25 μg/mL博来霉素。
YPD培养基(g/L):胰蛋白胨20,酵母粉10,葡萄糖20,固体培养基在此基础上加入20 g/L琼脂粉,必要时培养基中添加终质量浓度100 μg/mL博来霉素。
BMGY培养基(g/L):胰蛋白胨20,酵母粉10,甘油10,YNB 13.4,生物素4×10-4。
BMMY培养基(g/L):胰蛋白胨20,酵母粉10,YNB 13.4,生物素4×10-4。
Solution I(g/L):山梨醇109.2,无水醋酸锂6.6,二硫苏糖醇1.54,Tris 1.21,盐酸调节pH值至7.5。
1 mol/L山梨醇(g/L):山梨醇182.17。
DNS试剂(g/L):3,5-二硝基水杨酸10,NaOH 10,酒石酸钾钠200,苯酚2,无水亚硫酸钠5。
50×TAE缓冲液:Tris 242.0 g,冰醋酸57.1 mL,EDTA-2 Na 33.6 g,去离子水定容至1 L。
SDS-PAGE电泳缓冲液:Tris 3.0 g,SDS 1.0 g,甘氨酸14.4 g,去离子水1 L。
SDS-PAGE蛋白胶染色液:考马斯亮蓝R-250 1.0 g,冰醋酸100 mL,无水乙醇450 mL,去离子水450 mL。
SDS-PAGE蛋白胶脱色液:无水乙醇100 mL,冰醋酸100 mL,去离子水800 mL。
1.1.4 仪器与设备
PCR仪、蛋白电泳仪、凝胶成像系统,美国Bio-Rad公司;核酸电泳仪,北京六一电泳仪厂;酶标仪,美国BioTek公司;分光光度计,翱艺仪器有限公司;小型高速离心机、-80 ℃超低温冰箱、真空离心浓缩仪、冷冻离心机、移液器、电转化仪,德国Eppendorf公司;恒温培养箱,上海博讯实业有限公司;多功能摇床,强乐实验设备有限公司; KTA pure蛋白纯化系统,美国GE医疗公司。
KTA pure蛋白纯化系统,美国GE医疗公司。
1.2 实验方法
1.2.1 内切多聚半乳糖醛酸酶的同源建模
将来自P.arizonense的内切多聚半乳糖醛酸酶pePGB的氨基酸序列提交到AlphaFold2在线服务器(https://colab.research.google.com/github/sokrypton/ColabFold/blob/main/AlphaFold2.ipynb)进行同源建模。利用PyMOL软件对蛋白模型的三维结构进行分析。
1.2.2 突变菌株的构建
以实验室已构建的重组质粒pPICZαA-pePGB为模板,每个拟突变体设计两条含突变位点及重叠部分的引物(表1),进行全质粒PCR扩增引入突变位点。将获得的PCR产物用限制性内切酶Dpn I在37 ℃条件下酶切1 h,以消化模板质粒。消化后的产物利用纯化试剂盒进行纯化回收,转化至大肠杆菌E.coli TOP10感受态细胞中,涂布含博莱霉素的LLB抗性平板,选取阳性转化子,提取质粒进行酶切验证及测序验证。验证正确的质粒利用限制性内切酶Sac I在37 ℃下酶切1 h进行线性化,纯化浓缩后电转化入毕赤酵母K.phaffii X33感受态细胞中,涂布含博莱霉素的YPD抗性平板,选取阳性转化子进行菌落PCR验证,验证正确的菌株作为重组突变菌株进行保藏和后续实验。
表1 突变位点引物设计
Table 1 Primer design for mutation sites

引物核苷酸序列(5′-3′)V144A-FTTGAGAACACTCCCgctCAGGCGGTCAGCATCAACGV144A-RagcGGGAGTGTTCTCAATATAGAGATCGGTAAQ145A-FAGAACACTCCCGTTgctGCGGTCAGCATCAACGGAQ145A-RagcAACGGGAGTGTTCTCAATATAGAGATCGGS148A-FGGTCgctATCAACGGATGTGATGGATTGACTAS148A-RATCCGTTGATagcGACCGCCTGAACGGGAGTGI149A-FTCAGCgctAACGGATGTGATGGATTGACTATCAI149A-RACATCCGTTagcGCTGACCGCCTGAACGGGAGN150A-FTCAGCATCgctGGATGTGATGGATTGACTATCACTGN150A-RACATCCagcGATGCTGACCGCCTGAACGGGAGI180A-FCTTCGATgctGGTTCTAGCAGCAATGTGGTCAI180A-RTAGAACCagcATCGAAGCCGTCGGTGTTGTGAS182A-FTATTGGTgctAGCAGCAATGTGGTCATCTCCGS182A-RTGCTGCTagcACCAATATCGAAGCCGTCGGTGN203A-FTGCAGTCgctTCTGGAACCGATATCACTTTCGAN203A-RTTCCAGAagcGACTGCAACACAGTCGTCTTGGS204A-FTCAACgctGGAACCGATATCACTTTCGAGAACS204A-RATCGGTTCCagcGTTGACTGCAACACAGTCGTCTTGR229A-FTGGAgctTCGGACAACACCGTTGAGACTGTCAR229A-RTGTTGTCCGAagcTCCACCGACAGATCCAATGGS230A-FTGGAAGAgctGACAACACCGTTGAGACTGTCACCS230A-RTGTTGTCagcTCTTCCACCGACAGATCCAATGD231A-FAAGATCGgctAACACCGTTGAGACTGTCACCTTD231A-RCGGTGTTagcCGATCTTCCACCGACAGATCCAV248A-FGAACTCTgctAACGGTATTCGCATCAAGGCCAV248A-RTACCGTTagcAGAGTTCTTGACTGTAGATCCCTTGAL292A-FATGATGGTGGTGACgctGACGGCGGCACCCCTTCCL292A-RagcGTCACCACCATCATAGTTCTGCTCGATGAV248L-FCTttgAACGGTATTCGCATCAAGGCCAAGGAAV248L-RGCGAATACCGTTcaaAGAGTTCTTGACTGTAGATCCCTTGAV248R-FCTagaAACGGTATTCGCATCAAGGCCAAGGAAV248R-RGCGAATACCGTTtctAGAGTTCTTGACTGTAGATCCCTTGAG111R-FGACagaGAGGGAAGCAACGGTGGCGTGACGAAG111R-RTTGCTTCCCTCtctGTCCCACCAGCGGGATCCG111K-FGACaagGAGGGAAGCAACGGTGGCGTGACGAAG111K-RTTGCTTCCCTCcttGTCCCACCAGCGGGATCC
注:小写字母加下划线为突变位点。
1.2.3 突变菌株的诱导表达
将构建获得的重组突变菌株在含博莱霉素的YPD抗性平板上划线并置于30 ℃培养箱培养3 d。挑取单克隆接种于BMGY培养基,在30 ℃,200 r/min条件下培养16~18 h(OD600值约为2~6)。随后收集菌体转接至BMMY培养基中,同时每间隔24 h加入终体积分数为1%的甲醇作为诱导剂,将摇瓶置于28 ℃,200 r/min摇床中诱导培养96 h。
1.2.4 重组内切多聚半乳糖醛酸酶的纯化
诱导培养后的发酵液于4 ℃,6 000 r/min,离心10 min收集上清液。将上清液转移到透析袋(截留分子质量为8 000~14 000 Da)中放置在4 ℃层析柜透析24 h。透析液为20 mmol/L的PBS缓冲液(pH 7.0),每间隔8 h更换一次。使用阴离子交换柱PrePack Q Purose 6 HP结合 KTA pure蛋白纯化系统对重组蛋白进行纯化。用缓冲液A液(20 mmol/L PBS缓冲液,pH 7.0)进行柱平衡,上样后用缓冲液B液(20 mmol/L PBS缓冲液,1 mol/L NaCl,pH 7.0)进行梯度洗脱,收集穿透峰以及各梯度的洗脱峰。利用SDS-PAGE凝胶电泳对收集的各个峰进行鉴定分析,随后用10 kDa超滤离心管将纯化后的目的蛋白在4 ℃下进行超滤浓缩,并用Bradford蛋白浓度测定试剂盒测定蛋白浓度。
KTA pure蛋白纯化系统对重组蛋白进行纯化。用缓冲液A液(20 mmol/L PBS缓冲液,pH 7.0)进行柱平衡,上样后用缓冲液B液(20 mmol/L PBS缓冲液,1 mol/L NaCl,pH 7.0)进行梯度洗脱,收集穿透峰以及各梯度的洗脱峰。利用SDS-PAGE凝胶电泳对收集的各个峰进行鉴定分析,随后用10 kDa超滤离心管将纯化后的目的蛋白在4 ℃下进行超滤浓缩,并用Bradford蛋白浓度测定试剂盒测定蛋白浓度。
1.2.5 酶学性质测定
酶活力测定:取50 μL适当稀释的酶液加入到450 μL的3.3 g/L多聚半乳糖醛酸溶液(50 mmol/L Na2HPO4-柠檬酸缓冲液,pH 5.0)中,在65 ℃下反应10 min,加入750 μL DNS终止反应。将反应体系在沸水浴中处理5 min,立刻于冰水浴中冷却至室温,于13 000 r/min离心5 min,吸取200 μL上清液于96孔板中,在540 nm下测定其吸光度,根据标准曲线计算酶活力。1个多聚半乳糖醛酸酶的酶活力单位(U)定义为在特定的条件下,1 min内转化多聚半乳糖醛酸生成1 μmol D-(+)-半乳糖醛酸所需的酶量。
最适pH及pH稳定性测定:在65 ℃下,用pH 3.0~7.0的缓冲液适当稀释酶液,测定对应pH条件下的酶活力,以最高酶活力为100%,计算其余pH条件下的相对酶活力,确定其最适反应pH。将酶液加入不同pH的缓冲液中于25 ℃放置1 h,以未经处理的酶液酶活力为100%,测定计算残余酶活力,确定其pH稳定性。
最适温度及热稳定性测定:在最适pH下,分别测定酶液在20、30、40、40、50、55、60、65、70、75 ℃下的酶活力,以最高酶活力为100%,计算其余温度条件下的相对酶活力,确定其最适反应温度。将酶液在55 ℃下分别热处理5、10、20、30、40、50、60 min,以未经处理的酶液酶活力为100%,测定计算残余酶活力,确定其热稳定性。
动力学参数测定:将酶液与0.2~2.5 mg/mL聚半乳糖醛酸底物,在65 ℃、pH 5.0缓冲液中反应3 min,测定计算其比活力。根据Michaelis-Menten方程计算该酶的动力学参数,使用Origin软件非线性拟合计算Km和Vmax。
1.2.6 GalpA5与内切多聚半乳糖醛酸酶的分子对接
配体准备:对接配体Pentagalacturonic-acid(GalpA5)结构利用ChemDraw进行绘制,之后导入软件Schrödinger Maestro的LigPrep模块进行处理,选用Epik的方法来产生化合物在pH 5~9之间所有可能的质子化状态,采用的力场为OPLS4。
受体准备:对接受体为pePGB及其突变体的同源建模结构,导入软件Schrödinger Maestro的Protein Preparation Wizard模块进行处理,去除结晶水,补加缺失的氢原子,进行能量最小化,采用的力场为OPLS4。
分子对接:配体和蛋白受体处理完成后,利用Schrödinger Maestro的Induced Fit Docking模块进行分子诱导契合对接,选取蛋白的催化残基作为对接盒子的质心。
2 结果与分析
2.1 pePGB突变位点的选取
将来自P.arizonense的内切多聚半乳糖醛酸酶pePGB的氨基酸序列提交到AlphaFold2[12-13]蛋白质建模服务器进行同源建模,利用可视化软件PyMOL对蛋白结构进行展示和分析。
尽管不同的内切多聚半乳糖醛酸酶在一级序列间存在较大的差异,但其在三级结构上相对保守,呈现出很高的相似性。通过对已有文献报道的内切多聚半乳糖醛酸酶的亚位点进行序列和结构比对,确定了pePGB底物结合口袋中主要的亚位点残基(图1)。在酶底物结合口袋中,关键氨基酸残基侧链的尺寸大小是影响酶催化性能的重要因素。丙氨酸(Ala)是一种不带电荷的疏水性氨基酸,侧链为甲基,具有较小的空间位阻,对蛋白质的结构影响较小。内切多聚半乳糖醛酸酶作用的底物为多聚半乳糖醛酸,其是由半乳糖醛酸构成的线性直链多糖,聚合度高,分子质量较大。因此猜测将相关位点突变为丙氨酸可以扩大底物结合口袋,从而有效地提高内切多聚半乳糖醛酸酶的活力。对口袋处的31个氨基酸进行保守性分析,排除了保守性较高的以及在底物结合中发挥重要作用的氨基酸残基,最终选择了14个氨基酸位点(V144、Q145、S148、I149、N150、I180、S182、N203、S204、R229、S230、D231、V248和L292)分别进行丙氨酸突变。
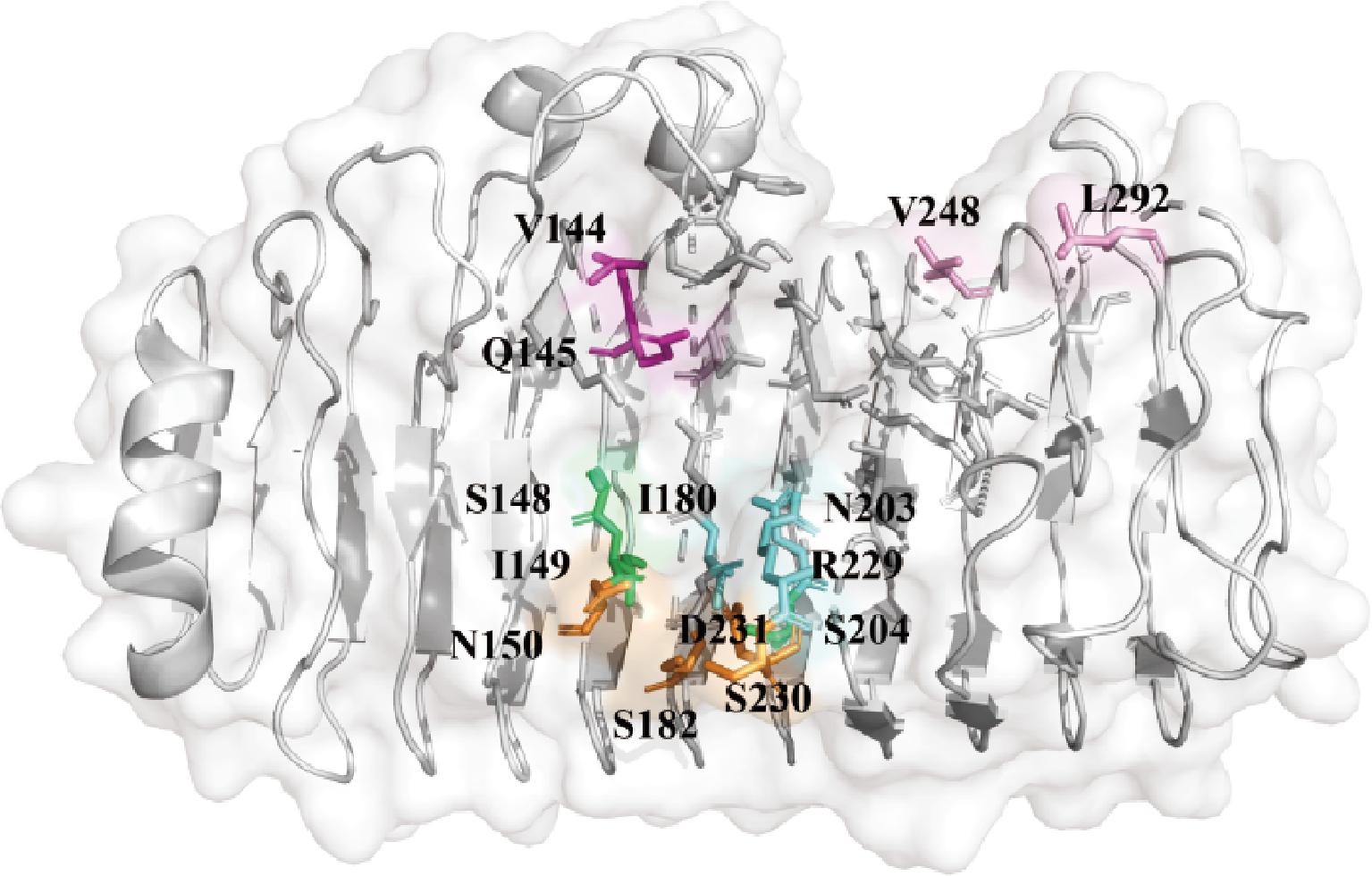
图1 pePGB底物结合口袋中亚位点氨基酸残基
Fig.1 The amino-acid residues of pePGB involved in the binding subsites
注:图中亚位点氨基酸残基用棍棒模型显示,选取的14个氨基酸位点用彩色表示,-4亚位点氨基酸用橙色表示,-3亚位点氨基酸用绿色表示,-2亚位点氨基酸用蓝色表示,-1亚位点氨基酸用紫色表示, +2亚位点氨基酸用粉色表示。
此外,根据文献报道,来源于嗜热真菌Achaetomium sp.Xz8的高比活多聚半乳糖醛酸酶PG8fn,其T3 loop区上的残基T113可能是使其具有高比活的原因之一[14]。且研究表明,该酶催化效率从大到小的顺序与113位点的氨基酸侧链性质相关,即带正电荷氨基酸(R、K)>极性氨基酸(S、Q、T)>非极性氨基酸(G、A、I)>带负电荷氨基酸(D)。因此,将pePGB与PG8fn进行序列比对,结果如图2所示,PG8fn的T113在pePGB对应的残基为G111。因此考虑对G111位点进行理性设计,将其突变为R和K。
图2 pePGB与PG8fn氨基酸序列比对
Fig.2 Amino-acid sequences alignment of pePGB and PG8fn
2.2 底物结合口袋的丙氨酸突变及验证
将选中的14株突变体进行菌株构建和摇瓶发酵验证,以确定合适的突变热点。对各突变体的粗酶液进行SDS-PAGE验证。其中I149A、I180A未能在K.phaffii中实现胞外表达,可能是由于突变后蛋白发生不正确折叠导致。其余突变体均正常表达,在SDS-PAGE上均显示为双条带且分子质量与野生型基本一致。
随后利用DNS法对突变体粗酶液进行酶活力测定,实验结果如图3所示。大部分突变体的催化活力都有不同程度的下降,突变体Q145A、N203A、R229A、L292A几乎检测不到酶活力,突变体S148A、S204A、S182A、D231A的酶活力大幅下降,而突变体V144A、S230A的酶活力也有略微下降。14个突变体中仅N150A和V248A酶活力分别提高了5.1%和9.2%。结果表明,在-3和-2亚位点中的残基对于催化作用都很重要,而远端亚位点的残基保守性相对较低。CHU等[15]将木聚糖酶亚位点上的一些残基突变为丙氨酸,其中位于+3亚位点的两个丙氨酸突变体W223A和Y256A表现出较高的催化效率。因此,选择活力提升最高的远端亚位点残基V248作为潜在突变热点,进行后续的理性设计。
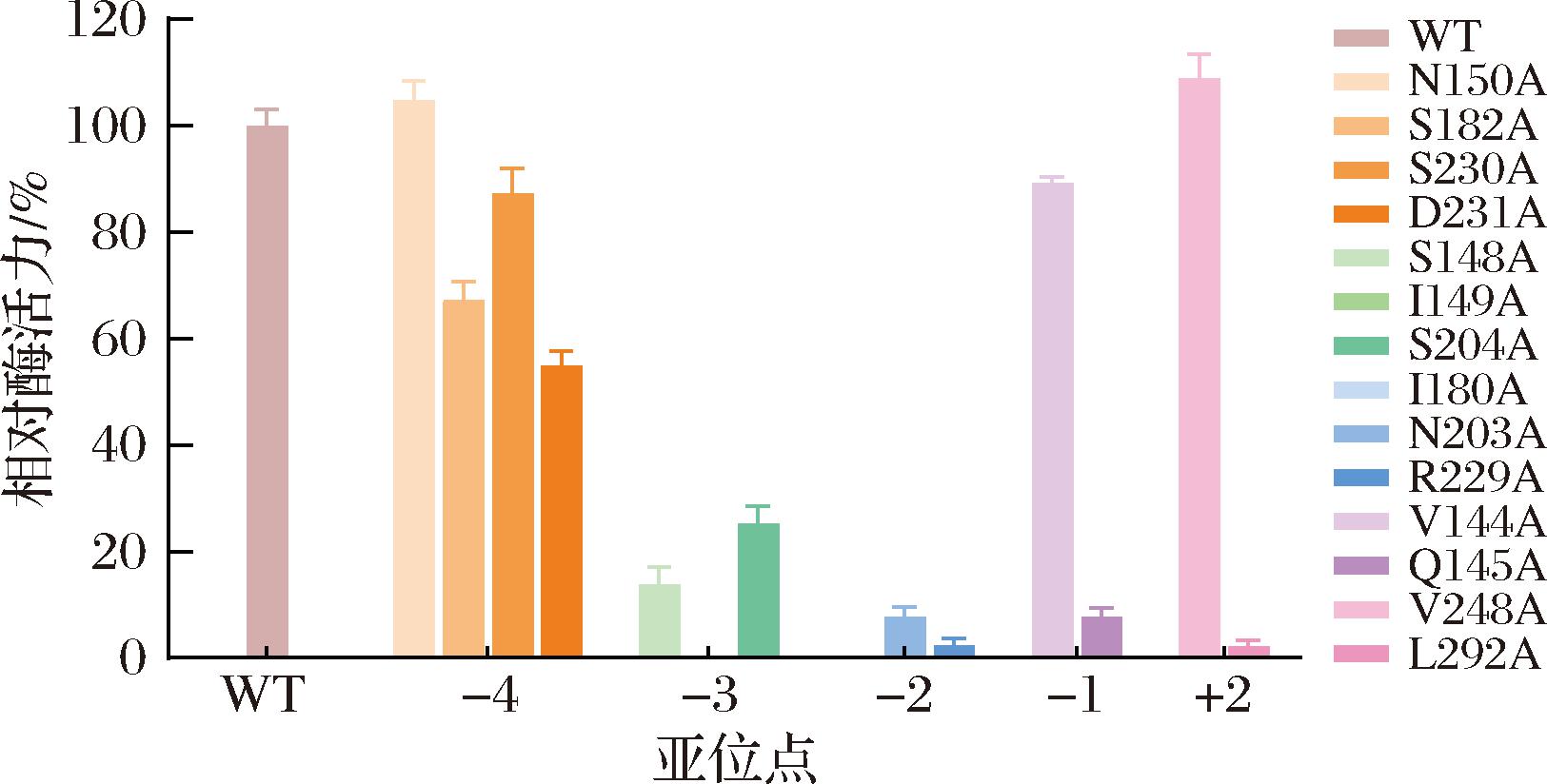
图3 pePGB及丙氨酸突变体的相对酶活
Fig.3 The relative activity of pePGB and alanine scanning mutants
2.3 突变位点的理性设计及验证
利用FoldX对pePGB的V248位点进行虚拟饱和突变,计算所有突变的折叠自由能变化DDG(DDG=DGMut-DGWt),根据表2的结果进行理性设计,选取了DDG值最低(<-1 kcal/mol)的两个突变体V248L、V248R。此外,从氨基酸侧链的空间角度以及所带电荷性质考虑,对pePGB的T3 loop区上的G111位点设计两个突变体G111R和G111K。
表2 突变体折叠自由能的变化
Table 2 Changes of folding free energy of mutants
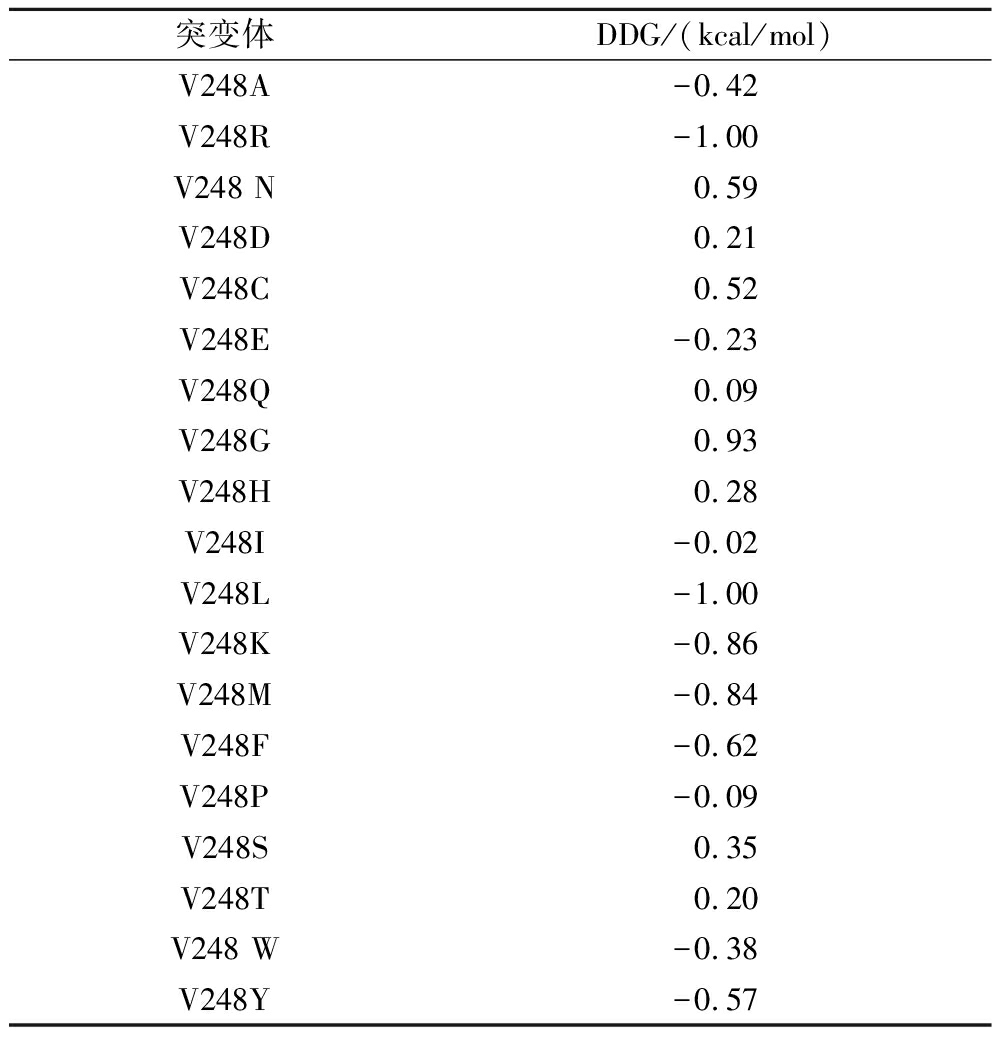
突变体DDG/(kcal/mol)V248A-0.42V248R-1.00V248 N0.59V248D0.21V248C0.52V248E-0.23V248Q0.09V248G0.93V248H0.28V248I-0.02V248L-1.00V248K-0.86V248M-0.84V248F-0.62V248P-0.09V248S0.35V248T0.20V248 W-0.38V248Y-0.57
将上述突变体进行菌株构建和摇瓶发酵,分别以多聚半乳糖醛酸和苹果果胶为底物与粗酶液进行反应,利用DNS法进行酶活力测定。结果如图4所示,除G111K外,其余突变体对于两种底物的酶活力相较于野生型都有不同程度的提高。其中V248R酶活力提升最为明显,无论是以多聚半乳糖醛酸还是以苹果果胶为底物,酶活力都能达到野生型的1.5倍左右。随后,将两个位点的有益突变体进行组合,构建双点突变体G111R/V248L和G111R/V248R,进行摇瓶发酵验证。结果如图5所示,双点突变体对于两种底物的酶活力有进一步提高,以多聚半乳糖醛酸为底物时,G111R/V248L和G111R/V248R的酶活力分别为野生型的1.72倍和1.84倍。由此可见,除了氨基酸残基侧链的尺寸大小外,氨基酸残基亲疏水性的强弱以及氨基酸残基所带电荷性质也是影响酶催化性能的关键因素。ABDUL WAHAB等[16]将来源于Geobacillus zalihae的脂肪酶氧阴离子洞中114位的的亲水性Gln分别替换为疏水性的Leu和Met,结果显示突变体Q114L的酯化反应转化率达到92%,显著高于野生型脂肪酶84.6%的转化率。汤恒[17]通过底物口袋电荷分析对蛋白酶SES7进行理性设计,重构了底物口袋的电荷分布和空间几何结构,从而使其对带正电荷的侧链残基底物的选择性从21%提高到50%。此外,结果也证明基于折叠自由能变化进行突变设计是一个有效的策略。ZHENG等[10]的研究也从一定程度上揭示了折叠自由能变化与催化活力变化之间的联系,研究发现突变体的稳定性在DDG>1时可能会降低,即使突变后的氨基酸在进化上是有利的,突变体的催化活力也会降低;而大多数DDG<0的突变体均表现出更好的催化活力。
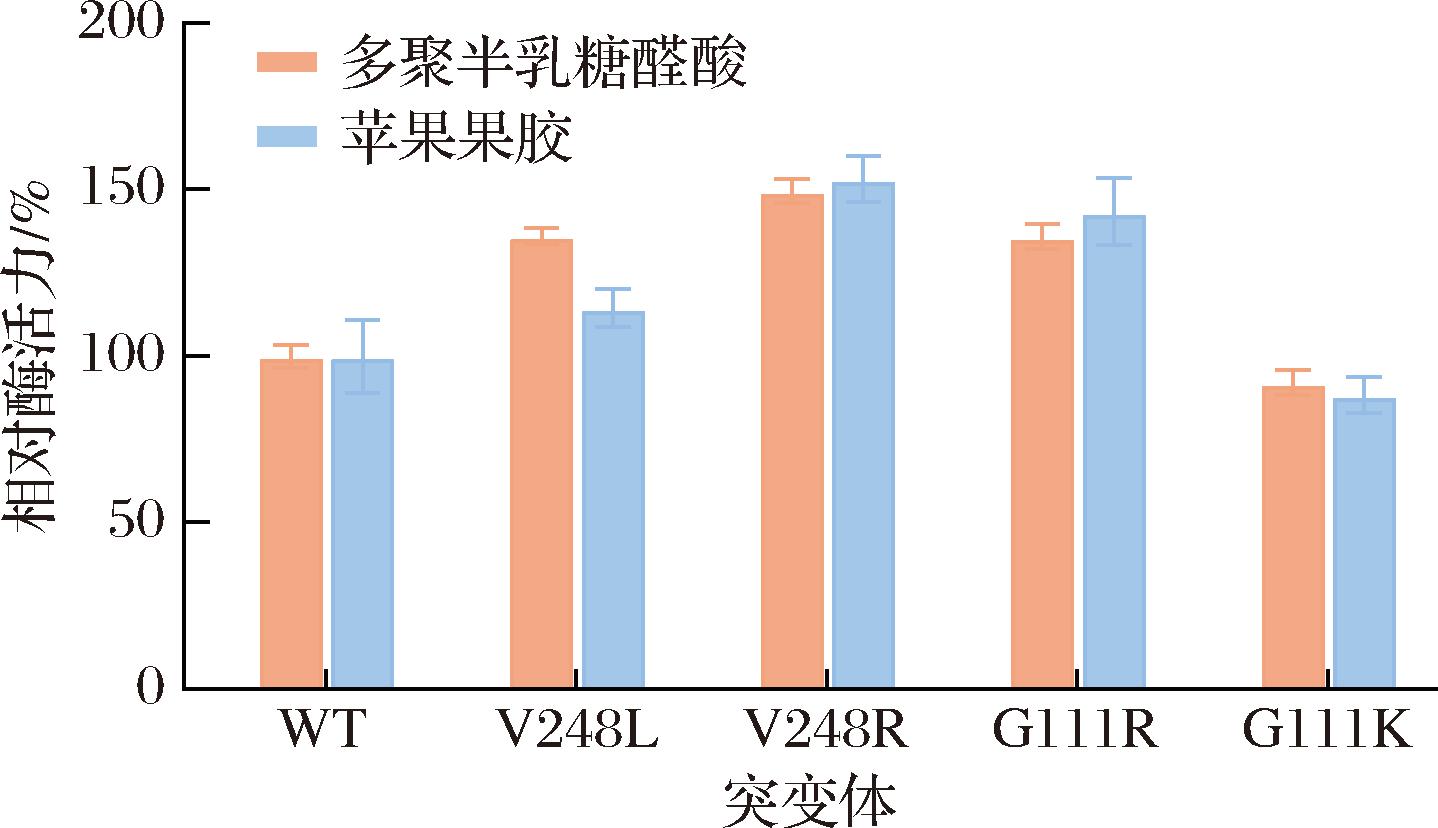
图4 pePGB及单点突变体的相对酶活
Fig.4 The relative activity of pePGB and single-point mutants
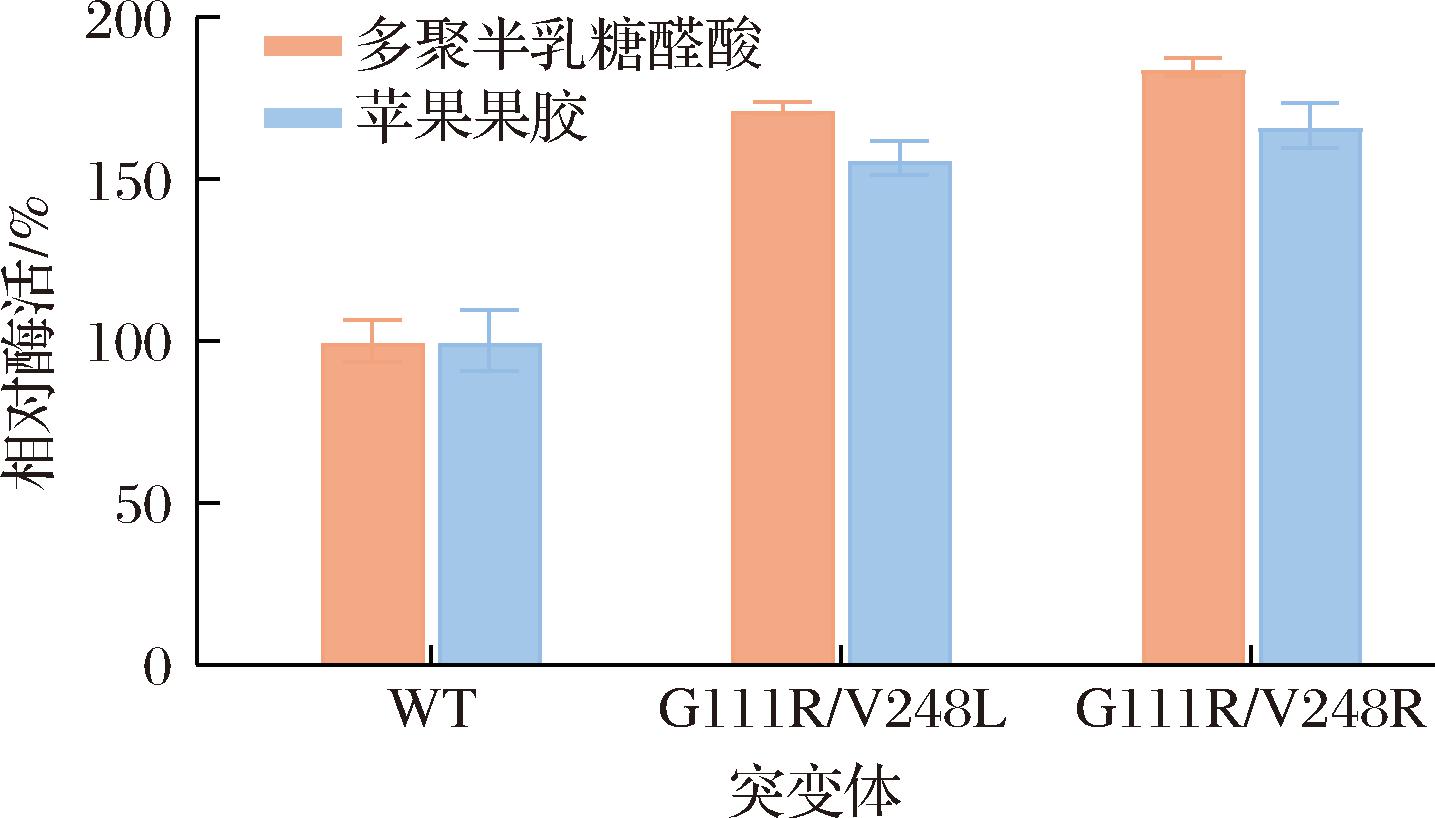
图5 pePGB及双点突变体的相对酶活
Fig.5 The relative activity of pePGB and double-point mutants
2.4 突变体的酶学性质测定
将双点突变体G111R/V248L和G111R/V248R发酵液进行纯化,探究突变对其酶学性质的影响。如图6所示,突变体与野生型的最适pH一致,均在pH 5.0时具有最大活力,突变体G111R/V248R在pH 5.5~6.0时相对活力高于野生型和突变体G111R/V248L。野生型和突变体在pH 3.0~8.0均具有较好的稳定性,在不同pH下孵育1 h后酶活力均未见明显损失。该结果与其他相关报道一致,表明内切多聚半乳糖醛酸酶是一类偏酸性的酶,且具有良好的pH稳定性[18-19]。
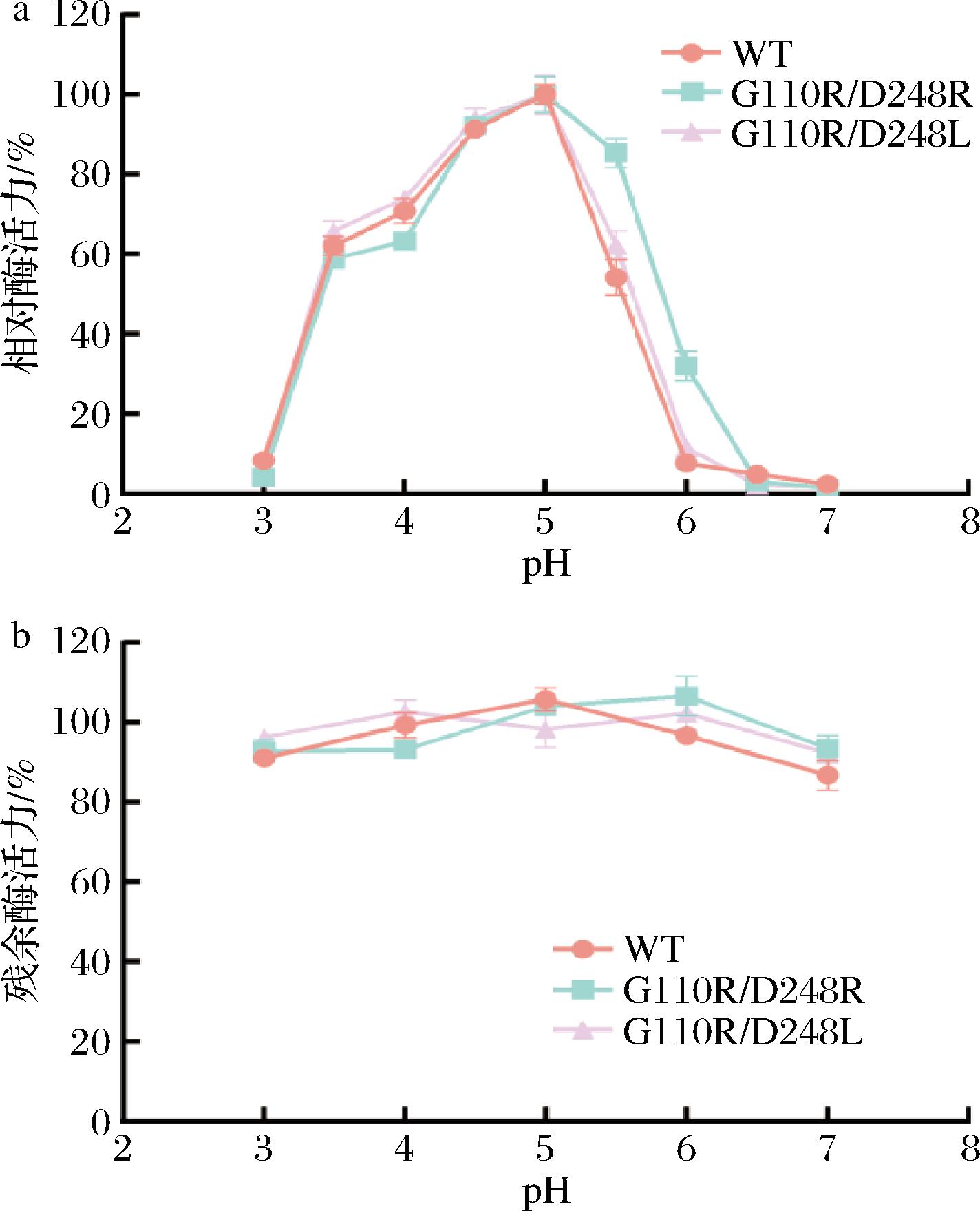
a-最适pH;b-pH稳定性
图6 双点突变体的最适pH和pH稳定性
Fig.6 The optimum pH and pH stability of double-point mutants
如图7所示,突变体与野生型的最适温度均为65 ℃,其中突变体G111R/V248R在70 ℃的相对活力为92.59%,明显高于野生型及突变体G111R/V248L的46.79%和45.87%,而60 ℃时突变体G111R/V248L的相对活力要高于另外两者,为95.31%。不同来源的内切多聚半乳糖醛酸酶具有不同的最适温度,大多介于40~50 ℃[20-22],只有少数嗜热真菌来源的酶最适温度能达到70 ℃左右[23-24]。在55 ℃下孵育20 min后,野生型残余活力为30.42%,突变体G111R/V248L和G111R/V248R残余活力分别为36.31%和16.85%。其中,突变体G111R/V248R整体热稳定性要略高于野生型及突变体G111R/V248L。当孵育时间延长至60 min,三者的残余活力均下降至5%以下,热稳定性都有所欠佳。内切多聚半乳糖醛酸酶多数属于中低温酶,基本都在30~50 ℃的环境中稳定。来自Penicillium oxalicum的内切多聚半乳糖醛酸酶PoxaEnPG28A在55 ℃下处理1 h后仅剩余约10%的残余酶活力[25]。
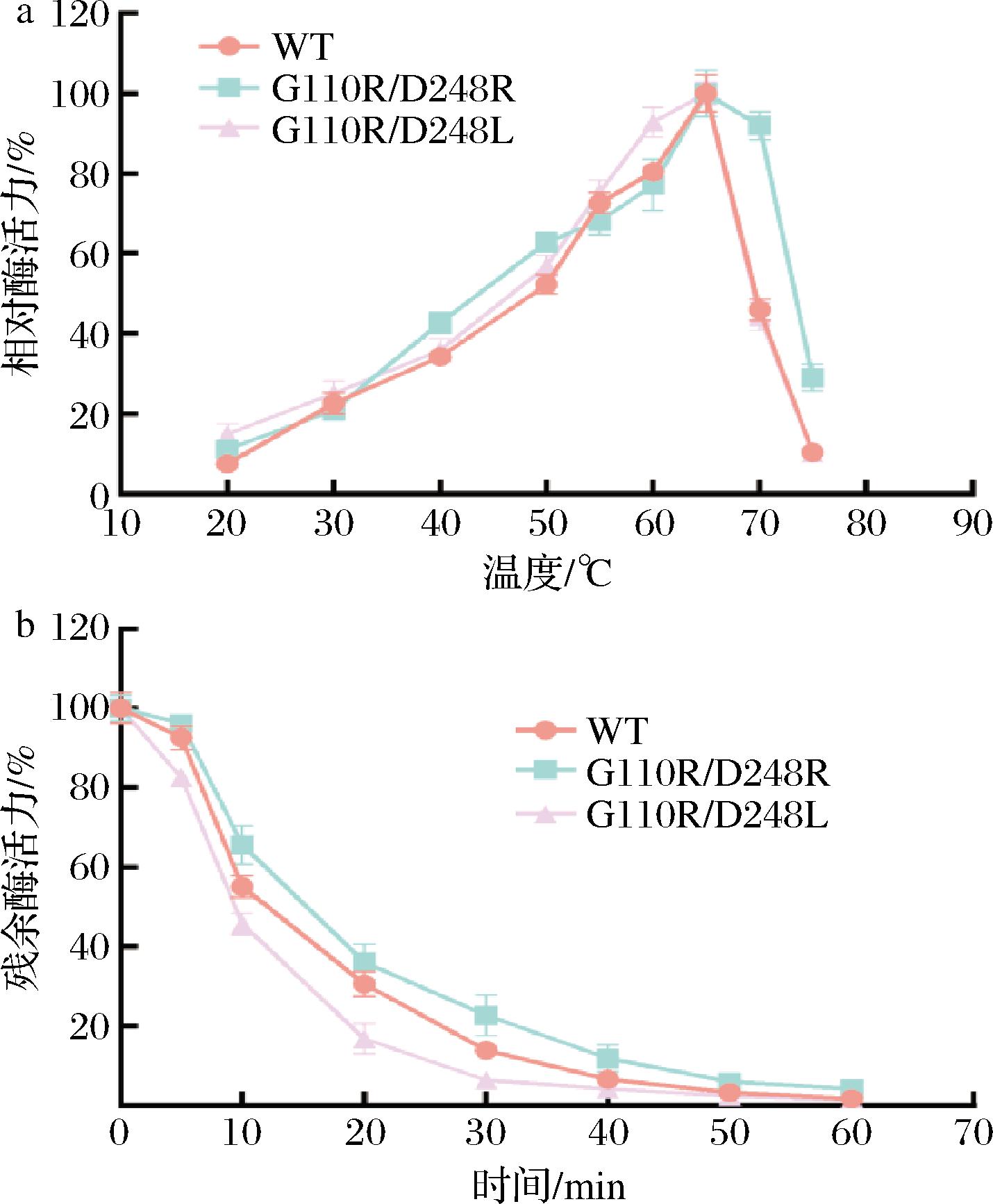
a-最适温度;b-热稳定性
图7 双点突变体的最适温度和热稳定性
Fig.7 The optimum temperature and thermostability of double-point mutants
突变体的动力学参数如表3所示,相较于野生型,突变体G111R/V248R具有更低的Km值和更高的kcat值,说明G111R/V248R具有更好的底物亲和力,且催化效率提升至野生型的2.06倍。而突变体G111R/V248R的Km值为3.61 g/L,比野生型略高,由于其kcat值较高,因此催化效率也能达到野生型的1.78倍。该催化速率远高于已有报道的Stereum purpureum[23]、Aspergillus nidulans[19]和P.oxalicum[26]等来源的内切多聚半乳糖醛酸酶。
表3 双点突变体的动力学参数
Table 3 The kinetic parameters of double-point mutants

名称Km/(g/L)Vmax/[μmol/(min·mg)]kcat/s-1kcat/Km/L/(g·s)野生型3.5518 17611 2383 165G111R/V248R3.1332 96120 3816 507G111R/V248L3.6132 94220 3695 644
2.5 突变位点分析
利用AlphaFold2[12-13]对pePGB及最佳突变体G111R/V248R进行了同源建模,随后通过Schrödinger Maestro[27]将其与底物寡糖五聚半乳糖醛酸(GalpA5)进行分子对接,利用PyMol对结果进行展示与分析。如图8所示,248位的缬氨酸突变为精氨酸后,与底物距离减小并形成了两个新的氢键,增强了酶与底物结合的相互作用,从而提高了酶的催化活力。大量研究表明,氢键在底物识别和结合中起着重要作用。ZHENG等[28]通过多序列比对及饱和突变筛选得到了突变体N233A和N233G,使得纤维素酶GtCel5的催化活力分别提高了1.3倍和1.7倍。分析表明该突变增加了酶与底物之间的局部氢键相互作用,使得底物亲和力和催化效率得到增强。此外,WANG等[29]研究表明,木聚糖酶TlXyn10A中Loop 4上的G149D能够与底物形成新的氢键,可能对其催化性能的提高起着重要作用。
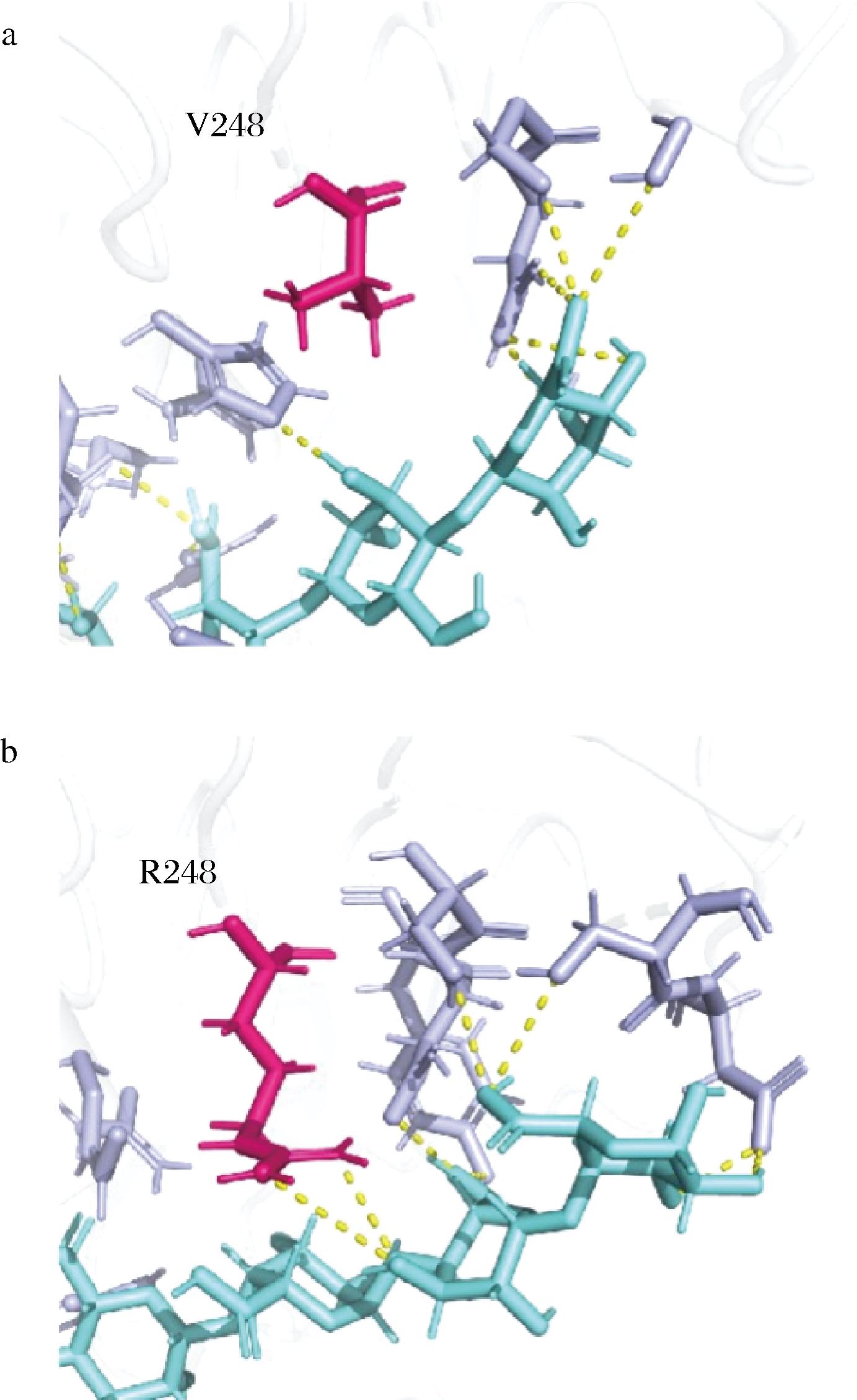
a-野生型pePGB;b-突变体G111R/V248R
图8 重组酶与GalpA5的相互作用
Fig.8 The interaction between recombinant enzymes and GalpA5
注:图中配体GalpA5用蓝色显示,突变前后的氨基酸残基用 红色显示,黄色虚线表示重组酶与GalpA5的氢键相互作用。
而111位的甘氨酸突变为精氨酸后,未直接对酶与底物间的相互作用造成影响,但可能与248位的精氨酸存在协同作用,使得底物口袋携带有更多的正电荷,从而进一步提高了酶与电负性底物的结合能力(图9)。先前也有研究发现,由于底物多聚半乳糖醛酸是一种带负电荷的高分子多糖,向底物口袋中引入带正电荷的氨基酸可能会促进酶与底物的结合。李烨青[30]研究了来源于Talaromyces leycettanus JCM12802的多聚半乳糖醛酸酶TePG28b,将其底物口袋的非催化位点中带负电的天冬氨酸突变为带正电的赖氨酸,使其比活力提高了0.8倍,催化效率提高了0.2倍,并使用同样的策略将Bispora sp.MEY-1来源的内切多聚半乳糖醛酸酶BsPG28a的比活力和催化效率分别提高了2.8倍和2.5倍。此外,该突变体的对接分数为-7.184 kcal/mol,小于野生型的-6.901 kcal/mol,也证明该突变有利于增强酶与底物的结合(表4)。

a-野生型pePGB;b-突变体G111R/V248R
图9 底物结合口袋的表面静电势
Fig.9 Surface electrostatic potential map of binding pocket
表4 重组酶与GalpA5的对接分数
Table 4 The docking score of recombinant enzymes with GalpA5

受体配体对接分数/(kcal/mol)pePGBPentagalacturonic-acid-6.901G111R/V248RPentagalacturonic-acid-7.184
3 结论
本研究利用同源建模预测了内切多聚半乳糖醛酸酶pePGB的三维结构,并结合文献报道及计算机预测对其相应的突变热点(底物口袋中的V248位点及口袋上方loop区的G111位点)进行了理性设计,筛选获得了3个酶活力提高的突变体V248L、V248R和G111R,有序叠加后获得最佳突变体G111R/V248R,在不损失其热稳定性的基础上,比活力和催化效率kcat/Km分别提高了1.84倍和2.06倍。分子对接及底物口袋静电势分析表明,氢键相互作用的增加及口袋正电性的增强是G111R/V248R突变体催化活力提高的可能原因。该研究为该酶后续工业化应用奠定了重要基础,也为其他工业酶的理性改造提供了思路和参考。但改造后的突变体热稳定性仍有所欠佳,后续可以尝试在此基础上对其进行提高热稳定性的改造,以拓宽其工业应用范畴,提升其工业价值。
[1] ROPARTZ D, RALET M C.Pectin Structure[M].KONTOGIORGOS V, ed.Pectin:Technological and Physiological Properties.Cham:Springer International Publishing, 2020:17-36.
[2] VAN SANTEN Y, BENEN J A, SCHRÖTER K H, et al.1.68-A crystal structure of endopolygalacturonase Ⅱ from Aspergillus niger and identification of active site residues by site-directed mutagenesis[J].Journal of Biological Chemistry, 1999, 274(43):30474-30480.
[3] WONGKAEW M, TANGJAIDEE P, LEKSAWASDI N, et al.Mango pectic oligosaccharides:A novel prebiotic for functional food[J].Frontiers in Nutrition, 2022, 9:798543.
[4] PINTO G P, CORBELLA M, DEMKIV A O, et al.Exploiting enzyme evolution for computational protein design[J].Trends in Biochemical Sciences, 2022, 47(5):375-389.
[5] TU T, LI Y Q, LUO Y, et al.A key residue for the substrate affinity enhancement of a thermophilic endo-polygalacturonase revealed by computational design[J].Applied Microbiology and Biotechnology, 2018, 102(10):4457-4466.
[6] SCHYMKOWITZ J, BORG J, STRICHER F, et al.The FoldX web server:An online force field[J].Nucleic Acids Research, 2005, 33(Web Server issue):W382-W388.
[7] ROHL C A, STRAUSS C E M, MISURA K M S, et al.Protein structure Prediction Using Rosetta[M].Amsterdam:Elsevier, 2004:66-93.
[8] DEHOUCK Y, KWASIGROCH J M, GILIS D, et al.PoPMuSiC 2.1:A web server for the estimation of protein stability changes upon mutation and sequence optimality[J].BMC Bioinformatics, 2011, 12:151.
[9] BEDNAR D, BEERENS K, SEBESTOVA E, et al.FireProt:Energy-and evolution-based computational design of thermostable multiple-point mutants[J].PLoS Computational Biology, 2015, 11(11):e1004556
[10] ZHENG J, LIU H Q, QIN X, et al.Identification and mutation analysis of nonconserved residues on the TIM-barrel surface of GH5_5 cellulases for catalytic efficiency and stability improvement[J].Applied and Environmental Microbiology, 2022, 88(17):e0104622.
[11] 郝梦洁. 青霉内切多聚半乳糖醛酸酶的表征及热稳定性改造[D].无锡:江南大学, 2023.HAO M J.Expression, characterization and thermostability modification of endo-polygalacturonase from Penicillium sp.[D].Wuxi:Jiangnan University, 2023.
[12] JUMPER J, EVANS R, PRITZEL A, et al.Highly accurate protein structure prediction with AlphaFold[J].Nature, 2021, 596(7873):583-589.
[13] MIRDITA M, SCHÜTZE K, MORIWAKI Y, et al.ColabFold:Making protein folding accessible to all[J].Nature Methods, 2022, 19(6):679-682.
[14] TU T, PAN X, MENG K, et al.Substitution of a non-active-site residue located on the T3 loop increased the catalytic efficiency of endo-polygalacturonases[J].Process Biochemistry, 2016, 51(9):1230-1238.
[15] CHU Y D, TU T, PENTTINEN L, et al.Insights into the roles of non-catalytic residues in the active site of a GH10 xylanase with activity on cellulose[J].Journal of Biological Chemistry, 2017, 292(47):19315-19327.
[16] ABDUL WAHAB R, BASRI M, RAJA ABDUL RAHMAN R N Z, et al.Development of a catalytically stable and efficient lipase through an increase in hydrophobicity of the oxyanion residue[J].Journal of Molecular Catalysis B:Enzymatic, 2015, 122:282-288.
[17] 汤恒. 高效降解β-乳球蛋白的蛋白酶的性能优化及结构解析[D].无锡:江南大学, 2020.TANG H.Optimization and structure analysis of a protease with highly beta-lactoglobulin degradation ability[D].Wuxi:Jiangnan University, 2020.
[18] HAO M J, WU D, XU Y, et al.A novel endo-polygalacturonase from Penicillium rolfsii with prebiotics production potential:cloning, characterization and application[J].Foods, 2022, 11(21):3469.
[19] XU H, ZHANG P F, ZHANG Y C, et al.Overexpression and biochemical characterization of an Endo-α-1, 4-polygalacturonase from Aspergillus nidulans in Pichia pastoris[J].International Journal of Molecular Sciences, 2020, 21(6):2100.
[20] TU T, BAI Y G, LUO H Y, et al.A novel bifunctional pectinase from Penicillium oxalicum SX6 with separate pectin methylesterase and polygalacturonase catalytic domains[J].Applied Microbiology and Biotechnology, 2014, 98(11):5019-5028.
[21] LIU M Q, DAI X J, BAI L F, et al.Cloning, expression of Aspergillus niger JL-15 endo-polygalacturonase a gene in Pichia pastoris and oligo-galacturonates production[J].Protein Expression and Purification, 2014, 94:53-59.
[22] TU T, LUO H Y, MENG K, et al.Improvement in thermostability of an Achaetomium sp.strain Xz8 endopolygalacturonase via the optimization of charge-charge interactions[J].Applied and Environmental Microbiology, 2015, 81(19):6938-6944.
[23] CARLI S, MELEIRO L P, WARD R J.Biochemical and kinetic characterization of the recombinant GH28 Stereum purpureum endopolygalacturonase and its biotechnological application[J].International Journal of Biological Macromolecules, 2019, 137:469-474.
[24] LI Y Q, WANG Y, TU T, et al.Two acidic, thermophilic GH28 polygalacturonases from Talaromyces leycettanus JCM 12802 with application potentials for grape juice clarification[J].Food Chemistry, 2017, 237:997-1003.
[25] CHENG Z, CHEN D, WANG Q Y, et al.Identification of an acidic endo-polygalacturonase from Penicillium oxalicum CZ1028 and its broad use in major tropical and subtropical fruit juices production[J].Journal of Bioscience and Bioengineering, 2017, 123(6):665-672.
[26] LU B, XIAN L, ZHU J, et al.A novel endo-polygalacturonase from Penicillium oxalicum:Gene cloning, heterologous expression and its use in acidic fruit juice extraction[J].Journal of Microbiology and Biotechnology, 2022, 32(4):464-472.
[27] SHERMAN W, DAY T, JACOBSON M P, et al.Novel procedure for modeling ligand/receptor induced fit effects[J].Journal of Medicinal Chemistry, 2006, 49(2):534-553.
[28] ZHENG F, TU T, WANG X Y, et al.Enhancing the catalytic activity of a novel GH5 cellulase Gt Cel5 from Gloeophyllum trabeum CBS 900.73 by site-directed mutagenesis on loop 6[J].Biotechnology for Biofuels, 2018, 11:76.
[29] WANG X Y, HUANG H Q, XIE X M, et al.Improvement of the catalytic performance of a hyperthermostable GH10 xylanase from Talaromyces leycettanus JCM12802[J].Bioresource Technology, 2016, 222:277-284.
[30] 李烨青. 真菌来源的嗜热果胶酶基因挖掘及其催化效率的改造[D].南昌:江西农业大学, 2018.LI Y Q.Fungal thermophilic polygalacturonase gene exploit and catalytic efficiency molecular modification[D].Nanchang:Jiangxi Agricultural University, 2017.