对绿色溶剂的研发和应用已成为绿色化学领域的聚焦热点。传统溶剂存在环境污染、毒性大且不可再生等问题,替代传统溶剂的离子液体虽对环境影响较小,但制备难度大、成本高且回收困难。因此,迫切需要一种能够有效替代离子液体的绿色溶剂来突破当前应用领域困境。低共熔溶剂(deep eutectic solvent,DES)是在2000年由ABBOTT等提出的一种溶剂,由两种或两种以上的氢键供体(hydrogen bond donor,HBD)和氢键受体(hydrogen bond acceptor,HBA)在氢键作用下形成[1]。作为一种新型溶剂来源,DES易于制备、成本低廉、可生物降解,具有良好的选择性和稳定性,能够作为离子溶剂的优秀替代品。DES具有熔点低、易制备、对环境友好等特点,在天然产物提取、化学催化、有机合成、药物溶解、生物转化和二氧化碳吸收等方面具有广阔前景[2]。DES不仅可提供一种独特的平台来探索各种化学反应和过程,还有助于解决一些传统溶剂难以处理的问题。例如,在黄酮类、酚酸类、多糖类等天然产物的成分提取方面,DES的应用能明显改善天然产物的提取率与选择性。此外,利用DES进行电化学吸附可实现高效、选择性和环境友好的金属沉积;同时,它也为生物大分子的提取和纯化提供新途径。目前DES的结构及其形成机理尚未有全面研究,但DES的形成主要依赖于氢键作用。DES的氢键作用是由氢键供体与受体形成的,不同比例HBA和HBD组成的DES可形成不同种类及数量的氢键。其中,氢键能使电子间产生离域现象,打破分子间稳定的结构,难以形成规则的晶体结构。氢键的强弱直接影响到DES的物化性质,如凝固点随HBA比例减少而呈现上升的趋势,氢键作用越强,凝固点越低。综上,本文将系统总结并重点概述DES的生化性质及其在天然产物提取、食品检测分析和催化反应介质等的应用趋势,阐述该领域目前存在的主要问题及解决方法,为进一步探究并应用此类绿色溶剂体系提供重要的科学依据。
1 生化性质
1.1 分类组成
根据不同HBD和HBA种类的组合,可将DES划分为5种类型(表1)。第1种为季铵盐和无水金属氯化物组合,例如氯化胆碱与AlCl3,这是最早被研究的DES体系之一;第2种为季铵盐和含结晶水金属氯化物组合,例如氯化胆碱和CoCl2·6H2O等;第3种为季铵盐与酰胺、羧酸、醇等组合,例如氯化胆碱和乙酸等;第4种为有机配体和金属卤化物组合,例如尿素和AlCl3等;第5种为天然氨基酸和天然植物酸组合,例如甜菜碱-柠檬酸组合等。此外,根据酸碱度的差异,可将DES进一步细分为酸性、中性和碱性DES。而根据其组成成分的不同,可将其进一步分为双相和三相DES,例如甜菜碱-脯氨酸-蔗糖的组合[3]。近年来,DES独特的组成特性使其具备了结构可设计性,可通过调控HBD和HBA的种类及含量合成不同类型的DES。
表1 DES的5种类型
Table 1 The five types of DES

类型通式条件例子特点季铵盐-无水金属氯化物R4N+X-+MClxM=Al、Fe、Ag、CuChCl+AlCl3容易受环境湿度影响季铵盐-含结晶水金属氯化物R4N+X-+MClx·xH2OM=Co、Fe、Ni、CuChCl+CoCl2·6H2O生产成本低廉、不受生产环境湿度影响季铵盐-酰胺、羧酸、醇R4N+X-+RZZ=OH、COOH、CONH4ChCl+CH3COOH能进行批量生产、成本低廉、能生物降解有机配体-金属卤化物有机配体+MClxM=Al、Zn有机配体=EG、UreaAlCl3+CH4N2O该类DES在非水体系中,不能离子化天然氨基酸-天然植物酸--L-脯氨酸-草酸、L-脯氨酸-葡萄糖、甜菜碱-苹果酸分子间作用明显、与水发生剧烈反应
1.2 物化特性
1.2.1 熔点
DES是一类由HBD和HBA在一定比例下混合形成的两相或多相系统,通常在室温下是液态且具有比单个组分更低的熔点。以常见尿素-氯化胆碱(1∶2)为例,其形成的强氢键作用使混合物的熔点降低至12 ℃,显著低于各单个组分的熔点[4]。在这种情况下,混合物可在12 ℃时融化,远低于尿素(约133 ℃)和氯化胆碱(约302 ℃)熔点。这是由于当两种或多种物质以特定摩尔比混合时可形成共熔点,这是混合物熔点比单组分熔点要低的原因。因而,可通过调整HBD和HBA的比例及组分来调控DES熔点。
1.2.2 密度和黏度
密度和黏度是DES应用的重要物性参数。DES性能主要受到HBD和HBA之间的氢键和范德华力的影响,其密度通常通过比重计进行测定,一般高于水的密度。CEA-KLAPP等[5]使用密度梯度理论以及扰动链统计关联流体理论来研究DES的物理化学性质,结果表明DES密度通常随着温度的升高而降低,这与一般物质的物理行为一致。而DES的黏度一般小于500 mPa,不过在常温下,其黏度比水高出十倍甚至几百倍,这主要是因为氢键网络结构导致DES分子流动性降低。从而表现出极高的黏性。KHOKHAR等[6]通过测定不同DES在不同温度下的动态黏度,发现随着尿素含量增加,DES的动态黏度降低。这可能是由于尿素的加入减弱了介质中的氢键作用和其他相互作用,导致黏度降低,此外,还发现动态黏度随着温度的升高而降低,这是由于温度升高导致氢键作用减弱。值得注意的是,DES的黏度与其成分,即包括HBD和铵盐类型、有机盐/HBD摩尔比、含水量及温度等因素密切相关。通常高含水量导致氢键断裂从而降低DES黏度。
1.2.3 电导率
溶剂的电导率是影响电化学应用的一个关键因素。DES的导电性受黏度、HBA/HBD摩尔比、HBA/HBD性质、季铵盐的阴离子以及含水量等因素的影响。QU等[7]对5种亲水性和3种疏水性DES的电导率进行测试,得出疏水性DES电导率普遍高于亲水性DES。电导率的差异可能会影响DES在特定应用中的选择,特别是在电化学或涉及离子传输的应用中。因黏度较高而导致大多数的电导率极低(室温下一般在2 mS/cm以下)。针对此现象,SIRVIÖ团队[4]对首次对氯化胆碱-尿素的导电性能进行探究,结果表明在温度上升的过程中,DES的黏度降低,提高流动性继而提高传质效率,且组成成分比例、含水量不同,均会影响DES体系的电导率。
1.2.4 溶解性
与传统的有机溶剂相比,DES更易于溶解金属氧化物、二氧化碳等气体以及难溶于水的有机物质,并且可以利用对不同成分的溶解度差异来进行分离和萃取。对于DES中的金属氧化物而言,随着温度升高,其溶解度也随之提升。气体的溶解能力则随温度升高而减弱。LIN等[8]开发了一种新型的支撑液膜,通过将DES嵌入到二维材料钛碳化物(Ti3C2Tx)的纳米缝隙中实现CO2的高效分离,结果表明Ti3C2Tx表面的官能团可与DES中的分子形成氢键,这种作用力对于稳定DES在Ti3C2Tx纳米膜间的位置至关重要,还影响到DES中气体分子的溶解和扩散行为。而且随着温度升高Ti3C2Tx纳米膜对CO2的选择性降低,这主要是因为高温会减弱包括氢键在内分子间相互力,从而减少CO2与DES的相互作用。
1.2.5 亲水性和疏水性
DES的亲/疏水性决定其与水和其他分子相互作用的方式。QU等[7]通过合成不同的DES并优化对磺胺类抗生素的提取条件,提出一种可减少有毒溶剂使用,并能简化操作步骤的分散液-液微萃取技术。LIU等[9]系统阐述了DES中亲水性和疏水性这两个关键概念,阐明DES的亲水性/疏水性平衡,即DES在具有亲水性成分的同时也可展现出对疏水性化合物的溶解能力,这种平衡转换对于DES在提取和溶解天然产物显得至关重要。
1.3 合成制备
不同的DES制备方法如表2所示。
表2 DES制备方法的优缺点及其应用
Table 2 Advantages, disadvantages and applications of DES preparation methods
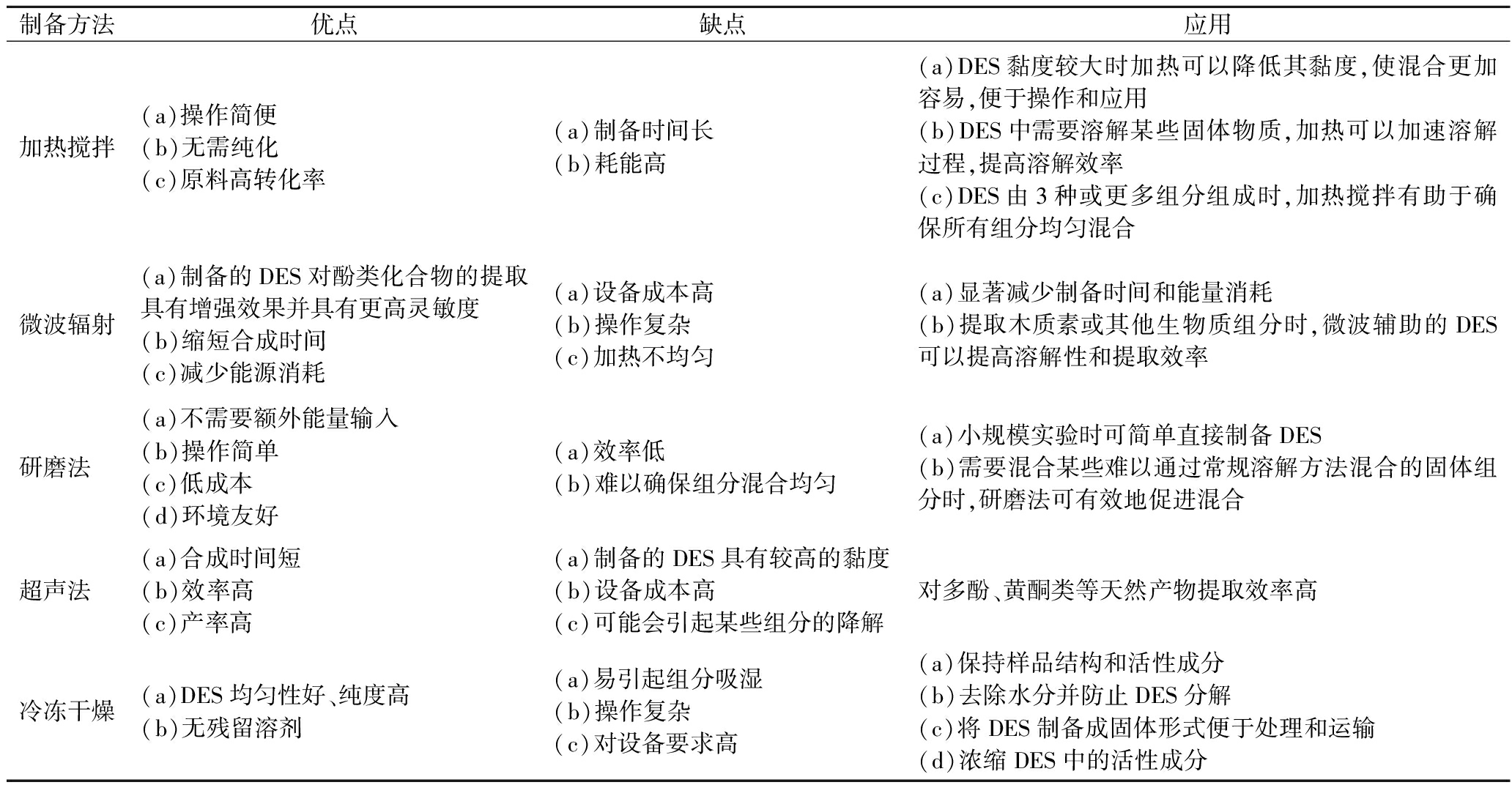
制备方法优点缺点应用加热搅拌(a)操作简便(b)无需纯化(c)原料高转化率(a)制备时间长(b)耗能高(a)DES黏度较大时加热可以降低其黏度,使混合更加容易,便于操作和应用(b)DES中需要溶解某些固体物质,加热可以加速溶解过程,提高溶解效率(c)DES由3种或更多组分组成时,加热搅拌有助于确保所有组分均匀混合微波辐射(a)制备的DES对酚类化合物的提取具有增强效果并具有更高灵敏度(b)缩短合成时间(c)减少能源消耗(a)设备成本高(b)操作复杂(c)加热不均匀(a)显著减少制备时间和能量消耗(b)提取木质素或其他生物质组分时,微波辅助的DES可以提高溶解性和提取效率研磨法(a)不需要额外能量输入(b)操作简单(c)低成本(d)环境友好(a)效率低(b)难以确保组分混合均匀(a)小规模实验时可简单直接制备DES(b)需要混合某些难以通过常规溶解方法混合的固体组分时,研磨法可有效地促进混合超声法(a)合成时间短(b)效率高(c)产率高(a)制备的DES具有较高的黏度(b)设备成本高(c)可能会引起某些组分的降解对多酚、黄酮类等天然产物提取效率高冷冻干燥(a)DES均匀性好、纯度高(b)无残留溶剂(a)易引起组分吸湿(b)操作复杂(c)对设备要求高(a)保持样品结构和活性成分(b)去除水分并防止DES分解(c)将DES制备成固体形式便于处理和运输(d)浓缩DES中的活性成分
1.3.1 加热搅拌
使用加热搅拌法能够简便地制备DES,即向圆底烧瓶中加入适量的HBA和HBD,并密封后放置于特定温度的水浴锅中进行磁力搅拌加热,直至形成澄澈透明的均质溶液,最后在阴凉干燥的环境中保存。这一方法为最常见的一种合成手段[10],具有操作简便,无需纯化,原料转化率高的优点。
1.3.2 微波辐射
一定量的HBA和HBD被混合后辅助微波辐射处理可迅速形成共熔体系[11],对微波辐射辅助合成的DES进行检测发现其将制备时间从传统的30~90 min显著缩短至20 min,并将能耗从0.650 kW·h/样品降低到0.001 kW·h/样品,同时保持与传统加热搅拌法相当的物理化学性质和分析性能,甚至在电化学检测中显示出更高的灵敏度,为DES可持续合成提供一种创新的解决方案。
1.3.3 研磨法
在室温下,适量的HBA和HBD混合后,通过用研钵进行研磨直至形成澄清液体。该方法主要通过物理方法促进组分间的相互作用形成氢键[12]。研磨法与加热法相比,不需要额外能量输入。LI等[13]将MgCl2·6H2O∶尿素(1∶2)混合,在室温下研磨可形成均匀的DES。该研磨法优点在于它的简单性、成本效益和环境友好性,避免使用大量的溶剂和高温条件,而且此方法还可通过改变研磨时间和力度来控制DES的均匀性和反应动力学。
1.3.4 超声法
超声波能量有助于促进HBA和HBD间的相互作用形成均一的DES。WANG等[14]将一定摩尔比的氯化胆碱分别和甘油、乳酸及1,2-丙二醇在超声波浴中60 ℃下处理60 min可形成均匀清澈的液体。相比传统制备方法,超声法制备DES的时间较短且效率较高,但是也可能导致获得的DES具有较高黏度从而影响其利用率。
1.3.5 冷冻干燥
冷冻干燥技术可将水分充分去除,获得纯净、均匀和无水的DES。NAM等[15]通过冷冻干燥法制备多种DES,并筛选出最适DES(L-脯氨酸/甘油)用黄酮类化合物的提取产率达到14%,比使用甲醇提取更有效。通过冷冻干燥合成的DES具有均匀性好、纯度高、无残留溶剂等优点,适合于对溶剂纯度要求高的生化应用。该方法有助于加速溶解组分,但也易引起吸湿,进而影响到溶剂中的水分含量,并且操作复杂且对设备要求较高。
1.4 影响因素
1.4.1 温度
温度是影响DES物化特性的关键因素之一。TARIKUZZAMAN等[16]对一系列糖基DES进行表征,以葡萄糖基DES为例,随着温度从22 ℃升到80 ℃,其密度从1.207 0 g/mL降至1.202 5 g/mL,黏度从569.33 mPa·s降至34.83 mPa·s,电导率从129 3 μS/cm增至357 3.33 μS/cm。随着温度的增加,DES密度降低,而电导率增加,这与分子振动的增强和离子迁移率的提升有关。同时,黏度呈现出随温度升高而显著降低的趋势,这对于降低工业应用中的流动阻力至关重要。FTIR分析表明,在DES中可能形成了超分子结构,且这种结构可能受到温度变化的影响。这些发现表明,通过精确控制温度,可有效地调节DES的物化特性,以满足各种工业过程的需求。
1.4.2 含水量的影响
DES中的含水量同样对其有显著影响。王岩等[17]通过近红外光谱分析,研究揭示了不同含水量对DES的氢键网络结构和流变性质的具体影响。实验观察到,水分子在DES中以3种形态存在:自由水、与尿素羰基结合的水和尿素氨基之间的桥接水。当含水量低于40%时,DES的氢键结构保持完整,体系黏度变化不大。随着含水量的增加至40%至80%,自由水开始形成,导致氢键断裂和黏度显著降低,但适量的桥接水有助于维持体系的稳定性。然而,含水量超过80%时,DES的稳定性降低,黏度进一步降低,体系趋向于水溶液特性。这些发现为调整DES的含水量以优化其性能提供重要依据。
1.4.3 氢键
氢键是分子间的一种强相互作用力,它能够显著改变物质的物理和化学性质。HBD与HBA之间会形成氢键,会降低混合物的熔点。ARAVENA等[18]通过分子动力学模拟量化不同分子对之间可以建立的氢键数量,发现氢键的数量和强度受到HBD与HBA之间相互作用的影响,这些相互作用不仅决定了DES的密度和黏度,还影响了它们与水混合时的行为。例如,增加的HBD可以破坏DES的有序结构,而HBD烷基链的延长则增强分子间的相互作用。这些发现对于设计和优化DES在各种工业应用中的使用至关重要,尤其是在需要特定溶剂特性的化学过程设计中。
1.4.4 溶质极性
溶质极性对DES的影响主要体现在萃取效率上。ALSHAMMARI等[19]分别使用4种DES在两种温度下提取7种简单溶质(包括丁酸、1-戊醇、2-戊酮、乙酸乙酯、苯酚、苯甲醇和环己醇),以确定相转移的热力学参数。研究表明能形成氢键的极性溶质更易被萃取,且萃取效率与溶质的pKa值成正比。由此可得出溶质的极性是影响DES萃取效率的一个重要因素。
2 功效应用
2.1 天然产物提取
天然产物提取通常用到有机溶剂,例如乙醇、己烷和氯仿等,但这些有机溶剂通常存在一定毒性,对环境易产生不良影响。DES作为新型绿色溶剂,具有溶解性强和低毒性等特质,在天然产物分离提取中具有广泛应用。DES在萃取中易与黄酮类、酚类、酚酸类和生物碱类等物质形成分子间氢键,可最大程度上增大提取效率。师聪等[20]用5种不同的DES提取草果中的总黄酮和总多酚,结果表明氯化胆碱/乙二醇组成的DES提取总黄酮量最高,氯化胆碱/草酸组成的DES提取物总多酚含量最高。目前,多数天然产物提取研究中最佳DES组成以氯化胆碱/尿素居多。同时,DES在天然产物提取应用中的辅助技术以超声波和微波为主。近年来新型萃取技术有空气辅助液相微萃取、液-液微萃取、涡旋辅助液微萃取等,与DES联用通常可获得更好的提取效果。DES在天然产物提取方面的效率超过了传统的有机溶剂,其最大的优点是稳定性高且污染较少、试剂可回收。
2.1.1 黄酮类化合物
黄酮类物质具有较高的生物利用度和良好的环境稳定性,在已知的多酚类中黄酮类化合物多达半数,是自然界中最常见的化合物之一,也是目前研究热点,主要功能活性以抗氧化为主,具体作用是自由基清除和螯合过渡金属。FENG等[21]利用超声辅助DES提取文冠果黄酮类化合物,对比甲醇和DES的提取效率,发现1,4-丁二醇/乙酸对没食子儿茶素、儿茶素和表儿茶素等的总提取率高达30.37 mg/g,提取率均明显高于甲醇溶剂。ASHRAF等[22]采用超声辅助DES优化黄酮类化合物的提取工艺,结果表明氯化胆碱/苹果酸、氯化胆碱/柠檬酸和氯化胆碱/1,4-丁二醇对黄酮类物质的提取量均大于10 mg/g,回收率最高可达92.69%,且DES均优于常规溶剂甲醇。
2.1.2 酚类化合物
酚类化合物是指由一个或多个与芳香环相连的羟基相连形成的一系列物质的总称。根据酚类化合物的分子结构差异,可以将其细分为单酚、酚酸、酚醛、多酚以及类黄酮等多种类型。酚类化合物有多种生物活性如抗菌、抗炎、抗氧化和抗肿瘤等,具有广泛应用前景[23]。DES能够有效提高多酚类物质的提取效率,为酚类化合物的深入研究奠定基础。ZANNOU等[24]采用DES来提取黑莓中花青素,以氯化胆碱为HBA,尿素、有机酸、多醇等为HBD形成的DES优化黑莓中酚类化合物的提取工艺,DES的应用为植物化学物质的研究提供了一种环保高效的方法。WANG等[25]采用超声辅助DES法绿色高效提取木瓜中5种多酚物质,得出最佳DES组成为氯化胆碱/尿素/丙二醇,各组分得率(3.92±0.03)mg/g均高于传统有机溶剂,提取得到的多酚物质具有更好的自由基清除能力。
2.1.3 多糖类
多糖是由糖苷键连接的长链单糖单元组成的高分子碳水化合物,具有广泛的生物活性如免疫调节、抗肿瘤、抗病毒、抗氧化和降血糖等。PAN等[26]利用超声辅助“氯化胆碱-草酸”提取羊肚菌多糖,在最佳条件下,羊肚菌多糖的提取率比热水提取法提高4.5倍,且羊肚菌碳水化合物(85.27%)和硫酸盐含量(34.16%)都更高,同时还发现利用DES所提取的多糖分子质量均低于热水提取法提取的多糖。FATAHI等[27]采用16种DES和4种常规溶剂对波斯甘露聚糖中的多糖和抗氧化剂进行提取,发现利用超声辅助的提取效率优于微波辅助提取法,超声辅助DES提取法与超声辅助水提取的方法比较,总糖含量提高26%,总多酚含量提高56%。详见表3。
表3 DES在天然产物中的应用
Table 3 Application of DES in natural products
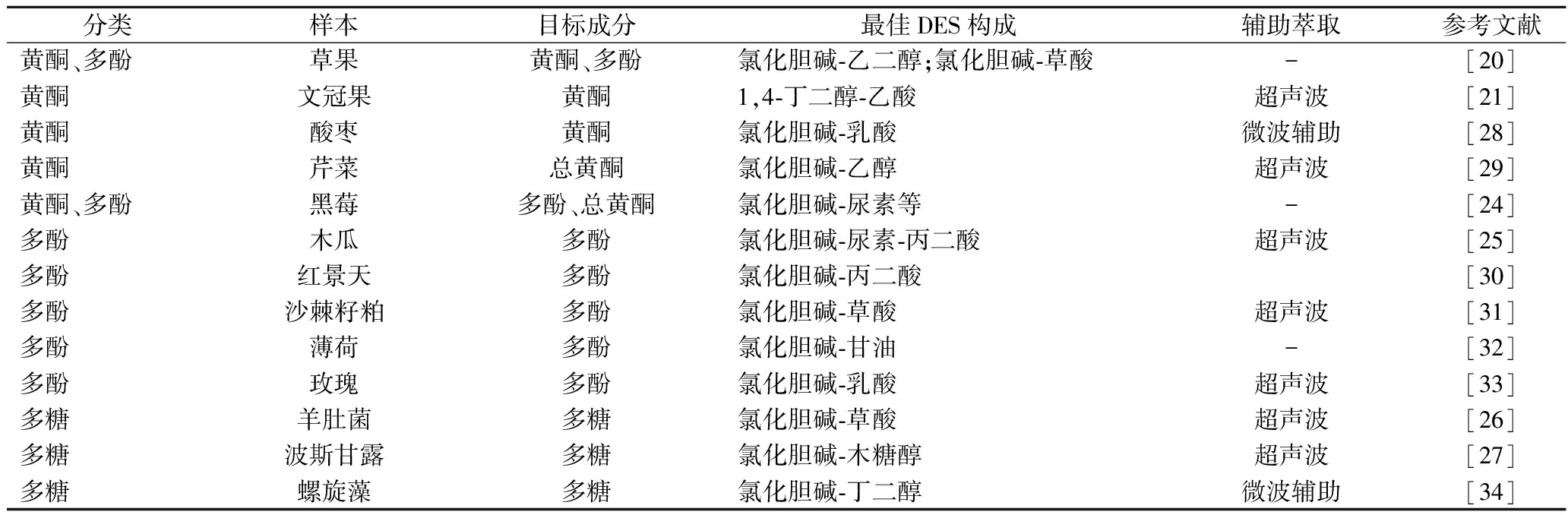
分类样本目标成分最佳DES构成辅助萃取参考文献黄酮、多酚草果黄酮、多酚氯化胆碱-乙二醇;氯化胆碱-草酸-[20]黄酮文冠果黄酮1,4-丁二醇-乙酸超声波[21]黄酮酸枣黄酮氯化胆碱-乳酸微波辅助[28]黄酮芹菜总黄酮氯化胆碱-乙醇超声波[29]黄酮、多酚黑莓多酚、总黄酮氯化胆碱-尿素等-[24]多酚木瓜多酚氯化胆碱-尿素-丙二酸超声波[25]多酚红景天多酚氯化胆碱-丙二酸[30]多酚沙棘籽粕多酚氯化胆碱-草酸超声波[31]多酚薄荷多酚氯化胆碱-甘油-[32]多酚玫瑰多酚氯化胆碱-乳酸超声波[33]多糖羊肚菌多糖氯化胆碱-草酸超声波[26]多糖波斯甘露多糖氯化胆碱-木糖醇超声波[27]多糖螺旋藻多糖氯化胆碱-丁二醇微波辅助[34]
2.2 食品检测分析
食品分析中检测色素含量的方法通常耗时耗力,而DES能够实现食品中色素的快速检测。ADIL等[35]基于甘草酸的DES超声辅助液-液微萃取来提取和富集食品样品中的溴氰菊酯,这是首次采用DES作为溴氰菊酯的提取溶剂。HAQ等[36]使用8-羟基喹啉作为锌离子的螯合剂并以胆碱氯化物和酚(1∶2)DES作为提取溶剂,提取鱼类和鳗鱼样品中的锌。检测发现锌的浓度低于检测限,证明这种方法具有高回收率、良好的精密度和低检测限的优点,适用于复杂基质如鱼和鳗鱼的真实样品分析。除色素以外,DES还能够充当萃取剂有效提高对生活用水、牛奶、饮料中的金属含量、毒素的检测效率。ÇITAK等[37]使用三己基十四烷基氯化鳞和新戊酸(1∶4)制成的DES作为萃取剂联合液相微萃取技术,实现对自来水、牛奶等液体中Cd2+的快速检测。PRADANAS-GONZ LEZ等[38]通过优化DES的组成和提取条件,实现霉菌毒素的高效提取,避免使用有机溶剂,减少对环境的污染和对人类健康的潜在危害。ELAHI等[39]建立食品样品中Ni2+和Zn2+富集测定的新方法,其中DES作为提取介质提高金属离子的富集效率,而且通过使用绿色溶剂减少了对环境的潜在影响。总之,DES能够运用于各类食品检测分析,相比与传统的化学试剂,DES具有快速高效、操作简单和环境负担小等优点。但在食品应用领域DES的运用仍然很局限,基本只停留在检测成分上,且成熟方法未能普及使用。详见表4。
LEZ等[38]通过优化DES的组成和提取条件,实现霉菌毒素的高效提取,避免使用有机溶剂,减少对环境的污染和对人类健康的潜在危害。ELAHI等[39]建立食品样品中Ni2+和Zn2+富集测定的新方法,其中DES作为提取介质提高金属离子的富集效率,而且通过使用绿色溶剂减少了对环境的潜在影响。总之,DES能够运用于各类食品检测分析,相比与传统的化学试剂,DES具有快速高效、操作简单和环境负担小等优点。但在食品应用领域DES的运用仍然很局限,基本只停留在检测成分上,且成熟方法未能普及使用。详见表4。
表4 DES在水产品及食品检测中的应用
Table 4 Application of DES in in aquatic products and food detection
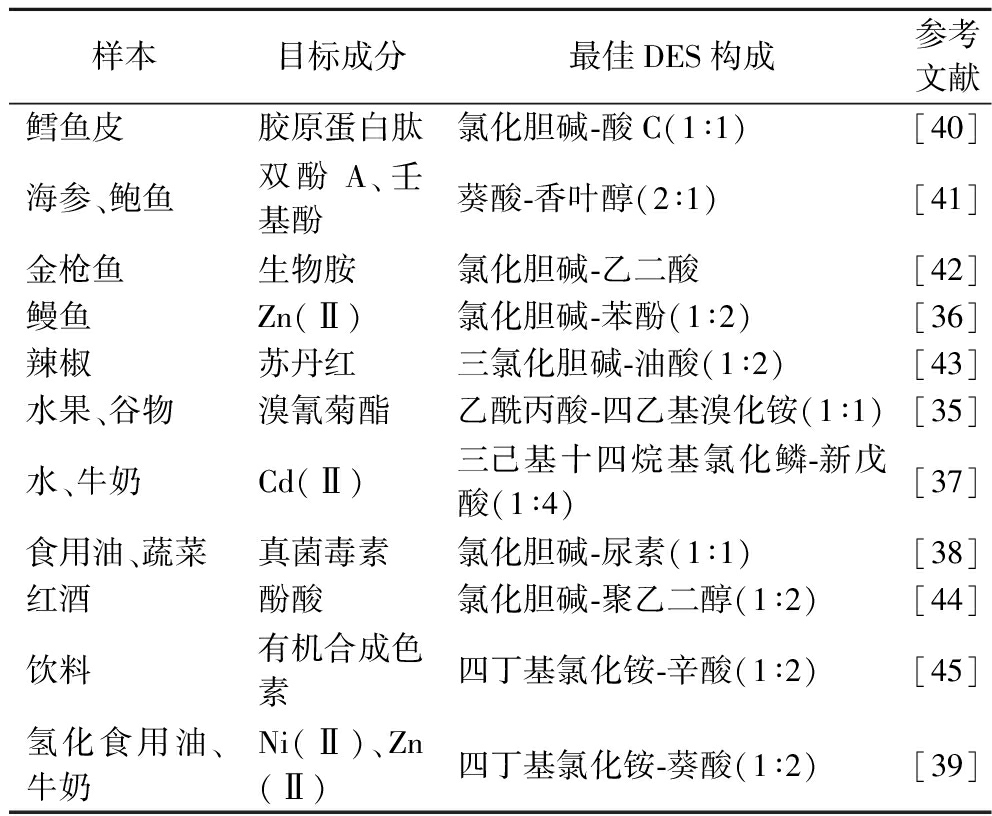
样本目标成分最佳DES构成参考文献鳕鱼皮胶原蛋白肽氯化胆碱-酸C(1∶1)[40]海参、鲍鱼双酚A、壬基酚葵酸-香叶醇(2∶1)[41]金枪鱼生物胺氯化胆碱-乙二酸[42]鳗鱼Zn(Ⅱ)氯化胆碱-苯酚(1∶2)[36]辣椒苏丹红三氯化胆碱-油酸(1∶2)[43]水果、谷物溴氰菊酯乙酰丙酸-四乙基溴化铵(1∶1)[35]水、牛奶Cd(Ⅱ)三己基十四烷基氯化鳞-新戊酸(1∶4)[37]食用油、蔬菜真菌毒素氯化胆碱-尿素(1∶1)[38]红酒酚酸氯化胆碱-聚乙二醇(1∶2)[44]饮料有机合成色素四丁基氯化铵-辛酸(1∶2)[45]氢化食用油、牛奶Ni(Ⅱ)、Zn(Ⅱ)四丁基氯化铵-葵酸(1∶2)[39]
2.3 绿色反应介质
2.3.1 木质纤维素预处理液
近年来,离子液体因其高效溶解纤维素、半纤维素、木质素的特性备受关注,成为生物质分离的新途径,但因其高成本、毒性和回收难等问题限制了其进一步发展。DES作为一种新型低毒易降解且制备成本低的溶剂,在木质纤维素预处理领域具有巨大应用潜力,有望开发出低能耗的木质纤维素加工工艺。BIAN等[46]学者的研究表明,相较于纯纤维素,通过部分去除木质素的方式,可降低木质素对纤维素解纤的阻碍作用。DES不仅可以用于生物质中木质素的分离提取,还可以利用其反应特性对纤维素进行化学改性。WANG等[47]通过使用胆碱氯化物/乳酸从纤维素微纤维中剥离出非纤维素组分,从而达到增强纤维素对纤维素酶的可及性,结果显示葡萄糖的转化率显著提高增加到90.56%。DES制备工艺简便、无毒、生物降解且易回收利用,可去除木质素,且不易溶解纤维素,对后续发酵不会产生抑制作用,在木质纤维素水解糖化上具有广阔前景。
2.3.2 酶促反应介质
在酶促催化反应中,溶剂选择是一个重要的因素,DES因其良好的生物相容性和广泛的溶解性能,被认为能够提高酶的催化活性和稳定性。DES中的氢键能够改变酶的二级结构从而提高酶的稳定性和活性,ZHOU等[48]研究DES对碳酸酐酶的影响,发现通过氢键相互作用形成的三维超分子网络增强了该酶的稳定性。HOPPE等[49]以乙酰胆碱和不同的HBD为基础制备了一系列新型DES,结果表明,DES能够提升酶的活性,可使β-半乳糖苷酶水解乳糖的产量提高3倍以上。
由于其特殊的催化特性和独特的结构,溶剂选择在对肪酶催化过程中具有重要意义。DES作为酶促反应的溶剂或共溶剂,能够显著提高反应效率,增强脂肪酶选择性,降低反应成本。NIAN等[50]发现假丝酵母脂肪酶B和氯化胆碱-甘油组成的DES具有正协同作用。CAO等[51]通过对4种不同的DES的配制,探讨对固定化脂肪酶MAS1催化甘油水解效果的影响。结果显示DES剂作为反应介质时,产物中三酰甘油的质量分数显著增加,产品更容易分离。
2.3.3 化学催化剂
DES作为化学催化剂具有成本低廉、无毒、可生物降解和可回收利用的优点,在有机合成领域中具有广阔的应用前景。聚酰亚胺(polyimide,PI)是一种在航空航天、机械、和电气等领域应用广泛的工程塑料,具有卓越的综合性能。冯树波等[52]学者使用尿素-氯化胆碱DES作为催化剂,乙酸酐作为脱水剂,在N,N-二甲基甲酰胺(N,N-dimethylformamide,DMF)中进行聚酰胺酸(polyamidic acid,PAA)的亚胺化反应。确定了最佳反应条件:温度80 ℃,DES与乙酸酐体积比1∶2,PAA与DES物质的量比1∶2,该方法具有操作简便、成本低、无毒、可生物降解等优点,且DES可循环使用。莫凡[53]使用酸性DES催化苯乙烯和甲醛水溶液进行普林斯缩合反应,合成了4-苯基-1,3-二氧杂环己烷。于亚莉[54]将松香改性为聚合松香以提高其附加值,并设计合成3类特定酸功能的DES用于催化松香聚合反应。详见表5。
表5 DES作为化学催化在有机合成中的优点
Table 5 Advantages of DES in organic synthesis

反应优点环化反应(a)增加反应速率(b)避免产物被污染(c)避免目标产物产率及结晶度并节约能量(d)产物可以通过结晶或者用乙酸乙酯从DES中分离,有利于循环利用多组分反应(a)具有很稳定的性质,因此可以使叠氮化与环加成在一起完成(b)无毒且成本低廉(c)反应无需催化剂(d)反应后处理简单,普适性好,产率高取代反应(a)降低反应温度,提高产率(b)循环利用但不会导致酶失活(c)避免了有毒溶剂与催化剂的使用(d)产物很容易从体系中分离出来酶催化反应(a)提高酶稳定性,并保持其良好催化活性和选择性(b)成本低廉,无毒性缩合反应(a)绿色环保,低毒性,高度可循环(b)底物适应性好(c)催化剂可用磁分离且生成物不溶于水,便于和溶于水的DES分离,有利于回收氧化还原反应(a)反应不需要再加酸性催化剂(b)既可以作为催化剂又可以作为萃取剂加成反应(a)降低反应温度,节约原料及能量消耗(b)提高产率(c)对环境友好(d)可重复利用
2.4 其他应用
通过DES制备的离子凝胶具备高度的导电性、透明度、黏附性和自愈合能力,即这种离子凝胶在受损后能够自行修复,恢复其原有的机械性能和导电性能,这对于提高材料的耐用性和可靠性,尤其是在柔性电子和可穿戴设备领域,具有重要的应用价值。MUKESH等[55]使用氯化胆碱和苔黑素制备的DES被用作甲基丙烯酸2-羟乙酯的聚合反应介质,制备具有良好透明度和可拉伸性的高电容凝胶。此外,黄浩铭等[56]则运用循环伏安法探究废铅膏在氯化胆碱-乙二醇(ChCl-EG)DES中的电化学行为,证实DES体系在电化学反应中可实现极低的碳排放,对二氧化碳减排及环境保护具有显著的积极影响。
3 结论与展望
DES具有类似于离子溶剂的性质,因其自身的多样性、生物降解性、低毒性和易于合成,目前对DES在不同学科交叉应用研究持续增加。基于DES的结构可设计性,可将其制备成反应底物溶剂或作为催化剂的功能溶剂;制备工艺上可简化合成步骤,减少有毒溶剂的使用,这些都是DES未来发展的趋势和热点。本文系统梳理综述DES的生化特性、及其在天然产物提取、食品检测分析和催化反应介质等方面的多功效应用。DES虽然目前展现出巨大的应用潜力和研究进展,但仍存在一些亟待解决的问题:①DES的形成机理尚未明确,需要通过更多实验方法(如核磁共振、红外光谱、X射线衍射等)来观察不同组分混合时的分子行为,以揭示DES形成过程中的分子相互作用并根据特定应用的需求,通过调整DES的组成或添加特定添加剂来优化其性能,未来将能更好地预测和设计具有特定性能的DES,为各种应用提供定制化的溶剂解决方案;②缺乏对DES理化性质系统研究,可尝试收集和整理不同DES的理化性质数据,建立一个系统化数据库,便于研究者查询和比较,并制定一套标准化的测试流程,用于评估DES的物理和化学性质,确保数据的准确性和可比性,可以促进DES的选择和优化,使其更广泛地应用于工业过程;③DES多功效应用尚需进一步拓展,可以探索DES在不同领域的潜在应用,如药物传递、食品加工、化妆品、环境保护等还可以通过实际案例研究展示DES在特定应用中的效果;④DES各组分间及其体系中分子间相互作用力尚不清楚。利用先进仪器表征技术(如拉曼光谱、红外光谱、差示扫描量热法和等温滴定量热分析)并结合分子动力学模拟来评估DES中分子间相互作用,以预测和佐证实验研究现象,将有助于开发新型DES体系。
[1] MOURA L, MOUFAWAD T, FERREIRA M, et al.Deep eutectic solvents as green absorbents of volatile organic pollutants[J].Environmental Chemistry Letters, 2017, 15(4):747-753.
[2] DAI Y T, WITKAMP G J, VERPOORTE R, et al.Natural deep eutectic solvents as a new extraction media for phenolic metabolites in Carthamus tinctorius L[J].Analytical Chemistry, 2013, 85(13):6272-6278.
[3] 刘艳霞, 胡建华, 李永丽, 等.低共熔溶剂的研究进展[J].现代化工, 2022, 42(10):51-55.LIU Y X, HU J H, LI Y L, et al.Research progress on deep eutectic solvents[J].Modern Chemical Industry, 2022, 42(10):51-55.
[4] SIRVIÖ J A, HAATAJA R, KANTOLA A M, et al.Insights into the role of molar ratio and added water in the properties of choline chloride and urea-based eutectic mixtures and their cellulose swelling capacity[J].Physical Chemistry Chemical Physics, 2022, 24(46):28609-28620.
[5] CEA-KLAPP E, GAJARDO-PARRA N, ARAVENA P, et al.Interfacial properties of deep eutectic solvents by density gradient theory[J].Industrial &Engineering Chemistry Research, 2022, 61(6):2580-2591.
[6] KHOKHAR V, DHINGRA D, PANDEY S.Effect of temperature and composition on density and dynamic viscosity of (lanthanide metal salts + urea) deep eutectic solvents[J].Journal of Molecular Liquids, 2022, 360:119396.
[7] QU Q, LYU Y Y, LIU L L, et al.Synthesis and characterization of deep eutectic solvents (five hydrophilic and three hydrophobic), and hydrophobic application for microextraction of environmental water samples[J].Analytical and Bioanalytical Chemistry, 2019, 411(28):7489-7498.
[8] LIN H Q, GONG K, HYKYS P, et al.Nanoconfined deep eutectic solvent in laminated MXene for efficient CO2 separation[J].Chemical Engineering Journal, 2021, 405:126961.
[9] LIU Y, FRIESEN J B, MCALPINE J B, et al.Natural deep eutectic solvents:Properties, applications, and perspectives[J].Journal of Natural Products, 2018, 81(3):679-690
[10] KURTULBA E, PEKEL A G, BILGIN M, et al.Citric acid-based deep eutectic solvent for the anthocyanin recovery from Hibiscus sabdariffa through microwave-assisted extraction[J].Biomass Conversion and Biorefinery, 2022, 12(2):351-360.
E, PEKEL A G, BILGIN M, et al.Citric acid-based deep eutectic solvent for the anthocyanin recovery from Hibiscus sabdariffa through microwave-assisted extraction[J].Biomass Conversion and Biorefinery, 2022, 12(2):351-360.
[11] GOMEZ F J V, ESPINO M, FERN NDEZ M A, et al.A greener approach to prepare natural deep eutectic solvents[J].ChemistrySelect, 2018, 3(22):6122-6125.
NDEZ M A, et al.A greener approach to prepare natural deep eutectic solvents[J].ChemistrySelect, 2018, 3(22):6122-6125.
[12] EL ACHKAR T, FOURMENTIN S, GREIGE-GERGES H.Deep eutectic solvents:An overview on their interactions with water and biochemical compounds[J].Journal of Molecular Liquids, 2019, 288:111028.
[13] LI N, CHANG Z D, ZHAN Y F, et al.Growth of cubic anhydrous magnesium carbonate single crystal in deep eutectic solvent[J].Journal of Solid State Chemistry, 2020, 292:121684.
[14] WANG X S, WU Y F, LI J, et al.Ultrasound-assisted deep eutectic solvent extraction of echinacoside and oleuropein from Syringa pubescens Turcz[J].Industrial Crops and Products, 2020, 151:112442.
[15] NAM M W, ZHAO J, LEE M S, et al.Enhanced extraction of bioactive natural products using tailor-made deep eutectic solvents:Application to flavonoid extraction from Flos sophorae[J].Green Chemistry, 2015, 17(3):1718-1727.
[16] TARIKUZZAMAN M, SAGAR V, WONG M J, et al. Temperature effects on physiochemical characteristics of sugar-based natural deep eutectic solvents[J]. Advances in Materials Science and Engineering, 2024, 2024(1):6641317.
[17] 王岩, 蔡文生, 邵学广. 近红外光谱用于低共熔溶剂中水结构的分析 [J]. 高等学校化学学报, 20, 44(6): 39-44.WANG Y, CAI W S, SHAO X G. Near-infrared spectroscopy for the analysis of water structure in low eutectic solvents [J]. Journal of Higher Education Chemistry, 20, 44(6): 39-44.
[18] ARAVENA P, CEA-KLAPP E, GAJARDO-PARRA N F, et al. Effect of water and hydrogen bond acceptor on the density and viscosity of glycol-based eutectic solvents[J]. Journal of Molecular Liquids, 2023, 389:122856.
[19] ALSHAMMARI O A O, ALMULGABSAGHER G A A, RYDER K S, et al. Effect of solute polarity on extraction efficiency using deep eutectic solvents[J]. Green Chemistry, 2021, 23(14):5097-5105.
[20] 师聪, 陈学红, 解春芝, 等.草果不同低共熔溶剂提取物活性成分与其抗氧化活性的相关性分析[J].中国食品添加剂, 2022, 33(6):24-29.SHI C, CHEN X H, XIE C Z, et al.Analysis of the active components in Amomum tsaoko with different low-eutectic solvent and their correlation with antioxidant activity[J].China Food Additives, 2022, 33(6):24-29.
[21] FENG Z A, YANG D, GUO J J, et al.Optimization of natural deep eutectic solvents extraction of flavonoids from Xanthoceras sorbifolia Bunge by response surface methodology[J].Sustainable Chemistry and Pharmacy, 2023, 31:100904.
[22] ASHRAF W, REHMAN A, HUSSAIN A, et al.Optimization of extraction process and estimation of flavonoids from fenugreek using green extracting deep eutectic solvents coupled with ultrasonication[J].Food and Bioprocess Technology, 2024, 17(4):887-903.
[23] 张雪, 刘娅, 刘秀敏, 等.超声辅助低共熔溶剂提取新疆红枣中环磷酸腺苷的工艺优化[J].食品工业科技, 2022, 43(14):243-250.ZHANG X, LIU Y, LIU X M, et al.Optimization of ultrasound-assisted extraction of cyclic adenosine 3′, 5′-monophosphate from Xinjiang jujube by deep eutectic solvent[J].Science and Technology of Food Industry, 2022, 43(14):243-250.
[24] ZANNOU O, KOCA I.Greener extraction of anthocyanins and antioxidant activity from blackberry (Rubus spp) using natural deep eutectic solvents[J].LWT, 2022, 158:113184.
[25] WANG W T, AN M, ZHAO G J, et al.Ultrasonic-assisted customized natural deep eutectic solvents extraction of polyphenols from Chaenomeles speciosa[J].Microchemical Journal, 2023, 193:108952.
[26] PAN X, XU L J, MENG J L, et al.Ultrasound-assisted deep eutectic solvents extraction of polysaccharides from Morchella importuna:Optimization, physicochemical properties, and bioactivities[J].Frontiers in Nutrition, 2022, 9:912014.
[27] FATAHI F, TABARAKI R.Deep eutectic solvent mediated extraction of polysaccharides and antioxidants from Persian Manna (taranjabin):Comparison of different extraction methods and optimization by response surface methodology[J].Microchemical Journal, 2023, 194:109336.
[28] DU G, HONG W, LI Z, et al.Process optimization of deep eutectic solvent-based microwave-assisted extraction of flavonoids from Ziziphi Spinosae Semen using response surface methodology[J].Food Science and Technology, 2023, 43:e122622.
[29] 刘琴, 周游, 陈轩, 等.超声辅助低共熔溶剂提取芹菜叶中的芹菜素及其抗氧化性分析[J].现代食品科技, 2021, 37(3):202-211;201.LIU Q, ZHOU Y, CHEN X, et al.Optimization of ultrasonic assisted deep eutectic solvents extraction process and antioxidant activity of apigenin from celery leaves[J].Modern Food Science and Technology, 2021, 37(3):202-211;201.
[30] NIKITA T, OKSANA P, NADEZHDA F, et al. Application of natural deep eutectic solvents for extraction of bioactive components from Rhodiola rosea (L.) [J]. Molecules, 20, 28(2): 91.
[31] 倪玉娇, 赵春建, 李春英, 等.超声辅助低共熔溶剂提取沙棘籽粕多酚的工艺优化[J].植物研究, 2017, 37(3):474-480.NI Y J, ZHAO C J, LI C Y, et al.Process optimization of ultrasonic assisted deep eutectic solvents(DESs) extraction of polyphenols from Hippophae rhamnoides seed meal[J].Bulletin of Botanical Research, 2017, 37(3):474-480.
[32] ATHANASIADIS V, PALAIOGIANNIS D, GRIGORAKIS S, et al.Food-grade deep eutectic solvent extraction of antioxidant polyphenols from peppermint (Mentha × piperita L.):Screening, optimization and metabolite profile[J].Journal of Applied Research on Medicinal and Aromatic Plants, 2023, 33:100456.
[33] 王晓艺, 李培坤, 李锦红, 等.超声辅助低共熔溶剂提取玫瑰多酚及其抗氧化活性[J].食品研究与开发, 2022, 43(8):98-105.WANG X Y, LI P K, LI J H, et al.Ultrasonic-assisted extraction of rose polyphenols by deep eutectic solvent and antioxidant activity[J].Food Research and Development, 2022, 43(8):98-105.
[34] 罗光宏, 王海蓉, 崔晶, 等.微波辅助低共熔溶剂提取、部分纯化螺旋藻多糖及其体外生物学活性研究[J].食品与发酵工业, 2022, 48(11):107-113.LUO G H, WANG H R, CUI J, et al.Microwave-assisted deep eutectic solvents extraction, partial purification and in vitro biological activity of polysaccharides from Spirulina platensis[J].Food and Fermentation Industries, 2022, 48(11):107-113.
[35] ELIK A, DURUKAN H, SARAC H, et al.Application of levulinic acid-based natural deep eutectic solvents for extraction and determination of deltamethrin in food samples[J].Sustainable Chemistry and Pharmacy, 2022, 30:100861.
[36] HAQ H U, BALAL M, CASTRO-MU OZ R, et al.Deep eutectic solvents based assay for extraction and determination of zinc in fish and eel samples using FAAS[J].Journal of Molecular Liquids, 2021, 333:115930.
OZ R, et al.Deep eutectic solvents based assay for extraction and determination of zinc in fish and eel samples using FAAS[J].Journal of Molecular Liquids, 2021, 333:115930.
[37] ÇITAK D, SABANC D.Response surface methodology and hydrophobic deep eutectic solvent based liquid phase microextraction combination for determination of cadmium in food and water samples[J].Journal of Food Measurement and Characterization, 2021, 15(2):1843-1850.
D.Response surface methodology and hydrophobic deep eutectic solvent based liquid phase microextraction combination for determination of cadmium in food and water samples[J].Journal of Food Measurement and Characterization, 2021, 15(2):1843-1850.
[38] PRADANAS-GONZ LEZ F, ARAGONESES-CAZORLA R, MERINO-SIERRA M
LEZ F, ARAGONESES-CAZORLA R, MERINO-SIERRA M  , et al.Extracting mycotoxins from edible vegetable oils by using green, ecofriendly deep eutectic solvents[J].Food Chemistry, 2023, 429:136846.
, et al.Extracting mycotoxins from edible vegetable oils by using green, ecofriendly deep eutectic solvents[J].Food Chemistry, 2023, 429:136846.
[39] ELAHI F, ARAIN M B, KHAN W A, et al.Ultrasound-assisted deep eutectic solvent-based liquid-iquid microextraction for simultaneous determination of Ni (II) and Zn (II) in food samples[J].Food Chemistry, 2022, 393:133384.
[40] 白晨洁. 低共熔溶剂(DESs)中鳕鱼皮胶原蛋白肽的分离纯化研究[D].哈尔滨:哈尔滨工业大学, 2017.BAI C J.Separation and Purification of Collagen Peptides from Cod Skin in deep eutectic solvents (DESs)[D].Harbin:Harbin Institute of Technology, 2017.
[41] 薛皓月, 刘海龙, 贾丽艳, 等.低共熔溶剂分散液液微萃取-悬浮固化-高效液相色谱法测定水产品中3种内分泌干扰物的含量[J].理化检验-化学分册, 2022, 58(3):279-284.XUE H Y, LIU H L, JIA L Y, et al.Determination of 3 endocrine disrupting chemicals in fishery products by HPLC with deep eutectic solvents dispersive liquid liquid microextraction-solidification of floating droplets[J].Physical Testing and Chemical Analysis (Part B (Chemical Analysis)), 2022, 58(3):279-284.
[42] NEMATI M, ALI FARAJZADEH M, MOHEBBI A, et al.Simultaneous application of deep eutectic solvent as extraction solvent and ion-pair agent in liquid phase microextraction for the extraction of biogenic amines from tuna fish samples[J].Microchemical Journal, 2020, 159:105496.
[43] ZHANG K G, LIU C, LI S Y, et al.Vortex-assisted liquid-liquid microextraction based on a hydrophobic deep eutectic solvent for the highly efficient determination of Sudan I in food samples[J].Analytical Letters, 2020, 53(8):1204-1217.
[44] 李亚茹. 可调性低共熔溶剂在食品和水样分析中的应用[D].保定:河北大学, 2021.LI Y R.Application of adjustable deep eutectic solvents in food and water sample analysis[D].Baoding:Hebei University, 2021.
[45] 周佳, 禹洁, 朱书强, 等.饮料及配制酒中11种有机合成色素的低共熔溶剂萃取/高效液相色谱法测定[J].分析测试学报, 2019, 38(11):1358-1363.ZHOU J, YU J, ZHU S Q, et al.Determination of 11 organic synthetic pigments in drink and compound wine by deep eutectic solvent extraction/high performance liquid chromatography[J].Journal of Instrumental Analysis, 2019, 38(11):1358-1363.
[46] BIAN H Y, GAO Y, YANG Y Q, et al.Improving cellulose nanofibrillation of waste wheat straw using the combined methods of prewashing, p-toluenesulfonic acid hydrolysis, disk grinding, and endoglucanase post-treatment[J].Bioresource Technology, 2018, 256:321-327.
[47] WANG G M, HUANG M J, LI F C, et al.Insights into the poplar cell wall deconstruction following deep eutectic solvent pretreatment for enhanced enzymatic saccharification and lignin valorization[J].International Journal of Biological Macromolecules, 2024, 254:127673.
[48] ZHOU Y, WU Y J, WANG L, et al.Natural deep eutectic solvents as green and biocompatible reaction medium for carbonic anhydrase catalysis[J].International Journal of Biological Macromolecules, 2021, 190:206-213.
[49] HOPPE J, BYZIA E, SZYMA SKA M, et al.Acceleration of lactose hydrolysis using beta-galactosidase and deep eutectic solvents[J].Food Chemistry, 2022, 384:132498.
SKA M, et al.Acceleration of lactose hydrolysis using beta-galactosidase and deep eutectic solvents[J].Food Chemistry, 2022, 384:132498.
[50] NIAN B B, CAO C, LIU Y F.Synergistic catalytic synthesis of gemini lipoamino acids based on multiple hydrogen-bonding interactions in natural deep eutectic solvents-enzyme system[J].Journal of Agricultural and Food Chemistry, 2020, 68(4):989-997.
[51] WANG X M, ZHAO X X, QIN X L, et al. Immobilized MAS1 lipase-catalyzed synthesis of n-3 PUFA-rich triacylglycerols in deep eutectic solvents[J]. Journal of Oleo Science, 2021, 70(2):227-236.
[52] 冯树波, 杨帅, 杨依依, 等.尿素-氯化胆碱低共熔溶剂催化聚酰胺酸亚胺化[J].精细化工, 2022, 39(4):741-745;782.FENG S B, YANG S, YANG Y Y, et al.Imidization of polyamide acid catalyzed by urea-choline chloride deep-eutectic solvent[J].Fine Chemicals, 2022, 39(4):741-745;782.
[53] 莫凡. 基于酸性低共熔溶剂[Im:2PTSA]的苯乙烯和甲醛普林斯缩合反应性能[D].上海:华东理工大学, 2020.MO F.Performance of prince condensation of styrene and formaldehyde based on acid deep eutectic solvents[im:2PTSA][D].Shanghai:East China University of Science and Technology, 2020.
[54] 于亚莉. 酸性低共熔溶剂催化松香聚合反应研究[D].青岛:青岛科技大学, 2022.YU Y L.Study on Polymerization of rosin catalyzed by acid deep eutectic solvents[D].Qingdao:Qingdao University of Science &Technology, 2022.
[55] MUKESH C, UPADHYAY K K, DEVKAR R V, et al.Preparation of a noncytotoxic hemocompatible ion gel by self-polymerization of HEMA in a green deep eutectic solvent[J].Macromolecular Chemistry and Physics, 2016, 217(17):1899-1906.
[56] 黄皓铭, 汝娟坚, 华一新, 等.氯化胆碱—乙二醇低共熔溶剂中高效电解回收废铅膏制备铅粉[J].过程工程学报, 2023, 23(1):107-114.HUANG H M, RU J J, HUA Y X, et al.Recycling of scrap lead paste to prepare lead powder by high efficiency electrolysis in choline chloride-ethylene glycol deep eutectic solvent[J].The Chinese Journal of Process Engineering, 2023, 23(1):107-114.