人参(Panaxginseng C.A.Meyer)作为我国药食同源资源的一种,为五加科人参属植物,主要产于东北地区,具有广泛的药理和生物活性[1]。人参皂苷是人参的主要活性成分,约占人参的4%,根据TLC板上斑点的Rf值顺序可从下到上分别命名为R0、Ra1、Ra2、Rb1、Rb2、Rb3、Rc、Rd、Re、Rf、Rg1、Rg2、Rg3、Rh1、Rh2、CK等[2-3]。人参皂苷属于三萜类糖苷化合物,可分为达玛烷型、齐墩果烷型以及奥克梯隆醇,其中达玛烷型人参皂苷进一步分为原人参二醇(protopanaxadiol,PPD)型皂苷和原人参三醇(protopanaxatriol,PPT)型皂苷。PPD 型(Rb1、Rb2、Rc、Rd、Rg3、Rh2、Rh3等)人参皂苷的糖基位于达玛烷的 C-3 和 C-20 位,PPT(Rg1、Re、Rf、Rg2、Rh1)型人参皂苷的糖基位于C-6位 和C-20 位,其结构不同,性质和活性也不同[2]。研究表明,人参皂苷真正的功效成分是在肠道内的代谢产物,其中糖基的数量是生物活性的关键。人参皂苷进入胃肠道后,在体内逐步脱糖基水解进而被人体吸收利用,因此可推断人参皂苷中糖基的数量越少越容易被人体吸收利用。
稀有人参皂苷(CK、Rg3、F2、Rh2等)是通过特定的糖苷酶水解人参皂苷的糖基后产生的衍生物,以达玛烷型皂苷为主,与原人参皂苷的母核结构相同,仅仅只是糖基的数量与组成有差别, C-3 位、C-6 位和 C-20 位上所连糖基小于等于3 个,且单个位置所连糖基小于等于 2 个[4]。但稀有皂苷在原人参中含量稀少甚至不存在,因此可通过修饰人参皂苷的C-3位和C-20位的糖基来制备生物活性更高的稀有人参皂苷。人参皂苷CK(亦称M1)[5]属达玛烷型,原名为20(S)原人参二醇-20-O-β-D- 吡喃葡萄糖苷,是PPD型人参皂苷在人体肠道内的主要代谢产物,比原人参皂苷具有更高的生物活性与生物利用度。该文就国内外人参皂苷CK的生物转化研究进展,探索适合大规模生产人参皂苷CK的方法,综述其生物活性,为人参皂苷CK的工业化制备及在食品、医药等领域的应用提供借鉴。
1 人参皂苷CK的化学结构
人参皂苷由疏水性糖苷配位基团与1~4个亲水性糖苷基团结合而成[6],人参皂苷CK为四环达玛烷型三萜皂苷,在C-20上只有一个糖苷键,因此更利于被人体吸收利用[7]。人参皂苷CK的分子质量为622.88,分子式为C36H62O8[8],结构式如图1所示。与其他皂苷相比,人参皂苷CK分子质量较低,有较高的渗透性,在人体内的生物利用度更高[9]。
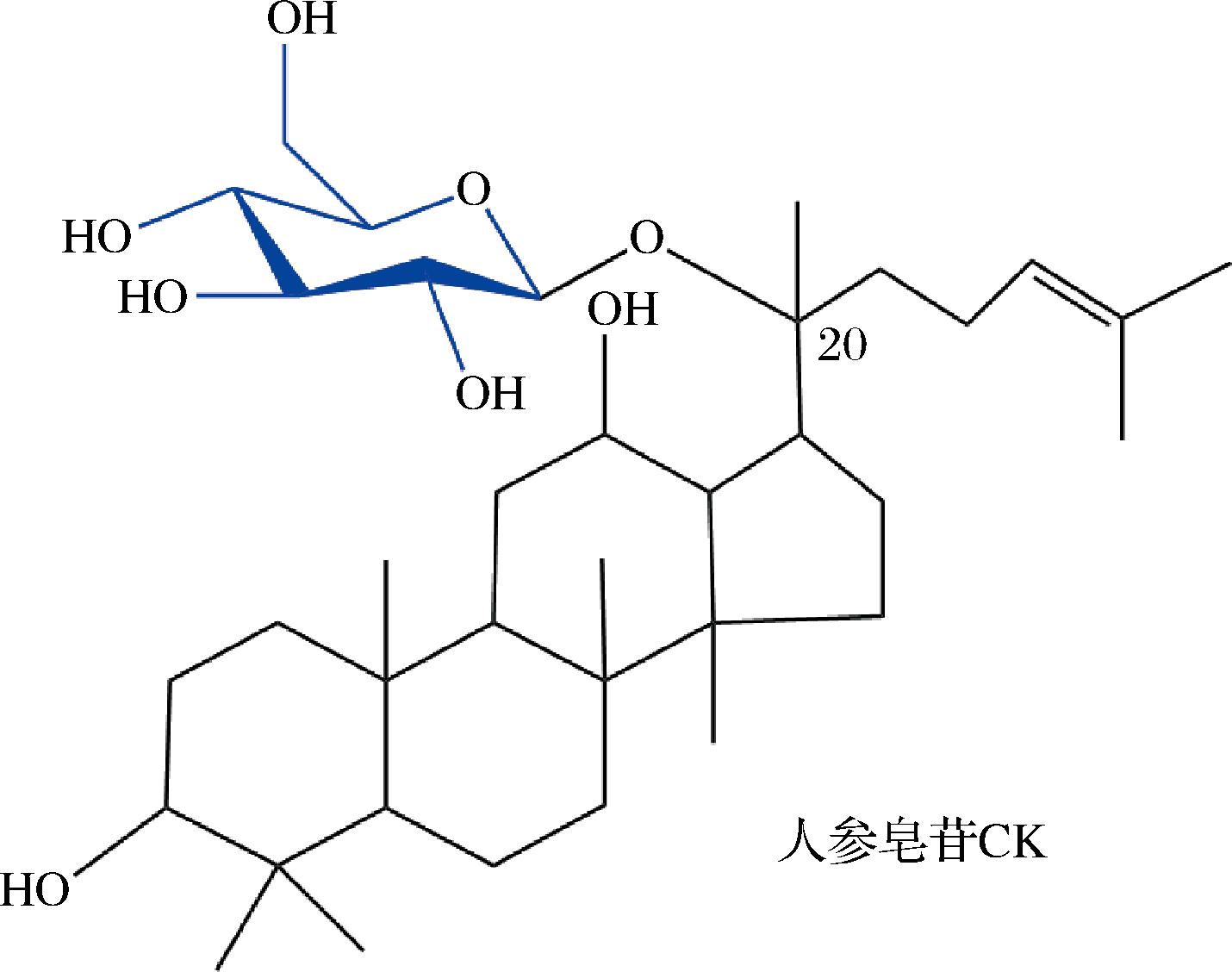
图1 人参皂苷CK的化学结构式
Fig.1 Chemical structure of the ginsenoside CK
2 人参皂苷CK的制备
人参皂苷CK由于其结构特性比原人参皂苷具有更高的药用价值,但在人参中仅占极小部分甚至不存在,无法满足其在食品、医疗、科研等领域的需求,因此通过人参皂苷高效率、规模化制备人参皂苷CK具有很大的实用价值。以下分别从化学法及生物转化法总结人参皂苷CK的制备过程,分别介绍每一种方法的利弊,总结适合高效率、大规模生产的制备方法,以期为人参皂苷CK的工业化生产及应用提供制备思路。
2.1 化学法
化学法主要利用酸水解糖苷键、氧化加成和乙酰化等反应改变取代基[10],可能导致C-20位置的糖苷键发生非特异性裂解,引发一系列副反应,如差向异构、水合和羟基化等[11]。许凌巧等[12]利用醋酸水解人参茎叶总皂苷提取物制备人参皂苷CK,在底物加入量为0.5 g、酸体积分数0.8%、温度110 ℃的条件下,人参皂苷CK的含量从0.4%提高到6.09%,该方法简便且快速。但总的来说,化学水解会产生物质残留、环境污染、条件复杂、副反应产物多、对人身体健康产生威胁等问题[13-14],不适宜在食品行业的应用,因此用化学法大规模制备人参皂苷CK较为困难。
2.2 生物转化法
生物转化法包括肠道菌群水解、微生物发酵以及酶转化,其本质是通过β-葡萄糖苷酶的作用水解糖苷键将原人参皂苷转化为人参皂苷CK。生物转化保留了糖苷键的构型、糖苷配基的结构以及关键的次级糖苷或寡糖[15],该方法较化学方法条件更温和,主要反应类型为糖基水解反应[2]。
2.2.1 肠道菌群转化
虽然有学者研究表明大鼠胃中有少量的Rg3、Rh2、F2、CK、PPD等,但人参皂苷在人体内的主要代谢场所为肠道而不是胃和肝脏,在肠道内的代谢由微生物介导。人体肠道内有大量微生物,与人体共生微生物大部分由细菌菌群组成,超过1 000种,总质量约1.5 kg[16]。肠道细菌在生长繁殖过程中产生糖苷酶[17],大部分药物的有效成分可被肠道内的菌群产生的糖苷酶分解,产生分子极性更低、药理活性更高的代谢产物,进而透过肠壁进入血液循环被人体吸收利用,发挥其药效作用,较小部分原成分直接被肠道吸收[18]。研究表明,大分子质量人参皂苷(如Rb1)在肠道菌群的作用下首先水解一分子C-20羟基末端的葡萄糖,产生中间代谢产物Rd,进而水解一分子C-3位的葡萄糖,产生F2,继续水解C-3位的一分子葡萄糖,最终生成小分子质量人参皂苷CK。
BAU等[19]研究发现肠道内的乳酸菌可将人参皂苷转化为人参皂苷CK,并成功分离该菌种。乳酸菌参与人参皂苷在肠道内的代谢途径如图2所示,其中清酒乳杆菌、植物乳杆菌和长双歧杆菌参与Rb1→Rd代谢,短乳杆菌参与Rd→F2→CK代谢[20]。因此可表明原人参皂苷能通过肠道内的菌群进行分解代谢,转化为生物活性更高的人参皂苷CK。但由于个体不同,肠道内微生物具有明显的差异性,转化效率也各不相同,因此在体外对原人参皂苷脱糖基可实现其药理作用的高效发挥以及人参皂苷CK的批量制备[21]。
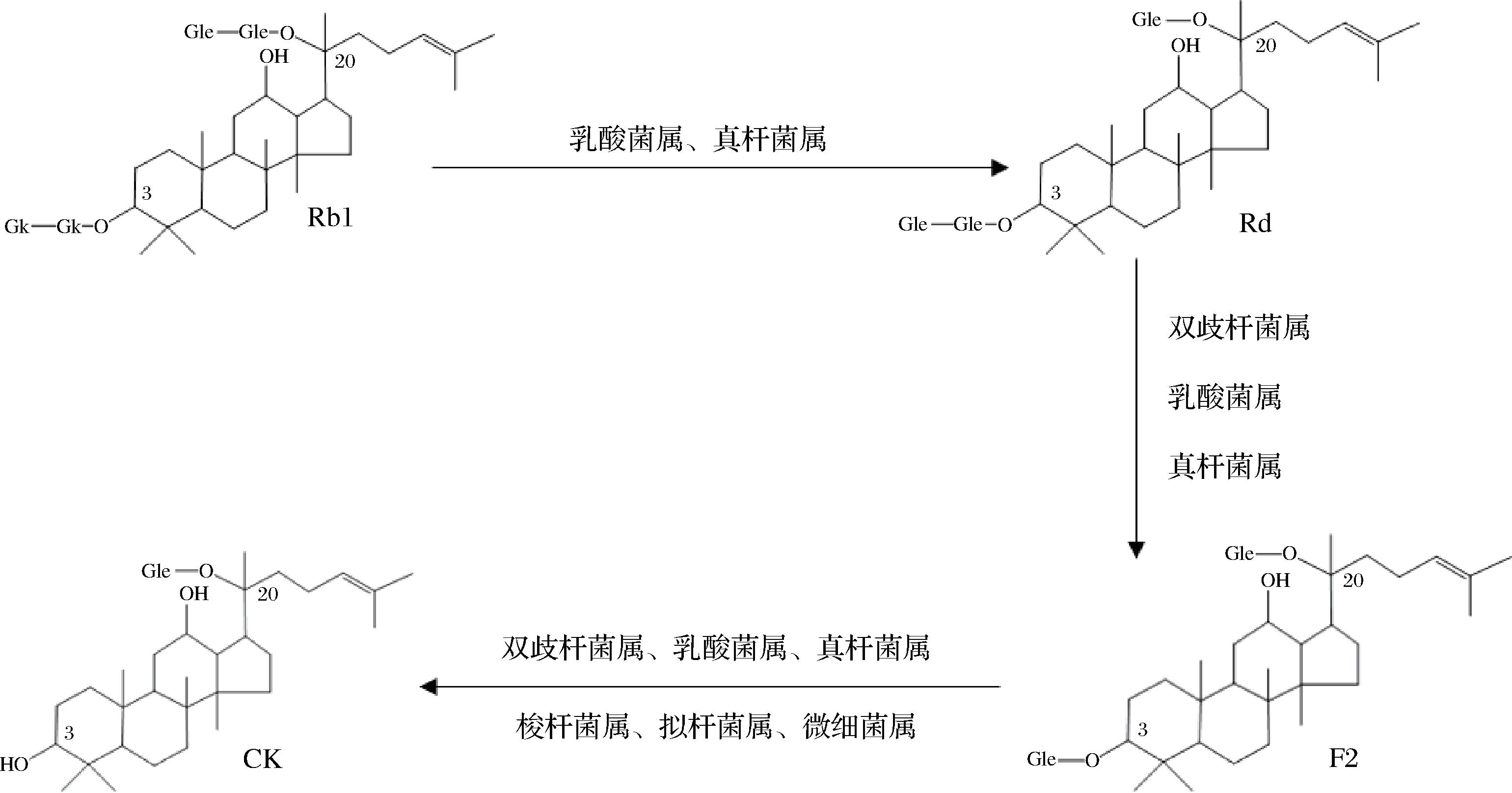
图2 人参皂苷Rb1在肠道菌群作用下转化人参皂苷CK的代谢过程
Fig.2 Metabolism of ginsenoside Rb1 into ginsenoside CK in the presence of intestinal flora
2.2.2 微生物发酵
微生物发酵是指用微生物产生的酶水解人参皂苷的糖苷键,进而转化为更易被人体吸收、生物活性更高的稀有人参皂苷。微生物在代谢过程中产生的β-葡萄糖苷酶的酶活性是决定稀有皂苷含量的主要原因。与其他方法相比,微生物发酵成本低、条件温和、利于观察培养、特异性强、安全环保、适合规模化生产[22]。除此之外,微生物还可将此过程中产生的糖类作为碳源,为其转化提供能量。相比于肠道菌群水解,微生物发酵能够在体外将人参皂苷转化为相应的活性成分,提高生物利用率,表现出显著优势[23]。人参皂苷的微生物发酵转化经历了以下3个阶段:混合菌群模拟人体转化、单一已知产酶菌种转化和筛选菌种转化。其中菌种包括土壤微生物、食品级微生物、植物内生菌等。由于人参皂苷CK在功能性食品和医药领域应用广泛,因此越来越多的研究者倾向寻找可食用菌进行转化。现将国内外对微生物制备人参皂苷CK的菌种、反应条件及转化过程进行总结,以期为规模化生产人参皂苷CK提供借鉴(表1)。
表1 人参皂苷CK的微生物发酵总结
Table 1 Summary of microbial fermentation of ginsenoside CK
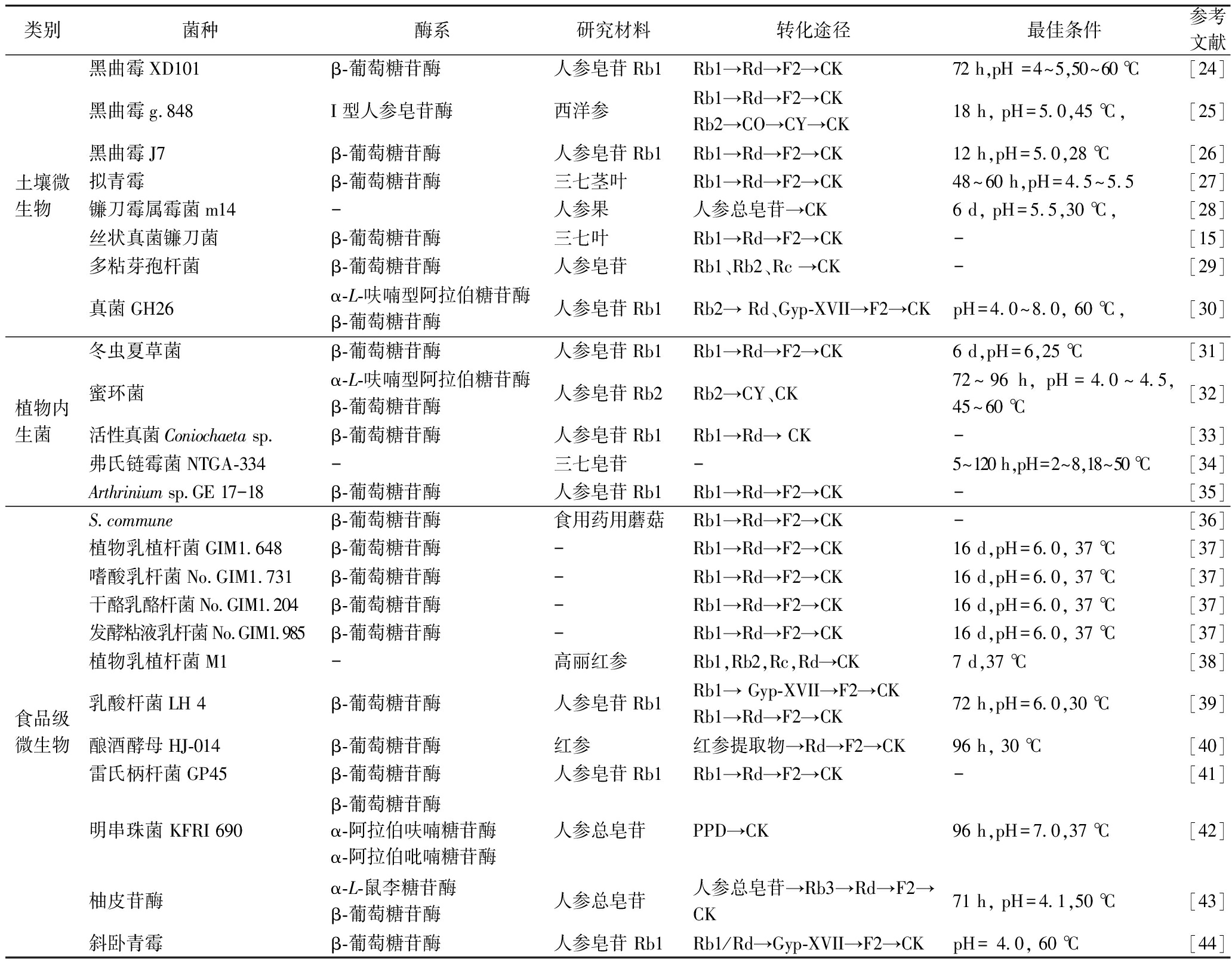
类别菌种酶系研究材料转化途径最佳条件参考文献土壤微生物黑曲霉XD101β-葡萄糖苷酶人参皂苷Rb1Rb1→Rd→F2→CK72 h,pH =4~5,50~60 ℃[24]黑曲霉g.848I型人参皂苷酶西洋参Rb1→Rd→F2→CKRb2→CO→CY→CK18 h, pH=5.0,45 ℃,[25]黑曲霉J7β-葡萄糖苷酶人参皂苷Rb1Rb1→Rd→F2→CK12 h,pH=5.0,28 ℃[26]拟青霉β-葡萄糖苷酶三七茎叶Rb1→Rd→F2→CK48~60 h,pH=4.5~5.5[27]镰刀霉属霉菌m14-人参果人参总皂苷→CK6 d, pH=5.5,30 ℃,[28]丝状真菌镰刀菌β-葡萄糖苷酶三七叶Rb1→Rd→F2→CK-[15]多粘芽孢杆菌β-葡萄糖苷酶人参皂苷Rb1、Rb2、Rc →CK-[29]真菌GH26α-L-呋喃型阿拉伯糖苷酶β-葡萄糖苷酶人参皂苷Rb1Rb2→ Rd、Gyp-XVII→F2→CKpH=4.0~8.0, 60 ℃,[30]植物内生菌冬虫夏草菌β-葡萄糖苷酶人参皂苷Rb1Rb1→Rd→F2→CK6 d,pH=6,25 ℃[31]蜜环菌α-L-呋喃型阿拉伯糖苷酶β-葡萄糖苷酶人参皂苷Rb2Rb2→CY、CK72~96 h, pH=4.0~4.5,45~60 ℃[32]活性真菌Coniochaeta sp.β-葡萄糖苷酶人参皂苷Rb1Rb1→Rd→ CK-[33]弗氏链霉菌NTGA-334-三七皂苷-5~120 h,pH=2~8,18~50 ℃[34]Arthrinium sp.GE 17-18β-葡萄糖苷酶人参皂苷Rb1Rb1→Rd→F2→CK-[35]食品级微生物S.communeβ-葡萄糖苷酶食用药用蘑菇Rb1→Rd→F2→CK-[36]植物乳植杆菌GIM1.648β-葡萄糖苷酶-Rb1→Rd→F2→CK16 d,pH=6.0, 37 ℃[37]嗜酸乳杆菌No.GIM1.731β-葡萄糖苷酶-Rb1→Rd→F2→CK16 d,pH=6.0, 37 ℃[37]干酪乳酪杆菌No.GIM1.204β-葡萄糖苷酶-Rb1→Rd→F2→CK16 d,pH=6.0, 37 ℃[37]发酵粘液乳杆菌No.GIM1.985β-葡萄糖苷酶-Rb1→Rd→F2→CK16 d,pH=6.0, 37 ℃[37]植物乳植杆菌M1-高丽红参Rb1,Rb2,Rc,Rd→CK7 d,37 ℃[38]乳酸杆菌LH 4β-葡萄糖苷酶人参皂苷Rb1Rb1→ Gyp-XVII→F2→CKRb1→Rd→F2→CK72 h,pH=6.0,30 ℃[39]酿酒酵母HJ-014β-葡萄糖苷酶红参红参提取物→Rd→F2→CK96 h, 30 ℃[40]雷氏柄杆菌GP45β-葡萄糖苷酶人参皂苷Rb1Rb1→Rd→F2→CK-[41]明串珠菌 KFRI 690β-葡萄糖苷酶α-阿拉伯呋喃糖苷酶α-阿拉伯吡喃糖苷酶人参总皂苷PPD→CK96 h,pH=7.0,37 ℃[42]柚皮苷酶α-L-鼠李糖苷酶β-葡萄糖苷酶人参总皂苷人参总皂苷→Rb3→Rd→F2→CK71 h, pH=4.1,50 ℃[43]斜卧青霉β-葡萄糖苷酶人参皂苷 Rb1Rb1/Rd→Gyp-XVII→F2→CKpH= 4.0, 60 ℃[44]
表2 重组酶及固定化酶制备CK的方法总结
Table 2 Summary of recombinant enzymes and immobilized enzymes for CK preparation
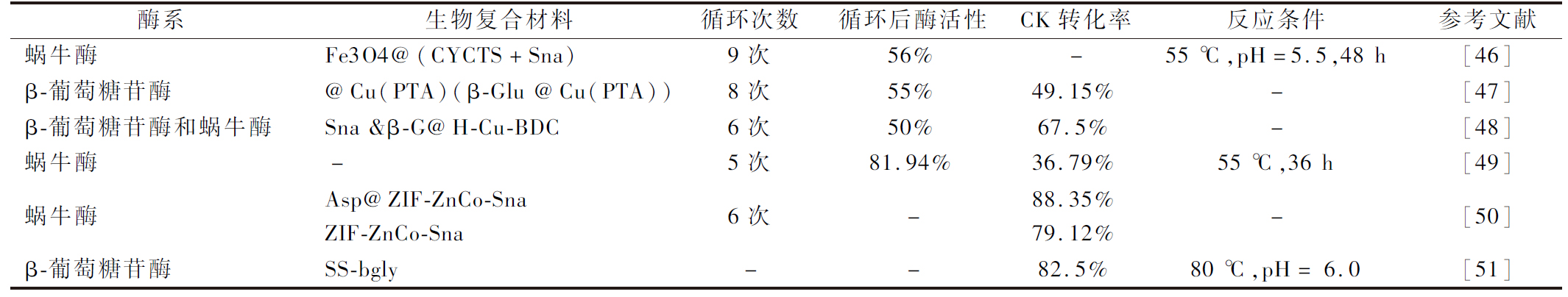
酶系生物复合材料循环次数循环后酶活性CK转化率反应条件参考文献蜗牛酶Fe3O4@(CYCTS+Sna)9次56%-55 ℃,pH=5.5,48 h[46]β-葡萄糖苷酶@Cu(PTA)(β-Glu @Cu(PTA))8次55%49.15%-[47]β-葡萄糖苷酶和蜗牛酶Sna &β-G@H-Cu-BDC6次50%67.5%-[48]蜗牛酶-5次81.94%36.79%55 ℃,36 h[49]蜗牛酶Asp@ZIF-ZnCo-SnaZIF-ZnCo-Sna6次-88.35%79.12%-[50]β-葡萄糖苷酶SS-bgly--82.5%80 ℃,pH= 6.0[51]
从表1中可以看出,微生物发酵法生产人参皂苷CK的主要机制为β-葡萄糖苷酶、α-阿拉伯呋喃糖苷酶、α-阿拉伯吡喃糖苷酶水解C-3和C-20位的葡萄糖,其中以β-葡萄糖苷酶水解为主。人参皂苷CK的主要生物转化过程如图3所示:
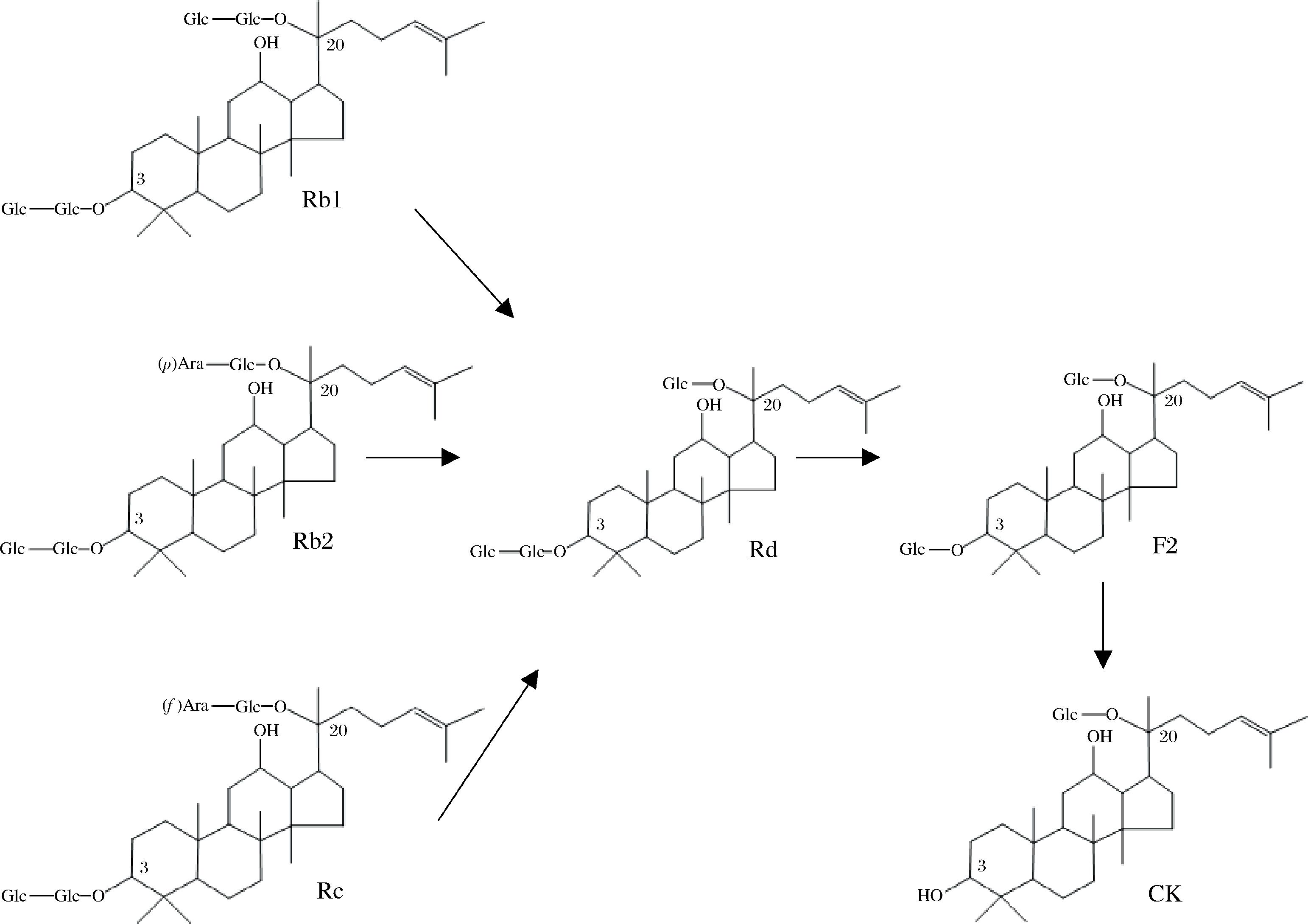
图3 人参皂苷CK的转化过程
Fig.3 Transformation process of ginsenoside CK

图4 人参皂苷CK抗炎症活性机制总结
Fig.4 Summary of the mechanism of anti-inflammatory activity of ginsenoside CK
从转化结果来看,大多数转化路径为Rb1→Rd→F2→CK,真菌会增加人参皂苷的含量,这表明真菌菌株在大规模生产人参皂苷CK方面具有巨大潜力[3]。周伟[27]利用拟青霉 (Paecilomyces Bainier sp.229)对人参皂苷进行转化, 10 L、50 L的中试放大实验CK转化率最高达到75.47%和83.22%,经过纯化工艺后纯化度可达92%以上,因此拟青霉是具有大规模发酵制备CK潜质的菌种。郭从亮等[33]筛选出植物内生菌Coniochaeta sp.对三七总皂苷中人参皂苷Rb1进行特异性转化,发酵12 d后人参皂苷C-K的转化率高达11.62%,可作为大量生产CK的菌株。文孟良等[34]将弗氏链霉菌(Streptomycesfradiae NTGA-334)在100 L全自动发酵罐中发酵转化三七总皂苷制备CK,该菌种生产成本低、产率高,是工业化生产CK的一种值得借鉴的方法。
除拟青霉 (Paecilomyces Bainier sp.229)、Coniochaeta sp.、弗氏链霉菌(Streptomycesfradiae NTGA-334)等已被证明有规模化生产CK潜质以外,黑曲霉XD101、黑曲霉g.848、黑曲霉Aspergillus niger sp.J7、丝状真菌镰刀菌(Fusarium sacchari)、镰刀霉属霉菌m14、多粘芽孢杆菌、Esteya vermicola CNU120806、真菌GH26、冬虫夏草菌(Cordyceps sinensis)、蜜环菌(Armillaria mellea)、Arthrinium sp. GE 17-18等菌株也为规模化制备人参皂苷CK提供了借鉴价值。
植物内生菌和土壤微生物虽然能够转化人参皂苷为人参皂苷CK,但随着食品、医疗、生物和化妆品行业对人参皂苷CK的需求越来越大,寻找食品级的微生物已成为一种必然趋势。LIU等[36]用食用和药用蘑菇筛选出S.commune 菌种可安全用于制备人参皂苷CK,该发酵过程成本低、绿色环保、无毒无害,这为研究者筛选食用微生物并绿色安全地制备人参皂苷CK提供参考。在以前的研究中,许多用于人参皂苷生物转化的微生物不是食品级,限制了它们在食品工业中的使用,泡菜里提取的乳酸杆菌LH 4、米酒里提取的酿酒酵母、HJ-014、植物乳植杆菌(GIM1.648)、嗜酸乳杆菌(No.GIM1.731)、干酪乳酪杆菌(No.GIM1.204)、发酵粘液乳杆菌(No.GIM1.985)、植物乳植杆菌M1(Lactiplantibacillas plantarumsub sp.)、双歧杆菌Int57、雷氏柄杆菌GP45、明串珠菌 KFRI 690、柚皮苷酶(naringinase)、斜卧青霉(Penicillium decumbens)都已被证实可作为制备人参皂苷CK的食品微生物。
2.2.3 酶转化法
微生物法转化人参皂苷会产生混合稀有人参皂苷,特异性较差,分离较为困难,循环性差。与微生物转化相比,酶转化法用特定的酶水解糖苷键,因此特异性更强,可以定向生成目标产物,且反应周期短、污染小、产物纯度高、可控性强。但酶转化法存在成本高和酶再生等问题。若能找到可循环利用的酶进行转化,则有利于人参皂苷CK的工业化生产[45]。随着基因工程技术的发展,研究者对通过重组酶及固定化酶转化原人参皂苷制备人参皂苷CK已取得了很大的进展,这些新技术的应用为人参皂苷的工业化生产提供了新思路和新途径。许多学者已对水解酶进行分类总结,该文主要总结利用重组酶和固定化酶大规模生产人参皂苷CK的方法。
目前大多数研究都是以蜗牛酶和β-葡萄糖苷酶进行固定化,固定方式各有不同,研究一种成本更低、转化效率更高的重组酶作为底物进行固定并改善固定方式有利于人参皂苷CK制备的进一步发展。除此之外,可以考虑和纳米技术结合,将纳米颗粒作为载体提高人参皂苷CK的生物利用度和酶的活性,也是更高效规模化制备人参皂苷CK的一个研究方向。通过特定且能循环利用的酶转化为特定的稀有人参皂苷则可以提高转化效率,减少分离混合产物过程中的损失,节约资源,并且循环使用酶可利于大规模生产特定人参皂苷CK。
3 人参皂苷CK的生物活性
3.1 抗肿瘤活性
人参皂苷在治疗和干预肿瘤方面具有巨大潜力,其主要的机制有抑制肿瘤细胞增殖和迁移、促进肿瘤细胞凋亡、抑制肿瘤血管生成、增强免疫功能、提高化疗药物对肿瘤细胞的敏感性、减轻对正常细胞的毒副作用及降低细胞的耐药性等[52-54]。其中,人参皂苷CK相比于原人参皂苷具有更少的糖基,易被人体吸收利用,可增强人体对化疗药物的敏感性、通过协同作用减少不良反应,在抗肿瘤方面具有较大潜质[8],已成为各研究人员热点研究对象。许多学者通过实验已证明人参皂苷CK对肝癌[7]、肺癌[55]、宫颈癌[56]、乳腺癌[57]等有明显的抑制作用。范励雯[55]利用人肺癌细胞A549和人肺腺癌细胞PC9细胞系,在人参皂苷CK和培美曲塞的协同作用下,A549、PC9细胞系的活力均降低30%以上,70%的A549和约67%的PC9被阻滞在G1期,结果表明人参皂苷CK具有协助抗癌药物抑制肺腺癌细胞的能力。
人参皂苷CK在抗肿瘤方面效果显著,但由于其达玛烷结构,对肿瘤组织缺乏靶向性[6],越来越多的学者倾向于将其和纳米技术结合,如纳米乳液、聚合物颗粒、脂质体等[58],通过改进给药系统提高人参皂苷的生物利用率。ZHANG等[59]以两亲性脱氧胆酸-O羧甲基壳聚糖为载体,将载有人参皂苷CK(CK-NPs)的壳聚糖纳米粒作为递送系统,其粒径范围为170~200 nm,结果表明人参皂苷CK和CK-NPs的IC50值分别为23.33和16.58 μg/mL,可推断CK-NPs能够提高人参皂苷CK的溶解度,增强其对癌细胞的抑制能力。尽管已有很多研究支持其抗肿瘤作用,但仍需要更多的临床和基础研究来验证其安全性和有效性,并探索其在肿瘤治疗中的具体应用方式和机制。
3.2 抗炎症活性
人参皂苷CK具有抗炎症活性,其主要机制如4图所示。FAN等[60]采用MTT法和流式细胞术测定人参皂苷CK对人角质形成细胞生长和凋亡的影响,进而推测其在咪喹莫特诱导的牛皮癣样皮炎中的治疗潜力。结果表明人参皂苷CK能够抑制人角质形成细胞的增殖,同时抑制人永生角质化形成细胞HaCaT中IL-36γ诱导的REG3A表达,在抗牛皮癣样皮炎中有一定的治疗效果。
除此之外,有的学者结合纳米给药系统制备相关纳米颗粒来发挥人参皂苷CK抗炎作用。KIM等[61]以金纳米粒子(AuNPs)为载体负载人参皂苷CK形成Bifi-CKAuNPs,抑制炎症中关键途径 NF-κB/MAPK 信号转导,结果表明其对小鼠肺、肾和肝组织的炎症具有明显的减轻作用且无毒性。目前已知炎症的作用机制,未来可增加人参皂苷CK对具体炎症的深入研究。此外,纳米技术的应用也为人参皂苷CK治疗炎症提供了更为高效的方法。
3.3 延缓皮肤衰老
皮肤衰老是一个普遍的生理过程,皮肤稳态由内层真皮中的间充质干细胞和外层表皮中的表皮干细胞维持[62]。随着人年龄的增长,皮肤逐渐松弛并出现皱纹、色斑,并伴随着细胞外基质蛋白的降解以及真皮结构的变化[63]。当今社会人们压力过大以及环境污染可能直接或间接损害皮肤细胞的DNA, 其中紫外线是干细胞DNA损伤的主要原因,可导致干细胞减少及功能下降,最终导致皮肤老化。有学者研究UVA辐照的成纤维细胞在经过人参皂苷CK处理后I型胶原蛋白增加,而基质金属蛋白酶-1活性降低[64]。
JIN等[65]利用重组 3-β-羟基类固醇脱氢酶将人参皂苷 CK酮化为 12-β-hydroxydammar-3-one-20(S)-O-β-D-glucopyranoside (3-oxo-CK),研究表明其对紫外线诱导的基质金属蛋白酶-1具有抑制活性,并促进了 I 型前胶原的合成。虽然目前对人参皂苷CK抗皮肤衰老的研究很少,但可通过化学方法将人参皂苷CK转化为具有抗衰老作用的衍生物发挥其抗衰老功效,在抗衰老功效成分方面具有巨大潜力,为未来化妆品行业挖掘抗衰老功效成分提供参考价值。
3.4 抗糖尿病及其并发症
糖尿病是一种慢性代谢性疾病,主要分为1型糖尿病和2型糖尿病两种类型,其特征是由于胰岛素缺乏或胰岛素效应不足导致的高血糖状态。糖尿病可能引发心血管疾病、肾脏疾病、眼部疾病等严重并发症。人参皂苷CK在抗糖尿病方面表现出较大活性,尤其是在治疗糖尿病并发症方面具有较大潜力,其起作用的机制主要为改善胰岛素抵抗、保护胰岛细胞、增强胰岛素分泌、促进葡萄糖转运及抗炎、抗氧化应激、调节糖脂代谢等。
有学者认为,骨骼肌胰岛素抵抗是2型糖尿病的主要原因,LI等[66]通过实验表明人参皂苷CK 能显著增加骨骼肌胰岛素敏感性,从而减轻高血糖和胰岛素抵抗。CHEN等[67]通过对哺乳动物的实验表明人参皂苷CK可以抑制微生物产生的咪唑丙酸酯诱导的 TLR4 激活来改善糖尿病肾病的发展,对肠道微生物群和血清代谢物有改善作用,在治疗糖尿病肾病这类糖尿病并发症方面有巨大的潜力。CHO等[68]研究表明人参皂苷CK在高血糖条件下对肌腱细胞凋亡、炎症、氧化应激和金属蛋白酶系统具有减轻作用,在糖尿病患者肌腱病治疗方面有一定的作用。相比于其他治疗药物,人参皂苷CK表现出强大的药理活性,且对人体无毒害、无副作用、无负担,可作为食品添加到日常饮食中,辅助糖尿病患者的治疗。
3.5 抗抑郁活性
抑郁症在当前社会是一种严重且常见的心理问题,有情绪低落、睡眠障碍、精力不足等症状,严重威胁人的日常生活和健康。据报道,人参皂苷CK能够通过抗炎治疗来进行抑郁症的防治,通过抑制中枢神经系统的NLRP3炎症小体来减轻中枢炎症进而体现抗抑郁活性[69]。SHIN等[70]通过实验表明调节“微生物-肠-脑轴” 和“下丘脑-垂体-肾上腺轴”来减轻小鼠的抑郁症和结肠炎。人参皂苷CK作为一种药食同源且无副作用的提取成分,能够为未来开发抗抑郁药物提供借鉴。
3.6 抗骨质疏松症活性
骨质疏松症是一种常见的骨骼系统疾病,当破骨细胞大于成骨细胞时,骨质疏松就会发生,主要特征是骨组织的密度和质量下降,增加了骨折的风险[71]。据统计,全球超过2亿人患有骨质疏松症,这种疾病通常在老年人中更为常见,其中女性比男性更容易患这种疾病。人参皂苷 CK 可以通过抑制 NF-κB 信号通路来抑制破骨细胞生成以及活性氧的活性,同时防止卵巢切除诱导的骨丢失[72]。人参皂苷CK与骨质疏松存在共同作用的138个靶点,通过干扰c-Fms 介导的MAPK和PI3K信号轴,来调节破骨细胞的分化,从而影响骨质疏松症的发生和进展[73]。随着人口老龄化的加剧,骨质疏松症已经成为一个全球性的公共卫生挑战,因此将人参皂苷CK应用于骨质疏松症的治疗具有现实意义。
4 总结与展望
人参皂苷CK作为人参中最具活性的成分之一,具有抗肿瘤、抗炎症、延缓皮肤衰老、抗糖尿病及其并发症、抗抑郁、抗骨质疏松症等生物活性,因此研究其工业化制备具有重要意义。与化学水解相比,生物转化被认为是制备人参皂苷CK的最有效途径。目前人参皂苷CK的制备已有一定的研究,但只停留于实验室阶段,尚未规模化生产。该文总结了适合规模化生产人参皂苷CK的菌株及重组酶、固定化酶。为了实现人参皂苷CK的大规模生产, 需进一步研究筛选特异性转化程度高的高产菌株,结合基因工程、纳米技术得到效率高、活性高、安全无污染的重组酶及固定化酶。但一些菌株及载体不适宜应用于食品领域,因此寻找食品级菌株及研究安全性更高的载体也是重点研究方向之一。在药物制备方面,纳米制剂作为载体提高人参皂苷CK在体内的溶解性与生物利用度也是开发医药食品的主要方向。除此之外,CK虽然已被证明在人体中的安全性,但有临床结果表明其可能引起腹泻和腹痛,因此需进一步通过临床试验研究人参皂苷CK对肝脏和肾器官的影响。
[1] KEUM Y S, PARK K K, LEE J M, et al.Antioxidant and anti-tumor promoting activities of the methanol extract of heat-processed ginseng[J].Cancer Letters, 2000, 150(1):41-48.
[2] 李忆红, 梁雨璐, 解嘉琪, 等.中药皂苷类化合物生物转化研究进展[J].中草药, 2024, 55(3):989-1003.LI Y H, LIANG Y L, XIE J Q, et al.Research progress on biotransformation of saponins from traditional Chinese medicine[J].Chinese Traditional and Herbal Drugs, 2024, 55(3):989-1003.
[3] 张薇. 人参根际土壤真菌与内生真菌的多样性及人参皂苷生物催化活性菌株的筛选[D].大连:辽宁师范大学, 2011.ZHANG W.Diversity of rhizosphere soil fungi and endophytic fungi of ginseng and screening of biocatalytic strains of ginsenosides[D].Dalian:Liaoning Normal University, 2011.
[4] 袁松竹, 王斌, 周旋, 等.稀有人参皂苷生物转化的研究进展[J].食品工业科技, 2023, 44(12):480-489.YUAN S Z, WANG B, ZHOU X, et al.Research progress on the biotransformation of rare ginsenosides[J].Science and Technology of Food Industry, 2023, 44(12):480-489.
[5] 赵升铭, 周旋, 袁松竹, 等.达玛烷型人参皂苷羧酸衍生物结构与抗肿瘤机制研究进展[J/OL].中成药, 2024 (2024-02-27.http://kns.cnki.net/kcms/detail/31.1368.R.20240227.0948.004.html.ZHAO S M, ZHOU X, YUAN S Z, et al.Research progress on Structure and anti-tumor mechanism of dammarane ginsenoside carboxylic acid derivatives[J/OL].Proprietary Chinese medicine:1-9 2024 (2024-02-27).http://kns.cnki.net/kcms/detail/31.1368.R.20240227.0948.004.html
[6] MURUGESAN M, MATHIYALAGAN R, BOOPATHI V, et al.Production of minor ginsenoside CK from major ginsenosides by biotransformation and its advances in targeted delivery to tumor tissues using nanoformulations[J].Nanomaterials, 2022, 12(19):3427.
[7] 赵会芬. 人参皂苷CK辅助治疗原发性肝癌的临床观察[J].医学综述, 2013, 19(15):2837-2840.ZHAO H F.Clinical observation of adjuvant therapy of ginsenoside CK on primary hepatocellular carcinoma[J].Medical Recapitulate, 2013, 19(15):2837-2840.
[8] OH J M, KIM E, CHUN S.Ginsenoside compound K induces ros-mediated apoptosis and autophagic inhibition in human neuroblastoma cells in vitro and in vivo[J].International Journal of Molecular Sciences, 2019, 20(17):4279.
[9] YANG W H, ZHOU J L, GU Q Y, et al.Combinatorial enzymatic catalysis for bioproduction of ginsenoside compound K[J].Journal of Agricultural and Food Chemistry, 2023,71(7):3385-3397
[10] CHI H, KIM D H, JI G E.Transformation of ginsenosides Rb2 and rc from Panax ginseng by food microorganisms[J].Biological and Pharmaceutical Bulletin, 2005, 28(11):2102-2105.
[11] ZHAO X S, WANG J, LI J, et al.Highly selective biotransformation of ginsenoside Rb1 to Rd by the phytopathogenic fungus Cladosporium fulvum (syn.Fulvia fulva)[J].Journal of Industrial Microbiology &Biotechnology, 2009, 36(5):721-726.
[12] 许凌巧, 王安琪, 何正有, 等.提高人参茎叶皂苷中稀有人参皂苷含量的工艺[J].食品工业, 2020, 41(2):50-53.XU L Q, WANG A Q, HE Z Y, et al.The technology of increasing the content of rare ginsenosides in ginseng stem and leaf saponins[J].The Food Industry, 2020, 41(2):50-53.
[13] 杨宁, 杨世林, 赵余庆.稀有人参皂苷糖苷化合成方法的研究进展[J].现代药物与临床, 2014, 29(5):574-582.YANG N, YANG S L, ZHAO Y Q.Research progress on glycosylation methods of rare ginsenosides[J].Drugs &Clinic, 2014, 29(5):574-582.
[14] 杨金玲, 高丽丽, 朱平.人参皂苷生物合成研究进展[J].药学学报, 2013, 48(2):170-178.YANG J L, GAO L L, ZHU P.Advances in the biosynthesis research of ginsenosides[J].Acta Pharmaceutica Sinica, 2013, 48(2):170-178.
[15] HAN Y, SUN B, JIANG B, et al.Microbial transformation of ginsenosides Rb1, Rb3 and Rc by Fusarium sacchari[J].Journal of Applied Microbiology, 2010, 109(3):792-798.
[16] NICHOLSON J K, HOLMES E, WILSON I D.Gut microorganisms, mammalian metabolism and personalized health care[J].Nature Reviews.Microbiology, 2005, 3(5):431-438.
[17] MIWA M K, HORIMOTO T, KIYOHARA M, et al.Cooperation of β-galactosidase and β-N-acetylhexosaminidase from bifidobacteria in assimilation of human milk oligosaccharides with type 2 structure[J].Glycobiology, 2010, 20(11):1402-1409.
[18] 柯仲成, 杨楠, 侯雪峰, 等.大鼠肠道菌群对芍药苷体外代谢转化的研究[J].中国中药杂志, 2016, 41(20):3839-3845.KE Z C, YANG N, HOU X F, et al.Metabolism of paeoniflorin by rat intestinal flora in vitro[J].China Journal of Chinese Materia Medica, 2016, 41(20):3839-3845.
[19] BAU E A, CHOO M K, PARK E K, et al.Metabolism of ginsenoside R(c) by human intestinal bacteria and its related antiallergic activity[J].Biological &Pharmaceutical Bulletin, 2002, 25(6):743-747.
[20] JEON J H, LEE J, PARK J H, et al.Effect of lactic acid bacteria on the pharmacokinetics and metabolism of ginsenosides in mice[J].Pharmaceutics, 2021, 13(9):1496.
[21] JIA L E, ZHAO Y Q, LIANG X J.Current evaluation of the millennium phytomedicine- ginseng (II):Collected chemical entities, modern pharmacology, and clinical applications emanated from traditional Chinese medicine[J].Current Medicinal Chemistry, 2009, 16(22):2924-2942.
[22] CHU L L, HANH N T Y, QUYEN M L, et al.Compound K production:Achievements and perspectives[J].Life, 2023, 13(7):1565.
[23] 马宗敏, 段绪红, 秦梦, 等.微生物发酵技术在中药苷类生物转化中的应用进展[J].世界科学技术-中医药现代化, 2017, 19(5):858-864.MA Z M, DUAN X H, QIN M, et al.Microbial transformation of glycosides in Chinese herbal medicine[J].Modernization of Traditional Chinese Medicine and Materia Medica-World Science and Technology, 2017, 19(5):858-864.
[24] JIANG Y Y, LI W N, FAN D D.Biotransformation of ginsenoside Rb1 to ginsenoside CK by strain XD101:A safe bioconversion strategy[J].Applied Biochemistry and Biotechnology, 2021, 193(7):2110-2127.
[25] LIU C Y, ZHOU R X, SUN C K, et al.Preparation of minor ginsenosides C-Mc, C-Y, F2, and C-K from American ginseng PPD-ginsenoside using special ginsenosidase type-I from Aspergillus niger g.848[J].Journal of Ginseng Research, 2015, 39(3):221-229.
[26] 高娟, 周安东, 原野, 等.黑曲霉降解人参皂苷Rb1制备稀有皂苷Compound K[J].生物技术进展, 2016, 6(2):98-104.GAO J, ZHOU A D, YUAN Y, et al.Enzymatic degradation of ginsenoside Rb1 for preparation of compound K by Aspergillus niger sp.J7[J].Current Biotechnology, 2016, 6(2):98-104.
[27] 周伟. 稀有人参皂苷compound K的制备和活性研究[D].上海:复旦大学, 2008.ZHOU W.Study on preparation and activity of rare ginsenoside compound K[D].Shanghai:Fudan University, 2008.
[28] 崔宇, 姜彬慧, 韩颖, 等.微生物对人参果总皂苷中人参皂苷化合物K的转化作用[J].中草药, 2007, 38(2):189-193.CUI Y, JIANG B H, HAN Y, et al.Microbial transformation on ginsenoside compound K from total saponins in fruit of Panax ginseng[J].Chinese Traditional and Herbal Drugs, 2007, 38(2):189-193.
[29] JI Q, GAO Y G, ZHAO Y, et al.Determination of ginsenosides by Bacillus polymyxa conversion and evaluation on pharmacological activities of the conversion products[J].Process Biochemistry, 2015, 50(6):1016-1022.
[30] 武伦鹏, 白龙律, 韩春峰, 等.微生物转化人参主要皂苷 Rb1 为 CK 的研究[J].人参研究, 2016(2):7-11.WU L P, BAI L L, HAN C F, et al.Study on microbial transformation of ginseng saponin Rb1 into CK[J].Ginseng Research, 2016(2):7-11.
[31] LI F, WU Z X, SUI X.Biotransformation of ginsenoside Rb1 with wild Cordyceps sinensis and Ascomycota sp.and its antihyperlipidemic effects on the diet-induced cholesterol of zebrafish[J].Journal of Food Biochemistry, 2020, 44(6):e13192.
[32] KIM M J, UPADHYAYA J, YOON M S, et al.Highly regioselective biotransformation of ginsenoside Rb2 into compound Y and compound K by β-glycosidase purified from Armillaria mellea mycelia[J].Journal of Ginseng Research, 2018, 42(4):504-511.
[33] 郭从亮, 杨晓艳, 陈子明, 等.一株植物内生菌Coniochaeta sp.对三七总皂苷中人参皂苷Rb1的特异性转化含量测定[J].中药材, 2016, 39(5):1075-1078.GUO C L, YANG X Y, CHEN Z M, et al.The content determination of biotransformation of Rb1 in the total saponins of Panax notoginseng by a plant endophyte Coniochaeta sp[J].Journal of Chinese Medicinal Materials, 2016, 39(5):1075-1078.
[34] 文孟良, 李铭刚, 刚 杜, 等.一种链霉菌发酵三七皂苷制备稀有人参皂苷Compound K的工艺.药物生物技术, 2009, 16(1):18-18.WEN M L, LI M G, GANG Du, et al.Process for preparing rare ginsenoside Compound K by fermentation of notoginseng saponins by Streptomyces.Pharmaceutical Biotechnology, 2009, 16(1):18-18.
[35] FU Y, YIN Z H, WU L P, et al.Biotransformation of ginsenoside Rb1 to ginsenoside C-K by endophytic fungus Arthrinium sp.GE 17-18 isolated from Panax ginseng[J].Letters in Applied Microbiology, 2016, 63(3):196-201.
[36] LIU Z, LI J X, WANG C Z, et al.Microbial conversion of protopanaxadiol-type ginsenosides by the edible and medicinal mushroom Schizophyllum commune:A green biotransformation strategy[J].ACS Omega, 2019, 4(8):13114-13123.
[37] XU Y Q, TANG Y Q, LIU T, et al.Optimization of rare ginsenosides and antioxidant activity quality of ginseng jiaosu based on probiotic strains and fermentation technology[J].Journal of Food Quality, 2023, 2023:5686929.
[38] KIM B G, CHOI S Y, KIM M R, et al.Changes of ginsenosides in Korean red ginseng (Panax ginseng) fermented by Lactobacillus plantarum M1[J].Process Biochemistry, 2010, 45(8):1319-1324.
[39] QUAN L H, KIM Y J, LI G H, et al.Microbial transformation of ginsenoside Rb1 to compound K by Lactobacillus paralimentarius[J].World Journal of Microbiology &Biotechnology, 2013, 29(6):1001-1007.
[40] CHOI H J, KIM E A, KIM D H, et al.The bioconversion of red ginseng ethanol extract into compound K by Saccharomyces cerevisiae HJ-014[J].Mycobiology, 2014, 42(3):256-261.
[41] CHENG L Q, KIM M K, LEE J W, et al.Conversion of major ginsenoside Rb1 to ginsenoside F2 by Caulobacter leidyia[J].Biotechnology Letters, 2006, 28(14):1121-1127.
[42] PARK S J, YOUN S Y, JI G E, et al.Whole cell biotransformation of major ginsenosides using Leuconostocs and Lactobacilli[J].Food Science and Biotechnology, 2012, 21(3):839-844.
[43] ZHENG Y, ZHENG Z Z, MING Y L, et al.Compound K producing from the enzymatic conversion of gypenoside by naringinase[J].Food and Chemical Toxicology, 2019, 130:253-261.
[44] KIM S Y, LEE H N, HONG S J, et al.Enhanced biotransformation of the minor ginsenosides in red ginseng extract by Penicillium decumbens β-glucosidase[J].Enzyme and Microbial Technology, 2022, 153:109941.
[45] GUO C L, CUI X M, YANG X Y, et al.Advances in studies on biotransformation of ginsensides[J].Zhongguo Zhong Yao Za Zhi = Zhongguo Zhongyao Zazhi = China Journal of Chinese Materia Medica, 2014, 39(20):3899-3904.
[46] LI W N, ZHANG X W, XUE Z Y, et al.Ginsenoside CK production by commercial snailase immobilized onto carboxylated chitosan-coated magnetic nanoparticles[J].Biochemical Engineering Journal, 2021, 174:108119.
[47] CAO S S, YANG F, TIAN F, et al.Immobilized β-glucosidase on Cu(PTA) for the green production of rare ginsenosides CK[J].Process Biochemistry, 2023, 133:169-178.
[48] CAO S S, LI R Z, TIAN F, et al.Construction of a hollow MOF with high sedimentation performance and co-immobilization of multiple-enzymes for preparing rare ginsenoside CK[J].Reaction Chemistry &Engineering, 2023, 8(11):2804-2817.
[49] 于兆慧, 刘其媛, 崔莉, 等.微球固定化蜗牛酶转化人参皂苷Rb1制备人参稀有皂苷Compound K研究[J].中草药, 2014, 45(21):3092-3097.YU Z H, LIU Q Y, CUI L, et al.Transformation of rare ginsenoside Compound K from ginsenoside Rb1 catalyzed by snailase immobilization onto microspheres[J].Chinese Traditional and Herbal Drugs, 2014, 45(21):3092-3097.
[50] TIAN D D, WU Z S, LIU X C, et al.Synthesis of l-aspartic acid-based bimetallic hybrid nanoflowers to immobilize snailase for the production of rare ginsenoside compound K[J].Journal of Materials Chemistry B, 2023, 11(11):2397-2408.
[51] WANG P, TANG C C, LIU Y N, et al.Biotransformation of high concentrations of ginsenoside substrate into compound K by β-glycosidase from Sulfolobus solfataricus[J].Genes, 2023, 14(4):897.
[52] JIN X, YANG Q, CAI N.Preparation of ginsenoside compound-K mixed micelles with improved retention and antitumor efficacy[J].International Journal of Nanomedicine, 2018, 13:3827-3838.
[53] BORGO C, RUZZENE M.Role of protein kinase CK2 in antitumor drug resistance[J].Journal of Experimental &Clinical Cancer Research, 2019, 38(1):287.
[54] OLIVEIRA M M S, D’AULERIO R, YONG T, et al.Increased cross-presentation by dendritic cells and enhanced anti-tumour therapy using the Arp2/3 inhibitor CK666[J].British Journal of Cancer, 2023, 128(6):982-991.
[55] 范励雯. 人参皂苷CK通过EGFR/AKT/G6PC3轴抑制肺腺癌糖酵解提高培美曲塞疗效及机制研究[D].长春:吉林大学, 2023.FAN L W.Ginsenoside CK inhibits glycolysis of lung adenocarcinoma through EGFR/AKT/G6PC3 axis to improve the therapeutic effect of pemetrexed and its mechanism[D].Changchun:Jilin University, 2023.
[56] 殷琪. 人参皂苷CK对人宫颈癌Hela细胞的抑制作用及机理研究[D].合肥:合肥工业大学, 2022.YIN Q.Inhibitory effect and mechanism of ginsenoside CK on human cervical cancer Hela cells[D].Hefei:Hefei University of Technology, 2022.
[57] 张波. 人参皂苷CK对三阴性乳腺癌谷氨酰胺代谢的影响及作用机制[D].西安:西北大学, 2022.ZHANG B.Effect of ginsenoside CK on glutamine metabolism in triple negative breast cancer and its mechanism[D].Xi’an:Northwest University, 2022.
[58] 李铭莹, 林霖, 王岩, 等.人参皂苷抗肿瘤机制及其纳米药物递送系统的研究进展[J].中草药, 2024, 55(2):688-696.LI M Y, LIN L, WANG Y, et al.Research progress on antitumor mechanism and nano-drug delivery system for ginsenosides[J].Chinese Traditional and Herbal Drugs, 2024, 55(2):688-696.
[59] ZHANG J M, WANG Y J, JIANG Y Y, et al.Enhanced cytotoxic and apoptotic potential in hepatic carcinoma cells of chitosan nanoparticles loaded with ginsenoside compound K[J].Carbohydrate Polymers, 2018, 198:537-545.
[60] FAN H Y, WANG Y, ZHANG X L, et al.Ginsenoside compound K ameliorates imiquimod-induced psoriasis-like dermatitis through inhibiting REG3A/RegIIIγ expression in keratinocytes[J].Biochemical and Biophysical Research Communications, 2019, 515(4):665-671.
[61] KIM S, WANG R B, DHANDAPANI S, et al.Novel modified probiotic gold nanoparticles loaded with ginsenoside CK exerts an anti-inflammation effect via NF-κB/MAPK signaling pathways[J].Arabian Journal of Chemistry, 2024, 17(4):105650.
[62] PANICH U, SITTITHUMCHAREE G, RATHVIBOON N, et al.Ultraviolet radiation-induced skin aging:The role of DNA damage and oxidative stress in epidermal stem cell damage mediated skin aging[J].Stem Cells International, 2016, 2016:7370642.
[63] FENG M Y, ZHENG X, WAN J, et al.Research progress on the potential delaying skin aging effect and mechanism of tea for oral and external use[J].Food &Function, 2021, 12(7):2814-2828.
[64] KIM E H, KIM W.An insight into ginsenoside metabolite compound K as a potential tool for skin disorder[J].Evidence-Based Complementary and Alternative Medicine, 2018, 2018:8075870.
[65] JIN Y, WANG D D, IM W T, et al.Ketonization of ginsenoside C-K by novel recombinant 3-β-hydroxysteroid dehydrogenases and effect on human fibroblast cells[J].Molecules, 2023, 28(9):3792.
[66] LI W L, LI H Y, ZHENG L J, et al.Ginsenoside CK improves skeletal muscle insulin resistance by activating DRP1/PINK1-mediated mitophagy[J].Food &Function, 2023, 14(2):1024-1036.
[67] CHEN Q, REN D W, LIU L K, et al.Ginsenoside compound K ameliorates development of diabetic kidney disease through inhibiting TLR4 activation induced by microbially produced imidazole propionate[J].International Journal of Molecular Sciences, 2022, 23(21):12863.
[68] CHO W J, OH H, ABD EL-ATY A M, et al.Therapeutic potential of ginsenoside compound K in managing tenocyte apoptosis and extracellular matrix damage in diabetic tendinopathy[J].Tissue and Cell, 2024, 86:102275.
[69] SONG W, LI G, TANG Y, et al.Ginsenoside compound K inhibits oxidative stress and NLRP3 inflammasome activity in mice exposed to chronic unpredictable mild stress[J].Biotechnology &Biotechnological Equipment, 2019, 33(1):1372-1379.
[70] SHIN Y J, LEE D Y, KIM J Y, et al.Effect of fermented red ginseng on gut microbiota dysbiosis- or immobilization stress-induced anxiety, depression, and colitis in mice[J].Journal of Ginseng Research, 2023, 47(2):255-264.
[71] WEITZMANN M N, OFOTOKUN I.Physiological and pathophysiological bone turnover-role of the immune system[J].Nature Reviews.Endocrinology, 2016, 12(9):518-532.
[72] DING L L, GAO Z, WU S L, et al.Ginsenoside compound-K attenuates OVX-induced osteoporosis via the suppression of RANKL-induced osteoclastogenesis and oxidative stress[J].Natural Products and Bioprospecting, 2023, 13(1):49.
[73] ZHANG S, SHEN S H, MA P, et al.Biochemical targets and molecular mechanism of ginsenoside compound K in treating osteoporosis based on network pharmacology[J].International Journal of Molecular Sciences, 2022, 23(22):13921.